Изобретение относится к соединениям формулы I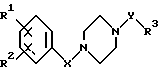
в которой R1 обозначает -C(=NH)-NH2, который может быть однократно замещен группой -СОА, -CO-[C(R6)2]n-Ar, -COOA, -ОН или обычной аминозащитной группой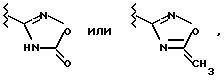
R2 обозначает Н, A, OR6, N(R6)2, NO2, CN, Hal, NHCOA, NHCOAr, NHSO2A, NHSО2Ar, COOR6, СОN(R6)2, CONHAr, COR6, COAr, S(O)nA или S(О)nAr,
R3 обозначает А, циклоалкил, - [C(R6)2]nAr, - [C(R6)2]n-O-Ar, -[C(R6)2] nHet или -C(R6)2=C(R6)2-Ar,
R6 обозначает Н, А или бензил,
X отсутствует или обозначает -СО-, -C(R6)2-, -C(R6)2-C(R6)2-, -C(R6)2-CO-, -C(R6)2-C(R6)2-CO-, -C(R6)= C(R6)-CO-, NR6СO-, -N{[CR6)2]n-COOR6} -CO- или -C(COOR6)R6-C(R6)2-CO-,
Y обозначает -C(R6)2-, -SO2-, -СО-, -СОО- или -CONR6-,
А обозначает алкил с 1-20 С-атомами, где одна либо две СН2-группы могут быть заменены на О- или S-атомы либо на -CR6=CR6-группы и/или 1-7 Н-атомов могут быть заменены на F,
Аr обозначает незамещенный либо одно-, дву- или трехкратно замещенный группой А, Аr', OR6, N(R6)2, NО2, CN, Hal, NHCOA, NHCOAr', NHSO2A, NHSО2Ar', COOR6, CON(R6)2, CONHAr', COR6, COAr', S(О)nA или S(О)nAr фенил или нафтил,
Аr' обозначает незамещенный либо одно-, дву- или трехкратно замещенный группой A, OR6, N(R6)2, NO2, CN, Hal, NHCOA, COOR6, СОN(R6)2, COR6 или S(0)nA фенил или нафтил,
Het обозначает одно- или двухядерную незамещенную либо одно- или многократно замещенную группой Hal, A, Ar', COOR6, CN, N(R6)2, NO2, Ar-CONH-CH2 и/или карбонильным кислородом насыщенную либо ненасыщенную гетероциклическую кольцевую систему, содержащую один, два, три или четыре идентичных либо разных гетероатомов, таких как азот, кислород или сера,
Hal обозначает F, C1, Вr или J,
n обозначает 0, 1 или 2,
а также к их солям.
Объектом изобретения являются также оптически активные формы, рацематы, диастереомеры, равно как и гидраты и сольваты указанных соединений.
В основу изобретения была положена задача получить соединения с ценными свойствами и прежде всего такие соединения, которые можно было бы применять для изготовления соответствующих лекарственных средств.
Как было установлено, соединения формулы I и их соли наряду с хорошей совместимостью обладают очень ценными фармакологическими свойствами, прежде всего они проявляют ингибирующие фактор Ха свойства, благодаря чему их можно применять для борьбы и предупреждения тромбоэмболических заболеваний, таких как тромбоз, инфаркт миокарда, артериосклероз, воспаления, апоплексия, стенокардия (Angina pectoris), рестеноз после ангиопластики и перемежающаяся хромота (Claudicatio intermittens).
Ароматические производные амидина с антитромбозным действием известны, например, из заявки ЕР 0540051 В1. Циклические гуанидины, используемые при лечении тромбоэмболических заболеваний, описаны, например, в международной заявке WO 97/08165. Ароматические гетероциклы с ингибирующей активностью по отношению к фактору Ха известны, например, из международной заявки WO 96/10022.
Антитромбозный и антикоагуляционный эффект соединений по изобретению объясняется ингибирующим действием по отношению к активированной протеазе в системе свертывания крови, известной под названием фактор Ха. Фактор Ха представляет собой одну из протеаз, вовлеченных в комплексный процесс свертывания крови. Фактор Ха катализует превращение протромбина в тромбин, который в свою очередь способствует образованию тромбов. Активация тромбина, следовательно, может привести к появлению тромбоэмболии. Ингибирование фактора Ха может тем самым препятствовать образованию тромбина. Предлагаемые в изобретении соединения формулы I, a также их соли благодаря ингибированию фактора Ха оказывают эффективное воздействие на процесс свертывания крови и подавляют таким образом образование тромбов.
Для определения эффективности ингибирования фактора Ха соединениями по изобретению и выявления антикоагуляционной и антитромбозной активности могут использоваться обычные in vitro- или in vivo-методы. Один из подобных методов описывается, например, J. Hauptmann и др. в Thrombosis and Haemostasis 63, стр. 220-223 (1990). Определять эффективность ингибирования фактора Ха можно, например, по методу Т. Наrа и др., описанному в Thromb. Haemostas. 71, стр. 314-319 (1994).
Соединения формулы I могут применяться в качестве активных веществ в лекарственных средствах, предназначенных для использования в медицине и ветеринарии, прежде всего для борьбы и предупреждения тромбоэмболических заболеваний, таких как тромбоз, инфаркт миокарда, артериосклероз, воспаления, апоплексия, стенокардия, рестеноз после ангиопластики и перемежающаяся хромота.
Объектом изобретения в соответствии с этим являются соединения формулы I и их соли, а также способ получения соединений формулы I согласно пункту 1 и их солей, который отличается тем, что
а) их высвобождают из одного из их функциональных производных за счет обработки агентом сольволиза или гидрогенолиза, при этом
1) амидиновую группу высвобождают путем гидрогенолиза из ее оксадиазольного производного,
2) обычную аминозащитную группу путем обработки агентом сольволиза или гидрогенолиза заменяют на водород либо высвобождают аминогруппу, защищенную обычной защитной группой, или
б) что для получения соединений формулы I, в которой R1 представляет собой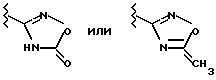
Х обозначает -СО- или -C(R6)2-СО-, а R2, R3 и Y имеют значения, указанные в пункте 1 формулы, подвергают взаимодействию соединение формулы II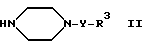
в которой R3 и Y имеют значения, указанные в пункте 1 формулы, и соединение формулы III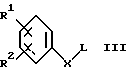
в которой R1 представляет собой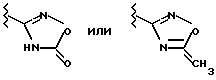
Х обозначает -СО- или -C(R6)2-CO-, R2 имеет значения, указанные в пункте 1 формулы, a L обозначает Cl, Br, J или свободную либо реакционноспособно функционально модифицированную ОН-группу, или
в) что для получения соединений формулы I, в которой R1 представляет собой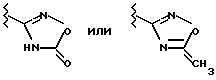
Y обозначает -SO2-, -СО-, -СОО- или -C(R6)2-, а R2 и Х имеют значения, указанные в пункте 1 формулы, подвергают взаимодействию соединение формулы IV
L-Y-R3, IV
в которой Y обозначает -SO2-, -CO-, -СОО- или -C(R6)2-, R3 имеет значения, указанные в пункте 1 формулы, а L обозначает Cl, Br, J или свободную либо реакционноспособно функционально модифицированную ОН-группу, и соединение формулы V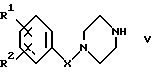
в которой R1 представляет собой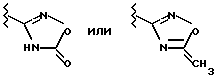
а R2 и Х имеют значения, указанные в пункте 1 формулы, или
г) что для получения соединений формулы I,
в которой R1 представляет собой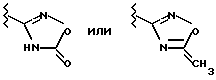
Y обозначает -CONH-, а R2 и Х имеют значения, указанные в пункте 1 формулы, подвергают взаимодействию соединение формулы VI
R3-N=C=О VI
в которой R3 имеет значения, указанные в пункте 1 формулы, и соединение формулы V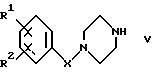
в которой R1 представляет собой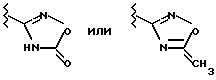
а R2 и Х имеют значения, указанные в пункте 1 формулы, или
д) что для получения соединений формулы I, в которой R1 обозначает -C(= NH)-NH2, циановую группу превращают в амидиновую группу и/или
е) что в соединении формулы I один либо несколько остатков R1, R2 и/или R3 превращают в другой, соответственно в несколько других остатков R1, R2 и/или R3, например,
1) гидролизуя сложноэфирную группу до карбоксильной группы,
2) восстанавливая нитрогруппу,
3) ацилируя аминогруппу, и/или
ж) основание либо кислоту формулы I переводят в одну из их солей.
Для всех остатков, неоднократно присутствующих в соединениях, как, например R6, справедливо то, что их значения не зависят друг от друга.
Выше и в последующем остатки, соответственно радикалы L, X, Y, R1, R2 и R3 имеют, если не указано иное, значения, указанные при расшифровке формул I-VI.
В вышеприведенных формулах А обозначает алкил и имеет 1-20, предпочтительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 С-атомов. Предпочтительными значениями А являются метил, кроме того, этил, пропил, изопропил, бутил, изобутил, втор-бутил либо трет-бутил, а также пентил, 1-, 2- либо 3-метилбутил, 1,1-, 1,2- либо 2,2-диметилпропил, 1-этилпропил, гексил, 1-, 2-, 3-либо 4-метилфенил, 1,1-, 1,2-, 1,3-, 2,2-, 2,3- либо 3,3-диметилбутил, 1-либо 2-этилбутил, 1-этил-1-метилпропил, 1-этил-2-метилпропил, 1,1,2- либо 1,2,2-триметилпропил, гептил, октил, нонил или децил. Кроме того, алкил обозначает, например, трифторметил, пентафторэтил, аллил или кротил.
Циклоалкил обозначает предпочтительно циклопропил, циклобутил, циклопентил, циклогексил или циклогептил. Прежде всего циклоалкил обозначает остаток бициклического терпена, как, например, 3-ментил, и наиболее предпочтительно камфор-10-ильный остаток.
COR6 представляет собой ацил и обозначает предпочтительно формил, ацетил, пропионил, а также бутирил, пентаноил или гексаноил.
Hal обозначает предпочтительно F, C1, Вr, а также J.
R2 обозначает предпочтительно Н, фтор, хлор, бром, иод, гидрокси-, метокси-, этокси-, пропокси-, нитро-, амино-, метиламино-, диметиламино-, этиламино-, диэтиламино-, ацетамидо-, сульфонамидо-, метилсульфонамидо-, фенилсульфонамидо-, метилтио-, этилтиогруппу, метилсульфинил, этилсульфинил, метилсульфонил, этилсульфонил, фенилсульфинил, фенилсульфонил, циан, карбоксигруппу, метоксикарбонил, этоксикарбонил, а также ацил или бензоил.
R3 обозначает предпочтительно, например, А, циклоалкил, Аr, СН2Аr, СН2ОАr, СH2СH2Аr, СH2Het, CH2CH2Het или СН=СН-Аr.
R6 обозначает Н, А или бензил, но особенно предпочтительно Н.
Х отсутствует или предпочтительно обозначает, например, -СО-, -СН2-, -CH2-CH2-, -СН2-СО-, -СН2-СН2-СО-, -СН=СН-СО-, NR6O-, -N{[CH2]n-COOR6}-CO- или -СH(СООR6)-СH2-СО-.
Y обозначает предпочтительно, например, -SO2- или -СО-, а также -COO-, -CONH- или -СН2-.
Аr обозначает предпочтительно незамещенный фенил или нафтил, а также предпочтительно, например, одно-, дву- либо тризамещенный группой А, фтором, хлором, бромом, иодом, гидрокси-, метокси-, этокси-, пропокси-, бутокси-, пентилокси-, гексилокси-, бензилокси-, фенетилокси-, метилтио-, этилтиогруппой, метилсульфинилом, этилсульфинилом, метилсульфонилом, этилсульфонилом, фенилсульфинилом, фенилсульфонилом, нитро-, амино-, метиламино-, этиламино-, диметиламино-, диэтиламино-, формамидо-, ацетамидо-, пропиониламино-, бутириламино-, метилсульфонамидо-, этилсульфонамидо-, пропилсульфонамидо-, бутилсульфонамидо-, фенилсульфонамидо-, (4-метилфенил)сульфонамидо-, карбоксиметокси-, карбоксиэтокси-, метоксикарбонилметокси-, метоксикарбонилэтокси-, гидроксиметокси-, гидроксиэтокси-, метоксиэтокси-, карбоксигруппой, метоксикарбонилом, этоксикарбонилом, цианом, фениламинокарбонилом, ацилом либо бензоилом фенил или нафтил, а также бифенил.
С учетом этого Аr обозначает предпочтительно, например, о-, м- либо п-толил, о-, м- либо п-этилфенил, о-, м- либо п-пропилфенил, о-, м- либо п-изопропилфенил, о-, м- либо п-трет-бутилфенил, о-, м- либо п-гидроксифенил, о-, м- либо п-нитрофенил, о-, м- либо п-аминофенил, о-, м- либо п-(N-метиламино)фенил, о-, м- либо п-ацетамидофенил, о-, м- либо п-метоксифенил, о-, м- либо п-этоксифенил, о-, м- либо п-карбоксифенил, о-, м- либо п-метоксикарбонилфенил, о-, м- либо п-(N,N-диметиламино)фенил, о-, м- либо п-(N-этиламино)фенил, о-, м- либо п-(N,N-диэтиламино)фенил, о-, м- либо п-ацетилфенил, о-, м- либо п-формилфенил, о-, м- либо п-фторфенил, о-, м- либо п-бромфенил, о-, м- либо п-хлорфенил, о-, м- либо п-метилсульфонилфенил, о-, м- либо п-(фенилсульфонамидо)фенил, (метилсульфонамидо) фенил, о-, м- либо п-метилтиофенил, а также предпочтительно 2,3-, 2,4-, 2,5-, 2,6-, 3,4- либо 3,5-дифторфенил, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- либо 3,5-дихлорфенил, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- либо 3,5-дибромфенил, 2,4- либо 2,5-динитрофенил, 2,5- либо 3,4-диметоксифенил, 3-нитро-4-хлорфенил, 3-амино-4-хлор-, 2-амино-3-хлор-, 2-амино-4-хлор-, 2-амино-5-хлор- либо 2-амино-6-хлорфенил, 2-нитро-4-N, N-диметиламино- либо 3-нитро-4-N,N-диметиламинофенил, 2,3-диаминофенил, 2,3,4-, 2,3,5-, 2,3,6-, 2,4,6- либо 3,4,5-трихлорфенил, 2,4,6-триметоксифенил, 2-гидрокси-3,5-дихлорфенил, п-иодфенил, 3,6-дихлор-4-аминофенил, 4-фтор-3-хлорфенил, 2-фтор-4-бромфенил, 2,5-дифтор-4-бромфенил, 3-бром-6-метоксифенил, 3-хлор-6-метоксифенил, 3-хлор-4-ацетамидофенил, 3-фтор-4-метоксифенил, 3-амино-6-метилфенил, 3-хлор-4-ацетамидофенил или 2,5-диметил-4-хлорфенил.
Наиболее предпочтительно Аr обозначает незамещенный фенил или нафтил и, кроме того, предпочтительно, например, одно-, дву- либо тризамещенный группой А, хлором, метоксигруппой, аминогруппой, диметиламиногруппой фенил или нафтил, а также бифенил.
Аr' обозначает прежде всего фенил или нафтил, предпочтительны далее и такие значения, как, например о-, м- либо п-толил, о-, м- либо этилфенил, о-, м- либо п-пропилфенил, о-, м- либо п-изопропилфенил, о-, м- либо п-трет-бутилфенил, о-, м- либо п-гидроксифенил, о-, м- либо п-нитрофенил, о-, м- либо п-аминофенил, о-, м- либо п-(N-метиламино) фенил, о-, м- либо п-ацетамидофенил, о-, м- либо п-метоксифенил, о-, м- либо п-этоксифенил, о-, м- либо п-карбоксифенил, о-, м- либо п-метоксикарбонилфенил, о-, м- либо п-(N, N-диметиламино)фенил, о-, м- либо п-(N-этиламино)фенил, о-, м- либо п-(N, N-диэтиламино) фенил, о-, м- либо п-ацетилфенил, о-, м- либо п-формилфенил, о-, м- либо п-фторфенил, о-, м- либо п-бромфенил, о-, м- либо п-хлорфенил или о-, м, либо п-метилсульфонилфенил.
Het представляет собой предпочтительно 2- либо 3-фурил, 2- либо 3-тиенил, 1-, 2- либо 3-пирролил, 1-, 2-, 4- либо 5-имидазолил, 1-, 3-, 4- либо 5-пиразолил, 2-, 4- либо 5-оксазолил, 3-, 4- либо 5-изоксазолил, 2-, 4- либо 5-тиазолил, 3-, 4- либо 5-изотиазолил, 2-, 3- либо 4-пиридил, 2-, 4-, 5- либо 6-пиримидинил, а также предпочтительно 1,2,3-триазол-1-, -4- либо -5-ил, 1,2,4-триазол-1-, -3- либо -5-ил, 1- либо 5-тетразолил, 1,2,3-оксадиазол-4- либо -5-ил, 1,2,4-оксадиазол-3- либо -5-ил, 1,3,4-тиадиазол-2- либо -5-ил, 1,2,4-тиадиазол-3- либо -5-ил, 1,2,3-тиадиазол-4- либо -5-ил, 3- либо 4-пиридазинил, пиразинил, 1-, 2-, 3-, 4-, 5-, 6- либо 7-индолил, 4- либо 5-изоиндолил, 1-, 2-, 4- либо 5-бензимидазолил, 1-, 3-, 4-, 5-, 6-, либо 7-бензопиразолил, 2-, 4-, 5-, 6- либо 7-бензоксазолил, 3-, 4-, 5-, 6- либо 7-бензизоксазолил, 2-, 4-, 5-, 6-, либо 7-бензтиазолил, 2-, 4-, 5-, 6- либо 7-бензизотиазолил, 4-, 5-, 6- либо 7-бенз-2,1,3-оксадиазолил, 2-, 3-, 4-, 5-, 6-, 7- либо 8-хинолил, 1-, 3-, 4-, 5-, 6-, 7- либо 8-изохинолил, 3-, 4-, 5-, 6-, 7- либо 8-циннолинил, 2-, 4-, 5-, 6-, 7- либо 8-хиназолинил, 5- либо 6-хиноксалинил, 2-, 3-, 5-, 6-, 7- либо 8-2Н-бензо[1,4]оксазинил, далее предпочтительно 1,3-бензодиоксол-5-ил, 1,4-бензодиоксан-6-ил, 2,1,3-бензотиадиазол-4- либо 5-ил, 2,1,3-бензоксадиазол-5-ил или дибензофуранил.
Гетероциклические остатки могут быть также частично либо полностью гидрированы.
Het, следовательно, может также обозначать, например, 2,3-дигидро-2-, -3-, -4- либо -5-фурил, 2,5-дигидро-2-, -3-, -4- либо -5-фурил, тетрагидро-2- либо -3-фурил, 1,3-диоксолан-4-ил, тетрагидро-2- либо -3-тиенил, 2,3-дигидро-1-, -2-, -3-, -4- либо -5-пирролил, 2,5-дигидро-1-, -2-, -3-, -4- либо -5-пирролил, 1-, 2- либо 3-пирролидинил, тетрагидро-1-, -2- либо -4-имидазолил, 2,3-дигидро-1-, -2-, -3-, -4- либо -5-пиразолил, тетрагидро-1-, -3- либо -4-пиразолил, 1,4-дигидро-1-, -2-, -3- либо -4-пиридил, 1,2,3,4-тетрагидро-1-, -2-, -3-, -4-, -5- либо -6-пиридил, 1-, 2-, 3- либо 4-пиперидинил, 2-, 3- либо 4-морфолинил, тетрагидро-2-, -3- либо -4-пиранил, 1,4-диоксанил, 1,3-диоксан-2-, -4- либо -5-ил, гексагидро-1-, -3- либо -4-пиридазинил, гексагидро-1-, -2-, -4- либо -5-пиримидинил, 1-, 2- либо 3-пиперазинил, 1,2,3,4-тетрагидро-1-, -2-, -3-, -4-, -5-, -6-, -7- либо -8-хинолил, 1,2,3,4-тетрагидро-1-, -2-, -3-, -4-, -5-, -6-, -7- либо -8-изохинолил, 2-, 3-, 5-, 6-, 7- либо 8-3,4-дигидро-2Н-бензо[1,4]оксазинил, далее предпочтительно 2,3-метилендиоксифенил, 3,4-метилендиоксифенил, 2,3-этилендиоксифенил, 3,4-этилендиоксифенил, 3,4-(дифторметилендиокси) фенил, 2,3-дигидробензофуран-5- либо -6-ил, 2,3-(2-оксометилендиокси)фенил или же 3,4-дигидро-2Н-1,5-бензодиоксепин-6- либо -7-ил, кроме того, предпочтительно 2,3-дигидробензофуранил либо 2,3-дигидро-2-оксофуранил.
Het является незамещенным либо одно- или многократно замещен группами Hal, A, Ar', COOR6, CN, N(R6)2, NO2, Ar-CONH-CH2. Под понятием "многократно замещен" имеется в виду дву-, трех-, четырех- либо пятикратное замещение.
Соединения формулы I могут иметь один или несколько хиральных центров и поэтому могут быть представлены в различных стереоизомерных формах. Формула I включает все эти формы.
В соответствии с этим объектом изобретения являются прежде всего такие соединения формулы I, в которых по меньшей мере один из названных остатков имеет одно из вышеуказанных предпочтительных значений. Некоторые предпочтительные группы соединений могут быть представлены следующими субформулами Ia-If, которые подпадают под формулу I и в которых не расшифрованные более подробно остатки имеют значения, указанные в формуле I, но при этом:
в Ia R1 обозначает -C(= NH)-NH2, который также может быть однократно замещен группой -СОА, -CO-[C(R6)2]n-Ar, -COOA-, -ОН либо обычной аминозащитной группой, или представляет собой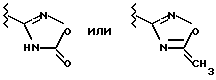
R2 обозначает Н, A, OR6, N(R6)2, NО2, CN, Hal, NHCOA, NHCOAr, NHSO2A, NHSО2Ar, COOR6, CON(R6)2, CONHAr, COR6, COAr, S(О)nА или S(О)nАr,
R3 обозначает А, циклоалкил, Аr, -СН2Аr, -СН2ОАr, -СН2СН2Аr, -СН2Неt, -СН2СН2Неt или -СН=СН-Аr,
R6 обозначает Н или А,
Х отсутствует или обозначает -СО-, -СН2-СО-, -СН2-СН2-СО-, -СН2-, -СН2-СН2-, -СН=СН-СО-, -NHCO-, -N(СН2-СООR6)-СО- или -СН(СООR6)-СН2-СО-,
Y обозначает -SO2-, -CO-, -COO-, -CO-NH- или -СН2-,
А обозначает алкил с 1-20 С-атомами, где одна либо две СН2-группы могут быть заменены на О- или S-атомы либо на -CR6=CR6-группы и/или 1-7 Н-атомов могут быть заменены на F,
Аr обозначает незамещенный либо одно-, дву- или трехкратно замещенный группой А, Аr', OR6, N(R6)2, NO2, CN, Hal, NHCOA, NHCOAr', NHSО2A, NHSO2Ar', COOR6, CON(R6)2, CONHAr', COR6, COAr', S(О)nA либо S(О)nAr фенил или нафтил,
Аr' обозначает незамещенный либо одно-, дву- или трехкратно замещенный группой A, OR6, N(R6)2, NO2, CN, Hal, NHCOA, COOR6, СОN(R6)2, COR6 либо S(О)nA фенил или нафтил,
Het обозначает одно- или двухядерную незамещенную либо одно- или многократно замещенную группой Hal, А, Аr', COOR6, CN, N(R6)2, NO2, Ar-CONH-CH2 и/или карбонильным кислородом насыщенную либо ненасыщенную гетероциклическую кольцевую систему, содержащую один, два, три или четыре идентичных либо разных гетероатома, таких как азот, кислород или сера,
Hal обозначает F, C1, Вr или J и
n обозначает 0, 1 или 2;
в Ib R1 обозначает -C(=NH)-NH2, который также может быть однократно замещен группой -СОА, -CO-[C(R6)2]n-Ar, -COOA-, -ОН либо обычной аминозащитной группой, или представляет собой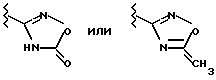
R2 обозначает Н,
R3 обозначает А, циклоалкил, Аr, -СН2Аr, -СН2ОАr, -СН2СН2Аr, -CH2Het, -CH2CH2Het или -СН=СН-Аr,
R6 обозначает Н или А,
Х отсутствует или обозначает -СО-, -СН2-СО-, -СН2-СН2-СО-, -СН2-, -СН2-СН2-, -СН=СН-СО-, -NHCO-, -N(CН2-СООR6)-СО- или -СН(СООR6)-СН2-СО-,
Y обозначает -SО2-, -СО-, -COO-, -CO-NH- или -СН2-,
А обозначает алкил с 1-20 С-атомами, где одна либо две СН2-группы могут быть заменены на О- или S-атомы либо на -СR6=CR6-группы и/или 1-7 Н-атомов могут быть заменены на F,
Аr обозначает незамещенный либо одно-, дву- или трехкратно замещенный группой А, Аr', OR6, NH2, NО2, CN, Hal, NHCOA, NHCOAr', NHSO2A, NHSO2Ar', COOR6, СОN(R6)2, CONHAr', COR6, COAr', S(О)nA либо S(О)nAr фенил или нафтил,
Аr' обозначает незамещенный либо одно-, дву- или трехкратно замещенный группой A, OR6, N(R6)2, NO2, CN, Hal, NHCOA, COOR6, CON(R6)2, COR6 либо S(О)nА фенил или нафтил,
Het обозначает одно- или двухядерную незамещенную либо одно- или многократно замещенную группой Hal, A, Ar', COOR6, CN, N(R6)2, NO2, Ar-CONH-CH2 и/или карбонильным кислородом насыщенную либо ненасыщенную гетероциклическую кольцевую систему, содержащую один, два, три или четыре идентичных либо разных гетероатома, таких как азот, кислород или сера,
Hal обозначает F, C1, Вr или J и
n обозначает 0, 1 или 2;
в Ic R1 обозначает -C(=NH)-NH2, который также может быть однократно замещен группой -СОА, -CO-[C(R6)2]n-Ar, -COOA-, -ОН либо обычной аминозащитной группой, или представляет собой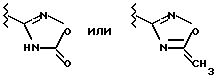
R2 обозначает Н,
R3 обозначает А, циклоалкил, Аr, -СН2Аr, -СН2ОАr, -СН2СН2Аr, -CH2Het, -СН2СH2Неt или -СН=СН-Аr,
R6 обозначает Н или А,
Х отсутствует или обозначает -СО-, -СН2-СО-, -СН2-СН2-СО-, -СН2-, -СН2-СН2-, -СН=СН-СО-, -NHCO-, -N(CH2-COOR6)-СО- или -СН(СООR6)-СН2-СО-,
Y обозначает -SO2-, -CO-, -COO-, -CO-NH- или -СН2-,
А обозначает алкил с 1-20 С-атомами, где одна либо две СН2-группы могут быть заменены на О- или S-атомы либо на -CR6=CR6-группы и/или 1-7 Н-атомов могут быть заменены на F,
Аr обозначает незамещенный либо одно-, дву- или трехкратно замещенный группой А, Аr', OR6, N(R6)2, NO2, CN, Hal, NHCOA, NHCOAr', NHSО2A, NHSО2Ar', COOR6, СОN(R6)2, CONHAr', COR6, COAr', S(О)nA либо S(О)nAr фенил или нафтил,
Аr' обозначает незамещенный либо одно-, дву- или трехкратно замещенный группой A, OR6, N(R6)2, NО2, CN, Hal, NHCOA, COOR6, CON(R6)2, COR6 либо S(O)nA фенил или нафтил,
Het обозначает одно- или двухядерную незамещенную либо одно- или многократно замещенную группой Hal, A, Ar', COOR6, CN, N(R6)2, NО2, Ar-CONH-CH2 и/или карбонильным кислородом гетероциклическую кольцевую систему, выбранную из группы, включающей тиофен, тетрагидрохинолин, хроман, пиразол, изоксазол, пиридин, бензодиоксол или бензотиофен,
Hal обозначает F, Cl, Вr или J и
n обозначает 0, 1 или 2;
в Id R1 обозначает -C(=NH)-NH2, который также может быть однократно замещен группой -СОА, -CO-[C(R6)2]n-Ar, -COOA-, -ОН либо обычной аминозащитной группой, или представляет собой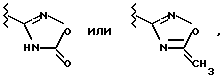
R2 обозначает Н,
R3 обозначает А, циклоалкил, Аr, -СН2Аr, -СН2ОАr, -СН2СН2Аr, -СН2Неt, -СH2СH2Неt или -СН=СН-Аr,
R6 обозначает Н или А,
Х отсутствует или обозначает -СО-, -СН2-СО-, -СН2-СН2-СО-, -СН2-, -СН2-СН2-, -СН=СН-СО-, -NHCO-, -N(CH2-COOR6)-СО- или -СH(СООR6)-СН2-СО-,
Y обозначает -SО2-, -СО-, -CO-NH- или -СН2-,
А обозначает алкил с 1-20 С-атомами, где одна либо две СН2-группы могут быть заменены на О- или S-атомы либо на -CR6=CR6-группы и/или 1-7 Н-атомов могут быть заменены на F,
Аr обозначает незамещенный либо одно-, дву- или трехкратно замещенный группой А, Аr', OR6, N(R6)2, NО2, CN, Hal, NHCOA, NHCOAr', NHSO2A, NНSО2Аr', COOR6, CON(R6)2, CONHAr', COR6, COAr', S(О)nA либо S(О)nAr фенил или нафтил,
Аr' обозначает фенил,
Het обозначает одно- или двухядерную незамещенную либо одно- или многократно замещенную группой Hal, А, Аr', COOR6, CN, N(R6)2, NO2, Ar-CONH-CH2 и/или карбонильным кислородом гетероциклическую кольцевую систему, выбранную из группы, включающей тиофен, тетрагидрохинолин, хроман, пиразол, изоксазол, пиридин, бензодиоксол, бензотиофен или дибензофуран,
Hal обозначает F, C1, Вr или J и
n обозначает 0, 1 или 2;
в Ie R1 обозначает -C(=NH)-NH2, который также может быть однократно замещен группой -СОА, -СО-[C(R6)2]n-Ar, -COOA-, -ОН либо обычной аминозащитной группой, или представляет собой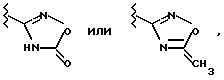
R2 обозначает Н,
R3 обозначает А, циклоалкил, Аr, -СН2Аr, -СН2ОАr, -СН2СН2Аr, -CH2Het, -CH2CH2Het или -СН=СН-Аr,
R6 обозначает Н или А,
Х отсутствует или обозначает -СО-, -СН2-СО-, -СН2-СН2-СО-, -СН2-, -СН2-СН2-, -NHCO-, -N(СН2-СООR6)-СО- или -CH(COOR6) -CH2-CO-,
Y обозначает -SO2-, -CO- или -СН2-,
А обозначает алкил с 1-20 С-атомами, где одна либо две СН2-группы могут быть заменены на О- или S-атомы либо на -CR6=CR6-группы и/или 1-7 Н-атомов могут быть заменены на F,
Аr обозначает незамещенный либо одно-, дву- или трехкратно замещенный группой А, Аr', OR6, N(R6)2, NО2, CN, Hal, NHCOA, NHCOAr', NHSО2A, NНSО2Аr', COOR6, СОN(R6)2, CONHAr', COR6, COAr', S(О)nA либо S(О)nAr фенил или нафтил,
Аr' обозначает фенил,
Het обозначает одно- или двухядерную незамещенную либо одно- или многократно замещенную группой Hal, A, Ar', COOR6, CN, N(R6)2, NO2, Ar-CONH-CH2 и/или карбонильным кислородом гетероциклическую кольцевую систему, выбранную из группы, включающей тиофен, тетрагидрохинолин, хроман, пиразол, изоксазол, пиридин, бензодиоксол, бензотиофен или дибензофуран,
Hal обозначает F, C1, Вr или J и
n обозначает 0, 1 или 2;
в If R1 обозначает -C(=NH)-NH2, который также может быть однократно замещен группой -СООА-, или представляет собой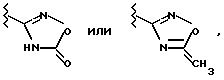
R2 обозначает Н,
R3 обозначает А, циклоалкил, Аr, -СН2Аr, -СН2ОАr, -СН2СН2Аr, -СН2Неt, -СН2СН2Неt или -СН=СН-Аr,
R6 обозначает Н или А,
Х отсутствует или обозначает -СО-, -СН2-СО-, -СН2-СН2-СО-, -СН2-, -СН2-СН2-, -NHCO-, -N(CH2-COOR6)-CO- или -CH(COOR6)-СН2-СО-,
Y обозначает -SO2-, -СО- или -СH2-,
А обозначает алкил с 1-20 С-атомами, где одна либо две СН2-группы могут быть заменены на О- или S-атомы либо на -CR6=CR6-группы и/или 1-7 Н-атомов могут быть заменены на F,
Аr обозначает незамещенный либо одно-, дву- или трехкратно замещенный группой А, Аr', OR6, N(R6)2, NO2, CN, Hal, NHCOA, NHCOAr', NHSO2A, NНSО2Аr', COOR6, СОN(R6)2, CONHAr', COR6, COAr', S(О)nA либо S(О)nAr фенил или нафтил,
Аr' обозначает фенил,
Het обозначает одно- или двухядерную незамещенную либо одно- или многократно замещенную группой Hal, A, Ar', COOR6, CN, N(R6)2, NO2, Ar-CONH-CH2 и/или карбонильным кислородом гетероциклическую кольцевую систему, выбранную из группы, включающей тиофен, тетрагидрохинолин, хроман, пиразол, изоксазол, пиридин, бензодиоксол, бензотиофен или дибензофуран,
Hal обозначает F, Cl, Вr или J и
n обозначает 0, 1 или 2.
Соединения формулы I, равно как и исходные вещества для их получения, в остальном получают по известным методам, описанным в литературе (например, в таких основополагающих публикациях, как Houben-Weyl, Methoden der Organischen Chemie, изд-во Georg-Thieme-Verlag, Stuttgart), а именно при соблюдении условий, известных и пригодных для осуществления указанных реакций. При этом могут использоваться также известные, не поясняемые в настоящем описании более подробно варианты.
Исходные вещества при необходимости могут быть также образованы in situ, что исключает необходимость их выделения из реакционной смеси и позволяет непосредственно использовать их для последующего превращения в соединения формулы I.
Одна из предпочтительных возможностей получения соединений формулы I состоит в том, что эти соединения формулы I высвобождают из одного из их функциональных производных путем обработки агентом сольволиза или гидрогенолиза. Предпочтительными исходными веществами для осуществления сольволиза соответственно гидрогенолиза являются такие вещества, которые в принципе подпадают под формулу I, но вместо одной либо нескольких свободных амино- и/или гидроксильных групп содержат соответствующие защищенные амино- и/или гидроксильные группы, предпочтительно такие, которые вместо Н-атома, связанного с N-атомом, несут аминозащитную группу, прежде всего такие, которые вместо HN-группы несут R'-N- группу, где R' обозначает аминозащитную группу, и/или такие, которые вместо Н-атома гидроксильной группы несут гидроксизащитную группу, например, такие, которые подпадают под формулу I, но вместо группы -СООН несут группу -COOR", где R" обозначает гидроксизащитную группу. К предпочтительным исходным веществам относятся и производные оксодиазола, которые можно переводить в соответствующие аминосоединения. Успешно вводить оксадиазольную группу можно, например, взаимодействием цианосоединений с гидроксиламином и реакцией с фосгеном, диалкилкарбонатом, эфиром хлормуравьиной кислоты, N,N'-карбонилдиимидазолом или ацетангидридом. В молекуле исходного вещества могут иметься также несколько - идентичных либо разных - защищенных амино- и/или гидроксильных групп. При наличии отличающихся друг от друга защитных групп их можно во многих случаях отщеплять селективно.
Понятие "аминозащитная группа" общеизвестно и относится к группам, которые способны защищать (блокировать) аминогруппу от химических превращений, но которые можно легко удалять по завершении требуемой химической реакции в других местах молекулы. Типичными представителями таких групп являются прежде всего незамещенные либо замещенные ацильные, арильные, аралкоксиметильные или аралкильные группы. Поскольку аминозащитные группы по завершении требуемой реакции (или соответствующей стадии) удаляют, их тип и величина в остальном не играют существенной роли, предпочтительны, однако, группы с 1-20, прежде всего с 1-8 С-атомами.
Понятие "ацильная группа" применительно к предлагаемому способу трактуется в самом широком смысле. Оно включает ацильные группы, являющиеся производными алифатических, аралифатических, ароматических или гетероциклических карбоновых кислот либо сульфокислот, а также прежде всего алкоксикарбонильные, арилоксикарбонильные и в первую очередь аралкоксикарбонильные группы. В качестве примеров таких ацильных групп можно назвать алканоил, такой как ацетил, пропионил, бутирил; аралканоил, такой как фенилацетил; ароил, такой как бензоил или толуил; арилоксиалканоил, такой как ФОА; алкоксикарбонил, такой как метоксикарбонил, этоксикарбонил, 2,2,2-трихлорэтоксикарбонил, БОК, (трет-бутилоксикарбонил) 2-иодэтоксикарбонил; аралкилоксикарбонил, такой как БзОК ("карбобензокси"), 4-метоксибензилоксикарбонил, Fmoc (9-флуоренилметоксикарбонил); арилсульфонил, такой как Мтр (4-метокси-2,3,6-триметилфенилсульфонил). Предпочтительными аминозащитными группами являются БОК и Мтр, а также БзОК, Fmoc, бензил и ацетил.
Понятие "гидроксизащитная группа" также общеизвестно и относится к группам, которые способны защищать гидроксигруппу от химических превращений, но которые можно легко удалять по завершении требуемой химической реакции в других местах молекулы. Типичными представителями таких групп являются указанные выше незамещенные либо замещенные арильные, аралкильные или ацильные группы, а также алкильные группы. Тип и величина гидроксизащитных групп не играют существенной роли, поскольку их по завершении требуемой химической реакции или соответствующей стадии снова удаляют; предпочтительны группы с 1-20, прежде всего с 1-10 С-атомами. В качестве примеров гидроксизащитных групп можно назвать среди прочих бензил, п-нитробензоил, п-толуолсульфонил, трет-бутил и ацетил, причем особенно предпочтительны из них бензил и трет-бутил.
Высвобождение соединений формулы I из их функциональных производных осуществляют - в зависимости от используемой защитной группы - например, с помощью сильных кислот, предпочтительно ТФК или перхлорной кислоты, а также с помощью других сильных неорганических кислот, таких как соляная кислота или серная кислота, сильных органических карбоновых кислот, таких как трихлоруксусная кислота, или сульфокислот, таких как бензол- или п-толуолсульфокислота. Присутствие дополнительного инертного растворителя возможно, но не всегда обязательно. В качестве инертных растворителей пригодны предпочтительно органические растворители, например карбоновые кислоты, такие как уксусная кислота, простые эфиры, такие как тетрагидрофуран или диоксан, амиды, такие как ДМФ, галогенированные углеводороды, такие как дихлорметан, кроме того, спирты, такие как метанол, этанол или изопропанол, а также вода. Могут использоваться и смеси названных растворителей. ТФК используют предпочтительно в избытке без добавления другого растворителя. Перхлорную кислоту используют в виде смеси из уксусной кислоты и 70%-ной перхлорной кислоты в соотношении 9:1. Температура, необходимая для отщепления, находится предпочтительно в интервале от приблизительно 0 до приблизительно 50oС, целесообразно работать в интервале от 15 до 30oС (комнатная температура).
Отщепление групп БОК, OBut и Мтр может осуществляться, например, предпочтительно с помощью ТФК в дихлорметане или с помощью приблизительно 3н. -5н. НС1 в диоксане при 15-30oС, Fmoc-группу можно отщеплять с помощью приблизительно 5-50%-ного раствора диметиламина, диэтиламина или пиперидина в ДМФ при 15-30oС.
Удаляемые гидрогенолитическим путем защитные группы (например, БзОК, бензил или высвобождение амидиновой группы из ее оксадиазольного производного) могут отщепляться, например, за счет обработки водородом в присутствии катализатора (например, катализатора на основе благородного металла, такого как палладий, предпочтительно на носителе, таком как уголь). В качестве растворителей при этом можно использовать таковые, из числа указанных выше, прежде всего, например, спирты, такие как метанол или этанол, либо амиды, такие как ДМФ. Гидрогенолиз осуществляют, как правило, при температурах в интервале от приблизительно 0 до 100oС и давлении в пределах от порядка 1 до 200 бар, предпочтительно при 20-30oС и давлении 1-10 бар. Гидрогенолиз БзОК-группы целесообразно проводить, например, в присутствии 5-10%-ного Pd/C в метаноле или с помощью формиата аммония (вместо водорода) в присутствии Pd/C в метаноле/ДМФ при 20-30oС.
Соединения формулы I, в которой R1 представляет собой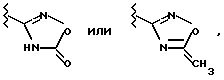
Х обозначает -СО- или -C(R6)2-CO-, а R2, R3 и Y имеют значения, указанные в пункте 1 формулы, могут быть получены взаимодействием соединений формулы II с соединениями формулы III. В соединениях формулы III L обозначает предпочтительно Cl, Br, J или реакционноспособно модифицированную ОН-группу, такую, например, как активированный сложный эфир, имидазолид или алкилсульфонилоксигруппа с 1-6 С-атомами (предпочтительно метилсульфонилокси) либо арилсульфонилоксигруппа с 6-10 С-атомами (предпочтительно фенил- или п-толилсульфонилокси). Указанную реакцию проводят, как правило, в инертном растворителе в присутствии связывающего кислоту агента, предпочтительно гидроксида, карбоната либо бикарбоната щелочного или щелочноземельного металла или же какой-либо другой соли слабой кислоты щелочных или щелочноземельных металлов, предпочтительно калия, натрия, кальция либо цезия. Целесообразным может оказаться и добавление органического основания, такого как триэтиламин, диметиланилин, пиридин либо хинолин, или добавление в избыточном количестве аминового компонента формулы II, соответственно алкилирующего производного формулы III. Продолжительность реакции в зависимости от используемых условий ее проведения составляет от нескольких минут до 14 дней, а температура реакции находится в интервале от примерно 0 до 150oС, обычно от 20 до 130oС.
В качестве инертных растворителей приемлемы среди прочих углеводороды, такие как гексан, петролейный эфир, бензол, толуол или ксилол; хлорированные углеводороды, такие как трихлорэтилен, 1,2-дихлорэтан, тетрахлорметан, хлороформ или дихлорметан; спирты, такие как метанол, этанол, изопропанол, н-пропанол, н-бутанол или трет-бутанол; простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран (ТГФ) или диоксан; простые гликолевые эфиры, такие как монометиловый либо моноэтиловый эфир этиленгликоля (метилгликоль либо этилгликоль), простые диметиловые эфиры этиленгликоля (диглимы); кетоны, такие как ацетон или бутанон; амиды, такие как ацетамид, диметилацетамид, N-метилпирролидон (N-МП) или диметилформамид (ДМФ); нитрилы, такие как ацетонитрил; сульфоксиды, такие как диметилсульфоксид (ДМСО); сероуглерод; карбоновые кислоты, такие как муравьиная кислота или уксусная кислота; нитросоединения, такие как нитрометан или нитробензол; сложные эфиры, такие как этилацетат, или же смеси вышеназванных растворителей.
Исходные соединения формул II и III, как правило, известны. Если же они окажутся новыми, то их можно получить по известным методам.
Соединения формулы I, в которой R1 представляет собой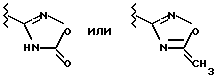
Y обозначает SO2, CO или COO, a R2 и Х имеют значения, указанные в пункте 1 формулы, могут быть предпочтительно получены взаимодействием соединений формулы IV с соединениями формулы V. В соединениях формулы IV L обозначает предпочтительно Cl, Br, J или реакционноспособно модифицированную ОН-группу, такую, например, как активированный сложный эфир, имидазолид или алкилсульфонилоксигруппа с 1-6 С-атомами (предпочтительно метилсульфонилокси) либо арилсульфонилоксигруппа с 6-10 С-атомами (предпочтительно фенил- или п-толилсульфонилокси). Взаимодействие соединений формулы IV с соединениями формулы V предпочтительно осуществлять в инертном растворителе, с добавками основания и при температурах в указанном выше интервале.
Исходные соединения формул IV и V, как правило, известны. Если же они окажутся новыми, то их можно получить по известным методам.
Соединения формулы I, в которой R1 представляет собой
Y обозначает CONH, а R2 и Х имеют значения, указанные в пункте 1 формулы, могут быть предпочтительно получены взаимодействием соединений формулы VI с соединениями формулы V. Это взаимодействие соединений формулы VI с соединениями формулы V предпочтительно осуществлять в инертном растворителе и при температурах в указанном выше интервале.
Исходные соединения формулы VI, как правило, известны. Если же они окажутся новыми, то их можно получить по известным методам.
Соединения формулы I, в которой R1 обозначает -C(=NH)-NH2, могут быть получены из соответствующих цианосоединений. Превращение цианогруппы в амидиновую группу осуществляют взаимодействием, например, с гидроксиламином и последующим восстановлением N-гидроксиамидина с помощью водорода в присутствии катализатора, такого, в частности, как Pd/C.
Для получения амидина формулы I [R1 обозначает -C(=NH)-NH2] к нитрилу формулы I (R1 обозначает CN) можно присоединять и аммиак. Такое присоединение целесообразно осуществлять в несколько стадий по известной технологии, а именно: а) превращать нитрил с помощью H2S в тиоамид, который под действием алкилирующего агента, например CH3I, переводят в соответствующий S-алкилимидотиоэфир, реагирующий в свою очередь с NH3 с образованием в результате амидина; б) превращать нитрил с помощью спирта, например этанола, в присутствии НС1 в соответствующий имидоэфир и обрабатывать этот имидоэфир аммиаком или в) подвергать нитрил взаимодействию с бис(триметилсилил)амидом лития, после чего гидролизовать полученный продукт.
Согласно другому варианту соединение формулы I можно трансформировать в другое соединение формулы I за счет превращения одного либо нескольких остатков R1, R2, R3, R4 и/или R5 в другой, соответственно другие остатки R1, R2, R3, R4 и/или R5, например, путем восстановления нитрогрупп (в частности, гидрированием в присутствии никеля Ренея или палладия на угле в инертном растворителе, таком как метанол либо этанол) до аминогрупп.
Сложные эфиры можно омылять, например, уксусной кислотой или NaOH либо КОН в воде, в смеси воды и ТГФ или в смеси воды и диоксана при температурах в интервале от 0 до 100oС.
Далее, свободные аминогруппы можно по обычной технологии ацилировать хлорангидридом либо ангидридом кислоты или алкилировать незамещенным либо замещенным алкилгалогенидом, целесообразно в инертном растворителе, таком как дихлорметан либо ТГФ, и/или в присутствии основания, такого как триэтиламин либо пиридин, при температурах в интервале от -60 до +30o.
Основание формулы I может переводиться с помощью кислоты в соответствующую кислотно-аддитивную соль, например, взаимодействием эквивалентных количеств основания и кислоты в инертном растворителе, таком как этанол, и последующим упариванием. Для такой реакции пригодны прежде всего кислоты, которые образуют физиологически приемлемые соли. Так, в частности, можно использовать такие неорганические кислоты, как серная кислота, азотная кислота, галогеноводородные кислоты, такие как хлористоводородная кислота либо бромистоводородная кислота, фосфорные кислоты, такие как ортофосфорная кислота, сульфаминокислота, а также органические кислоты, прежде всего алифатические, алициклические, аралифатические, ароматические или гетероциклические одно- либо многоосновные карбоновые, сульфоновые или серные кислоты, как, например, муравьиная кислота, уксусная кислота, пропионовая кислота, пивалиновая кислота, диэтилуксусная кислота, малоновая кислота, янтарная кислота, пимелиновая кислота, фумаровая кислота, малеиновая кислота, молочная кислота, винная кислота, яблочная кислота, лимонная кислота, глюконовая кислота, аскорбиновая кислота, никотиновая кислота, изоникотиновая кислота, метан- либо этансульфокислота, этандисульфокислота, 2-гидроксиэтансульфокислота, бензолсульфокислота, п-толуолсульфокислота, нафталинмоно- и -дисульфокислоты, лаурилсерная кислота. Касательно солей физиологически неприемлемых кислот, например пикратов, следует отметить, что они могут использоваться для выделения и/или очистки соединений формулы I.
С другой стороны, соединения формулы I с помощью оснований (например, гидроксида либо карбоната натрия или калия) можно превращать в соответствующие соли металлов, прежде всего щелочных либо щелочноземельных металлов, или в соответствующие соли аммония.
Предлагаемые в изобретении соединения формулы I благодаря особенностям структуры их молекул могут быть хиральными и в соответствии с этим могут быть представлены в различных энантиомерных формах, что делает возможным их наличие в рацемической или в оптически активной форме.
Поскольку фармацевтическая эффективность рацематов, соответственно стереоизомеров соединений по изобретению может отличаться друг от друга, может оказаться целесообразным применять энантиомеры. В этих случаях конечный продукт или даже промежуточные продукты с помощью известных специалисту в данной области химических либо физических операций можно разделять на энантиомерные соединения или же использовать их как таковые при синтезе.
В случае рацемических аминов из смеси взаимодействием с оптически активным разделяющим агентом образуют диастереомеры. В качестве разделяющих агентов пригодны, например, оптически активные кислоты, такие как R- и S-формы винной кислоты, диацетилвинной кислоты, дибензоилвинной кислоты, миндальной кислоты, яблочной кислоты, молочной кислоты, пригодны, кроме того, N-защищенные аминокислоты (например, N-бензоилпролин или N-бензолсульфонилпропин) либо различные оптически активные камфорсульфоновые кислоты. В равной степени эффективно и хроматографическое разделение энантиомеров с помощью оптически активного разделяющего агента (как, например, динитробензоилфенилглицин, триацетат целлюлозы либо другие производные углеводов или фиксированные на силикагеле хирально дериватизированные метакрилатные полимеры). В качестве растворителей для указанных целей могут использоваться водные либо спиртовые смеси растворителей, такие, например, как смесь состава гексан/изопропанол/ацетонитрил, например в соотношении 82:15:3).
Еще одним объектом изобретения является применение соединений формулы I и/или их физиологически приемлемых солей для получения фармацевтических композиций, прежде всего нехимическим путем. При этом их можно использовать совместно с по меньшей мере одним твердым, жидким и/или полужидким носителем либо вспомогательным веществом и при необходимости в сочетании с одним или несколькими другими активными веществами для изготовления соответствующих дозированных форм.
Объектом изобретения являются далее фармацевтические композиции, содержащие в своем составе по меньшей мере одно соединение формулы I и/или одну из его физиологически приемлемых солей. Эти композиции могут применяться в качестве лекарственных средств в медицине и ветеринарии. В качестве носителей для этих композиций могут рассматриваться органические или неорганические вещества, пригодные для энтерального (например, орального), парентерального или местного введения и не реагирующие с новыми соединениями, например, вода, масла растительного происхождения, бензиловые спирты, алкиленгликоли, полиэтиленгликоли, триацетат глицерина, желатин, углеводы, такие как лактоза или крахмал, стеарат магния, тальк, вазелины. Для орального назначения служат прежде всего таблетки, пилюли, драже, капсулы, порошки, грануляты, сиропы, микстуры или капли, для ректального применения - суппозитории, для парентерального применения - растворы, предпочтительно масляные либо водные растворы, кроме того, суспензии, эмульсии или имплантаты, для местного применения пригодны мази, кремы или пудра. Новые соединения можно также подвергать лиофилизации и полученные лиофилизаты использовать, например, для приготовления инъекционных препаратов. Указанные композиции можно стерилизовать и/или они могут содержать в своем составе вспомогательные вещества, такие как замасливатели, консерванты, стабилизаторы и/или смачиватели, эмульгаторы, соли для регуляции осмотического давления, буферные субстанции, красители, вкусовые добавки и/или одно либо несколько других активных веществ, например один или несколько витаминов.
Соединения формулы I и их физиологически приемлемые соли могут применяться для борьбы и предупреждения тромбоэмболических заболеваний, таких как тромбоз, инфаркт миокарда, артериосклероз, воспаления, апоплексия, стенокардия, рестеноз после ангиопластики и перемежающаяся хромота.
При этом предлагаемые согласно изобретению субстанции рекомендуется вводить, как правило, в дозировках от порядка 1 до 500 мг, прежде всего от 5 до 100 мг на одну унифицированную дозу. Суточная доза составляет предпочтительно от порядка 0,02 до 10 мг/кг веса тела пациента. Однако при назначении конкретно тому или иному пациенту специальной дозы последняя зависит от самых разных факторов, например от эффективности применяемого соединения, от возраста и веса тела пациента, общего состояния его здоровья, пола, особенностей питания, от времени и метода введения препарата, скорости выделения, комбинации лекарственных средств и степени тяжести соответствующего заболевания, которое требует данной терапии. Предпочтительно парентеральное применение.
Выше и в последующем все температуры указаны в градусах Цельсия. Под используемым в нижеследующих примерах понятием "обычная переработка" имеется в виду следующее: при необходимости добавляют воду, в зависимости от структурных особенностей конечного продукта устанавливают при необходимости назначения рН от 2 до 10, экстрагируют этилацетатом или дихлорметаном, фазы разделяют, органическую фазу сушат над сульфатом натрия, упаривают, очищают посредством хроматографии на силикагеле и/или путем кристаллизации. Rf-значения на силикагеле; элюенты: этилацетат/метанол в соотношении 9:1.
Масс-спектрометрия (МC): EI (ионизация электронным ударом) M+; FAB (бомбардировка ускоренными атомами) (M + Н)+
Пример 1
К раствору из 10,0 г 4-(5-метил-1,2,4-оксадиазол-3-ил)бензойной кислоты в 150 мл толуола добавляют 46 мл тионилхлорида и 1 мл ДМФ. Затем этот раствор нагревают в течение 5 часов с обратным холодильником. После удаления растворителя получают 4-(5-метил-1,2,4-оксадиазол-3-ил)бензоилхлорид, EI 222. Последующим взаимодействием с 9,3 г 1-трет-бутоксикарбонилпиперазина в 150 мл дихлорметана и 48 мл триэтиламина после обычной переработки получают трет-бутиловый эфир 4-[4-(5-метил [1,2,4] оксадиазол-3-ил)бензоил]пиперазин-1-карбоновой кислоты, FAB 373.
Отщепление БОК-группы проводят с помощью 4н. НС1 в диоксане. Раствор из 100 мг полученного [4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]пиперазин-1-илметанона (соединение "А") и 120 мг 6-хлорнафталин-2-сульфонилхлорида в 5 мл дихлорметана смешивают с 400 мг диметиламинопиридина на полистироле и в течение 18 часов перемешивают при комнатной температуре. После фильтрации и удаления растворителя получают [4-(6-хлорнафталин-2-сульфонил)пиперазин-1-ил]-[4-(5-метил [1,2,4 ]оксадиазол-3-ил) фенил] метанон, FAB 497.
Аналогичным путем взаимодействием соединения "А"
с 4-бифенилил-2-сульфонилхлоридом получают [4-(4-бифенилилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 2-нафтилсульфонилхлоридом получают [4-(2-нафтилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 4-пропилфенилсульфонилхлоридом получают [4-(4-пропилфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 2-фенилвинилсульфонилхлоридом получают [4-(2-фенилвинилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 3-нитро-4-хлорфенилсульфонилхлоридом получают [4-(3-нитрохлорфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 2-нитро-4-метоксифенилсульфонилхлоридом получают [4-(2-нитро-4-метоксифенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил] метанон;
с п-толилсульфонилхлоридом получают [4-(4-толилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с децилсульфонилхлоридом получают [4-(децилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с бензилсульфонилхлоридом получают [4-(бензилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 3-нитро-6-метилбензилсульфонилхлоридом получают [4-(3-нитро-6-метилбензилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] метанон;
с 2,3-дихлорфенилсульфонилхлоридом получают [4-(2,3-дихлорфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 3,4-дихлорфенилсульфонилхлоридом получают [4-(3,4-дихлорфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с фенилсульфонилхлоридом получают [4-(фенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 3-бромфенилсульфонилхлоридом получают [4-(3-бромфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 3,4-диметоксифенилсульфонилхлоридом получают [4-(3,4-диметоксифенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 4-ацетамидо-3-хлорфенилсульфонилхлоридом получают [4-(4-ацетамидо-3-хлорфенилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил] метанон;
с 4-хлор-2,5-диметилфенилсульфонилхлоридом получают [4-(4-хлор-2,5-диметилфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил] метанон;
с м-толилсульфонилхлоридом получают [4-(3-толилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 2-метокси-5-метилфенилсульфонилхлоридом получают [4-(2-метокси-5-метилфенилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] метанон;
с 3-хлорфенилсульфонилхлоридом получают [4-(3-хлорфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 4-метоксифенилсульфонилхлоридом получают [4-(4-метоксифенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 2-тиенилсульфонилхлоридом получают [4-(2-тиенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 4-хлорфенилсульфонилхлоридом получают [4-(4-хлорфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с изопропилсульфонилхлоридом получают [4-(изопропилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил] метанон;
с 8-хинолилсульфонилхлоридом получают [4-(8-хинолилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 4-нитрофенилсульфонилхлоридом получают [4-(4-нитрофенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 3-хлор-6-метоксифенилсульфонилхлоридом получают [4-(3-хлор-6-метоксифенилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] метанон;
с 4-ацетамидофенилсульфонилхлоридом получают [4-(4-ацетамидофенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил] метанон;
с 2,2,5,7,8-пентаметилхроман-6-илсульфонилхлоридом получают [4-(2,2,5,7,8-пентаметилхроман-6-илсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]метанон;
с камфор-10-илсульфонилхлоридом получают [4-(камфор-10-илсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 5-(1-метил-5-трифторметил-3-пиразолил)-2-тиенилсульфонилхлоридом получают { 4-[5-(1-метил-5-трифторметил-3-пиразолил)-2-тиенилсульфонил] пиперазин-1-ил}-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 2,5-дихлорфенилсульфонилхлоридом получают [4-(2,5-дихлорфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 2,4,6-триметилфенилсульфонилхлоридом получают [4-(2,4,6-триметилфенилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]метанон;
с 2-метилсульфонилфенилсульфонилхлоридом получают [4-(2-метилсульфонилфенилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] метанон;
с 5-бензамидометил-2-тиенилсульфонилхлоридом получают [4-(5-бензамидометил-2-тиенилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]метанон;
с метилсульфонилхлоридом получают [4-(метилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 1,3-диметил-5-хлор-4-пиразолилсульфонилхлоридом получают [4-(1,3-диметил-5-хлор-4-пиразолилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]метанон;
с 3,5-диметил-4-изоксазолилсульфонилхлоридом получают [4-(3,5-диметил-4-изоксазолилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]метанон;
с 4-бром-2-этилфенилсульфонилхлоридом получают [4-(4-бром-2-этилфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 1-нафтилсульфонилхлоридом получают [4-(1-нафтилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 5-диметиламино-1-нафтилсульфонилхлоридом получают [4-(5-диметиламино-1-нафтилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]метанон;
с 3,4-дифторфенилсульфонилхлоридом получают [4-(3,4-дифторфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 4-трет-бутилфенилсульфонилхлоридом получают [4-(4-трет-бутилфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 4-этилфенилсульфонилхлоридом получают [4-(4-этилфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 4-(1,1-диметилпропил)фенилсульфонилхлоридом получают [4-(4-(1,1-диметилпропил)фенилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]метанон;
с 4-изопропилфенилсульфонилхлоридом получают [4-(4-изопропилфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 4-трифторметилфенилсульфонилхлоридом получают [4-(4-трифторметилфенилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]метанон;
с 3-нитро-4-метилфенилсульфонилхлоридом получают [4-(3-нитро-4-метилфенилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]метанон;
с 4-пентилфенилсульфонилхлоридом получают [4-(4-пентилфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 4-бутилфенилсульфонилхлоридом получают [4-(4-бутилфенилсульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 3-хлор-4-метилфенилсульфонилхлоридом получают [4-(3-хлор-4-метилфенилсульфонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]метанон.
Пример 2
Раствор из 100 мг [4-(6-хлорнафталин-2-сульфонил)пиперазин-1-ил]-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] метанона в 5 мл метанола смешивают со 100 мг никеля Ренея и одной каплей уксусной кислоты и гидрируют до завершения реакции при нормальном давлении и комнатной температуре. После удаления катализатора и растворителя получают 4- [4-(6-хлорнафталин-2-сульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 457.
Аналогичным путем из представленных в примере 1 производных метанона получают следующие соединения:
4-[4-(4-бифенилилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 449;
4-[4-(2-нафтилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, EI 405 (M+-NH2);
4-[4-(4-пропилфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 415;
4-[4-(2-фенилвинилсульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 399;
4-[4-(3-амино-4-хлорфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 422;
4-[4-(2-амино-4-метоксифенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 418;
4-[4-(4-толилсульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 387;
4-[4-(децилсульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 437;
4-[4-(бензилсульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 387;
4-[4-(3-амино-6-метилбензилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 402;
4-[4-(2,3-дихлорфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 441;
4-[4-(3,4-дихлорфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 441;
4-[4-(фенилсульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 373;
4-[4-(3-бромфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 451, 453;
4-[4-(3,4-диметоксифенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 433;
4-[4-(4-ацетамидо-3-хлорфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 464;
4-[4-(4-хлор-2,5-диметилфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 435;
4-[4-(3-толилсульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 387;
4-[4-(2-метокси-5-метилфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 417;
4-[4-(3-хлорфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 407;
4-[4-(4-метоксифенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 402;
4-[4-(2-тиенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 379;
4-[4-(4-хлорфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 407;
4-[4-(изопропилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 339;
4-[4-(1,2,3,4-тетрагидрохинолин-8-илсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 428;
4-[4-(4-аминофенилсульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 388;
4-[4-(3-хлор-6-метоксифенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 437;
4-[4-(4-ацетамидофенилсульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 437;
4-[4-(2,2,5,7,8-пентаметилхроман-6-илсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 499;
4-[4-(камфор-10-илсульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 447;
4-{ 4-[5-(1-метил-5-трифторметил-3-пиразолил)-2-тиенилсульфонил] пиперазин-1-карбонил}бензамидин, ацетат, FAB 527;
4-[4-(2,5-дихлорфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 441;
4-[4-(2,4,6-триметилфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 415;
4-[4-(2-метилсульфонилфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 451;
4-[4-(5-бензамидометил-2-тиенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 512;
4-[4-(метилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, El 292 (M+-NH2);
4-[4-(1,3-диметил-5-хлор-4-пиразолилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат;
4-[4-(3,5-диметил-4-изоксазолилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат;
4-[4-(4-бром-2-этилфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, EI 461, 463 (M+-NH2);
4-[4-(1-нафтилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, EI 405(M+-NH2);
4-[4-(5-диметиламино-1-нафтилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, EI 448 (M+-NH2);
4-[4-(3,4-дифторфенилсульфонил)пиперазин-1-карбонил]бензамидин, ацетат;
4-[4-(4-трет-бутилфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 429;
4-[4-(4-этилфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 401;
4-[4-(4-(1,1-диметилпропил)фенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 442;
4-[4-(4-изопропилфенилсульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 415;
4-[4-(4-трифторметилфенилсульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 441;
4-[4-(3-амино-4-метилфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 402;
4-[4-(4-пентилфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 443;
4-[4-(4-бутилфенилсульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 429;
4-[4-(3-хлор-4-метилфенилсульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 421.
Пример 3
Взаимодействием с эквимолярными количествами метилового эфира хлормуравьиной кислоты в пиридине и каталитическими количествами диметиламинопиридина из 4-[4-(6-хлорнафталин-2-сульфонил)пиперазин-1-карбонил]бензамидина после обычной переработки получают метиловый эфир {имино-[4-(4-(6-хлорнафталин-2-сульфонил)пиперазин-1-карбонил) фенил]метил}карбаминовой кислоты.
Пример 4
Аналогично примеру 1 взаимодействием 3-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил] -1-пиперазин-1-илпропан-1-она [получаемого из 3-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] -1-(4-трет-бутилоксикарбонил)пиперазин-1-илпропан-1-она обработкой ТФУК/СН2С12] с 6-хлорнафталин-2-сульфонилхлоридом получают 1-[4-(6-хлорнафталин-2-сульфонил)пиперазин-1-ил] -3-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] пропан-1-он и после гидрирования получают 4-{3-оксо-3-[4-(6-хлорнафталин-2-сульфонил)пиперазин-1-ил]пропил}бензамидин.
Пример 5
Аналогично примерам 1 и 2 взаимодействием [3-(5-метил[1,2,4]оксадиазол-3-ил)фенил]пиперазин-1-илметанона с 5-хлорнафталин-2-сульфонилхлоридом и последующим гидрированием получают 3-[4-(6-хлорнафталин-2-сульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 457.
Аналогичным путем взаимодействием [3-(5-метил[1,2,4] оксадиазол-3-ил)фенил] пиперазин-1-илметанона с 4-пропилфенилсульфонилхлоридом и последующим гидрированием получают 3-[4-(4-пропилфенилсульфонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 415.
Пример 6
Аналогично примеру 1 взаимодействием 2-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил] -1-пиперазин-1-илэтан-1-она (соединение "Б") с 4-пропилфенилсульфонилхлоридом получают 1-[4-(4-пропилфенилсульфонил)пиперазин-1-ил]-2-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] этан-1-он, а после гидрирования получают 4-[2-оксо-2- [4-(4-пропилфенилсульфонил)пиперазин-1-ил]этил}бензамидин, FAB 429.
Аналогичным путем взаимодействием соединения "Б"
с децилсульфонилхлоридом получают 1-[4-(децилсульфонил)пиперазин-1-ил] -2-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]этан-1-он;
с фенилсульфонилхлоридом получают 1-[4-(фенилсульфонил)пиперазин-1-ил] -2-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]этан-1-он;
с 3,4-дихлорфенилсульфонилхлоридом получают 1-[4-(3,4-дихлорфенилсульфонил)пиперазин-1-ил]-2-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]этан-1-он;
с бензилсульфонилхлоридом получают 1-[4-(бензилсульфонил)пиперазин-1-ил] -2-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]этан-1-он;
с 3,4-диметоксифенилсульфонилхлоридом получают 1-[4-(3,4-диметоксифенилсульфонил)пиперазин-1-ил] -2-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] этан-1-он;
с изопропилсульфонилхлоридом получают 1-[4-(изопропилсульфонил)пиперазин-1-ил] -2-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]этан-1-он;
с камфор-10-илсульфонилхлоридом получают 1-[4-(камфор-10-илсульфонил)пиперазин-1-ил]-2-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]этан-1-он;
с 3-метокси-4-метоксикарбонил-2-тиенилсульфонилхлоридом получают 1-[4-(3-метокси-4-метоксикарбонил-2-тиенилсульфонил)пиперазин-1-ил] -2-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]этан-1-он;
с 2,4,6-триметилфенилсульфонилхлоридом получают 1-[4-(2,4,6-триметилфенилсульфонил)пиперазин-1-ил] -2-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] этан-1-он;
с 2-фенилвинилсульфонилхлоридом получают 1-[4-(2-фенилвинилсульфонил)пиперазин-1-ил]-2-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]этан-1-он;
с метилсульфонилхлоридом получают 1-[4-(2-метилсульфонил)пиперазин-1-ил] -2-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]этан-1-он;
с [2,1,3] бензотиадиазол-4-илсульфонилхлоридом получают 1-[4-([2,1,3] бензотиадиазол-4-илсульфонил)пиперазин-1-ил]-2-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]этан-1-он;
с 2,4-дихлорфенилсульфонилхлоридом получают 1-[4-(2,4-дихлорфенилсульфонил)пиперазин-1-ил]-2-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]этан-1-он;
с 1-нафтилсульфонилхлоридом получают 1-[4-(1-нафтилсульфонил)пиперазин-1-ил]-2-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]этан-1-он;
с 2-нафтилсульфонилхлоридом получают 1-[4-(2-нафтилсульфонил)пиперазин-1-ил]-2-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]этан-1-он;
с 5-диметиламино-1-нафтилсульфонилхлоридом получают 1-[4-(5-диметиламино-1-нафтилсульфонил)пиперазин-1-ил] -2-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]этан-1-он;
с 4-метилсульфонилфенилсульфонилхлоридом получают 1-[4-(4-метилсульфонилфенилсульфонил)пиперазин-1-ил]-2-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил] этан-1-он.
Путем гидрирования из представленных выше соединений получают следующие амидиновые производные:
4-{ 2-оксо-2-[4-(децилсульфонил)пиперазин-1-ил] этил}бензамидин, ацетат, FAB 450;
4-{ 2-оксо-2-[4-(фенилсульфонил)пиперазин-1-ил] этил}бензамидин, ацетат, FAB 387;
4-{2-оксо-2-[4-(3,4-дихлорфенилсульфонил)пиперазин-1-ил]этил}бензамидин, ацетат, FAB 454;
4-{ 2-оксо-2-[4-(бензилсульфонил)пиперазин-1-ил]этил}бензамидин, ацетат, FAB 401;
4-{ 2-оксо-2-[4-(3,4-диметоксифенилсульфонил)пиперазин-1-ил] этил}бензамидин, ацетат, FAB 447;
4-{ 2-оксо-2-[4-(изопропилсульфонил)пиперазин-1-ил]этил}бензамидин, ацетат, FAB 353;
4-{ 2-оксо-2-[4-(камфор-10-илсульфонил)пиперазин-1-ил] этил} бензамидин, ацетат, FAB 353;
4-{2-оксо-2-[4-(3-метокси-4-метоксикарбонил-2-тиенилсульфонил)пиперазин-1-ил]этил}бензамидин, ацетат, FAB 481;
4-{ 2-оксо-2-[4-(2,4,6-триметилфенилсульфонил)пиперазин-1-ил] этил} бензамидин, ацетат, FAB 429;
4-{ 2-оксо-2-[4-(2-фенилвинилсульфонил)пиперазин-1-ил] этил} бензамидин, ацетат, FAB 413;
4-{ 2-оксо-2-[4-(метилсульфонил)пиперазин-1-ил] этил}бензамидин, ацетат, FAB 325;
4-{ 2-оксо-2-[4-(2,3-диаминофенилсульфонил)пиперазин-1-ил] этил}бензамидин, ацетат, FAB 415;
4-{2-оксо-2-[4-(2,4-дихлорфенилсульфонил)пиперазин-1-ил]этил}бензамидин, ацетат, FAB 455;
4-{ 2-оксо-2-[4-(1-нафтилсульфонил)пиперазин-1-ил] этил}бензамидин, ацетат, FAB 437;
4-{ 2-оксо-2-[4-(2-нафтилсульфонил)пиперазин-1-ил] этил}бензамидин, ацетат, FAB 437;
4-{ 2-оксо-2-[4-(5-диметиламино-1-нафтилсульфонил)пиперазин-1-ил] этил} бензамидин, ацетат, FAB 480;
4-{ 2-оксо-2-[4-(4-метилсульфонилфенилсульфонил)пиперазин-1-ил]этил}бензамидин, ацетат, FAB 465.
Пример 7
Аналогично примеру 1 взаимодействием соединения "А"
с хлорангидридом 4-бифенилилкарбоновой кислоты получают [4-(4-фенилбензоил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с хлорангидридом циклопентилкарбоновой кислоты получают [4-(циклопентилкарбонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] метанон;
с феноксиацетилхлоридом получают [4-(феноксиацетил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с хлорангидридом 1-нафтилкарбоновой кислоты получают [4-(1-нафтилкарбонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с хлорангидридом 2-нафтилкарбоновой кислоты получают [4-(2-нафтилкарбонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с никотиноилхлоридом получают [4-(никотиноил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 3-нитробензоилхлоридом получают [4-(3-нитробензоил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с хлорангидридом бензо[b] тиофен-2-карбоновой кислоты [4-(бензо[b]тиофен-2-карбонил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил] метанон;
с 4-трифторметоксибензоилхлоридом получают [4-(4-трифторметоксибензоил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 2,5-диметоксифенилацетилхлоридом получают [4-(2,5-диметоксифенилацетил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с 4-хлорфенилацетилхлоридом получают [4-(4-хлорфенилацетил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с хлорангидридом 1,3-бензодиоксол-5-карбоновой кислоты [4-(1,3-бензодиоксол-5-карбонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] метанон;
с 3,4-дихлорбензоилхлоридом получают [4-(3,4-дихлорбензоил)пиперазин-1-ил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]метанон;
с изобутиловым эфиром хлормуравьиной кислоты получают [4-(изобутилоксикарбонил)пиперазин-1-ил] -[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]метанон.
Путем гидрирования из представленных выше соединений получают следующие амидиновые производные:
4-[4-(4-фенилбензоил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 413;
4-[4-(циклопентилкарбонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 329;
4-[4-(феноксиацетил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 367;
4-[4-(1-нафтилкарбонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 387;
4-[4-(2-нафтилкарбонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 387;
4-[4-(никотиноил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 338;
4-[4-(3-аминобензоил)пиперазин-1-карбонил] бензамидин;
4-[4-(бензо[b]тиофен-2-карбонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 393;
4-[4-(4-трифторметоксибензоил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 421;
4-[4-(2,5-диметоксифенилацетил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 411;
4-[4-(4-хлорфенилацетил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 385;
4-[4-(1,3-бензодиоксол-5-карбонил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 381;
4-[4-(3,4-дихлорбензоил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 381;
4-[4-(изобутилоксикарбонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 333.
Пример 8
Взаимодействием с эквимолярными количествами ацетилхлорида в пиридине и каталитическими количествами диметиламинопиридина после обычной переработки из 4-[4-(6-хлорнафталин-2-сульфонил)пиперазин-1-карбонил] бензамидина получают N-{ имино-4-[4-(6-хлорнафталин-2-сульфонил)пиперазин-1-карбонил]фенилметил}ацетамид.
Пример 9
Взаимодействием эквимолярных количеств 4-цианбензилбромида, БОК-пиперазина и триэтиламина в дихлорметане получают 1-(4-цианбензил)-4-(трет-бутилоксикарбонил)пиперазин. Взаимодействием с а) гидроксиламингидрохлоридом, триэтиламином в этаноле и б) ацетангидридом получают 1-[4-(5-метил[1,2,4] оксадиазол-3-ил)бензил]-4-(трет-бутилоксикарбонил)пиперазин.
После отщепления БОК-группы с помощью ТФУК в СН2С12 аналогично примерам 1 и 2 взаимодействием 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензил]пиперазина с 6-хлорнафталин-2-сульфонилхлоридом, последующим гидрированием и после обычной переработки получают 4- [(6-хлорнафталин-2-сульфонил)пиперазин-1-илметил] бензамидин.
Аналогичным путем получают следующие соединения:
4-[(4-бифенилилсульфонил)пиперазин-1-илметил]бензамидин,
4-[(2-нафтилсульфонил)пиперазин-1-илметил]бензамидин,
4-[(4-пропилфенилсульфонил)пиперазин-1-илметил]бензамидин и
4-[(2-фенилвинилсульфонил)пиперазин-1-илметил]бензамидин.
Пример 10
Взаимодействием эквимолярных количеств 4-(5-метил[1,2,4]оксадиазол-3-ил] бензойной кислоты, азида дифенилового эфира фосфорной кислоты и триэтиламина в ДМФ после обычной переработки получают 4-(5-метил [1,2,4] оксадиазол-3-ил)бензоилазид.
Нагреванием с использованием БОК-пиперазина в толуоле путем перегруппировки и после обычной переработки получают 1-БОК-4-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенилкарбамоил]пиперазин. После отщепления БОК-группы с помощью ТФУК в СН2С12 получают 4-[4-(5-метил [1,2,4]оксадиазол-3-ил)фенилкарбамоил]пиперазин (соединение "В").
Взаимодействием соединения "В" с 6-хлорнафталинсульфонилхлоридом и последующим гидрированием аналогично примерам 1 и 2 получают N-(4-амидинофенил)амид.
Аналогичным путем получают следующие соединения:
N-(4-амидинофенил)амид 4-(4-бифенилилсульфонил)пиперазин-1-карбоновой кислоты,
N-(4-амидинофенил)амид 4-(2-нафтилсульфонил)пиперазин-1-карбоновой кислоты,
N-(4-амидинофенил)амид 4-(4-пропилфенилсульфонил)пиперазин-1-карбоновой кислоты и
N-(4-амидинофенил) амид 4-(2-фенилвинилсульфонил)пиперазин-1-карбоновой кислоты.
Пример 11
Взаимодействием эквимолярных количеств 1-БОК-4-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенилкарбамоил]пиперазина, метилового эфира бромуксусной кислоты и трет-бутилата калия в ДМФ после обычной переработки получают метиловый эфир { (4-БОК-пиперазин-1-карбонил)- [4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] амино}уксусной кислоты.
Реакцией с а) HCl/диоксаном и б) NaOH получают метиловый эфир { (пиперазин-1-карбонил)-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]амино}уксусной кислоты.
Взаимодействием с 6-хлорнафталинсульфонилхлоридом аналогично примеру 1 получают метиловый эфир {[4-(6-хлорнафталин-2-сульфонил)пиперазин-1-карбонил]-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]амино}уксусной кислоты.
Гидрированием в присутствии никеля Ренея из последнего соединения получают метиловый эфир {[4-(6-хлорнафталин-2-сульфонил)пиперазин-1-карбонил] -[4-амидинофенил]амино}уксусной кислоты.
Расщепление метилового эфира проводят обработкой NaOH в смеси метанола и воды. После обычной переработки получают { [4-(6-хлорнафталин-2-сульфонил)пиперазин-1-карбонил]-[4-амидинофенил]амино}уксусную кислоту.
Аналогичным путем получают следующие соединения:
{ [4-(4-бифенилилсульфонил)пиперазин-1-карбонил] -[4-амидинофенил]амино} уксусную кислоту,
{ [4-(2-нафтилсульфонил)пиперазин-1-карбонил] -[4-амидинофенил]амино}уксусную кислоту,
{[4-(4-пропилфенилсульфонил)пиперазин-1-карбонил]-[4-амидинофенил]амино} уксусную кислоту и
{ [4-(2-фенилвинилсульфонил)пиперазин-1-карбонил]-[4-амидинофенил]амино} уксусную кислоту.
Пример 12
Взаимодействием эквимолярных количеств 4-(5-метил[1,2,4]оксадиазол-3-ил)фенилуксусной кислоты, метилиодида и карбоната калия получают метиловый эфир 4-(5-метил[1,2,4] оксадиазол-3-ил)фенилуксусной кислоты (соединение "Г").
Нагреванием эквимолярных количеств БОК-пиперазина и хлорацетилхлорида в толуоле после обычной переработки получают 1-БОК-4-хлорметилкарбонилпиперазин (соединение "Д").
Взаимодействием соединений "Г" и "Д" с NaH в ДМФ после обычной переработки получают метиловый эфир 4-(4-БОК-пиперазин-1-ил)-2-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]-4-оксомасляной кислоты.
Реакцией с а) HCl/диоксаном и б) NaOH получают метиловый эфир 4-(пиперазин-1-ил)-2-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] -4-оксомасляной кислоты.
Взаимодействием с 6-хлорнафталинсульфонилхлоридом аналогично примеру 1 получают метиловый эфир 4-[4-(6-хлорнафталин-2-сульфонил)пиперазин-1-ил]-2-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]-4-оксомасляной кислоты.
Гидрированием аналогично примеру 2 из последнего соединения получают метиловый эфир 4-[4-(6-хлорнафталин-2-сульфонил)пиперазин-1-ил] -2-(4-амидинофенил)-4-оксомасляной кислоты.
Расщепление метилового эфира осуществляют обработкой NaOH в смеси метанола и воды. После обычной переработки получают 4-[4-(6-хлорнафталин-2-сульфонил)пиперазин-1-ил]-2-(4-амидинофенил)-4- оксомасляную кислоту.
Аналогичным путем получают следующие соединения:
4-[4-(4-бифенилилсульфонил)пиперазин-1-ил] -2-(4-амидинофенил)-4-оксомасляную кислоту,
4-[4-(2-нафтилсульфонил)пиперазин-1-ил] -2-(4-амидинофенил)-4-оксомасляную кислоту,
4-[4-(4-пропилфенилсульфонил)пиперазин-1-ил] -2-(4-амидинофенил)-4-оксомасляную кислоту,
4-[4-(2-фенилвинилсульфонил)пиперазин-1-ил] -2-(4-амидинофенил)-4-оксомасляную кислоту.
Пример 13
Взаимодействием эквимолярных количеств соединения "А" и фенилизоцианата в дихлорметане, осуществляемом при комнатной температуре, после обычной переработки получают N-фениламид 4-[4-(5-метил[1,2,4] оксадиазол-3-ил)бензоил]пиперазин-1-карбоновой кислоты.
Аналогичным путем взаимодействием соединения "А"
с 4-трифторметилфенилизоцианатом получают N-(4-трифторметилфенил)амид 4-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензоил]пиперазин-1-карбоновой кислоты;
с бутилизоцианатом получают N-бутиламид 4-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензоил]пиперазин-1-карбоновой кислоты;
с 1-нафтилизоцианатом получают N-(1-нафтил)амид 4-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензоил]пиперазин-1-карбоновой кислоты;
с 4-метоксифенилизоцианатом получают N-(4-метоксифенил)амид 4- [4-(5-метил[1,2,4]оксадиазол-3-ил)бензоил]пиперазин-1-карбоновой кислоты;
с 4-нитрофенилизоцианатом получают N-(4-нитрофенил)амид 4-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензоил]пиперазин-1-карбоновой кислоты;
с циклогексилизоцианатом получают N-циклогексиламид 4-[4-(5-метил[1,2,4] оксадиазол-3-ил)бензоил]пиперазин-1-карбоновой кислоты;
с 3-этоксикарбонилфенилизопианатом получают N-(3-этоксикарбонилфенил)амид 4-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензоил]пиперазин-1-карбоновой кислоты.
Гидрированием аналогично примеру 2 из представленных выше соединений получают следующие амидиновые производные:
N-фениламид 4-(4-амидинобензоил)пиперазин-1-карбоновой кислоты, ацетат, FAB 352;
N-бутиламид 4-(4-амидинобензоил)пиперазин-1-карбоновой кислоты, ацетат, FAB 332;
N-(1-нафтил)амид 4-(4-амидинобензоил)пиперазин-1-карбоновой кислоты, ацетат, FAB 402;
N-(4-метоксифенил)амид 4-(4-амидинобензоил)пиперазин-1-карбоновой кислоты, ацетат, FAB 382;
N-(4-аминофенил)амид 4-(4-амидинобензоил)пиперазин-1-карбоновой кислоты, ацетат, FAB 367;
N-циклогексиламид 4-(4-амидинобензоил)пиперазин-1-карбоновой кислоты, ацетат, FAB 358;
N-(3-этоксикарбонилфенил)амид 4-(4-амидинобензоил)пиперазин-1-карбоновой кислоты, ацетат, FAB 424.
Пример 14
Аналогично примерам 1 и 2 получают следующие соединения:
3-[4-(2-нафтилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 423;
3-[4-(3-хлор-4-метилфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 421;
3-[4-(2,4,6-трихлорфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 475, 477;
3-[4-(3-амино-4-хлорфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 422;
3-[4-(4-хлорфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 407;
3-[4-(3-трифторметилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 441;
3-[4-(4-бифенилилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 449;
4-[4-(3,5-диметоксифенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 433;
4-[4-(дибензофуран-2-илсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 463;
4-[4-(3-фтор-4-метоксифенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 421;
4-[4-(2,4-дихлор-6-метоксифенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 471;
4-(4-бензилпиперазин-1-карбонил)бензамидин, ацетат, FAB 323;
4-[4-(2-нафтилметил)пиперазин-1-карбонил]бензамидин, ацетат, FAB 373;
4-[4-(4-метоксифенилметил)пиперазин-1-карбонил]бензамидин, диацетат, FAB 353;
4-[4-(4-метоксикарбонилфенилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 431;
4-[4-(4-пропилфенилсульфонил)пиперазин-1-карбонил] -3-метилбензамидин, ацетат, FAB 429;
4-[4-(2-нафтилсульфонил)пиперазин-1-карбонил]-3-метилбензамидин, ацетат, FAB 437;
4-[4-(6-хлор-2-нафтилсульфонил)пиперазин-1-карбонил] -3-метилбензамидин, ацетат, FAB 471;
4-[4-(7-метокси-2-нафтилсульфонил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 453;
4-[4-(3,5-диметоксифенилметил)пиперазин-1-карбонил] бензамидин, ацетат, FAB 383.
Пример 15
Аналогично примеру 6 получают следующие соединения:
4-{3-оксо-3-[4-(бутилсульфонил)пиперазин-1-ил]пропил}бензамидин, ацетат, FAB 381;
4-{3-оксо-3-[4-(4-пропилфенилсульфонил)пиперазин-1-ил]пропил}бензамидин, ацетат, FAB 443;
4-{ 3-оксо-3-[4-(6-хлор-2-нафтилсульфонил)пиперазин-1-ил]пропил}бензамидин, ацетат, FAB 485;
4-{3-оксо-3-[4-(2-нафтилсульфонил)пиперазин-1-ил]пропил}бензамидин, ацетат, FAB 451;
4-{ 3-оксо-3-[4-(3-хлор-4-метилфенилсульфонил)пиперазин-1-ил]пропил}бензамидин, ацетат, FAB 449;
4-{ 3-оксо-3-[4-(4-хлорфенилсульфонил)пиперазин-1-ил] пропил}бензамидин, ацетат, FAB 435;
4-{ 3-оксо-3-[4-(4-бифенилилсульфонил)пиперазин-1-ил] пропил}бензамидин, ацетат, FAB 477;
4-{ 3-оксо-3-[4-(2,4,6-триметилфенилсульфонил)пиперазин-1-ил]пропил}бензамидин, ацетат, FAB 443;
3-{3-оксо-3-[4-(бутилсульфонил)пиперазин-1-ил]пропил}бензамидин, ацетат, FAB 381;
3-{ 3-оксо-3-[4-(4-метоксифенилсульфонил)пиперазин-1-ил] пропил}бензамидин, ацетат, FAB 431;
3-[3-оксо-3-[4-(4-хлорфенилсульфонил)пиперазин-1-ил] пропил} бензамидин, ацетат, FAB 435;
3-[3-оксо-3-[4-(4-изопропилфенилсульфонил)пиперазин-1-ил]пропил}бензамидин, ацетат, FAB 443;
3-{ 3-оксо-3-[4-(2,4,6-триметилфенилсульфонил)пиперазин-1-ил]пропил}бензамидин, ацетат, FAB 443;
3-{ 3-оксо-3-[4-(3-хлор-4-метилфенилсульфонил)пиперазин-1-ил]пропил}бензамидин, ацетат, FAB 449;
3-[3-оксо-3-[4-(6-хлор-2-нафтилсульфонил)пиперазин-1-ил] пропил}бензамидин, ацетат, FAB 485;
3-[3-оксо-3-[4-(2-нафтилсульфонил)пиперазин-1-ил]пропил}бензамидин, ацетат, FAB 451;
3-{ 3-оксо-3-[4-(4-бифенилилсульфонил)пиперазин-1-ил] пропил}бензамидин, ацетат, FAB 477.
Пример 16
Аналогично примеру 13 взаимодействием 4-(5-метил[1,2,4]оксадиазол-3-ил)фенилизоцианата (соединение "Е")
с 1-(2-нафтилсульфонил)пиперазином получают N-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]амид 4-(2-нафтилсульфонилпиперазин-1-карбоновой кислоты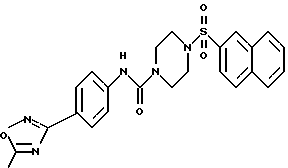 ;
;
с 1-(2-фенилвинилсульфонил)пиперазином получают N-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] амид 4-(2-фенилвинилсульфонил)пиперазин-1-карбоновой кислоты;
с 1-(4-пропилфенилсульфонил)пиперазином получают N-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] амид 4-(4-пропилфенилсульфонил)пиперазин-1-карбоновой кислоты;
с 1-(4-хлорфенилсульфонил)пиперазином получают N-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил] амид 4-(4-хлорфенилсульфонил)пиперазин-1-карбоновой кислоты;
с 1-(2,4,6-триметилфенилсульфонил)пиперазином получают N-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]амид 4-(2,4,6-триметилфенилсульфонил)пиперазин-1-карбоновой кислоты;
с 1-(6-хлор-2-нафтилсульфонил)пиперазином получают N-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил] амид 4-(6-хлор-2-нафтилсульфонил)пиперазин-1-карбоновой кислоты.
Гидрированием аналогично примеру 2 из представленных выше соединений получают следующие амидиновые производные:
N-(4-амидинофенил)амид 4-(2-нафтилсульфонил)пиперазин-1-карбоновой кислоты, ацетат, FAB 438;
N-(4-амидинофенил)амид 4-(2-фенилвинилсульфонил)пиперазин-1-карбоновой кислоты, ацетат, FAB 414;
N-(4-амидинофенил)амид 4-(4-пропилфенилсульфонил)пиперазин-1-карбоновой кислоты, ацетат, FAB 430;
N-(4-амидинофенил)амид 4-(4-хлорфенилсульфонил)пиперазин-1-карбоновой кислоты, ацетат, FAB 422;
N-(4-амидинофенил)амид 4-(2,4,6-триметилфенилсульфонил)пиперазин-1-карбоновой кислоты, ацетат, FAB 430;
N-(4-амидинофенил)амид 4-(6-хлор-2-нафтилсульфонил)пиперазин-1-карбоновой кислоты, ацетат, FAB 472.
Пример 17
Аналогично примеру 1 взаимодействием 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензил]пиперазина (соединение "Ж")
с 4-пропилфенилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензил]-4-(4-пропилфенилсульфонил)пиперазин;
с 4-метоксифенилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензил]-4-(4-метоксифенилсульфонил)пиперазин;
с 4-бифенилилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4] оксадиазол-3-ил)бензил]-4-(4-бифенилилсульфонил)пиперазин;
с 2-нафтилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензил]-4-(2-нафтилсульфонил)пиперазин;
с 6-хлор-2-нафтилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензил]-4-(6-хлор-2-нафтилсульфонил)пиперазин;
с 7-метокси-2-нафтилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензил]-4-(7-метокси-2-нафтилсульфонил)пиперазин;
с 3,5-диметоксибензилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензил]-4-(3,5-диметоксибензил)пиперазин;
с 4-изопропилфенилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензил]-4-(4-изопропилфенилсульфонил)пиперазин;
с хлорангидридом 4-бифенилилкарбоновой кислоты получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензил]-4-(4-бифенилилкарбонил)пиперазин;
с хлорангидридом 2-нафтилкарбоновой кислоты получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензил]-4-(2-нафтилкарбонил)пиперазин;
с 3,5-диметоксибензилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)бензил]-4-(3,5-диметоксибензил)пиперазин;
с 2-нафтилметилхлоридом получают 1-[4-(5-метил[1,2,4] оксадиазол-3-ил)бензил]-4-(2-нафтилметил)пиперазин.
Гидрированием аналогично примеру 2 из представленных выше соединений получают следующие амидиновые производные:
1-(4-амидинобензил)-4-(4-пропилфенилсульфонил)пиперазин, ацетат, FAB 401;
1-(4-амидинобензил)-4-(4-метоксифенилсульфонил)пиперазин, ацетат, FAB 389;
1-(4-амидинобензил)-4-(4-бифенилилсульфонил)пиперазин, ацетат, FAB 435;
1-(4-амидинобензил)-4-(2-нафтилсульфонил)пиперазин, ацетат, FAB 409;
1-(4-амидинобензил)-4-(6-хлор-2-нафтилсульфонил)пиперазин, ацетат, FAB 443;
1-(4-амидинобензил)-4-(7-метокси-2-нафтилсульфонил)пиперазин, ацетат, FAB 439;
1-(4-амидинобензил)-4-(3,5-диметоксибензил)пиперазин, ацетат, FAB 369;
1-(4-амидинобензил)-4-(4-изопропилфенилсульфонил)пиперазин, ацетат, FAB 441;
1-(4-амидинобензил)-4-(4-бифенилилкарбонил)пиперазин, диацетат, FAB 399;
1-(4-амидинобензил)-4-(2-нафтилкарбонил)пиперазин, диацетат, FAB 373;
1-(4-амидинобензил)-4-(2-нафтилметил)пиперазин, диацетат, FAB 359.
Пример 18
Взаимодействием 4-[4-(6-хлор-2-нафтилсульфонил)пиперазин-1-карбонил] -3-метилбензамидина с метиловым эфиром хлормуравьиной кислоты в дихлорметане после обычной переработки получают метиловый эфир (имино-{4-[4-(6-хлор-2-нафтилсульфонил)пиперазин-1-карбонил]фенил}метил)карбаминовой кислоты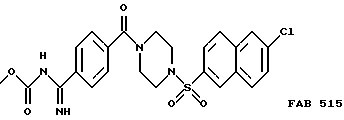
Пример 19
Аналогично примеру 1 взаимодействием 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]пиперазина (соединение "З")
с 4-пропилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]-4-(4-пропилфенилсульфонил)пиперазин;
с 4-бутилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]-4-(4-бутилсульфонил)пиперазин;
с 4-метоксифенилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]-4-(4-метоксифенилсульфонил)пиперазин;
с 4-хлорфенилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]-4-(4-хлорфенилсульфонил)пиперазин;
с 4-изопропилфенилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]-4-(4-изопропилфенилсульфонил)пиперазин;
с 4-бифенилилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4] оксадиазол-3-ил)фенил]-4-(4-бифенилилфенилсульфонил)пиперазин;
с 2,4,6-триметилфенилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]-4-(2,4,6-триметилфенилсульфонил)пиперазин;
с 3-хлор-4-метилфенилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]-4-(3-хлор-4-метилфенилсульфонил)пиперазин;
с 2-нафтилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]-4-(2-нафтилсульфонил)пиперазин;
с 6-хлор-2-нафтилсульфонилхлоридом получают 1-[4-(5-метил[1,2,4]оксадиазол-3-ил)фенил]-4-(6-хлор-2-нафтилсульфонил)пиперазин.
Путем гидрирования аналогично примеру 2 из представленных выше соединений получают следующие амидиновые производные:
1-(4-амидинофенил)-4-(4-пропилфенилсульфонил)пиперазин, ацетат, FAB 387;
1-(4-амидинофенил)-4-(4-бутилсульфонил)пиперазин, ацетат, FAB 325;
1-(4-амидинофенил)-4-(4-метоксифенилсульфонил)пиперазин, ацетат, FAB 375;
1-(4-амидинофенил)-4-(4-хлорфенилсульфонил)пиперазин, ацетат, FAB 379;
1-(4-амидинофенил)-4-(4-изопропилфенилсульфонил)пиперазин, ацетат, FAB 387;
1-(4-амидинофенил)-4-(4-бифенилилфенилсульфонил)пиперазин, ацетат, FAB 421;
1-(4-амидинофенил)-4-(2,4,6-триметилфенилсульфонил)пиперазин, ацетат, FAB 387;
1-(4-амидинофенил)-4-(3-хлор-4-метилфенилсульфонил)пиперазин, ацетат, FAB 393;
1-(4-амидинофенил)-4-(2-нафтилсульфонил)пиперазин, ацетат, FAB 395;
1-(4-амидинофенил)-4-(6-хлор-2-нафтилсульфонил)пиперазин, ацетат, FAB 429.
В нижеследующих примерах представлены фармацевтические композиции и технология их приготовления в соответствующих дозированных формах.
Пример А: Склянки для инъекционных растворов
Раствор из 100 г активного вещества формулы I и 5 г гидрофосфата динатрия в 3 л дважды дистиллированной воды с помощью 2н. соляной кислоты устанавливают на рН 6,5, стерильно фильтруют, заполняют склянки, лиофилизуют в стерильных условиях и стерильно укупоривают. В каждой склянке содержится 5 мг активного вещества.
Пример Б: Суппозитории
Вначале приготавливают смесь из 20 г активного вещества формулы I, 100 г соевого лецитина и 1400 г масла какао, затем расплавляют, разливают в формы и дают застыть. Каждый суппозиторий содержит 20 мг активного вещества.
Пример В: Раствор
Приготавливают раствор из 1 г активного вещества формулы I, 9,38 г NaH2PO4•2H2O, 28,48 г Na2HPO4•12H2O и 0,1 г хлорида бензалкония в 940 мл дважды дистиллированной воды. Затем устанавливают на рН 6,8, доводят до объема 1 л и стерилизуют облучением. Этот раствор может применяться в виде глазных капель.
Пример Г: Мазь
При соблюдении асептических условий приготавливают смесь из 500 мг активного вещества формулы I и 99,5 г вазелина.
Пример Д: Таблетки
Приготавливают смесь из 1 кг активного вещества формулы I, 4 кг лактозы, 1,2 кг картофельного крахмала, 0,2 кг талька и 0,1 кг стеарата магния, которую затем таблетируют по обычной технологии таким образом, что каждая таблетка содержит 10 мг активного вещества.
Пример Е: Драже
Аналогично примеру Д прессуют таблетки, которые затем по обычной технологии покрывают оболочкой из сахарозы, картофельного крахмала, талька, траганта и красителя.
Пример Ж: Капсулы
Из 2 кг активного вещества формулы I по обычной технологии изготавливают капсулы с твердожелатиновым покрытием таким образом, что каждая капсула содержит 20 мг активного вещества.
Пример З: Ампулы
Раствор из 1 кг активного вещества формулы I в 60 л дважды дистиллированной воды стерильно фильтруют, разливают в ампулы, в стерильных условиях лиофилизуют и стерильно укупоривают. В каждой ампуле содержится 10 мг активного вещества.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ БЕНЗАМИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 1998 |
|
RU2203897C2 |
| ПРОИЗВОДНЫЕ ОКСАЗОЛИДИНОНКАРБОНОВОЙ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2156765C2 |
| ПРОИЗВОДНЫЕ ОКСАЗОЛИДИН-2-ОНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1996 |
|
RU2163602C2 |
| ПРОИЗВОДНЫЕ ЦИКЛОПЕПТИДОВ | 1997 |
|
RU2202557C2 |
| БИЦИКЛИЧЕСКИЕ АРОМАТИЧЕСКИЕ АМИНОКИСЛОТЫ | 1998 |
|
RU2187506C2 |
| ПРОИЗВОДНЫЕ ЦИКЛОПЕПТИДОВ В КАЧЕСТВЕ ИНГИБИТОРОВ АДГЕЗИИ | 1998 |
|
RU2200166C2 |
| ПРОИЗВОДНЫЕ ХРОМЕНОНА И ХРОМАНОНА В КАЧЕСТВЕ ИНГИБИТОРОВ ИНТЕГРИНОВ | 1999 |
|
RU2234505C2 |
| ОКСАЗОЛИДИНОНЫ, ИХ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1994 |
|
RU2145961C1 |
| ПРОИЗВОДНЫЕ ИНДОЛ-3-ИЛА | 2001 |
|
RU2257380C2 |
| ПИПЕРАЗИНОВЫЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩАЯ ИХ КОМПОЗИЦИЯ | 1999 |
|
RU2208610C2 |
Описываются производные бензамидина общей формулы I, где R1 обозначает -С(= NH)-NH2, который может быть однократно замещен группой -СОА или -СООА, R2 обозначает Н или А, R3 обозначает А, циклоалкил, -[С(R6)2]nAr, [С(R6)2] n-О-Ar, -[С(R6)2] n Het или -С(R6)2-Ar, R6 обозначает Н, Х отсутствует или обозначает -СО-, -С(R6)2-, -С(R6)2 -С(R6)2-, -С(R6)2-СО-, -С(R6)2 -С(R6)2-СО- или NR6СО-, Y обозначает -С(R6)2-, -SO2-, -СО-, -СОО- или -СОNR6-, А обозначает алкил с 1-20 С-атомами, где одна либо две СН2-группы могут быть заменены на О- или S-атомы либо на CR6=CR6-группы и/или 1-7 Н-атомов могут быть заменены на F, Ar обозначает незамещенный либо одно-, дву- или трехкратно замещенный группой А, фенилом, OR6, N(R6)2, Hal, NHCOA или COOR6 фенил или нафтил, Het обозначает 2-тиенил, 1,2,3,4-тетрагидрохинолин-8-ил, 2,2,5,7,8-пентаметилхроман-6-ил, камфор-10-ил, 5-(1-метил-5-трифторметил-3-пиразолил)-2-тиенил, 5-бензамидометил-2-тиенил, 1,3-диметил-5-хлор-4-пиразолил, 3,5-диметил-4-изоксазолил, 3-метокси-4-метоксикарбонил-2-тиенил, пиридил, бензо-[b]тиофен-2-ил, 1,3-бензодиоксол-5-ил, дибензофуран-2-ил, Hal обозначает F, Cl, Br или J, n означает 0, 1 или 2, способ их получения и фармацевтическая композиция. Описываемые соединения являются ингибиторами коагуляционного фактора Ха и могут применяться для профилактики и терапии тромбоэмболических заболеваний. 3 с. и 2 з.п. ф-лы.
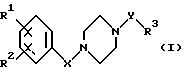
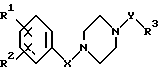
в которой R1 обозначает -C(= NH)-NH2, который может быть однократно замещен группой -СОА, -COOA;
R2 обозначает Н или A;
R3 обозначает А, циклоалкил, -[C(R6)2] nAr, -[C(R6)2] n-O-Ar, -[C(R6)2] nHet или -C(R6)2= C(R6)2-Ar;
R6 обозначает Н;
X отсутствует или обозначает -СО-, -C(R6)2-, -C(R6)2-C(R6)2-, -C(R6)2-CO-, -C(R6)2-C(R6)2-CO-, или NR6CO-;
Y обозначает -C(R6)2-, -SO2-, -СО-, -СОО- или -CONR6-;
А обозначает алкил с 1-20 С-атомами, где одна либо две СН2-группы могут быть заменены на О- или S-атомы либо на -CR6= CR6-группы и/или 1-7 Н-атомов могут быть заменены на F;
Аr обозначает незамещенный либо одно-, дву- или трехкратно замещенный группой А, фенилом, OR6, N(R6)2, Hal, NHCOA или COOR6 фенил или нафтил;
Het обозначает 2-тиенил, 1,2,3,4-тетрагидрохинолин-8-ил, 2,2,5,7,8-пентаметилхроман-6-ил, камфор-10-ил, 5-(1-метил-5-трифторметил-3-пиразолил)-2-тиенил, 5-бензамидометил-2-тиенил, 1,3-диметил-5-хлор-4-пиразолил, 3,5-диметил-4-изоксазолил, 3-метокси-4-метоксикарбонил-2-тиенил, пиридил, бензо-[b] тиофен-2-ил, 1,3-бензодиоксол-5-ил, дибензофуран-2-ил;
Hal обозначает F, C1, Вr или J;
n обозначает 0, 1 или 2,
а также их соли.
а) 4-[4-(4-пропилфенилсульфонил)-1-пиперазинилкарбонил] бензамидин,
б) 4-[4-(3-амино-4-хлорфенилсульфонил)-1-пиперазинилкарбонил] -бензамидин,
в) 4-[4-(6-хлорнафталин-2-сульфонил)-1-пиперазинилкарбонил] бензамидин,
г) 4-[4-(2-фенилвинилсульфонил)-1-пиперазинилкарбонил] бензамидин,
и их соли.
| Способ регенерации аммиака из хлористого аммония | 1975 |
|
SU608759A1 |
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
| Пружинный стартер | 1975 |
|
SU540051A1 |
| ПРОСТЫЕ ЭФИРЫ (ТИО)МОРФОЛИНИЛ- ИЛИ ПИПЕРАЗИНИЛ АЛКИЛФЕНОЛОВ, ИЛИ ИХ СТЕРЕОИЗОМЕРЫ, ИЛИ ИХ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ И АНТИВИРУСНАЯ КОМПОЗИЦИЯ | 1990 |
|
RU2057130C1 |
Авторы
Даты
2002-12-10—Публикация
1998-09-16—Подача