Изобретение относится к области медицины и может быть использовано в гинекологии, гистологии.
Рост заболеваемости раком тела матки в последние годы диктует необходимость более углубленного изучения патологических состояний слизистой тела матки с целью раннего выявления предопухолевых процессов и выявления групп высокого риска по раку эндометрия среди больных с гиперпластическими процессами [1, 4, 8].
Ведущая роль в распознавании патологического процесса в эндометрии принадлежит морфологическому исследованию, однако в настоящее время дополнительные данные об особенностях роста тканей являются отправной точкой при выборе метода лечения и прогноза [6].
Гиперпластические процессы эндометрия представляют собой пролиферативные изменения [9]. Процессы тканевого гомеостаза и гиперплазии регулируются факторами роста, отвечающими за жизнеспособность клеток, и апоптозом, контролирующим размеры ткани [5].
Смерть биологической клетки как естественный, запрограммированный природой процесс, не связанный с патологией, впервые был описан почти полвека назад, а термин "апоптоз" предложил Kerr и соавторы [11]. Принято считать, что основное предназначение апоптоза как физиологического процесса - поддержание постоянного количества клеточных элементов в органах и тканях организма и удаление клеток, прошедших свой жизненный цикл. Исследования последних лет позволяют сделать вывод о существовании двух фундаментальных типов клеточной смерти - апоптоза и некроза. В отличие от некроза процессы апоптоза происходят в ядре и цитоплазме при сохранении целостности клеточной оболочки [3, 7].
Большинство касающихся апоптоза исследований посвящено злокачественным неопластическим процессам эндометрия. Работы по изучению апоптоза при фоновых процессах эндометрия в доступной нам литературе не найдены.
Задачей изобретения является выявление цитоморфологических факторов риска развития рака эндометрия.
Поставленную задачу решают за счет того, что вычисляют количество апоптозных и некротических клеток, правильных и патологических митозов в процентах по отношению к общему числу эпителиальных клеток при фоновых процессах эндометрия, высчитывают метофазно-профазное соотношение в каждом индивидуальном случае, количество клеток с апоптозом и патологическими митозами, равное 0,6%, и метофазно-профазное соотношение большее 0,48 считают цитоморфологическими критериями высокого риска развития рака эндометрия.
Способ осуществляют следующим образом: материалом для исследования служит слизистая оболочка матки, полученная при раздельном диагностическом выскабливании. Гистологические срезы окрашивают гематоксилин-эозином для определения соединительной ткани - по Ван-Гизону. Исследование проводят на световом микроскопе при самом малом и большом увеличении (40 и 300 соответственно). Диагноз гиперпластических процессов эндометрия ставят на основании общепринятых критериев [10] . Под иммерсионным объективом при увеличении х1350 в фиксированных препаратах, нескольких срезах и полях зрения на общее число эпителиальных клеток не менее чем 2000 проводят подсчет: апоптозных клеток, некротических клеток, клеток с патологическими митозами, определяют все формы митоза при фоновых процессах эндометрия.
Объект исследования: изучены соскобы эндометрия 102 больных с нарушением менструальной функции в репродуктивном возрасте, у которых диагностированы полипы и гиперплазия эндометрия, составившие основную группу. В зависимости от гистологического диагноза все обследованные были разделены на 3 группы. В 1 группе были объединены женщины с полипами эндометрия - 70 человек. Эта группа больных в зависимости от гистоструктуры последних была разделена на две подгруппы: 1a - с железистыми полипами - 34 женщины; 1в - с железисто-фиброзными полипами - 36 женщин. 32 пациентки с железисто-кистозной гиперплазией составили вторую группу. Группу сравнения составили 50 женщин без патологии эндометрия. В контрольной группе ткань эндометрия для гистологического изучения была получена у 30 в I фазу менструального цикла и у 20 во II фазу.
Средний возраст больных с железистыми полипами составил 32,1±1,4 года; с железисто-фиброзными полипами - 33,5±1,5; железисто-кистозной гиперплазией - 34,7±1,3; средний возраст здоровых женщин был 29,3±1,09.
Среди 102 обследованных больных длительность заболевания в течение 1 месяца отмечена у 66; до 6 месяцев - у 11; от года и более - 22 и лишь трое обратились с жалобами к гинекологу впервые. Лечебно-диагностические выскабливания эндометрия ранее производились 12 больным от 1 до 3 раз.
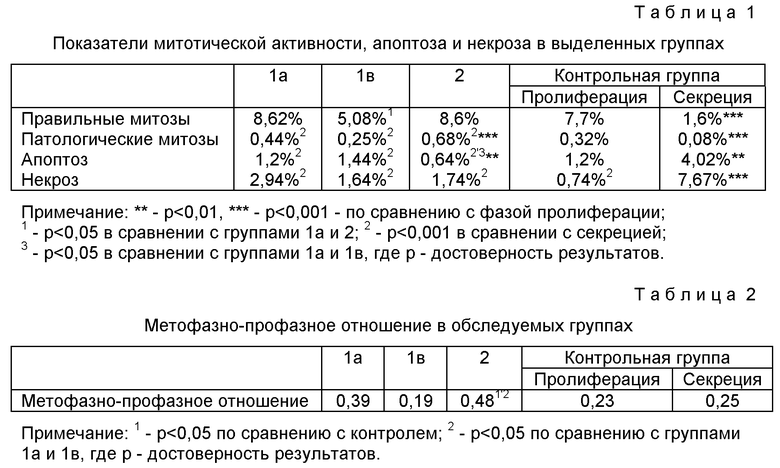
В результате проведенного исследования (табл. 1) установлено, что в фазе пролиферации эндометрия отмечается высокая митотическая активность в железистом эпителии, равная 7,7%, которая в фазе секреции достоверно (р<0,001) снижается до 1,6%. Это не удивительно, поскольку общеизвестно, что в фазе пролиферации эндометрия женщин наблюдается усиленное размножение клеток, сменяющееся в фазе секреции их дифференцировкой и затем отторжением. При железисто-кистозной гиперплазии эндометрия в эпителии желез количество правильных митозов колебалось от 2,0% до 18,4% и в среднем составило 8,6%. При железистых полипах эндометрия и железисто-кистозной гиперплазии количество митозов было одинаковым 8,62% и 8,6%, что свидетельствует, по-видимому, о сходных изменениях уровня пролиферации клеток при этих патологических состояниях. При железисто-фиброзных полипах выявлено достоверное (р<0,05) снижение митотической активности по сравнению с группами 1а и 2, что объясняется меньшим количеством желез и преобладанием стромального компонента в структуре полипа.
В контрольной группе женщин выявлено небольшое количество патологических митозов в эндометрии в стадии пролиферации (0,32%) и имеется достоверная (р<0,001) тенденция к их уменьшению (0,08%) в фазе секреции менструального цикла. При железисто-кистозной гиперплазии эндометрия процент патологических митозов колебался от 0,2% до 2,04% (в среднем составил 0,68%) и значительно превышал таковой в фазу пролиферации. Отмечается незначительное увеличение числа патологических митозов, в сравнении с контрольной группой, при железистых полипах эндометрия - до 0,44% и снижение при железисто-фиброзных - до 0,25% (соответственно группам 1в и 1а). Значения в этом случае достоверно были незначимы. Умеренное повышение числа патологических митозов в железистом эпителии слизистой тела матки связано с действием эстрогенов, активно влияющих на процессы клеточного размножения [2].
Очень важными в дифференциально-диагноситческом плане являются изменения метофазно-профазного отношения в ядрах железистого эпителия неизмененной слизистой тела матки и при гиперпластических процессах разной степени выраженности. В неизмененном эндометрии этот показатель в нашем исследовании равнялся 0,23-0,25, при железисто-кистозной гиперплазии эндометрия отмечается его увеличение в 2 раза (0,48). В случаях развития полипов эндометрия в зависимости от их гистоструктуры метофазно-профазное отношение равнялось 0,19 в группе 1в и 0,39 в группе 1а.
Процентное содержание клеток в состоянии апоптоза в фазе пролиферации согласно полученных нами результатов было равно 1,2%, некроза - 0,74%; в фазе секреции - 4,02% и 7,67% соответственно (р<0,01) и (р<0,001). В железисто-фиброзных полипах количество апоптозных клеток составило 1,44%, в железистых полипах - 1,2%; количество клеток, подвергшихся некрозу, - 1,64% и 2,94% соответственно. Апоптозные тела во 2-й группе выявлены в 0,64%, что достоверно отличалось от аналогичного показателя во всех остальных группах (р<0,01 с контролем), (р<0,05 по сравнению с группами 1а и 1в). Увеличение нормальной (апоптозной) гибели клеток в фазу секреторных изменений эндометрия логично связать с дифференцировкой, а усиление некроза с нарушением трофики и отторжением эндометрия в конце этой фазы. Снижение апоптозного индекса при железисто-кистозной гиперплазии может отражать атипичные изменения в клетках эпителия желез эндометрия. В нашем исследовании наблюдалась обратная корреляционная зависимость между апоптозным индексом и митотической активностью, количеством патологических митозов.
Таким образом, в результате проведенного исследования нами установлено, что:
1) высокий митотический индекс, характерный как для неизмененного эндометрия в фазе пролиферации, так и для железистых полипов и железисто-кистозной гиперплазии не позволяет судить о степени патологической пролиферации клеток;
2) фоновые процессы эндометрия развиваются на фоне не усиления пролиферации клеток, а ингибировании их запрограммированной гибели, то есть апоптоза;
3) при преобладании железистого компонента (в железистых полипах и железисто-кистозной гиперплазии) происходит задержка деления ядра на стадии метофазы. Поскольку задержка деления ядра на стадии метофазы является одним из ранних признаков нарушения митотического деления клеток, то увеличение метофазно-профазного отношения может быть одним из критериев ранних признаков озлокачествления эпителия;
4) дифференциально-диагностическую ценность приобретает показатель - число патологических митозов (рассеивание, набухание и склеивание хромосом в метафазе);
5) апоптоз является более выгодным для ткани механизмом поддержания структурно-функционального гомеостаза. Усиление некротических изменений может индуцировать вторичные повреждения в ткани эндометрия.
Отсюда следует, что при гиперпластических процессах эндометрия качественные изменения митотического режима (число патологических митозов, увеличение метофазно-профазного соотношения), апоптоза имеют дифференциально-диагностическую ценность, могут служить критериями оценки степени пролиферации клеток и могут быть использованы для дополнительной характеристики степени тяжести процесса, а также для выявления лиц высокого онкологического риска.
Источники информации:
1. Бохман Я.В., Вишневский А.С., Волкова А.Г. Профилактика, ранняя диагностика и комплексное лечение рака тела матки./ Л. 1981. - С. 6-7.
2. Казанцева И.А. // Архив патологии. - 1980. - 2. - С. 77-82.
3. Лушников Е. Ф. , Абросимов А.Ю. Сравнительная морфология апоптоза и некроза клеток опухолей. / Тезисы 1 Белорусского съезда патологоанатомов и судебных медиков// Минск, 1990-1991.- 2.- С. 299-300.
4. Мерабишвили В.М., Бохман Я.В. Профилактика, ранняя диагностика и комплексное лечение рака тела макти./ Л. 1981. - С. 3-5.
5. Новожилова А.П., Плужников Н.Н., Новиков В.С. Программированная клеточная гибель / СПб: Наука, 1996.- 276 с.
6. Особенности митотического режима при гиперплазиях и раке эндометрия./ Полищук Л.3., Бучинская Л.Г., Винниченко В.Н., Миляновский А.И.// Акушерство и гинекология. - 1984. 11.- С. 26-28.
7. Робинсон М.В., Труфакин В.А. Апоптоз клеток иммунной системы // Успехи современной биологии.-1991.- Т. 111, 2.- С. 246-259.
8. Савельева Г.М. Профилактика, ранняя диагностика и комплексное лечение рака тела матки./ Л. 1981. - С. 18.
9. Савельева Г. М. Предрак эндометрия. / М.- 1980. - 200 с.
10. Хмельницкий O. K. Патоморфологическая диагностика гинекологических заболеваниий./СПб, СОТИС. 1994. - 180 с.
11. Kerr Y. F.R., Wyllie A.R. Apoptosis: a basic biological phenomenon with wide ranging implications in tissue kinetics. Br. J. Cancer. 1972, 26: 2: 239-257.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ ДОБРОКАЧЕСТВЕННЫХ ГИПЕРПЛАСТИЧЕСКИХ ПРОЦЕССОВ ЭНДОМЕТРИЯ | 2000 |
|
RU2190221C2 |
| СПОСОБ УЛЬТРАЗВУКОВОЙ ДИАГНОСТИКИ ГИПЕРПЛАСТИЧЕСКИХ ПРОЦЕССОВ ЭНДОМЕТРИЯ | 2004 |
|
RU2267993C1 |
| Способ диагностики эндометриоза матки | 1989 |
|
SU1751674A1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА ФОРМИРОВАНИЯ ГИПЕРПЛАСТИЧЕСКИХ ПРОЦЕССОВ ЭНДОМЕТРИЯ | 2014 |
|
RU2557977C1 |
| СПОСОБ ЛЕЧЕНИЯ ГИПЕРПЛАСТИЧЕСКИХ ПРОЦЕССОВ ЭНДОМЕТРИЯ | 2001 |
|
RU2214823C2 |
| СПОСОБ И СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ДОБРОКАЧЕСТВЕННЫХ ГИПЕРПЛАСТИЧЕСКИХ ПРОЦЕССОВ ЭНДОМЕТРИЯ | 2004 |
|
RU2275194C1 |
| СПОСОБ ДИАГНОСТИКИ ГИПЕРПЛАСТИЧЕСКИХ ПРОЦЕССОВ И РАКА ЭНДОМЕТРИЯ | 1995 |
|
RU2127429C1 |
| СПОСОБ ДИАГНОСТИКИ ТЕКОМАТОЗА ЯИЧНИКОВ В ПЕРИОД МЕНОПАУЗЫ | 2010 |
|
RU2438581C1 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ НИЗКОДИФФЕРЕНЦИРОВАННОЙ АДЕНОКАРЦИНОМЫ ЭНДОМЕТРИЯ | 2004 |
|
RU2268472C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ С ВНУТРЕННИМ ЭНДОМЕТРИОЗОМ (АДЕНОМИОЗОМ) | 2003 |
|
RU2243009C1 |
Изобретение относится к медицине, а именно к гинекологии. Способ заключается в следующем: готовят фиксированные препараты соскобов эндометрия, определяют в них количество клеток с апоптозом и патологическими митозами в процентах по отношению к общему числу клеток железистого эпителия, вычисляют метофазно-профазное отношение в ядрах железистого эпителия, при количестве клеток с апоптозом, равном 0,64%, количестве патологических митозов 0,68% и метофазно-профазном соотношении 0,48 и более диагностируют железисто-кистозную гиперплазию. Способ позволяет повысить точность диагностики и выявить лиц высокого онкологического риска. 2 табл.
Способ диагностики железисто-кистозной гиперплазии, заключающийся в том, что готовят фиксированные препараты соскобов эндометрия, определяют в них количество клеток с апоптозом и патологическими митозами в процентах по отношению к общему числу клеток железистого эпителия, вычисляют метофазно-профазное отношение в ядрах железистого эпителия, при количестве клеток с апоптозом, равном 0,64%, количестве патологических митозов 0,68% и метофазно-профазном соотношении 0,48 и более диагностируют железисто-кистозную гиперплазию.
| ПОЛИЩУК Л.З | |||
| и др | |||
| Особенности митотического режима при гиперплазиях и раке эндометрия | |||
| Колосниковая решетка с чередующимися неподвижными и движущимися возвратно-поступательно колосниками | 1917 |
|
SU1984A1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ГИПЕРПЛАСТИЧЕСКИХ ЗАБОЛЕВАНИЙ И РАКА ЭНДОМЕТРИЯ | 1993 |
|
RU2054183C1 |
| СПОСОБ ДИАГНОСТИКИ ГИПЕРПЛАСТИЧЕСКИХ ПРОЦЕССОВ И РАКА ЭНДОМЕТРИЯ | 1995 |
|
RU2127429C1 |
| Способ диагностики эндометриоза матки | 1989 |
|
SU1751674A1 |
| ТУРУСБЕКОВА Г.Б | |||
| Диагностика, мониторинг и прогноз рака эндометрия | |||
| Автореф | |||
| на соиск | |||
| уч | |||
| ст | |||
| канд | |||
| мед | |||
| н | |||
| - Бишкек, 1993 | |||
| АШРАФЯН Л.А | |||
| Стандартизованная диагностика рака эндометрия | |||
| Автореф | |||
| на соиск | |||
| уч | |||
| ст | |||
| докт | |||
| мед | |||
| н | |||
| - М., 1989 | |||
| MORA L.B | |||
| et al | |||
| Differential diagnosis of endometrial hyperplasia and carcinoma by computerized image cytometry of cell proliferation, apoptosis and Bcl-2 expression | |||
| Ann | |||
| Clin | |||
| Lab | |||
| Sci | |||
| Металлический водоудерживающий щит висячей системы | 1922 |
|
SU1999A1 |
Авторы
Даты
2003-02-27—Публикация
2000-04-10—Подача