Настоящее изобретение относится к новому применению L-карнитина, его производных и фармакологически пригодных солей в сочетании с антиретровирусными лекарственными препаратами для лечения ВИЧ-инфекции и СПИДа. Более подробно, настоящее изобретение относится к применению L-карнитина, ацил-L-карнитинов, где ацильная группа, линейная или разветвленная, имеет 2-6 атомов углерода, и их фармакологически приемлемых солей в сочетании с нуклеозидоподобными ингибиторами обратной транскриптазы, не нуклеозидными ингибиторами обратной транскриптазы и ингибиторами ВИЧ-протеазы для снижения содержания церамидов и повышения активности указанных антиретровирусных лекарственных препаратов у ВИЧ-инфицированных пациентов.
Большинство патогенных механизмов, которые вносят вклад в прогрессирование инфекции, вызванной вирусом иммунодефицита человека 1 и 2 (ВИЧ-1, ВИЧ-2), прямо или косвенно касаются состояния общей активации иммунной системы.
Хроническая активация иммунной системы активирует вирусную репликацию через секрецию ряда цитокинов, благоприятствующих экспрессии ВИЧ, и путем сохранения резерва активированных иммунных клеток, которые действуют как мишени для ВИЧ и способствуют его репликации.
Кроме того, состояние устойчивой активации иммунной системы индуцирует патологии такой природы (например, повышенный апоптоз), которые ведут к ослаблению иммунных реакций.
Таким образом, имеем порочный круг: прогрессивная утрата нормального функционирования иммунной системы --> вирусное дессиминированное пониженное удаление вируса --> хроническая активация иммунной системы. Данный процесс может длиться годы до тех пор, пока не происходит указанное истощение иммунной системы, что ведет к неконтролируемой вирусной репликации и атаке условно-патогенных инфекций или к развитию синдрома приобретенного иммунодефицита (СПИД).
На основании описанных выше патогенных механизмов становится ясно, что нужно иметь в виду любое анти-ВИЧ лечение, снижающее вирусную репликацию и блокирующее истощение иммунной системы.
Что касается антиретровирусной терапии, к сожалению, ВИЧ характеризуется высокой степенью генетической изменчивости, происходящей, главным образом, при очень существенном недостатке обратной транскриптазы. Ретровирусный фермент лишает ферментативные системы контроля возможных ошибок транскрипции. Результатом является появление вариантов вируса - сверх диапазона, который является функцией вирусной репликации - которые отвечают за прогрессивное отклонение иммунной системы и сопротивляемости антиретровирусным лекарствам. В случае зидовудина (zidovudine - AZT,ZDV) потеря клинической эффективности в ситуациях монотерапии является широко признанным фактом. Даже открытые в последнее время антиретровирусные агенты, например зальцитабин [ddc], диданозин [ddI] и ламивудин [ЗТС] страдают от такого недостатка.
Недавно было продемонстрировано, что церамид стимулирует ВИЧ-экспрессию. Более того, церамид является одним из факторов, способных индуцировать клеточный апоптоз, явление, которое усиливается у людей с ВИЧ-инфекцией и которое вносит вклад в снижение количества TCD4 и TCD8 лимфоцитов. Таким образом, ясно, что изменения концентрации или метаболизма церамида могут влиять на вирусную нагрузку и клеточный апоптоз у ВИЧ-инфицированных пациентов (Рарр В. и др., AIDS, Res. Hum. Retrovirus, 10(7), 775-80).
К удивлению, обнаружено, что L-карнитин, его производные, а именно ацил-L-карнитины, в которых ацильная группа, линейная или разветвленная, имеет 2-6 атомов углерода, и их фармакологически пригодные соли ингибируют синтез церамида, по крайней мере, на 25%, а когда их используют в сочетании с антиретровирусными лекарственными препаратами, такими как, например, AZT, ставудин [4dT], фтортимидин [FLT], азидоридин [Azdu], фосфонированные ациклические нуклеозиды [РМЕА], ВИЧ-1 специфические нуклеозиды ([TSAO], зальцитабин [ddC] , диданозин [ddI] и ламивудин [3ТС], дипиридодиазепиноны, тетрагидроимидазобензодиазепиноны, пиридоны или L лекарственные препараты, бис-гетероарилпиперазины, производные альфа-анилинофенилацетамида, производные хиноксалина, Ro-31-8959, U-81749, KNI-227, SC-52151, HOE/BAY 793 и подобные, повышают антиретровирусную активность и защиту иммунной системы, на которую оказывают влияние эти лекарственные препараты.
Фармацевтически приемлемые соли L-карнитина или ацил-L-карнитина включают в дополнение к внутренним солям любые соли этих веществ с кислотами, которые не вызывают нежелательных токсических или побочных эффектов. Такие кислоты хорошо известны специалистам-фармакологам и экспертам по фармацевтической технологии.
Неограничивающие примеры подходящих солей включают хлорид; бромид; иодид; аспартат, в частности кислый аспартат; цитрат, в частности кислый цитрат; тартрат; фосфат, в частности кислый фосфат; фумарат, в частности кислый фумарат; глицерофосфат; фосфат глюкозы; лактат; малеат, в частности кислый малеат; оротат; оксалат, в частности кислый оксалат; сульфат, в частности кислый сульфат; трихлорацетат; трифторацетат и метансульфонат.
Особо предпочтительны L-карнитин, ацетил, пропионил, бутирил, валерил и изовалерил-L-карнитин.
Совместное введение L-карнитина и его производных, как определено выше, вместе с антиретровирусным агентом обычно осуществляют оральным или парентеральным способом при дневной дозе от 1 до 500 мг/кг, особо предпочтительны дозы от 20 до 100 мг/кг, при соотношении L-карнитина и его определенных выше производных и антиретровирусного агента в диапазоне от 1:40 до 40:1, особо предпочтительно соотношение от 1:10 до 10:1.
Обычно вводят препарат в виде стандартной дозированной формы, включающей оба активных ингредиента, которая может также включать наполнители и дополнительные активные ингредиенты, хорошо известные специалистам, такие как, например, декстран, TNF-альфа ингибиторы (например, пентоксифиллин), глутатион и другие антиоксидантные лекарственные препараты (например, ацетилцистеин, иммуномодуляторные лекарственные препараты, иммунодепрессивные или химиотерапевтические агенты, витамины и олигоэлементы.
Наконец, необходимо отметить, что, судя по всему, другие основные аминокислоты, в частности лизин, ацильные производные основных аминокислот и их фармацевтически приемлемые соли способны снижать содержание церамидов и повышать активность антиретровирусных лекарственных препаратов для терапии ВИЧ-инфекции и СПИДа.
Целью приведенных ниже примеров является иллюстрация данного изобретения, их нельзя истолковывать как ограничивающие каким-либо образом диапазон возможностей.
Пример 1
Оценивали эффект от введения сочетания L-карнитина (8 г в день через рот в течение 4 недель) плюс AZT (600 мг в день через рот) 13 пациентам, страдающим от СПИДа, с нормальными сывороточными и внутриклеточными уровнями карнитина и ацетилкарнитина, которых до этого лечили AZT (600 мг в день через рот) в течение, по крайней мере, 6 месяцев.
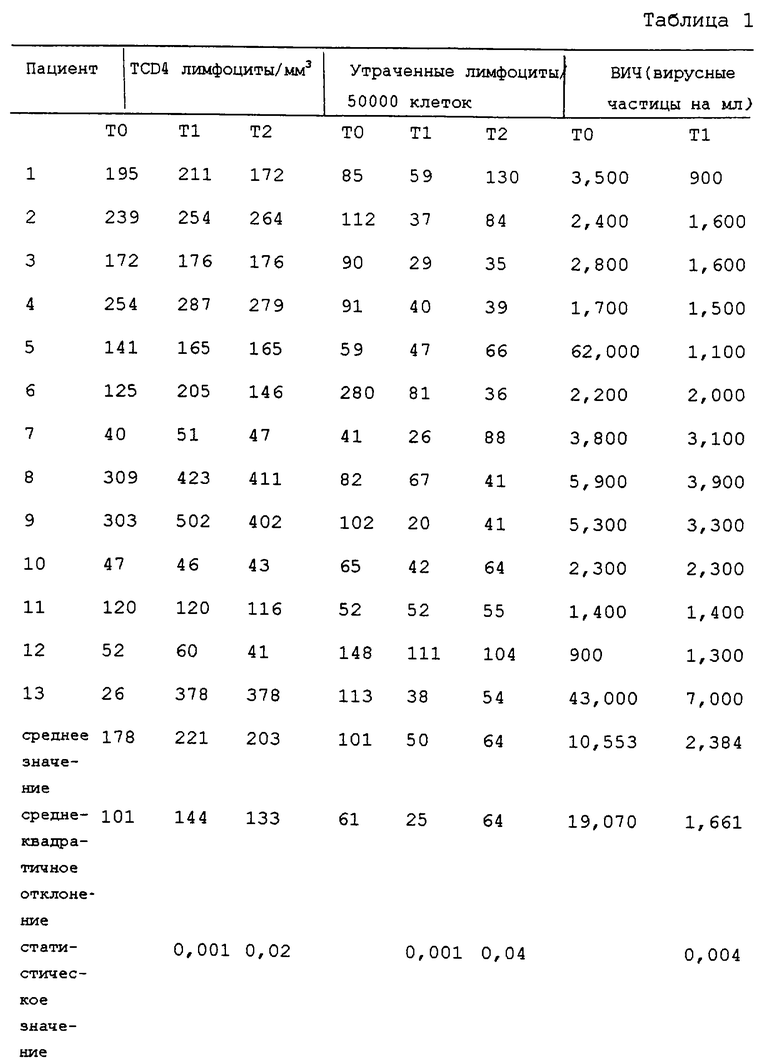
Определения проводили до лечения сочетанием, когда пациенты принимали только AZT (ТО), через 4 недели терапии сочетанием L-карнитин-АZТ (Т1) и один месяц спустя после прекращения лечения L-карнитином (Т2), оставляя пациентам только AZT терапию. Измеряли TCD4 лимфоциты путем проточной цитометрии при помощи специфических моноклональных антител (количество лимфоцитов на мм3) и утраченные лимфоциты методом проточной цитометрии после окрашивания пропидиумиодидом, количественного определения клеток с гиподиплоидными ядрами (количество лимфоцитов на 50000 клеток). Вирусную нагрузку (количество вирусных частиц на мл сыворотки) определяли путем количественного определения HVI-1 РНК при помощи полимеразной цепной реакции (система детектирования Роше: Amplicor HIV detection system by Roche). Для статистической обработки использовали тест Wilcoxon.
Результаты приведены в табл. 1.
У одних и тех же пациентов уровни лимфоцит-церамида, измеренные посредством исследования DAG(диацилглицерин)киназы (Cifone M.G. и др., J. Exp. Med. , 180(4), 1547-52), снизившиеся с 48±8 пикомолей/106 лимфоцитов [измерено до лечения комбинацией (ТО)] до 27±5 пикомолей/106 лимфоцитов (Т1) (Р<0,01), снова возрастает до 38±9 пикомолей/106 лимфоцитов через месяц после прекращения введения L-карнитина (Т2).
Эти результаты ясно показывают, что лечение только AZT, даже продолжающееся более 6 месяцев (ТО), не может дать таких иммунологических и вирусологических улучшений, которых можно достичь, принимая сочетания L-карнитин-АЕТ в течение лишь 4 недель (Т1). Эти улучшения имеют тенденцию снижаться после прекращения лечения (Т2).
Пример 2
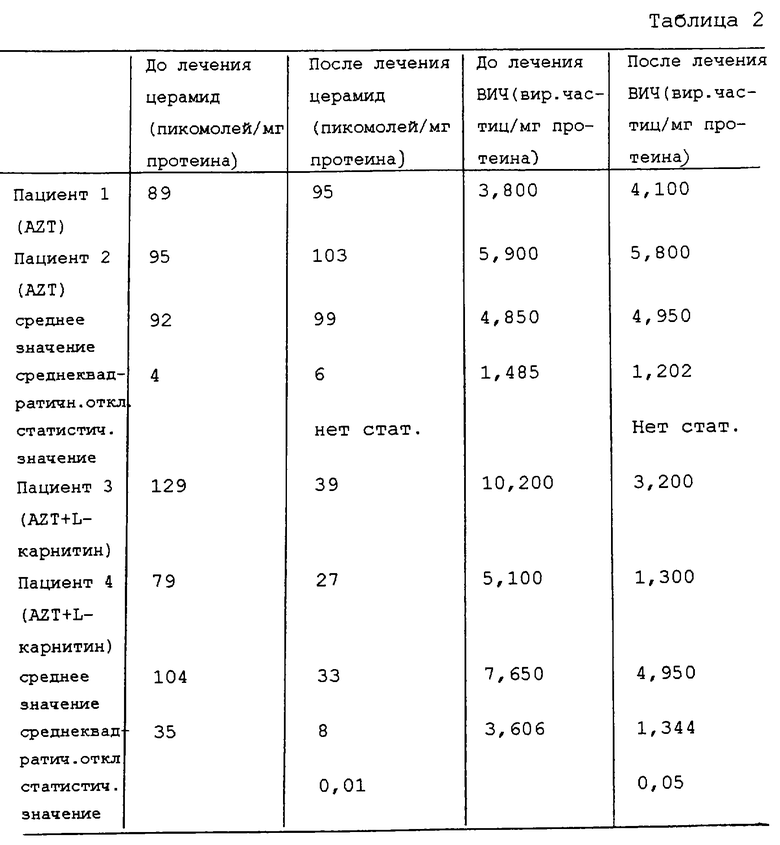
Четверых пациентов со СПИДом лечили, давая по 600 мг AZT ежедневно через рот. Двое из них принимали также L-карнитин по 3 г в день. Общая продолжительность лечения составляла 6 месяцев. До и после лечения проводили биопсии мышц. Содержание церамида в клетках мышц определяли до и после лечения после разрушения клеток ультразвуком и гомогенизации материала биопсии. Вирусную нагрузку определяли в тех же гомогенатах, как описано в примере 1.
Результаты представлены в табл. 2.
Ясно, что лечение сочетанием L-карнитин-AZT заметно более эффективно в снижении вирусной нагрузки и содержания церамида, также содержания в мышцах, по сравнению с лечением одним только AZT.
Пример 3
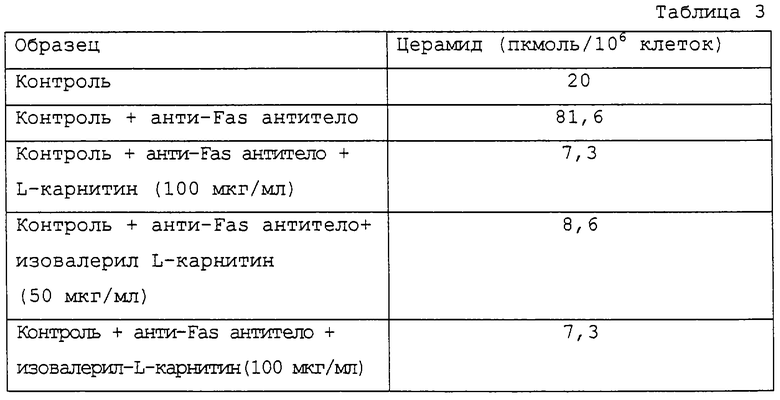
Лимфоциты периферической крови субъекта, пораженного СПИДом, выделяют в соответствии с классическими методиками. Клетки в течение 30 мин инкубируют с L-карнитином или изовалерил-L-карнитином при 37oС и после этого еще в течение 30 мин с моноклональным анти-Fas антителом. Затем клетки центрифугируют, убирают надосадочную жидкость и клеточный осадок делипидируют. Проводят количественный анализ органической фазы (содержащей церамид) в наборе для анализа DAG-киназы для определения содержания фосфорилирующего церамида, которое в последующем подтверждается с помощью авторадиографии.
Результаты представлены в табл. 3.
Известно, что соответствующим образом стимулированные клетки (т.е. Fas-L, интерлейукином-1- и т.д.) генерируют церамид. Для увеличения выработки церамида с базальной величины 20 пкмоль на 106 клеток до 81,6 пкмоль на 106 клеток было использовано анти-Fas антитело.
Пример 4
С соблюдением протокола примера 3, но с использованием клеток U937 (линия опухолевых клеток моноцитарного лейкоза человека), были получены результаты, представленные в табл. 4.
Для увеличения выработки церамида с базальной величины 56,51 пкмоль на 106 клеток до 70,67 пкмоль на 106 клеток было использовано анти-Fas антитело.

Предложено: фармацевтические композиции для снижения содержания церамидов на основе L-карнитина или ацил-Е-карнитина, или L-карнитина или ацил-L-карнитина и нуклеозидоподобного ингибитора обратной транскриптазы, не нуклеозидоподобного ингибитора обратной транскриптазы или ингибитора ВИЧ-протеазы. Композиции лечат ВИЧ-инфекции или СПИД за счет снижения уровня церамида, вирусной нагрузки и усиления иммунной активности пациентов. Изобретение расширяет арсенал средств указанного назначения. 3 с. и 5 з.п. ф-лы, 4 табл.
| ЭЛЕКТРОМАГНИТНАЯ ФОКУСИРУЮЩАЯ СИСТЕМА | 1974 |
|
SU560275A1 |
| МАРТЫНОВА Е.А | |||
| и др | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Биохимия | |||
| - М.: Наука, 1995 т.6, вып.4 с.618-625. | |||
Авторы
Даты
2003-04-27—Публикация
1996-07-19—Подача