Изобретение относится к иммунологии, иммунофармакологии, медицинской биотехнологии и фармацевтической промышленности. Иммунотропные вещества из кожи после соответствующих испытаний могут найти применение как лекарственные средства для иммунокоррекции в качестве иммуномодуляторов.
Известен способ получения тимопоэтина из эмбриональной кожи крупного рогатого скота путем ее измельчения в растворе бикарбоната аммония, центрифугирования, ультрафильтрации, центрифугирования, гель-хроматографии, гидрофобной хроматографии, анионообменной хроматографии в системе высокоэффективной жидкостной хроматографии, обессоливания и лиофилизации [1]. Однако процесс получения технологически довольно сложен, выход препарата незначителен, этап разделения путем высокоэффективной жидкостной хроматографии трудно применить при промышленном получении препарата. Иммунотропное вещество тимопоэтин, полученное из эмбриональной кожи крупного рогатого скота описанным выше методом, обладает активностью в иммунологических тестах: индуцирует дифференцировку протимоцитов и стимулирует образование циклического GMP в Т-клеточной линии СЕМ. Однако оно обнаружено лишь в эмбриональной коже и отсутствует в коже крупного рогатого скота.
В качестве прототипа взят наиболее близкий к настоящему изобретению способ получения иммунотропных веществ из кожи свиньи путем измельчения кожи в растворе хлористого натрия, центрифугирования, нагревания, центрифугирования, обработки надосадочной жидкости ацетоном, центрифугирования, хроматографии на Сефадексе G-50, обессоливания и лиофилизации [2]. Этот же способ ранее был запатентован как способ получения вещества с молекулярной массой от 1400 до 15000 Д из кожи свиньи, влияющего на пролиферацию и дифференцировку кератиноцитов человека [3]. Однако, применяя этот метод, получают два иммунотропных вещества; одно - с молекулярной массой более 15000 Д и другое - с молекулярной массой от 1400 до 15000 Д, стимулирующие В-систему иммунитета. Они увеличивают количество антителообразующих клеток селезенки мышей на пике первичного иммунного ответа. Однако эти вещества не влияют на Т-систему иммунитета в тесте восстановления чувствительности фоновых розеткообразующих клеток селезенки тимэктомированных мышей к ингибирующему действию азатиоприна.
Цель изобретения - увеличить активность получаемых иммунотропных веществ с помощью заявляемого метода так, чтобы они влияли и на В- и на Т-систему иммунитета.
Эта цель достигается тем, что в способ, взятый в качестве прототипа, были введены три этапа высаливания сульфатом аммония. До стадии получения "ацетонового порошка" этапы методов совпадают: кожу свиньи измельчают, гомогенизируют в растворе хлористого натрия, центрифугируют, подвергают термоденатурации при 75-85oС в течение 10-20 мин, центрифугируют при 5000-15000 g в течение 10-30 мин, обрабатывают охлажденным до -20oС (или ниже) ацетоном в соотношении 1: 6-1: 8, высушивают "ацетоновый порошок" при комнатной температуре. Далее вводятся следующие этапы: "ацетоновый порошок" растворяют в 0,005-0,015 М растворе трис-HCl буфера рН 6,0-8,0, центрифугируют при 8000-10000 g в течение 10-20 мин при 4-6oС; осадок отбрасывают, а к супернатанту прикапывают насыщенный раствор сульфата аммония в соотношении 2:1-3: 1, центрифугируют при 8000-10000 g в течение 40-50 мин при 4-6oС, доводят рН супернатанта до 3,5-4,5 с помощью 8-10% раствора уксусной кислоты, добавляют сухой сульфат аммония из расчета: 14-15 г на 100 мл супернатанта, центрифугируют при 10000-12000 g в течение 20-30 мин при 4-6oС, гомогенизируют осадок в 0,01-0,02 М трис-НСl рН 7,5-8,5, прикапывают к гомогенату насыщенный раствор сульфата аммония в соотношении 1:1-1,5:1, центрифугируют при 16000-18000 g в течение 20-30 мин при 4-6oС. Далее делают по прототипу: гомогенизируют осадок в 30-50 мл 0,01-0,02 М трис-НСl + 0,14-0,15 М NaCl рН 7,5-8,5, центрифугируют при 16000-18000 g в течение 20-30 мин при 4-6oС, хроматографируют на колонке с Сефадексом G-50, собирают две фракции: одну с молекулярной массой выше 15000 Д и другую - с молекулярной массой от 1400 до 15000 Д, обессоливают и лиофилизируют.
Температура термоденатурации 75-85oС и время термоденатурации подобраны таким образом, что нужные вещества остаются в растворе, в то время как часть неактивного материала денатурируется. Центрифугирование при 5000-15000 g в течение 10-30 мин и температуре 4-6oС подобраны так, что при этих параметрах денатурированные белки удаляются. При центрифугировании ниже 5000 g и менее 10 мин часть денатурированного неактивного материала остается в супернатанте, что загрязняет препарат. Увеличивать скорость центрифугирования более 15000 g и время более 30 мин не имеет смысла, т.к. при этих условиях денатурированный материал полностью осаждается. Изменение соотношения вес порошка после обезжиривания: объем воды менее 1:4 и более 1:6 приводит к загрязнению препарата. Три стадии высаливания сульфатом аммония подобраны таким образом, что удаляется неактивный материал и супрессорные вещества, а активный материал остается и подвергается очистке. Выбор концентрации буфера (0,005-0,015 М) и его рН (6,0-8,0) обусловлен тем, что в нем не происходит потери активности получаемых веществ, в то же время препараты хорошо разделяются по молекулярным массам на Сефадексе G-50. Хлористый натрий до концентрации 0,14-0,15 М добавляется к буферу для того, чтобы можно было определять активность веществ в пробах сразу после разделения на Сефадексе.
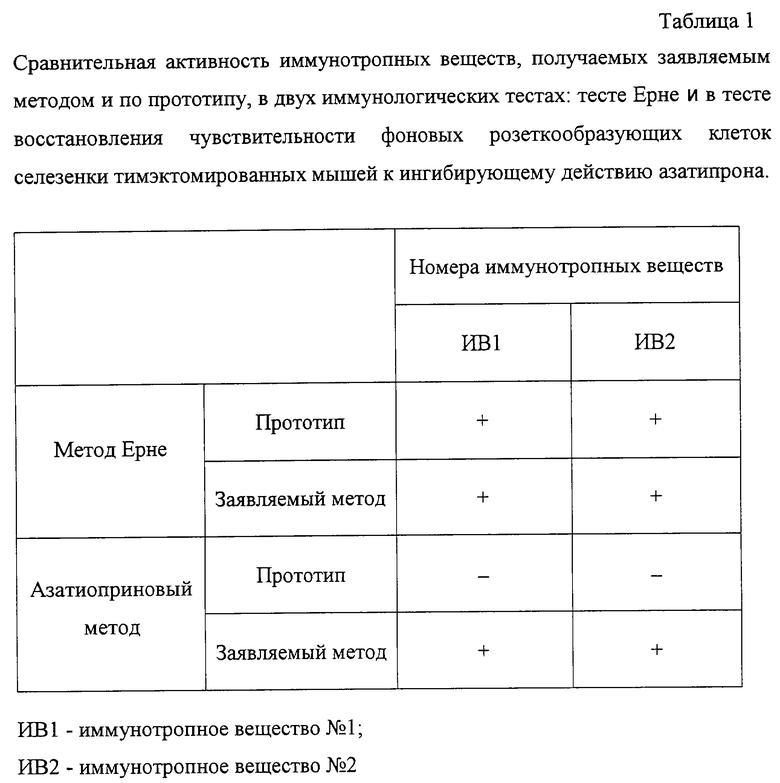
Определяли активность иммунотропных веществ в двух тестах: тесте Ерне и азатиоприновом тесте. В тесте Ерне определяли влияние иммунотропных веществ на количество антителообразующих клеток (АОК) селезенки мышей СВА на пике первичного иммунного ответа [2, 4]. Эритроциты барана вводили внутрибрюшинно в 0,5 мл физиологического раствора в концентрации 400 млн/мл. Одновременно подкожно вводили испытуемые препараты в дозе 1, 10 и 100 мкг на мышь. На пятые сутки животных забивали, выделяли селезенки и подсчитывали число зон гемолиза в чашках Петри. Определяли процент АОК по отношению к контролю, принимая среднюю арифметическую в контрольной группе за 100%. Все результаты соотносили со средней арифметической в контрольной группе.
В азатиоприновом тесте Баха определяли влияние иммунотропных веществ на восстановление чувствительности фоновых розеткообразующих клеток (фРОК) селезенки тимэктомированных мышей к ингибирующему действию азатиоприна [5]. Мышей-самцов С 57 В 1/6 тимэктомировали в возрасте 6-8 недель для создания модели частичного иммунодефицита по Т-системе иммунитета и брали в опыт через 2-8 недель после операции. Получали суспензию клеток селезенки. В опытные пробы помимо азатиоприна добавляли испытуемые препараты до конечной концентрации 1, 5, 10, 20, 50 и 100 мкг/мл. Подсчитывали количество фРОК селезенки тимэктомированных мышей на 104 ядросодержащих клеток.
Результаты выражали в процентах фРОК по формуле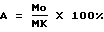 ,
,
где Мк - средняя арифметическая фРОК в контроле;
Мо - то же, в опыте.
Активными считали фракции, для которых процент фРОК был менее 50%. Для сравнения активности препаратов определяли минимальную концентрацию, при которой препарат проявлял активность.
В табл. 1, 2 и 3 представлено сравнение активности иммунотропных веществ прототипа и заявляемого способа по влиянию на В-систему иммунитета в тесте Ерне и Т-систему иммунитета в тесте восстановления чувствительности фоновых розеткообразующих клеток селезенки тимэктомированных мышей к ингибирующему действию азатипрона. Как видно из этих данных, иммунотропные вещества, получаемые по заявляемому способу, активны в обоих методах: Ерне и азатиоприновом, в то время как вещества, получаемые по прототипу, активны лишь в методе Ерне. Помимо этого, иммунотропные вещества, имеющие одинаковые молекулярные массы и полученные по прототипу и по заявляемому методу, имеют в методе Ерне различный характер зависимости активности от дозы. Иммунотропное вещество 1 (ИВ1), полученное по прототипу, имеет максимальную активность при дозе 10 мкг/мышь, в то время как ИВ1, полученное по заявляемому способу, - при дозе 100 мкг/мышь. Иммунотропное вещество 2 (ИВ2), полученное по прототипу, имеет минимальную активность при дозе 10 мкг/мышь; ИВ2, полученное по заявляемому способу, имеет минимальную активность при 1 мкг/мышь.
Таким образом, заявляемый способ позволяет получить более активные иммунотропные вещества, влияющее как на В-, так и на Т-систему иммунитета.
Пример 1 (прототип).
Свиную кожу измельчают ножницами и гомогенизируют в 0,14 М растворе хлористого натрия рН 7,0 при 4oС (1094 Homogenizer, Tecator, Sweden). На 50 г кожи берут 650 мл 0,14 М раствора NaCl (соотношение вес ткани: объем раствора - 1: 13). Гомогенат центрифугируют при 2500g в течение 30 мин при 4oС (центрифуга J-6M/E, ротор 4.2, Beckman, Великобритания). Осадок отбрасывают, а супернатант в объеме 630 мл подвергают термоденатурации при 75oС в течение 20 мин на водяной бане при постоянном перемешивании, смесь охлаждают до 4oС. Денатурированный материал осаждают центрифугированием при 10000 g в течение 20 мин при +4oС (центрифуга J2-21M, ротор JA-14, Beckman, США), а супернатант в объеме 620 мл прикапывают к 4 л ацетона, охлажденного до -20oС. Выпавший осадок отмывают ацетоном путем центрифугирования при 2500 g в течение 15 мин при 4oС и высушивают под тягой при комнатной температуре. В результате получают 800 г "ацетонового порошка" (800±50 мг). Полученный ацетоновый порошок растворяют в 30 мл 0,01 М растворе трис-НСl буфера + 0,15М NaCl pH 8,0 при комнатной температуре. Нерастворимую часть удаляют центрифугированием при 4000 g в течение 30 мин при 4oС, а супернатант наносят на колонку 2,5•100 см с Сефадексом G-50 (2,5х80 см), уравновешенной тем же буфером. Собирают две фракции: одну с молекулярной массой более 15000 Д (иммунотропное вещество 1), а другую - с молекулярной массой от 1400 до 15000 Д (иммунотропное вещество 2), обессоливают и лиофилизируют.
Оба вещества обладают иммунологической активностью в тесте Ерне: увеличивают количество антителообразующих клеток селезенки мышей на пике первичного иммунного ответа, но неактивны в тесте восстановления чувствительности фоновых розеткообразующих клеток селезенки тимэктомированных мышей к ингибирующему действию азатиприна (табл. 1, 2, 3). Иммунотропное вещество 1 (ИВ1) имеет максимальную активность при дозе 10 мкг/мышь, иммунотропное вещество 2 (ИВ2) - при дозе 1 мкг/мышь.
Пример 2 (по предлагаемому методу)
Свиную кожу измельчают ножницами и гомогенизируют в 0,14 М растворе хлористого натрия pH 7,0 при 4oС (1094 Homogenizer, Tecator, Sweden). На 50 г кожи берут 650 мл 0,14 М раствора NaCl (соотношение вес ткани: объем раствора 1:13). Гомогенат центрифугируют при 2500 g в течение 30 мин при 4oС (центрифуга J-6M/E, ротор 4.2, Beckman, Великобритания). Осадок отбрасывают, а супернатант в объеме 630 мл подвергают термоденатурации при 75oС в течение 20 мин на водяной бане при постоянном перемешивании, смесь охлаждают до 4oС. Денатурированный материал осаждают центрифугированием при 10000g в течение 20 мин при + 4oС (центрифуга J2-21M, ротор JA-14, Beckman, США), а супернатант в объеме 620 мл прикапывают к 4 л ацетона, охлажденного до -20oС. Выпавший осадок отмывают ацетоном путем центрифугирования при 2500 g в течение 15 мин при 4oС и высушивают под тягой при комнатной температуре. В результате получают 800 г "ацетонового порошка" (800±50 мг).
Затем его растворяли в 0,01 М трис-НСl буфере рН 8,0 при комнатной температуре и центрифугировали при 10000 g в течение 20 мин при 4oС. Осадок отбрасывали, а к супернатанту прикапывали насыщенный раствор сульфата аммония в соотношении 3:1 при 4oС. Нерастворимую часть удаляли центрифугированием при 10000g в течение 50 мин при 4oС. Доводили рН супернатанта до 4,0 с помощью 10% раствора уксусной кислоты. Затем добавляли сухой сульфат аммония при постоянном помешивании из расчета: 14,6 г на 100 мл супернатанта и 30 г на 100 мл уксусной кислоты, перемешивали при комнатной температуре и центрифугировали при 12000 g в течение 30 мин при 4oС. Супернатант сливали, осадок гомогенизировали в 0,01 М трис-НСl рН 8,0. Затем насыщенный раствор сульфата аммония прикапывали к гомогенату в ледяной бане в соотношении 1,5:1 и центрифугировали при 18000 g в течение 30 мин при 4oС. Супернатант сливали, осадок гомогенизировали в минимальном объеме 0,01М трис-НСl + 0,15 М NaCl рН 8,0 и центрифугировали при 18000 g в течение 30 мин при 4oС. Осадок отбрасывали, а супернатант наносили на колонку 2,5х100 см с Сефадексом G-50 с маркерами: голубым декстраном и DNP-L-аланином. Собирали две фракции: одну с молекулярной массой более 15000 Д (иммунотропное вещество 1, ИВ1) и другую - с молекулярной массой от 1400 до 15000 Д (иммунотропное вещество 2, ИВ2) обессоливали и лиофилизировали.
Получали иммунотропные вещества 1 и 2, активные как в методе Ерне - увеличивающие количество антителообразующих клеток селезенки мышей на пике первичного иммунного ответа, так и в тесте восстановления чувствительности фоновых розеткообразующих клеток селезенки тимэктомированных мышей к ингибирующему действию азатиприна (табл. 1, 2, 3). В тесте Ерне иммунотропное вещество 1 обладало максимальной активностью в концентрации 100 мкг/мышь, а ИВ2 - в концентрации 10 мкг/мышь. В азатиоприновом тесте ИВ1 обладало активностью в концентрации 20 мкг/мл, а ИВ2 - в концентрации 10 мкг/мл.
Литература
1. Audhya Т. К., Goldstein G. Amino acid sequence of thymopoietin isolated from skin. Ann. N.Y. Acad. Sci. 1988, V. 548, P. 233-240.
2. Арион В.Я., Белова О.В., Луканидина Т.А., Сысоева О.Б.,. Дворцова В. В., Бреусов Ю.Н. Иммунологические свойства препаратов из кожи. Бюлл. экспер. биол. мед. - 2000. - Т.129. - 2. - С. 194-197.
3. Арион В. Я., Белова О.В., Орлова В.Ф., Капитанов А.Б., Лопухин Ю.М. Способ получения вещества из кожи свиньи, влияющего на пролиферацию и дифференцировку кератиноцитов человека. Патент 2038087. Зарегистрирован 27.06.1995. Бюлл. изобрет. откр. 18, С. 24, 1995.
4. Зигль Э., Бем Э. "Метод локального гемолиза в геле." В кн.: Иммунологические методы. С. 96-107,1979.
5. Dardenne M., Bach J.-F. "The sheep cell rosette assay for the evaluation of thymic hormones. " In: Biologycal activity of thymic hormones. P. 235-243, 1975.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ ИЗ НЕЙРОСЕКРЕТОРНЫХ СТРУКТУР ЭПИТАЛАМУСА МОЗГА МЛЕКОПИТАЮЩИХ | 1996 |
|
RU2126258C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЕЩЕСТВА ИЗ КОЖИ СВИНЬИ, ВЛИЯЮЩЕГО НА ПРОЛИФЕРАЦИЮ И ДИФФЕРЕНЦИРОВКУ КЕРАТИНОЦИТОВ ЧЕЛОВЕКА | 1992 |
|
RU2038087C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЕЩЕСТВ, ВЛИЯЮЩИХ НА ПРОЛИФЕРАЦИЮ ЭПИДЕРМОИДНЫХ КЛЕТОК КАРЦИНОМЫ ЧЕЛОВЕКА А431 | 2011 |
|
RU2481113C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОЛОГИЧЕСКИ АКТИВНОГО ВЕЩЕСТВА ИЗ МОЧИ МЛЕКОПИТАЮЩИХ, В ТОМ ЧИСЛЕ И ЧЕЛОВЕКА, ОБЛАДАЮЩЕГО БИОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ СЫВОРОТОЧНОГО ТИМИЧЕСКОГО ФАКТОРА | 1997 |
|
RU2139065C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТИМИЧЕСКИХ ПЕПТИДОВ | 2006 |
|
RU2332423C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОАКТИВНЫХ ПОЛИПЕПТИДОВ/ПЕПТИДОВ, ОБЛАДАЮЩИХ ИММУНОКОРРИГИРУЮЩИМИ СВОЙСТВАМИ | 2006 |
|
RU2327475C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НЕОБХОДИМОСТИ И ЭФФЕКТИВНОСТИ ИММУНОКОРРЕКЦИИ Т-ЗВЕНА ИММУННОЙ СИСТЕМЫ | 2000 |
|
RU2187119C2 |
| Способ получения водорастворимых антигенов из опухолевых тканей | 1989 |
|
SU1747076A1 |
| Способ оценки лечения ретинобластомы у детей | 1989 |
|
SU1704086A1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ИММУНОМОДУЛИРУЮЩЕГО ПРЕПАРАТА ИЗ ТИМУСА СЕВЕРНОГО ОЛЕНЯ | 2001 |
|
RU2205013C1 |


Изобретение относится к иммунологии, иммунофармакологии, медицинской биотехнологии и фармацевтической промышленности, а именно к способу получения иммунотропных веществ из кожи свиньи. Способ включает измельчение, гомогенизацию кожи, центрифугирование, термоденатурацию супернатанта, центрифугирование денатурированного материала, обработку супернатанта охлажденным ацетоном, отмывку осадка охлажденным ацетоном, высушивание, растворение осадка и центрифугирование, с последующей хроматографией на колонке с Сефадексом G-50 и сбором фракции целевого продукта с молекулярной массой 1400-15000 Д, обессоливанием и лиофилизацией, где центрифугирование растворенного осадка проводят при 8000-10000 g в течение 10-20 мин при 4-6oС, к супернатанту прикапывают насыщенный раствор сульфата аммония в соотношении 2:1-3:1, центрифугируют при 8000-10000 g в течение 40-50 мин при 4-6oС, доводят рН полученного супернатанта до 3,5-4,5 прикапыванием 8-10%-ного раствора уксусной кислоты, добавляют сухой сульфат аммония из расчета 14-15 г - на 100 мл супернатанта, центрифугируют при 10000-12000 g в течение 20-30 мин при 4-6oС, гомогенизируют осадок в 0,01-0,02 М трис-HCl рН 7,5-8,5, прикапывают к гомогенату насыщенный раствор сульфата аммония в соотношении 1:1-1,5:1, центрифугируют при 16000-18000 g в течение 20-30 мин при 4-6oС, осадок гомогенизируют в 30-50 мл 0,01-0,02 М трис-HCl + 0,14-0,15 М NaCl рН 7,5-8,5, центрифугируют при 16000-18000 g в течение 20-30 мин при 4-6oС, а при хроматографии на колонке с Сефадексом G-50 одновременно собирают фракцию с молекулярной массой выше 15000 Д. Технический результат: изобретение позволяет увеличить активность получаемых иммунотропных веществ и получить вещества, влияющие как на В-, так и на Т-систему иммунитета. 3 табл.
Способ получения иммунотропных веществ из кожи свиньи, включающий измельчение, гомогенизацию кожи в растворе хлористого натрия, центрифугирование, термоденатурацию супернатанта при температуре 75-85oС в течение 10-20 мин, охлаждение смеси до 4oС, центрифугирование денатурированного материала при 5000-15000 g в течение 10-30 мин при 4oС, обработку супернатанта охлажденным до -20oС или ниже ацетоном в соотношении 1:6-1:8, отмывку выпавшего осадка охлажденным ацетоном, высушивание при комнатной температуре, растворение осадка в 0,005-0,015 М растворе трис-HCl буфера рН 6,0-8,0 и центрифугирование, с последующей хроматографией на колонке с Сефадексом G-50 и сбором фракции целевого продукта с молекулярной массой 1400-15000 Д, обессоливанием и лиофилизацией, отличающийся тем, что центрифугирование растворенного осадка проводят при 8000-10000 g в течение 10-20 мин при 4-6oС, к супернатанту прикапывают насыщенный раствор сульфата аммония в соотношении 2:1-3:1, центрифугируют при 8000-10000 g в течение 40-50 мин при 4-6oС, доводят рН полученного супернатанта до 3,5-4,5 прикапыванием 8-10%-ного раствора уксусной кислоты, добавляют сухой сульфата аммония из расчета 14-15 г - на 100 мл супернатанта, центрифугируют при 10000-12000 g в течение 20-30 мин при 4-6oС, гомогенизируют осадок в 0,01-0,02 М трис-HCl рН 7,5-8,5, прикапывают к гомогенату насыщенный раствор сульфата аммония в соотношении 1:1-1,5:1, центрифугируют при 16000-18000 g в течение 20-30 мин при 4-6oС, осадок гомогенизируют в 30-50 мл 0,01-0,02 М трис-HCl + 0,14-0,15 М NaCl pH 7,5-8,5, центрифугируют при 16000-18000 g в течение 20-30 мин при 4-6oС, а при хроматографии на колонке с Сефадексом G-50 одновременно собирают фракцию с молекулярной массой выше 15000 Д.
| СПОСОБ ПОЛУЧЕНИЯ ВЕЩЕСТВА ИЗ КОЖИ СВИНЬИ, ВЛИЯЮЩЕГО НА ПРОЛИФЕРАЦИЮ И ДИФФЕРЕНЦИРОВКУ КЕРАТИНОЦИТОВ ЧЕЛОВЕКА | 1992 |
|
RU2038087C1 |
| БИОЛОГИЧЕСКИ АКТИВНОЕ СРЕДСТВО, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРЕПАРАТ, СОДЕРЖАЩИЙ УКАЗАННОЕ СРЕДСТВО, И СПОСОБ ИСПОЛЬЗОВАНИЯ ПРЕПАРАТА | 1992 |
|
RU2041717C1 |
| RU 2055589 C1, 10.03.1996 | |||
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОСТИМУЛИРУЮЩИХ ТИМУСНЫХ ПОЛИПЕПТИДОВ | 1989 |
|
SU1737798A1 |
| US 5382428 А, 17.01.1995. | |||
Авторы
Даты
2003-04-27—Публикация
2001-06-14—Подача