Область изобретения
Изобретение относится к способам и устройству для получения заменителей эритроцитов. Это изобретение также относят к заменителю эритроцитов, включающему по существу свободный от тетрамера, поперечно сшитый, полимеризованный, пиридоксилированный раствор гемоглобина, который свободен от примесей стромы.
Предшествующий уровень техники
В течение ряда лет для замещения крови во время хирургических операций, вследствие травмы или по поводу других ситуаций консервированная кровь заменяла цельную кровь. Однако цельная кровь, полученная у людей-доноров, не подходит для использования во многих случаях. В частности, использование цельной крови проблематично вследствие необходимости типирования доноров, проблем устойчивости и возможности хранения, а также токсичности, вызванной вирусами и другими примесями. Эти проблемы особенно относятся к неотложным ситуациям, таким как использование крови в военно-полевых условиях. Было приложено много усилий для разработки заменителей цельной крови, полученной у людей-доноров. Эта разработка привела в результате к различным модификациям крови, получаемой у людей или у других млекопитающих. Из предшествующего уровня техники известно, что свободный от стромы гемоглобин обладает способностями транспорта кислорода и обратимого связывания кислорода (или лиганда). Поскольку проблемы токсичности предопределяли использование свободного от стромы гемоглобина в качестве заменителя крови, он потребовал дальнейших модификаций для предоставления нетоксичного, пригодного для использования фармацевтического продукта.
Эти модификации включают (1) получение гемоглобина, свободного или по существу свободного от стромы и примесей стромы; (2) пиридоксилирование; (3) полимеризацию или поперечную сшивку; (4) удаление тетрамера; и (5) модификацию с помощью окиси углерода или других лигандов.
Однако использование растворов гемоглобина, полученных с помощью этих методик, хотя и способных переносить достаточные количества кислорода для поддержания жизни, связано со множеством нежелательных побочных эффектов и свойств. Например, главным вызывающим тревогу побочным эффектом является снижение функции почек. Считалось, что эти изменения возникают вследствие присутствия нежелательных примесей, таких как бактериальный эндотоксин или фрагменты мембран эритроцитов (стромы). Хотя примеси, подобные этим, действительно могут вызвать почечные изменения, растворы гемоглобина, по существу свободные от указанных выше примесей, все же вызывают существенное нарушение почечной функции. Причина нарушения функции почек приписывалась физиологически неприемлемым количествам тетрамера неполимеризованного гемоглобина. Другими нежелательными побочными эффектами вливания тетрамерного гемоглобина являются сужение сосудов, гемоглобинурия, угнетение сердечного ритма, подъем среднего артериального давления и эктравазация вливаемого раствора, особенно в брюшную полость.
На практике ни в одном случае использования известных заменителей крови, полученных из гемоглобина, не был достигнут успех полного исключения проблем токсичности. Эти продукты также имеют неприемлемо короткий период полувыведения после введения людям-пациентам. Такие периоды полувыведения требуют повторного замещения объема крови в течение коротких периодов времени. Следовательно, имеется существенная потребность в продуктах гемоглобина, которые не токсичны для пациентов и имеют существенные периоды полувыведения после введения. Конечно, эти продукты должны обладать способностью обратимо транспортировать кислород к тканям способом, подобным способу, достигаемому цельной кровью.
Сущность изобретения
Настоящее изобретение представляет заменители гемоглобина, которые нетоксичны для людей и имеют значительные периоды полувыведения, составляющие при введении людям, по меньшей мере, 15 ч. Продукты гемоглобина согласно изобретению являются свободными от стромы, пиридоксилированными и полимеризованными, а также свободными от вирусных и других токсических примесей. Далее, эти продукты являются по существу свободными от лейкоцитов (белых клеток, крови) и тромбоцитов.
Настоящее изобретение также охватывает способы для получения заменителей гемоглобина изобретения. Способы включают удаление лейкоцитов и тромбоцитов из крови; отмывание и лизирование эритроцитов; удаление примесей стромы и стромы с помощью фильтрации и тепловой обработки; получение дезоксиформы гемоглобина; пиридоксилирование и полимеризацию; дальнейшую очистку и концентрацию; и дезоксигенацию. Затем можно составить композицию полученного в результате продукта гемоглобина для предоставления продукта гемоглобина, имеющего уровни различных электролитов в нормальных физиологических диапазонах.
Изобретение также представляет водную композицию пиридоксилированного, полимеризованного гемоглобина, в которой гемоглобин представляет собой полимеризированный глютаральдегидом гемоглобин, содержащий тетрамерный материал, имеющий профиль молекулярной массы, показанный на фиг.3. Эта композиция может применяться для получения заменителя внеклеточных эритроцитов. В этом аспекте композицию сначала очищают для удаления тетрамера и затем комбинируют с соответствующими количествами электролитов для производства физиологически приемлемого внеклеточного заменителя эритроцитов, который в последующем может использоваться для лечения людей-пациентов, требующих вливания носителя кислорода.
Краткое описание чертежей
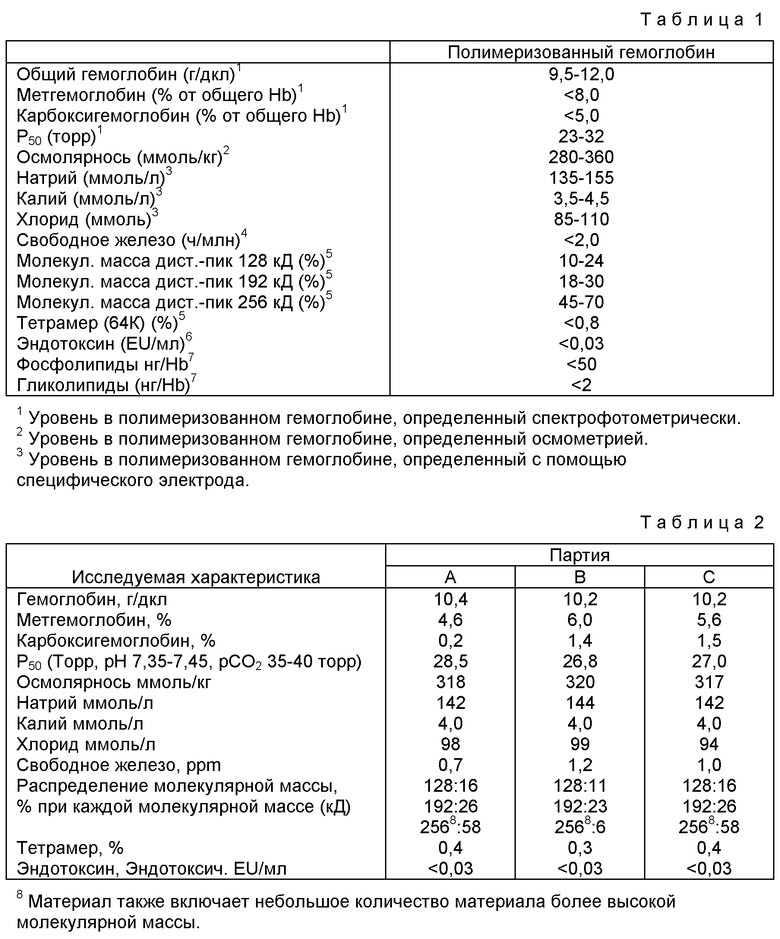
Фиг. 1 представляет собой график, представляющий часть способа и оборудования, используемых для получения раствора дезоксигенированного гемоглобина, приготовленного для пиридоксилирования и полимеризации.
Фиг. 2 представляет график, представляющий часть способа и устройства, начинающийся с пиридоксилирования и полимеризации и приводящий к получению дезоксигенированного, очищенного, пиридоксилированного, полимеризованного продукта гемоглобина, и часть способа и устройства, используемых для составления композиции конечного продукта гемоглобина, имеющего физиологические уровни электролитов.
Фиг.3 представляет собой выявление с помощью ВЭЖК полимеризованного материала после обработки глицином перед очисткой. Полимеризованный продукт указан пиками при времени удерживания (ВУ) 15,57; 16,08; 17,00 и 18,19. Тетрамический материал указан пиками при ВУ 19,88 и 20,51. Полимер составляет 76,2% этого материала.
Фиг. 4 представляет собой выявление с помощью ВЭЖХ продукта гемоглобина. Полимеризованный гемоглобин указан пиками при ВУ 15,7; 16,33; 17,32 и 18,56. Тетрамер указан пиком при ВУ 21,18.
Фиг. 5 представляет собой график, представляющий процесс очистки на хроматографической колонке.
Фиг.6 представляет собой график, представляющий процесс очистки с помощью мембранной фильтрации.
Подробное описание предпочтительного варианта осуществления
Настоящее изобретение относится к бесклеточному заменителю эритроцитов, содержащему по существу свободный от тетрамера, поперечно сшитый, полимеризованный, пиридоксилированный гемоглобин, который по существу свободен от стромы, примесей стромы и других примесей.
Используемый здесь термин "поперечно сшитый" обозначает химическое размещение молекулярных "мостиков" на или внутри молекулы или между молекулами с целью изменения формы, размера, функции или физических характеристик молекулы. Поперечно сшитые молекулы могут быть полимеризованными или неполимеризованными, т.е. поперечно сшитые молекулы могут быть тетрамерными.
Используемый здесь термин "тетрамер" относится к молекулам гемоглобина, имеющим молекулярную массу приблизительно 64 кД; то есть термин относится как к нативным, так и внутримолекулярно поперечно сшитым молекулам гемоглобина.
Используемый здесь термин "по существу свободный от тетрамера" обозначает уровень чистоты относительно примеси тетрамера, при которой больше не присутствуют определенные биологические реакции на тетрамер, введенный млекопитающему. Главным критерием является отсутствие изменений почечной функции, когда вводятся фармацевтически эффективные количества, то есть на уровне чистоты приблизительно 99% или выше (присутствует менее чем приблизительно 1% тетрамера). Предпочтительный продукт, полученный с помощью заявленного способа, содержит не более чем приблизительно 0,8% тетрамера от общей массы гемоглобина (ОНb). Другими словами, по существу свободный от тетрамера продукт, в соответствии с изобретением, содержит не более чем физиологически приемлемые количества неполимеризованного тетрамера гемоглобина. Особенно предпочтительные продукты изобретения содержат менее чем приблизительно 0,5% тетрамера; наиболее предпочтительные продукты изобретения содержат приблизительно 0,3-0,4% тетрамера. Было установлено, что такие количества тетрамера являются физиологически приемлемыми.
Термины "сверхочищенный продукт" или "очищенный продукт" имеют такое же значение, как термин "по существу свободный от тетрамера".
Используемое обозначение % общего гемоглобина (ОНb) определен в виде граммов гемоглобина/100 мл раствора.
Термин "полимеризующий раствор" обозначает раствор, содержащий "поперечно сшивающее" или полимеризующее средство, такое как глютаральдегид, имидо эфиры, диаспирин или другие, в биохимически приемлемом носителе.
Термин полимеризованный обозначает размещение молекулярных мостиков между молекулами или тетрамерные субъединицы, где размер и масса полученной в результате пслимеризованной молекулы увеличена относительно нативного или тетрамерного гемоглобина. Полимеризованный гемоглобин не является тетрамерным гемоглобином,
Под термином раствор гемоглобина подразумевается раствор тетрамерного гемоглобина или молекул полимеризованного гемоглобина, в котором молекулы не содержатся внутри эритроцита. К такому раствору не представляется требований, что он должен быть свободен или по существу свободен от стромы эритроцитов или примесей стромы. Однако предпочтительные растворы полимеризованного гемоглобина свободны от стромы эритроцитов или примесей стромы.
Под термином "полупроницаемая мембрана" подразумевается мембрана, проницаемая для некоторых видов молекул, но не для других, т.е. мембрана, которая действует в качестве избирательного фильтра, исключающего определенные молекулярные массы.
Продукт способа в соответствии с настоящим изобретением, раствор полимеризованного, пиридоксилированного гемоглобина, по существу свободный от тетрамерного (нативного или внутримолекулярно поперечно сшитого) гемоглобина, примесей стромы и различных других примесей, полученный из подвергнутого тепловой обработке, вирусно инактивированный тетрамерный гемоглобин, является физиологически приемлемым, а также пригодным для терапевтического и клинического применения. Продукт имеет обратимую способность связывания кислорода, которая необходима для транспорта кислорода. Наиболее примечательно то, что продукт проявляет хорошие характеристики загрузки и разгрузки при использовании, что коррелирует с наличием кривой диссоциации оксигемоглобина (P50), аналогичной цельной крови. Продукт с высоким сродством связывает кислород в капиллярах легких, и затем адекватно высвобождает кислород в ткани в организме. Продукт также не требует исследований совместимости у реципиента.
Продукт также имеет период полувыведения при введении людям, составляющий приблизительно, по меньшей мере, 15 ч, а более предпочтительно, приблизительно 24 ч. Этот продукт гемоглобина может вливаться пациентам в количествах, достигающих приблизительно 3,0 л и даже выше приблизительно до 5,0 л. Другими словами, гемоглобин согласно изобретению может использоваться для возмещения по существу всего объема крови пациента, не вызывая сужение сосудов, токсического действия на почки, гемоглобинурию или другие проблемы, связанные с внутривенным введением синтетических или полусинтетических носителей кислорода и заменителей крови. Таким образом, изобретение включает способ переливания пациенту, предпочтительно пациенту-человеку, количества свободного от стромы, свободного от тетрамера, полимеризованного, пиридоксилированного продукта гемоглобина, который не токсичен для пациента, в котором количество достигает, по меньшей мере, приблизительно 5,0 л. Такой способ включает подключение пациента или субъекта к инфузионному устройству или другому оборудованию для вливания или переливания крови пациенту.
Способ этого изобретения уникален в том, что он предоставляет продукт, имеющий уровень тетрамера не более чем приблизительно 1%, а более предпочтительно не более чем приблизительно 0,8 мас.% от общей массы гемоглобина в растворе. Способ согласно этому изобретению дает дополнительное преимущество в том, что он может предоставить конечный продукт, по существу свободный от микробных и вирусных антигенов и патогенов. Содержание таких микробных и вирусных антигенов и патогенов снижено до не выявляемых уровней, т.е. продукт является стерильным, по данным определения с помощью анализа, изложенного в главе XXIII Фармакопеи США <71>. Примерами таких антигенов и патогенов являются, например, бактериальные, рикеттсиозные, грибковые, протозойные, вирусные и другие организмы. Наиболее важно, что способ предоставляет биологический продукт, свободный от вирусов, которые вызывают гепатит и синдром приобретенного иммунодефицита (СПИД).
Что касается физиологических свойств, то биологический продукт этого изобретения при вливании в количествах, достигающих, по меньшей мере, приблизительно 5,0 л, не вызывает сужения сосудов, токсического действия на почки, гемоглобинурии и других проблем, связанных с внутривенным введением известных растворов гемоглобина, содержащих физиологически нежелательные количества тетрамерного гемоглобина. Внутривенное введение продукта, полученного с помощью заявленного способа, не приводит к выявляемому снижению выработки мочи, к не выявляемому снижению скорости клубочковой фильтрации, к не выявляемой экстравазации в брюшную полость и к не выявляемому изменению цвета вырабатываемой мочи.
Поэтому способ изобретения предоставляет бесклеточный заменитель эритроцитов, который можно применять при лечении травмы, инфаркта миокарда, инсульта, острой анемии и расстройств, связанных с недостаточностью кислорода, таких как гипоксемия, гипоксия или терминальная гипоксия вследствие повреждения или неспособности легких полностью оксигенировать кровь. Продукт также может применяться при лечении любого заболевания или патологического состояния, требующего введения жидкости с целью реанимации (например, травма, в частности, геморрагический шок), средства для увеличения внутрисосудистого объема или обменного переливания. В дополнение к медицинскому лечению, продукт может применяться при консервации органов для трансплантации.
Способ включает следующие процедуры:
1) аспирация и фильтрация эритроцитов,
2) отмывание/лизис клеток,
3) тепловая обработка,
4) концентрация ультрафильтрацией,
5) дегазация,
6) химическая модификация,
7) очистка,
8) поликонцентрация ненасыщенного полиэфира,
9) дезоксигенация,
10) составление композиции.
Предпочтительным исходным материалом в способе настоящего изобретения является цельная кровь или консервированные эритроциты человека с истекшим сроком годности. Кроме того, также может использоваться кровь с неистекшим (действующим) сроком годности. Предпочтительно, в этом способе не используется цельная кровь, если она хранилась более 2 недель после даты срока годности, указанного на мешке. Использование цельной крови со сроком годности, просроченным более чем на 2 недели, создает дополнительную трудность при экстрагировании гемоглобина и удалении клеточных остатков, таких как белки стромы и примеси.
Все описанные способы применимы для крови других млекопитающих с возможными небольшими модификациями в пределах известного уровня техники. Большая часть способа может проводиться при температуре от приблизительно 2oС до приблизительно 8oC, предпочтительно приблизительно 4oС.
Во время аспирации и фильтрации эритроцитов эритроциты (Э) асептически экстрагируются из мешков с донорской кровью без введения воздуха в кровь и пропускаются через серию фильтров для получения в результате суспензии Э, имеющей сниженные количества лейкоцитов и тромбоцитов. Полученную в результате суспензию затем подвергают отмыванию/лизису клеток.
Суспензия отмывается в атмосфере окиси углерода приблизительно 1%-ным раствором NaCl для удаления остаточных белков плазмы. Затем отмытые Э обрабатывают водой для инъекций (ВДИ) для лизирования клеток, и полученную в результате смесь затем осветляют с использованием блока перекрестно-поточной фильтрации. Затем осветленный продукт подвергают тепловой обработке для осаждения дополнительного материала стромы, который удаляется с помощью фильтрации. Полученный продукт представляет собой раствор свободного от стромы гемоглобина (ССГ) с ОНb приблизительно 3% (мас./об.).
Подвергнутый тепловой обработке и свободный от стромы раствор гемоглобина, содержащий карбоксигемоглобин, концентрируют и дегазируют для получения раствора ССГ, содержащего дезоксигемоглобин. Дегазация включает во-первых насыщение раствора карбоксигемоглобина кислородом в течение приблизительно 16 ч для получения раствора оксигенированного гемоглобина и приблизительно 7 мас. % карбоксигемоглобина от общей массы гемоглобина. Затем кислород вытесняется азотом, аргоном или гелием для образования раствора, содержащего свободный гемоглобин, т.е. не связанный гемоглобин, и приблизительно 7 мас.% оксигемоглобина от общей массы гемоглобина. Полученный в результате дегазированный раствор фильтруют и переносят в сосуд для химической модификации.
Вслед за дегазацией свободный от стромы раствор гемоглобина пиридоксилируют с использованием пиридоксал-5'-фосфата (П5Ф) в молярном соотношении пиридоксал-5'-фосфата и гемоглобина приблизительно от 1:1 до 3:1. Альтернативно, свободный от стромы гемоглобин может пиридоксилироваться с использованием 2-Нор-2-формилпиридоксал-5'-фосфата. В смесь пиридоксилирования добавляют восстанавливающее средство, такое как цианоборгидрид натрия или, предпочтительно, боргидрид натрия. Избыточные реактивы и соли удаляют с помощью диализа против свободной от пирогена воды, или, предпочтительно, диафильтрации с ВДИ. Затем пиридоксилированный гемоглобин полимеризуют раствором глютаральдегида.
Свободный от стромы, пиридоксилированный раствор гемоглобина полимеризуют с использованием водного раствора глютаральдегида. Продолжительность полимеризации и количество добавляемого глютаральдегида зависит от объема раствора гемоглобина, желательного выхода полимеров и желательного распределения молекулярной массы. В целом, более длительная полимеризация увеличивает выход и распределение молекулярной массы полимеров. Выход, составляющий приблизительно 75 мас.% полимера от общей массы гемоглобина получают приблизительно через 16-18 ч. Предпочтительная конечная точка полимеризации определяется как точка, в которой раствор содержит приблизительно 75 мас.% полимера от общей массы гемоглобина, по данным мониторинга с помощью ВЭЖХ с исключением по размеру. Альтернативно, конечная точка определяется как точка, в которой раствор содержит приблизительно 65 мас.% полимера на основании общей массы гемоглобина, т.е. приблизительно 2,5 ч.
Реакцию полимеризации прекращают с помощью добавления водного глицина. Как можно быстрее должен добавляться буфер. Поперечные сшивки затем стабилизируют с помощью как можно более быстрого добавления раствора водного боргидрида натрия. Затем этот полимеризованный раствор концентрируют и затем проводят диафильтрацию в атмосфере кислорода для оксигенации раствора. Наконец, в раствор добавляют воду, до тех пор пока раствор не будет содержать приблизительно 4 мас.% гемоглобина.
Полимеризация в соответствии с изобретением приводит в результате к высокому выходу полимеров, имеющих узкий диапазон молекулярной массы, как показано ниже на фиг.3 и примере.
Затем раствор полимеризованного, пиридоксилированного гемоглобина очищают с помощью хроматографии на колонках, фильтрации, например мембранной фильтрации или их обоих, для удаления остаточного неполимеризованного (тетрамерного) гемоглобина из раствора. Очищенный раствор полимеризованного гемоглобина концентрируют приблизительно до 6% с использованием устройства ультрафильтрации при подготовке к газообмену.
Затем концентрированный раствор дезоксигенируют азотом. Дезоксигенация имеет место при температуре приблизительно 10-12oС до тех пор пока количество оксигемоглобина в растворе составляет менее чем приблизительно 16 мас.% от общего гемоглобина.
Полученный в результате дезоксигенированный, очищенный и полимеризованный раствор гемоглобина концентрируют с помощью ультрафильтрации в атмосфере азота в охлажденном сосуде. рН доводят приблизительно до 8,8-9,0. Количество электролитов могут по необходимости корригироваться до уровней, представляющих уровни в нормальной плазме. Кроме того, необязательно могут добавляться обычные антиоксиданты, такие как глютатион, аскорбат или глюкоза. После концентрации раствора до желательного уровня, предпочтительно приблизительно 10 мас.% "олимеризованного, пиридоксилированного, очищенного, свободного от тетрамера, свободного от стромы гемоглобина, раствор стерилизуют с помощью фильтрации и переносят через устройство стерильного переноса в подходящие фармацевтически приемлемые контейнеры.
Характеристики полученного в результате раствора гемоглобина показаны в табл.1.
Следующие примеры демонстрируют определенные аспекты настоящего изобретения. Однако следует понимать, что эти примеры приведены только в иллюстративных целях и не имеют намерений полностью определить условия и диапазон этого изобретения. При отсутствии других определений все величины температуры выражены в градусах Цельсия. При отсутствии других указаний все проценты/ например, общего гемоглобина (ОНb), выражены как отношение масса/объем (мас. /об. ). Следует понимать, что в случаях приведения типичных условий реакции (например, температуры, времени реакции), хотя в целом и с меньшими удобствами, могут также использоваться условия, находящиеся как выше, так и ниже этих определенных диапазонов.
При отсутствии противоположных указаний все сосуды и емкости в способе изобретения изготовлены из нержавеющей стали марки 316-L. Предпочтительно, фармацевтическая степень обработки такой нержавеющей стали, которая была подвергнута очень тщательной полировке, облегчает и ускоряет ее очистку. Различные соединительные трубочки и трубки изготовлены из такой же нержавеющей стали или из тефлоновых или силиконовых трубок фармацевтической марки. Фильтры и мембраны, применяемые в способе, могут закупаться у компаний Millipore inc., Pall-Filtron или Cuno Inc.
Период полувыведения конечного продукта определяется in vivo у млекопитающих, например людей. Обычно, пробу крови берут у млекопитающего через период времени после вливания продукта млекопитающему. Количество продукта затем определяют с помощью центрифугирования образца крови, отделения части плазмы, спектрофотометрического определения уровней гемоглобина в плазме, и затем корреляции количества продукта, остающегося у млекопитающего, с периодом полувыведения продукта.
Хроматография ВЭЖХ с исключением по размеру в соответствии с изобретением проводится следующим образом:
Образец разводят 0,2 М калий-фосфатным буфером с рН 6,9 до 0,2 г/дкл, фильтруют через фильтр 0,2 мкм и вводят в систему ВЭЖХ, состоящую из следующих компонентов (в порядке потока по системе):
1. Насос Pharmacia модель 2248
- подвижной фазой является 0,2 М фосфат калия рН 6,9,
- скорость потока составляет 1,0 мл/мин.
2. Трубка из PEEK или титана длиной 45 см и внутренним диаметром 0,010 дюйма (0,254 мм).
3. Инжектор Pheodyne модель 7725i с петлей для взятия образцов PEEK 200 мкл.
4. Трубка из PEEK или титана длиной 18 см и внутренним диаметром 0,010 дюйма (0,254 мм).
5. Фильтр Upchurch модель А431 0,5 мкм.
6. Трубка из PEEK или титана длиной 9 см и внутренним диаметром 0,010 дюйма (0,254 мм).
7. Колонка Phenomenex Biosep SEC S-3000 75•7,8 mm Guard.
8. Трубка из PEEK или титана длиной 24 см и внутренним диаметром 0,010 дюйма (0,254 мм).
9. Колонка Phenomenex Biosep SEC S-3000 600•7,8 mm Analytical.
10. Трубка из PEEK или титана длиной 23 см и внутренним диаметром 0,010 дюйма (0,254 мм).
11. УФ детектор Pharmacia Uvicord SD
- длина волны 280 нм,
- проточная кювета: объем 8 мкл, длина канала 2,5 мм,
- диапазон: 2 AUFS,
- постоянная времени 10 секунд.
Максимальная спектральная поглощательная способность регистрируется с помощью Integrator LKB 2221, который интегрирует площади отдельных пиков и расчитывает площадь общего гемоглобина для каждого вида полимера.
Дальнейшее понимание изобретения можно получить из следующих неограничивающих примеров.
Пример
Ссылаясь теперь на фиг. 1, мешки 20 с донорской просроченной кровью (цельной кровью или эритроцитарной массой) располагают в подходящем асептическом аспирационном устройстве 22. Примером подходящего аспирационного устройства является система, имеющая два положения аспирации. Как только мешок с донорской кровью расположен в положении аспирации, игла в аспирационном устройстве протыкает мешок с донорской кровью, вводит приблизительно 150 мл 1% (мас./об.) водного раствора хлорида натрия и аспирирует просроченную кровь из мешка с донорской кровью под пониженным давлением или вакуумом. Аспирированная кровь проходит через фильтр 24 глубиной 100 мкм и затем подряд через два фильтра 26 глубиной 5 мкм. При прохождении крови через фильтры глубиной 5 мкм лейкоциты удаляются из крови. Обычно аспирируют приблизительно 170 единиц просроченной цельной крови, фильтруют и затем переносят в контейнер как показано на фиг.1. Затем фильтры промывают приблизительно 75 литрами 1% (мас./об.) водного раствора хлорида натрия.
Перед введением крови в контейнер 1, контейнер 1 заполняют приблизительно 70 л 1%-ного водного раствора хлорида натрия. После аспирации, фильтрации и переноса всех 170 единиц просроченной цельной крови и промывания фильтров контейнер содержит приблизительно 250 литров 4%-ного раствора гемоглобина. При проведении аспирации и фильтрации в контейнере 1 поддерживают пониженное давление, т.е. вакуум 20-28 мм рт.ст. После переноса всей просроченной крови в контейнер 1 вакуум отключают, и в контейнер вводят окись углерода так, что контейнер содержит атмосферу окиси углерода.
Как показано на фиг.1, контейнер 1 присоединяют к фильтру 28 тангенциального потока с размером пор 0,65 мкм. Первоначальное заполнение 250 литров 4%-ного раствора гемоглобина с помощью микрофильтрации через фильтр тангенциального потока концентрируют приблизительно до 125 л 8%-ного раствора гемоглобина. рН раствора гемоглобина в этот момент составляет приблизительно от 6 до 6,5. Вслед за концентрацией до 8% общего гемоглобина раствор промывают добавлением 1% (мас./об.) раствора хлорида натрия. Проводят диафильтрацию и удаление фильтрата и с той же скоростью добавляют раствор хлорида натрия. Обычно 125 л раствора гемоглобина промывают приблизительно 8 объемами 1%-ного раствора хлорида натрия (приблизительно, 1000 л). Вслед за промыванием раствор концентрируют приблизительно до 70 л, т.е. добавляют приблизительно 14% общего гемоглобина и "воды для инъекций" (ВДИ) для доведения объема раствора приблизительно до 180 л. При добавлении ВДИ клетки набухают и лопаются, высвобождая гемоглобин в раствор. Концентрация конечного раствора гемоглобина составляет приблизительно 5% общего гемоглобина (OHb).
Конечный раствор, еще находящийся в контейнере 1, осветляют. Сначала раствор концентрируют приблизительно до 50 л и фильтрат переносят в контейнер 2. При перекачке раствора через фильтр примеси стромы эритроцитов и материал клеточных стенок задерживается и удаляется фильтром. Остающиеся 50 л раствора в контейнере промывают (диафильтрируют) приблизительно 2,5 объемами ВДИ. Эти 2,5 объема промывки добавляют в контейнер 2. Затем материал, остающийся в контейнере 1, концентрируют приблизительно до 20 л и фильтрат добавляют в контейнер 2. Конечный объем в контейнере 2 составляет приблизительно 280 л 3,3%-ного раствора общего гемоглобина.
Затем свободный от стромы конечный раствор обрабатывают в контейнере 2 при температуре приблизительно 60-62oС в течение периода приблизительно 10 ч. В течение этого времени раствор умеренно перемешивают. По мере нагревания и достижения температуры приблизительно 55oС образуется преципитат.
Затем образовавшийся свободный от стромы, подвергнутый тепловой обработке 3,3% ОНb (мас./об.) раствор гемоглобина фильтруют через фильтр 30 с размером пор 0,2 мкм с последующей фильтрацией через фильтр 32 с размером пор 0,1 мкм и переносят в контейнер 3. Затем отфильтрованный раствор гемоглобина концентрируют приблизительно до 18% ОНb и затем промывают и диафильтруют 4 объемами ВДИ (180 л). Концентрацию и диафильтрацию осуществляют с использованием ультрафильтра 34 молекулярной массы 10 килодальтон (кД). Приемник стока 35, связанный с ультрафильтром 34, собирает фильтрат. В этот момент 45 л 18%-ного раствора гемоглобина содержит менее 50 нг фосфолипида на грамм гемоглобина, менее чем 2 нг гликолипида на грамм гемоглобина, менее чем 1% метгемоглобина, менее чем приблизительно 0,03 эндотоксиновых единиц эндотоксина на миллилитр при рН приблизительно от 6 до 6,5. Этот гемоглобин в растворе представляет собой карбоксигемоглобин.
Затем полученный раствор карбоксигемоглобина переносят в контейнер 4, где карбоксигемоглобин сначала оксигенируют, а затем дезоксигенируют. Контейнер 4 снабжен уплотнителем для предотвращения утечки газа, соединенным с газовыми магистралями подачи кислорода и азота, линией подачи из днища контейнера к мерному распылительному устройству, расположенному на верхней части контейнера 4, и коллектором перетока пены, соединенным с банкой для пены 1 так, что пена, образующаяся в контейнере 4, подается в банку для пены 36, где пена конденсируется в жидкость и подается назад в контейнер 4. Контейнер 4, кроме того, включает набор уплотнителей Pall Rings, заполняющих приблизительно одну треть объема контейнера. Банка для пены 36 включает газовый выпускной клапан для удаления газа. Раствор в контейнере 4 представляет собой 13%-ный раствор гемоглобина.
На первой стадии оксигенации кислород барботируют в раствор со скоростью, достаточной для обеспечения равномерной дисперсии газа в сосуде. В сосуд объемом 200 л барботируют газ со скоростью, приблизительно, 25 л/мин. Оксигенацию карбоксигемоглобина проводят в течение периода приблизительно 16 ч так, что полученный раствор содержит менее чем 5% карбоксигемоглобина от общей массы гемоглобина. Оксигенацию проводят при температуре приблизительно 10oС. Пену, образующуюся в контейнере 4, собирают в банку для пены 36 и после осаждения полученный в результате раствор переносят назад в контейнер 4.
После оксигенации в раствор барботируют аналогичный поток азота в течение приблизительно 6 ч или до тех пор, пока в растворе не останется менее чем 10% оксигемоглобина от общей массы гемоглобина. Барботирование азотом проводят при температуре приблизительно 10oС и рН приблизительно от 6 до 6,5. Альтернативно, карбоксигемоглобин может превращаться в дезоксигемоглобин с использованием мембранного обменника. Отмечено, что на стадии образования пены по существу не происходит денатурации гемоглобина, чего обычно следовало бы ожидать. Полученный в результате дезоксигенированный раствор теперь подготовлен для химической модификации.
Ссылаясь на фиг. 2, раствор дезоксигемоглобина переносят в контейнер 5 для химической модификации. Затем в контейнер 5, содержащий дезоксигемоглобин, приблизительно при 4oС добавляют водный раствор пиридоксил-5-фосфата (П5Ф)(93,75 г/л) при молярном соотношении П5Ф и гемоглобина от 1:1 до 3:1. Предпочтительно молярное соотношение П5Ф и гемоглобина 2:1. Пиридоксилирование проводят при температуре приблизительно 4oС. Раствор П5Ф обычно добавляют в течение приблизительно 1 мин и смешивают в течение приблизительно 15 мин, после чего в раствор гемоглобина добавляют раствор боргидрида натрия/гидроокиси натрия в молярном соотношении боргидрида натрия и гемоглобина приблизительно 20:1. Подходящий водный раствор боргидрида натрия/гидроокиси натрия содержит 0,8 г гидроокиси натрия на 2 л и 90,8 г боргидрида натрия на 2 л. Раствор боргидрида добавляют насколько возможно быстро в течение периода приблизительно 1 мин и затем перемешивают в течение одного часа. Полученные в результате 50 л раствора пиридоксилированного гемоглобина затем подвергают диафильтрации с использованием ультрафильтра 38 10 кД для удаления избытка реагентов 4 объемами ВДИ. Приемник стока 40, связанный с ультрафильтром 38, собирает фильтрат из фильтра 38.
После диафильтрации 4 объемами, т.е. 200 л ВДИ, гемоглобин полимеризуется. В контейнер 5, содержащий пиридоксилированный гемоглобин, добавляют достаточное количество ВДИ для приготовления 4,5%-ного раствора гемоглобина (приблизительно 175 л раствора гемоглобина). В раствор пиридоксилированного раствора добавляют раствор глютаральдегида в молярном соотношении глютаральдегида и гемоглобина приблизительно 24:1. Раствор глютаральдегида обычно добавляют в течение периода приблизительно 2,5 ч с помощью мерного насоса в раствор гемоглобина. Реакция полимеризации протекает в течение приблизительно 18 ч. Распределение молекулярной массы составляет приблизительно 75% полимера и 25% тетрамера. Целевые полимеры имеют молекулярные массы менее чем приблизительно 600000 с преобладающей фракцией молекулярных масс, находящихся в диапазоне 100000-350000.
Когда реакция полимеризации достигает целевого распределения молекулярной массы (приблизительно через 18 ч) в раствор гемоглобина добавляют (в качестве вещества, прекращающего реакцию) водный глицин (приблизительно 166 г/л) в молярном соотношении глицина и гемоглобина 140:1. См. фиг.3, которая представляет собой исследование с помощью ВЭЖХ полученного в результате полимеризованного, остановленного глицином гемоглобинового продукта. Затем полученный в результате раствор смешивают в течение приблизительно 10 мин, после чего в раствор гемоглобина добавляют раствор боргидрида натрия/гидроокиси натрия (имеющий концентрацию, определенную выше) в молярном соотношении боргидрата натрия и гемоглобина приблизительно 28:1. Эту полученную в результате смесь перемешивают в течение приблизительно 1 ч. Затем раствор концентрируют приблизительно до 50 л (ультрафильтр 38) и промывают 4 объемами (200 л) ВДИ. В концентрированный раствор в течение 1 ч добавляют дополнительное аликвотное количество боргидрида натрия в том же молярном соотношении, как указано выше. Полученный в результате раствор промывают 4 объемами ВДИ (200 л), приводя в результате к получению полимеризованного, пиридоксилированного, свободного от стромы гемоглобина, который подвергают тепловой обработке.
Полученный в результате раствор оксигенируют, позволяя раствору стоять в атмосфере кислорода, и затем переносят в систему очистки 42. Очистку можно достичь с помощью хроматографии на колонках, фильтрации, предпочтительно мембранной фильтрации (диафильтрации), или комбинации фильтрации и хроматографии на колонках.
В одном варианте реализации раствор переносят в сосуд подачи для хроматографии, контейнер 6, как показано на фиг.5. В этом варианте реализации полученный в результате раствор оксигемоглобина затем разводят приблизительно до 200 л (4%-ный общий гемоглобин) в контейнере 6 и концентрацию хлорида доводят до 22 мМ с помощью раствора хлорида натрия. Доведение концентрации натрия не требуется.
Затем проводят хроматографию пяти аликвотных количеств по 40 л полученного в результате раствора гемоглобина с использованием колонки 44. Колонка 44 содержит гель аффинитета, который представляет собой агарозный гель, модифицированный желтым красителем (имеющимся в продаже у Affinity Chromatography, Ltd., в виде Mimetic Yellow No.l), имеющим большее сродство к полимеру, чем к тетрамеру.
Хроматографию осуществляют следующим образом. 40 л оксигенированного, полимеризованного, пиридоксилированного, свободного от стромы раствора гемоглобина загружают в колонку 44. Колонку промывают 15 объемами колонки (750 л) водного буфера NaCl 30 мМ для удаления тетрамера. Затем колонку промывают приблизительно 250 л 300 мМ буфера хлорида натрия для отмывания полимера. Фракции полимера собирают в контейнер 7. Нежелательные фракции направляют в сток 46. После удаления каждого аликвотного количества колонку регенерируют 15 мМ раствором НСl (150 л), повторно уравновешивают 30 мМ водным NaCl (250 л) и в колонку загружают другое аликвотное количество исходного раствора (40 л). Колонку снова промывают 30 мМ Nad с последующим 300 мМ NaCl. В колонку добавляют аликвотные количества по 40 л раствора гемоглобина и проводят хроматографию до тех пор, пока контейнер 6 не опустеет.
Фракции, собранные в контейнер 7, подвергают ультрафильтрации (концентрируют) с использованием фильтра 48, связанного со стоком 50, до объема приблизительно 40 л (6% общий гемоглобин). Затем концентрированный раствор гемоглобина переносят в газообменный контейнер 8 для дезоксигенации.
Альтернативно, раствор переносят в сосуд 10 фильтрационной рециркуляции, как показано на фиг.6. Затем в контейнере 10 гемоглобин разводят приблизительно до 4% ОНb. Затем 4%-ный раствор ОНb подвергают диафильтрации с использованием 10 мМ NaCl и фильтра 52 молекулярной массы 300000, имеющегося в продаже у компании Pall-Filtron. Фильтрацию продолжают до тех пор, пока приблизительно 97% гемоглобинового материала не пройдет через фильтр и в контейнер 11. (Приблизительно 3% материала, т.е. полимеры с высокой молекулярной массой, удерживаются в контейнере 10). Количество гемоглобина определяют спектрофотометрически с использованием кооксиметра.
Полученный в результате материал в контейнере 11 представляет собой приблизительно 2-4% ОНb и содержит приблизительно 7-10% тетрамера на основании ОНb. Затем 2-4% ОНb подвергают диафильтрации с использованием 10 мM NaCl и фильтра 54 молекулярной массы 100000, имеющегося в продаже у компании Pall-Filtron, связанного со стоком или ловушкой 56. Фильтрацию продолжают до тех пор, пока уровень тетрамера, по данным определения по хроматографии с исключением по размеру с использованием колонки BioSep SEC-S3000 600•7,8 мм, не будет меньше чем 0,8% массы гемоглобина по массе. Полученный в результате очищенный раствор гемоглобина первоначально остается в контейнере 11 и затем переносят в газообменный контейнер 8 для дезоксигенации.
Газообменный контейнер 8 может быть таким же контейнером, как контейнер 4 или предпочтительно другой контейнер. Газообменный контейнер 8 оборудован по существу таким же образом, как газообменный контейнер 4 на фиг.1, и прикреплен к банке для пены 58 образом, идентичным таковому контейнера 4 и банки для пены 36. Дезоксигенацию осуществляют приблизительно через 2,5 ч барботированием азота приблизительно при 10oС и раствором с рН приблизительно 7,5. Барботирование азота продолжают до тех пор, пока в растворе остается менее чем 16% оксигемоглобина на основании массы общего гемоглобина. Затем полученный в результате раствор дезоксигемоглобина в последующем переносят в контейнер 9 для составления композиции.
В контейнере 9 для составления композиции раствор сначала концентрируют приблизительно до 7% общего гемоглобина и рН доводят приблизительно до 8,8-9,0 при 4oС. рН доводят с использованием 0,2 М NaOH. Затем в раствор гемоглобина с рН от 8,8 до 9,0 добавляют растворы электролитов. Добавляют глюкозу и глицин для достижения конечных концентраций приблизительно 5 г/л и 1,75 г/л, соответственно. Добавляют хлорид калия в раствор для получения концентрации калия приблизительно от 3,5 до 4,5 мМ. Затем добавляют 3М хлорид натрия для получения концентрации хлорида от 85 до 110 мМ. В последующем добавляют лактат натрия для получения концентрации иона натрия от 135 до 155 мМ. Наконец, добавляют 0,45 молярный раствор аскорбиновой кислоты для подъема концентрации аскорбиновой кислоты приблизительно до 1000 мг/л. В качестве консерванта/антиоксиданта для хранения добавляют аскорбиновую кислоту. Полученный в результате раствор гемоглобина имеет окончательную осмоляльность приблизительно 280-360 ммоль на кг.
Затем составленную композицию раствора гемоглобина концентрируют приблизительно до 10% общего гемоглобина с использованием фильтра 60, связанного с ловушкой 62, и 10%-ный раствор гемоглобина затем стерилизуют с помощью фильтрации фильтром 64 и в асептических условиях заливают в предварительно стерилизованные мешки.
Характеристики продукта партии А, полученного в этом примере, показаны в табл. 1. Кроме того, характеристики партии В и С, обе из которых получены в соответствии с процедурой, изложенной выше для партии А, показаны в табл. 2.
Выше было представлено подробное описание предпочтительных вариантов реализации настоящего изобретения с целью иллюстрации, а не ограничения. Следует понимать, что все другие модификации, отклонения и эквиваленты, очевидные для специалистов в этой области, основанные на этом описании, как предполагается, находятся в пределах диапазона притязаний настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| РАСТВОРЫ ПОЛИМЕРИЗОВАННОГО ГЕМОГЛОБИНА С ПОНИЖЕННЫМ КОЛИЧЕСТВОМ ТЕТРАМЕРА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2004 |
|
RU2337705C2 |
| СПОСОБ ЛЕЧЕНИЯ ПАЦИЕНТОВ С МАССИВНОЙ ПОТЕРЕЙ КРОВИ | 2003 |
|
RU2325924C2 |
| КРОВЕЗАМЕНИТЕЛЬ С ФУНКЦИЕЙ ПЕРЕНОСА КИСЛОРОДА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ) | 2008 |
|
RU2361608C1 |
| КОНЪЮГАТЫ ГЕМОГЛОБИНА С ПОЛИСАХАРИДОМ | 1999 |
|
RU2225222C2 |
| ПОЛИФУНКЦИОНАЛЬНЫЙ ПОЛИГЕМОГЛОБИН-ФЕРМЕНТНЫЙ КОМПЛЕКС | 2010 |
|
RU2432172C1 |
| СПОСОБ ПОЛУЧЕНИЯ КРОВЕЗАМЕНИТЕЛЯ И УСТАНОВКА ДЛЯ ОСУЩЕСТВЛЕНИЯ СПОСОБА | 2007 |
|
RU2341286C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ЛЕКАРСТВЕННОГО ПРЕПАРАТА, СОДЕРЖАЩЕГО ПЕРЕНОСЧИК КИСЛОРОДА, СТАБИЛЬНОГО ПРИ ВЫСОКИХ ТЕМПЕРАТУРАХ, И ЕГО ПРИМЕНЕНИЕ | 2011 |
|
RU2475252C1 |
| ПРИМЕНЕНИЕ ГЕМОГЛОБИНА ПОЛИМЕРИЗОВАННОГО ДЛЯ МОБИЛИЗАЦИИ КРОВИ ИЗ ДЕПО ПРИ КРОВОПОТЕРЯХ | 2021 |
|
RU2811253C2 |
| КРОВЕЗАМЕНИТЕЛЬ - ПЕРЕНОСЧИК КИСЛОРОДА, СОСТАВ ДЛЯ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРНОГО МОДИФИЦИРОВАННОГО ГЕМОГЛОБИНА | 1999 |
|
RU2162707C2 |
| СПОСОБ ОЧИСТКИ ГЕМОГЛОБИНА В КОММЕРЧЕСКОМ МАСШТАБЕ | 1994 |
|
RU2145873C1 |





Изобретение относится к медицине и касается заменителя эритроцитов, а также способа его получения. Сущностью изобретения является свободный от тетрамера, поперечно сшитый, полимеризованный, пиридоксимелированный раствор гемоглобина, который свободен от примесей стромы, который можно вливать людям - пациентам в количестве, доходящем приблизительно до 5 л. Способ включает удаление лейкоцитов и тромбоцитов из крови; отмывание и лизирование эритроцитов; удаление примесей стромы и стромы с помощью фильтрации и тепловой обработки; получение дезоксиформы гемоглобина; пиридоксилирование и полимеризацию; дальнейшую очистку и концентрацию; дезоксигенацию. Техническим результатом является получение заменителя гемоглобина, не токсичного для людей и имеющего значительный период полувыведения, составляющий при введении людям по меньшей мере 15 ч. 6 с. и 12 з.п. ф-лы, 2 табл., 6 ил.
| US 4826811 A, 02.05.1989 | |||
| US 5194590 A, 16.03.1993 | |||
| В П | 0 |
|
SU361720A1 |
| Устройство для выпрямления опрокинувшихся на бок и затонувших у берега судов | 1922 |
|
SU85A1 |
| LOWE K.C | |||
| Blood substitutes: Preparation, Physiology and Medical Applications | |||
| Ellis Horwood Ltd., Chichester (England), 1988, p | |||
| Торфодобывающая машина с вращающимся измельчающим орудием | 1922 |
|
SU87A1 |
| СОКОЛОВ А.В | |||
| Замещение острой смертельной кровопотери раствором фракции модифицированного полигемоглобина | |||
| Канд | |||
| дисс | |||
| - М., 1992, с | |||
| Прялка для изготовления крученой нити | 1920 |
|
SU112A1 |
| ВЯЗОВА Е.П., АЖИГИРОВА М.А | |||
| Модифицированный гемоглобин как основа искусственного переносчика кислорода | |||
| - Химико-фармацевтический журнал, 1989 г., 23 №6, с | |||
| ТУРБИНА ВНУТРЕННЕГО ГОРЕНИЯ | 1923 |
|
SU645A1 |
| БАЛАХОВСКИЙ С.Д., БАЛАХОВСКИЙ И.С | |||
| Методы химического анализа крови | |||
| - Медгиз, 1953, с | |||
| Пружинная погонялка к ткацким станкам | 1923 |
|
SU186A1 |
Авторы
Даты
2003-04-27—Публикация
1997-03-27—Подача