Изобретение относится к бензоилгуанидинам формулы I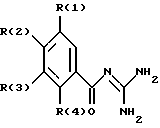
где обозначают:
R(1) - Н, F, Cl, Br, I, CN, NO2, С1-С8-алкил, С1-C8-алкокси, С3-C8-циклоалкил, С3-C8-циклоалкокси или Хa-(СН2)b-(CF2)c-СF3; Х - кислород, S, NR(5),
а - ноль или 1;
b - ноль, 1 или 2;
с - ноль, 1, 2 или 3;
R(5) - Н, С1-С4-алкил или -CdH2dR(6);
d - ноль, 1, 2, 3 или 4
R(6) - С3-C8-циклоалкил, фенил, бифенилил или нафтил,
причем фенил, бифенилил или нафтил не замещены или замещены 1-3 заместителями, выбранными из группы, состоящей из F, Cl, CF3, метила, метокси и NR(7)R(8);
R(7) и R(8) независимо друг от друга Н или С1-C4-алкил
или
R(1) - -SR(10), -OR(10) или -CR(10)R(11)R(12);
R(10) - -СfН2f-С3-C8-циклоалкил или фенил, незамещенный или замещенный 1-3 заместителями, выбранными из группы, состоящей из F, Cl, СF3, СН3, метокси, гидрокси, амино, метиламино и диметиламино,
f - ноль, 1 или 2;
R(11) и R(12) независимо друг от друга R(10), водород или С1-С4-алкил;
или
R(1) - фенил, нафтил, бифенилил или C1-C9-гетероарил, последний связан через С- или N-атом кольца, которые соответственно не замещены или замещены 1-3 заместителями, выбранными из группы, состоящей из F, Сl, СF3, метокси, гидрокси, амино, метиламино и диметиламино,
или
R(1) - -SR(13), -OR(13), -NHR(13), -NR(13)R(14), -CHR(13)R(15), -C[R(15)R(16)OH] , -C≡CR(18), -C[R(19)] = CHR(18), -C[R(20)R(21)]к-(CO)-[CR(22)R(23)]I-R(24).
к - ноль, 1, 2, 3 или 4;
I - ноль, 1, 2, 3 или 4;
R(13) и R(14) одинаковые или различные -(СН2)g-(СНОН)h-(СН2)i-(СНОН)j-R(17) или -(СН2)g-O-(CH2-CH2O)h-R(24);
R(17) - водород или метил, g, h и i одинаковые или различные ноль, 1, 2, 3 или 4,
j - 1, 2, 3 или 4;
R(15) и R(16) одинаковые или различные водород, С1-С6-алкил или вместе с соединяющим их атомом углерода образуют С3-С8-циклоалкил;
R(18) - фенил, незамещенный или замещенный 1-3 заместителями, выбранными из группы, состоящей из F, Cl, СF3, метила, метокси и NR(25)R(26);
R(25) и R(26) -
Н или С1-С4-алкил;
или
R(18) - С1-С9-гетероарил незамещенный или замещенный как фенил;
или
R(18) - С1-С6-алкил незамещенный или замещенный 1-3 ОН-группой,
или
R(18) - С3-C8-циклоалкил;
R(19), R(20), R(21), R(22) и R(23) одинаковые или различные водород или метил;
R(24) - С1-С6-алкил, C3-C8-циклоалкил или -CmH2m-R(18);
m - 1, 2, 3 или 4;
один из двух заместителей R(2) и R(3) гидроксил;
и
соответственно другой из заместителей R(2) и R(3) является R(1);
R(4) - С1-С4-алкил, С1-С4-алкокси, F, Сl, Вr, I или -(СH2)n-(CF2)o-CF3;
n - ноль или 1;
о - ноль или 1;
и к их фармацевтически приемлемым солям.
Предпочтительны соединения формулы I, в которых обозначают:
R(1) - Н, F, Cl, Вr, I, CN, NO2, С1-С8-алкил, С1-С8-алкокси, C3-C8-циклоалкил, С3-С8-циклоалкокси или Хa-(СF2)c-CF3;
Х - кислород;
а - ноль или 1;
с - ноль, 1, 2 или 3;
или
R(1) - -SR(10) или -OR(10);
R(10) - -CfН2f -C3-C8-циклоалкил или фенил, незамещенный или замещенный 1-3 заместителями, выбранными из группы, состоящей из F, Cl, CF2, СН3, метокси, гидрокси, амино, метиламино и диметиламино;
f - ноль или 1;
или
R(1) - фенил, бифенилил или С1-C9-гетероарил, последний связан через С- или N-атом кольца, которые не замещены или замещены 1-3 заместителями, выбранными из группы, состоящей из F, Cl, CF3, СН3, метокси, гидрокси, амино, метиламино и диметиламино,
или
R(1) - -SR(13), -OR(13), -NHR(13), -NR(13)R(14), -C≡CR(18) или -C[R(19)] =CHR(18);
R(13) и R(14) одинаковые или различные -(СН2)g-(СНОН)h-(СН2)i-(СНОН)j-R(17) или -(СН2)g-O-(СН2-СН2O)h-R(24);
R(17) - водород или метил, g, h и i одинаковые или различные ноль, 1 или 2;
j - 1 или 2;
R(18) - фенил, незамещенный или замещенный 1-3 заместителями, выбранными из группы, состоящей из F, Cl, СF3, метила, метокси и NR(25)R(26);
R(25) и R(26) - Н или С1-C4-алкил;
или
R(18) - С1-С9-гетероарил незамещенный или замещенный как фенил;
или
R(18) - C1-С6-алкил незамещенный или замещенный 1-3 ОН-группой,
или
R(18) - С3-С8-циклоалкил;
R(19) - водород или метил;
один из заместителей R(2) и R(3) гидроксил;
и
соответственно другой из заместителей R(2) и R(3) является
R(1);
R(4) - С1-С2-алкил, метокси, F, Cl, Br, CN или -(СН2)n-(СF2)o-СF3;
n - ноль или 1;
о - ноль или 1;
и их фармацевтически приемлемые соли.
Особенно предпочтительны соединения формулы I, в которых обозначают:
R(1) - Н, F, Cl, С1-C4-алкил, С1-С4-алкокси, С5-С6-циклоалкил, С5-С6-циклоалкокси или -Хa-(СF2)c-CF3;
Х - кислород;
а - ноль или 1;
с - ноль, 1, 2 или 3;
или
R(1) - -SR(10) или -OR(10);
R(10) - С4-C6-циклоалкил или фенил, незамещенный или замещенный 1-3 заместителями, выбранными из группы, состоящей из F, Cl, CF3, СН3, метокси, гидрокси, амино, метиламино и диметиламино;
или
R(1) - хинолил, изохинолил, пиридил, которые связаны через С- или N-атом кольца;
и которые не замещены или замещены 1-3 заместителями, выбранными из группы, состоящей из F, Cl, СF3, СН3, метокси, гидрокси, амино, метиламино и диметиламино,
или
R(1) - фенил, незамещенный или замещенный 1-3 заместителями, выбранными из группы, состоящей из F, Cl, CF3, CH3, метокси, гидрокси, амино, метиламино и диметиламино,
или
R(1) - -C≡CR(18);
R(18) - фенил или С5-С6-циклоалкил;
один из двух заместителей R(2) и R(3) гидроксил;
и соответственно другой из заместителей R(2) и R(3) является R(1);
R(4) - метил, метокси, F, Cl или СF3;
и их фармацевтически приемлемые соли.
Особенно предпочтительны соединения формулы I, в которых обозначают:
R(1) - Н, F, Cl, С1-С4-алкил, С1-C4-алкокси, С5-С6-циклоалкил, С5-С6-циклоалкокси или СF3;
один из заместителей R(2) и R(3) гидроксил,
и
соответственно другой из заместителей R(2) и R(3) является R(1);
R(4) - метил, метокси, F, Cl или CF3;
и их фармацевтически приемлемые соли.
Особенно предпочтительны соединения формулы I, выбранные из группы, состоящей из 2,6-дихлор-бензоилгуанидин-гидрохлорида, 3-хлор-2,6-диметокси-бензилгуанидин-гидрохлорида, 4-гидрокси-2,3,5,6-тетрафтор-бензоилгуанидин-гидрохлорида, 4-гидрокси-2,5-трифторметил-бензоилгуанидин-гидрохлорида и 4-гидрокси-2-метил-5-трифторметил-бензоилгуанидин-гидрохлорида.
Под С1-С9-гетероарилом имеют в виду радикалы, образованные из фенила или нафтила, в которых одна или несколько СН-групп заменены N и/или в которых, по меньшей мере, две рядом расположенные СН-группы (при образовании пятичленного ароматического кольца) заменены S, NH или О. Один или оба атома в месте конденсации бициклических остатков (как в индолизиниле) могут быть также N-атомами. В качестве С1-С9-гетероарила особенно подходят фуранил, тиенил, пирролил, имидазолил, пиразолил, триазолил, тетразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиридил, пиразинил, пиримидинил, пиридазинил, индолил, индазолил, хинолил, изохинолил, фталазинил, хиноксалинил, хиназолинил, циннолинил; особенно фуранил, тиенил, пирролил, имидазолил, пиразолил, тиазолил, триазолил, пиридил, индолил, хинолил и изохинолил.
Если один из заместителей R(1)-R(4) содержит один или несколько центров асимметрии, то они могут иметь как S-, так и R-конфигурацию. Соединения могут существовать в виде оптических изомеров, диастереомеров, рацематов или их смесей.
Названные алкильные остатки могут иметь линейную или разветвленную цепь.
Далее изобретение относится к способу получения соединения I, отличающемуся тем, что соединение формулы II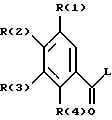
подвергают взаимодействию с гуанидином, где R(1)-R(4) имеет указанное значение и L обозначает легко замещаемую нуклеофильно остаточную группу.
Активированные производные кислоты формулы II, где L обозначает алкокси-, предпочтительно метоксигруппу, феноксигруппу, фенилтио-, метилтио-, 2-пиридилтиогруппу, азотный гетероцикл, предпочтительно 1-имидазолил, получают известным способом из хлорангидридов карбоновой кислоты (формула II, L= Сl), которые в свою очередь получают известным способом из карбоновых кислот (формула II, L=OH), например, и хлористого тионила.
Наряду с хлорангидридами карбоновой кислоты формулы II (L=Cl) можно получать также другие активированные производные кислоты формулы II известным способом непосредственно из производных бензойной кислоты (формула II, L= ОН), - сложный метиловый эфир формулы II с L=ОСН3 обрабатывают газообразной НСl в метаноле, имидазолиды формулы II обрабатывают карбонилдиимидазолом [L= 1-имидазолил, Staab, Angew. Chem. Int. Ed. Англия 1,351 367 (1962)], смешанные ангидриды II обрабатывают С1-СООС2Н5 или хлористым тозилом в присутствии триэтиламина в инертном растворителе, а также активированием бензойных кислот дициклогексилкарбодиимидом (DCC) или O-[(циано(этоксикарбонил)метилен)амино] -1,1,3,3-тетраметилуроний-тетрафторборатом ("TOTU") [Вайс и Кроммер, Chemiker Zeitimg 98, 817 (1974)]. Ряд подходящих способов получения активированных производных карбоновой кислоты формулы II указан в литературном источнике J. March, Advanced Organic Chemistry, Третье издание (John Wiley & Sons, 1985), стр. 350.
Взаимодействие активированного производного карбоновой кислоты формулы II с гуанидином происходит в протонном или апротонном, полярном, но инертном органическом растворителе. При взаимодействии сложных метиловых эфиров бензойной кислоты (II, L=ОМе) с гуанидином хорошо зарекомендовали себя метанол, изопропанол или THF от 20oС до температуры кипения этих растворителей. При большинстве превращений соединений II с бессолевым гуанидином выгодно работать в апротонных инертных растворителях, как THF, диметоксиэтан, диоксан. При использовании основания, например NaOH, в качестве растворителя при взаимодействии II с гуанидином можно применять также воду.
Если L=Cl, выгодно добавлять кислотоулавливатель, например, в форме избыточного гуанидина для связывания галоидоводородной кислоты.
Часть производных бензойной кислоты формулы II известна и описана в литературе. Неизвестные соединения формулы II можно получать известными из литературы методами. Полученные бензойные кислоты по одному из вышеописанных вариантов способа превращают до соединений I по изобретению.
Введение некоторых заместителей в 2-, 3-, 4- и 5-положении осуществляют известными из литературы методами перекрестной связи посредством палладия арилгалогенидов или арилтрифлататов, например, с органостаннанами, борорганическими кислотами или органоборанами или медьорганическими или цинкорганическими соединениями.
Бензоилгуанидины I представляют собой, в общем, слабые основания и могут связывать кислоту с образованием солей. В качестве кислых аддитивных солей применяют соли всех фармакологически приемлемых кислот, например галогениды, особенно гидрохлориды, лактаты, сульфаты, цитраты, тартраты, ацетаты, фосфаты, метилсульфонаты, р-толуолсульфонаты.
Соединения I представляют замещенные ацилгуанидины.
Соединения, подобные соединениям I, известны из европейской заявки 612 723 A I (HOE 93/F 054). Они содержат гидроксильные группы в качестве заместителей в фениловом ядре, однако заместителей в орто-положении нет.
В противоположность известным соединениям соединения по изобретению отличаются исключительно высокой эффективностью в ингибировании Na+/H+-обмена и улучшенной растворимостью в воде.
Они не имеют, как известные соединения, никаких нежелательных и отрицательных мочегонных свойств, однако очень хорошие противоаритмические свойства, имеющие важное значение для лечения заболеваний, которые возникают при явлениях гипоксии. Эти соединения вследствие своих фармакологических свойств с успехом применяются в качестве противоаритмических лекарственных средств с кардиозащитной компонентой для профилактики и лечения инфаркта, а также для лечения стенокардии, причем они также предупредительно тормозят или сильно уменьшают патофизиологические процессы при возникновении вызванных ишемией повреждений, особенно при появлении вызванных ишемией аритмий сердца. Благодаря их защищающим действиям против патологических гипоксических и ишемических ситуаций соединения по изобретению формулы I вследствие торможения клеточного Na+/Н+-механизма обмена можно применять в качестве лекарственного средства для лечения всех острых или хронических повреждений, вызванных ишемией или вызванных этим первично или вторично заболеваний. Это относится и к их применению в качестве лекарственных средств для оперативных вмешательств, например, при трансплантациях органов, причем эти соединения можно применять как для защиты органов в доноре перед или во время взятия, для защиты взятых органов, например, при лечении или при их хранении в физиологических растворах, так и при переносе в организм реципиента. Соединения представляют также ценные лекарственные средства с защитным действием при проведении ангиопластических оперативных вмешательств, например, на сердце и на периферических сосудах. В соответствии с их защитным действием против вызванных ишемией повреждений соединения применяют также в качестве лекарственных средств для лечения ишемий нервной системы, особенно центральной нервной системы, причем они пригодны, например, для лечения инсульта или отека головного мозга. Кроме того, соединения по изобретению формулы I применяют также для лечений различных форм шока, например, аллергического, кардиогенного, гиповолемического или бактериального шока.
Соединения формулы I по изобретению отличаются сильным ингибирующим действием на пролиферации клеток, например пролиферацию клеток фибробластов и на пролиферацию клеток мускулатуры сосудов. Поэтому соединения формулы I применяют как ценные терапевтические средства для заболеваний, при которых пролиферация клеток представляет первичную или вторичную причину, и поэтому их можно применять как противоатеросклеротические средства, средства против диабетических поздних осложнений, раковых заболеваний, фибромных заболеваний, как фиброз легких, фиброз печени или фиброз почек, против гипертрофии и гиперплазии органов, особенно при гиперплазии или гипертрофии предстательной железы.
Соединения по изобретению представляют эффекивные ингибиторы клеточного антиносителя натрий-протонов (Na+/H+-обмена), который при многочисленных заболеваниях (эссенциальная гипертония, атеросклероз, диабет и т.д.) повышен также в клетках, которые легко доступны для измерений, как например, в эритроцитах, тромбоцитах или лейкоцитах. Поэтому соединения по изобретению применяются как простые научные инструменты, при использовании в качестве диагностических средств для определения и распознавания определенных форм гипертонии, атеросклероза, диабета, пролиферативных заболеваний и т.д.. Кроме того, соединения формулы I пригодны для профилактической терапии для предотвращения генеза высокого кровяного давления, например эссенциальной гипертонии.
Лекарственные средства, которые содержат соединения I, можно назначать орально, парентерально, внутривенно, ректально или в виде ингаляции, причем назначение предпочтительно зависит от соответствующей клинической картины заболевания. При этом соединения I можно применять одни или вместе с галеновыми вспомогательными препаратами как в ветеринарии, так и в медицине.
Какие вспомогательные вещества применяют для рецептуры лекарственного средства, специалисту известно на основе его специальных знаний. Наряду с растворителями, гелеобразователями, основами свечей, вспомогательными веществами таблеток и другими носителями активного вещества, можно применять, например, антиоксиданты, диспергаторы, эмульгаторы, пеногасители, вещества, корригирующие неприятный вкус лекарства, консерванты, агенты растворения или красители.
Для оральной формы применения активные соединения перемешивают с подходящими для этой цели добавками, как вещества-носители, стабилизаторы или инертные растворители, и обычными методами получают подходящие формы введения, как таблетки, драже, капсулы в оболочке, водные, спиртовые или масляные растворы. В качестве инертных носителей можно применять, например, гуммиарабик, магнезию, карбонат магния, фосфат калия, молочный сахар, глюкозу или крахмал, особенно кукурузный крахмал. При этом лекарственная форма может представлять как сухой, так и влажный гранулят. В качестве маслянистых веществ-носителей или в качестве растворителей применяют, например, растительные или животные масла, как подсолнечное масло или рыбий жир.
Для подкожного или внутривенного назначения активные соединения растворяют, в случае необходимости с обычными для этой цели веществами, как агенты растворения, эмульгаторы или другие вспомогательные вещества, получают суспензию или эмульсию. В качестве растворителей применяют, например, воду, физиологический раствор хлористого натрия или спирты, например, этанол, пропанол, глицерин, растворы сахара, растворы глюкозы или маннита, или смесь из различных названных растворителей.
Для назначения в форме аэрозолей или распылителей пригодны растворы, суспензии или эмульсии активного вещества формулы I в фармацевтически не вызывающем опасений растворителе, особенно этаноле или воде, или смеси таких растворителей.
Рецептура в зависимости от использования может также содержать другие фармацевтические вспомогательные вещества, как поверхностно-активные вещества, эмульгаторы и стабилизаторы, а также парообразующий газ. Такая лекарственная форма содержит активное вещество обычно в концентрации приблизительно от 0,1 до 10, особенно приблизительно от 0,3 до 3 вес. %.
Дозировка назначаемого активного вещества формулы I и частота назначения зависят от эффективности и от продолжительности действия применяемых соединений; от вида и тяжести заболевания, а также от пола, возраста, веса и от индивидуальной предрасположенности млекопитающего, которого лечат.
В среднем, ежедневная доза соединения формулы I составляет для пациента весом около 75 кг минимально 0,001 мг/кг, предпочтительно 0,01 мг/кг, максимально до 10 мг/кг, предпочтительно 1 мг/кг веса тела. При острых вспышках заболевания, например непосредственно после перенесения инфаркта миокарда, могут потребоваться еще более высокие и более частые дозировки, например до 4 разовых доз в день. В частности, при внутривенном применении, например, у пациента с инфарктом в отделении интенсивной терапии необходимы до 200 мг в сутки.
Список сокращений:
МеОН метанол
DMF N,N-диметилформамид
ЕЕ этилацетат (EtOAc)
THF тетрагидрофуран
Экспериментальная часть.
Общая методика получения бензоил-гуанидинов (I).
Вариант А: из бензойных кислот (II, L=ОН).
1,0 экв. производного бензойной кислоты формулы II растворяют или суспендируют в безводном THF (5 мл/ммол) и затем смешивают с 1,1 экв. карбонилдиимидазола. После перемешивания более 2 часов при комнатной температуре в реакционный раствор вносят 5,0 экв. гуанидина. После перемешивания в течение ночи отгоняют THF при пониженном давлении (ротационный выпарной аппарат), смешивают с водой, устанавливают рН до 6-7 при помощи 2 н НСl и отфильтровывают соответствующий бензоилгуанидин (формула I). Полученные бензоилгуанидины обработкой водным, метаноловым или эфирным раствором соляной кислоты или другими фармакологически переносимыми кислотами можно переводить в соответствующие соли.
Общая методика получения бензоил-гуанидинов (I).
Вариант В: из сложных алкиловых эфиров бензойной кислоты (II, L=O-алкил).
1,0 экв. сложного алкилового эфира бензойной кислоты формулы II и 5,0 экв. гуанидина (свободное основание) растворяют в изопропаноле или суспендируют в THF и до полного превращения (тонкослойный контроль), нагревают до кипения (типичное время реакции от 2 до 5 часов). Растворитель отгоняют при пониженном давлении (ротационный выпарной аппарат), поглощают в ЕЕ и промывают 3 раза при помощи раствора NaHCO3. Сушат над Na2SO4, отгоняют растворитель в вакууме и хроматографируют на силикагеле с подходящим растворителем, например ЕЕ/МеОН 5:1.
(Солеобразование ср. Вариант А).
ПРИМЕР 1: 2-хлор-4-гидрокси-бензоилгуанидин-гидрохлорид. Бесцветные кристаллы.
Точка плавления 247oС
из 2-хлор-4-гидрокси-бензойной кислоты по варианту А.
ПРИМЕР 2: 2-хлор-4-гидрокси-5-йод-бензоилгуанидин-гидрохлорид. Бесцветные кристаллы.
Точка плавления 246-247oС.
Способ синтеза:
а) Сложный метиловый эфир 2-хлор-4-гидрокси-бензойной кислоты получают из 2-хлор-4-гидрокси-бензойной кислоты этерификацией с метанолом (избыток) в присутствии 10 эквивалентов хлористого ацетила в течение 24 часов при RT. После водной обработки происходит кристаллизация из простого эфира/циклогексана.
Бесцветные кристаллы.
Точка плавления 128-130oС
б) Сложный метиловый эфир 2-хлор-4-гидрокси-5-йод-бензойной кислоты получают а) реакцией со смесью 1,1 эквивалента N-хлорсукцинимида и 2,1 эквивалента йодистого калия в присутствии 10 эквивалентов ацетата натрия в полуконцентрированной ледяной уксусной кислоте при RT в течение 1,5 часа. Водная обработка и хроматография на колонке с циклогексаном/ уксусным эфиром 9:1 дает желаемый продукт в виде бесцветного твердого вещества.
Точка плавления 191-192oС.
А также сложный метиловый эфир 2-хлор-4-гидрокси-3,5-ди-йод-бензойной кислоты.
Бесцветное твердое вещество.
Точка плавления 131-132oС.
с) 2-хлор-4-гидрокси-5-йод-бензоилгуанидин-гидрохлорид из сложного метилового эфира 2-хлор-4-гидрокси-5-йод-бензойной кислоты (ср. 2б) по варианту В.
ПРИМЕР 3: 2-хлор-4-гидрокси-3,5-ди-йод-бензоилгуанидин-гидрохлорид.
Бесцветное твердое вещество.
Точка плавления 205-210oС (разложение), из сложного метилового эфира 2-хлор-4-гидрокси-3,5-ди-йод-бензойной кислоты (ср. 2 б) по способу В.
ПРИМЕР 4: 2-хлор-4-гидрокси-5-трифторметил-бензоилгуанидин-гидрохлорид. Бесцветное твердое вещество, аморфное (M+H)+ 282
Способ синтеза:
а) Сложный метиловый эфир 2-хлор-4-бензилокси-5-йод-бензойной кислоты из сложного метилового эфира 2-хлор-4-гидрокси-5-йод-бензойной кислоты реакцией с 1,1 эквивалента бензилбромида в присутствии карбоната калия в DMF при 80oС в течение 3 часов.
После водной обработки перекристаллизовывают из изопропанола,
бесцветные криссталлы,
точка плавления 102-108oС.
б) Сложный метиловый эфир 2-хлор-4-бензилокси-5-трифторметил-бензойной кислоты из 4 а) нагреванием до 160oC с 2 эквивалентами трифторацетата калия в N-метилпирролид-2-оне в присутствии йодида меди (I) в течение 5 часов. Водная обработка и хроматография на колонке с циклогексаном/уксусным эфиром 9: 1 дает бесцветные кристаллы,
точка плавления 126-127oС.
с) 2-хлор-4-бензилокси-5-трифторметил-бензоилгуанидин из 4 б) по способу В без образования соли.
Бесцветные кристаллы,
точка плавления 180oС.
d) 2-хлор-4-гидрокси-5-трифторметил-бензоилгуанидин-гидрохлорид из 4 с) гидрированием при помощи палладий/угля и последующим образованием гидрохлорида, бесцветное твердое вещество, аморфное, (М+Н)+ 282.
ПРИМЕР 5: 4-гидрокси-2,5-трифторметил-бензоилгуанидин-гидрохлорид:
бесцветные кристаллы,
точка плавления 211oС.
Способ синтеза:
а) сложный метиловый эфир 4-бензилокси-2,5-трифторметил-бензойной кислоты из 4 б) аналогичным трифторметилированием, но при повышенной температуре (180oС) и при времени реакции 5 часов,
бесцветные кристаллы,
точка плавления 116oС.
б) 4-бензилокси-2,5-трифторметил-бензоилгуанидин-гидрохлорид из 5 а) по общей инструкции,
бесцветные кристаллы,
точка плавления 221oС.
с) 4-гидрокси-2,5-трифторметил-бензоилгуанидин-гидрохлорид из 5 б) гидрированием на 10%-палладий/уголь в метаноле при RT.
ПРИМЕР 6: 4-гидрокси-2-метил-5-трифторметил-бензоилгуанидин-гидрохлорид:
Аморфное твердое вещество.
Способ синтеза:
а) Сложный метиловый эфир 2-метил-4-бензилокси-5-трифторметил-бензойной кислоты из сложного метилового эфира 2-хлор-4-бензилокси-5-трифторметил-бензойной кислоты (4 б) посредством перекрестного сочетания с 1,2 эквивалента хлористого метилцинка (из хлористого метилмагния трансметаллизацией с комплексом хлористого цинка (II) THF) перемешивают при 80oС в DMF в присутствии каталитических количеств ацетата палладия (II) и йодистой меди (I), бесцветные кристаллы,
точка плавления 105oС.
б) 4-бензилокси-2-метил-5-трифторметил-бензоилгуанидин-гидрохлорид из 6 а) по общей инструкции, бесцветные кристаллы,
точка плавления 255oС.
с) 4-гидрокси-2-метил-5-трифторметил-бензоилгуанидин-гидрохлорид из 6 б) по аналогии с 5 с).
Фармакологическиие данные:
Ингибирование Na+/H+-обмена в эритроцитах кролика.
Белые кролики из Новой Зеландии (Ivanovas) принимали стандартную диету с 2% холестерина на шесть недель для активирования Na+/H+-обмена и определения посредством пламенного фотометра Na+-приток в эритроциты при помощи Na+/H+-обмена. Кровь брали из ушных артерий и делали несвертываемой при помощи 25 международных единиц калий-гепарина. Часть каждой пробы использовали для двойного определения гематокрита центрифугированием. Аликвоты соответственно 100 мл использовали для измерения Na+-исходного содержания эритроцитов.
Чтобы определить очень чувствительный к амилориду приток натрия, 100 мкл каждого анализа крови инкубировали соответственно в 5 мл гипермолярной соль-сахароза-среды (ммол/1: 140 Nad, 3 KCl, 150 сахарозы, 0,1 убаина, 20 трис-гидроксиметил-аминометана) при рН 7,4 и 37oС. После этого эритроциты промывали 3 раза холодным, как лед, раствором MgCl2-убаин (ммол/1:112 MgCl2, 0,1 убаина) и вызывали гемолиз в 2,0 мл дистиллированной воды. Внутриклеточное содержание натрия определяли при помощи пламенного фотометра.
Na+-нетто-приток вычисляли из разности между исходными величинами натрия и содержанием натрия в эритроцитах после инкубирования. Ингибируемый амилоридом приток натрия получали из разности содержания натрия в эритроцитах после инкубирования с амилоридом и без амилорида 3•10-4 мол/л.
Таким способом действовали и в случае соединений по изобретению.
Результаты: ингибирование Na+/Н+-обмена
Пример - IС50 (мол/1)
1: - 40•10-6
2: - 0,24•10-6
3: - 0,10•l0-6
4: - 0,14•10-6е
| название | год | авторы | номер документа |
|---|---|---|---|
| ОРТОЗАМЕЩЕННЫЕ БЕНЗОИЛГУАНИДИНЫ И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 1997 |
|
RU2193025C2 |
| ОРТОЗАМЕЩЕННЫЕ БЕНЗОИЛГУАНИДИНЫ И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 1997 |
|
RU2214397C2 |
| СУЛЬФОНИМИДАМИДЫ, ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1996 |
|
RU2180658C2 |
| ЗАМЕЩЕННЫЕ БЕНЗИЛОКСИКАРБОНИЛГУАНИДИНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СРЕДСТВО, ИНГИБИРУЮЩЕЕ NA/H-ОБМЕН | 1996 |
|
RU2188191C2 |
| ЗАМЕЩЕННЫЕ ГУАНИДИДЫ ТИОФЕНИЛАЛКЕНИЛКАРБОНОВОЙ КИСЛОТЫ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 1997 |
|
RU2193033C2 |
| ЗАМЕЩЕННЫЕ ОСНОВАНИЕМ БЕНЗОИЛГУАНИДИНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ИНГИБИРОВАНИЯ КЛЕТОЧНОГО NA/H-АНТИПОРТЕРА | 1996 |
|
RU2161604C2 |
| АМИНОЗАМЕЩЕННЫЕ БЕНЗОИЛГУАНИДИНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1993 |
|
RU2085555C1 |
| ФЕНИЛЗАМЕЩЕННЫЕ ГУАНИДИДЫ АЛКЕНИЛКАРБОНОВОЙ КИСЛОТЫ И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 1997 |
|
RU2193026C2 |
| ЗАМЕЩЕННЫЕ БЕНЗОИЛГУАНИДИНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СПОСОБ ИНГИБИРОВАНИЯ И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 1995 |
|
RU2159762C2 |
| ЗАМЕЩЕННЫЕ ГУАНИДИДЫ КОРИЧНОЙ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1996 |
|
RU2190601C2 |
Изобретение относится к новым орто-замещенным бензоилгуанидинам формулы (1), где R(1) обозначает Н, галоген, Ха-(СН2)b-(CF2)с-CF3, а, b, с обозначают ноль, один из двух заместителей R(2) и R(3) обозначает гидроксил, и соответственно другой из заместителей R(2) и R(3) является R(1), R(4) обозначает С1-С4-алкил, галоген, (СН2)n-(CF2)o-CF3, n, о обозначают ноль, и их фармацевтически приемлемые соли. Лекарственное средство, обладающее ингибирующей активностью в отношении Na+/H+-обмена, содержащее соединение формулы (1) и фармацевтические добавки. Соединения формулы (1) используются для получения медикамента для лечения или профилактики инфарктов, стенокардии. Технический результат - получение новых соединений, обладающих ингибирующей активностью в отношении Na+/Н+-обмена. 2 с. и 12 з.п. ф-лы.
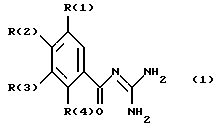
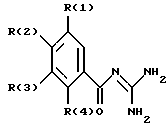
где R(1) обозначает Н, галоген, Ха-(СН2)b-(СF2)с-СF3, а, b, с обозначают ноль;
один из двух заместителей R(2) и R(3) обозначает гидроксил, и соответственно другой из заместителей R(2) и R(3) является R(1);
R(4) обозначает С1-С4-алкил, галоген, (СН2)n-(СF2)o-СF3, n, о обозначают ноль,
и их фармацевтически приемлемые соли.
| Способ получения бензоилгуанидина | 1990 |
|
SU1836338A3 |
| АМИНОЗАМЕЩЕННЫЕ БЕНЗОИЛГУАНИДИНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1993 |
|
RU2085555C1 |
| Устройство для комплектации печатной корреспонденции | 1976 |
|
SU612723A1 |
| DE 4422685 A1, 04.01.1996 | |||
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| DE 4328869 A1, 02.03.1995. | |||
Авторы
Даты
2003-09-20—Публикация
1997-03-03—Подача