Изобретение относится к клинической медицине, а конкретнее к неврологии, и может быть применено при лечении болезни Паркинсона, лекарственного паркинсонизма и травматических гиперкинезов.
Болезнь Паркинсона (БП) или "дрожательный паралич" - хроническое прогрессирующее дегенеративное заболевание головного мозга - относится к наиболее частым заболеваниям пожилого возраста. Неуклонно прогрессируя, БП приводит к инвалидизации больного. Болезнь Паркинсона составляет около 80-90% случаев синдрома паркинсонизма и является наиболее распространенной нозологической формой проявления последнего.
Паркинсонизм - клинический синдром, вызванный повреждением базальных ганглиев и обусловленный формированием нейрохимического дисбаланса (снижение уровня дофамина, увеличение количества ацетилхолина и глютамата), затрагивающего преимущественно нигростриарные нейроны. Клиническая картина БП включает четыре основных признака. Это гипо- или акинезия, ригидность, тремор покоя и постуральная нестабильность.
Гипокинезия и акинезия выражаются в снижении или полном угнетении способности к началу и продолжению движения с нормальной скоростью и угасании инициативы к осуществлению движений. Гипокинезия мышц лица приводит к гипомимии, формированию маскообразного лица, угнетению мигательного рефлекса.
Ригидность мышц вызвана повышением мышечного тонуса по пластическому типу при пассивных движениях. Нарастание мышечного тонуса в процессе исследования лежит в основе феномена "зубчатого колеса", что проявляется в ритмичных колебаниях степени ригидности.
Тремор начинается с дистальных отделов одной из конечностей, обычно руки, и усиливается при волнении; со временем тремор становится постоянным. При генерализации тремора в дрожание вовлекаются голова, нижняя челюсть, губы, язык.
В основе возникновения постуральной нестабильности лежат, в первую очередь, гипокинезия и ригидность, а также нарушение постуральных рефлексов и постурального тонуса.
Двигательные нарушения при БП могут дополняться вегетативными расстройствами и нейропсихическими нарушениями. Вегетативные расстройства более выражены на поздних стадиях заболевания и проявляются преимущественно запорами, импотенцией, нарушением терморегуляции, себорреей, потерей веса, ортостатической гипотензией. Нейропсихические нарушения на ранней стадии БП проявляются брадифренией, депрессией, сужением круга интересов, обеднением эмоциональной сферы, утратой инициативы, тревожным синдромом. На поздних стадиях болезни часто развивается деменция.
Патофизиология и биохимия БП связаны с прогрессирующей дегенерацией дофаминэргических нигростриарных нейронов и снижением тормозной функции дофаминэргической системы базальных ганглиев среднего мозга. Развивающееся повышение функциональной активности холинэргической системы и активирующих влияний на холинэргические нейроны возбудительного нейротрансмиттера глутамата усугубляют дисбаланс основных нейромедиаторов базальных ганглиев.
Этиология БП неизвестна. К факторам, способствующим дегенерации нейронов черной субстанции, относят нарушения тканевого и внутриклеточного метаболизма, в частности, митохондриального дыхания и сопряженный энергетический дефицит клеток, избыточное накопление ионов кальция, нарушение обмена железа. Эти нарушения приводят к накоплению токсичных кислородных интермедиатов, увеличение образования которых принято связывать с повышением активности моноаминоксидазы типа Б (МАО-Б) нейроглии и ускорением катаболизма дофамина.
Известен способ терапии для восстановления старческого слабоумия путем комплексного введения лечебных препаратов и витаминов (патент США 4735953, НКИ 514-313, опубл. 1988).
Недостатком терапии является сравнительно высокая токсичность препаратов, побочные эффекты холинергической природы (тремор, диарея, саливация), а также заменительный, симптоматический характер терапии, не препятствующий прогрессирующему развитию собственно болезни.
Наиболее близким из известных по своей технической сущности и достигаемому результату является выбранный в качестве прототипа способ лечебного воздействия на организм пациента при лечении болезни Паркинсона, включающий комплексный курс традиционной терапии с использованием основного фармакологически действующего вещества (Карлов В.А. Терапия нервных болезней. - М., 1996, с.406-414).
Существенным недостатком способа является длительность терапии во времени с практически непредсказуемым лечебным эффектом.
Сущность заявляемого изобретения выражается в совокупности существенных признаков, достаточных для достижения обеспечиваемого предлагаемым изобретением технического результата, выражающегося в повышении эффективности лечебного воздействия за счет компенсации функциональной недостаточности структур мозга при лечении болезни Паркинсона, лекарственного паркинсонизма и травматических гиперкинезов и нормализации симптоматического лечения экстрапирамидных и вегетативных нарушений, развивающихся при болезни Паркинсона.
Заявленная совокупность существенных признаков находится в прямой причинно-следственной связи с достигаемым результатом.
Указанный технический результат достигается тем, что в способе лечебного воздействия на организм пациента при лечении болезни Паркинсона, включающем комплексный курс традиционной терапии с использованием основного фармакологически действующего вещества, в качестве последнего используют водный раствор низкоконцентрированного пероксида водорода, который вводят вместе с фармакологическим стабилизатором, введение осуществляют эндоназально распылением, по меньшей мере, двукратным впрыском в каждый носовой ход с интервалом между аэрозольными дозами в 10-15 с от 1 до 3 раз в день, причем в качестве стабилизаторов используют водные растворы маннита, бензольной кислоты, динатриевой соли этилендиаминтетрауксусной кислоты, при этом в зависимости от состояния лечение осуществляют одним или несколькими курсами от 4-5 недель до 3-4 месяцев с перерывом до 2-3 недель.
Сравнение заявленного технического решения с прототипом позволило установить соответствие его критерию "новизна", так как оно не известно из уровня техники.
Предложенный способ является промышленно применимым существующими техническими средствами и соответствует критерию "изобретательский уровень", т. к. он явным образом не следует из уровня техники, при этом из последнего не выявлено каких-либо преобразований, характеризуемых отличительными от прототипа существенными признаками, на достижение указанного технического результата.
Таким образом, предложенное техническое решение соответствует установленным условиям патентоспособности изобретения.
Других известных технических решений аналогичного назначения с подобными существенными признаками заявителем не обнаружено.
Сущность предложенного способа лечебного воздействия на организм пациента при лечении болезни Паркинсона состоит в применении комплексного курса традиционной терапии с использованием основного фармакологически действующего вещества и введении фармакологических стабилизаторов.
В качестве основного фармакологически действующего вещества используют водный раствор низкоконцентрированного пероксида водорода с концентрацией в готовом к применению растворе 10-4 М (или 0,00034%), а в качестве фармакологических стабилизаторов используют водные растворы маннита, бензольной кислоты, динатриевой соли этилендиаминтетрауксусной кислоты (ЭДТА-Na2) необходимой концентрации, которые вводят в виде жидкости, распыляемой эндоназально из ингалятора по, меньшей мере, двукратным впрыском в каждый носовой ход с интервалом между аэрозольными дозами в 10-15 с три раза в день, обеспечивая рефлекторный характер действия.
В зависимости от состояния пациента лечение осуществляют одним или несколькими курсами от 4-5 недель до 3-4 месяцев с перерывом до 2-3 недель.
Авторами разработан лекарственный препарат, получивший название Паркон, представляющий средство, активирующее допаминэргическую систему, нарушения которой являются одной из основных причин возникновения болезни Паркинсона.
Основные известные механизмы действия Паркона обусловлены защитным и нейропротекторным действием этого лекарства. Защитное действие Паркона обусловлено активацией эндогенных механизмов защиты дофамина от разрушения, в основе которых лежит предотвращение разрушения нейромедиатора моноаминоксидазами мозга. Нейропротекторные эффекты Паркона вызваны активацией эндогенных антиокислительных систем организма, в первую очередь ферментов супероксиддисмутазы, глутатиопероксидазы, каталазы, а также восстановленного глутатиона.
Примеры. Было обследовано 19 пациентов с болезнью Паркинсона (8 мужчин и 11 женщин), которым проводилось комплексное обследование: клинико-неврологическое с определением степени тяжести заболевания по шкале Hoehn & Yahr, объективизацией выраженности имеющихся двигательных нарушений по унифицированной рейтинговой шкале UPDRS (Fahn S., Eiton S., 1987 ) и нейрофизиологическое, включающее высокочастотную транскраниальную магнитную стимуляцию rTMS и игольчатую электронейромиографию. Анализ полученных показателей проводился на стандартном IBM-совместимом компьютере с обработкой материала с помощью современных статистических программ. Все приведенные далее данные являются статистически достоверными, результаты статистической обработки представлены в виде (M(SD).
Согласно критериям включения у всех больных при обследовании были выявлены гипокинезия различной степени выраженности и наличие по меньшей мере одного из следующих симптомов: мышечная ригидность, тремор покоя 4-6 Гц, постуральная неустойчивость, не связанная со зрительной, вестибулярной, мозжечковой или проприо-цептивной дисфункцией.
Учитывая проведение магнитной стимуляции, в исследование не были включены пациенты с кардиостимуляторами или металлическими инородными телами.
Из 19 пациентов с болезнью Паркинсона 10 человек было с преимущественно дрожательной формой и 9 - с преимущественно ригидной формой.
Больные обследовались в ходе двойного слепого плацебо-контролируемого исследования.
Анализ данных в зависимости от характера получаемого вещества (паркон или плацеба) выполнялся после окончания всего исследования.
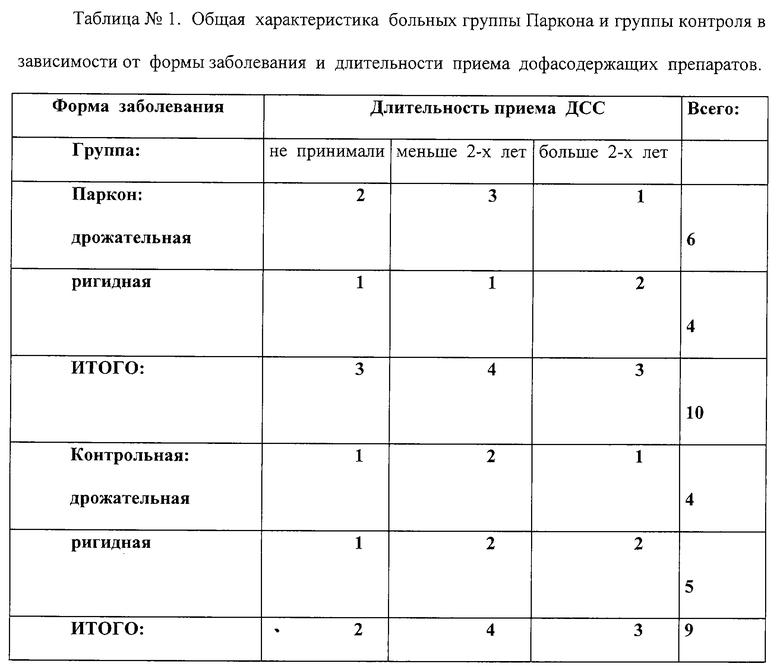
При анализе данных первую группу больных составили 10 человек, которые принимали Паркон (группа Паркона), вторую - 9 больных, получавших плацебо (контрольная группа). Группы были сопоставимы по возрасту, полу, длительности и форме заболевания. Средний возраст больных составил 60,7±9,4 года. Средняя длительность заболевания составила 4,1±2,3 года. Из 10 пациентов в группе Паркона 3 не принимали ранее ДСС, 4 больных получали дофасодержащие препараты не более 2-х лет и 3 больных принимали ДСС свыше 2-х лет. В контрольной группе 2 больных не принимали ранее дофасодержащие препараты, 4 пациентов получали ДСС до 2-х лет и 3 больных - от 2-х до 3-х лет (таблица 1). Достоверных отличий по шкале Hoehn & Yahr и UPDRS в основной и контрольной группах до лечения не выявлено. Из 6 больных с преимущественно дрожательной формой в группе Паркона 1 пациент имел стадию 1,5 по шкале Hoehn & Yahr, 4 обследуемых было со стадией 2,0 по шкале Hoehn & Yahr и у 1 больного была отмечена стадия 2,5 по шкале Hoehn & Yahr. У больных с преимущественно ригидной формой в этой группе отмечалось следующее распределение по стадиям заболевания: 3-е больных имели стадию 2,5 по шкале Hoehn & Yahr, a 1 пациент - 2,0 стадию по шкале Hoehn & Yahr. В контрольной группе из 4-х больных с дрожательной формой 2 пациента имели стадию 1,5 по шкале Hoehn & Yahr и 2 пациента - стадию 2,0 по шкале Hoehn & Yahr; у 5 больных с преимущественно ригидной формой 3 пациентов имели стадию 2,0 и 2 больных стадию 2,5 по шкале Hoehn & Yahr.
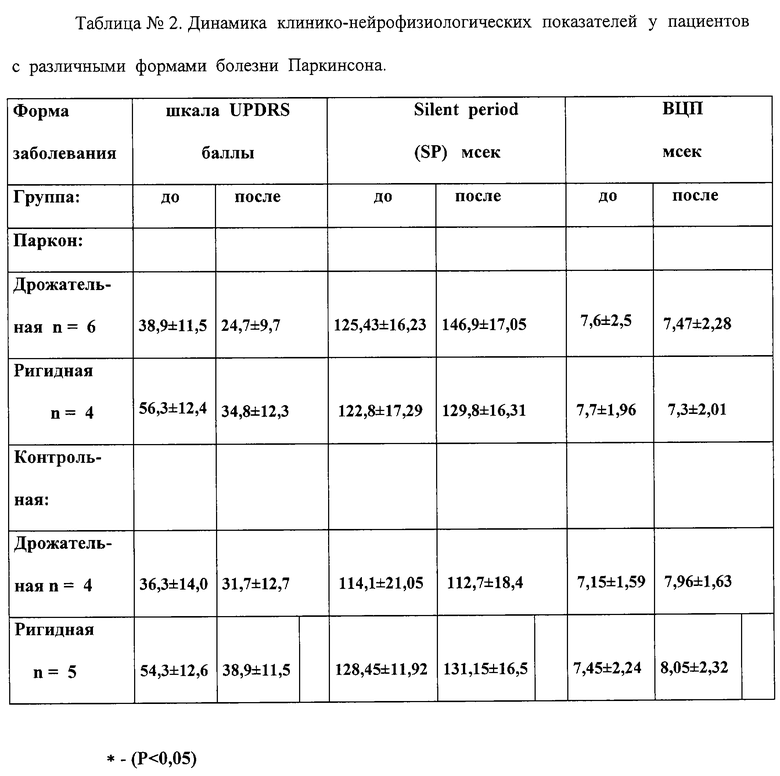
На фоне лечения Парконом ни у одного из пациентов не было ухудшений со стороны ЭКГ, не возникали нарушения ритма, артериальная гипотония и постуральных реакций, не наблюдалось психических нарушений. У всех больных отмечалась хорошая переносимость препарата. На фоне лечения препаратом у больных из группы Паркона отмечалось статистически достоверное улучшение симптоматики по шкале UPDRS. Средний балл по шкале UPDRS в группе Паркона у больных с преимущественно дрожательной формой составил до лечения 38,9±11,5 баллов, на фоне приема препарата в течение 4-х недель - 24,7±9,7 балла (Р<0,05). У больных с преимущественно ригидной формой в этой группе показатель выраженности двигательных и нейропсихологических нарушений составил 56,3±12,4 балла по шкале UPDRS, на фоне приема препарата также отмечалась статистически достоверная динамика (Р<0,05) в виде уменьшения среднего балла по шкале UPDRS до 34,8±12,8 баллов. В контрольной группе достоверного улучшения не выявлено. Общее значение по шкале UPDRS в группе больных с преимущественно дрожательной формой до лечения составило 36,3±14,0 балла, после - 31,8±12,7 балла; в группе больных с преимущественно ригидной формой средний балл по шкале UPDRS до лечения составил 54,3±12,6 балла и 45,7±14,6 балла после (таблица 2). Следует заметить, что в процессе лечения у большинства больных как основной, так и контрольной групп отмечались улучшения в эмоционально-мотивационной сфере, снижение депрессивных проявлений, что было отражено изменением соответствующих показателей первой части шкалы UPDRS. При анализе эффективности лечения Парконом у больных в зависимости от длительности приема ДСС было выявлено, что статистически достоверное клиническое улучшение наблюдается у всех больных из группы Паркона вне зависимости от давности приема ДСС.
Нейрофизиологические исследования проводились с помощью магнитного стимулятора "Maglite" и прибора "Keypoint" производства Медтроник-Дантек (США-Дания). Транскраниальная магнитная стимуляция (rTMS) применялась во всех группах больных. В нашем исследовании при проведении магнитной стимуляции ни у одного больного не было зарегистрировано побочных эффектов.
Нейрофизиологическое обследование проводилось не менее двух раз за время исследования, до начала приема препарата и после 4 недель приема.
Применялась методика транскраниальной магнитной стимуляции (Leis A.A, 1993; 1998) с исследованием периода молчания (Silent period).
Проводился количественный анализ следующих параметров: длительности периода молчания (silent period), времени центрального проведения (ВЦП) по двигательному пути. При исследовании параметров высокочастотной магнитной стимуляции (rTMS) с регистрацией Мс-ответа в группе больных с различными формами паркинсонизма сравнение проводилось с данными контрольной группы. При сравнении показателей ВЦП достоверных различий параметров у больных с преимущественно дрожательной и преимущественно ригидной формами как в контрольной, так и в основной группах не выявлено. При проведении магнитной стимуляции головного мозга ВЦП по двигательным волокнам при первом исследовании до начала лечения в группе Парконом у больных с преимущественно дрожательной формой составило 7,60±2,50 мс и после курса лечения -7,47±2,28 мс; у больных с преимущественно ригидной формой ВЦП до лечения составило 7,70±1,96 мс и 7,30±2,01 мс - после. В контрольной группе у больных с преимущественно дрожательной формой ВЦП до приема препарата составило 7,15±1,59 мс и 7,96±2,01 мс после курса лечения; в группе больных с преимущественно ригидной формой парметры ВЦП составили 7,70±1,96 мс до начала лечения и 8,05±2,32 мс после проведенного курса лечения. При анализе длительности периода молчания были обнаружены достоверные различия до и после лечения у больных из группы Паркона с преимущественно дрожательной формой заболевания.
Длительность периода молчания у больных с преимущественно дрожательной формой достоверно увеличилась на фоне приема препарата (до лечения -125,43±16,23 мс, после проведенного курса - 146,9±17,05 мс). У больных из группы Паркона с преимущественно ригидной формой статистически достоверных изменений выявлено не было. Длительность периода молчания (SP) до приема препарата составила - 122,8±17,29 мс и 129,9±16,31 - после применения Паркона.
В контрольной группе достоверных изменений длительности SP выявлено не было. (Таблица 2.)
Таким образом, у пациентов с болезнью Паркинсона (как с преимущественно дрожательными, так и с ригидными формами) на фоне лечения Парконом отмечается положительная динамика клинических симптомов, что отражено статистически достоверным (Р<0,05) уменьшением среднего суммарного балла по шкале UPDRS.
При нейрофизиологическом анализе периода молчания было выявлено увеличение его длительности на фоне применения Паркона у больных с преимущественно дрожательной формой заболевания, что позволяет объектививзировать положительную клиническую динамику в данной группе больных. Механизмы этих изменений нуждаются в дополнительном изучении и, очевидно, связаны с возможным ингибирующим влиянием Паркона на активность моноаминооксидаз, в первую очередь МАО-Б, в области базальных ганглиев и гипоталамуса с воздействием на таламокортикальные, рубро- и ретикулос-пинальные системы.
При применении плацебо динамики показателей нейрофизиологического обследования выявлено не было.
В общем случае у большинства больных с симптомокомплексом паркинсонизма отмечаются положительные сдвиги экстрапирамидальных дискинетических симтомов (тремора покоя, скованности, затруднения движений), а также неврологических, психомоторных и вегетативных симптомов (эндогенная депрессия, подавленность, нарушения речи и мимики, шум в голове, сальность лица, слюнотечение и др.).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА | 2007 |
|
RU2353382C1 |
| ПРИМЕНЕНИЕ ГЕПТАПЕПТИДА ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА И СПОСОБ ЛЕЧЕНИЯ ТАКОЙ БОЛЕЗНИ | 2011 |
|
RU2450822C1 |
| СПОСОБ РЕАБИЛИТАЦИИ БОЛЬНЫХ С БОЛЕЗНЬЮ ПАРКИНСОНА | 2010 |
|
RU2436557C1 |
| Способ диагностики центральных вестибулярных нарушений, характерных для ранней стадии болезни Паркинсона | 2017 |
|
RU2657963C1 |
| СПОСОБ ЛЕЧЕНИЯ ПАРКИНСОНИЗМА | 2008 |
|
RU2381818C2 |
| Способ прогнозирования развития когнитивных нарушений у пациентов с болезнью Паркинсона | 2024 |
|
RU2828959C1 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ БОЛЕЗНИ ПАРКИНСОНА | 2019 |
|
RU2722666C1 |
| Способ диагностики позных нарушений при болезни Паркинсона | 2020 |
|
RU2733037C1 |
| СПОСОБ РЕАБИЛИТАЦИИ БОЛЬНЫХ ПАРКИНСОНИЗМОМ | 2006 |
|
RU2315632C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА | 2008 |
|
RU2423981C2 |
Изобретение относится к области медицины, а именно к неврологии. В качестве основного фармакологически действующего вещества используют водный раствор низкоконцентрированного пероксида водорода, который вводят вместе с фармакологическим стабилизатором. Введение осуществляют эндоназально распылением, по меньшей мере, двукратным впрыскиванием в каждый носовой ход с интервалом между аэрозольными дозами в 10-15 с от 1 до 3 раз в день. При этом в качестве стабилизатора используют водные растворы маннита, бензольной кислоты, динатриевой соли этилендиаминтетрауксусной кислоты. Способ позволяет повысить эффективность лечебного воздействия. 2 з.п. ф-лы, 2 табл.
| КАРЛОВ В.А | |||
| Терапия нервных болезней | |||
| - М.: Медицина, 1987, с.321-324 | |||
| СИНЕРГИЧЕСКОЕ ЛЕЧЕНИЕ ПАРКИНСОНИЗМА | 1995 |
|
RU2176145C2 |
| СПОСОБ ЛЕЧЕНИЯ СИНДРОМА ПАРКИНСОНИЗМА | 1994 |
|
RU2057529C1 |
| СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ЭКСТРАПИРАМИДНОЙ НЕРВНОЙ СИСТЕМЫ | 2000 |
|
RU2168997C1 |
| ОДНОРЕАКТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ПЕРГОЛИДА | 1993 |
|
RU2108333C1 |
Авторы
Даты
2003-10-10—Публикация
2002-06-24—Подача