Изобретения относятся к медицине, в частности к нейрохирургии, неврологии и иммунологии, и могут найти широкое применение для прогнозирования присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы и для их профилактики.
Известно, что при черепно-мозговых травмах поражаются отделы головного мозга, осуществляющие центральную регуляцию иммуногенеза, что сказывается не только на течении посттравматического периода, но и способствует развитию инфекционно-воспалительных осложнений, которые наблюдаются у 50-80,4% больных черепно-мозговой травмы.
О тяжести состояния в динамике заболевания судят по сочетанию показателей иммунореактивности организма и концентрации в крови и ликворе токсических веществ, по показателям состояния гематоликворного и гематоэнцефалического барьеров, состоянию мозгового кровотока, выраженности гормональных нарушений, характеру и степени нарушений функций внутренних органов. Считается, что именно эти показатели наиболее полно характеризуют прогноз черепно-мозговой травмы.
В качестве средства, предупреждающего возникновение каких-либо осложнений при черепно-мозговой травме, можно рассматривать хирургическое вмешательство, которое тем эффективнее, чем оно радикальнее и раньше произведено (А. П. Ромоданова. Современные аспекты диагностики и комплексного лечения закрытой черепно-мозговой травмы в остром периоде. В журнале "Вопросы нейрохирургии им. Н.Н. Бурденко", вып. 5, 1989 г., с. 35-37).
Известен способ прогнозирования присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы, выбранный в качестве ближайшего аналога, предусматривающий определение показателя гуморального ответа крови, учитывающего наличие синдрома функциональной асимметрии в иммунном ответе при правополушарной и левополушарной локализациях очагов повреждения (В.И. Горбунов, Л. Б. Лихтерман, И.В. Ганнушкина. Иммунопатология травматической болезни головного мозга. - Ульяновск, 1996 г., с. 409-421).
Известен способ профилактики присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы, выбранный в качестве ближайшего аналога, предусматривающий проведение иммунокорригирующей терапии по результатам прогнозирования присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы (там же, с. 418-421).
В качестве показателей гуморального ответа в известном способе используются такие иммунологические показатели как Т-лимфоциты, В-лимфоциты, IgM, IgA, IgG, клеточная сенсибилизация, титры ФАЛ, титры ПМА и содержание ЦИК.
Авторами данной методики установлено, что в первые две недели острого периода отсутствует достоверная разница в динамике иммунологических показателей при полушарной латерализации очаговых повреждений мозга, хотя уже в эти сроки отмечено преимущественное нарушение показателей клеточного иммунитета при левосторонних поражениях и преобладание аутоиммунных процессов при правосторонних.
На третьей неделе, когда выраженность иммунного ответа становится максимальной, разница в клеточно-опосредованном и аутоиммунном звене иммунитета становится по многим параметрам достоверно (Р<0,05) зависимой от полушарной латерализации повреждений мозга. Статистически достоверно (Р<0,05) ниже уровень Т-, В-лимфоцитов и Тc при травме левого полушария.
Статистически достоверно (Р<0,05) выше выработка ПМА при травме правого полушария.
Таким образом, на третьей неделе травматического периода можно говорить о иммунологическом синдроме функциональной асимметрии в иммунном ответе, который обусловлен латерализацией очагового повреждения мозга, по которому возможно прогнозирование осложнений в остром и последствий в отдаленном периоде черепно-мозговой травмы.
Знание особенностей очагового повреждения мозга позволяет рекомендовать иммунокорригирующую терапию с профилактической целью, не ожидая развития осложнений.
В качестве средства для иммунокорригирующей терапии рекомендованы для левополушарной локализации очага повреждения L-dopa, для правополушарной локализации - L-глютаминовая кислота.
Как видно, прогноз присоединения воспалительного осложнения согласно известной методике можно сделать только на 3-й неделе после получения черепно-мозговой травмы, что делает его малоэффективным, поскольку развитие воспалительных осложнений начинается, как правило, с 4-х суток после возникновения черепно-мозговой травмы.
Кроме того, при использовании препаратов, рекомендованных при профилактике для иммунокорригирующей терапии по известному способу, в частности L-dopa, по мнению многих авторов наблюдается регресс симптомов, регулируемых левым полушарием, и некоторое нарастание проявления дисфункций со стороны правого полушария. Не является секретом и значительно выраженные побочные явления при их применении.
Таким образом, техническими результатами, на решение которых направлены данные изобретения, являются повышение эффективности способа прогнозирования присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы и повышение эффективности профилактики их присоединения в остром периоде черепно-мозговой травмы.
Указанные технические результаты достигаются тем, что в известном способе прогнозирования присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы, предусматривающем определение показателя гумморального ответа крови, учитывающего наличие синдрома функциональной асимметрии в иммунном ответе при правополушарной и левополушарной локализациях очагов повреждения, согласно изобретению дополнительно предусматривают определение показателя гумморального ответа ликвора больного, также учитывающего наличие синдрома функциональной асимметрии в иммунном ответе при правополушарной и левополушарной локализациях очагов повреждения, при этом в качестве показателя гумморального ответа крови и ликвора используют цитокиновый ответ провоспалительного интерлейкина 1-β и присоединение воспалительного осложнения при правополушарной и левополушарной локализации очагов повреждения прогнозируют с 1 по 14 сутки после возникновения черепно-мозговой травмы при следующих значениях этого показателя в крови и ликворе, при правополушарной локализации очага повреждения:
- в крови: свыше 350 пг/мл, а также менее 150 пг/мл в 1-3 сутки, свыше 150 пг/мл в 4-7 сутки и свыше 62 пг/мл в 8-14 сутки;
- в ликворе: свыше 80 пг/мл, а также менее 30 пг/мл в 1-3 сутки, свыше 71 пг/мл в 4-7 сутки и при отсутствии нормализации его значений к концу 8-14 суток,
а при левополушарной локализации очага повреждении:
- в крови: свыше 200 пг/мл, а также менее 40 пг/мл в 1-3 сутки, свыше 240 пг/мл в 4-7 сутки и свыше 120 пг/мл в 8-14 сутки;
- в ликворе: свыше 17 пг/мл, а также менее 5 пг/мл в 1-3 сутки, свыше 48 пг/мл в 4-7 сутки и отсутствии нормализации его значений к концу 8-14 суток.
Указанные технические результаты достигаются тем, что в известном способе профилактики присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы, предусматривающем проведение иммунокорригирующей терапии по результатам прогнозирования присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы, согласно изобретению она проводится с 4-х - 14-х суток после возникновения черепно-мозговой травмы при всех значениях показателя, исследуемого при прогнозировании присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы - провоспалительного интерлейкина-1β - в крови и ликворе кроме значений в 1-3 сутки после возникновения черепно-мозговой травмы для правополушарной локализации очага повреждения - в крови свыше 350 пг/мл и в ликворе свыше 80 пг/мл, а для левополушарной локализации очага повреждения - в крови свыше 200 пг/мл и в ликворе свыше 17 пг/мл, при этом вводят больному иммуностимулирующее средство - беталейкин (рекомбинантный IL-1β) - ежедневно в течение 7 дней по 5 нг/кг внутривенно капельно в 200 мл физиологического раствора для регуляции выработки провоспалительного цитокина интерлейкина -1β или контактно воздействуют иммуномодулирующим низкоинтенсивным лазерным излучением с длиной волны 0,89 мкм на сонные и позвоночные артерии с двух сторон, на проекции правого и левого надпочечников, решетчатой кости и сосцевидного отростка со стороны повреждения при следующих режимах воздействия:
- на сонные артерии - ежедневно, в течение 10 дней по 1-3 минуты на каждую излучением с частотой импульса 1500-3000 Гц и мощностью в импульсе 5-10 Вт;
- на позвоночные артерии - ежедневно, в течение 10 дней по 1,5-3 минуты на каждую излучением с частотой импульса 80-150 Гц и мощностью в импульсе 5-10 Вт;
- на проекции правого и левого надпочечников - ежедневно, в течение 5-7 дней по 1-2 минуты на каждую, излучением с частотой импульса 80-150 Гц и мощностью в импульсе 3-7 Вт;
- на проекцию решетчатой кости - ежедневно, в течение 5-7 дней длительностью 5 минут с частотой импульса 1500-3000 Гц и мощностью в импульсе 3-7 Вт;
- на проекцию сосцевидного отростка - ежедневно, в течение 5-7 дней по 3-5 минут с частотой импульса 1500-3000 Гц и мощностью в импульсе 3-7 Вт.
Авторами экспериментально установлено, что именно одновременное определение показателя гумморального ответа ликвора и крови больного - цитокинового ответа провоспалительного интерлейкина-1β, учитывающего наличие синдрома функциональной асимметрии в иммунном ответе при правополушарной и левополушарной локализациях очагов повреждения позволяет достоверно (Р<0,05) установить факт присоединения воспалительного осложнения, причем на ранней стадии, что значительно повышает эффективность способа.
Авторами также экспериментально выявлены значения данного показателя в 1-14 сутки после возникновения черепно-мозговой травмы, позволяющие достоверно (Р<0,05), на ранней стадии и эффективно устанавливать факт присоединения воспалительного осложнения.
Авторами экспериментально установлено, что назначение профилактических мероприятий с 4-х - 14-х суток после возникновения черепно-мозговой травмы при всех значениях показателя, исследуемого при прогнозировании присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы - провоспалительного интерлейкина -1β, кроме его значений в 1-3 сутки для правополушарной локализации очага повреждения - в крови свыше 350 пг/мл и в ликворе свыше 80 пг/мл и для левополушарной локализации очага повреждения - в крови свыше 200 пг/мл и в ликворе свыше 17 пг/мл, позволило значительно снизить процент присоединяемых воспалительных осложнений, что свидетельствует об эффективности способа.
Исключение из значений исследуемого показателя значений, полученных в 1-3 сутки после возникновения черепно-мозговой травмы, объясняется тем, что в этот период требуется проведение не профилактических мероприятий, а лечебных, причем не связанных с регуляцией выработки провоспалительного цитокина интерлейкина-1β.
Авторами также экспериментально установлено, что наилучших результатов профилактических мероприятий удается достичь именно регулируя выработку у больного провоспалительного цитокина интерлейкина-1β, что обеспечивается при введении больному либо иммуностимулирующего средства - беталейкина (рекомбинантного IL-1β) либо иммуномодулирующим контактным воздействием низкоинтенсивным лазерным излучением в заявляемых режимах на заявляемые области.
По мнению авторов, это объясняется тем, что именно цитокины, представляющие собой группу полипептидов или белковых медиаторов, участвующих в формировании и регуляции воспаления и иммунного ответа, являются первичными регуляторами воспалительного процесса, определяющими направленность иммунного ответа.
По мнению авторов, низкая скорость выработки нейрорегулирующих провоспалительных пептидов (IL-1β) снижает эффективность борьбы с чужеродным, что грозит хроническим, затяжным или прогредиентным течением заболевания. Патология нейроиммунорегуляции повышает восприимчивость к патогенному действию различных факторов вторичного иммунодефицитного состояния. Как следствие иммунологическая недостаточность и угнетение механизмов неспецифической противоинфекционой защиты формирует предрасположенность к инфекциям, которая может реализовываться тяжелыми осложнениями воспалительного характера.
Эффективность проведения профилактических мероприятий заявляемым способом - именно введение больному беталейкина (рекомбинантного-1β) по заявляемой схеме или иммуномодулирующее контактное воздействие низкоинтенсивным лазерным излучением по заявляемой схеме, по мнению авторов, объясняется тем, что именно эти мероприятия способствую эффективной регуляции выработки нейрорегуляторного провоспалительного пептида цитокина IL-1β, который повышает устойчивость к патогенному действию различных факторов иммунодефицитного состояния, развивающегося в острый период черепно-мозговой травмы, определяет направленность иммунного ответа на скорейшую ликвидацию иммунодефицитного состояния.
Кроме того известно, что именно низкоинтенсивное лазерное излучение способствует повышению сопротивляемости организма, оказывает иммуномодулирующее действие.
В связи с тем, что в патогенезе черепно-мозговой травмы среди многочисленных факторов, отражающихся на формировании и клиническом течении как острого, так и отдаленного периода черепно-мозговой травмы, доминирующее значение имеет сосудистый фактор, а сонные и позвоночные артерии являются основными магистральными сосудами, снабжающими головной мозг, воздействие низкоинтенсивным лазерным излучением именно на сонные и позвоночные артерии с двух сторон способствует значительной стимуляции восстановительных процессов и как следствие затуханию патологического процесса.
При воздействии низкоинтенсивным лазерным излучением на позвоночные артерии, проекции правого и левого надпочечников, решетчатой кости и сосцевидного отростка со стороны повреждения, локализация которых совпадает с анатомической проекцией структур головного мозга, наблюдаются функциональные изменения соответствующей области коры большого мозга, где имеют представительство различные функции организма пациента, которые также способствуют затуханию патологического процесса.
Способ прогнозирования присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы осуществляется следующим образом.
У больного с черепно-мозговой травмой в остром периоде осуществляют забор крови и ликвора. Забор ликвора осуществляют традиционным методом во время люмбальной пункции. Забор крови осуществляют из периферической вены обычной методикой. После предварительного центрифугирования, в крови и ликворе хемилюминесцентным методом на автоматическом хемилюминесцентном анализаторе IMMULITE DRC (компания Diagnostic Prodact Соrp. (США) или иммуноферментным "сэндвич" методом с помощью иммуноферментного набора CYTELISA, определяют количество провоспалительных цитокинов интерлейкина-1β в 1-14 сутки после возникновения черепно-мозговой травмы.
По результатам данного исследования у больного прогнозируют или не прогнозируют присоединение воспалительного осложнения в зависимости от локализации (правополушарной или левополушарной) черепно-мозговой травмы. Присоединение воспалительного осложнения при правополушарной локализации очага повреждения прогнозируют при следующих значениях провоспалительного цитокина интерлейкина-1β в крови: свыше 350 пг/мл, а также менее 150 пг/мл в 1-3 сутки после возникновения черепно-мозговой травмы, свыше 150 пг/мл в 4-7 сутки и свыше 62 пг/мл в 8-14 сутки и ликворе: свыше 80 пг/мл, а также менее 30 пг/мл в 1-3 сутки, свыше 71 пг/мл в 4-7 сутки и отсутствии нормализации его значений к концу 8-14 суток, т.е. при значениях свыше 12 пг/мл.
Присоединение воспалительных осложнений при левополушарной локализации очага повреждения прогнозируют при следующих значениях провоспалительного цитокина интерлейкина-1β в крови: свыше 200 пг/мл, а также менее 40 пг/мл в 1-3 сутки после возникновения черпно-мозговой травмы, свыше 240 пг/мл в 4-7 сутки и свыше 120 пг/мл в 8-14 сутки и ликворе: свыше 17 пг/мл, а также менее 5 пг/мл в 1-3 сутки, свыше 48 пг/мл в 4-7 сутки и отсутствии нормализации его значений к концу 8-14 суток, т.е. при значениях его в этот промежуток времени свыше 12 пг/мл.
Способ профилактики присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы осуществляют следующим образом.
При прогнозе присоединения воспалительных осложнений их профилактику начинают проводить с 4-х - 14-х суток после возникновения черепно-мозговой травмы. Профилактика присоединения воспалительных осложнений для значений показателя, исследуемого при прогнозировании присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы, - провоспалительного интерлейкина-1β в 1-3 сутки после возникновения черепно-мозговой травмы для правополушарной локализации очага повреждения - в крови свыше 350 пг/мл и в ликворе свыше 80 пг/мл и для левополушарной локализации очага повреждения - в крови свыше 200 пг/мл и в ликворе свыше 17 пг/мл не проводится, поскольку с 1-х по 3-и сутки после возникновения черепно-мозговой травмы проводят интенсивную терапию, не предусматривающую регуляцию выработки провоспалительного цитокина интерлейкина-1β.
Профилактические мероприятия при всех остальных значениях исследуемого показателя направлены на регуляцию выработки (восполнение дефицита выработки или снижения выработки) провоспалительного цитокина интерлейкина-1β, которое осуществляют либо введением больному иммуностимулирующего средства - беталейкина (рекомбинантного IL-1β) ежедневно в течение 7 дней в количестве 5 нг/кг внутривенно капельно в 200 мл физиологического раствора (восполнение дефицита выработки), либо иммуномодулирующим (стимуляция или снижение выработки собственного провоспалительного цитокина интерлейкина-1β) контактным воздействием низкоинтенсивным лазерным излучением с длиной волны 0,89 мкм на сонные и позвоночные артерии с двух сторон, на проекции правого и левого надпочечников, решетчатой кости и сосцевидного отростка со стороны повреждения, при следующих режимах воздействия:
- на сонные артерии - ежедневно, в течение 10 дней по 1-3 минуты на каждую за один сеанс излучением с частотой импульса 1500-3000 Гц и мощностью в импульсе 5-10 Вт;
- на позвоночные артерии - ежедневно, в течение 10 дней по 1,5-3 минуты на каждую за один сеанс излучением с частотой импульса 80-150 Гц и мощностью в импульсе 5-10 Вт;
- на проекции правого и левого надпочечников - ежедневно, в течение 5-7 дней по 1-2 минуты на каждую за один сеанс излучением с частотой импульса 80-150 Гц и мощностью в импульсе 3-7 Вт:
- на проекцию решетчатой кости - ежедневно, в течение 5-7 дней по 5 минут за один сеанс с частотой импульса 1500-3000 Гц и мощностью в импульсе 3-7 Вт;
- на проекцию сосцевидного отростка - ежедневно, в течение 5-7 дней по 3-5 минут за один сеанс с частотой импульса 1500-3000 Гц и мощностью в импульсе 3-7 Вт.
Согласно заявляемой методике присоединение воспалительных осложнений прогнозируется задолго до появления общеизвестных признаков данного осложнения. Спустя несколько дней данные прогнозы подтверждаются, в частности с помощью рентгенограмм или с помощью компьютерной томографии а также традиционными лабораторными методами и клинически.
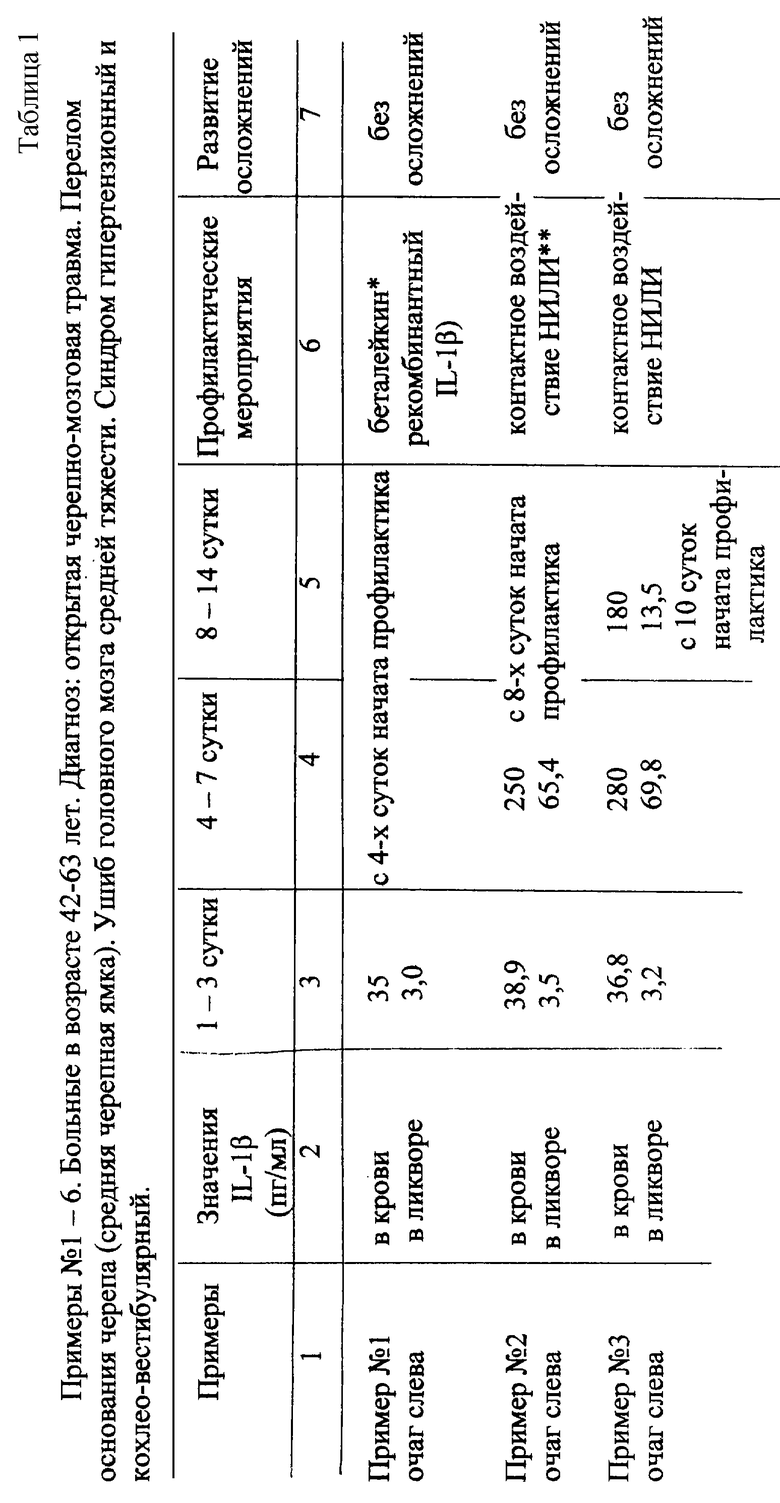
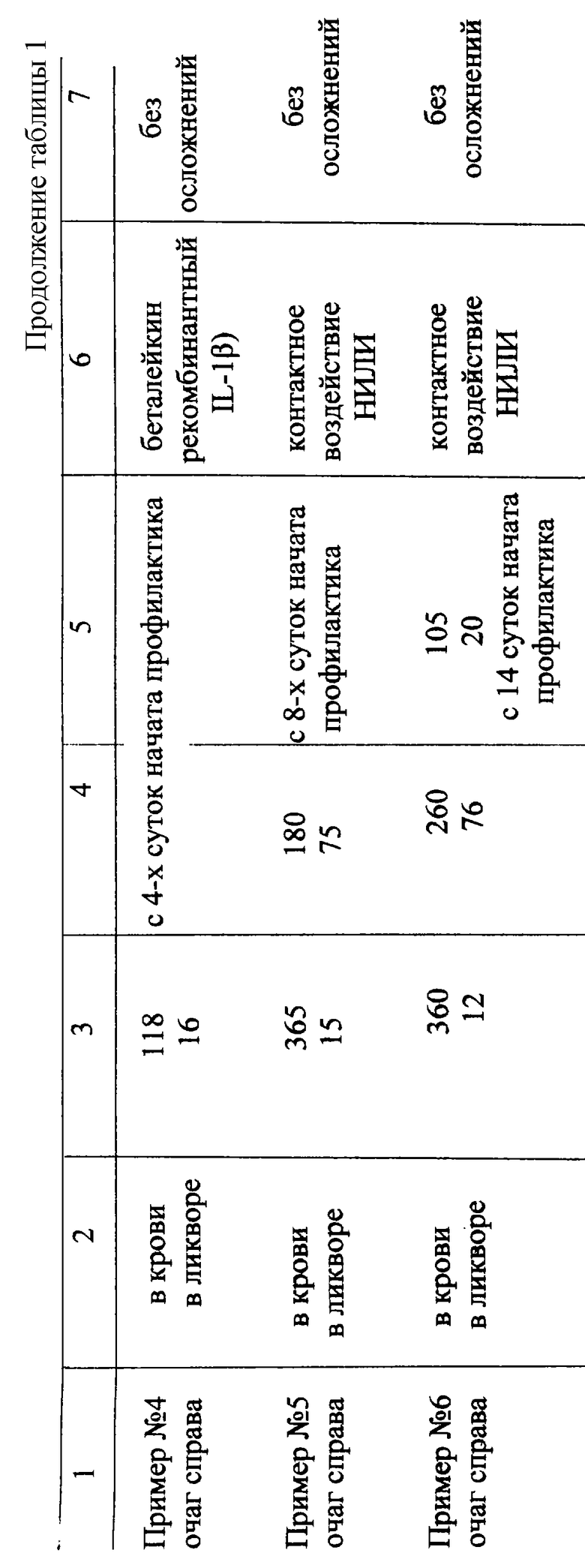
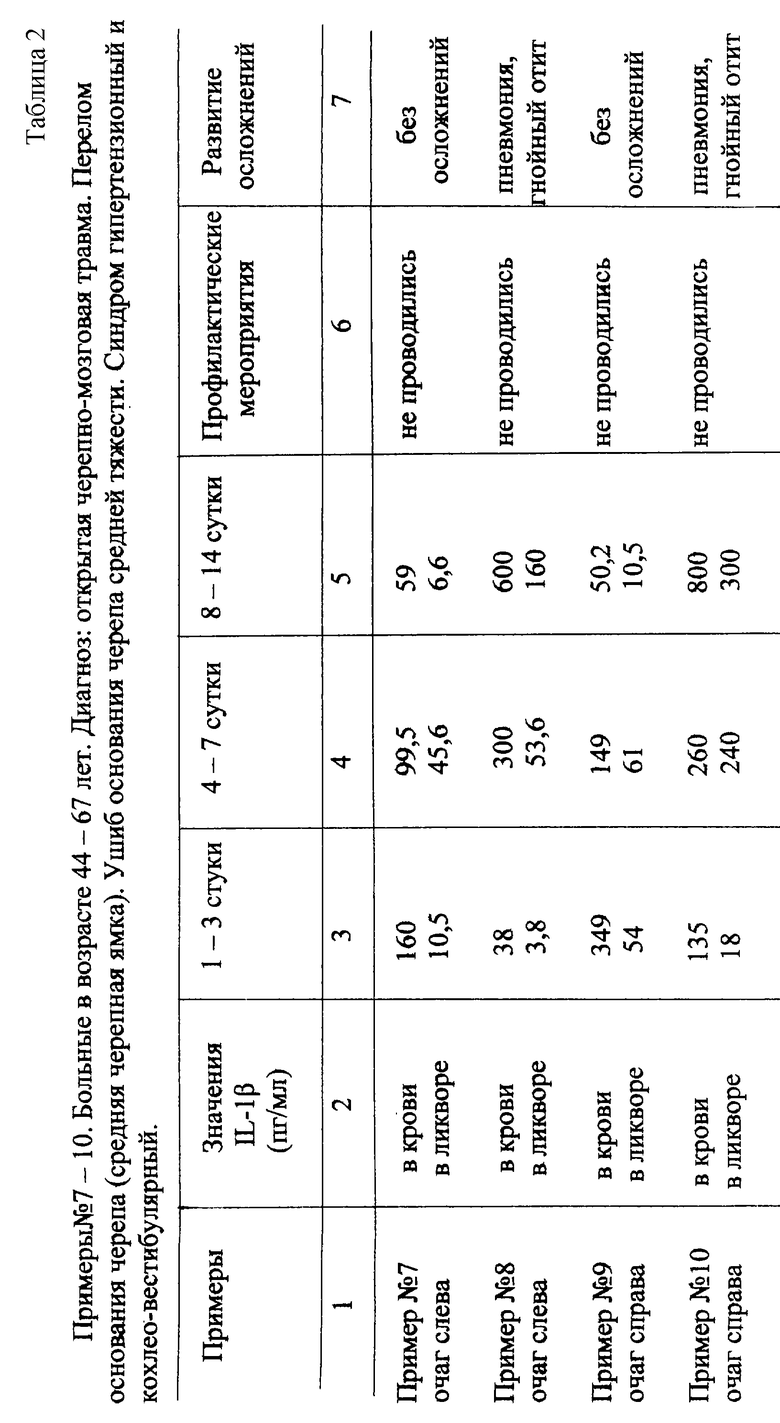
Заявляемый способ подтвержден примерами, сведенными в таблицы 1 и 2.
В таблице 1 представлены примеры, подтверждающие заявляемый способ, в таблице 2 - контрольные примеры, в частности примеры 7 и 9 таблицы 2 приведены для случаев, когда исследуемые показатели у больных отличны от заявляемых, т.е. когда воспалительные осложнения не присоединяются, а примеры 8 и 10 - для случаев, когда при значениях исследуемых показателей, прогнозирующих присоединение воспалительного осложнения, больным по ряду причин не проводились профилактические мероприятия.
Примечание:
1. При значениях цитокинового ответа провоспалительного цитокина интерлейкина-1β(IL-1β) в 1-3 сутки (таблица 1) для правополушарной локализации свыше 350 пг/мл в крови и свыше 80 пг/мл в ликворе и для левополушарной локализации в крови свыше 200 пг/мл и ликворе свыше 17 пг/мл с 1-х суток после возникновения черепно-мозговой травмы прогнозируется (диагностируется) присоединение воспалительных осложнений, для лечения которых терапия НИЛИ и беталейкином не применяется (Р<0,05).
2. * - профилактика присоединения воспалительного осложнения в острый период черепно-мозговой травмы предусматривает введение больному иммуностимулирующего средства - беталейкина (рекомбинантного-1β) ежедневно в течение 7 дней в количестве за одно введение 5 нг на 1 кг массы больного внутривенно капельно в 200 мл физиологического раствора.
3. ** - режимы контактного воздействия иммуномодулирующего низкоинтенсивного лазерного излучения (НИЛИ) по заявляемой схеме для примеров 2, 3, 5 и 6.
Пример 2.
- на сонные артерии - ежедневно, в течение 10 дней по 1 минуте на каждую излучением с частотой импульса 3000 Гц и мощностью в импульсе 5 Вт;
- на позвоночные артерии - ежедневно, в течение 10 дней по 1,5 минут на каждую излучением с частотой импульса 150 Гц и мощностью в импульсе 5 Вт;
- на проекции правого и левого надпочечников - ежедневно, в течение 5 дней по 1 минуте на каждую излучением с частотой импульса 150 Гц и мощностью в импульсе 3 Вт;
- на проекцию решетчатой кости - ежедневно в течение 5 дней по 5 минут с частотой импульса 3000 Гц и мощностью в импульсе 3 Вт;
- на проекцию сосцевидного отростка - ежедневно в течение 5 дней по 3 минуты с частотой импульса 3000 Гц и мощностью в импульсе 3 Вт.
Пример 3. Схема воздействия ПИЛИ согласно примеру 2. Исключение составляют режимы излучения и время воздействия:
- на сонные артерии - по 3 минуты на каждую излучением с частотой импульса 1500 Гц, мощность в импульсе 10 Вт;
- на позвоночные артерии - по 3 минуты на каждую излучением с частотой импульса 80 Гц и мощностью в импульсе 10 Вт;
- на проекции правого и левого надпочечников в течение 7 дней по 1 минуте на каждую излучением с частотой импульса 80 Гц и мощностью в импульсе 7 Вт;
- на проекцию решетчатой кости, ежедневно в течение 7 дней с частотой импульса 1500 Гц и мощностью в импульсе 7 Вт;
- на проекцию сосцевидного отростка, в течение 7 дней по 3 минуты с частотой импульса 1500 Гц и мощностью в импульсе 7 Вт.
Пример 5. Схема и режимы воздействия НИЛИ согласно примеру 2 за исключением режимов воздействия на проекции правого и левого надпочечников, которые составляют: ежедневно в течение 7 дней по 2 минуты на каждую излучением с частотой импульса 80 Гц и мощностью в импульсе 5 Вт.
Пример 6. Схема и режимы воздействия НИЛИ согласно примеру 2 за исключением режимов воздействия на проекцию решетчатой кости, которые составляют: в течение 5 дней по 5 минут с частотой импульса 3000 Гц и мощностью в импульсе 5 Вт.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛАЗЕРНОЙ ТЕРАПИИ ЧЕРЕПНО-МОЗГОВОЙ ТРАВМЫ С ПЕРЕЛОМОМ ОСНОВАНИЯ ЧЕРЕПА | 2002 |
|
RU2207173C1 |
| СПОСОБ ДИАГНОСТИКИ СТЕПЕНИ ТЯЖЕСТИ И ТЕЧЕНИЯ ЧЕРЕПНО-МОЗГОВОЙ ТРАВМЫ | 2002 |
|
RU2213967C1 |
| СПОСОБ ЛАЗЕРНОЙ ТЕРАПИИ ЧЕРЕПНО-МОЗГОВОЙ ТРАВМЫ У БОЛЬНЫХ ПОЖИЛОГО И СТАРЧЕСКОГО ВОЗРАСТА | 2002 |
|
RU2207172C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ТРАВМАТИЧЕСКОЙ БОЛЕЗНИ ГОЛОВНОГО МОЗГА | 2010 |
|
RU2426992C1 |
| СПОСОБ ЛАЗЕРНОГО ГЕМОСТАЗА ПОЛОСТИ УДАЛЕННОЙ ВНУТРИМОЗГОВОЙ ГЕМАТОМЫ | 2002 |
|
RU2212915C1 |
| СПОСОБ ЛЕЧЕНИЯ РОЖИ | 2012 |
|
RU2502530C1 |
| СТЕРЕОТАКСИЧЕСКИЙ СПОСОБ ЛОКАЛЬНОЙ ДЕСТРУКЦИИ ФУНКЦИОНАЛЬНО ЗНАЧИМЫХ СТРУКТУР ГОЛОВНОГО МОЗГА | 2000 |
|
RU2164787C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ КОЛОТО-РЕЗАНЫХ ПОВРЕЖДЕНИЙ ПАРЕНХИМАТОЗНЫХ ОРГАНОВ | 1999 |
|
RU2151567C1 |
| СПОСОБ АЛЛОНЕЙРОПЛАСТИКИ С ПОМОЩЬЮ ОЧИЩЕННОГО АЛЛОТРАНСПЛАНТАТА | 2000 |
|
RU2164780C1 |
| СПОСОБ БЕСШОВНОГО СОЕДИНЕНИЯ ТКАНЕЙ РАНЫ ПРИ КОЖНО-ПЛАСТИЧЕСКИХ ОПЕРАЦИЯХ | 2000 |
|
RU2162298C1 |
Изобретение относится к области медицины, в частности к нейрохирургии, неврологии и иммунологии. Технический результат заключается в повышении эффективности способа прогнозирования присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы и повышение эффективности их профилактики. Проводят определение показателя гумморального ответа крови, учитывающего наличие синдрома функциональной асимметрии в иммунном ответе при правополушарной и левополушарной локализации очагов повреждения. При этом дополнительно проводят определение показателя гумморального ответа ликвора больного, также учитывающего наличие синдрома функциональной асимметрии в иммунном ответе при правополушарной и левополушарной локализациях очагов повреждения, при этом в качестве показателя гумморального ответа крови и ликвора используют цитокиновый ответ провоспалительного цитокина интерлейкина-1β и присоединение воспалительного осложнения при правополушарной и левополушарной локализации очагов повреждения прогнозируют с 1 по 14 сутки после возникновения черепно-мозговой травмы при следующих значениях этого показателя в крови и ликворе, при правополушарной локализации очага повреждения: в крови - свыше 350 пг/мл, а также менее 150 пг/мл в 1-3 сутки, свыше 150 пг/мл в 4-7 сутки и свыше 62 пг/мл в 8-14 сутки; в ликворе - свыше 80 пг/мл, а также менее 30 пг/мл в 1-3 сутки, свыше 71 пг/мл в 4-7 сутки и при отсутствии нормализации его значений к концу 8-14 суток, а при левополушарной локализации очага повреждения: в крови - свыше 200 пг/мл, а также менее 40 пг/мл в 1-3 сутки, свыше 240 пг/мл в 4-7 сутки и свыше 120 пг/мл в 8-14 сутки; в ликворе - свыше 17 пг/мл, а также менее 5 пг/мл в 1-3 сутки, свыше 48 пг/мл в 4-7 сутки и отсутствии нормализации его значений к концу 8-14 суток. Для профилактики присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы проводят иммунокорригирующую терапию по результатам прогнозирования присоединения воспалительных осложнении в остром периоде черепно-мозговой травмы, при этом она проводится с 4-х - 14-х суток после возникновения черепно-мозговой травмы при всех значениях показателя, исследуемого при прогнозировании присоединения воспалительных осложнений в остром периоде черепно-мозговой травмы - провоспалительного интерлейкина-1β - в крови и ликворе, кроме значений в 1-3 сутки после возникновения черепно-мозговой травмы для правополушарной локализации очага повреждения - в крови - свыше 350 пг/мл и в ликворе - свыше 80 пг/мл, а для левополушарной локализации очага повреждения - в крови - свыше 200 пг/мл и в ликворе - свыше 17 пг/мл, при этом вводят больному иммуностимулирующее средство - беталейкин (рекомбинантный IL-1β) ежедневно в течение 7 дней по 5 нг/кг внутривенно капельно в 200 мл физиологического раствора для регуляции выработки провоспалительного цитокина интерлейкина-1β или контактно воздействуют иммуномодулирующим низкоинтенсивным лазерным излучением с длиной волны 0,89 мкм на сонные и позвоночные артерии с двух сторон, на проекции правого и левого надпочечников, решетчатой кости и сосцевидного отростка со стороны повреждения, при следующих режимах воздействия: на сонные артерии - ежедневно, в течение 10 дней по 1-3 мин на каждую излучением с частотой импульса 1500-3000 Гц и мощностью в импульсе 5-10 Вт; на позвоночные артерии - ежедневно, в течение 10 дней по 5-3 мин на каждую излучением с частотой импульса 80-150 Гц и мощностью в импульсе 5-10 Вт; на проекции правого и левого надпочечников - ежедневно, в течение 5-7 дней по 1-2 мин на каждую излучением с частотой импульса 80-150 Гц и мощностью в импульсе 3-7 Вт; на проекцию решетчатой кости - ежедневно, в течение 5-7 дней по 5 мин с частотой импульса 1500-3000 Гц и мощностью в импульсе 3-7 Вт; на проекцию сосцевидного отростка - ежедневно, в течение 5-7 по 3-5 мин с частотой импульса 1500-3000 Гц и мощностью в импульсе 3-7 Вт. 2 c.п.ф-лы, 2 табл.
| ГОРБУНОВ В.И | |||
| и др | |||
| Иммунопатология травматической болезни головного мозга | |||
| - Ульяновск, 1996, с.409-421 | |||
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ РЕСПИРАТОРНОГО ДИСТРЕСС-СИНДРОМА ВЗРОСЛЫХ ПРИ ТЯЖЕЛОЙ ЧЕРЕПНО-МОЗГОВОЙ ИЗОЛИРОВАННОЙ ТРАВМЕ | 1993 |
|
RU2085947C1 |
| СПОСОБ ДИАГНОСТИКИ ЛИКВОРЕИ ПРИ ЧЕРЕПНО-МОЗГОВОЙ ТРАВМЕ | 1993 |
|
RU2085950C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ГНОЙНЫХ ОСЛОЖНЕНИЙ В ПОСТТРАВМАТИЧЕСКОМ ПЕРИОДЕ | 1995 |
|
RU2102752C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ГНОЙНЫХ ЛЕГОЧНЫХ ОСЛОЖНЕНИЙ ПРИ ТЯЖЕЛОЙ ЧЕРЕПНО-МОЗГОВОЙ ТРАВМЕ | 1990 |
|
RU2089244C1 |
Авторы
Даты
2003-10-20—Публикация
2002-09-09—Подача