Данное изобретение относится к применению агентов для блокирования синтеза тирозиназы для предотвращения постоянной пигментации радужной оболочки, вызванной отложением меланина, индуцированным фармакологическими лечениями или метаболическим дисбалансом.
Предпосылки к созданию изобретения
Обнаружено, что латанопрост (13,14-дигидро-17-фенил-18,19,20-тринор--PGF2α изопропиловый эфир), синтетический аналог простагландина, (ЕР-А-0364317), а также встречающиеся в природе простагландины, такие как PGF2α и РGF2, вызывают усиленную пигментацию радужной оболочки обезьян во время хронического лечения (Selen G., Stjernschantz J., Resul В. Prostaglandin-induced iridial pigmentation in primates. Surv. Ophthalrool 1997; 41, Suppi. 2: S125-S128). Точный механизм реакции, происходящей после лечения простагландином, не известен, но усиленный синтез меланина (меланогенез) должен происходить, т. к. цвет глаз становится темнее. Кроме того, у пациентов, проходивших лечение латанопростом (Wistrand P.J., Stjernschantz J., Olsson К. The incidence and time-course of latanoprost-induced iridial pigmentation as a function of eye color. Surv. Ophthalmol 1997; 41, Suppl. 2: S129-S138) или изопропил-унопростоном ((13,14-дигидро-15-кето-20-этил--PGF2α изопропиловый эфир) (Yamamoto Т., Kitazawa Y. Iris-color change developed after topical isopropyl unoprostone treatment. J. Glaucoma 1997; 6: 430-432), иногда отмечается потемнение радужной оболочки во время хронической терапии. В особенности пациенты с гетерохромной радужной оболочкой, т.е. голубой-коричневой, серой-коричневой, зеленой-коричневой или с ореховым цветом глаз предрасположены к этому побочному эффекту. Так как побочный эффект может привести к косметическим нарушениям, в особенности у пациентов с односторонней глаукомой, когда лечат только один глаз, и так как побочный эффект является необратимым и относительно часто встречается, полезно было бы избежать его, хотя он и не выглядит представляющим опасность для здоровья пациентов, у которых он проявляется.
Меланин, широко распространенный в природе полимер, образуется из аминокислоты тирозина. На начальной стадии образования меланина тирозин гидроксилируется до L-Dopa, который далее окисляется до допахинона. Фермент, катализирующий обе реакции, называется тирозиназой. Допахинон является лабильным соединением, которое превращается в допахром, черное соединение, которое необходимо для образования олигомеров DHICA (дигидроксииндолкарбоновой кислоты), которые необходимы для окончательной полимеризации с образованием эумеланина (черного или коричневого меланина). Допахинон альтернативно может взаимодействовать с цистеином, образуя в результате серусодержащие олигомеры и в итоге феомеланин (желтоватый или красноватый меланин). Важным для реализации является то, что стадией, ограничивающей скорость продуцирования меланина, является реакция, катализируемая тирозиназой. Недостаточность функциональной тирозиназы, например, по причине мутации гена тирозиназы, часто ведет к альбинизму, т.к. в организме не может образовываться пигмент. Интересно, что тот же фермент тирозиназа также требуется для продуцирования норадреналина, нейротрансмиттера, и адреналина, гормона, в симпатических нейронах и мозговом веществе надпочечников, поскольку эти соединения синтезируются из тирозина. Поэтому соединения, которые блокируют фермент тирозиназу, будут оказывать воздействие как на меланогенез, так и на функцию симпатической нервной системы.
Краткое описание изобретения
В настоящее время обнаружено, что ингибиторы фермента тирозиназы, в особенности α-метил-п-тирозин, ингибируют продуцирование меланина, вызываемое введением производных PGF2α и РGF2, таких как латанопрост и унопростон.
Таким образом, лечение указанными ингибиторами тирозиназы до, во время или после введения производных простагландина пациентам с глаукомой ингибирует продуцирование меланина меланоцитами радужной оболочки, исключая изменения окраски глаз у этих пациентов.
Подробное описание изобретения
Классическим агентом для блокирования синтеза тирозингид-роксилазы является α-метил-пара-тирозин, лекарство, известное под названием метирозин (J. Am. Chem. Soc. 11, 100, 1958), который является ложным субстратом для фермента. Поэтому L-Dopa не образуется и, следовательно, ни меланин, ни адреналин/норадреналин не могут образовываться. Лекарство используют в паллиативном лечении феохромацитомы, опухоли мозгового вещества надпочечника, приводящей к высоким концентрациям катехоламинов в крови и вследствие этого к повышенному кровяному давлению. Применяемый в достаточно высоких концентрациях α-метил-пара-тирозин может существенно блокировать биосинтез адреналина/норадреналина, а также меланина. При использовании катехоламина в клинических концентрациях для лечения феохромацитомы его концентрацию в организме значительно снижают (Weiner N. , Drugs that inhibit adrenergic nerves and block adrenergic receptors. In Goodman Gilman A., Goodman L.S., Rall T.W., Murad F. , eds; Goodman and Gilman's the Pharmacological Basis of Therapeutics, Macmillan, New York, 1985, pp. 181-214) и в экспериментах in vitro данного изобретения продуцирование меланина было значительно снижено. По существу любой агент, который мешает ферменту тирозиназе, будет иметь тот же полезный эффект, результатом которого является блокада продуцирования меланина.
Такими агентами являются, например, гидроксихинон и вещества, которые взаимодействуют с ионами меди, потому что медь является необходимым кофактором для фермента тирозиназы, и различные виды ложных субстратов для фермента. Следовательно, если эти агенты давать либо отдельно, либо в смеси вместе с латанопростом, изопропил-унопростоном или каким-либо другим простагландином, который индуцирует меланогенез, образование пигмента в радужной оболочке может быть предотвращено или по меньшей мере значительно затруднено.
Эта активность α-метил-п-тирозина продемонстрирована следующими экспериментами.
Материалы и методы Культура клеток
Ювеальные меланоциты выделяют из глаза взрослого донора и культивируют. Радужную оболочку вырезают и помещают в чашку задней поверхностью вверх. Пигментированный эпителий радужной оболочки отделяют от стромы после погружения в 0,25% раствор тирозина (Gibco, USA) при 37oС на 2 часа. Оставшуюся строму радужной оболочки помещают в 0,25% раствор тирозина при 4oС на 18 часов с последующим инкубированием при 37oС в течение 1 часа. Выделенные клетки собирают. Раствор тирозина замещают раствором коллагеназы (400 ЕД/мл в среде F-12, Sigma, США) и инкубируют при 37oС. Раствор коллагеназы заменяют и клетки собирают, центрифугируют, ресуспендируют и высевают на чашки каждый час в течение 3 часов.
Выделенные ювеальные меланоциты культивируют в сосудах для культивирования Falcon (Becton Dickinson, USA) со средой FIC, которая состоит из среды F-12 с добавлением 10% фетальной телячьей сыворотки, 2 мМ глутамина (все - Gibco), 10 нг/мл холерного токсина, 0,1 мМ изобутилметилксантина, 50 мкг/мл гентамицина (все - Sigma) и 20 нг/мл основного ростового фактора фибробластов (Promega, США). Сосуды для культивирования инкубируют в увлажненной 5% CO2 атмосфере. Среду заменяют три раза в неделю. Генетицин (Sigma, США), цитотоксический агент добавляют (100 мкг/мл) при необходимости в течение от 3 до 7 дней.
8 штаммов клеток ювеальных меланоцитов, используемых в данном исследовании, выделяют у доноров с различным цветом радужной оболочки (коричневой и коричневой-голубой).
Измерение меланина
Культивированные ювеальные меланоциты отделяют раствором тирозин-EDTA и определяют их количество в гемоцитометре, суспензии клеток центрифугируют и осадок растворяют в 1н. NaOH. Концентрацию меланина определяют путем измерения оптической плотности при 475 нм и сравнивают со стандартной кривой, полученной с использованием синтетического меланина (Sigma). Содержание меланина выражают как нг/клетка.
Расчет продуцирования меланина
Продуцирование меланина рассчитывают путем определения содержания меланина и количества клеток в начале и в конце каждой генерации по следующей формуле:
Ср=СtР-C0/l,3D(P-l),
где С0 и Ct - содержание меланина на клетку во время 0 и время t соответственно;
Р - увеличение популяции за время t,
D - время удвоения численности ювеальных меланоцитов, и
Ср - продуцирование меланина на клетку в сутки в течение времени t.
Активность тирозиназы
Активность тирозиназы оценивают в девяти штаммах клеток с использованием адаптированного метода Pomerantz, который основан на измерении 3H2O, выделяемой путем ферментативного гидроксилирования тирозина.
Результаты
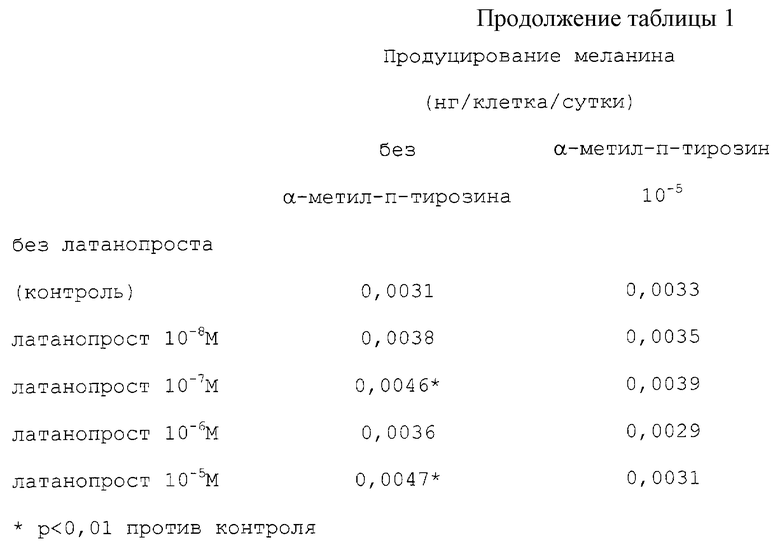
Содержание меланина в культивированных меланоцитах радужной оболочки из 5 клеточных штаммов из коричневых радужных оболочек и 3 клеточных штаммов из коричневых-голубых радужных оболочек оказывается повышенным, когда латанопрост добавляют в самых высоких молярных концентрациях. То же самое обнаруживают для продуцирования меланина и активности тирозиназы (таблицы 1 и 2).
Затем добавляют α-метил-п-тирозин
(10-5 М), заметное снижение содержания и продуцирования меланина и активности тирозиназы обнаруживают с латанопростом в количестве от 10-7 до 10-5М в культивированных меланоцитах как из коричневых радужных оболочек, так и из коричневых-голубых радужных оболочек (таблицы 1 и 2).
Эти результаты показывают, что продуцирование меланина меланоцитами радужной оболочки ингибируется α-метил-п-тирозином.
Данное изобретение также относится к фармацевтическим препаратам, содержащим производное PGF2α или РGF2 с активностью против глаукомы и ингибитор тирозиназы как объединенные препараты для одновременного, раздельного или последовательного применения при лечении глаукомы. В частности, изобретение относится к фармацевтическим продуктам, содержащим латанопрост в качестве агента против глаукомы и α-метил-п-тирозин как объединенные препараты для одновременного, раздельного или последовательного применения при лечении глаукомы.
Для рассматриваемых терапевтических целей α-метил-п-тирозин предпочтительно вводить местным путем или перорально в суточной дозе около 100-500 мг.
Хотя данное описание касается, в частности, ингибирования продуцирования меланина, вызванного латанопростом, α-метил-п-тирозин может быть успешно использован для ингибирования такого же побочного эффекта пигментации, вызванного другими фармакологическими лечениями или метаболическим дисбалансом другого происхождения.



Изобретение относится к медицине. Применение ингибиторов тирозиназы в качестве средства, которое предотвращает продуцирование меланина меланоцитами радужной оболочки, вызванное производными PGF2α и PGE2. Фармацевтические препараты, содержащие производное PGF2α в качестве агента против глаукомы и ингибитор тирозиназы. Способ предотвращения продуцирования меланина меланоцитом радужной оболочки, включающий введение эффективного количества ингибитора тирозиназы. Изобретение позволяет реализовать указанное назначение. 4 с. и 7 з.п.ф-лы, 2 табл.
| JP 04300812 А, 23.10.1992 | |||
| JP 04117313 A, 17.04.1992 | |||
| РЛС | |||
| Энциклопедия лекарств | |||
| - М., 2000, с.468 | |||
| JP 03501025 A, 07.03.1991. |
Авторы
Даты
2003-12-10—Публикация
1998-04-21—Подача