Настоящее изобретение относится к фотобиологии и медицине, а более конкретно к спектрально-флуоресцентным способам контроля топологии патологических, в частности злокачественных, тканей.
Известен способ флуоресцентного контроля топологии злокачественных новообразований [G.A. Meerovich, V.B. Loschenov, A.A. Stratonnikov, K.G. Linkov, V. P. Zhuravleva, V.A. Stepushkin, E.A. Luk'yanets, G.N. Worozhtsov. "Laser Fluorescent System for endoscopic tumor diagnostic and irradiation control in the photodynamic therapy". Proc. SPIE, vol.2728, "Laser Use in Oncology", 1996, pp. 35-38] , включающий введение в организм опухолетропного фотосенсибилизатора, облучение исследуемого участка оптическим излучением в спектральном диапазоне поглощения фотосенсибилизатора, контроль распределения интенсивности, вызванной этим облучением, флуоресценции фотосенсибилизатора и определение участка с повышенной интенсивностью флуоресценции. Поскольку предполагается, что концентрация фотосенсибилизатора пропорциональна интенсивности флуоресценции, а опухолетропный фотосенсибилизатор накапливается преимущественно в опухоли, этот участок с повышенной интенсивностью флуоресценции считается патологическим (опухолевым) участком.
Недостатком известного способа является то, что при исследовании in vivo реальных объектов - органов и тканей организма практически невозможно обеспечить равномерное освещение всего исследуемого участка. А поскольку соотношение между концентрациями фотосенсибилизатора в опухоли и нормальной ткани для большинства фотосенсибилизаторов обычно не очень высоко (1,5-3 раза), то неравномерность облучения может привести к такому распределению по участку интенсивности флуоресценции, которое не соответствует особенностям тканей организма, в частности наличию на нем патологических тканей и их топологии.
Этот недостаток частично устранен в способе флуоресцентного контроля топологии злокачественных новообразований, описанном в [V.V. Sokolov, V.I. Chissov, V.V. Smirnov, V.I. Fabelinsky, N.N. Zharkova "Real-time fluorescence imaging system for cancer diagnostics". Proc. SPIE, vol.2626, "Biomedical Optoelectronics in Clinical Chemistry and Biotechnology", 1995, pp. 385-390] , включающем введение в организм опухолетропного фотосенсибилизатора, в частности сульфофталоцианина алюминия, облучение исследуемого участка оптическим излучением в спектральном диапазоне поглощения фотосенсибилизатора, контроль распределения по участку интенсивности флуоресценции фотосенсибилизатора, контроль распределения по участку интенсивности нормирующего излучения, в качестве которого используется возбуждающее оптическое излучение, рассеянное поверхностью участка, поточечное нормирование интенсивности флуоресценции фотосенсибилизатора на интенсивность нормирующего излучения и определение участка с повышенными значениями нормированной интенсивности флуоресценции, который и считают патологическим участком.
Недостатком известного способа является то, что оптические свойства поверхности биологических тканей и органов, обусловливающие выход из исследуемых тканей излучения флуоресценции (микрорельеф поверхности, коэффициенты рассеяния и поглощения в коже (или слизистой) и подкожной ткани), существенно отличаются от тех, которые определяют коэффициент рассеяния поверхностью возбуждающего излучения (особенно с учетом того, что как оптический путь, так и спектральный диапазон возбуждающего излучения существенно отличаются от аналогичных параметров для флуоресцентного излучения). Поэтому хотя нормирование интенсивности флуоресценции на интенсивность нормирующего рассеянного возбуждающего излучения и позволяет избежать систематической ошибки, связанной с неоднородностью распределения по участку интенсивности возбуждающего излучения, но при этом в результат может быть внесена ошибка, связанная с неоднородностью распределения по участку различных оптических свойств поверхности, которая к тому же может иметь динамический характер.
Еще одним недостатком известного способа является то, что практически для всех известных фотосенсибилизаторов, в частности сульфофталоцианина алюминия, существенное отличие между интенсивностью флуоресценции патологических и здоровых тканей достигается через 2-20 часов после введения фотосенсибилизатора в организм. Это затрудняет использование известного способа, например, при необходимости провести диагностическое исследование оперативно, в частности интраоперационно.
Эти недостатки приводят к снижению эффективности и достоверности флуоресцентного контроля топологии новообразований.
В изобретении решается задача повышения эффективности и достоверности флуоресцентного контроля топологии новообразований.
Задача решается тем, что во флуоресцентном способе контроля топологии новообразований, включающем системное введение в организм фотосенсибилизатора, тропного к опухолевым тканям, облучение исследуемого участка оптическим излучением в спектральном диапазоне поглощения фотосенсибилизатора, контроль распределения по участку интенсивности флуоресценции фотосенсибилизатора, контроль распределения по участку интенсивности нормирующего излучения, поточечное нормирование интенсивности флуоресценции фотосенсибилизатора на интенсивность нормирующего излучения и определение участка с повышенным значением уровня нормированной интенсивности флуоресценции, в качестве фотосенсибилизатора используют бактериохлорофилл-серин, введение в организм фотосенсибилизатора осуществляют за 10-40 минут до флуоресцентного контроля, облучение исследуемого участка осуществляют в спектральном диапазоне 620-650 нм, контроль распределения по участку интенсивности флуоресценции фотосенсибилизатора осуществляют в спектральном диапазоне 760-780 нм, а контроль распределения по участку интенсивности нормирующего излучения осуществляют в спектральном диапазоне 730-745 нм.
Задача решается тем, что в способе контроля топологии новообразований нормирование интенсивности флуоресценции осуществляют в соответствии с формулой: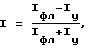
где I - нормированная интенсивность флуоресценции,
Iфл - интенсивность флуоресценции в спектральном диапазоне 760-780 нм,
Iу - интенсивность флуоресценции в диапазоне спектральном 730 - 745 нм, а патологическим считают участок, на котором
I>0,08.
Сущность изобретения поясняется чертежом, где приведены спектры флуоресценции патологического (1, 2, 3) и нормального (4, 5, 6) участков мышей bdf1 с опухолью - солидной формой лейкоза р-388 через 17 минут после введения бактериохлорин-серина.
Предлагаемый флуоресцентный способ определения топологии патологического участка осуществляют следующим образом. В организм системно (как правило, внутривенно) вводят бактериохлорин-серин в дозе 5-20 мг/кг веса. Через определенный временной интервал, лежащий в пределах 10-40 минут, контролируют интенсивность флуоресценции на обследуемом участке, возбуждая ее оптическим излучением, лежащим в спектральном диапазоне 620-650 нм (например, излучением He-Ne лазера с длиной волны 633 нм). Для контроля интенсивности флуоресценции по обследуемому участку может быть использован волоконный спектроанализатор, позволяющий контролировать спектр флуоресценции в каждой точке участка и осуществлять в ЭВМ его анализ, либо видеокамера со сменными узкополосными фильтрами, пропускающими излучение в спектральных диапазонах 760-780 нм и 730-745 нм соответственно, и аппаратурно-программным обеспечением, позволяющим передать сигналы видеокамер, соответствующие обоим изображениям, в ЭВМ и провести нормировку в соответствии с предложенной формулой.
После этого, оценивая значение нормированной интенсивности флуоресценции в разных точках исследуемого участка, определяют топологию патологического участка.
Авторами экспериментально обнаружено, что спектр флуоресценции бактериохлорин-серина в опухолевых и нормальных тканях имеет отличия не только в интенсивности, но и в форме спектра. Эти отличия не зависят от интенсивности возбуждающего флуоресценцию излучения, а связаны с наличием опухолевого процесса в исследуемой точке.
Ниже приведен конкретный пример реализации предлагаемого флуоресцентного способа определения топологии патологического участка.
Проведены исследования на группе мышей bdf1 с опухолью - солидной формой лейкоза р-388 через 17 минут после введения бактериохлорин-серина (фирма "S. E. D. R. ", Израиль). Для исследования использован спектроанализатор "ЛЭСА-01-Биоспек". Результаты спектральных исследований патологической зоны и симметричной ей нормальной зоны показаны на чертеже. По данным спектральных исследований значения 1 составляют 019...0,21 на патологическом участке и менее 0,01 на нормальном, что согласуется с данными морфологических исследований.
Предложенный способ флуоресцентного контроля новообразований обеспечивает более достоверное определение топологии новообразования, причем его результат не зависит от распределения интенсивности возбуждающего излучения. При этом значения нормированной интенсивности флуоресценции, которые позволяют судить о наличии и топологии патологическоого участка, можно получить уже через 10 минут после введения в организм фотосенсибилизатора, что позволяет использовать предложенный метод, например, при интраоперационной диагностике.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФОТОСЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2013 |
|
RU2549953C2 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ НОВООБРАЗОВАНИЙ ШЕЙКИ МАТКИ И ВУЛЬВЫ ПОД КОНТРОЛЕМ СОВМЕСТНОЙ ВИДЕО- И СПЕКТРАЛЬНО-ФЛУОРЕСЦЕНТНОЙ ДИАГНОСТИКИ С ПРИМЕНЕНИЕМ ФОТОСЕНСИБИЛИЗАТОРОВ ХЛОРИНОВОГО РЯДА | 2021 |
|
RU2782643C1 |
| МАТРИЧНОЕ СВЕТОДИОДНОЕ УСТРОЙСТВО ДЛЯ ФЛУОРЕСЦЕНТНОЙ ДИАГНОСТИКИ И ФОТОТЕРАПИИ ПАТОЛОГИЧЕСКИХ УЧАСТКОВ | 2000 |
|
RU2176475C1 |
| ФОТОСЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2012 |
|
RU2479585C1 |
| УСТРОЙСТВО ДЛЯ ЛЮМИНЕСЦЕНТНОЙ ДИАГНОСТИКИ И ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2001 |
|
RU2221605C2 |
| АМИНОАМИДЫ В РЯДУ БАКТЕРИОХЛОРОФИЛЛА A, ОБЛАДАЮЩИЕ ФОТОДИНАМИЧЕСКОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2548675C9 |
| СПОСОБ КОЛИЧЕСТВЕННОЙ ОЦЕНКИ КОНЦЕНТРАЦИИ ФОТОСЕНСИБИЛИЗАТОРА ПО ВИДЕОИЗОБРАЖЕНИЮ В РЕЖИМЕ РЕАЛЬНОГО ВРЕМЕНИ ПРИ ПРОВЕДЕНИИ ФЛУОРЕСЦЕНТНОГО ИССЛЕДОВАНИЯ | 2017 |
|
RU2641519C1 |
| ПРЕПАРАТ ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ И СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ РАКА С ЕГО ИСПОЛЬЗОВАНИЕМ | 2012 |
|
RU2521327C1 |
| СПЕКТРАЛЬНОЕ УСТРОЙСТВО ДЛЯ КОНТРОЛЯ И МОНИТОРИНГА ПРОЦЕССА ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2000 |
|
RU2169590C1 |
| УСТРОЙСТВО ДЛЯ СПЕКТРАЛЬНО-ФЛУОРЕСЦЕНТНОГО КОНТРОЛЯ СОСТОЯНИЯ БИОЛОГИЧЕСКИХ ТКАНЕЙ В ПРОЦЕССЕ ФОТОДИНАМИЧЕСКОГО ВОЗДЕЙСТВИЯ С ПРИМЕНЕНИЕМ ФОТОСЕНСИБИЛИЗАТОРОВ НА ОСНОВЕ ХЛОРИНА E6 | 2022 |
|
RU2807133C1 |
Изобретение относится к медицине и предназначено для флуоресцентного контроля топологии новообразований. В организм вводят фотосенсибилизатор бактериохлорофилл-серин за 10-40 мин до контроля. Осуществляют облучение исследуемого участка в спектральном диапазоне 620-650 нм. Контроль распределения по участку интенсивности флуоресценции фотосенсибилизатора осуществляют в спектральном диапазоне 760-780 нм. Контроль распределения по участку интенсивности нормирующего излучения осуществляют в спектральном диапазоне 730-745 нм. Нормирование интенсивности флуоресценции осуществляют в соответствии с формулой: 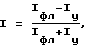 где I - нормированная интенсивность флуоресценции, Iфл - интенсивность флуоресценции в спектральном диапазоне 760-780 нм, Iу - интенсивность флуоресценции в спектральном диапазоне 730-745 нм, а патологическим считают участок, на котором I>0,08. Способ позволяет повысить эффективность и достоверность флуоресцентного контроля топологии новообразований. 1 з.п.ф-лы, 1 ил.
где I - нормированная интенсивность флуоресценции, Iфл - интенсивность флуоресценции в спектральном диапазоне 760-780 нм, Iу - интенсивность флуоресценции в спектральном диапазоне 730-745 нм, а патологическим считают участок, на котором I>0,08. Способ позволяет повысить эффективность и достоверность флуоресцентного контроля топологии новообразований. 1 з.п.ф-лы, 1 ил.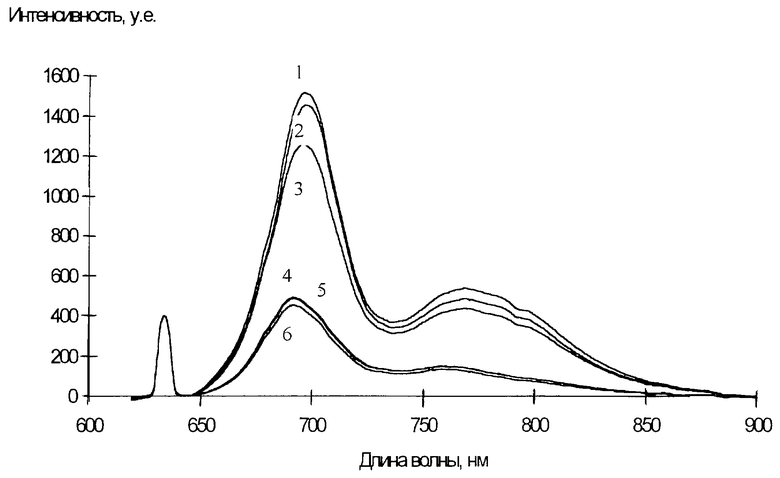
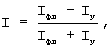
где I - нормированная интенсивность флуоресценции;
Iфл - интенсивность флуоресценции в спектральном диапазоне 760-780 нм;
Iу - интенсивность флуоресценции в спектральном диапазоне 730-745 нм,
а патологическим считают участок, на котором I>0,08.
| SOKOLOV V.V | |||
| et al | |||
| Real-time fluorescence imaging system for cancer diagnostics | |||
| Proc | |||
| SPIE, vol | |||
| Способ изготовления разрядных трубок с катодами Венельта | 1925 |
|
SU2626A1 |
| СПОСОБ ЭНДОСКОПИЧЕСКОЙ ФЛЮОРЕСЦЕНТНОЙ ДИАГНОСТИКИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ПОЛЫХ ОРГАНОВ | 1997 |
|
RU2129273C1 |
| СПОСОБ ДИАГНОСТИКИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ ЖЕЛУДКА И ЛЕГКИХ | 1991 |
|
RU2012243C1 |
| УСПЕНСКИЙ Л.В | |||
| и др | |||
| Лазерная флюоресцентная спектроскопия в интраоперационной диагностике и оценке распространенности рака легкого | |||
| Предохранительное устройство для паровых котлов, работающих на нефти | 1922 |
|
SU1996A1 |
| СТРАНАДКО Е.Ф | |||
| и др | |||
| Пятилетний опыт клинического применения фотодинамической терапии | |||
| Российский онкологический журнал, 1998, №4, с.13-18 | |||
| HOMASSON J.P | |||
| et al | |||
| [Lung autofluorescence | |||
| Preliminary study of two systems without laser illumination or photosensitization] | |||
| Rev | |||
| Pneumol | |||
| Clin | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
Авторы
Даты
2004-01-10—Публикация
2002-12-10—Подача