Настоящее изобретение относится к медицине, а более конкретно к лекарственному препарату на основе производного бактериопурпуринимида, используемого в качестве фотосенсибилизатора (ФС), и способу проведения фотодинамической терапии (ФДТ) с ним.
В настоящее время применяются в клинике или находятся на разных стадиях клинических испытаний ФС различных классов (порфирины и их металлокомплексы, хлорины, бензопорфирины, фталоцианины и др.), но особый интерес представляют природные хлорофиллы и их производные с интенсивным поглощением в ближней ИК-области спектра, поскольку их терапевтическое окно поглощения (750-850 нм) открывает новые возможности для диагностики и лечения злокачественных новообразований. Свет с подобной длиной волны проникает в ткани на глубину до 20-25 мм, это существенно расширяет возможности используемых в настоящее время методов лечения крупных, глубокозалегающих в неполых органах (молочная железа, простата) и плотно окрашенных (меланома) опухолей.
Известен ФС, представляющий собой наноструктурированную дисперсию на основе производного бактериохлорина p - метиловый эфир О-этилоксим N-этоксициклоимид бактериохлорина p C38H46N6O6, а также способ его получения и способ ФДТ, включающий системное введение известного ФС и облучение патологического участка оптическим излучением в спектральном диапазоне 790-810 нм через 0,7-5 часов после введения (RLJ 2411943). Вышеуказанный ФС и способ ФДТ являются ближайшими аналогами настоящего изобретения.
Наличие в структуре у известного ФС - метилового эфира O-этилоксима N-этоксициклоимида бактериохлорина p двух этильных групп придает молекуле определенную гидрофобность, которой, однако, недостаточно для реализации эффективного трансмембранного переноса в опухолевых клетках, что приводит к невысокой фотоиндуцированной противоопухолевой активности.
К недостаткам известного ФС-прототипа следует отнести низкую селективность накопления в опухоли (индекс селективности не превышает 2) и отсутствие результата полной излеченности животных.
Наличие вышеназванных недостатков известного ФС диктует поиск новых высокоэффективных ФС, у которых повышение гидрофобности достигается путем увеличения углеродной цепи боковых заместителей (пропокси-заместители) в макроциклическом кольце.
Заявляемая группа изобретений направлена на решение задачи создания ФС, препарата для ФДТ на основе бактериопурпуринимида, имеющего высокую фотоиндуцированную противоопухолевую активность и обеспечивающего эффективность ФДТ глубокозалегающих опухолей.
Использование заявляемого препарата для ФДТ позволяет достичь следующих технических результатов:
- повышение гидрофобности ФС за счет увеличения углеродной цепи периферических заместителей (пропокси-заместители) в макроциклическом кольце;
- обеспечение химической и фотостабильности препарата;
- высокая фотоиндуцированная активность по отношению к опухолевым клеткам человека различного генеза при отсутствии темновой токсичности;
- селективное накопление в опухоли и быстрое выведение из организма млекопитающих;
- повышение эффективности ФДТ глубокозалегающих опухолей.
Указанные технические результаты при осуществлении группы изобретений достигаются за счет того, что так же как известный ФС, препарат для ФДТ выполнен в форме наноструктурированной водной дисперсии на основе производного бактериопурпуринимида.
ФДТ осуществляют путем системного введения препарата, выполненного в форме наноструктурированной водной дисперсии на основе производного бактериопурпуринимида и воздействия на патологический участок оптическим излучением.
Особенность заявляемого препарата для ФДТ заключается в том, что в качестве ФС он содержит метиловый эфир O-пропилоксим-N-пропоксибактериопурпуринимида C40H50N6O6 со структурной формулой
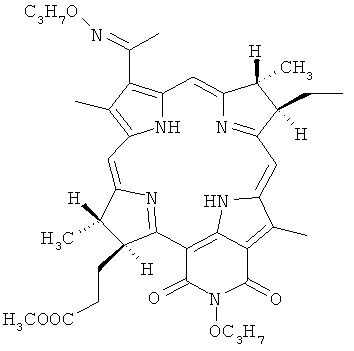
Наноструктурированная водная дисперсия на основе метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида представляет собой:
- кремофорную наноэмульсию;
- твиновую наноэмульсию;
- хитозановую эмульсию;
- декстриновую эмульсию;
- мицеллярную дисперсию с поверхностно-активным веществом - блок-сополимером оксиэтилена и оксипропилена (Эмуксол 268).
Особенность заявляемого способа ФДТ заключается в том, что осуществляют системное введение наноструктурированной водной дисперсии на основе метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида в дозах от 1,0 до 10,0 мг/кг и облучение патологического участка оптическим излучением через 0,25-8 часов после введения препарата в спектральном диапазоне 789-831 нм при плотности энергии от 45 до 360 Дж/см2.
Сущность изобретения заключается в следующем:
Выбор природных пигментов для создания новых ФС обусловлен рядом факторов, в том числе их распространенностью в природе, интенсивностью поглощения в длинноволновой области спектра, структурной близостью к эндогенным порфиринам. Наличие указанных свойств позволяет предположить низкий уровень токсичности подобных соединений и их быстрое выведение из организма.
В качестве соединений, обладающих перечисленными выше свойствами, могут быть рассмотрены хлорины и бактериохлорины. Однако сами хлорины и бактериохлорины имеют ограниченное применение в качестве ФС из-за высокой гидрофобности, низкой химической и фотостабильности, умеренной селективности накопления в опухолевых клетках.
Несмотря на то что гидрофильные вещества удобны с точки зрения приготовления растворов для внутривенного введения, их способность проникать сквозь клеточные мембраны к жизненно важным мишеням клетки довольно ограничена. В то же время известно, что гидрофобные ФС обычно проникают внутрь опухоли и опухолевых клеток, а гидрофильные накапливаются в кровеносных сосудах и строме на периферии опухоли.
Следует отметить, что активность ФС с различной длиной алкильной боковой цепи зависит от количества углеродных атомов в ней. Известно, что максимальной активностью in vitro и in vivo обладают ФС с боковыми цепями из трех и шести атомов углерода [Boyle R., Dolphin D. Structure and biodistribution relationship of phothodynamic sensitizer. Photochem. Photobiol. 1996., v.64, p.469-485].
Это диктует необходимость создания устойчивых производных хлоринов и бактериохлоринов с улучшенными спектральными характеристиками, а также обладающих значительной тропностью к опухолям.
Синтезированный авторами ФС - метиловый эфир O-пропилоксим-N-пропоксибактериопурпуринимида обладает всеми перечисленными свойствами. Способ ФДТ с его использованием обеспечивает высокую фотоиндуцированную противоопухолевую активность и эффективность при воздействии на глубокозалегающие опухоли.
Предлагаемое изобретение иллюстрируется нижеследующими примерами.
Пример 1. Получение метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида
Субстанцию метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида получали одностадийной реакцией по нижеприведенной схеме.
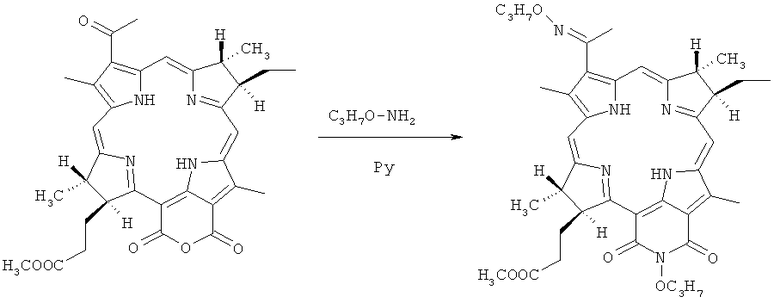
К раствору 30 мг (0,05 ммоль) бактериопурпурина в 2 мл пиридина прибавляли 0,5 ммоль гидрохлорида пропоксиамина. Полученный раствор перемешивали в течение 20 часов при комнатной температуре. Ход реакции контролировали спектрофотометрически и при помощи ТСХ. Затем реакционную смесь разбавляли 150 мл воды и 5 мл 1N HCl и экстрагировали хлороформом до полного обесцвечивания хлороформного слоя (5×30 мл).
Хлороформные экстракты объединяли, сушили над безводным сульфатом натрия и упаривали на роторном испарителе. Полученный продукт очищали с помощью препаративной ТСХ на силикагеле в системе CHCl3:CH3OH (v/v 50:1).
Выход 80%. Спектр 1Н ЯМР (300 МГц, CDCl3, δ, м.д.): 1H ЯМР (CDCl3, δ, м.д.): 8.65 (Н, с, 5-Н), 8.58 (Н, с, 10-Н), 8.40 (Н, с, 20-Н), 5.21 (Н, м, 17-Н), 4.59 (4Н, м, -OCH2CH3), 4.18 (2Н, м, 7-Н, 18-Н), 4.00 (Н, м, 8-Н), 3.64 (3H, с, 12-CH3), 3.58 (3H, с, 173-COOCH3), 3.30 (3H, с, 2-CH3), 2.78 (3Н, с, 32-CH3), 2.75 (Н, м, 172-CH2), 2.40 (3H, м, 81-CH2, 171-CH2, 172-CH2), 2.08 (2Н, м, 81-CH2, 171-CH2), 1.80 (3H, д, J 7.24 Гц, 7-CH3), 1.70 (9Н, м, 18-CH3, -CCH2CH3), 1.10 (3H, т, J 7.38 Гц, 82-CH-3), 0.00 (с, NH), -0.26 (с, NH). UV-VIS, λmax, нм (ε×10-3, M-1 см-1): 368 (100), 418 (53), 541 (40), 800 (49). Масс-спектр (MALDI), m/z: 710,30 (M+-OC3H7), 592,20 (M+-OC3H7, -OC3H7).
Пример 2. Получение наноструктурированной водной эмульсии метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида с использованием Кремофора Е1.
Растворяли 5 мг метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида в 0,25 мл Кремофора EL. К полученному раствору добавляли 0,9% раствор хлористого натрия до концентрации 1 мг/мл при перемешивании при комнатной температуре. Полученный объем фильтровали через мембранный фильтр «Millipore» с размером пор 0.22 мкм.
Пример 3. Оценка стабильности наноструктурированной водной эмульсии метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида на основе Кремофора в бесклеточной среде.
Оценку стабильности в затемненных условиях проводили с помощью абсорбционного и флуоресцентного методов анализа. Растворы для проведения исследований готовили ex tempore, достигая выбранной концентрации путем последовательных разведений исходного раствора. Концентрация исходного раствора составляла 1 мг/мл. В качестве растворителя использовали среду Игла, содержащую 10% ЭТС и 0,9% раствор хлористого натрия. Спектры поглощения регистрировали на спектрофотометре «Genesys 2» (США) в диапазоне длин волн от 600 до 900 нм. Регистрацию флуоресценции растворов проводили в динамике контактным способом на лазерном спектральном анализаторе для флуоресцентной диагностики опухолей «ЛЭСА-6» (ТОО «БиоСпек», Россия). Флуоресценцию возбуждали He-Ne лазером при длине волны генерации 632,8 нм, спектральный диапазон от 600 до 950 нм.
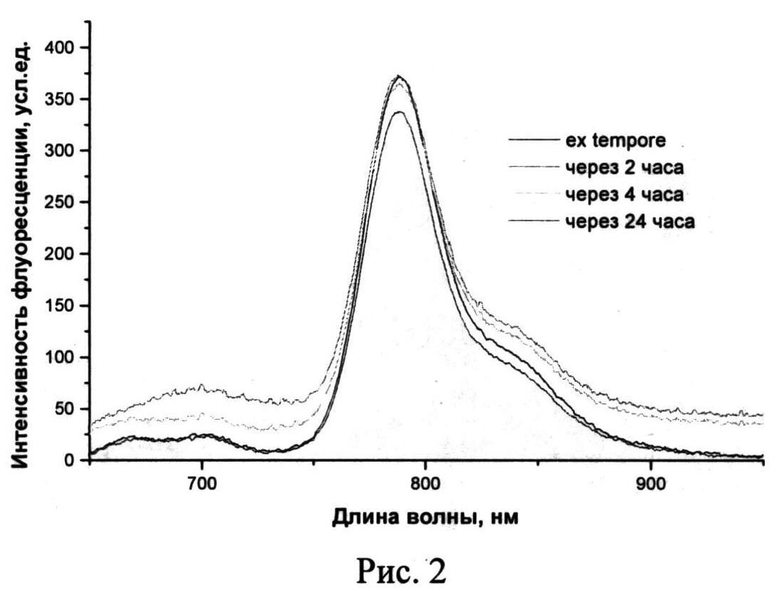
Раствор метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида стабилен в течение суток инкубации в 0,9% растворе NaCl и среде Игла MEM с содержанием 10% эмбриональной телячьей сыворотки (ЭТС) при варьировании концентрацией от 15 до 35 мкМ в темновых условиях (Рис.1,2).
Пример 4. Оценка фотостабильности наноструктурированной водной эмульсии метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида на основе Кремофора в бесклеточной среде.
Оценку фотовыцветания проводили в среде Игла MEM, содержащей 10% ЭТС, при облучении полихроматическим светом. В качестве источника света использовали галогеновую лампу мощностью 500 Вт с широкополосным фильтром КС-19 (λmax≥20 нм) и водным фильтром толщиной 5 см. Световая доза составляла 1, 2, 5 и 10 Дж/см2 при плотности мощности 13,0-25,0 мВт/см2. Измерения флуоресценции проводили контактным способом на лазерном спектральном анализаторе «ЛЭСА-06» в спектральном диапазоне 650-950 нм. Спектры флуоресценции регистрировали сразу после приготовления раствора и через различные промежутки после начала облучения.
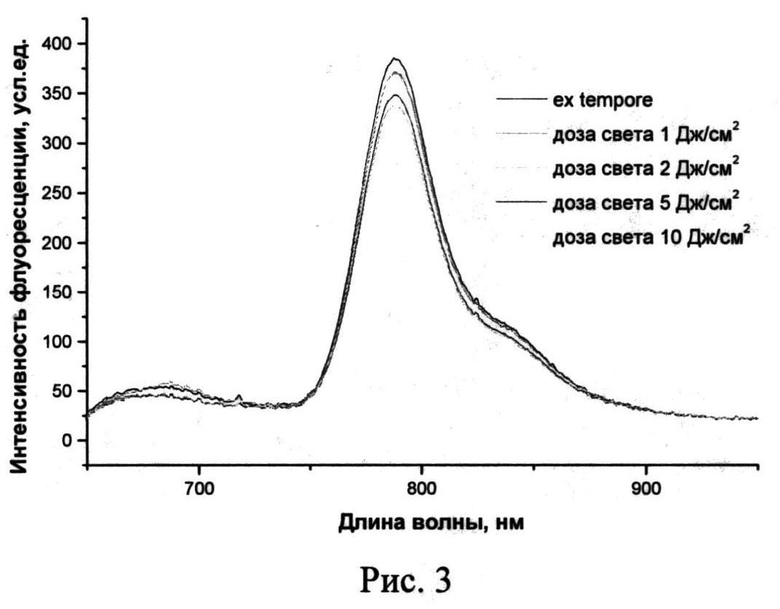
При облучении ФС не происходило сдвига максимума флуоресценции (λmax=799±2 нм), интенсивность флуоресценции снижалась незначительно без изменений в профиле спектра, что свидетельствовало о его стабильности при воздействии светом (Рис.3).
Оценку фотоиндуцированной активности наноструктурированной водной эмульсии метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида на основе Кремофора проводили:
- в системе in vitro на опухолевых клетках человека различного эпителиального происхождения: эпидермальной карциноме гортани (НЕр2), аденокарциноме легкого (А549), карциноме толстой кишки (НТ29) и мочевого пузыря (Т24);
- в системе in vivo на мышах с опухолями различного генеза: эпидермоидной карциноме легкого Льюис (LLC), саркоме 37 (S37) и лимфолейкозе Р388 (Р388).
Пример 5. Фотоиндуцированная активность наноструктурированной водной эмульсии метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида на основе Кремофора в отношении клеток карциномы толстой кишки (НТ29).
Оценку фотоиндуцированной активности проводили при варьировании концентрации ФС от 0,1 до 15,0 мкМ, времени инкубации до светового воздействия от 0,5 до 24 часов, с удалением и без удаления ФС перед облучением.
В качестве источника света использовали галогеновую лампу мощностью 500 Вт с широкополостным фильтром КС-19 (λmax≥720 нм) и водным фильтром толщиной 5 см. Уровень ингибирования роста клеток в культуре вычисляли по формуле:
ИР(%)=[(Пк-По)/Пк]×100%
где: ИР - ингибирование роста клеток культуры, в процентах;
По и Пк - число жизнеспособных клеток, выраженное в единицах оптической плотности соответственно в опытных (с ФС) и контрольных (без ФС) пробах.
Биологически значимым эффектом считали ингибирование роста культуры на 50% (ИК50).
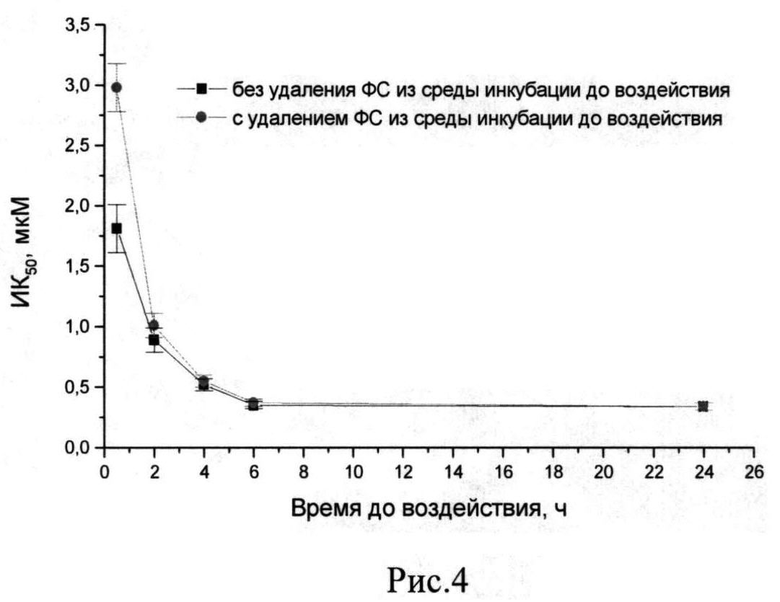
Выявлено, что ФС проявил максимальную фотоиндуцированную активность относительно клеток культуры НТ29 при 6-часовой инкубации (ИК50 составляла 0,35±0,03 мкМ) с увеличением времени инкубации до 24 часов величина ИК50 не изменялась (Рис.4). Инкубация клеток с ФС в концентрациях до 15 мкМ в отсутствии светового воздействия в течение 24 часов не влияла на рост клеточной культуры.
Удаление ФС из культуральной среды перед воздействием светом незначительно снижало эффективность фотодинамического воздействия, что свидетельствует о том, что фотоиндуцированная активность реализуется преимущественно за счет активации внутриклеточного ФС.
Таким образом, результаты, полученные in vitro, показали, что метиловый эфир O-пропилоксим-N-пропоксибактериопурпуринимида эффективно накапливался в клетках и обладал высокой фотоиндуцированной активностью.
Пример 6. Распределение наноструктурированной водной эмульсии метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида на основе Кремофора в опухоли LLC и флуоресцентная контрастность относительно окружающей ткани.
Оценку распределения красителя в опухолевой и окружающей тканях проводили у мышей с карциномой LLC в интервале от 5 минут до 72 часов методом локальной флуоресцентной спектроскопии (ЛФС). Наноструктурированную кремофорную дисперсию O-пропилоксим-N-пропоксибактериопурпуринимида вводили внутривенно в дозе 5,0 мг/кг. Флуоресценцию регистрировали контактным способом на лазерном спектральном анализаторе для флуоресцентной диагностики опухолей и контроля за ФДТ «ЛЭСА-06».
В опухолевой ткани нормированная флуоресценция (НФ) ФС достигала максимального значения через 15 минут и сохранялась на высоком уровне до 8 часов после введения, а затем к 72 часам снижалась на 90%-98% от максимального значения. Наиболее высокие уровни ФН в нормальных коже и мышце наблюдались через 0,25-4 часа после введения ФС. Максимальная флуоресцентная контрастность относительно окружающих нормальных тканей кожи и мышцы регистрировалась в интервале от 0,25 до 8 часов после введения и составляла 2,2-2,8 усл.ед. и 1,6-2,2 усл. ед. соответственно.
Пример 7. Фотоиндуцированная противоопухолевая активность наноструктурированной водной эмульсии метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида на основе Кремофора у животных с опухолью LLC.
Исследование ФДТ с метиловым эфиром O-пропилоксим-N-пропоксибактериопурпуринимида в виде наноструктурированной водной дисперсии на основе Кремофора проводили у животных с карциномой легкого Льюис, привитой подкожно с внешней стороны правого бедра мышам BDF1, в зависимости от дозы ФС на 7 сутки после инокуляции опухоли.
В первой и второй опытных группах животным вводили ФС однократно внутривенно в хвостовую вену в дозах 2,5 и 5,0 мг/кг соответственно. Облучение проводили через 30 минут после введения ФС. Для облучения использовали светодиодный источник (ФГУП «ГНЦ РФ НИОПИК») с длиной волны 810±21 нм и плотностью мощности 100 мВт/см2 (плотность энергии 150 Дж/см2). Третья группа животных - контрольная без воздействия.
Эффективность ФДТ оценивали, используя общепринятые в экспериментальной онкологии критерии:
- торможение роста опухоли ТРО=[(Vк-Vоп)/Vk]·100%, где Vоп и Vк - объем опухоли в опытной и контрольной группах, соответственно;
- увеличение продолжительности жизни УПЖ=[(СПЖоп-СПЖк)/СПЖк]·100%, где СПЖоп и СПЖк - средняя продолжительность жизни в опытной и контрольной группах соответственно;
- критерий излеченности КИ=[Nи/No]·100%, где Nи и No - количество излеченных животных и общее количество животных в опытной группе соответственно.
Объем опухоли рассчитывали по формуле: V=d1·d2·d3, где d1, d2 и d3 - три взаимно перпендикулярных диаметра опухоли.
Измерение объема опухоли проводили в течение 20 суток после проведенного облучения с помощью электронного цифрового кронциркуля STORMtm 3C301 «Central». За животными наблюдали 120 суток.
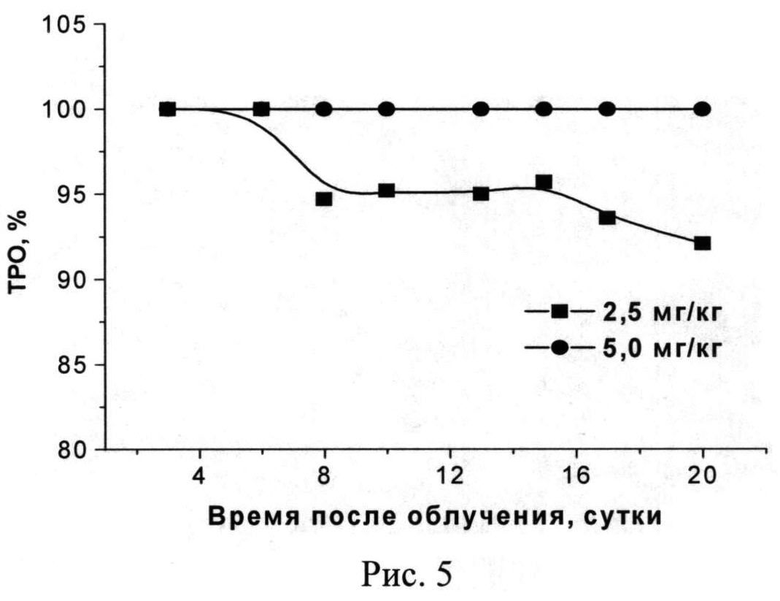
В опытных группах в течение суток после облучения у животных образовывался интенсивный отек в зоне воздействия, который сохранялся до 4-5 суток. При использовании метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида в дозе 2,5 мг/кг среднее значение объема опухоли увеличивалось медленно по отношению к объему опухоли контрольной группы. ТРО составило 92,1-100%, УПЖ - 62,2%, КИ - 33,3%. Для дозы 5,0 мг/кг выявлена еще более высокая эффективность: 100% торможение роста опухоли в течение всего срока наблюдения, УПЖ - 111,1% и 50% излеченность животных (Рис.5).
Пример 8. Фармакокинетика наноструктурированной водной эмульсии метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида на основе Кремофора у интактных мышей.
Фармакокинетику метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида изучали методом ЛФС в органах и тканях интактных мышей в дозе 5,0 мг/кг.
Максимум спектра флуоресценции ФС в тканях животных регистрировали при 796±2 нм. Флуоресцирующая форма ФС быстро (в течение 15-30 минут) регистрировалась во внутренних органах и тканях организма, преимущественно в печени, затем снижалась с различной скоростью.
Во внутренних органах через 24 часа уровень НФ снижался в печени на 33%, почках - на 63%, селезенке - на 93% от максимального значения. Флуоресцирующая форма ФС в дозе 5,0 мг/кг определялась в почках и селезенке до 48 часов, а в печени остаточное количество определялось до 7 суток.
В коже максимальное значение флуоресценции регистрировалось через 15 минут после введения ФС, затем его НФ быстро снижалась и через 24 часа не определялась. Это свидетельствовало о быстром элиминировании ФС из кожи. В мышце через 24 часа уровень НФ также снижался на 83%, в жировой ткани - на 58%. Флуоресцирующая форма ФС определялась в мышце до 48 часов, а в жировой ткани - до 4 суток.
Полученные данные свидетельствуют о быстрой циркуляции метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида в организме млекопитающих и его выведении преимущественно через печень с желчью.
Таким образом, заявляемые препарат для ФДТ, представляющий собой наноструктурированную водную дисперсию на основе метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида, и способ ФДТ с использованием этого ФС обеспечивают: высокую фотоиндуцированную противоопухолевую активность, 100%-ное торможение роста опухоли и 90%-ную излеченность животных за счет селективного накопления в опухоли и быстрого выведения из организма.
Установлено, что использование наноструктурированной водной дисперсии на основе метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида при ФДТ приводит к существенному увеличению продолжительности жизни (от 65 до 120%) и излеченности животных (от 30 до 90%).
На Рис.1 представлены спектры флуоресценции ФС в среде Игла MEM, содержащей 10% ЭТС, в динамике (λmax=799 нм).
На Рис.2 представлены спектры флуоресценции ФС в 0,9% растворе хлористого натрия в динамике (λmax=789 нм).
На Рис.3 представлены спектры флуоресценции ФС в среде Игла MEM, содержащей 10% ЭТС, до и после облучения (λmax=799 нм).
На Рис.4 представлена зависимость фотоиндуцированной активности метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида от времени инкубации и удаления ФС из среды инкубации до воздействия.
На Рис.5. представлена зависимость фотоиндуцированной противоопухолевой активности O-пропилоксим-N-пропоксибактериопурпуринимида у мышей с опухолью LLC от дозы ФС.
| название | год | авторы | номер документа |
|---|---|---|---|
| АМИНОАМИДЫ В РЯДУ БАКТЕРИОХЛОРОФИЛЛА A, ОБЛАДАЮЩИЕ ФОТОДИНАМИЧЕСКОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2548675C9 |
| ФОТОСЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2013 |
|
RU2549953C2 |
| ФОТОСЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2012 |
|
RU2479585C1 |
| ФОТОСЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2013 |
|
RU2536966C1 |
| ФОТОСЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2013 |
|
RU2548726C2 |
| ФОТОСЕНСИБИЛИЗАТОР БАКТЕРИОХЛОРИНОВОГО РЯДА ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2019 |
|
RU2720806C2 |
| ФОТОСЕНСИБИЛИЗАТОР НА ОСНОВЕ ПРОИЗВОДНОГО БАКТЕРИОХЛОРИНА p, СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО БАКТЕРИОХЛОРИНА p И СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ РАКА С ИСПОЛЬЗОВАНИЕМ ЭТОГО ФОТОСЕНСИБИЛИЗАТОРА | 2009 |
|
RU2411943C2 |
| ФОТОСЕНСИБИЛИЗАТОРЫ ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2012 |
|
RU2476218C1 |
| ФОТОСЕНСИБИЛИЗАТОРЫ ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2005 |
|
RU2282646C1 |
| ВОДОРАСТВОРИМАЯ ЛЕКАРСТВЕННАЯ ФОРМА МЕЗО-ТЕТРА(3-ПИРИДИЛ)БАКТЕРИОХЛОРИНА ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2017 |
|
RU2663900C1 |

Группа изобретений относится к медицине, а более конкретно к лекарственному препарату, используемому в качестве фотосенсибилизатора (ФС), и к способу фотодинамической терапии с его использованием. Препарат представляет собой наноструктурированную водную дисперсию метилового эфира O-пропилоксим-N-пропоксибактериопурпуринимида C40H50N6O6. Изобретение обеспечивает высокую фотоиндуцированную противоопухолевую активность в системе in vitro и in vivo, 100%-ное торможение роста опухоли и 90% излеченности животных за счет селективного накопления в опухоли и быстрого выведения из организма. 2 н. и 5 з.п. ф-лы, 5 ил., 8 пр.
1. Препарат для фотодинамической терапии, выполненный в форме наноструктурированной водной дисперсии, включающий фотосенсибилизатор - производное бактериопурпуринимида, отличающийся тем, что производное бактериопурпуринимида представляет собой метиловый эфир O-пропилоксим-N-пропоксибактериопурпуринимида C40H50N6O6 со структурной формулой:

2. Препарат по п.1, отличающийся тем, что наноструктурированная водная дисперсия представляет собой кремофорную наноэмульсию.
3. Препарат по п.1, отличающийся тем, что наноструктурированная водная дисперсия представляет собой твиновую наноэмульсию.
4. Препарат по п.1, отличающийся тем, что наноструктурированная водная дисперсия представляет собой хитозановую эмульсию.
5. Препарат по п.1, отличающийся тем, что наноструктурированная водная дисперсия представляет собой декстриновую эмульсию.
6. Препарат по п.1, отличающийся тем, что наноструктурированная водная дисперсия представляет собой мицеллярную дисперсию с поверхностно-активным веществом - блок-сополимером оксиэтилена и оксипропилена (Эмуксол 268).
7. Способ фотодинамической терапии, включающий системное введение наноструктурированной водной дисперсии, включающей фотосенсибилизатор - производное бактериопурпуринимида, и воздействия на патологический участок оптическим излучением, отличающийся тем, что в качестве фотосенсибилизатора используют метиловый эфир O-пропилоксим-N-пропоксибактериопурпуринимида, препарат вводят в дозах от 1,0 до 10,0 мг/кг и облучение патологического участка осуществляют оптическим излучением в спектральном диапазоне 789-831 нм при плотности энергии от 45 до 360 Дж/см2 через 0,25-8 часов после введения препарата.
| ФОТОСЕНСИБИЛИЗАТОР НА ОСНОВЕ ПРОИЗВОДНОГО БАКТЕРИОХЛОРИНА p, СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО БАКТЕРИОХЛОРИНА p И СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ РАКА С ИСПОЛЬЗОВАНИЕМ ЭТОГО ФОТОСЕНСИБИЛИЗАТОРА | 2009 |
|
RU2411943C2 |
| УЛУЧШЕННЫЕ КОМПОЗИЦИИ ФОТОСЕНСИБИЛИЗАТОРОВ И ИХ ПРИМЕНЕНИЕ | 2005 |
|
RU2371181C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПОРФИРИНОВ, В ЧАСТНОСТИ ХЛОРИНЫ И/ИЛИ БАКТЕРИОХЛОРИНЫ, И ИХ ПРИМЕНЕНИЕ В ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2005 |
|
RU2399622C2 |
| СЕНСИБИЛИЗАТОР ДЛЯ ФОТОДИНАМИЧЕСКОГО РАЗРУШЕНИЯ КЛЕТОК ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С ЕГО ИСПОЛЬЗОВАНИЕМ | 2004 |
|
RU2259200C1 |
| US 0007169753 B2, 30.01.2007 | |||
| WO 1995032206 A1, 30.11.1995 | |||
Авторы
Даты
2014-06-27—Публикация
2012-12-12—Подача