Область техники, к которой относится изобретение
Предлагаемое изобретение относится к медицине и фотобиологии, и может найти применение в клинической практике для мониторинга эффективности противоопухолевой терапии, контролирования состояния сенсибилизированных биологических тканей в процессе фотодинамической терапии и в лабораторных исследованиях эффективности фотосенсибилизаторов на основе хлорина е6.
Уровень техники
Одной из основных целей современной клинической онкологии является повышение эффективности хорошо зарекомендовавших себя методов лечения, к которым относится фотодинамическая терапия. Персонификация процесса фотодинамического воздействия на опухоли различных локализаций может улучшить клиническую эффективность данного метода. Фотодинамическая терапия включает два основных этапа: введение в организм пациента фотосенсибилизатора, который способен селективно накапливаться в тканях/клетках опухоли и воздействие на сенсибилизированные ткани опухоли светом с определенной длиной волны, соответствующей одному из пиков поглощения фотосенсибилизатора для запуска процесса генерации активных форм кислорода (преимущественно синглетного кислорода) [Chen, Bin, et al. "Effect of tumor host microenvironment on photodynamic therapy in a rat prostate tumor model." Clinical Cancer Research 11.2 (2005): 720-727.]. Кроме участия в реакциях с биологическими субстратами, синглетный кислород может взаимодействовать с молекулами фотосенсибилизатора, приводя к их необратимой деструкции. В процессе фотодинамического воздействия молекула фотосенсибилизатора может подвергаться фотобличингу, т.е. в молекуле могут произойти фотохимические изменения, которые способствуют временной или необратимой потере молекулой флуоресцентных свойств. Фотобличинг фотосенсибилизатора может уменьшать скорость генерации синглетного кислорода и других его активных форм, таким образом, уменьшая эффективность проводимой противоопухолевой терапии [Ericson М.В. et al. Photodynamic therapy of actinic keratosis at varying fluence rates: assessment of photobleaching, pain and primary clinical outcome // British Journal of Dermatology. - 2004. - T. 151. - №. 6. - C. 1204-1212.]. Однако положительная сторона фотобличинга фотосенсибилизатора состоит в том, что этот процесс можно использовать для исследования эффективности проводимой терапии и защиты нормальных (здоровых) тканей от фотодинамического повреждения [Boyle D.G., Potter W. R. Photobleaching of Photofrin II as a means of eliminating skin photosensitivity // Photochemistry and photobiology. - 1987. - T. 46. - №. 6. - C. 997-1001.].
Выделяют три основных механизма действия фотодинамической терапии на биологические ткани, которые влекут разрушение опухоли [Dolmans D.Е., Fukumura D., Jain R.K. Photodynamic therapy for cancer // Nature reviews cancer. - 2003. - T. 3. - №. 5. - C. 380-387.]. Активные формы кислорода могут приводить как к прямому повреждению клеток опухоли, вызывая их гибель путем апоптоза или некроза, так и разрушать кровеносную систему опухоли за счет тромбирования сосудистой системы облучаемых тканей и, тем самым, нарушая процесс снабжения опухоли кислородом [Chen, Bin, et al. "Vascular and cellular targeting for photodynamic therapy." Critical Reviews™ in Eukaryotic Gene Expression 16.4 (2006).]. Также, фотодинамическая терапия может значительно влиять на иммунный ответ организма посредством его стимуляции, либо подавления [Falk-Mahapatra R., Gollnick S.О. Photodynamic therapy and immunity: an update // Photochemistry and photobiology. - 2020. - T. 96. - №. 3. - C. 550-559.].
В процессе фотодинамической терапии потребляется много молекулярного кислорода (фотохимическое потребление за счет образования синглетного кислорода) и наблюдается снижение уровня оксигенации тканей за счет разрушения сосудистой системы опухоли, что может усугублять гипоксию опухолевых тканей и снижать противоопухолевую эффективность фотодинамической терапии [Van Geel I.P. J. et al. Vascular perfusion and hypoxic areas in RJF-1 tumours after photodynamic therapy // British journal of cancer. - 1996. - T. 73. - №. 3. - C. 288-293.]. Скорость потребления кислорода пропорциональна произведению концентрации фотосенсибилизатора и плотности потока лазерного излучения [Cottrell W.J. et al. Irradiance-dependent photobleaching and pain in δ-aminolevulinic acid-photodynamic therapy of superficial basal cell carcinomas // Clinical cancer research. - 2008. - T. 14. - №. 14. - C. 4475-4483.]. Если в процессе фотодинамической терапии к тканям не будет непрерывно подаваться кислород, эффективность дальнейшей терапии может быть ограничена, поэтому важно последовательно контролировать уровень оксигенации тканей непосредственно в процессе светового воздействия, что может иметь решающее значение для проведения эффективной фотодинамической терапии.
Одним из самых распространенных способов определения фотодинамической дозы в процессе светового воздействия является контролирование фотобличинга фотосенсибилизатора, который может служить показателем генерации синглетного кислорода, и, соответственно, эффективности терапии [Algorri, José Francisco, et al. "Light technology for efficient and effective photodynamic therapy: a critical review." Cancers 13.14 (2021): 3484.]. Дозиметрическим методом контроля фотодинамической терапии также является измерение концентрации синглетного кислорода [Li, Buhong, et al. "Photosensitized singlet oxygen generation and detection: Recent advances and future perspectives in cancer photodynamic therapy." Journal of biophotonics 9.11-12 (2016): 1314-1325.]. Однако клиническое применение данного подхода является труднодостижимым из-за технической сложности осуществления.
Фотодинамическая терапия новообразований, направленная на разрушение сосудистой системы опухоли, привлекает значительное внимание в связи с ее высокой клинической эффективностью [Chen В. et al. Vascular and cellular targeting for photodynamic therapy // Critical Reviews™ in Eukaryotic Gene Expression. - 2006. - T. 16. - №. 4.]. Наиболее часто применяемыми препаратами, преимущественно воздействующими на сосудистую систему опухоли, являются фотосенсибилизаторы на основе хлорина е6 [Kustov А.V. et al. Transurethral resection of non-muscle invasive bladder tumors combined with fluorescence diagnosis and photodynamic therapy with chlorin е6-type photosensitizers // Journal of clinical medicine. - 2021. - T. 11. - №. 1. - C. 233.]. Фотосенсибилизаторы на основе хлорина е6 накапливаются преимущественно в клетках эндотелия кровеносных сосудов, а в процессе фотодинамической терапии эндотелий сосудов повреждается, что приводит к запуску процесса их тромбирования [Khludeyev, I.I., et al. "Speckle optical monitoring of blood microcirculation for different types of treatment of the vascular system." Journal of Applied Spectroscopy 80.2 (2013): 299-304.]. Хотя хлорин е6 демонстрирует слабое внутриклеточное накопление [Yang, Lan, et al. "Clickable amino acid tuned self-assembly of a nucleus-selective multi-component nanoplatform for synergistic cancer therapy." Chemical Science 12.24 (2021): 8394-8400.], его противоопухолевое воздействие, помимо повреждения сосудистой системы опухоли, может значительно подавлять продолженный рост опухоли за счет повреждения как патологических клеток по механизму некроза и/или апоптоза, так и уменьшения доли опухоль-ассоциированных макрофагов М2 [Soyama Т. et al. Photodynamic therapy exploiting the anti-tumor activity of mannose-conjugated chlorin е6 reduced M2-like tumor-associated macrophages // Translational Oncology. - 2021. - T. 14. - №. 2. - C. 101005.]. В процессе фотодинамической терапии с применением хлорина е6 существует вероятность изменения поляризации противовоспалительных макрофагов фенотипа М2 в провоспалительный фенотип M1 [Yu Т.Т. et al. Macrophages mediated delivery of chlorin е6 and treatment of lung cancer by photodynamic reprogramming // International Immunopharmacology. - 2021. - T. 100. - C. 108164.]. Однако условия запуска данного процесса зависят от оптимальных энергетических параметров светового воздействия, которые могут варьироваться в различных тканях.
Таким образом, итоговый цитотоксический эффект фотодинамической терапии зависит от множества параметров, таких как исходная концентрации и локализация фотосенсибилизатора, уровень содержания молекулярного кислорода в опухолевой ткани (уровень оксигенации), скорость повреждения сосудистой системы опухоли, длина волны лазерного излучения, плотность мощности лазерного излучения и время воздействия на биологические ткани.
Известен способ определения фотодинамической активности in vitro (патент RU 2185103 C2), где в биологическую среду, содержащую культуру сенсибилизированных опухолевых клеток, непосредственно перед облучением вводят эритроциты (0,2-1,0 об.%) и по соотношению вкладов спектров окси- и дезоксигемоглобина определяют степень оксигенации гемоглобина в среде и скорость ее изменения. Таким образом определяется фотодинамическая активность фотосенсибилизатора по отношению скорости изменения оксигенации среды к плотности мощности облучения.
Известен способ исследования биораспределения и фармакокинетики фотосенсибилизатора в биологических тканях (патент RU 2395124 C2) и устройства с возможностью интраоперационной видеофлуоресцентной визуализации или спектроскопического анализа сенсибилизированных тканей опухоли для исследования распределения фотосенсибилизаторов в биотканях, а также для осуществления контролируемого фотодинамического воздействия (патенты RU 206470 U1, RU 2661029 C1, RU 2290855 C1, RU 2736909 C1, RU 2777486 C1, RU 2169590 C1, RU 2464975 C1).
Известны методы и устройства для проведения фототераностики, включающие проведение флуоресцентной диагностики во время фотодинамической терапии с внутривенным введением фотосенсибилизаторов на основе хлорина е6 пациентам (патенты RU 2641519 C1, RU 2767264 C1, RU 2782643 C1) или с совместным внутривенным введением двух фотосенсибилизаторов - хлорин е6 и индоцианин зеленый (патенты RU 2736909 C1, RU 203175 U1). В патенте RU 2775461 C1 представлено устройство для определения состава иммунокомпетентных клеток в опухолевой ткани спектрально-флуоресцентными методами с применением фотосенсибилизатора на основе хлорина е6 в процессе проведения фотодинамической терапии.
В патенте RU 2625297 C2 представлен способ персонифицированной фотодинамической терапии обширных косметических дефектов кожи, где подбор оптимальной плотности энергии (в диапазоне 5-45 Дж/см2) проводится на основании интенсивности флуоресценции тканей (чем ниже интенсивность, тем меньше доза облучения). В патенте RU 2297858 C1 представлено устройство, которое, помимо определения точной локализации участка опухолевой ткани, позволяет проводить эндоскопический контроль и автоматически корректировать процесс светового облучения.
Известен способ фотодинамической терапии онкологических заболеваний (патент RU 2438733 C1), который включает определение объемной концентрации кровеносных сосудов и степень оксигенации биоткани до проведения светового воздействия. Также известен способ фотодинамической терапии опухоли с предварительным определением точного места локализации стволового клона клеток в опухоли (патент RU 2184578 C), который позволяет определять время окончания фотодинамического воздействия по уменьшению перфузии крови в ткани по сравнению со значениями до фотодинамической терапии.
В патенте RU 2683858 C1 представлен способ оценки эффективности фотодинамической терапии методом оптической когерентной ангиографии с визуальной оценкой состояния кровотока в опухоли, трансплантированной мышам на наружной поверхности ушной раковины в центральной ее части через 24 часа после фотодинамической терапии.
В патенте RU 92617 U1 представлено устройство для проведения внутритканевой лазерной гипертермии и фотодинамической терапии, включающее лазерное облучение кожи через охлаждающее устройство с возможностью пропускания оптического излучения, которое позволяет проводить флуоресцентную диагностику в процессе фотодинамической терапии.
Известны устройство и способ флуоресцентной диагностики и фотодинамической терапии заболеваний кожи, которые представлены в патенте RU 2382660 C1, позволяющие проводить одновременно видео-флуоресцентную диагностику и фотодинамическую терапию путем облучения опухоли излучением в импульсном режиме с непрерывной регистрацией флуоресцентных изображений с помощью спектрально-селективной камеры.
Известны спектральные способы флуоресцентного контроля топологии новообразований в спектральном диапазоне 730-745 нм с введением в организм пациента фотосенсибилизатора бактериохлорофилл-серин за 10-40 мин до проведения исследования (патент RU 2220753 C1) и способ диагностики онкологических заболеваний, который включает исследование нормальных тканей за счет возбуждения монохроматическим светом в диапазоне длин волн 400-800 нм с регистрацией спектра отражения и дальнейшее сравнение со значениями тканей опухоли (патент RU 2184486 C2).
Недостатками данных способов и устройств являются отсутствие возможности одновременного интраоперационного контролирования фотобличинга
фотосенсибилизатора, оксигенации облучаемых тканей и изменяющихся в процессе светового воздействия оптических свойств биологических тканей.
Известен способ фотодинамической терапии онкологических заболеваний (патент RU 2539367 C1), который является наиболее близким к заявленному изобретению. Данное изобретение позволяет определять структурно-морфологические параметры ткани (концентрацию кровеносных сосудов и фотосенсибилизатора, а также относительное содержание оксигемоглобина и метгемоглобина в крови) и направлено на решение задач определения оптимальных параметров лазерного воздействия (дозы облучения и длины волны излучения). Определение структурно-морфологических параметров тканей основывается на сравнении модельных (в приближении модели кожи с тонким верхним слоем и полубесконечным однородным нижним слоем) и экспериментальных спектров диффузного отражения тканей. Данный способ предполагает, что в ряде случаев (например, при высокой пигментации кожи) могут наблюдаться большие погрешности. При этом следует учитывать, что опухоли одного типа у разных пациентов имеют структурные различия, которые могут быть даже между первичной (исходной) и вторичной опухолью у одного пациента. Гетерогенность (неоднородность) опухоли играет важную роль в диагностике и терапии рака, так как влияет на картину распространения света в данных тканях. Погрешности могут также увеличиваться вследствии отсутствия возможности проведения диагностики тканей опухоли в процессе светового воздействия, так как оптические свойства тканей могут меняться в процессе фотодинамической терапии, вследствии фотобличинга фотосенсибилизатора или тромбирования кровеносных сосудов.
Раскрытие сущности изобретения
Задачей изобретения является создание устройства и метода спектрально-флуоресцентного контроля состояния тканей опухолей с высоким уровнем гетерогенности, которое позволит одновременно контролировать фотобличинг фотосенсибилизаторов на основе хлорина е6 в ближнем инфракрасном диапазоне, оксигенацию тканей и оптические свойства биологических тканей непосредственно в процессе фотодинамического воздействия.
Поставленная задача решается посредством того, что устройство и метод спектрально-флуоресцентного контроля состояния биологических тканей в процессе фотодинамического воздействия с применением фотосенсибилизаторов на основе хлорина е6 включает один полупроводниковый источник лазерного излучения с длиной волны 660±5 нм для возбуждения флуоресценции хлорина е6 с целью проведения флуоресцентной диагностики и фотодинамической терапии; волоконно-оптический кабель для доставки лазерного излучения от источника к поверхности облучаемых тканей; широкополосный источника белого света со встроенным оптическим фильтром, отсекающим длинноволновую часть спектра красного и ближнего инфракрасного диапазонов для регистрации спектров поглощения гемоглобина в диапазоне длин волн 500-600 нм; портативный спектрометр со встроенным оптическим фильтром для регистрации в одном динамическом диапазоне уровня оксигенации гемоглобина, обратно рассеянного лазерного излучения и флуоресценции фотосенсибилизаторов на основе хлорина е6 в ближнем инфракрасном диапазоне; волоконно-оптический зонд, который содержит пучок из семи оптических волокон (центральное волокно обеспечивает доставку белого света, а шесть волокон, расположенных равномерно вокруг центрального, соединены со спектрометром и обеспечивают регистрацию спектров поглощения гемоглобина, обратно рассенного лазерного излучения и флуоресценции тканей); персональный компьютер со специальным программным обеспечением, позволяющим обрабатывать регистрируемые спектры и рассчитывать изменения соотношения вкладов спектров поглощения окси- и дезоксигемоглобина в диапазоне 500-600 нм (уровень оксигенации гемоглобина), интенсивности обратно рассеянного лазерного излучения и флуоресценции хлорина е6 в ближнем инфракрасном диапазоне в процессе фотодиннамической терапии в режиме реального времени. Краткое описание фигур
Описание изобретения поясняется фигурами, на которых представлена реализация устройства и метода:
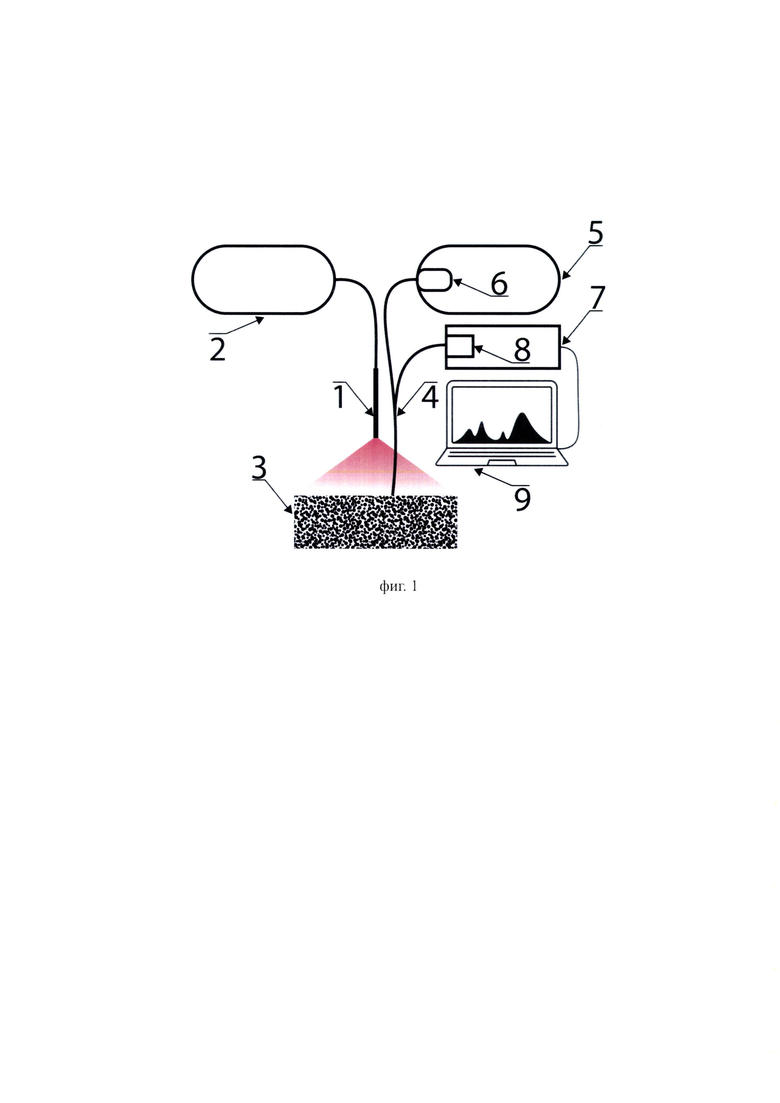
• на фиг. 1 представлена общая схема предложенного устройства и метода контроля состояния опухолевых тканей в процессе фотодинамической терапии;
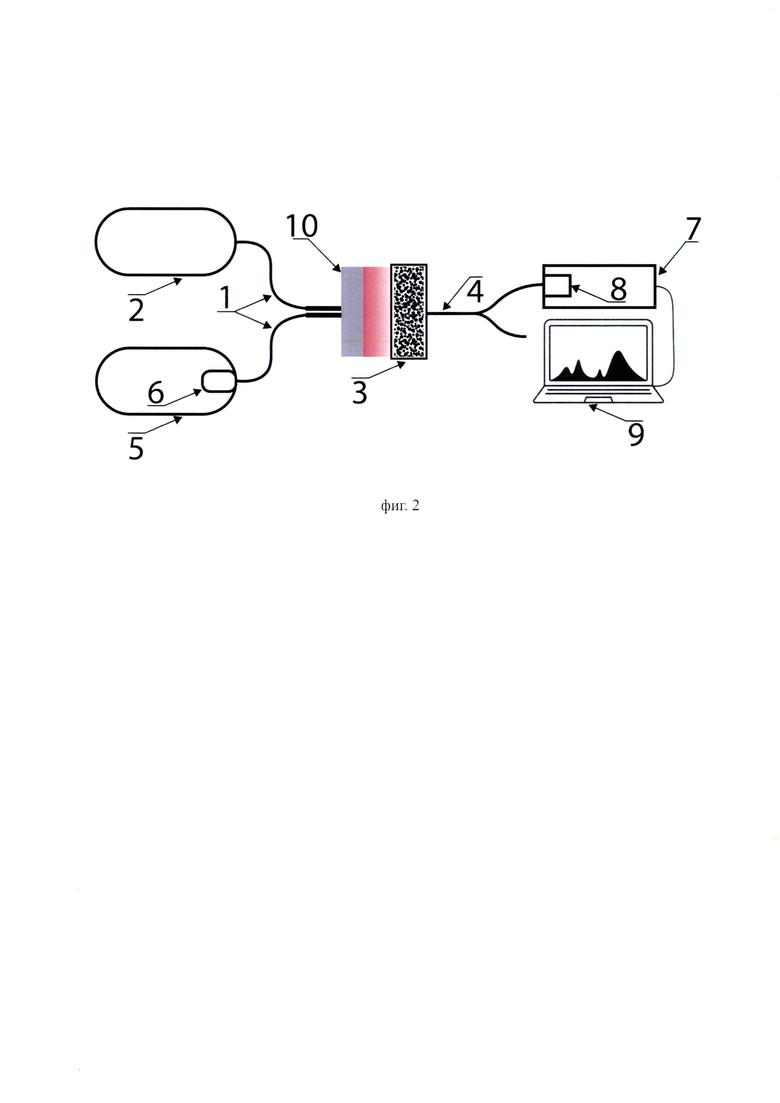
• на фиг. 2 представлена модифицированная схема предложенного устройства и метода исследования фотодинамической активности фотосенсибилизаторов на основе хлорина е6;
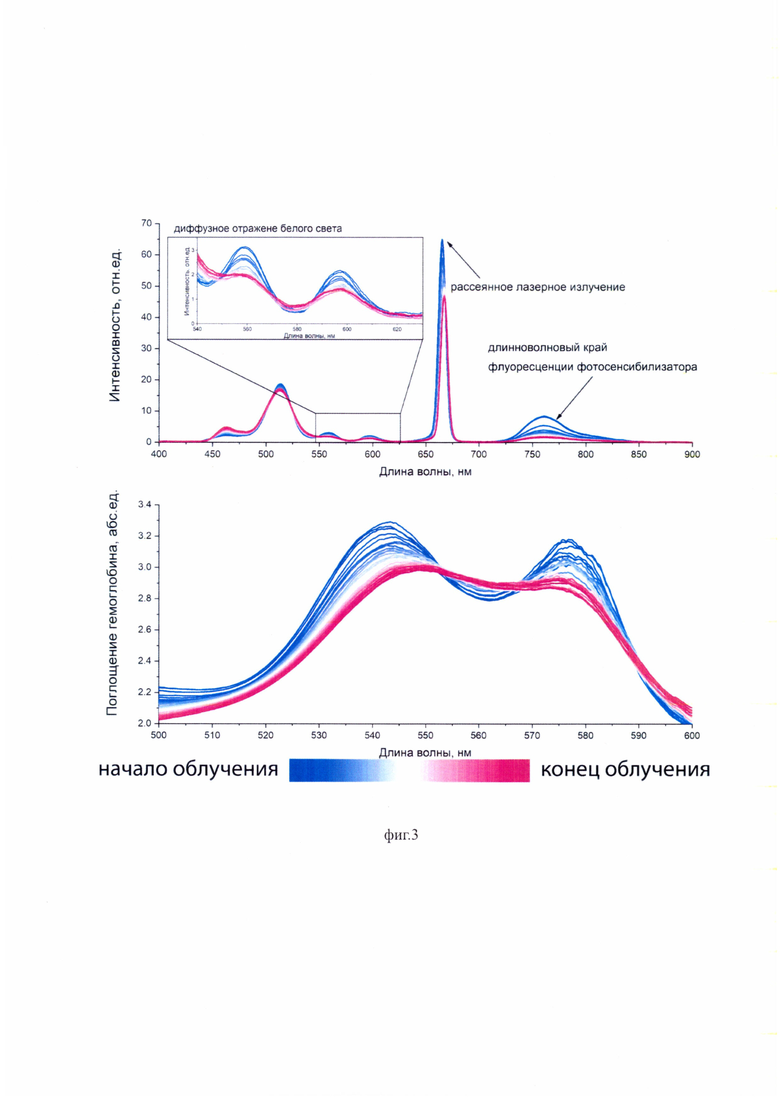
• на фиг. 3 представлены регистрируемые предложенным устройством спектры в процессе проведения фотодинамической терапии, которые включают диффузное отражение/пропускание белого света (поглощение гемоглобина), рассеянное лазерное излучение и флуоресценцию хлорина е6 в ближнем инфракрасном диапазоне;
• на фиг. 4 представлено интраоперационное применение предложенного устройства и метода в процессе фотодинамического воздействия;
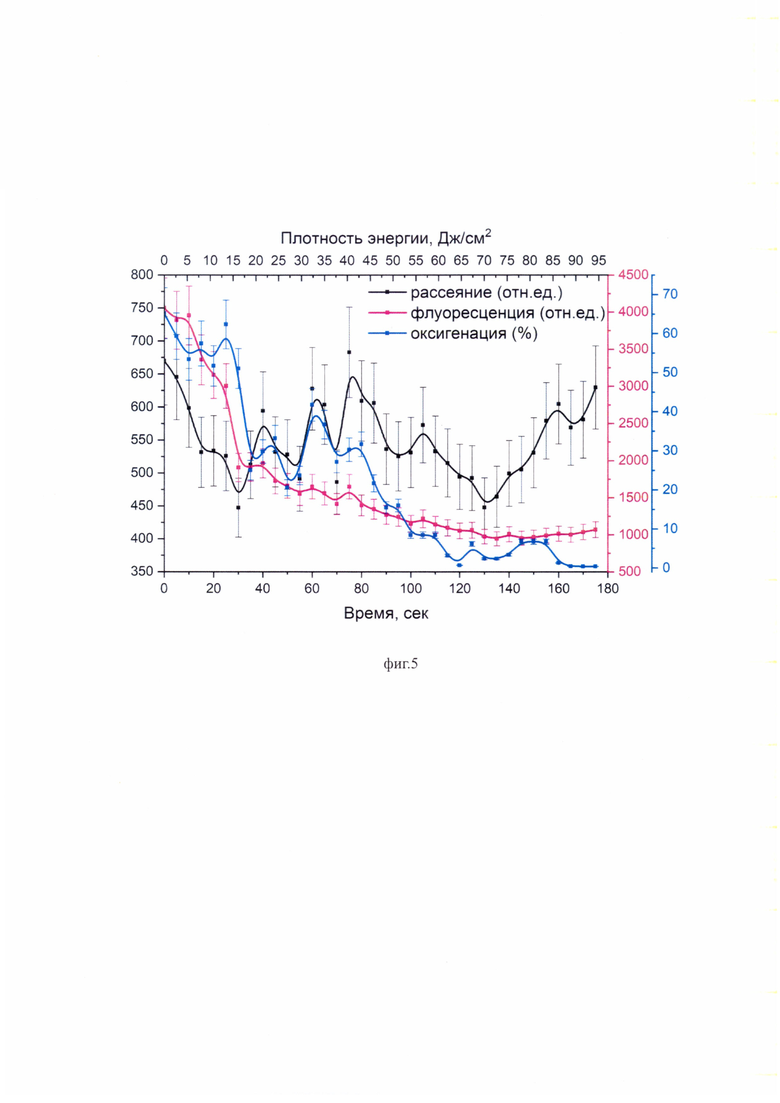
• на фиг. 5 представлены интегральные распределения интенсивностей обратно рассеянного лазерного излучения, флуоресценции хлорина е6 в ближнем инфракрасном диапазоне и оксигенации тканей опухоли пациента MP в процессе фотодинамической терапии;
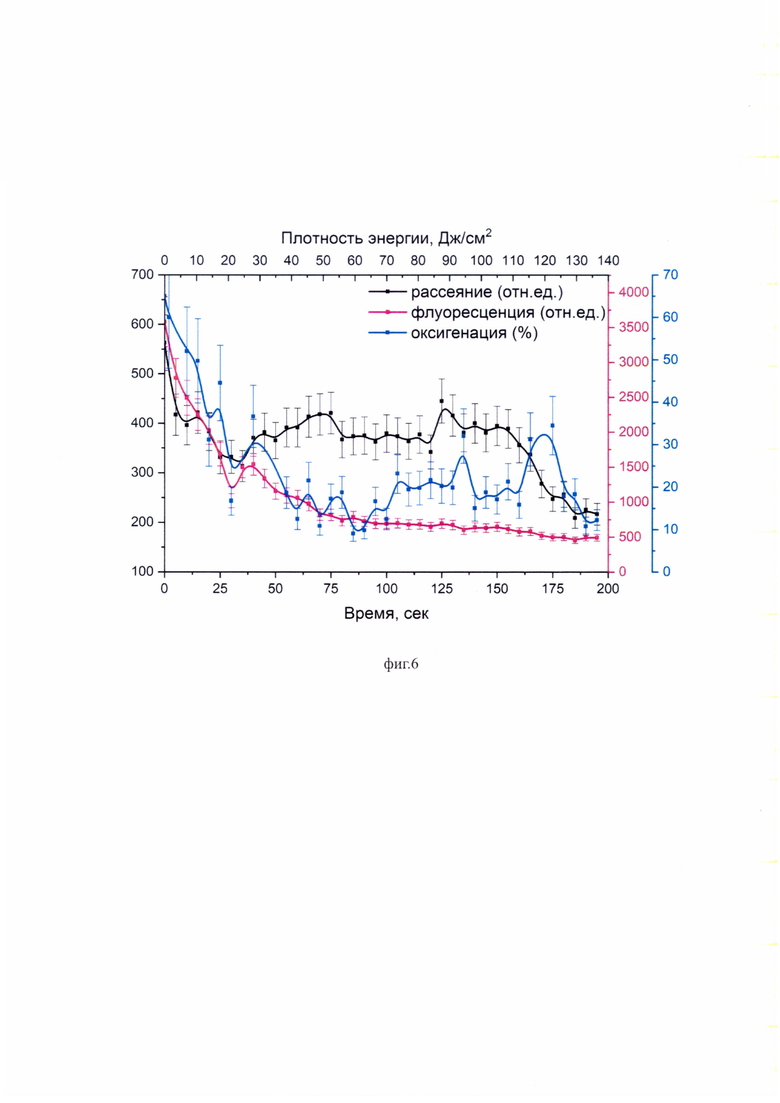
• на фиг. 6 представлены интегральные распределения интенсивностей обратно рассеянного лазерного излучения, флуоресценции хлорина е6 в ближнем инфракрасном диапазоне и оксигенации тканей опухоли пациента СА в процессе фотодинамической терапии;
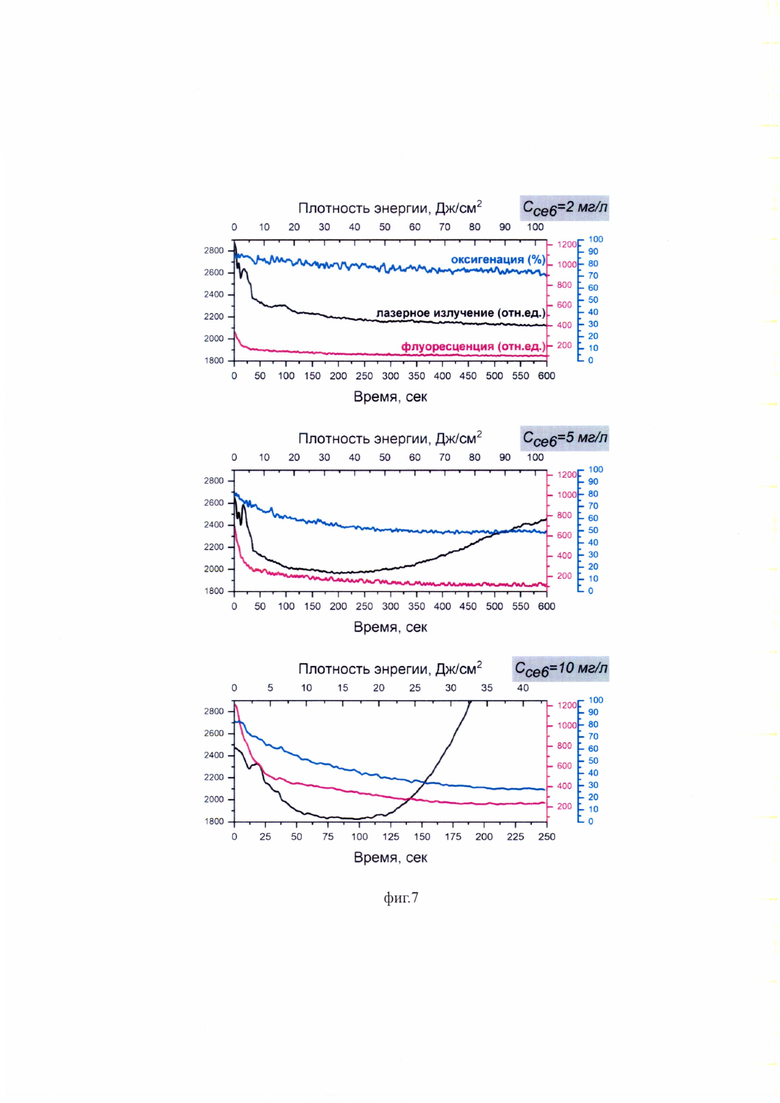
• на фиг. 7 представлены интегральные распределения интенсивностей диффузного пропускания рассеянного лазерного излучения, флуоресценции хлорина е6 в ближнем инфракрасном диапазоне и оксигенации оптических фантомов, содержащих хлорин е6 в концентрации 2, 5 и 10 мг/л, в процессе фотодинамической терапии.
Клиническое применение предлагаемого изобретения проводилось в Институте кластерной онкологии имени Л.Л. Лёвшина на базе Университетской клинической больнице №1 ФГАОУ ВО Первого МГМУ имени И.М. Сеченова Минздрава России.
Осуществление изобретения
Устройство и метод спектрально-флуоресцентного контроля состояния биологических тканей в процессе фотодинамического воздействия с применением фотосенсибилизаторов на основе хлорина е6 работают следующим образом. С помощью волоконно-оптического кабеля 1, соединенного с полупроводниковым источником лазерного излучения 2, осуществляется доставка лазерного излучения от источника к поверхности тканей 3. Волоконно-оптический зонд 4, торец которого расположен в "мягком контакте" с поверхностью облучаемых тканей 3, содержащий пучок из семи оптических волокон, обеспечивает доставку белого света (одно центральное оптическое волокно) и регистрацию спектров поглощения гемоглобина, обратно рассеянного лазерного излучения и флуоресценции фотосенсибилизатора в тканях в ближнем инфракрасном диапазоне (шесть оптических волокон, расположенных равномерно вокруг центрального). Волоконно-оптический зонд соединен с широкополосным источником белого света 5 со встроенным оптическим фильтром 6, обеспечивающим подавление длинноволновой части красного и ближнего инфракрасного диапазонов, и портативным спектрометром 7 со встроенным оптическим фильтром 8, обеспечивающим одновременную регистрацию спектров поглощения гемоглобина, обратно рассеянного лазерного излучения и флуоресценции фотосенсибилизатора в тканях в одном динамическом диапазоне. Специальное программное обеспечение на персональном компьютере 9 позволяет в режиме реального времени в процессе фотодинамического воздействия обрабатывать регистрируемые спектры и рассчитывать уровень оксигенации гемоглобина по соотношению спектров окси- и дезоксигемоглобина [Стратонников А. А., Ермишова Н.В., Лощенов В.Б. Диагностика реакции капиллярного русла тканей на лазерное излучение // Квантовая электроника. - 2002. - Т. 32. - №. 10. - С. 917-922.], интенсивности рассеянного лазерного излучения в красном диапазоне оптического спектра и флуоресценции хлорина е6 в ближнем инфракрасном диапазоне.
Изобретение позволяют исследовать фотодинамическую активность фотосенсибилизаторов на основе хлорина е6, благодаря возможности изменения геометрии воздействия светового излучения и проведения спектральной диагностики, а именно, равномерного светового облучения на просвет биологических сред, содержащих биологический субстрат, фотосенсибилизатор и эритроциты, обеспечиваемого установкой коллиматора 10 для получения параллельных пучков белого света и лазерного излучения. Данная геометрия измерений позволяет в процессе фотодинамической терапии регистрировать спектры диффузного пропускания белого света, лазерного излучения и флуоресценции хлорина е6 в одном динамическом диапазоне.
Изобретение позволяют проводить спектрально-флуоресцентое исследование распределения фотосенсибилизаторов на основе хлорина е6 в тканях опухоли в ближнем инфракрасном диапазоне спектра за счет возбуждения флуоресценции фотосенсибилизатора в биологических тканях источником лазерного излучения в красном диапазоне спектра (λ=660±5 нм) с длиной волны, соответствующей одному из пиков поглощения хлорина еб, что способствует выявлению глубокозалегающих опухолевых очагов накопления фотосенсибилизатора.
Одновременный контроль изменений оксигенации гемоглобина, оптических свойств тканей и флуоресценции хлорина е6 в процессе фотодинамического воздействия позволяет персонифицировать облучение тканей опухолей с высоким уровнем гетерогенности посредством определения оптимальных дозиметрических параметров лазерного излучения и минимизации неблагоприятных побочных эффектов, что способствует повышению эффективности проводимой терапии.
Примеры, которые демонстрируют применение предлагаемого изобретения
Пример 1. Пациент MP (75 лет) с базально-клеточным раком кожи. Диагноз по МКБ-10 при поступлении в Онкологическое отделение противоопухолевой терапии - С44.2, другие злокачественные новообразования кожи уха и наружного слухового прохода.
С целью остановить дальнейшее прогрессирования опухоли была проведена фотодинамическая терапия с применение фотосенсибилизатора на основе хлорина е6 - Фоторан Е6® (см. фиг. 1). До проведения фотодинамической терапии пациенту внутривенно капельно вводился раствор фотосенсибилизатора в концентрации 1 мг/кг. Спустя 3 часа после введения фотосенсибилизатора посредством проведения видео-флуоресцентной визуализации была выявлена патологическая сенсибилизированная зона, которая затем подвергалась фотодинамической терапии. С помощью волоконно-оптического кабеля диаметром 600 мкм к сенсибилизированным тканям опухоли подволилось лазерное излучение с длиной волны 660±5 нм (см. фиг. 4). Диаметр зоны облучения составлял 1,5 см. Плотность мощности лазерного излучения на поверхности опухоли составляла 540 мВт/см2. Торец волоконно-оптического зонда в режиме "мягкого контакта" устанавливался на поверхности облучаемых тканей. Излучение от широкополосного источника белого света с выходной мощностью 10-15 мВт доставлялось к зоне облучения с помощью центрального оптического волокна. Шесть оптических волокон волоконно-оптического зонда, подключенных к портативному спектрометру, обеспечивали одновременную регистрацию в одном динамическом диапазоне диффузно отраженного белого света в интервале длин волн 500-600 нм, обратно рассеянного лазерного излучения с длиной волны 660±5 нм и флуоресценции фотосенсибилизатора в тканях в ближнем инфракрасном диапазоне длин волн 725-800 нм. В процессе лазерного облучения двугорбый спектр поглощения, соответствующий оксигенированному гемоглобину, трансформируется в одногорбый, характерный для дезоксигенированного гемоглобина (см. фиг. 3). Специальное программное обеспечение на персональном компьютере позволяло в режиме реального времени в процессе фотодинамического воздействия обрабатывать регистрируемые с частотой 5 секунд спектры и рассчитывать уровень оксигенации гемоглобина, интегральные интенсивности обратно рассеянного лазерного излучения в диапазоне длин волн 655-675 нм и флуоресценции хлорина е6 в диапазоне длин волн 725-800 нм (см. фиг. 5). Фотодинамическое воздействие прекращалось при достижении фотобличинга фотосенсибилизатора более 70% и оксигенации гемоглобина в тканях до уровня 0-10%. Суммарная плотность энергии в зоне облучения составила 94,5 Дж/см2 (см. фиг. 5).
Пример 2. Пациент СА (69 лет) с базально-клеточным раком кожи. Диагноз по МКБ-10 при поступлении в Онкологическое отделение противоопухолевой терапии -С44.3, другие злокачественные новообразования кожи других и неуточненных частей лица. С целью остановить дальнейшее прогрессирование опухоли была проведена фотодинамическая терапия с применение фотосенсибилизатора на основе хлорина е6 - Фотодитазин® (см. фиг. 1). До проведения фотодинамической терапии пациенту внутривенно капельно вводился раствор фотосенсибилизатора в концентрации 1 мг/кг. Спустя 3 часа после введения фотосенсибилизатора проводилась видео-флуоресцентная визуализация, в результате которой была выявлена патологическая сенсибилизированная зона, которая далее подвергалась фотодинамическому воздействию. С помощью волоконно-оптического кабеля к сенсибилизированным тканям опухоли подволилось лазерное излучение с длиной волны 660±5 нм. Диаметр зоны облучения составлял 1 см. Плотность мощности лазерного излучения на поверхности опухоли составляла 715 мВт/см2. Торец волоконно-оптического зонда в режиме "мягкого контакта" устанавливался на поверхности облучаемых тканей (см. фиг. 4). Излучение от широкополосного источника белого света доставлялось к зоне облучения с помощью центрального оптического волокна. Шесть оптических волокон волоконно-оптического зонда, подключенных к портативному спектрометру, обеспечивают одновременную регистрацию в одном динамическом диапазоне диффузно отраженного белого света в диапазоне длин волн 500-600 нм, обратно рассеянного лазерного излучения с длиной волны 660±5 нм и флуоресценции тканей в ближнем инфракрасном диапазоне 725-800 нм. Специальное программное обеспечение на персональном компьютере позволяло в режиме реального времени в процессе фотодинамического воздействия обрабатывать регистрируемые с частотой 5 секунд спектры и рассчитывать уровень оксигенации, интегральные интенсивности обратно рассеянного лазерного излучения в диапазоне 655-675 нм и флуоресценции фотосенсибилизатора хлорина е6 в ближнем инфракрасном диапазоне 725-800 нм (см. фиг. 6). Фотодинамическое воздействие прекращалось при достижении фотобличинга фотосенсибилизатора более 70%, а оксигенации тканей на уровне 0-10%. Суммарная плотность энергии в зоне облучения составила 140 Дж/см2 (см. фиг. 6).
После начала лазерного воздействия в первые 25 сек в случае пациента MP и 35 сек в случае пациента СА в тканях опухоли наблюдалось резкое уменьшение интенсивности флуоресценции хлорина е6 и уровня оксигенации гемоглобина, что, в основном, было связано с тем, что в процессе фотодинамической терапии происходит утилизация растворенного в этой среде молекулярного кислорода, так как основным цитотоксическим агентом при фотодинамическом воздействии является синглетный кислород [Loschenov V.В., Konov V.I., Prokhorov А.М. Photodynamic therapy and fluorescence diagnostics // LASER PHYSICS-LAWRENCE-. - 2000. - T. 10. - №. 6. - C. 1188-1207.]. Данный процесс протекает тем быстрее, чем выше скорость фотодинамической реакции (см. фиг. 5, 6). Интенсивность обратно рассеянного лазерного излучения также резко уменьшалась, что преимущественно было связано с переходом гемоглобина из оксигенированной формы в дезоксигенированную, коэфициент поглощения которой значительно больше на длине волны 660 нм [Jacques S.L. Optical properties of biological tissues: a review // Physics in Medicine & Biology. - 2013. - T. 58. - №. 11. - C. R37.]. В определенный момент времени фотодинамической терапии наблюдалось увеличение интенсивности обратно рассеянного лазерного излучения в связи с полным тромбированием сосудистой системы облучаемой зоны [Abels С.Targeting of the vascular system of solid tumours by photodynamic therapy (PDT) // Photochemical & photobiological sciences. - 2004. - T. 3. - №. 8. - C. 765-771.], что привело к увеличению плотности тканей. Фотосенсибилизаторы на основе хлорина е6 могут вызывать полное тромбирование кровеносных сосудов в зоне лазерного воздействия [Juzeniene A. Chlorin е6-based photosensitizers for photodynamic therapy and photodiagnosis // Photodiagnosis and photodynamic therapy. - 2009. - T. 2. - №. 6. - C. 94-96.]. Можно предположить, что пока к тканям опухоли поступала кровь, наблюдался быстрый фотобличинг хлорина е6 за счет наличия оксигенированной формы гемоглобина. Данные результаты демонстрируют возможность спектрально-флуоресцентного контроля процесса тромбирования кровеносных сосудов непосредственно в процессе фотодинамической терапии. Таким образом, предлагаемое устройство для спектрально-флуоресцентного контроля состояния биологических тканей в процессе фотодинамического воздействия с применением фотосенсибилизаторов на основе хлорина е6 позволяет персонифицировать процесс фотодинамической терапии опухолей за счет определения оптимальных дозиметрических параметров фотодинамического воздействия.
Пример 3. Пример конкретной реализации возможности применения устройства для исследования фотодинамической активности фотосенсибилизаторов на основе хлорина е6. Оптические фантомы на основе эритроцитарной массы, физраствора (натрия хлорид 0,9%) и фотосенсибилизатора на основе хлорина е6 (Фотолон®) помещались в оптически прозрачную кювету для фотобиологических исследований толщиной 1 мм и шириной 10 мм. Объем оптических фантомов, имитирующих биологические ткани человека, составлял 125 мкл. Процентное содержание эритроцитарной массы от общего объема оптических фантомов составляло 10%. Концентрация фотосенсибилизатора составляла 2, 5 и 10 мг/л. В процессе светового воздействия на фантомы кювета герметично запечатывалась для избежания диффузии кислорода в среду. Световое облучение белым светом и лазерным излучением оптических фантомов проводилось на просвет (см. фиг. 2). Волоконно-оптический зонд регистрировал в процессе фотодинамической терапии спектры диффузного пропускания белого света в диапазоне длин волн 500-600 нм, лазерного излучения с длиной волны 660±5 нм и флуоресценции хлорина е6 в ближнем инфракрасном диапазоне 725-800 нм. Плотность мощности лазерного излучения на поверхности фантома составляла 173 мВт/см2, а плотность мощности белого света 11 мВт/см2. Экспериментально было подтверждено, что при включенном источнике белого света и выключенном лазерном источнике окисигенация остается на одном уровне, а изменение интенсивности сигнала флуоресценции хлорина е6 в оптическом фантоме сравнима с шумами. Основными рассеивающими частицами в данных фантомах являются цельные эритроциты, поэтому по величине рассеянного лазерного излучения можно определить процессы, происходящие с эритроцитами во время лазерного облучения. На полученных кривых интенсивности диффузного пропускания лазерного излучения виден момент времени, когда наблюдалось временное гиперосмотическое разбухание эритроцитов, увеличение интенсивности рассеяния из-за увеличения размеров рассеивающих частиц (см. фиг. 7). В дальнейшем, с увеличением концентрации фотосенсибилизатора до 5 и 10 мг/л наблюдалось увеличение интенсивности диффузного пропускания лазерного излучения из-за разрушения эритроцитов (уменьшения количества рассеивающих частиц) в процессе фотодинамической реакции (см. фиг. 7). С увеличением концентрации фотосенсибилизатора наблюдалось увеличение скорости дезоксигенации гемоглобина, а флуоресценция хлорина е6 уменьшалась по двухэкспоненциальному закону. Быстрое уменьшение интенсивности флуоресценции в начале облучения было обусловлено дезоксигенацией гемоглобина за счет реакции переноса электрона между молекулой хлорина е6 в триплетном состоянии и молекулами кислорода, которая является одним из основных механизмов фотобличинга фотосенсибилизатора [Beltukova D.М. et al. Kinetics of photobleaching of Radachlorin® photosensitizer in aqueous solutions // Chemical Physics Letters. - 2016. - T. 662. - C. 127-131]. При фотодинамической терапии происходит фотобличинг фотосенсибилизатора, содержащегося в данной среде, и данный процесс протекает медленнее при уменьшении в среде содержания молекулярного кислорода. Таким образом, предлагаемое устройство и метод спектрально-флуоресцентного контроля состояния биологических тканей в процессе фотодинамического воздействия с применением фотосенсибилизаторов на основе хлорина е6 позволяет проводить исследования фотодинамической активности фотосенсибилизаторов на основе хлорина е6.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ОПТИМАЛЬНЫХ ЭНЕРГЕТИЧЕСКИХ ПАРАМЕТРОВ ЛАЗЕРНО-ИНДУЦИРОВАННОЙ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ДИСПЛАЗИИ И РАКА ШЕЙКИ МАТКИ | 2023 |
|
RU2815258C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ НОВООБРАЗОВАНИЙ ШЕЙКИ МАТКИ И ВУЛЬВЫ ПОД КОНТРОЛЕМ СОВМЕСТНОЙ ВИДЕО- И СПЕКТРАЛЬНО-ФЛУОРЕСЦЕНТНОЙ ДИАГНОСТИКИ С ПРИМЕНЕНИЕМ ФОТОСЕНСИБИЛИЗАТОРОВ ХЛОРИНОВОГО РЯДА | 2021 |
|
RU2782643C1 |
| Способ внутрипротоковой фототераностики холангиоцеллюлярного рака | 2021 |
|
RU2767264C1 |
| УСТРОЙСТВО ДЛЯ ПРОВЕДЕНИЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ С ВОЗМОЖНОСТЬЮ ОДНОВРЕМЕННОГО СПЕКТРАЛЬНО-ФЛУОРЕСЦЕНТНОГО КОНТРОЛЯ ФОТОБЛИЧИНГА ФОТОСЕНСИБИЛИЗАТОРА | 2021 |
|
RU2777486C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2438733C1 |
| СПОСОБ КОМБИНИРОВАННОЙ ЛУЧЕВОЙ И ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2019 |
|
RU2724480C2 |
| УСТРОЙСТВО ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ РЕЗИДУАЛЬНЫХ ОПУХОЛЕЙ ГОЛОВНОГО МОЗГА С ФЛУОРЕСЦЕНТНЫМ КОНТРОЛЕМ ФОТООБЕСЦВЕЧИВАНИЯ ФОТОСЕНСИБИЛИЗАТОРА | 2021 |
|
RU2801893C2 |
| Способ фотодинамической диагностики и терапии центрального рака легкого и устройство его осуществления | 2019 |
|
RU2736909C1 |
| УСТРОЙСТВО ДЛЯ ФЛУОРЕСЦЕНТНОЙ НАВИГАЦИИ В НЕЙРОХИРУРГИИ | 2017 |
|
RU2661029C1 |
| СПЕКТРАЛЬНОЕ УСТРОЙСТВО ДЛЯ КОНТРОЛЯ И МОНИТОРИНГА ПРОЦЕССА ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2000 |
|
RU2169590C1 |

Изобретение относится к медицинской технике. Техническим результатом изобретения является осуществление спектрально-флуоресцентного контроля состояния тканей опухолей с высоким уровнем гетерогенности, обеспечивающего одновременное контролирование фотобличинга фотосенсибилизатора в ближнем инфракрасном диапазоне, оксигенации и оптических свойств биологических тканей (поглощающие и рассеивающие свойства) непосредственно в процессе фотодинамической терапии. Устройство включает полупроводниковый источник лазерного излучения с длиной волны 660±5 нм для возбуждения флуоресценции хлорина Е6, волоконно-оптический кабель для доставки лазерного излучения от источника к поверхности тканей, широкополосный источник белого света со встроенным оптическим фильтром, отсекающим длинноволновую часть спектра красного и ближнего инфракрасного диапазонов, портативный спектрометр со встроенным оптическим фильтром для регистрации в одном динамическом диапазоне спектров поглощения окси- и дезоксигемоглобина в диапазоне 500-600 нм, обратно рассеянного лазерного излучения и флуоресценции хлорина Е6 в ближнем инфракрасном диапазоне, а также волоконно-оптический зонд, который обеспечивает доставку белого света и регистрацию спектров поглощения окси- и дезоксигемоглобина, обратно рассеянного лазерного излучения и флуоресцентного сигнала тканей в ближнем инфракрасном диапазоне. 7 ил.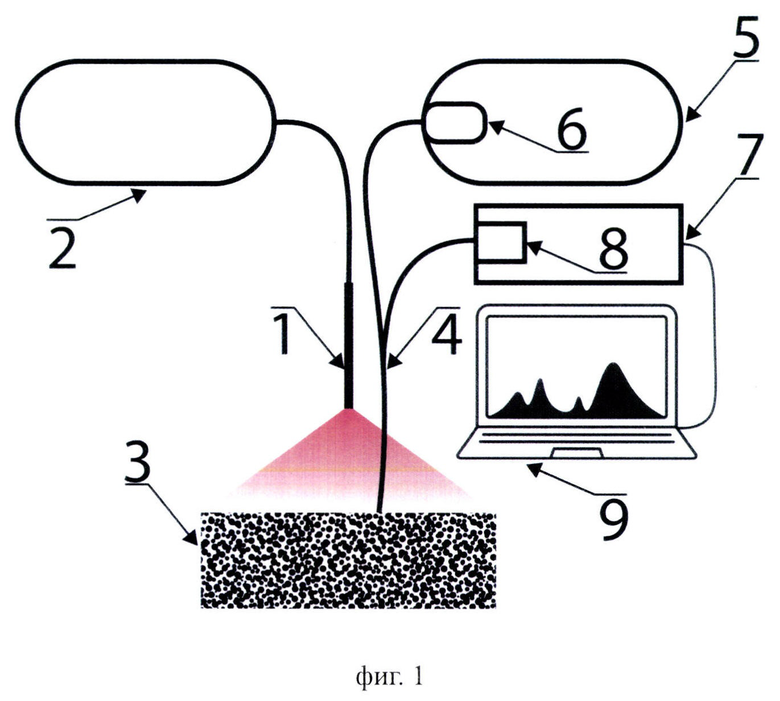
Устройство для спектрально-флуоресцентного контроля состояния биологических тканей в процессе фотодинамического воздействия с применением фотосенсибилизаторов на основе хлорина Е6, включающее волоконно-оптический кабель, соединенный с полупроводниковым источником лазерного излучения с возможностью регулирования мощности излучения, обеспечивающий доставку лазерного излучения к поверхности биотканей для возбуждения флуоресценции фотосенсибилизатора и запуска фотодинамической реакции, волоконно-оптический зонд, обеспечивающий доставку лазерного излучения от широкополосного источника белого света со встроенным оптическим фильтром, отсекающим длинноволновую часть спектра красного и ближнего инфракрасного диапазонов, и регистрацию в одном динамическом диапазоне спектров поглощения гемоглобина, рассеянного лазерного излучения и флуоресценции фотосенсибилизаторов на основе хлорина Е6 портативным спектрометром со встроенным оптическим фильтром, который соединен с персональным компьютером с программным обеспечением, позволяющим в процессе фотодинамической терапии в режиме реального времени обрабатывать регистрируемые спектры и рассчитывать изменения уровня оксигенации, интенсивности рассеянного лазерного излучения и флуоресценции фотосенсибилизатора в ближнем инфракрасном диапазоне.
| УСТРОЙСТВО ДЛЯ ПРОВЕДЕНИЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ С ВОЗМОЖНОСТЬЮ ОДНОВРЕМЕННОГО СПЕКТРАЛЬНО-ФЛУОРЕСЦЕНТНОГО КОНТРОЛЯ ФОТОБЛИЧИНГА ФОТОСЕНСИБИЛИЗАТОРА | 2021 |
|
RU2777486C1 |
| Способ внутрипротоковой фототераностики холангиоцеллюлярного рака | 2021 |
|
RU2767264C1 |
| ПЕРЕСТАВИТЕЛЬ СТЕКЛОИЗДЕЛИЙ | 0 |
|
SU203175A1 |
| Способ фотодинамической диагностики и терапии центрального рака легкого и устройство его осуществления | 2019 |
|
RU2736909C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2539367C1 |
Авторы
Даты
2023-11-09—Публикация
2022-12-12—Подача