Текст описания в факсимильном виде (см. графическую часть)н
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАРИАНТЫ КОШАЧЬИХ АНТИТЕЛ | 2021 |
|
RU2840969C1 |
| ОДНОВАЛЕНТНЫЕ МОДУЛИ-ПЕРЕНОСЧИКИ ЧЕРЕЗ ГЕМАТОЭНЦЕФАЛИТИЧЕСКИЙ БАРЬЕР | 2014 |
|
RU2799436C1 |
| IN VITRO ПРОГНОЗИРОВАНИЕ ВРЕМЕНИ ПОЛУЖИЗНИ АНТИТЕЛ IN VIVO | 2015 |
|
RU2688349C2 |
| ПОЛИПЕПТИДНЫЕ ВАРИАНТЫ С ИЗМЕНЕННОЙ ЭФФЕКТОРНОЙ ФУНКЦИЕЙ | 2005 |
|
RU2367667C2 |
| ИНДУЦИРУЮЩИЙ ЦИТОТОКСИЧНОСТЬ ТЕРАПЕВТИЧЕСКИЙ АГЕНТ | 2011 |
|
RU2663123C2 |
| УЛУЧШЕННЫЕ СПОСОБЫ ЛЕЧЕНИЯ ВАСКУЛЯРИЗИРОВАННЫХ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 2015 |
|
RU2692248C2 |
| ОДНОВАЛЕНТНЫЕ МОДУЛИ-ПЕРЕНОСЧИКИ ЧЕРЕЗ ГЕМАТОЭНЦЕФАЛИЧЕСКИЙ БАРЬЕР | 2014 |
|
RU2694659C2 |
| ИНДУЦИРУЮЩИЙ ЦИТОТОКСИЧНОСТЬ ТЕРАПЕВТИЧЕСКИЙ АГЕНТ | 2011 |
|
RU2774414C2 |
| ПРЕДПОЧТИТЕЛЬНОЕ СПАРИВАНИЕ ДОМЕНОВ АНТИТЕЛ | 2018 |
|
RU2792440C2 |
| ПОЛИПЕПТИДЫ И ПОЛИНУКЛЕОТИДЫ И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ИММУНОЛОГИЧЕСКИХ НАРУШЕНИЙ И РАКА | 2012 |
|
RU2623161C2 |







































































































































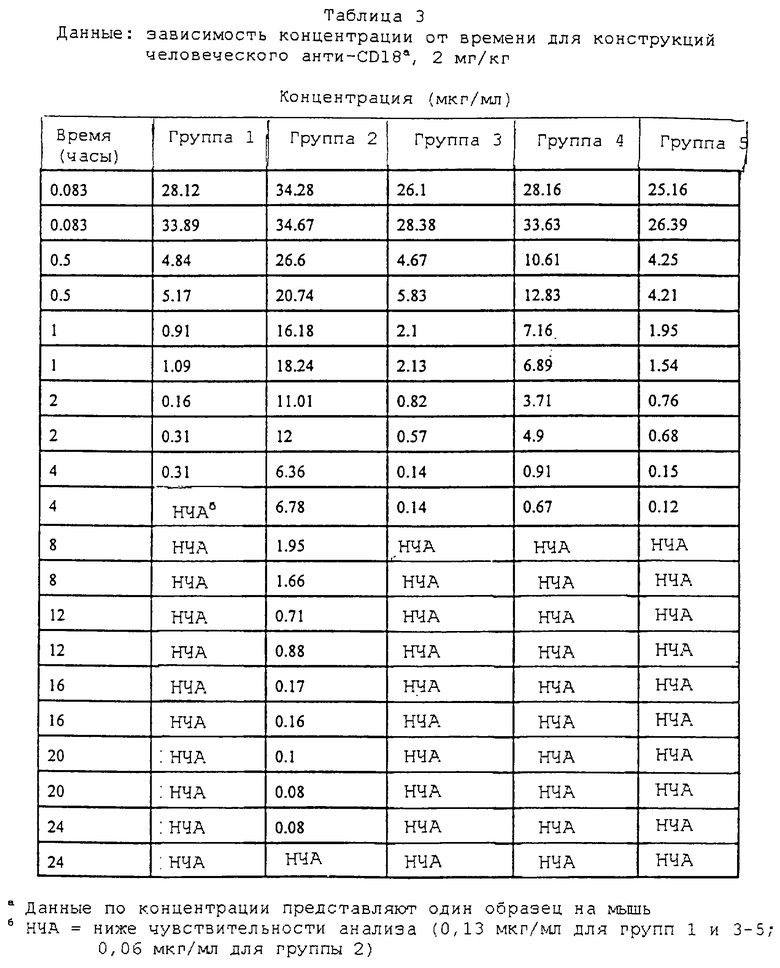












Изобретение относится к биотехнологии, может быть использовано в медицинской практике и касается полипептида, который выводится через почки и не содержит в своей исходной форме Fc-области IgG. Исходный полипептид модифицируют так, чтобы включить спасательный рецепторсвязывающий эпитоп Fc-области IgG и посредством этого увеличить циркуляторное время полужизни. Модифицированный полипептид содержит аминокислотную последовательность Ig-домена или Ig-подобного, который не является СН2-доменом, и аминокислотную последовательность спасательного рецепторсвязывающего эпитопа Fc-области IgG, расположенную в пределах Ig-домена или Ig-подобного домена. Аминокислотная последовательность модифицированного полипептида, по меньшей мере, на 70% идентична таковой исходного полипептида. Раскрыт способ получения указанного полипептида с использованием ДНК (в конструкции вектора), кодирующей указанный полипептид. Полученный полипептид может использоваться для лечения опосредованного LFA-1 нарушения у млекопитающих, в том числе человека. Изобретение позволяет увеличить время полужизни полипептида, за счет чего повышается эффективность лечения. 8 с. и 17 з.п. ф-лы, 4 ил., 3 табл.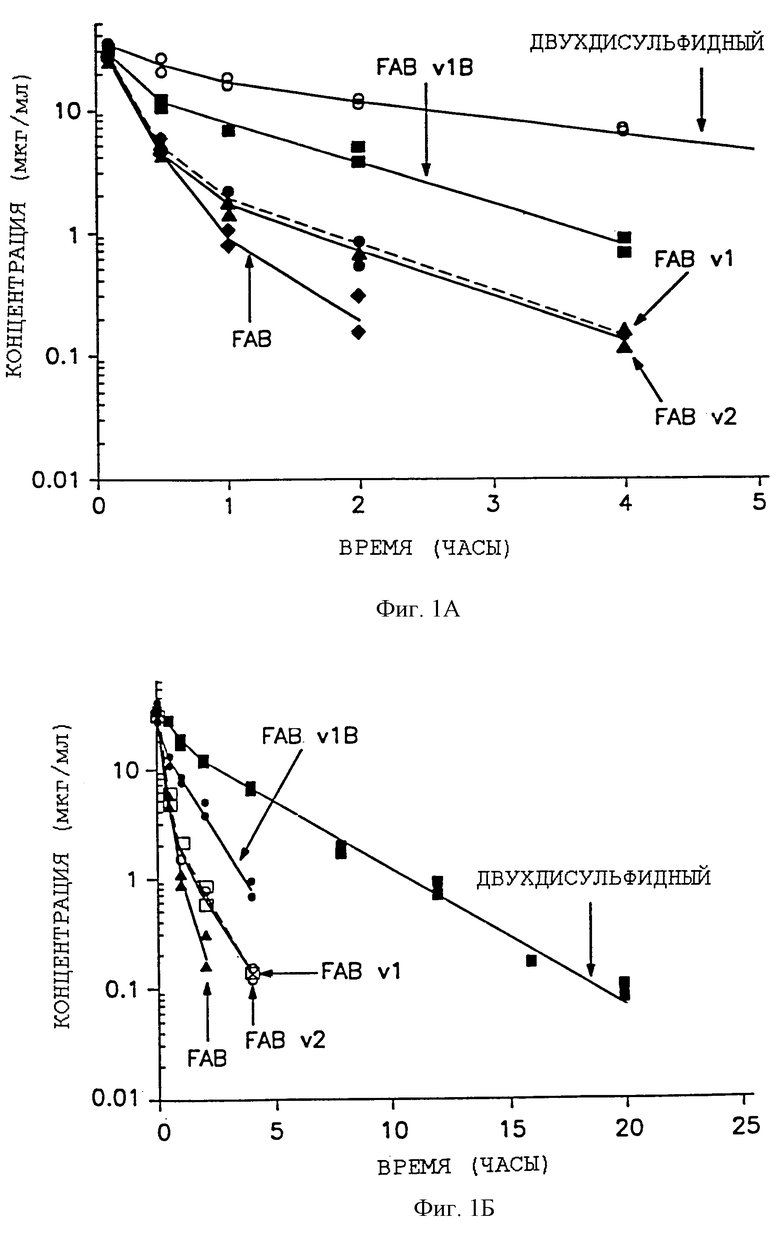
| WO 9404689 А, 03.03.1994 | |||
| J | |||
| Batra et al | |||
| Приспособление с иглой для прочистки кухонь типа "Примус" | 1923 |
|
SU40A1 |
| J.Molecular Immunology, v.30, № 4, 1993 | |||
| WO 9322332 A, 11.11.1993. | |||
Авторы
Даты
2004-02-27—Публикация
1996-03-28—Подача