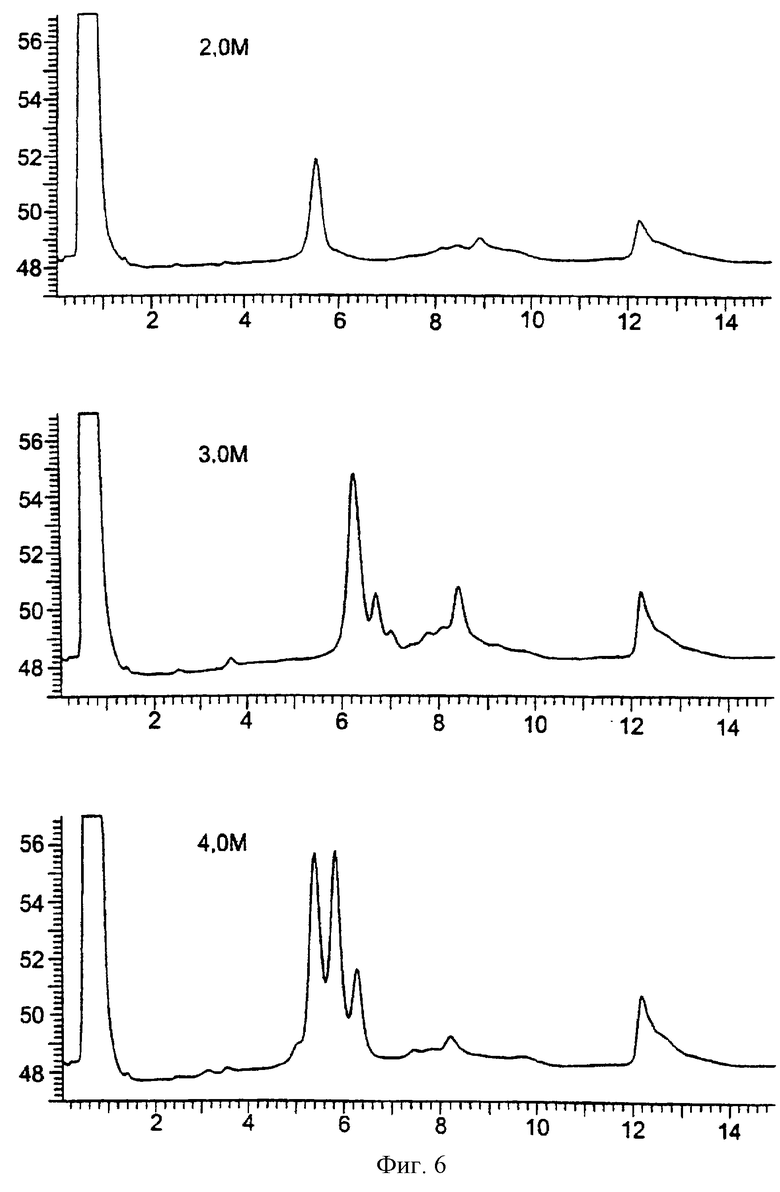
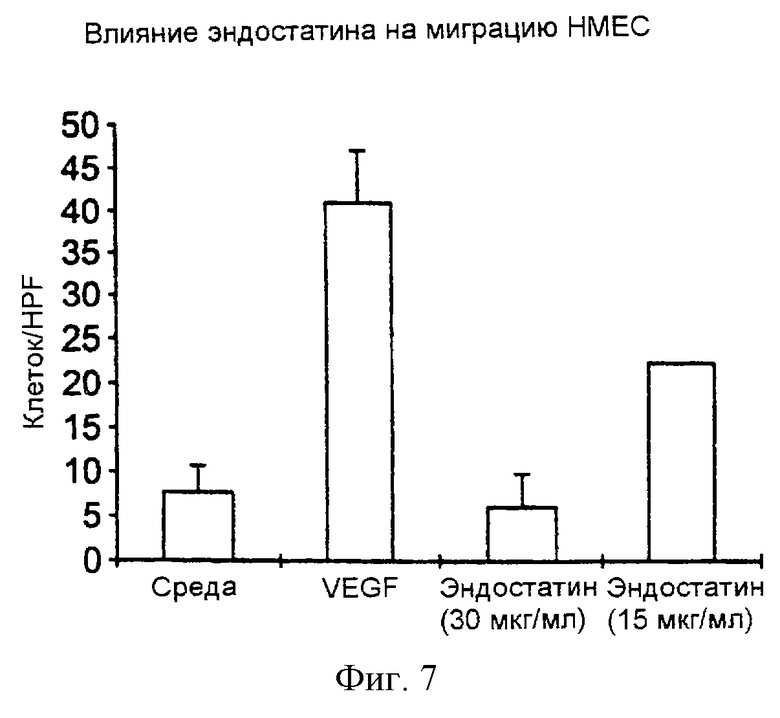
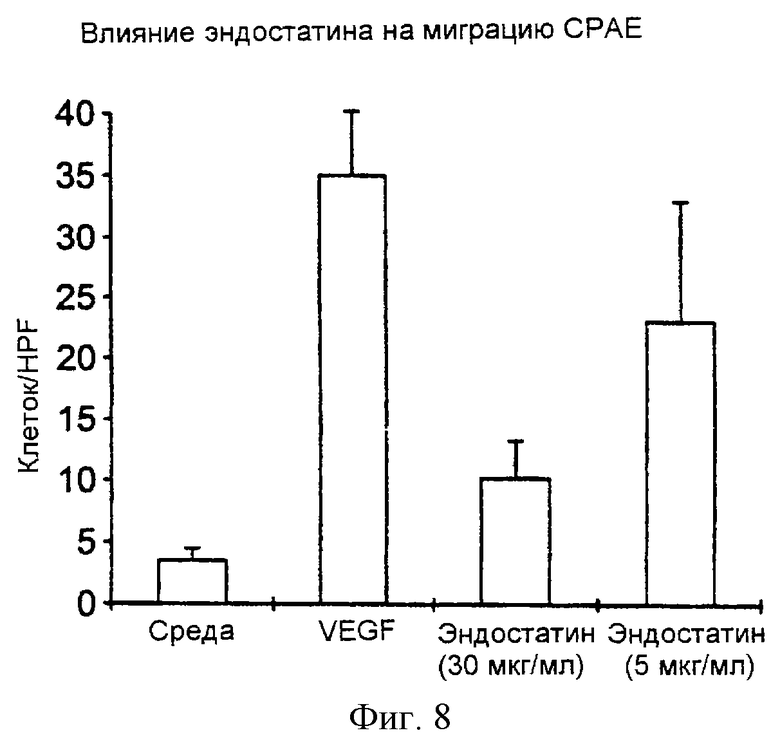
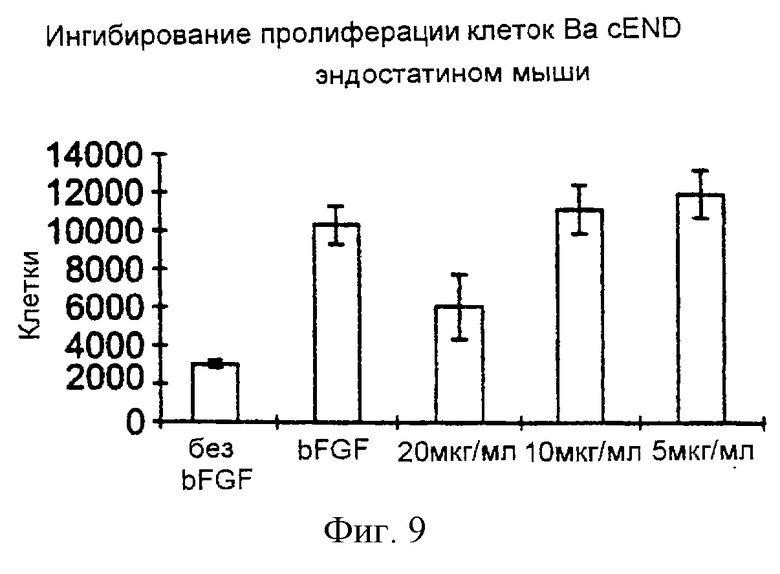
Текст описания в факсимильном виде (см. графическую часть).
Изобретение относится к производству эндостатина мыши и человека. Сущность изобретения заключается в создании способа получения и очистки эндостатина из внутриклеточных телец, экспрессируемых в клетках бактерий и нуклеиновых кислотах, кодирующие эндостатин полной длины и укороченные формы эндостатина. Технический результат - расширение арсенала средств для диагностики и лечения новообразований. 3 с. и 88 з.п. ф-лы, 10 ил., 3 табл.
1. Способ получения эндостатина, предусматривающий следующие стадии:
(а) культивирование клеток-хозяев, которые экспрессируют ген эндостатина;
(б) выделение продукта экспрессии указанного гена;
(в) растворение указанного генного продукта при повышенном значении рН;
(г) рефолдинг указанного растворенного генного продукта при значениях рН приблизительно 6-8,5 и
(д) выделение правильно упакованных форм указанного генного продукта.
2. Способ получения эндостатина, предусматривающий следующие стадии:(а) культивирование клеток-хозяев, которые экспрессируют ген эндостатина;
(б) выделение продукта экспрессии указанного гена;
(в) рефолдинг указанного генного продукта при значениях рН приблизительно 6-8,5 и
(г) выделение правильно упакованных форм указанного генного продукта.
3. Способ по п.1, при котором указанное повышенное значение рН на стадии растворения составляет приблизительно 9-11,5.4. Способ по п.3, при котором указанное повышенное значение рН составляет приблизительно 10-11.5. Способ по п.4, при котором указанное повышенное значение рН приблизительно составляет рН 10,5.6. Способ по п.2, при котором указанное значение рН на стадии рефолдинга составляет приблизительно 7,0-8,0.7. Способ по п.6, при котором указанное значение рН на стадии рефолдинга приблизительно составляет 7,5.8. Способ по п.1 или 2, при котором на указанной стадии растворения, если таковая стадия предусмотрена, мочевина присутствует в концентрации, составляющей приблизительно 4-10 М.9. Способ по п.8, при котором на указанной стадии растворения мочевина присутствует в концентрации, составляющей приблизительно 6 М.10. Способ по п.1 или 2, при котором на указанной стадии рефолдинга мочевина присутствует в концентрации, составляющей приблизительно 0,5-5 М.11. Способ по п.10, при котором на указанной стадии рефолдинга мочевина присутствует в концентрации, составляющей приблизительно 3,5 М.12. Способ по п.1 или 2, при котором на указанной стадии растворения, если таковая стадия предусмотрена, гуанидингидрохлорид присутствует в концентрации, составляющей приблизительно 2-8 М.13. Способ по п.12, при котором на указанной стадии растворения гуанидингидрохлорид присутствует в концентрации, составляющей приблизительно 4 М.14. Способ по п.1 или 2, при котором на указанной стадии рефолдинга гуанидингидрохлорид присутствует в концентрации, составляющей приблизительно 0,2-2 М.15. Способ по п.14, при котором на указанной стадии рефолдинга гуанидингидрохлорид присутствует в концентрации, составляющей приблизительно 1,5 М.16. Способ по п.1 или 2, выполняемый в присутствии восстановителя, способного восстанавливать дисульфидные связи до сульфгидрильных групп.17. Способ по п.16, при котором указанный восстановитель выбран из группы, состоящей из DTT, ВМЕ, цистеина и восстановленного глутатиона.18. Способ по п.17, при котором на указанной стадии растворения, если таковая стадия предусмотрена, DTT присутствует в концентрации, составляющей приблизительно 2-10 мМ.19. Способ по п.18, при котором на указанной стадии растворения DTT присутствует в концентрации, составляющей приблизительно 5 мМ.20. Способ по п.17, при котором на указанной стадии рефолдинга DTT присутствует в концентрации, составляющей приблизительно 0,2-2 мМ.21. Способ по п.20, при котором на указанной стадии рефолдинга DTT присутствует в концентрации, составляющей приблизительно 0,5 мМ.22. Способ по п.17, при котором на указанной стадии растворения, если таковая стадия предусмотрена, восстановленный глутатион присутствует в концентрации, составляющей приблизительно 5-20 мМ.23. Способ по п.22, при котором на указанной стадии растворения восстановленный глутатион присутствует в концентрации, составляющей приблизительно 10 мМ.24. Способ по п.17, при котором на указанной стадии рефолдинга восстановленный глутатион присутствует в концентрации, составляющей приблизительно 1-4 мМ.25. Способ по п.24, при котором на указанной стадии рефолдинга восстановленный глутатион присутствует в концентрации, составляющей приблизительно 2 мМ.26. Способ по п.17, при котором на указанной стадии растворения, если таковая стадия предусмотрена, цистеин присутствует в концентрации, составляющей приблизительно 5-20 мМ.27. Способ по п.26, при котором на указанной стадии растворения цистеин присутствует в концентрации, составляющей приблизительно 10 мМ.28. Способ по п.17, при котором на указанной стадии рефолдинга цистеин присутствует в концентрации, составляющей приблизительно 0,5-4 мМ.29. Способ по п.28, при котором на указанной стадии рефолдинга цистеин присутствует в концентрации, составляющей приблизительно 1 мМ.30. Способ по п.1 или 2, при котором в ходе указанной стадии рефолдинга присутствует агент, способный усиливать смену дисульфидных связей.31. Способ по п.30, при котором в качестве указанного агента выбран либо цистин, либо окисленный глутатион.32. Способ по п.31, при котором на указанной стадии рефолдинга цистин присутствует в концентрации, составляющей приблизительно 0,2-5 мМ.33. Способ по п.32, при котором на указанной стадии рефолдинга цистин присутствует в концентрации, составляющей приблизительно 1 мМ.34. Способ по п.1 или 2, при котором образование дисульфидных связей в ходе указанной стадии рефолдинга происходит благодаря окислению кислородом воздуха.35. Способ по п.34, при котором указанная стадия окисления кислородом воздуха проводится в течение приблизительно 12-96 ч.36. Способ по п.35, при котором указанная стадия окисления кислородом воздуха проводится в течение приблизительно 24-72 ч.37. Способ по п.36, при котором указанная стадия окисления кислородом воздуха проводится приблизительно в течение 60 ч.38. Способ по п.1 или 2, при котором концентрация указанного генного продукта в ходе указанной стадии растворения, если таковая стадия предусмотрена, составляет приблизительно 1-20 мг/мл.39. Способ по п.38, при котором концентрация указанного генного продукта в ходе указанной стадии растворения составляет приблизительно 2,5 мг/мл.40. Способ по п.1 или 2, при котором концентрация указанного генного продукта в ходе указанной стадии рефолдинга составляет приблизительно 0,1-5 мг/мл.41. Способ по п.40, при котором концентрация указанного генного продукта в ходе указанной стадии рефолдинга составляет приблизительно от 0,25 мг/мл.42. Способ по п.1 или 2, который далее предусматривает стадию очистки эндостатина в соответствии с методикой, выбранной из группы, в которую входят ионообменная хроматография, гидрофобная хроматография и ВЭЖХ с обращенной фазой.43. Способ по п.1 или 2, при котором указанный ген экдостатина состоит из ДНК, кодирующей животный, отличный от человеческого эндостатин.44. Способ по п.1 или 2, при котором указанный ген экдостатина выбран из группы последовательностей, состоящей из SEQ ID NO: 5; SEQ ID NO: 6; SEQ ID NO: 7 и SEQ ID NO: 8.45. Способ по п.1 или 2, при котором указанный ген эндостатина состоит из ДНК, кодирующей эндостатин человека.46. Способ по п.1 или 2, при котором указанный ген эндостатина состоит из SEQ ID NO: 9.47. Способ получения эндостатина из внутриклеточных телец, выделенных из бактерий, предусматривающий следующие стадии:(а) культивирование клеток-хозяев, которые экспрессируют ген эндостатина;
(б) выделение продукта экспрессии указанного гена;
(в) растворение указанного генного продукта при повышенном значении рН;
(г) рефолдинг указанного растворенного генного продукта при значениях рН приблизительно 6-8,5 и
(д) выделение правильно упакованных форм указанного генного продукта.
48. Способ по п.47, при котором указанное повышенное значение рН на стадии растворения составляет приблизительно 9,0-11,5.49. Способ по п.48, при котором указанное повышенное значение рН составляет приблизительно 10-11.50. Способ по п.49, при котором указанное повышенное значение рН приблизительно составляет 10,5.51. Способ по п.47, при котором указанное значение рН на стадии рефолдинга составляет приблизительно 7,0-8,0.52. Способ по п.51, при котором указанное значение рН на стадии рефолдинга приблизительно составляет 7,5.53. Способ по п.47, при котором на указанной стадии растворения мочевина присутствует в концентрации, составляющей приблизительно 4-10 М.54. Способ по п.53, при котором на указанной стадии растворения мочевина присутствует в концентрации, составляющей приблизительно 6 М.55. Способ по п.47, при котором на указанной стадии рефолдинга мочевина присутствует в концентрации, составляющей приблизительно 0,5-5 М.56. Способ по п.55, при котором на указанной стадии рефолдинга мочевина присутствует в концентрации, составляющей приблизительно 3,5 М.57. Способ по п.47, при котором на указанной стадии растворения гуанидингидрохлорид присутствует в концентрации, составляющей приблизительно 2-8 М.58. Способ по п.57, при котором на указанной стадии растворения гуанидингидрохлорид присутствует в концентрации, составляющей приблизительно 4 М.59. Способ по п.47, при котором на указанной стадии рефолдинга гуанидингидрохлорид присутствует в концентрации, составляющей приблизительно 0,2-2 М.60. Способ по п.59, при котором на указанной стадии рефолдинга гуанидингидрохлорид присутствует в концентрации, составляющей приблизительно 1,5 М.61. Способ по п.47, выполняемый в присутствии восстановителя, способного восстанавливать дисульфидные связи до сульфгидрильных групп.62. Способ по п.61, при котором указанный восстановитель выбран из группы, состоящий из DTT, ВМЕ, цистеина и восстановленного глутатиона.63. Способ по п.62, при котором на указанной стадии растворения DTT присутствует в концентрации, составляющей приблизительно 2-10 мМ.64. Способ по п.63, при котором на указанной стадии растворения DTT присутствует в концентрации, составляющей приблизительно 5 мМ.65. Способ по п.62, при котором на указанной стадии рефолдинга DTT присутствует в концентрации, составляющей приблизительно 0,2-2 мМ.66. Способ по п.65, при котором на указанной стадии рефолдинга DTT присутствует в концентрации, составляющей приблизительно 0,5 мМ.67. Способ по п.62, при котором на указанной стадии растворения восстановленный глутатион присутствует в концентрации, составляющей приблизительно 5-20 мМ.68. Способ по п.67, при котором на указанной стадии растворения восстановленный глутатион присутствует в концентрации, составляющей приблизительно 10 мМ.69. Способ по п.62, при котором на указанной стадии рефолдинга восстановленный глутатион присутствует в концентрации, составляющей приблизительно 1-4 мМ.70. Способ по п.69, при котором на указанной стадии рефолдинга восстановленный глутатион присутствует в концентрации, составляющей приблизительно 2 мМ.71. Способ по п.62, при котором на указанной стадии растворения цистеин присутствует в концентрации, составляющей приблизительно 5-20 мМ.72. Способ по п.71, при котором на указанной стадии растворения цистеин присутствует в концентрации, составляющей приблизительно 10 мМ.73. Способ по п.62, при котором на указанной стадии рефолдинга цистеин присутствует в концентрации, составляющей приблизительно 0,5-4 мМ.74. Способ по п.73, при котором на указанной стадии рефолдинга цистеин присутствует в концентрации, составляющей приблизительно 1 мМ.75. Способ по п.47, при котором в ходе указанной стадии рефолдинга присутствует агент, способный усиливать смену дисульфидных связей.76. Способ по п.75, при котором в качестве указанного агента выбран либо цистин, либо окисленный глутатион.77. Способ по п.76, при котором на указанной стадии рефолдинга цистин присутствует в концентрации, составляющей приблизительно 0,2-5 мМ.78. Способ по п.77, при котором на указанной стадии рефолдинга цистин присутствует в концентрации, составляющей приблизительно 1 мМ.79. Способ по п.47, при котором образование дисульфидных связей в ходе указанной стадии рефолдинга происходит благодаря окислению кислородом воздуха.80. Способ по п.79, при котором указанная стадия окисления кислородом воздуха проводится в течение приблизительно 12-96 ч.81. Способ по п.80, при котором указанная стадия окисления кислородом воздуха проводится в течение приблизительно 24-72 ч.82. Способ по п.81, при котором указанная стадия окисления кислородом воздуха проводится приблизительно в течение 60 ч.83. Способ по п.47, при котором концентрация указанного генного продукта в ходе указанной стадии растворения составляет приблизительно 1-20 мг/мл.84. Способ по п.83, при котором концентрация указанного генного продукта в ходе указанной стадии растворения составляет приблизительно 2,5 мг/мл.85. Способ по п.47, при котором концентрация указанного генного продукта в ходе указанной стадии рефолдинга составляет приблизительно 0,1-5 мг/мл.86. Способ по п.85, при котором концентрация указанного генного продукта в ходе указанной стадии рефолдинга составляет приблизительно 0,25 мг/мл.87. Способ по п.47, который далее предусматривает стадию очистки эндостатина в соответствии с методикой, выбранной из группы, в которую входят ионообменная хроматография, гидрофобная хроматография и ВЭЖХ с обращенной фазой.88. Способ по п.47, при котором указанный ген эндостатина состоит из ДНК, кодирующей животный, отличный от человеческого эндостатин.89. Способ по п.47, при котором указанный ген эндостатина выбран из группы последовательностей, состоящей из SEQ ID NO: 5; SEQ ID NO: 6; SEQ ID NO: 7 и SEQ ID NO: 8.90. Способ по п.47, при котором указанный ген эндостатина состоит из ДНК, кодирующей эндостатин человека.91. Способ по п.47, при котором указанный ген эндостатина состоит из SEQ ID NO: 9.