Изобретение относится к фторорганической химии, а именно к способу получения фторангидридов полифторалкоксипропионовых кислот формулы
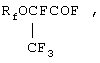
где Rf - перфторалкил C1-С9, перфторалкоксиалкил C1-С9 линейного или разветвленного строения, возможно, содержащие другие атомы галогенов, H.
Данные соединения используются в качестве промежуточных продуктов для синтеза перфторалкилвиниловых эфиров, а также для получения эмульгаторов, фторсодержащих ПАВ, химически и термически устойчивых жидкостей, смазочных масел, полимеров (В.А. Пономаренко. Фторсодержащие гетероцепные полимеры, 1973, c. 118-123).
Известные способы получения фторангидридов перфторалкоксипропионовых кислот основаны на взаимодействии гексафторпропиленоксида (ОГФП) с фторангидридами перфторкарбоновых кислот
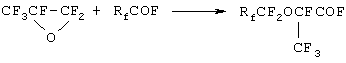
Синтез осуществляют в среде полярного органического растворителя при температуре от -80 до 200°С в присутствии различных катализаторов, например галогенидов щелочных металлов (US 3250808, 10.05.60; ЕР 265052, 27.04.88), четвертичных солей аммония (WO 97/44303, 27.11.97), трис-диметиламинодифторфосфорана (DЕ 2461445, 08.07.76), сульфониевых солей (US 4081466, 28.03.78), тетраалкилмочевины (JP 2-4733, 09.01 90).
В вышеуказанных способах реакцию ОГФП с низкокипящими фторангидридами перфторкарбоновых кислот, такими как карбонилфторид и трифторацетилфторид, обычно проводят под давлением, которое составляет от 0,7 до 24 атм. Это затрудняет проведение процесса и требует специального оборудования.
Известен метод получения галогенированных фторангидридов карбоновых кислот взаимодействием фторангидрида формулы RCOF (R - ССl3 или группа X(CF2)n, где Х=Н, Вr или SO2F, n=1-6) с ОГФП в присутствии каталитической системы, состоящей из фторида щелочного металла и двух полярных апротонных растворителей - динитрила насыщенной алифатической дикарбоновой кислоты С5-C8 и простого эфира формулы СН3О(СН2СН2O)zСН3 (z=2-6) (US 4940814, 10.07.90). Реакцию проводят при температуре от -30 до 100°С. Количество катализатора составляет 5-45% от веса фторангидрида карбоновой кислоты.
Применяемая каталитическая система для реакции фторангидридов перфторированных карбоновых кислот с ОГФП недостаточно эффективна, так как выходы целевых продуктов ниже 50%.
Наиболее близким техническим решением является способ получения фторангидридов перфторалкоксипропионовых кислот формулы

где Rf = перфторалкил C1-С8, n=0-4, каталитической реакцией ОГФП с фторангидридом перфторкарбоновой кислоты формулы R'f COF (R'f - фтор или перфторалкил C1-С7) в полярном апротонном растворителе при температуре от -50 до 20°С (GB 1550268, 08.08.79, прототип). В качестве катализатора применяют N,N,N’,N’-тетразамещенный диаминодифторметан формулы

где R1-R4 - алкил C1-C4, а также NR1R3 или NR2R4 представляют пяти- или шестичленный гетероцикл, возможно, содержащий –O-, 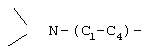 алкил или
алкил или  . Полярный апротонный растворитель, например ацетонитрил или диглим, может включать до двух объемных частей инертного неполярного растворителя, например пентана, гексана, циклогексана, или фторсодержащего алкана, в частности трифтортрихлорэтана. В конкретных примерах осуществления данного способа в качестве исходного фторангидрида используют только фторангидрид пентафторпропионовой кислоты, при взаимодействии которого с ОГФП получают смесь низкомолекулярных олигомеров, состоящую в основном из димеров, тримеров и тетрамеров ОГФП, с суммарным выходом 75-90%.
. Полярный апротонный растворитель, например ацетонитрил или диглим, может включать до двух объемных частей инертного неполярного растворителя, например пентана, гексана, циклогексана, или фторсодержащего алкана, в частности трифтортрихлорэтана. В конкретных примерах осуществления данного способа в качестве исходного фторангидрида используют только фторангидрид пентафторпропионовой кислоты, при взаимодействии которого с ОГФП получают смесь низкомолекулярных олигомеров, состоящую в основном из димеров, тримеров и тетрамеров ОГФП, с суммарным выходом 75-90%.
Недостатком способа является низкая селективность процесса получения целевых продуктов моноприсоединения - фторангидридов перфторалкоксипропионовых кислот и их невысокий выход, который, например, для перфторпропоксипропионилфторида составляет 6-12%.
Задачей изобретения является разработка универсального селективного метода синтеза, обеспечивающего высокий выход фторангидридов полифторалкоксипропионовых кислот.
Поставленная задача достигается взаимодействием гексафторпропеноксида с фторангидридом полифторкарбоновой кислоты в среде, представляющей два несмешивающихся органических растворителя, в присутствии катализатора -N,N,N',N'-тетразамещенного диаминометана формулы
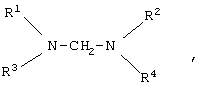
где R1-R4 - линейные или разветвленные алкил C1-С6 или перфторалкил C1-С6, группа C2H4OH или R1 и R2 и/или R3 и R4 совместно с атомом азота могут образовывать гетероциклический остаток, возможно, содержащий еще один гетероатом - кислород или азот и замещенный одной или несколькими алкильными группами.
В качестве катализаторов могут быть использованы бис(диметиламино)метан, бис(диэтиламино)метан, ди(пиперидино)метан, ди(морфолино)метан, бис(диоксиэтил) аминометан.
Применяемое количество катализатора в реакции составляет ~10-15 вес.% от количества используемого перфторированного эпоксида. Уменьшение количества катализатора приводит к снижению выхода целевых продуктов, а увеличение его количества выше 15 вес.% нецелесообразно.
В данном способе используют двухкомпонентный органический растворитель, образующий два слоя жидкой фазы за счет несмешиваемости компонентов.
Одним из компонентов является полярный апротонный растворитель, в котором протекает конденсация гексафторпропеноксида с фторангидридами полифторкарбоновых кислот. В качестве таких растворителей используют алифатические простые полиэфиры, например диалкиловые эфиры этиленгликоля, полиэтиленгликолей и нитрилы - пропионитрил, бензонитрил и ацетонитрил.
Другим компонентом органической среды является перфторированный неполярный растворитель, представляющий перфторированный циклический С7-С11 или алифатический С6-С9 углеводород, способный избирательно растворять продукты реакции и инертный по отношению к ним. Он экстрагирует образующиеся фторангидриды полифторалкоксипропионовых кислот и выводит их непосредственно из реакционной зоны. Это обеспечивает селективность образования продуктов моноприсоединения и исключает образование высокомолекулярных олигомерных аддуктов.
Наиболее предпочтительными перфторированными растворителями являются перфторгептан, перфтороктан, перфторметилциклогексан, перфтор-1,3-диметилциклогексан, перфтордекалин, перфторметилдекалин. Содержание перфторированного растворителя в органической среде находится в пределах 80-90 вес.%, что достаточно для экстракции целевых продуктов.
Конденсацию ОГФП с фторангидридами полифторкарбоновых кислот ведут при температуре от -20 до 20°С. При более низкой температуре скорость реакции замедляется, а нагревание реакционной смеси выше 20°С приводит к снижению выхода целевых продуктов.
Фторангидриды карбоновых кислот, которые могут быть использованы в процессе, включают: COF2, CF3COF, C2F5COF, C2F5OCF2COF, н-C3F7COF, изо-С3F7СОF, С3F7OСF(СF3)СОF, C2F5OC2F4COF, C4F9COF, C7F15COF и другие, содержащие отличные от фтора атомы галогена, Н, например BrCF2COF и НСF2(СF2)3СОF и т.д.
Мольное соотношение ОГФП и исходного фторангидрида составляет 1:1,0-2. При этом преимущественно образуются продукты моноприсоединения и лишь в незначительной степени продукты изомеризации гексафторпропеноксида. Синтез осуществляют в реакторе с мешалкой при атмосферном давлении.
Образующиеся в результате реакции фторангидриды полифторалкоксипропионовых кислот экстрагируются перфторированным растворителем. Полученный экстракт после окончания реакции отделяют от реакционной массы и подвергают перегонке. Целевые продукты анализируют методом ГЖХ и идентифицируют методами ИК- и ЯМР спектроскопии.
Выход фторангидридов полифторалкоксипропионовых кислот достигает 97-99%. В условиях проведения данного процесса олигомеры ОГФП не образуются, так же как и продукты присоединения двух и более молекул гексафторпропеноксида к исходному фторангидриду.
Таким образом, разработанный способ позволяет селективно получать целевые продукты с высоким выходом и вести процесс при атмосферном давлении.
Нижеследующие примеры иллюстрируют предлагаемое изобретение, но не ограничивают его.
Пример 1. Синтез перфтор-2-метоксипропионилфторида.
В стеклянную колбу вместимостью 500 мл, снабженную мешалкой, обратным холодильником, охлаждаемым до минус 30°С, ловушкой, охлаждаемой до минус 60°С, и барботерами для подачи исходных реагентов, загружают 25 г ацетонитрила, 11 г ди(пиперидина)метана, 210 г перфтороктана и пропускают при перемешивании 125 г (0,75 моль) гексафторпропеноксида и 80 г (1,2 моль) карбонилфторида.
Реакционную массу перемешивают в течение 1-2 часов при температуре минус 15 - минус 18°С, затем температуру поднимают до комнатной. Нижний слой, представляющий экстракт продуктов реакции в перфтороктане, отделяют и выделяют перегонкой целевой продукт.
В результате получают 170 г фторангидрида перфтор-2-метоксипропионовой кислоты
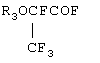
с температурой кипения 10-12°С и 3 г фторангидрида перфторпропионовой кислоты. Выход целевого продукта составляет 97,3%.
Последующие синтезы (примеры 2-8) проведены аналогично примеру 1. Условия проведения и полученные результаты представлены в таблице.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПЕРФТОРИРОВАННЫХ ПРОСТЫХ ЭФИРОВ С КОНЦЕВЫМИ ФУНКЦИОНАЛЬНЫМИ ГРУППАМИ | 2000 |
|
RU2179548C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРФТОРИРОВАННЫХ ПРОСТЫХ ЭФИРОВ С КОНЦЕВЫМИ ФУНКЦИОНАЛЬНЫМИ ГРУППАМИ | 2012 |
|
RU2473533C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИФТОРАЛКАНОВ | 2001 |
|
RU2189966C1 |
| ОКСА- И ПОЛИОКСАПЕРФТОРАЛКИЛБРОМИДЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2497801C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГАЛОГЕНПОЛИФТОРБЕНЗОЛОВ | 2018 |
|
RU2687554C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИФТОРАРОМАТИЧЕСКИХ СОЕДИНЕНИЙ | 1999 |
|
RU2164508C1 |
| СПОСОБ ДЕКАРБОКСИЛИРОВАНИЯ ПРОИЗВОДНЫХ ПЕРФТОРИРОВАННЫХ КАРБОНОВЫХ КИСЛОТ | 1999 |
|
RU2188187C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 1-О-АЦИЛ-2-ДЕЗОКСИ-2-ФТОР-4-ТИО-β-D-АРАБИНОФУРАНОЗ | 2010 |
|
RU2559364C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРФТОРИРОВАННЫХ ЭПОКСИДОВ | 1998 |
|
RU2157805C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРФТОРЭТИЛИЗОПРОПИЛКЕТОНА | 2015 |
|
RU2607897C1 |

Изобретение относится к способу получения фторангидридов полифторалкоксипропионовых кислот формулы 1
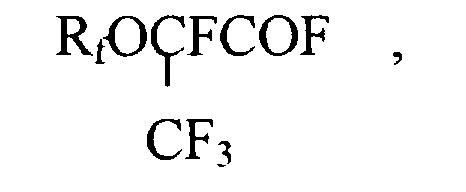 (1)
(1)
где Rf представляет перфторалкил C1-С9, перфторалкоксиалкил C1-C9 линейного или разветвленного строения, возможно, содержащий другие атомы галогенов, Н, взаимодействием гексафторпропеноксида с соответствующим фторангидридом полифторкарбоновой кислоты в органической среде, состоящей из двух компонентов, где одним из компонентов является полярный апротонный растворитель, в присутствии катализатора. Вторым компонентом органической среды является перфторированный неполярный растворитель, представляющий перфторированный циклический С7-С11 или алифатический С6-С9 углеводород, способный экстрагировать образующиеся фторангидриды формулы (1), причем его количество в органической среде находится в пределах 80-90 вес.%. В качестве катализатора используют N, N, N', N' -тетразамещенный диаминометан формулы
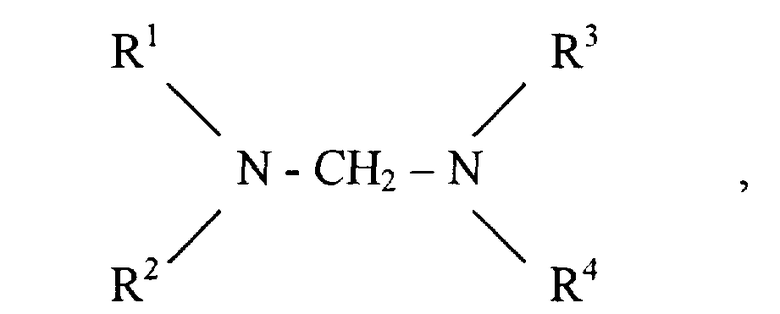
где R1 - R4 представляют линейные или разветвленные алкил C1-С6 или перфторалкил C1-С6, группу С2Н4OH или R1 и R2 и R3 и R4 совместно с атомом азота могут образовывать гетероциклический остаток, возможно, содержащий еще один гетероатом - кислород и замещенный одной или несколькими алкильными группами. Изобретение позволяет селективно получать целевые продукты с высоким выходом и вести процесс при атмосферном давлении. 1 з.п. ф-лы, 1 табл.
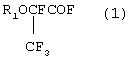
где Rf представляет перфторалкил C1-С9, перфторалкоксиалкил C1-С9 линейного или разветвленного строения, возможно содержащий другие атомы галогена, Н,
взаимодействием гексафторпропеноксида с соответствующим фторангидридом полифторкарбоновой кислоты в органической среде, состоящей из двух компонентов, где одним из компонентов является полярный апротонный растворитель, в присутствии катализатора, отличающийся тем, что вторым компонентом органической среды является перфторированный неполярный растворитель, представляющий перфторированный циклический С7-С11 или алифатический С6-С9 углеводород, способный экстрагировать образующиеся фторангидриды формулы (1), причем его количество в органической среде находится в пределах 80-90 вес.%, а в качестве катализатора используют N, N, N/, N/ -тетразамещенный диаминометан формулы

где R1 - R4 представляют линейные или разветвленные алкил C1-С6 или перфторалкил C1-С6, группу С2Н4OН или R1 и R2 и R3 и R4 совместно с атомом азота могут образовывать гетероциклический остаток, возможно содержащий еще один гетероатом - кислород и замещенный одной или несколькими алкильными группами.
| Способ Герлиги-Погосова контроля запаса теплогидравлической устойчивости замкнутого парогенерирующего контура | 1987 |
|
SU1550268A1 |
Авторы
Даты
2004-06-10—Публикация
2002-11-18—Подача