Изобретение относится к химии полимеров и может быть использовано в медицине для диагностики сахарного диабета, а именно для аффинного определения гликозилированного гемоглобина.
Известен сорбент аналогичного назначения - агароза с иммобилизованной мета-аминофенилбороновой кислотой (м-АФБК), который используется для определения гликозилированного гемоглобина (Каталог фирмы Glico-Gel Pierce Chemical Company, 1986, p.3-7). Емкость агарозы по лиганду составляет 5-15 мкМ на 1 мл сорбента.
Недостатком сорбента на основе агарозы является то, что кратность использования одной порции сорбента ограничивается 3-6 циклами достоверного количественного определения гликозилированного гемоглобина. Это дорогостоящий сорбент.
Известен сорбент аналогичного назначения - сшитый поливиниловый спирт (носитель) с иммобилизованной м-АФБК, который используется для аффинного определения гликозилированного гемоглобина (Ггб) (Патент РФ № 2093525, МПК С 08 F 30/06, опубл. 20.10.97 г.). Емкость агарозы по лиганду составляет 5-15 мкМ на 1 мл сорбента.
Недостатком сорбента на основе поливинилового спирта также следует считать недостаточное количество достоверных определений Ггб на одной порции сорбента (20-30).
Наиболее близким к предложенному по химическому составу является сорбент на основе кремнезема, содержащий привитые группы м-аминофенилбороновой кислоты, имеющий структурную формулу
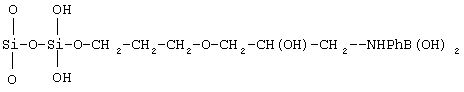
(RU 2040963, МПК B 01 J 20/10 от 08.09.1995 г.).
Недостатком указанного сорбента является высокое значение неспецифического связывания белков и гликопротеидов, делающее его низкоэффективным при использовании в качестве сорбента для аффинного определения гликозилированного гемоглобина.
Задача изобретения - повышение эффективности сорбента за счет увеличения селективности связывания гликопротеидов.
Поставленная задача решается сорбентом для аффинного определения гликозилированного гемоглобина на основе кремнезема, содержащим иммобилизованную мета-аминофенилбороновую кислоту, в котором в отличие от прототипа в качестве носителя используется пористый силикагель, модифицированный глицерилпропилсиланом, активированный эпихлоргидрином, причем сорбент имеет следующую формулу:
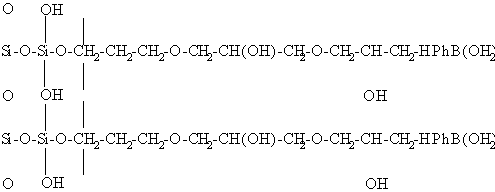
Введение в соответствии с заявленной сущностью в качестве спейсера (мостика) между силикагелем и м-АФБК глицерилпропилсилана и эпихлоргидрина увеличивает гидрофильность сорбента, в результате чего снижается неспецифическая сорбция гликопротеидов, что приводит к повышению селективности определения гликозилированного гемоглобина.
Сорбент для аффинного определения гликозилированного гемоглобина получают следующим образом.
1) Активация эпихлоргидрином пористого силикагеля, модифицированного глицерилпропилсиланом

2) Реакция связывания активированного носителя с м-АФБК

Подтверждением протекания химической реакции между лигандом (м-АБФК) и носителем, активированным эпихлоргидрином, служит результат иодометрического титрования альдегидных групп носителя, получающихся после его окисления периодатом натрия до и после посадки м-АФБК: количество альдегидных групп после связывания м-АФБК на 14, 2±0,6% меньше их количества, полученного для немодифицированного носителя.
Согласно заявленного для получения сорбента использовали силикагель фирмы "Serva" марки SP-500, модифицированный глицерилпропилсиланом (Л.А.Остерман. Хроматография белков и нуклеиновых кислот. М.: Наука, 1985 г., с.60). Носитель представляет собой микрочастицы силикагеля с общей формулой SiO2·H2O, пронизанные порами со средним диаметром 500 ангстрем. Поверхность частиц модифицирована глицерилпропилсиланом за счет реакции между его силанольными группами и поверхностными силанольными группами силикагеля. В результате этой модицикации поверхность носителя теряет сорбционную способность и приобретает поверхностные гидроксильные группы.
Указанное соединение активировали эпихлоргидрином в щелочных условиях для введения на поверхность активных оксирановых групп. Затем проводили связывание с м-АФБК в щелочных условиях за счет реакции аминогруппы м-АФБК с оксирановыми группами, связанными с поверхностью сорбента. Непрореагировавшие оксирановые группы устраняли за счет реакции с моноэтаноламином.
Элементный анализ 30 проб полученного сорбента показал, что содержание бора в нем составляет 0,18±0,04%, что подтверждает его высокую специфическую емкость.
Сущность заявленного изобретения подтверждается примерами.
Пример 1
К 50 мл силикагеля фирмы "Serva" марки SP-500, модифицированного глицерилпропилсиланом, суспендированного в 50 мл дистиллированной воды добавляли 10 мл эпихлоргидрина и 20 мл 2М NaOH, встряхивали в течение 15-18 часов при комнатной температуре в присутствии 0,1 г NaBH4. Затем активированный носитель промывали 100 объемами дистиллированной воды и 0,1 М карбонатным буфером связывания рН 9,5, после чего добавляли м-АФБК из расчета 20 мг/мл носителя и встряхивали при комнатной температуре в течение 18 часов. Отмытый от избытка м-АФБК сорбент использовали для количественного определения Ггб. По данным элементного анализа сорбент содержит 0,18±0,6% бора. В прототипе содержание бора по результатам элементного анализа составляет 0,12%.
Пример 2
Для определения гликозилированного гемоглобина полученный сорбент помещали в колонку (1 мл) и отмывали стартовым буфером (0,025 М натрий-фосфатный буфер, рН 8,5). Гемолизат готовили добавлением к одному объему отмытых эритроцитов трех объемов 0,02% раствора азида натрия. На колонку наносили 0,1 мл гемолизата. Для связывания пробы ток буфера останавливали на 15 минут и промывали колонку стартовым буфером для сбора негликозилированного гемоглобина. Гликозилированный гемоглобин элюировали буфером, содержащим 200 мМ сорбитола рН 8,5. Полученные фракции №1 и 2 фотометрировали при 414 нм. Содержание гликозилированного гемоглобина определяли по формуле

где ОП(1) и ОП(2) - оптическая плотность при 414 нм фракций №1 и 2 соответственно;
V1 и V2 - объем фракций №1 и 2, мл.
Кратность достоверных определений на полученном сорбенте составила 45-50. При попытке дальнейшего использования порции сорбента происходило достоверное снижение количества связанного гемоглобина в пробах, вероятно, за счет частичного разрушения сорбента и связанного с этим снижения емкости.
Пример 3
Для определения гликозилированного гемоглобина полученный сорбент помещали в колонку (1 мл) и отмывали стартовым буфером (0,025 М натрий-фосфатный буфер, рН 8,5). Гемолизат готовили добавлением к одному объему отмытых эритроцитов трех объемов 0,02% раствора азида натрия. В гемолизате проводили определение количества гликозилированного гемоглобина на хроматографе AUTO A1 СТМНА-8110 (Kyoto, Kagaku Co, Japan). Результат этого определения считали истинным значением содержания гликозилированной формы в пробе. На колонку с испытуемым сорбентом наносили 0,1 мл гемолизата. Для связывания пробы ток буфера останавливали на 15 минут и промывали колонку стартовым буфером для сбора негликозилированного гемоглобина. Гликозилированный гемоглобин элюировали буфером, содержащим 200 мМ сорбитола рН 8,5. Полученные фракции №1 и 2 фотометрировали при 414 нм. Содержание гликозилированного гемоглобина определяли по формуле

Кратность достоверных определений (дающих результат, отличающийся от результата, полученного с использованием хроматографа, не более чем на 5%) на полученном сорбенте составила 45-50. При попытке дальнейшего использования порции сорбента происходило достоверное снижение количества связанного гемоглобина в пробах, вероятно, за счет частичного разрушения сорбента и связанного с этим снижения емкости.
Пример 4
Определение Ггб проводили аналогично примеру 3 с той разницей, что вместо предложенного сорбента использовали сорбент, приготовленный по прототипу. Количество гемоглобина, определенное в пробах, на 90±15% превышало количество гликогемоглобина, определенное на хроматографе AUTO A1 СТМНА-8110 (Kyoto, Kagaku Co, Japan), что свидетельствует о том, что использование этого сорбента для количественного определения гликозилированной формы гемоглобина приводит к недостоверным результатам.
Таким образом, заявленный сорбент на основе пористого силикагеля, модифицированного глицерилпропилсиланом и эпихлоргидрином, с иммобилизованной мета-аминофенилбороновой кислотой обеспечивает 45-кратное определение Ггб с высокой точностью, значительно превышающей точность его определения при использовании сорбента по прототипу.
| название | год | авторы | номер документа |
|---|---|---|---|
| СШИТЫЙ ПОЛИВИНИЛОВЫЙ СПИРТ С ИММОБИЛИЗОВАННОЙ М-АМИНОФЕНИЛБОРОНОВОЙ КИСЛОТОЙ В КАЧЕСТВЕ СОРБЕНТА ДЛЯ АФФИННОГО ОПРЕДЕЛЕНИЯ ГЛИКОЗИЛИРОВАННОГО ГЕМОГЛОБИНА | 1995 |
|
RU2093525C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТА ДЛЯ ОПРЕДЕЛЕНИЯ ГЛИКОЗИЛИРОВАННЫХ БЕЛКОВ КРОВИ | 2002 |
|
RU2229129C1 |
| СОРБЕНТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1996 |
|
RU2094117C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ГЛИКОГЕМОГЛОБИНА | 2002 |
|
RU2234703C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЛИКОЛИЗИРОВАННОГО ГЕМОГЛОБИНА В ПРИСУТСТВИИ НЕГЛИКОЛИЗИРОВАННОГО ГЕМОГЛОБИНА, АНАЛИТИЧЕСКИЙ ТЕСТОВЫЙ НАБОР | 1990 |
|
RU2111494C1 |
| СПОСОБ КОНЦЕНТРИРОВАНИЯ ВИРУСА | 1997 |
|
RU2130069C1 |
| АДСОРБЕНТ ДЛЯ ИЗВЛЕЧЕНИЯ АТЕРОГЕННЫХ ЛИПОПРОТЕИНОВ ИЗ БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ | 1992 |
|
RU2029564C1 |
| УДАЛЕНИЕ ПЛАЗМИН(ОГЕН)А ИЗ БЕЛКОВЫХ РАСТВОРОВ | 2002 |
|
RU2344143C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЛИКИРОВАННОГО ГЕМОГЛОБИНА В КРОВИ | 1993 |
|
RU2038597C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ПЛАЗМИНОГЕНА ИЛИ ПЛАЗМИНА В ПРИСУТСТВИИ ФИБРИНОГЕНА ИЗ СМЕСИ | 2002 |
|
RU2458067C2 |
Сорбент для аффинного определения гликозилированного гемоглобина содержит пористый силикагель, модифицированный глицерилпропилсиланом марки SP-500, активированный эпихлоргидрином, общей формулы
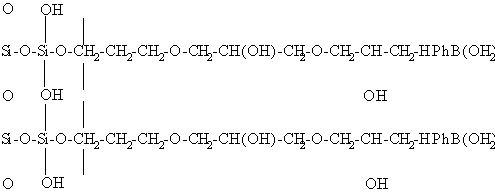
Изобретение обеспечивает получение сорбента с высокой селективностью.
Сорбент для аффинного определения гликозилированного гемоглобина на основе кремнезема, содержащий иммобилизованную метааминофенилбороновую кислоту, отличающийся тем, что в качестве носителя используется пористый силикагель, модифицированный глицерилпропилсиланом, активированный эпихлоргидрином, общей формулы
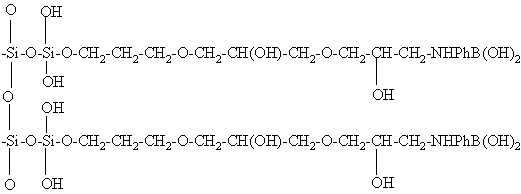
| СОРБЕНТ НА ОСНОВЕ КРЕМНЕЗЕМА | 1993 |
|
RU2040963C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЛИКИРОВАННОГО ГЕМОГЛОБИНА В КРОВИ | 1993 |
|
RU2038597C1 |
| US 5240602 А, 31.08.1993 | |||
| E.HAGEMEIER | |||
| "Synthesis and application of a boronic acid-substituted silica for high-performance liguid affinity chromatography" | |||
| - Journal of Chromatoraphy, 1983, v.268, №2, р.291-295 | |||
| СШИТЫЙ ПОЛИВИНИЛОВЫЙ СПИРТ С ИММОБИЛИЗОВАННОЙ М-АМИНОФЕНИЛБОРОНОВОЙ КИСЛОТОЙ В КАЧЕСТВЕ СОРБЕНТА ДЛЯ АФФИННОГО ОПРЕДЕЛЕНИЯ ГЛИКОЗИЛИРОВАННОГО ГЕМОГЛОБИНА | 1995 |
|
RU2093525C1 |
| СОРБЕНТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1996 |
|
RU2094117C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТА | 1997 |
|
RU2125907C1 |
| US 4269605 а, 26.05.1981 | |||
| US 6562581 A, 13.05.2003 | |||
| US 6462179 А, 08.10.2002. | |||
Авторы
Даты
2004-06-20—Публикация
2003-07-01—Подача