Изобретение относится к медицине, конкретно к средствам для связывания из биологической жидкости липопротеинов низкой и очень низкой плотности (ЛНП и ЛОНП).
Согласно современным представлениям высокая концентрация ЛНП+ЛОНП в циркулирующей крови является ведущим фактором в развитии атеросклероза. Наиболее эффективным способом снижения уровня ЛНП в крови является их адсорбция специфическими сорбентами.
Известны сорбенты для связывания атерогенных липопротеинов из плазмы крови, представляющие собой гелевые матрицы, модифицированные сульфополи- сахаридами, обеспечивающими специфичность этих сорбентов по отношению к атерогенным липопротеинам - это сефароза, модифицированная гепарином, и поливиниловый спирт, модифицированный декстрансульфатом. Главным недостатком этих сорбентов является невозможность работы с цельной протекающей кровью из-за плохих гидродинамических свойств гелей и их высокой стоимости.
Известен гемосорбент для извлечения атерогенных липопротеинов полученный иммобилизацией гепарина на поверхности силохрома (СХ) с диаметром пор 100-300 нм. Жесткая матрица - силохром обладает прочностью и устойчивостью в физиологических условиях и большой однородностью пор, что позволяет осуществлять сорбцию непосредственно из крови, а наличие специфического лиганда к ЛНП - гепарина обеспечивает емкость по общему холестерину, равную 8,7 мг/г. Однако, указанный сорбент не обладает высокой емкостью по отношению к атерогенным липопротеинам (7,0 мг/г).
В патенте описаны сорбенты для извлечения атерогенных липопротеинов из биологических жидкостей, полученные путем модификации органических (целлофан, биогель) и неорганических матриц (макропористое стекло) различными сульфополисахаридами, такими как гепаpин, декстрансульфат натрия (ДС) и хондроитинсульфат и т. д. При этом наибольшей емкостью к атерогенным липопротеинам обладает сорбент на основе макропористого стекла (МПС), содержащий иммобилизованный ДС (65% извлечения). Однако, этот показатель зависит от оптимального сочетания ряда факторов: диаметр пор, размер гранул, молекулярная масса (характеристическая вязкость) ДС, содержание в нем серы. Так, наибольший процент извлечения (65%) отмечен при следующих характеристиках сорбента: размер гранул - 0,08-0,12 мм, мол.м. ДС 7,0 кД (или характеристическая вязкость [η] = 0,027 дл/г), содержание серы 17,7 вес.%. При этом увеличение молекулярной массы с 7,0 кД до 500 кД ([η] = 0,2 дл/г) при прочих равных условиях снижает степень извлечения до 18%. К такому же результату приводит использование ДС с низким (5,7%) содержанием серы.
Недостатками прототипа являются:
Использование гранул размером 0,08-0,12 мм, что не пригодно для перфузии цельной крови, вследствие травматизации форменных элементов. Все используемые в практике гемосорбенты имеют гранулы с диаметром более 0,2 мм.
Заведомо низкая скорость перфузии (0,3 мл/мин), в то время как в практической гемосорбции скорость перфузии составляет от 40 до 100 мл/мин.
Использование низкомолекулярного (7,0 кД) и высокозамещенного ДС, получение которого связано с трудностями и использование которого ведет к значительному расходу при иммобилизации его на носителе.
Все перечисленное препятствует использованию данных сорбентов в практической гемосорбции.
Целью изобретения является создание специфического сорбента, позволяющего осуществлять эффективную сорбцию атерогенных липопротеинов из любых биологических жидкостей, включая цельную кровь, обладающего высокой избирательностью к атерогенным липопротеинам и пригодного к использованию в условиях практической гемосорбции.
Цель достигается тем, что сорбент содержит в качестве лиганда N-сульфосукцинат хитозана с молекулярной массой 5-300 кД и содержанием серы 3-9 мас.% со структурной формулой
XT-NHCO-CH-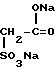 при весовом соотношении матрица:лиганд = 1:0,003-1: 0,025 (г/г).
при весовом соотношении матрица:лиганд = 1:0,003-1: 0,025 (г/г).
Сравнительный анализ с прототипом показывает, что заявляемое техническое решение отличается тем, что в качестве иммобилизуемого полисахарида (лиганда) используют новое, неописанное ранее в литературе соединение.
Из прототипа также следует, что лигандами, пригодными для эффективной сорбции, могут считаться лишь те представители широкого класса сульфополисахаридов, которые обладают мол.м. не более 30 кД при содержании в них серы не менее 15 вес.%.
Предлагаемый лиганд обладает сорбционными свойствами по отношению к атерогенным липопротеинам, неочевидными для соединений этого класса, проявляя высокую сорбционную способность при низком содержании серы (3-9 мас.% ).
Предлагаемый в качестве иммобилизуемого лиганда N-сульфосукцинат хитозана получают сульфатированием предварительно малеилированного согласно (6) хитозана пиросульфитом натрия при рН среды 3-6 и мольном соотношении мелеилированный хитозан: пиросульфит натрия 1: 1,5-1:8 в течение 1-5 ч при 35-70oC с последующим выделением продукта известным способом.
Получение и свойства сорбентов с иммобилизованным N-сульфосукцинатом хитозана иллюстрируются следующими примерами:
П р и м е р 1. Подготовка носителя к активации. Образцы гранулированных частиц носителя (СХ, МПС, силикагель (СГ) со средним размером 0,3-0,7 мм обрабатывают 0,2 М водным раствором азотной кислоты в отношении 1:20 при 70-80oC в течение 3 ч, затем промывают водой до нейтрального значения рН промывных вод и сушат при 500-600oC в течение 3 ч.
П р и м е р ы 2-4. Активация носителя.
П р и м е р 2. 10 г МПС с диаметром пор 200 нм обрабатывают 50 мл 3%-ного водного раствора - γ-аминопропилтриоксисилана при 95-100oC в течение 6 ч, затем суспензию промывают водой до нейтрального значения рН промывных вод и сушат в вакууме при 60oC. Количество введенных аминогрупп - 0,3 ммоль/г.
П р и м е р 3. К 10 г МПС с диаметром пор 70 нм добавляют 150 мл толуола и 6 мл глицидоксипропилтриоксисилана, кипятят в течение 8 ч, затем суспензию промывают толуолом, ацетоном и сушат в вакууме при 60oС. Количество введенных аминогрупп -0,21 ммоль/г.
П р и м е р 4. К 10 г МПС с диаметром пор 40 нм добавляют 30 мл 0,01М водного раствора NaOH и 5 мл диглицидилового эфира диэтиленгликоля, перемешивают в течение 6 ч, и выдерживают при комнатной температуре 12 ч, затем суспензию промывают водой до нейтрального значения рН промывных вод и сушат в вакууме при 60oC. Количество введенных эпоксигрупп - 0,19 ммоль/г.
Примеры 5-8. Приготовление адсорбентов.
П р и м е р 5. К 1 г активированного по примеру 3 носителя добавляют 5 мл 1,5% -ного раствора N-сульфосукцината хитозана (мол.м. - 250 кД, cера 7,5% ) в 0,5%-ном растворе NaOH, перемешивают в течение 1 ч. при комнатной температуре, суспензию фильтруют, промывают 10%-ным раствором NaCl, водой и сушат. Весовое соотношение матрица:лиганд (г/г) = 1:0,0185.
П р и м е р 6. К 1 г активированного по примеру 4 носителя добавляют 5 мл 1,5%-ного раствора N-сульфосукцината хитозана (мол.м. -250 кД, сера 9,0% ) в 0,5%-ном растворе NaOH, перемешивают в течение 18 ч при комнатной температуре, суспензию фильтруют, промывают 10%-ным раствором NaСl, водой и сушат.
Весовое соотношение матрица:лиганд (г/г) = 1:0,0215.
П р и м е р 7. К 1 г активированного по примеру 2 носителя добавляют 5 мл 2%-ного раствора N-сульфосукцината хитозана (мол.м.-70 кД, сера 7,0%) в 0,2 М ацетатном буфере, рН 4,5, вносят 6 мг N-этил-N-(3-диметиламинопропил)карбодиимида, перемешивают при 4oC в течение 24 ч, суспензию фильтруют, промывают 10%-ным раствором NaCl, водой и сушат.
Весовое соотношение матрица:лиганд (г/г) = 1:0,018.
П р и м е р 8. К 1 г активированного по примеру 2 носителя добавляют 5 мл 4%-ного раствора N-сульфосукцината хитозана (мол.м.-5,0 кД, сера 6,0%) в 0,1 М фосфатном буфере, рН 7,4, перемешивают в течение 6 ч при комнатной температуре, реакционную смесь фильтруют, промывают водой, затем суспендируют в 1%-ном растворе боргидрида натрия в течение 30 мин, суспензию промывают 10%-ным раствором NaCl, водой и сушат.
Весовое соотношение матрица:лиганд (г/г) = 1:0,015.
П р и м е р 9. Аналогично примерам 2-8, но отличающийся тем, что в качестве матрицы (носителя) используют силохром и силикагель (табл.1).
П р и м е р 10. Определение сорбционной емкости адсорбентов.
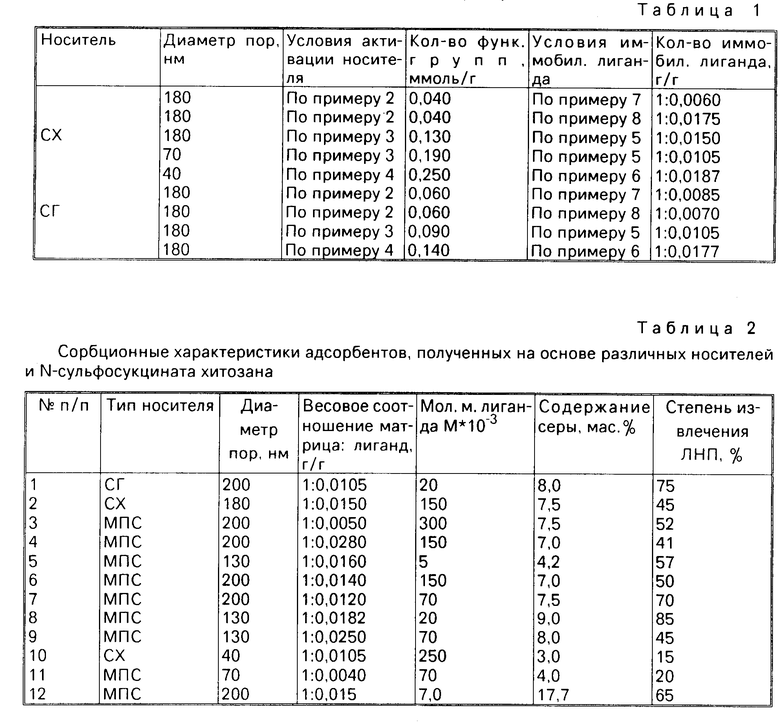
Кровь пропускают через колонку объемом 1 см3 с адсорбентом приготовленным по примеру 7, по замкнутому контуру со скоростью 1 мл/мин в течение 45 мин, при соотношении кровь:адсорбент 6:1 по объему. В плазме крови, содержащей 300 мг/дл общего холестерина, а также содержание ЛНП и ЛОНП методом ракетного электрофореза. В табл.2 даны сорбционные характеристики адсорбентов, приготовленных согласно вышеприведенным примерам.
При молекулярной массе аффинного лиганда меньше 5 кД специфичность адсорбентов по извлекаемому компоненту резко ухудшается, а при увеличении молекулярной массы больше 300 кД наблюдается уменьшение количества иммобилизованного лиганда на матрице менее 3 мг на 1 г сорбента и, следовательно, снижение емкости адсорбентов по ЛНП. С другой стороны, увеличение количества иммобилизованного лиганда больше 25 мг практически не влияет на емкость сорбента.
Снижение емкости сорбентов также наблюдается при использовании лиганда с содержанием серы менее 3 мас.% (Теоретически максимальное количество серы в N-сульфосукцинате хитозана равно 10 мас.%).
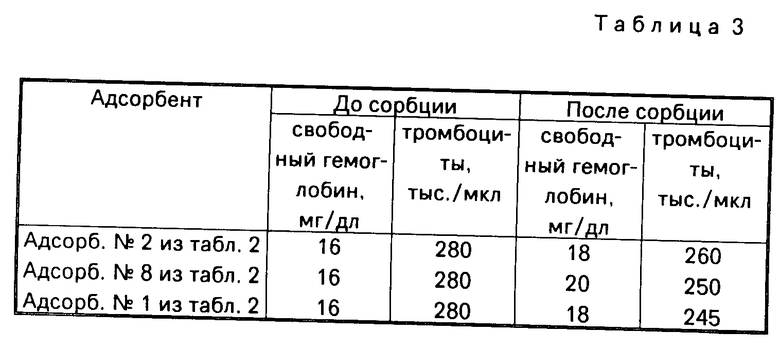
П р и м е р 10. Определение гемосовместимости. Донорскую кровь (10 мл) пропускают через колонку, содержащую 1 см3 адсорбента со скоростью 5 мл/мин в течение 30 мин. До и после сорбции определяют количество тромбоцитов и концентрацию свободного гемоглобина в плазме (табл.3).
Как видно из табл.3, перфузия крови через колонку с адсорбентом приводит к адгезии тромбоцитов на их поверхности (10-12%) не превышающей показатели, характерные для активированных углей (40% и больше), широко применяющихся в гемосорбции.
Таким образом, предлагаемые сорбенты обладают повышенной селективной емкостью по отношению к атерогенным липопротеинам и гемосовместимостью при сорбции из протекающей крови, при этом по стоимости предлагаемые значительно экономичнее известных (например, гепарин-сефарозы).
| название | год | авторы | номер документа |
|---|---|---|---|
| АДСОРБЕНТ ДЛЯ ИЗВЛЕЧЕНИЯ АТЕРОГЕННЫХ ЛИПОПРОТЕИНОВ ИЗ БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ | 1992 |
|
RU2029565C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФАТИРОВАННОГО ХИТОЗАНА | 1992 |
|
RU2048475C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНТЕРПОЛИМЕРНЫХ КОМПЛЕКСОВ ХИТОЗАНА С ДЕКСТРАНСУЛЬФАТОМ НАТРИЯ | 1992 |
|
RU2048473C1 |
| СПОСОБ ОЧИСТКИ ЩЕЛОЧНОЙ ФОСФАТАЗЫ ИЗ ТОНКОГО КИШЕЧНИКА ТЮЛЕНЯ | 1992 |
|
RU2036236C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФАТИРОВАННОГО ХИТОЗАНА | 1992 |
|
RU2048474C1 |
| Сшитые гели на основе хитозана | 1978 |
|
SU827492A1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОСОРБЕНТА ДЛЯ СВЯЗЫВАНИЯ ГРУППОСПЕЦИФИЧЕСКИХ АНТИТЕЛ α- И β- -АГГЛЮТИНИНОВ | 1988 |
|
RU2040274C1 |
| Способ получения карбоксилсодер-жАщиХ пРОизВОдНыХ ХиТОзАНА | 1978 |
|
SU802290A1 |
| СПОСОБ ИМПРЕГНАЦИИ ГИДРОКСИЛСОДЕРЖАЩИХ ПОЛИМЕРОВ | 2006 |
|
RU2318839C1 |
| СПОСОБ ХИМИЧЕСКОЙ ОБРАБОТКИ КСЕНОПЕРИКАРДА | 2008 |
|
RU2384348C2 |
Изобретение относится к медицине, конкретно к средствам для связывания из цельной крови атерогенных липопротеинов, высокая концентрация которых является решающим фактором развития атеросклероза. Предлагаемые сорбенты позволяют проводить сорбцию из цельной протекающей крови (плазмы, лимфы). Имеют высокую емкость и избирательность по отношению к атерогенным липопротеинам, хорошую гемосовместимость и низкую стоимость. Сорбенты представляют собой твердые, гранулированные, пористые носители (силохром, макропористое стекло, силикагель) с оптимальным диаметром пор (130 - 250 нм), модифицированные N - сульфосукцинатом хитозана. 3 табл.
АДСОРБЕНТ ДЛЯ ИЗВЛЕЧЕНИЯ АТЕРОГЕННЫХ ЛИПОПРОТЕИНОВ ИЗ БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ, включающий модифицированную миандом матрицу, отличающийся тем, что в качестве лиганда он содержит N-сульфосукцинат хитозана со структурной формулой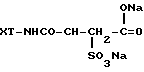
и мол. м. 5 - 300 кД, содержанием серы 3 - 9 мас.% при массовом соотношении матрица : лиганд 1 : 0,003 - 0,025.
| Патент США N 4576928, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1995-02-27—Публикация
1992-12-25—Подача