ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к способу получения амида из нитрила действием нитрилгидратазы, которая является ферментом, получаемым из микроорганизма.
Амид используется в различных областях как промышленно важное вещества. Например, акриламид используется в качестве флокулянта для обработки отработанной воды, в качестве активного наполнителя бумаги для прочности, в качестве агента для регенерации нефти и проч., а метакриламид используется в качестве клея в лакокрасочном материале, и проч.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Соответственно амид производится промышленным способом путем гидратации соответствующего нитрила с использованием в качестве катализатора восстановленных состояний меди. Однако недавно вместо метода с медным катализатором был разработан метод с использованием фермента микроорганизма и в настоящее время особенно практикуется использование этого метода.
В ферментативном методе условия реакции являются мягкими и практически не образуется побочных продуктов. Таким образом, такой метод может быть осуществлен как исключительно простой способ. Поэтому ферментативный метод рассматривается как эффективный в качестве промышленного метода получения. Ранее были найдены многие микроорганизмы, обладающие способностью гидролизовать нитрил, образуя амид.
В качестве таких микроорганизмов, например, могут быть упомянуты группа Bacillus, группа Bacteridium, группа Micrococcus и группа Brevibacterium (JP-B-62-21519, соответствующая Патенту США 4001081) (термин JP, здесь используемый, означает "рассмотренная публикация патента Японии); группа Corynebacterium и группа Nocardia (JP-B-56-17918, соответствующая патенту США 4248968); группа Pseudomonas (JP-B-59-37951, соответствующая патенту США 4637982); группа Rhodococcus и группа Microbacterium (JP-B-4-4873, соответствующая патенту США 5179014); вид Rhodococcus rhodochrous (JP-B-6-55148, соответствующая патенту США 5334519) и группа штамма Rhodococcus (JP-B-7-40948, соответствующая патенту США 5200331).
В то же время для того, чтобы повысить ферментативную активность и соответственно подавить снижение ферментативной активности (деактивацию) в процессе реакции, введены различные новации, которые заключаются в следующем: способ, в котором реакция эффективна при низкой температуре, от точки замерзания до 15°С (JP-B-56-38118, соответствующая патенту США 4248968), способ, в котором субстрат, имеющий низкую концентрацию, непрерывно подается через многочисленные отверстия для загрузки (JP-B-57-1234, соответствующая патенту США 4248968), способ, в котором микроорганизм или обрабатываемый им продукт обрабатывается в органическом растворителе (JP-A-5-308980) (здесь используемый термин JP-A означает "нерассмотренное применение опубликованного патента Японии), способ, в котором реакция осуществляется в присутствии более высокой ненасыщенной жирной кислоты (JP-A-7-265090), способ, в котором клетка микроорганизма обрабатывается по принципу кросс-сочетания, например, глутаровым альдегидом (JP-A-7-265091 и 8-154691) и проч.
Согласно вышеописанным признакам изобретатели настоящего изобретения вводят разнообразные новации, относящиеся к улучшению производства амида по ферментативному способу. В результате было найдено, что деактивация происходит во времени в течение реакции, что не может быть преодолено общепринятым способом. Естественно, что чем больше протекает такая деактивации, тем больше фермента необходимо для реакции. Соответственно решение этой проблемы исключительно важно, особенно при производстве в промышленном масштабе.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ.
Изобретатели настоящего изобретения провели широкое исследование и приложили усилия для решения вышеописанной проблемы. В результате найдено, что следовые количества синильной кислоты в композиции, содержащиеся в нитриле, ускоряют деактивацию фермента - нитрилгидратазы. Далее, может быть также показано, что при использовании композиции с пониженным количеством синильной кислоты деактивация фермента уменьшается настолько, что амид может быть успешно получен из нитрила, так что при использовании меньших количеств фермента могут быть получены большие количества амида. Таким образом, настоящее изобретение было успешно реализовано.
Таким образом, в соответствии с настоящим изобретением предлагается способ для получения амида, в котором нитрил, соответствующий амиду, образуется посредством действия нитрилгидратазы; способ характеризуется тем, что концентрация синильной кислоты в композиции, содержащей нитрил, понижается химическим способом и, таким образом, нитрилгидратаза воздействует на нитрил.
Нитрил, например акрилонитрил, производится в промышленности аммоксидированием пропилена. После завершения реакции синильная кислота удаляется вместе с другими побочными продуктами в процессе очистки дистилляцией. Однако коммерческий продукт обычно включает синильную кислоту в количестве от 0.1 до 5 м.д., которая не может быть удалена этим способом. Синильную кислоту, возникающую при последующем разложении циангидрина, остающегося в продукте, также следует принимать во внимание как часть коммерческого продукта. До сих пор не предполагали влияния таких следовых количеств синильной кислоты на деактивацию.
ДЕТАЛЬНОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Тип нитрила, используемый в настоящем изобретении (например, акрилонитрил), существенно не ограничивается, поскольку он превращается в соответствующий амид действием нитрилгидратазы и является главным компонентом композиции, которая также содержит синильную кислоту в концентрации, вызывающей деактивацию фермента. Количества нитрила в композиции составляет около 90% или более. Примеры нитрила включают алифатические насыщенные нитрилы, такие как ацетонитрил, пропионитрил, сукцинонитрил и адипонитрил; алифатические ненасыщенные нитрилы, такие как акрилонитрил и метакрилонитрил; ароматические нитрилы, такие как бензонитрил, фталодинитрил; и гетероциклические нитрилы, такие как никотинонитрил. Их типичные примеры включают нитрилы, имеющие от 2 до 4 атомов углерода, такие как ацетонитрил, пропионитрил, акрилонитрил, метакрилонитрил, н-бутиронитрил и изобутиронитрил. Особенно предпочтительным является акрилонитрил.
Дальнейшее понижение содержания синильной кислоты, остающейся в используемой в настоящем изобретении композиции, содержащей нитрил, может быть осуществлено с помощью следующего химического способа. Используются различные способы такого понижения. Однако подходящие способы не повышают количеств побочных продуктов или загрязнений, способных вызвать денатурацию нитрила или понизить количество получаемого амида. В качестве таких способов могут быть упомянуты следующие методы: метод, в котором синильная кислота в композиции, содержащей нитрил, превращается в комплекс металла; метод, использующий ионообменную смолу; и в случае, когда нитрил является ненасыщенным нитрилом, способ, в котором синильная кислота прибавляется к нитрилу в щелочных условиях.
Способ превращения в комплекс металла включает прибавление к нитрилу металла, например ванадия, хрома, марганца, свинца, меди, серебра, цинка, кобальта или никеля, который способен образовывать металл-цианидный комплекс, реагируя с синильной кислотой, в виде солей металлов, таких как нитраты, хлориды, сульфаты или карбоксилаты, чтобы перевести синильную кислоту в металл-цианидный комплекс (см. JP-A-7-228563). Затем вместо соли металла может быть использован алкоксид металла) (см. патент США 5519162). Количество прибавленного металла предпочтительно составляет от 0.00001 до 0.01%, хотя оно изменяется с концентрацией синильной кислоты в композиции, содержащей нитрил.
В том случае, если фермент, превращающий нитрил в амид, не подвергается действию иона металла или металл-цианидного комплекса, не требуется удалять соль металла. Однако с точки зрения удаления больших количеств синильной кислоты металл-цианидный комплекс предпочтительно удалять адсорбентом, и проч.
Удаление металл-цианидного комплекса может быть осуществлено, например, адсорбентом (например, активированным углем, активированным оксидом алюминия, цеолитом или силикагелем) или действием анионообменной смолы.
Способ, использующий ионообменную смолу, включает контактирование нитрила с анионообменной смолой для удаления синильной кислоты, содержащейся в нитриле. Так как используется анионообменная смола, предпочтительны те из них, которые являются высокопористой (микросетчатой) и анионообменной смолой типа пористого геля (например, Amberlist A-21 (производства Japan Organo Co., Ltd.), Dianion WA 20, 21, 30 (например, производства Mitsubishi Chemical Со., и др.), так как они обладают в нитриле эффективной ионообменной способностью.
Способ с применением ионообменных смол может быть осуществлен в неподвижном слое, подвижном слое или в псевдоожиженном слое, это также может быть либо серийный способ или непрерывный способ. Из этих способов непрерывный процесс в неподвижном слое предпочтителен с точки зрения стоимости и пригодности к работе. В этом случае скорость прохождения раствора нитрила через ионообменную смолу предпочтительно должна быть примерно не более чем 100 объемов раствора по отношению к объему смолы в час, хотя она изменяется с изменением концентрации синильной кислоты в композиции, содержащей нитрил.
Однако такой метод очистки с использованием анионообменной смолы обычно сопровождается денатурацией нитрила. Таким образом, необходимо тщательное исследование, например, в отношении времени контакта, методов контактирования и прочее.
В качестве способа, в котором синильная кислота прибавляется к ненасыщенному нитрилу в щелочных условиях для получения насыщенного динитрила, может быть использован способ, в котором водный раствор прибавляют к нитрилу (см. патент США 2481580), и способ, в котором нитрил находится в контакте с анионообменной смолой в качестве щелочного катализатора (JP-B-46-41290).
Тип водного щелочного раствора, используемого в настоящем изобретении, существенно не ограничивается, но его следует выбирать из щелочей, которые не оказывают влияния на качество амида и активность фермента. Примерами подходящего водного щелочного раствора являются водные растворы гидроксидов щелочных металлов и гидроксидов щелочноземельных металлов, а также аммиак или амины. Из них предпочтительными являются водный раствор гидроксида щелочного металла, гидроксида щелочноземельного металла и аммиак, особенно предпочтителен водный раствор гидроксида натрия и гидроксида калия.
Концентрация водного щелочного раствора, используемого в настоящем изобретении, особенно не ограничивается, но следует выбирать область концентраций, которые не влияют на качество амида и активность фермента. Предпочтителен водный щелочной раствор от 0.00001 до 5 N, особенно предпочтителен водный щелочной раствор от 0.00001 до 0.5 N. Количество водного щелочного раствора, используемого в настоящем изобретении, особенно не ограничивается. Подходящими являются концентрации от 0.0001 до 10 мас.%.
Желательно удалять большие количества синильной кислоты. Обычно количество синильной кислоты понижают до такого уровня, что концентрация синильной кислоты в нитриле составляет 3 м.д. или меньше, предпочтительно до 1 м.д. или меньше, или более предпочтительно до 0.5 м.д. или меньше.
Нитрилгидратаза является металлоферментом, в конструкции активного центра которого заняты железо, кобальт или им подобные. Предполагают, что ферментативная деактивация вызвана координацией с цианидом атома железа или кобальта в активном центре. Таким образом, в настоящем изобретении нитрилгидратаза может быть получена из любой группы микроорганизма.
Микроорганизмы, способные продуцировать нитрилгидратазу, являются микроорганизмами, перечисленными выше. Нитрилгидратаза, продуцируемая этими микроорганизмами, может использоваться в настоящем изобретении во всех случаях. Из этих микроорганизмов предпочтительны микроорганизмы, принадлежащие к группе Corynebacterium, группе Pseudomonas, группе Rhodococcus, группе Nocardia, группе Gordona и особенно к группе Rhodococcus, имеющей высокую ферментативную активность. Недавно были проведены исследования, в которых фермент нитрилгидратаза, полученный из этих микроорганизмов, был искусственно модифицирован, а также нитрилгидратаза была продуцирована с использованием других микроорганизмов. Для получения активной нитрилгидратазы может быть также использован микроорганизм, полученный согласно технике генной реаранжировки.
Как описано в каждой из вышеупомянутых публикаций, взаимодействие нитрилгидратазы с нитрилом осуществляется путем контакта нитрила с клеткой микроорганизма, полученной культивированием, или с обработанным ею продуктом в водной среде. Клетка микроорганизма для обработки продукта может быть перфорированной клеткой, клеточным экстрактом микроорганизма, или неочищенным или очищенным ферментом, экстрагированным из клетки микроорганизма, и эти клетки микроорганизма и ферменты смешиваются с полиакриламидом, альгиновой кислотой, каррагеном (испанским мхом) и др.
Далее настоящее изобретение проиллюстрировано более детально со ссылкой на следующие примеры. Однако из этого не следует, что настоящее изобретение ограничено этими примерами. Если не указано по другому, то все приведенные проценты в следующих примерах и примерах сравнения являются массовыми.
ПРИМЕР 1 и ПРИМЕР СРАВНЕНИЯ 1
(1) Получение клетки микроорганизма
Rhodococcus rhodochrous У-1 (фермент FERM BP-1478) (JP-В-6-55148), обладающий нитрилгидратазной активностью, культивирован аэробно в культуральной среде (рН 7.0), состоящей из 2 мас.% глюкозы, 1 мас.% мочевины, 0.5 мас.% пептона, 3 мас.% дрожжевого грибка и 0.05 мас.% хлорида кобальта. Полученный культуральный продукт промыт 50 мМ фосфатного буфера (рН 7,0) с образованием суспензии клеток микроорганизма (20 мас.% в расчете на высушенные клетки). К 500 г суспензии прибавляют 500 г сложного мономерного раствора, состоящего из 20 мас.% акриламида, 2 мас.% метиленбисакриламида и 2 мас.% 2-диметиламинопропил-метакриламида, затем полученную смесь тщательно суспендируют. Последовательно туда же прибавляют 2 г 5% раствора персульфата аммония и 2 г 50%-ного раствора тетраметилэтилендиамина, чтобы вызвать полимеризацию и гелеобразование. Полученный гель разрезают на части, размером 1 мм3, которые промывают пять раз одним литром 0.5%-ного раствора сульфата натрия. Таким образом получают фрагменты иммобилизованных клеток микроорганизма, то есть катализатор для получения акриламида.
(2) Обработка для снижения содержания синильной кислоты
К десяти литрам технического акрилонитрила (содержащего 5 м.д. синильной кислоты) прибавляют 100 г 0.1 N раствора гидроксида натрия, полученную смесь тщательно встряхивают до растворения, и затем полученный раствор выдерживают в течение 30 минут (щелочная обработка). После этого периода к нему прибавляют для нейтрализации 20 г водного раствора акриловой кислоты с концентрацией 1 моль/литр. При такой обработке концентрация синильной кислоты в композиции акрилонитрила падает до 1.0 м.д.
(3) Реакция образования амида
В делительную воронку объемом 5 литров помещают 3200 г водного раствора акрилата натрия с концентрацией 0.2 г/литр. Затем туда прибавляют при перемешивании 3 г вышеописанных иммобилизованных клеток микроорганизма, поддерживая величину рН 7.0 и температуру 10°С.
Затем постепенно вводят туда акрилонитрил так, чтобы концентрация акрилонитрила постоянно составляла 2 мас.% и реакция накопления продолжалась до тех пор, пока концентрация акриламида не достигнет 48%.
Для сравнения реакция накопления была продолжена подобным образом до тех пор, пока концентрация акриламида не достигла 48 мас.% при использовании акрилонитрила, не прошедшего щелочной обработки.
В результате, в то время как начальные скорости реакции были одинаковы в обоих случаях, в акрилонитриле, который был подвергнут щелочной обработке, деактивация была подавлена и понадобилось только половина того времени, чтобы получить акриламид по сравнению со случаем, когда использовался акрилонитрил, не подвергнутый щелочной обработке.
Полученные результаты приведены в таблице 1.

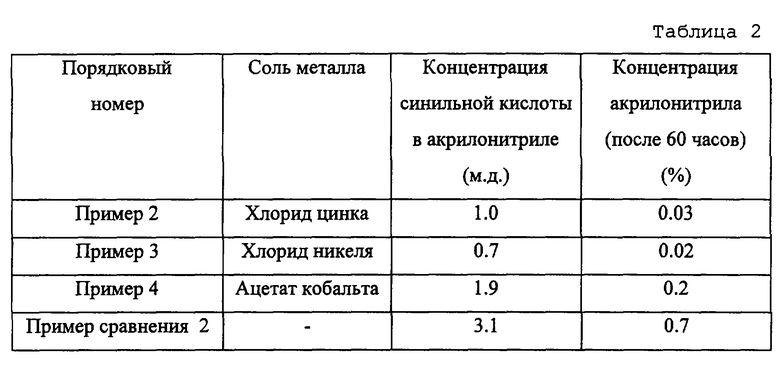
ПРИМЕРЫ 2-4 И ПРИМЕР СРАВНЕНИЯ 2
К 200 г 50%-ного водного раствора акриламида прибавляют 0.1 г иммобилизованных клеток микроорганизма, полученного согласно Примеру 1, и далее перемешивают при 15°С. К тому же техническому акрилонитрилу, как и в примере 1, прибавляют соль металла, приведенную в таблице 2, для удаления синильной кислоты, так что концентрация металла в нем составила 10 м.д., и затем из него удаляют образующийся металлцианидный комплекс действием активным оксидом алюминия. Каждый из образующихся образцов акрилонитрила в количестве 4 г прибавляют к раствору акрилоамида, полученному, как указано выше. Определяют концентрацию акрилонитрила через 60 часов после начала реакции.
Для сравнения той же самой обработке подвергают акрилонитрил, не содержащий добавленной к нему соли металла.
В результате начальные скорости реакции были одинаковы. Однако в акрилонитриле, к которому не была прибавлена соль металла, наблюдалось понижение скорости реакции с уменьшением количества акрилонитрила вследствие деактивации фермента.
Результаты приведены в таблице 2.
ПРИМЕРЫ 5-7 И ПРИМЕР СРАВНЕНИЯ 3
(1) Обработка для уменьшения содержания синильной кислоты.
Помещают тот же самый технический акрилонитрил, использованный в примере 1, в три пластиковых контейнера в количестве по 5 л в каждом. Затем прибавляют в каждый контейнер 50 мл 0.1 N водного раствора гидроксида натрия и тщательно перемешивают. Через две минуты после прибавления гидроксида натрия в один контейнер прибавляют водный раствор акриловой кислоты с концентрацией в 1 моль/литр, через десять минут после этого прибавления добавляют в другой контейнер водный раствор акриловой кислоты с концентрацией в 1 моль/литр, и через двадцать минут после этого прибавления в третий контейнер добавляют также водный раствор акриловой кислоты с концентрацией 1 моль/литр. Каждое прибавленное количество раствора акриловой кислоты с концентрацией 1 моль/литр составляет 5 мл. Таким образом все образцы подвергнуты нейтрализации.
(2) Реакция образования амида.
Вышеописанный образец акрилонитрила и воды постепенно прибавляют в 1 литровую разделительную воронку, содержащую 10 г иммобилизованных клеток микроорганизма, получение которого описано в примере 1, контролируя, чтобы величина рН составляла 8, и температура соответствовала 20°С.
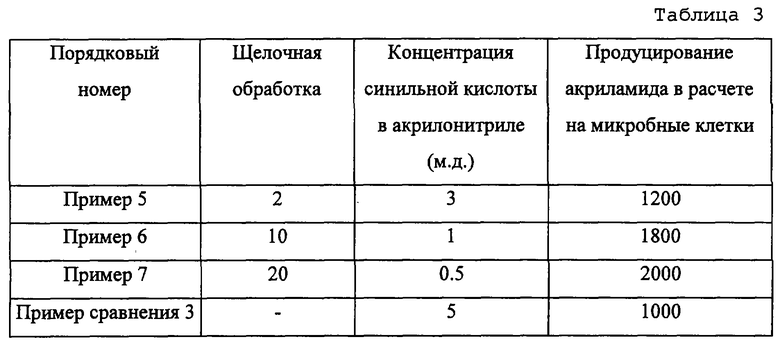
Вышеописанный образец акрилонитрила и дистиллированная вода были сохранены для контроля концентрации акриламида, равной 50%, и концентрации акрилонитрила, равной 2%. Скорость реакции устанавливают по скорости расхода акрилонитрила и скорость деактивации устанавливают по изменению скорости реакции. На основе этих значений рассчитывают продуцирование акриламида.
Для сравнения также осуществляют тот же самый процесс с акрилонитрилом, который не был подвергнут щелочной обработке.
Результатом является пониженная концентрация синильной кислоты в акрилонитриле и снижение скорости деактивации. Продуцирование акриламида на 1 г клеток микроорганизма с использованием обработанного акрилонитрила было вдвое больше по сравнению с продуцированием с использованием акрилонитрила, не вступавшего в эту реакцию.
Результаты приведены в таблице 3.
Согласно настоящему изобретению может быть эффективно предотвращено уменьшение активности фермента - нитрилгидратазы, так что амид успешно продуцируется из нитрила.
Поскольку изобретение было описано детально и со ссылкой на специфические примеры его осуществления, специалистам в данной области техники очевидно, что внутри данного изобретения могут быть сделаны различные изменения и модификации без отступления от его сущности и объема.
Способ получения амида из акрилонитрила включает химическую обработку композиции, содержащей акрилонитрил, с последующим воздействием на указанный акрилонитрил нитрилгидратазой. В результате химической обработки концентрация синильной кислоты в композиции, содержащей акрилонитрил, снижается до 3 долей/млн или менее. Химическая обработка может представлять собой процесс превращения синильной кислоты в комплекс металла, контактирование с ионообменной смолой или обработку в щелочных условиях. В часном случае исполнения используют нитрилгидратазу, полученную из Rhodococcus rhodochrous. Способ позволяет за счет снижения концентрации синильной кислоты в композиции, содержащей акрилонитрил, эффективно тормозить деактивацию нитрилгидратазы. Это позволяет снизить требуемое для проведения реакции количество фермента. 6 з.п. ф-лы, 3 табл.
| СПОСОБ ПОЛУЧЕНИЯ АКРИЛАМИДА | 1996 |
|
RU2077588C1 |
| ШТАММ БАКТЕРИЙ RHODOCOCCUS RHODOCHROUS - ПРОДУЦЕНТ НИТРИЛГИДРАТАЗЫ | 1993 |
|
RU2053300C1 |
| US 4343900 A, 10.08.1982 | |||
| US 4900672 A, 13.02.1990 | |||
| DE 4313649 C1, 26.01.1995. | |||
Авторы
Даты
2004-07-10—Публикация
1998-10-22—Подача