Данное изобретение относится к новым процессам получения промежуточных соединений (в частности, некоторых ариламинов и производных арилгидразинов), полезных при получении пестицидов. В европейских патентных публикациях №№0295117 и 0234119 описано получение пестицидно-активных фенилпиразолов и 5-амино-1-арил-3-цианопиразольных промежуточных соединений, использованных в их синтезе.
Известны различные способы получения данных соединений. Цель данного изобретения предоставить улучшенные или более экономичные способы получения пестицидов и промежуточных соединений, полезных при их изготовлении.
4-Трифторметиланилин, 2-хлор-4-трифторметиланилин и 2,6-дихлор-4-трифторметиланилин являются ценными соединениями, используемыми для синтеза пестицидно-активных фенилпиразольных соединений. Известен ряд методов получения данных соединений. Однако эти приемы дороги, а соединения трудны для получения, требуя многостадийных процедур синтеза. Например, в патентной публикации US №4096185 описано получение 4-трифторметиланилина реакцией 4-хлорбензотрифторида с аммиаком при 200°С в присутствии фторида калия и хлорида меди в сосуде Hastelloy. Остается все еще потребность в разработке новых способов получения указанных соединений.
Заявители настоящего изобретения неожиданно обнаружили новые способы получения некоторых замещенных ариламинов и арилгидразинов, предоставляя таким образом новый способ получения важных 5-амино-1-арил-3-цианопиразольных соединений, которые являются ценными промежуточными продуктами для получения пестицидов.
Соответственно данное изобретение предоставляет способ (А) получения соединения формулы (I):
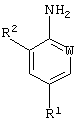
в которой R1 означает галогеналкил (предпочтительно трифторметил), галогеналкокси (предпочтительно трифторметокси) или -SF5;
W означает N или CR3; и
R2 и R3 каждый независимо представляет водород или хлор; или его аддитивной соли с кислотой (кислотно-аддитивной соли), который предусматривает гидрогенолиз соединения формулы (II):
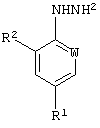
или его кислотно-аддитивной соли металлом или соединением металла (например, солью металла) в восстановительных условиях. Некоторые соединения формул (I) и (II) являются новыми и таким образом составляют часть настоящего изобретения.
Если не оговорено иное в данном изобретении, “галогеналкил” и “галогеналкокси” являются линейными или разветвленными алкилами или алкоксигруппами соответственно, имеющими от одного до трех атомов углерода, замещенными одним или более атомами галогена, выбранными из фтора, хлора и брома.
Аддитивные соли с кислотами, относящиеся к изобретению, являются предпочтительно солями, образуемыми сильными кислотами, такими как минеральные кислоты, например, серная кислота или соляная кислота.
Гидрогенолиз может проводиться с использованием металла или соли металла, выбранного из никеля Ренея (сплав никеля и алюминия), необязательно, в присутствии железа, марганца, кобальта, меди, цинка или хрома; хлорида олова; цинка в присутствии уксусной кислоты; и соли молибдена (III). Реакцию можно также проводить с применением никеля Ренея, платины или палладия (который может быть нанесен на древесный уголь или другой инертный материал) в присутствии газообразного водорода. Когда реакцию проводят с газообразным водородом, обычно используют давление от 2 до 20 бар (предпочтительно от 5 до 10 бар). Предпочтительно гидрогенолиз проводят с применением никеля Ренея.
Реакцию обычно проводят в растворителе, который может быть выбран из спиртов, таких как метанол или этанол; простых эфиров; и ароматических углеводородов (метанол и этанол являются предпочтительными растворителями).
Температура реакции предпочтительно составляет от 20 до 150°С, предпочтительно от 20 до 90°С, более предпочтительно от 50 до 80°С. Количество применяемого катализатора обычно составляет от 0,01 до 3 молярных эквивалентов (предпочтительно от 0,5 до 2 молярных эквивалентов), хотя когда реакцию проводят в атмосфере водорода, меньшие количества дают в общем удовлетворительные результаты. В формулах (I) и (II) и в формулах, приводимых ниже, R1 предпочтительно представляет трифторметил, трифторметокси или -SF5, более предпочтительно трифторметил.
Особенно предпочтительными соединениями формулы (I) являются 2,6-дихлор-4-трифторметиланилин; 2-хлор-4-трифторметиланилин; и 4-трифторметиланилин, Целью процесса (А) является обеспечение возможности получения ариламинов формулы (I) с высоким выходом из легко доступных исходных материалов. Кроме того, реакция может быть очень простой и экономичной в осуществлении, и выделение продукта может производиться непосредственно. Другим достоинством данного способа является то, что соединения формулы (I) могут быть получены при умеренных температурах и давлениях, в то время как прежние способы требуют высоких температур.
Если необходимо, соединения формулы (I) могут быть очищены кристаллизацией, например, из петролейного эфира, для удаления нежелательных изомерных продуктов, которые могут присутствовать в небольших количествах. В качестве альтернативы кристаллизация может быть эффективной на более поздней стадии схемы синтеза.
Соединения формулы (II) могут быть получены по способу (В), в котором соединение формулы (III):
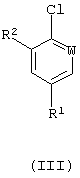
подвергают реакции с гидразином или его аддитивной солью с кислотой или источником ее.
Соединения формулы (III) известны или могут быть получены известными способами.
В соответствии с дополнительным аспектом изобретения процесс (А) может быть объединен с процессом (В) для получения соединения формулы (I) из соединения формулы (III).
Предпочтительно в процессе (В) используют гидразингидрат. Когда применяют аддитивную соль гидразина с кислотой, необязательно присутствует основание, такое как триалкиламин (например, триэтиламин).
Особенно предпочтительными соединениями формулы (II) являются 2,6-дихлор-4-трифторметилфенилгидразин; 2-хлор-4-трифторметилфенилгидразин; и 4-трифторметилфенилгидразин.
Процесс (В) может проводиться в растворителе, выбранном из циклических или алифатических простых эфиров, таких как тетрагидрофуран, 1,4-диоксан или 1,2-диметоксиэтан; N-метилпирролидона; диметилсульфоксида; N,N-диметилформамида; сульфолана; N,N,N',N'-тетраметилмочевины; ароматических углеводородов, которые могут быть замещены одной или более алкильными группами или атомами хлора, таких как хлорбензол или ксилол; спиртов, таких как изопропанол; и пиридина. Предпочтительные растворители включают пиридин, тетрагидрофуран, N,N,N',N'-тетраметилмочевину и 1,4-диоксан (пиридин и тетрагидрофуран являются особенно предпочтительными). Количество используемого растворителя обычно составляет от 1 до 10 мл (предпочтительно от 4 до 8 мл) на грамм соединения формулы (III).
Процесс (В) обычно осуществляют в автоклаве или другом герметизированном сосуде. Обычно применяют давление 1-8 бар (предпочтительно 2-6 бар).
Температура реакции для процесса (В) обычно составляет от 50°С до 250°С, предпочтительно от 120°С до 180°С. Наиболее предпочтительна температура реакции от 120°С до 150°С, когда коррозия сосуда и термическое разложение продукта являются минимальными. Реакцию обычно проводят с использованием от 1 до 20 молярных эквивалентов (предпочтительно от 4 до 8 эквивалентов) источника гидразина.
Катализатор может необязательно использоваться в процессе (В), и, когда он присутствует, его обычно выбирают из фторидов щелочных и щелочноземельных металлов, таких как фторид калия. Количество применяемого катализатора обычно составляет от 0,05 до 2 молярных эквивалентов (предпочтительно от 0,5 до 1 молярного эквивалента). Реакция может также проводиться в присутствии меди или соли меди, предпочтительно хлорида меди (I).
Согласно дополнит ель ним признакам изобретения процесс (А) или объединенные процессы (А) и (В) дают соединение формулы (I), которое очищают осаждением соли, образуемой с помощью обработки сильной кислотой в присутствии органического растворителя.
Объединенный процесс (А) и (В) изобретения является особенно ценным, когда он используется для получения и реакции важного промежуточного 2-хлор-4-трифторметилфенилгидразина, поскольку процесс стадии (В) протекает с высоким выходом и дает вместе с другими процессами данного изобретения эффективный способ получения важных пестицидных соединений фенилпиразола. Однако получение 2-хлор-4-трифторметилфенилгидразина часто дает небольшое количество нежелательного 2-хлор-5-трифторметилфенилгидразина в качестве примеси в дополнение к желаемому изомеру. Обнаружено, что указанная смесь может использоваться непосредственно в следующем процессе (А) с последующей очисткой. Очистка 2-хлор-4-трифторметиланилина может достигаться осаждением соли, образуемой с сильной кислотой, предпочтительно хлористоводородной кислотой, в присутствии органического растворителя. Гидрохлоридная соль может быть получена с применением газообразного хлористого водорода или водной соляной кислоты. Растворителем обычно является спирт, предпочтительно этанол, или галогенированное ароматическое соединение, предпочтительно хлорбензол, или их смесь. Указанная процедура приводит к очень эффективному удалению нежелательного изомера 2-хлор-5-трифторметиланилина с осаждением желаемого изомера в виде гидрохлоридной соли 2-хлор-4-трифторметиланилина с высоким выходом и высокой чистотой.
Таким образом, согласно предпочтительному признаку изобретения процесс (А) или объединенные процессы (А) и (В), в которых R1 означает трифторметил, W означает CR3, R2 означает хлор и R3 означает водород, направлены на получение соединения формулы (I), которое очищают осаждением соли, образуемой с помощью обработки сильной кислотой в присутствии органического растворителя.
Более того, когда для получения 4-трифторметилфенилгидразина используют процесс (В), в котором реагент (4-хлорбензотрифторид) практически нереакционноспособен, реакция протекает с превосходной региоспецифичностью. Кроме того, было обнаружено, что использование катализаторов повышает скорость реакции. В данном случае не могут существовать никакие изомерные продукты, и поэтому процесс в сочетании с последующими стадиями, дает дополнительный полезный способ получения важных пестицидных фенилпиразольных соединений. Как указывалось, особым преимуществом изобретения является то, что оно позволяет эффективно получать соединения формулы (I), в которой оба R2 и R3 означают атом водорода.
Согласно предпочтительному признаку изобретения процесс (А) или объединенные процессы (А) и (В) сопровождаются процессом (С), который предусматривает реакцию соединения формулы (I), в которой W означает N или CR3 и один или оба из R2 и R3 означают атом водорода с хлорирующим агентом для замены одного или каждого атома водорода, обозначенного R2 и R3, и получения соответствующего соединения формулы (I), в которой каждый из R2 и R3 означает атом хлора. Хлорирование может проводиться с применением газообразного хлора или сульфурилхлорида в инертном растворителе, таком как галогенированный углеводород, например, дихлорметан, согласно известным приемам.
В соответствии с дополнительным признаком изобретения процесс (А) или объединенные процессы (А) и (В), (А) и (С), или (А), (В) и (С) могут объединяться с дальнейшей стадией процесса (D), на которой соединение формулы (I) диазотируют с получением соединения формулы (IV):
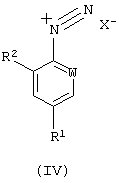
в которой Х означает анион, обычно кислый сульфат или хлорид, которое подвергают реакции с соединением формулы (V):
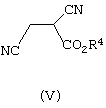
в которой R4 означает C1-6алкил, и, необязательно, реакции с основанием с получением соединения формулы (VI):
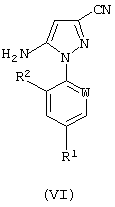
в которой R1, R2 и W имеют значения, определенные выше.
Указанные выше процессы получения соединений формулы (VI) согласно изобретению, в сочетании с указанными выше стадиями реакции для превращения соединений формулы (III) в соединения формул (II) и (I) предоставляют преимущественный новый путь синтеза.
В соответствии с дополнительным признаком изобретения объединенные процессы (А) и (D); (А), (С) и (D); (А), (В) и (D); или (А), (В), (С) и (D) могут быть объединены с дальнейшей стадией процесса (Е) с получением соединения формулы (VII):
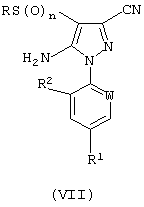
в которой R означает алкил или галогеналкил и п означает 0, 1 или 2. Особенно предпочтительными соединениями формулы (VII) являются 5-амино-1-(2,6-дихлор-4-трифторметилфенил)-3-циано-4-трифторметилсульфинилпиразол (фипронил) и 5-амино-1-(2,6-дихлор-4-трифторметилфенил)-3-циано-4-этилсульфинилпиразол этипрол). Стадия процесса (Е) является известной, описанной, например, в европейских патентных публикациях №№0295117 и 0374061 и патентной публикации US №5814652.
Соединения формулы (I), полученные по способу (А) изобретения, особенно полезны при получении пестицидно-активных производных 5-амино-1-арил-3-цианопиразола формулы (VII), полученных из промежуточных соединений формулы (VI), например, согласно следующей схеме реакций:
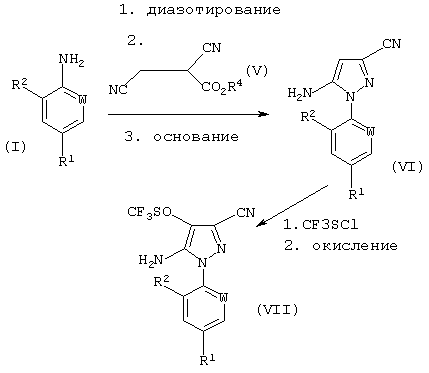
на которой R1, R2, R3 или R4 имеют значения, определенные выше.
Следующие неограничивающие примеры иллюстрируют изобретение. Показано, что каждый продукт идентичен известному приведенному в ссылках образцу соединения.
Пример 1
Получение 4-трифторметиланилина
Никель Ренея (2 г) добавляли к раствору 4-трифторметилфенилгидразина (1 г) в метаноле (5 мл) и нагревали с обратным холодильником в течение 1 часа. Охлажденную смесь фильтровали и упаривали, получая указанное в заголовке соединение со 100%-ным выходом.
Пример 2
Получение 2-хлор-4-трифторметиланилина
Процедуру примера 1 повторяли с использованием 2-хлор-4-трифторметилфенилгидразина и получали указанное в заголовке соединение со 100%-ным выходом.
Пример 3
Получение 4-трифторметиланилина
Процедуру примера 1 повторяли, но с использованием каталитического количества никеля Ренея в метаноле (8-10 мл на ммоль 4-трифторметилфенилгидразина) в атмосфере водорода (5 бар) при перемешивании при 20°С в течение 2 часов. Смесь фильтровали и упаривали, получая чистое указанное в заголовке соединение с 75%-ным выходом (неоптимизированное).
При осуществлении способа сходным образом получали также с аналогичными результатами:
2-хлор-4-трифторметиланилин; и
2,6-дихлор-4-трифторметиланилин.
Пример 4
Получение 4-трифторметилфенилгидразина
Смесь 4-хлорбензотрифторида (1,08 г), гидразингидрата (1,8 г, 6 молярных эквивалентов) и пиридина (5 мл) нагревали в автоклаве (продутом аргоном) в течение 6 часов при 180°С. Смесь охлаждали, избыток гидразина декантировали, и органическую фазу упаривали. Остаток кристаллизовали из петролейного эфира, получая указанное в заголовке соединение с 20%-ным выходом. Показано, что потреблялось 20% исходного материала, что свидетельствует о том, что реакция протекает с высокой селективностью.
Пример 5
Получение 4-трифторметилфенилгидразина с применением фторида калия в качестве катализатора
Процедуру примера 4 повторяли, но с добавлением фторида калия (0,8 молярных эквивалента), получая указанное в заголовке соединение с 30%-ным выходом. Было показано, что потреблялось 30% исходного материала, что свидетельствует о том, что реакция протекает с высокой селективностью.
Вышеуказанную реакцию повторяли, но с использованием в качестве растворителя N,N,N',N'-тетраметилмочевины, получая указанное в заголовке соединение с 40%-ным выходом. Показано, что потреблялось 40% исходного материала, что свидетельствует о том, что реакция протекает с высокой селективностью.
Пример 6
Получение 4-трифторметилфенилгидразина с применением в качестве катализатора фторида калия и хлорида меди (I)
Процедуру примера 4 повторяли, но с добавлением фторида калия (0,1 молярного эквивалента) и хлорида меди (I) (0,1 молярного эквивалента), и получали указанное в заголовке соединение с 14%-ным выходом. Показано, что потреблялось 14% исходного материала, что свидетельствует о том, что реакция протекает с высокой селективностью.
Пример 7
Получение 2-хлор-4-трифторметилфенилгидразина
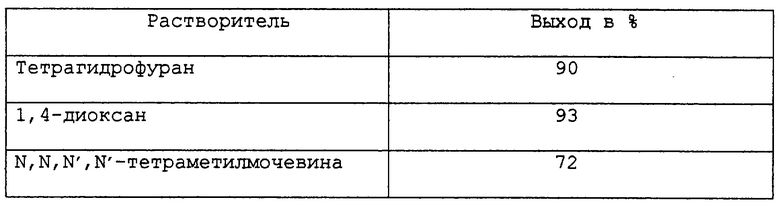
Процедуру примера 4 повторяли, но с использованием 3,4-дихлорбензотрифторида. После обработки выделяли указанное в заголовке соединение с 95%-ным выходом. Было показано, что потреблялось 100% исходного материала, что свидетельствует о том, что реакция протекает как с высокой селективностью, так и с высоким выходом.
Вышеуказанную реакцию повторяли, но с применением различных других растворителей. Получали следующие выходы указанного в заголовке соединения, см. таблицу.
Пример 8
Двустадийное получение и очистка 2-хлор-4-трифторметиланилина, исходя из 3,4-дихлорбензотрифторида
(а) Смесь 3,4-дихлорбензотрифторида (48 г), гидразингидрата (65 г) и пиридина (240 г) перемешивали и нагревали при 150°С 6 часов в автоклаве под давлением 4 бара. Охлажденную смесь гасили раствором гидроксида натрия, и органический слой упаривали в вакууме. Остаток растворяли в диэтиловом эфире, промывали (водой), и эфир упаривали, получая 2-хлор-4-трифторметилфенилгидразин и 2-хлор-5-трифторметилфенилгидразин в виде смеси 95/5 (36 г),
(b) к раствору вышеуказанной смеси изомеров (35,85 г) в этаноле добавляли никель Ренея (0,7 г) в реакторе гидрирования при 50°С в атмосфере водорода при 5 барах в течение 5 часов. Смесь охлаждали, фильтровали и упаривали, получая смесь 95/5 2-хлор-4-трифторметиланилина и 2-хлор-5-трифторметиланилина (33,1 г). Газообразный хлористый водород добавляли на протяжении 0,5 часа к раствору вышеуказанной смеси в этаноле и хлорбензоле, охлаждали до 0°С и фильтровали, получая гидрохлорид 2-хлор-4-трифторметиланилина (33,5 г), имеющий чистоту >99%. Общий выход в расчете на 3,4-дихлорбензотрифторид составил 85%.
Изобретение относится к новому способу получения производных аминобензола формулы (I)
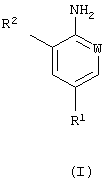
где R1 – галогеналкил, галогеналкокси, W представляет CR3, R2 и R3 независимо представляют водород или хлор, или их кислотно-аддитивных солей, который предусматривает гидрогенолиз соединения формулы (II)
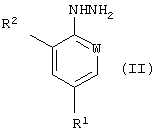
или его кислотно-аддитивной соли, где R1, R2 и W имеют вышеуказанные значения, с металлом или соединением металла в восстановительных условиях. Полученное соединение формулы (I) можно подвергнуть очистке путем обработки его сильной кислотой в органическом растворителе с последующим осаждением образующейся соли. Способ позволяет упростить процесс получения целевого продукта за счет проведения процесса при более низких температурах и давлении, чем в известном способе, а также повысить выход целевого продукта. 2 н. и 5 з.п. ф-лы, 1 табл.
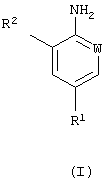
в которой R1 представляет галогеналкил, галогеналкокси;
W представляет CR3;
R2 и R3 каждый независимо представляет водород или хлор;
или его кислотно-аддитивной соли; который предусматривает гидрогенолиз соединения формулы (II)
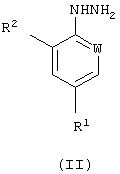
или его кислотно-аддитивной соли с металлом или соединением металла в восстановительных условиях.
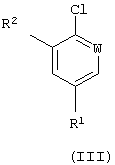
в которой R1, R2 и W имеют значения, определенные выше,
с гидразином или его кислотно-аддитивной солью.
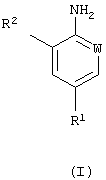
в которой R1 представляет галогеналкил, галогеналкокси;
W представляет CR3;
R2 и R3 каждый независимо представляет водород или хлор,
или его кислотно-аддитивной соли путем дополнительной очистки соединения, полученного по пп.1-4 осаждением соли, образуемой с помощью обработки сильной кислотой в присутствии органического растворителя.
| СПОСОБ ПОЛУЧЕНИЯ 2-БРОМ-4,6-ДИНИТРОАНИЛИНА | 1988 |
|
RU2007385C1 |
| US 4096185 A, 20.06.1978 | |||
| US 4535154 A, 13.08.1985 | |||
| US 5437853 A, 01.08.1995. | |||
Авторы
Даты
2004-09-10—Публикация
2000-03-30—Подача