Дигалоидазолопиримидины полезны в качестве промежуточных соединений в получении разнообразных агрохимических и фармацевтических соединений. В частности, 5,7-дигалоид-6-арил- 1,2,4-триазоло[1,5-a] пиримидины являются ключевыми промежуточными соединениями в получении фунгицидных производных триазолопиримидина, которые описаны в EP-A2-550113.
В EP-A2-550113 описан способ получения 5,7-дигалоид-6-арил-1,2,4- триазоло[1,5-a] пиримидинов из эфиров малоновой кислоты и 3- амино-1,2,4-триазола. Однако этот способ не является полностью удовлетворительным, т.к. эти соединения пиримидина получают с низким выходом.
G. Fischer (Advances in Heterocyclic Chemistry 1993, 57, 81-138) описывает образование триазолопиримидинов из 1,3-дикарбонильных соединений и 3-амино-1,2,4-триазола и утверждает, что нагревание с обратным холодильником в ледяной уксусной кислоте представляет собой "стандартные условия". Y. Makisumi (Chem. Pharm. Bull., 1961, 9, 801-808) сообщает, что при этих условиях не происходит конденсация диэтилмалоната с 3-амино- 1,2,4-триазолом. Makisumi описывает, что эта реакция может осуществляться в присутствии этоксида натрия в этаноле и что продукт дигидрокситриазолопиримидин может превращаться в соответствующий дихлортриазолопиримидин с использованием большого избытка оксихлорида фосфора. Однако способ Makisumi не является полностью удовлетворительным для получения дигалоидазолопиримидинов, т.к. требуется большой избыток оксихлорида фосфора, и общий выход реакций, исходя из диэтилмалоната, часто является низким.
Краткое изложение существа изобретения
Данное изобретение обеспечивает эффективный и производительный способ получения дигалоидазолопиримидина, имеющего структурную формулу I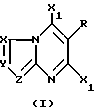
где X1 обозначает хлор или бром;
R обозначает фенил, необязательно замещенный одним или более галогенами, нитро, циано, C1-C6-алкильными, C1-C6-галогеналкильными, C1-C6-алкокси, C1-C6-галоидалкокси, C1-C4-алкоксикарбонильными, фенильными, фенокси или бензилокси группами, нафтил, необязательно замещенный одним или более галогенами, нитро, циано, C1-C6-алкильными, C1-C6- галоидалкильными, C1-C6-галогеналкокси, C1-C4- алкоксикарбонильными, фенильными, фенокси или бензилокси группами, водород,
C1-C6-алкил, необязательно замещенный одним или более заместителями: галоген, нитро, циано, C1-C4-алкил, C1-C4-галоидалкил, C1-C4-алкокси или C1-C4-галоидалкокси группы, или C2-C6-алкенил, необязательно замещенный одним или более галогенами, нитро, циано, C1-C4-алкилами, C1-C4-галоидалкилами, C1-C4-алкокси или C1-C4-галоидалкокси группами;
X обозначает CR1 или N;
Y обозначает CR2 или N;
Z обозначает CR3 или N;
R1, R2 и R3 каждый независимо представляет собой водород или C1-C6-алкил, необязательно замешенный одним или более галогенами, нитро, циано, C1-C4-алкилами, C1-C4-галоидалкилами, C1-C4-алкокси, C1-C4-галоидалкокси, амино, C1-C4-алкиламино или ди-(C1-C4-алкил)амино группами, и когда R1 и R2 взяты вместе с атомами, к которым они присоединены, они могут образовывать кольцо, в котором R1R2 представлен структурой: -CR4= CR5-CR6=CR7-, где R4, R5, R6 и R7 каждый независимо представляет собой водород, нитро, циано, C1-C4-алкил, C1-C4-галоидалкил, C1-C4-алкокси или C1-C4-галоидалкокси.
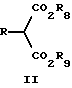
Данный способ предусматривает: (a) реакцию (1) эфира малоновой кислоты, имеющего структурную формулу II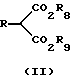
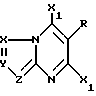
где R8 и R9 каждый независимо представляет собой C1-C6-алкил и R имеет данное выше значение, с (2) гетероциклиламином, имеющим структурную формулу III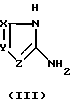
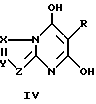
где X, Y и Z имеют данные выше значения, при температуре не менее приблизительно 100oC с образованием промежуточной соли; (b) необязательное подкисление промежуточной соли водной кислотой для образования дигидроксиазолопиримидина, имеющего структурную формулу IV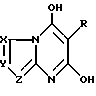
где R, X, Y и Z имеют значения, описанные выше; и (c) галоидирование промежуточной соли или дигидроксиазолопиримидина, по крайней мере, примерно двумя молярными эквивалентами галоидирующего агента, например оксихлорида форсфора, оксибромида фосфора, пентахлорида фосфора или пентабромида фосфора или их подходящей смеси при температуре, по крайней мере, приблизительно 100oC.
Данное изобретение обеспечивает также эффективный и производительный способ получения дигидроксиазолопиримидина, имеющего структурную формулу IV
где R, X, Y и Z имеют данные выше значения. Продукт IV получают с помощью описанной выше процедуры, согласно которой промежуточную соль подкисляют; затем продукт IV можно выделять, если нужно.
Таким образом, целью данного изобретения является обеспечение эффективного нового способа получения дигалоидазолопиримидинов.
Другой целью данного изобретения является обеспечение нового способа получения дигидроксиазолопиримидинов.
Другие цели и преимущества данного изобретения будут очевидными для специалистов в данной области из следующего далее описания и прилагаемой формулы изобретения.
Подробное описание изобретения
Согласно одному из предпочтительных вариантов данного изобретения эфир малоновой кислоты формулы (II) подвергают реакции, по меньшей мере, с одним молярным эквивалентом гетероциклиламина, представленного формулой III, предпочтительно в пределах температур приблизительно 120oC - 200oC, более предпочтительно приблизительно 150oC - 180oC, и необязательно в присутствии основания и/или растворителя с образованием промежуточной соли. Промежуточную соль галоидируют, по меньшей мере, двумя молярными эквивалентами оксихлорида фосфора, оксибромида фосфора, пентахлорида фосфора или пентабромида фосфора или их подходящими смесями предпочтительно в пределах температур приблизительно 120oC - 150oC.
В качестве преимущества было обнаружено, что дигалоидазолопиримидины могут быть получены с высоким выходом и хорошей чистотой эффективным и производительным способом данного изобретения. В противоположность этому дигалоидазолопиримидины получают со сравнительно низким выходом при получении их известными в этой области способами.
Другим преимуществом данного изобретения является то, что способ изобретения можно проводить в одной емкости, когда промежуточную соль не подкисляют. Проведение цепи реакций в одном резервуаре является высокожелательным, поскольку это позволяет избежать выделения промежуточных соединений и значительно снижает количество получаемых отработанных химикатов.
Согласно еще одному предпочтительному варианту данного изобретения промежуточную соль получают в присутствии добавленного основания. Основание предпочтительно присутствует в количестве, по меньшей мере, одного молярного эквивалента по отношению к эфиру малоновой кислоты. Основания, подходящие для использования в способе данного изобретения, включают третичные амины, такие как три(C2-C6-алкил) амины, пиридин, замещенные пиридины, хинолин, замещенные хинолины и мочевины; гидроксиды щелочных металлов, такие как гидроксид натрия и гидроксид калия; гидроксиды щелочноземельных металлов, такие как гидроксид кальция и гидроксид магния; C1-C6-алкоксиды щелочных металлов, такие как этоксид натрия и трет-бутоксид калия; C1-C6-алкоксиды щелочноземельных металлов, такие как этоксид магния; карбонаты щелочных металлов, такие как карбонат натрия и карбонат калия; и карбонаты щелочноземельных металлов, такие как карбонат кальция. Предпочтительные основания включают три (C2-C6-алкил) амины, такие как триэтиламин и трибутиламин, пиридин, 4-(N, N-диметиламино) пиридин, хинолин и N,N,N',N'-тетраметилмочевина, причем триэтиламин и трибутиламин являются более предпочтительными.
Промежуточная соль данного изобретения представлена структурной формулой V при получении в отсутствие добавленного основания и структурной формулой VI при получении в присутствии добавленного основания: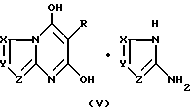
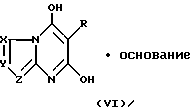
где R, X, Y и Z имеют данные выше значения и "основание" обозначает добавленное основание.
Согласно еще одному предпочтительному варианту данного изобретения присутствует растворитель. Растворители, подходящие для использования в способе данного изобретения, имеют точку кипения, по меньшей мере, приблизительно 80oC и включают мезитилен (сим-триметилбензол), толуол, ксилолы и их смеси; хлорированные ароматические углеводороды, такие как моно- и дигалоидбензолы и их смеси; полициклические ароматические углеводороды, такие как нафталин, алкилнафталины и их смеси; спирты, такие как бутанол; и их смеси. Растворитель данного изобретения предпочтительно имеет точку кипения в пределах приблизительно 80oC - 220oC, более предпочтительно - приблизительно 120oC - 180oC. Мезитилен является одним из предпочти тельных растворителей данного изобретения.
Реакцию между эфиром малоновой кислоты и гетероциклиламином предпочтительно проводят при давлении приблизительно 1 атм или выше. Если реакция включает в себя растворитель, имеющий точку кипения (определенную при нормальном атмосферном давлении) ниже температуры реакции, то давление реакции следует повысить таким образом, чтобы точка кипения растворителя повысилась, по меньшей мере, до температуры реакции.
В некоторых вариантах способа изобретения используют водную кислоту для подкисления промежуточной соли. Водными кислотами, подходящими для использования в способе, являются водные минеральные кислоты, такие как соляная кислота, бромистоводородная кислота и серная кислота, и водные органические кислоты, такие как трифторуксусная кислота, причем соляная кислота, бромистоводородная кислота и серная кислота являются предпочтительными.
Реакция галоидирования может включать реакцию промежуточной соли или дигидроксиазолопиримидина с подходящим галоидирующим агентом при условиях, способствующих образованию желаемого дигалоидазолопиримидина. Можно использовать любой галоидирующий агент и условия, известные в этой области знаний. Предпочтительно галоидирующий агент и условия являются такими, которые описаны здесь для предпочтительных вариантов данного изобретения. Благоприятно проводить реакцию галоидирования при атмосферном давлении или при давлении, большем, чем атмосферное давление. Термин "их подходящая смесь" применительно к данной заявке и формуле изобретения в отношении галоидирующих агентов, описанных здесь, определяется как смесь оксихлорида фосфора и пентахлорида фосфора или смесь оксибромида фосфора и пентабромида фосфора.
Способ данного изобретения особенно полезен для получения дигалоидазолопиримидинов, в которых
X1 обозначает хлор;
R обозначает фенил, необязательно замещенный одним или более заместителями: галогеном, C1-C4-алкилом, C1-C4-галоидалкилом, C1-C4-алкокси, C1-C4-галоидалкокси, фенилом, фенокси или бензилокси группами, или
нафтил;
X обозначает CR1 или N;
Y обозначает CR2;
Z обозначает N и
R1 и R2 каждый независимо обозначает водород и, когда R1 и R2 взяты вместе с атомами, к которым они присоединены, они могут образовывать кольцо, в котором R1R2 представлен структурой:
-CH=CH-CH=CH-.
В качестве преимущества данное изобретение особенно полезно для получения 5,7-дигалоид-6-арил-1,2,4-триазоло[1,5-a]пиримидинов формулы I, где X1 обозначает хлор;
R обозначает фенил, необязательно замещенный одним или более радикалами: галогеном, C1-C4-алкилом, C1-C4-галоидалкилом, C1-C4-алкокси или C1-C4-галоидалкокси группами;
X и Z обозначают N и
Y обозначает CH.
Способ данного изобретения может давать удивительно высокие выходы дигидроксиазолопиримидинов и дигалоидазолопиримидинов. Одним из ключевых факторов является температура реакции между эфиром малоновой кислоты и гетероциклиламином. Применение основания и/или растворителя может также повышать выход в некоторых вариантах. Специалисты в данной области смогут без излишнего экспериментирования выбрать предпочтительную комбинацию температуры и необязательных основания и/или растворителя для того или иного конкретного варианта в объеме данного изобретения при рассмотрении предшествующего описания предпочтительных вариантов и следующих ниже примеров.
Для облегчения дальнейшего понимания изобретения представлены нижеследующие иллюстративные примеры. Изобретение не ограничивается конкретными описанными или проиллюстрированными вариантами воплощения и охватывает полный объем прилагаемой формулы изобретения.
Пример 1
Получение 3-амино-1,2,4-триазольной соли 5,7-дигидрокси-6-(2-хлор- 6-фторфенил)-1,2,4-триазоло[1,5-a]пиримидина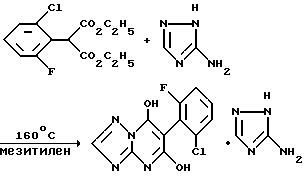
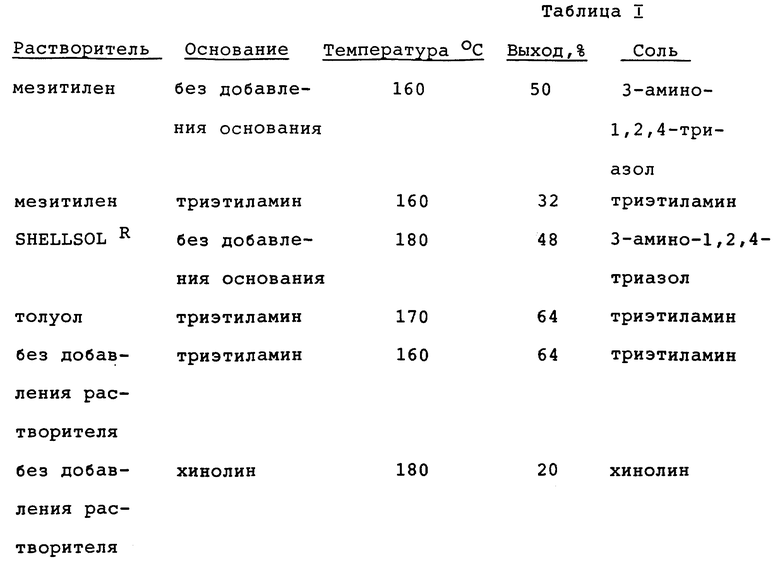
Смесь диэтил-(2-хлор-6-фторфенил)-малоната (29 г, 0,1 моль), 3-амино-1,2,4-триазола (8,4 г, 0,1 моль) и растворителя мезитилена (10 мл) нагревают при 160oC в течение 7 часов и фильтруют, получая твердое вещество. Твердое вещество промывают диизопропиловым эфиром и сушат, получая указанный в заголовке продукт в виде твердого вещества (18 г, 50% выход, т.пл. 260-266oC).
Следуя, в основном, той же процедуре, но с использованием подходящего растворителя и/или основания, получают соли 5,7-дигидрокси-6-(2-хлор-6-фторфенил)-1,2,4-триазоло[1,5-a] пиримидина, представленные в Таблице I.
Пример 2
Получение 5,7-дихлор-6-(2-хлор-6-фторфенил)-1,2,4-триазоло [1,5-a]пиримидина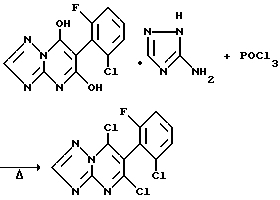
Смесь 3-амино-1,2,4-триазоловой соли 5,7-дигидрокси-6-(2- хлор-6-фторфенил)-1,2,4-триазоло[1,5-a] пиримидина (34,8 г, 0,095 моль) и хлорокиси фосфора (100 мл) нагревается в автоклаве при 140oC (2,8 бар) в течение 4 часов, и избыток хлорокиси фосфора удаляется с помощью перегонки. Полученная в результате реакционная смесь охлаждается до комнатной температуры и выливается в смесь воды и дихлорметана (300 мл, 1:1) при поддержании температуры смеси ниже 30oC. Органическая фаза отделяется, сушится над безводным сульфатом натрия и концентрируется в вакууме, давая масло, которое кристаллизуется на протяжении ночи, давая целевой продукт в виде твердого вещества (22,4 г, 74% выход, т.пл. 118-120oC).
Пример 3
Получение 5,7-дихлор-6-(2-хлор-6-фторфенил)-1,2,4-триазоло [1,5-a]пиримидина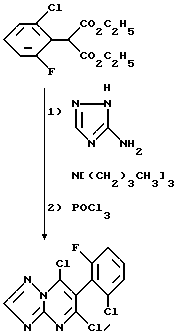
Смесь 3-амино-1,2,4-триазола (12,6 г, 0,15 моль), диэтил- (2-хлор-6-фторфенил) малоната (47,6 г, 0,15 моль) и трибутиламина (27,8 г, 0,15 моль) нагревают при 170oC, давая возможность отгоняться образующемуся во время реакции этанолу. После 2 часов оставшийся этанол удаляют медленным током азота в течение 30 минут. Затем реакционную смесь охлаждают до 130oC и добавляют оксихлорид фосфора (69 г, 0,45 моль) по каплям в течение 20 минут. Полученный прозрачный коричневый раствор нагревают с обратным холодильником в течение 6 часов, охлаждают до комнатной температуры и медленно добавляют к смеси толуол/вода (5:6) (1100 мл) при перемешивании. Органическую фазу отделяют, промывают последовательно разбавленной соляной кислотой и водой, сушат над безводным сульфатом натрия и концентрируют в вакууме, получая коричневое вязкое масло (44,5 г), содержащее 90% указанного в заголовке продукта (83% выход).
Пример 4
Получение 5,7-дигидрокси-6-(2-хлор-6-фторфенил)-1,2,4-триазоло [1,5-a] пиримидина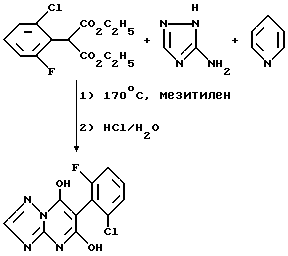
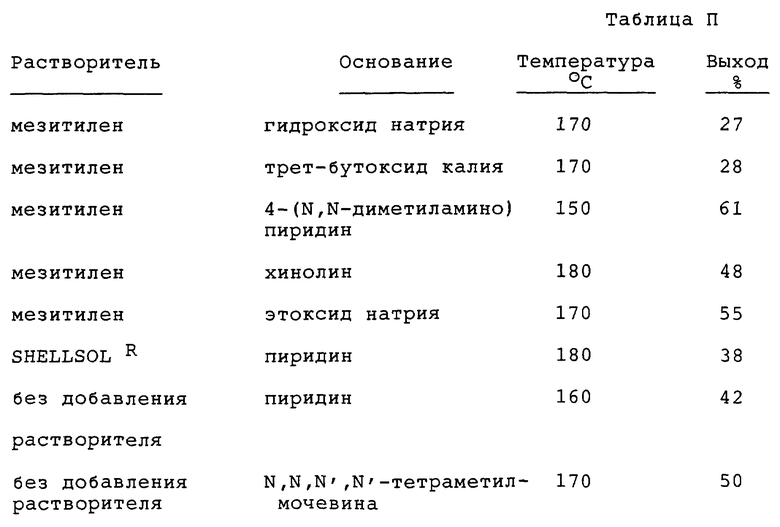
Смесь диэтил-(2-хлор-6-фторфенил)-малоната (7,3 г, 0,025 моля), 3-амино-1,2,4-триазола (2,1 г, 0,025 моль), мезитилена (20 мл) и пиридина (5 мл) нагревают с обратным холодильником в течение 7 часов при 170oC, охлаждают до комнатной температуры и декантируют, получая твердое вещество. Раствор твердого вещества в воде (50 мл) подкисляют концентрированной соляной кислотой (5 мл), и полученный осадок собирают, промывают водой и сушат, получая указанный в заголовке продукт в виде твердого вещества (5 г, 71% выход, т. пл. 220oC).
Следуя в основном такой же процедуре, но с использованием подходящего растворителя и/или основания, получают 5,7-дигидрокси-6- (2-хлор-6-фторфенил)-1,2,4-триазоло[1,5-a]пиримидин с выходами, указанными в Таблице II.
Сравнительный пример
Получение 5,7-дигидрокси-6-(2-хлор-6-фторфенил)-1,2,4-триазоло [1,5-a] пиримидина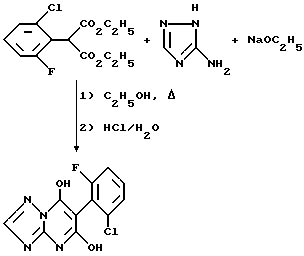
Диэтил-(2-хлор-6-фторфенил)малонат (108 г, 0,37 моль) и 3-амино-1,2,4-триазол (31,2 г, 0,37 моль) добавляют к раствору этоксида натрия (приготовленному предварительно растворением натрия (8,5 г, 0,37 моль) в этаноле (250 мл)). Полученную реакционную смесь нагревают с обратным холодильником в течение 50 часов, охлаждают до комнатной температуры и фильтруют, получая твердое вещество, которое промывают диизопропиловым эфиром. Раствор промытого твердого вещества в воде подкисляют концентрированной соляной кислотой и полученный осадок собирают, промывают водой и сушат, получая указанный в заголовке продукт в виде твердого вещества (15,7 г, 14,5% выход, т.пл. 215oC).
Пример 5
Получение 2-аминобензимидазольной соли 5,7-дигидрокси-6- (2-хлор-6-фторфенил)бензимидазопиримидина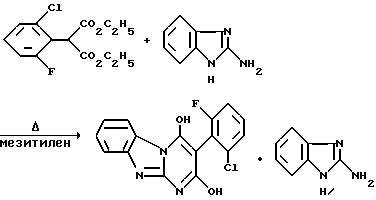
Смесь диэтил-(2-хлор-6-фторфенил)-малоната (5,8 г, 0,02 моль) и мезитилена нагревают с обратным холодильником, обрабатывают порциями 2-аминобензимидазолом (2,7 г, 0,02 моль) в течение 2 часов, нагревают с обратным холодильником в течение 4 часов, охлаждают до комнатной температуры и разбавляют ацетоном. Полученную смесь фильтруют, получая указанный в заголовке продукт в виде белых кристаллов (5,1 г, 55% выход, т.пл. 313-325oC.
Изобретение описывает эффективный и производительный способ получения дигалоидазолопиримидина, имеющего структурную формулу I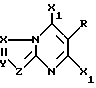
В этом способе эфир малоновой кислоты (II) подвергают реакции с гетероазолиламином (III) с образованием промежуточной соли, которая необязательно может быть подкислена для образования дигидроксиазолопиримидина (IV); затем соль или дигидроксиазолопиримидин галоидируют. 2 с. и 26 з.п.ф-лы, 2 табл.
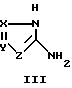
в которой X1 представляет хлор или бром;
R представляет фенил, необязательно замещенный одним или более галогенами, нитро, циано, C1 - C6 алкил, C1 - C6 галоидалкил, C1 - C6 алкокси, C1 - C6 галоидалкокси, C1 - C4 алкоксикарбонил, фенил, фенокси или бензилоксигруппами; нафтил, необязательно замещенный одним или более галогенами, нитро, циано, C1 - C6 алкил, C1 - C6 галоидалкил, C1 - C6 алкокси, C1 - C6 галоидалкокси, C1 - C4 алкоксикарбонил, фенил, фенокси или бензилоксигруппами; водород; C1 - C6 алкил, необязательно замещенный одним или более галогенами, нитро, циано, C1 - C4 алкил, C1 - C4 галоидалкил, C1 - C4 алкокси или C1 - C4 галоидалкоксигруппами; C3 - C8 циклоалкил, необязательно замещенный одним или более галогенами, нитро, циано, C1 - C4 алкил, C1 - C4 галоидалкил, C1 - C4 алкокси или C1 - C4 галоидалкоксигруппами; C2 - C6 алкенил, необязательно замещенный одним или более галогенами; нитро, циано, C1 - C4 алкил, C1 - C4 галоидалкил, C1 - C4 алкокси или C1 - C4 галоидалкоксигруппами;
X представляет CR1 или N;
Y представляет CR2 или N;
Z представляет CR3 или N;
R1, R2 и R3 представляют каждый независимо водород или C1 - C6 алкил, необязательно замещенный одним или более галогенами, нитро, циано, C1 - C4 алкил, C1 - C4 галоидалкил, C1 - C4 алкокси, C1 - C4 галоидалкокси, амино, C1 - C4 алкиламино или ди(C1 - C4алкил)аминогруппами; или когда R1 и R2 взяты вместе с атомами, к которым они присоединены, они могут образовывать кольцо, в котором R1R2 представлен структурой -CR4=CR5-CR6=CR7-, где R4, R5,
R6 и R7 представляют каждый независимо водород, нитро, циано, C1 - C4 алкил, C1 - C4 галоидалкил, C1 - C4 алкокси или C1 - C4 галоидалкокси;
который предусматривает реакцию эфира малоновой кислоты общей формулы II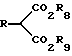
в которой R8 и R9 представляют каждый независимо C1 - C6 алкил;
R имеет указанные выше значения,
с гетероазолиламином общей формулы III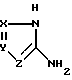
в которой X, Y и Z имеют указанные выше значения,
и галоидирование, отличающийся тем, что взаимодействие соединений II и III ведут при температуре не менее 100oС, если необходимо, в присутствии основания с получением промежуточной соли дигидроксипиримидина и исходного гетероазолиламина II или используемого основания и галоидированию подвергают или непосредственно промежуточную соль, или дигидроксиазолопиримидин, полученный при подкислении промежуточной соли водной кислотой, используя для галоидирования, по крайней мере, два эквивалента галоидирующего агента.
в которой R представляет фенил, необязательно замещенный одним или более галогенами, нитро, циано, C1 - C6 алкил, C1 - C6 галоидалкил, C1 - C6 алкокси, C1 - C6 галоидалкокси, C1 - C4 алкоксикарбонил, фенил, фенокси или бензилоксигруппами; нафтил, необязательно замещенный одним или более галогенами, нитро, циано, C1 - C6 алкил, C1 - C6 галоидалкил, C1 - C6 алкокси, C1 - C6 галоидалкокси, C1 - C4 алкоксикарбонил, фенил, фенокси или бензилоксигруппами; водород; C1 - C6 алкил, необязательно замещенный одним или более галогенами, нитро, циано, C1 - C4 алкил, C1 - C4 галоидалкил, C1 - C4 алкокси или C1 - C4 галоидалкоксигруппами; C3 - C8 циклоалкил, необязательно замещенный одним или более галогенами, галоген, нитро, циано, C1 - C4 алкил, C1 - C4 галоидалкил, C1 - C4 алкокси или C1 - C4 галоидалкоксигруппами; C2 - C6 алкенил, необязательно замещенный одним или более галогенами, нитро, циано, C1 - C4 алкил, C1 - C4 галоидалкил, C1 - C4 алкокси или C1 - C4 галоидалкоксигруппами; X представляет CR1 или N; Y представляет CR2 или N; Z представляет CR3 или N; R1, R2 и R3 представляют, каждый независимо, водород или C1 - C6 алкил, необязательно замещенный одним или более галогенами, нитро, циано, C1 - C4 алкил, C1 - C4 галоидалкил, C1 - C4 алкокси, C1 - C4 галоидалкокси, амино, C1 - C4 алкиламино или ди(C1 - C4алкил)аминогруппами, или когда R1 и R2 взяты вместе с атомами, к которым они присоединены, они могут образовывать кольцо, в котором R1R2 представлен структурой -CR4= CR5-CR6= CR7-, где R4, R5, R6 и R7 представляют каждый независимо водород, нитро, циано, C1 - C4 алкил, C1 - C4 галоидалкил, C1 - C4 алкокси или C1 - C4 галоидалкокси,
который предусматривает реакцию эфира малоновой кислоты общей формулы II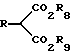
в которой R8 и R9 представляют каждый независимо C1 - C6 алкил;
R имеет указанные выше значения,
с гетероазолиламином общей формулы III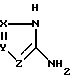
в которой X, Y и Z имеют указанные выше значения,
отличающийся тем, что взаимодействие соединений II и III ведут при температуре не менее 100oС, если необходимо, в присутствии основания с получением промежуточной соли дигидроксипиримидина и исходного гетероазолиламина II или используемого основания, которую подкисляют водной кислотой.
| Кассета для красящей ленты | 1973 |
|
SU550113A3 |
| RU 2066295 C1, 10.01.95 | |||
| SU 1366060 A3, 07.01.88 | |||
| Способ получения 3-замещенных тетрагидропирроло/1,2- @ / пиримидинов,их кислотно-аддитивных или четвертичных солей | 1980 |
|
SU1048986A3 |
| Заграждающий фильтр | 1975 |
|
SU628559A1 |
| Устройство для бескольцевого прядения | 1973 |
|
SU531901A1 |
| Способ химико-термической обработки труб | 1975 |
|
SU591528A1 |
Авторы
Даты
2000-04-20—Публикация
1996-09-30—Подача