ОПИСАНИЕ
Данное изобретение относится к новым способам получения промежуточных соединений (в частности определенных анилиновых соединений и производных фенилгидразина), применяемых в синтезе пестицидов.
3,5-Дигалогеноанилины, и, в частности, 3,5-дихлоранилин, являются важными синтетическими промежуточными продуктами для множества различных соединений, включая агрохимические фунгициды, например, как описано в патентной публикации США №3755350 или в немецкой патентной публикации №2906574.
Известны различные способы синтеза указанных соединений (в частности, 3,5-дихлоранилина), например, как описано в японских патентных публикациях №№05194330 и 60048500 и в патентной публикации США №4508922. Однако указанные способы обычно неэффективны, медленны и страдают слабой селективностью и низкими выходами. Более того, они обычно требуют использования аммиака при высоких температурах и/или давлении. Таким образом остается нужда в разработке новых способов для получения указанных соединений, в частности нахождения способов, которые безопасны в проведении, эффективны и могут быть осуществлены при умеренных температурах и давлении.
Неожиданно обнаружены новые способы получения определенных замещенных анилинов и фенилгидразинов, которые не страдают указанными недостатками, являясь, таким образом, новым способом получения ценных синтетических промежуточных продуктов.
Данное изобретение, таким образом, предлагает способ (А) получения замещенного анилина формулы (I)
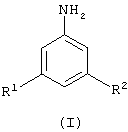
где каждый из R1 и R2 независимо означает атом галогена; или его кислотно-аддитивной соли, который включает гидрогенолиз замещенного фенилгидразина формулы (II)
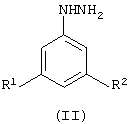
где R1 и R2 определены выше; или его кислотно-аддитивной соли в присутствии металла или соединения металла (например, соли металла) в восстановительных условиях.
Если не оговорено особо, в данном описании атомы галогена выбраны из фтора, хлора, брома и йода.
Кислотно-аддитивные соли, упомянутые в изобретении, предпочтительно являются солями, образованными сильными кислотами, такими как минеральные кислоты, например, серная кислота или соляная кислота.
Гидрогенолиз может быть осуществлен с применением металла или соли металла, выбранных из никеля Ренея (никель-алюминиевого сплава), необязательно в присутствии железа, марганца, кобальта, меди, цинка или хрома, двухлористого олова, цинка в присутствии уксусной кислоты, и соли молибдения (III). Реакция также может быть проведена с применением никеля Ренея, платины или палладия (который может быть нанесен на уголь или другой инертный материал) в присутствии газообразного водорода. Если реакцию ведут с газообразным водородом, обычно применяют давление от 2 до 20 бар (предпочтительно от 5 до 10 бар). Обычно гидрогенолиз проводят с применением никеля Ренея.
Реакция может быть осуществлена в отсутствие или в присутствии растворителя, но обычно ее проводят в растворителе, который может быть выбран из спиртов, таких как метанол, этанол, пропанол, изопропанол, бутанол, изобутанол или третичный бутанол, простых эфиров, ароматических углеводородов и воды (или их смесей). Метанол и этанол являются предпочтительными растворителями.
Температура реакции обычно равна от 20 до 150°С, предпочтительно от 20 до 90°С. Количество используемого катализатора обычно составляет от 0,01 до 3 молярных эквивалентов (предпочтительно от 0,05 до 2 молярных эквивалентов), хотя, если реакцию ведут в атмосфере водорода, меньшие количества обычно дают удовлетворительные результаты.
Способ (А) направлен на получение замещенных анилиновых соединений формулы (I) и их кислотно-аддитивных солей с высоким выходом из легко доступных исходных материалов. Более того, реакция может быть осуществлена просто и экономично, и выделение продукта может быть непосредственным. Другим преимуществом данного способа является то, что указанные соединения формулы (I) могут быть получены при умеренных температурах и давлении, тогда как известные способы требуют высоких температур и давления.
Согласно другому варианту данного изобретения предложен способ (В) получения замещенного фенилгидразина формулы (II), как определено выше, или его кислотно-аддитивной соли, который включает реакцию соединения формулы (III):
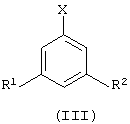
где R1 и R2 определены выше и Х означает атом галогена, с гидразином или его кислотно-аддитивной солью или с его предшественником.
При соответствующем выборе атомов галогена, которые представляют R1, R2 и Х в формуле (III) таким образом, чтобы Х являлся более реакционноспособным, чем R1 и R2, можно получить замещенные фенилгидразины формулы (II) и их соли, имеющие различные комбинации атомов галогенов. В частности предпочтительными соединениями являются такие, где каждый из R1 и R2 в формулах (I) и (II) является атомом хлора.
Соединения формулы (III) обычно известны.
В процессе предпочтительно используют гидразингидрат.
Если применяют кислотно-аддитивную соль гидразина, может необязательно присутствовать основание, такое как триалкиламин (например триэтиламин).
В частности предпочтительным соединением формулы (III) является 1,3,5-трихлорбензол.
Реакция может быть проведена в растворителе, выбранном из циклических и алифатических простых эфиров, таких как тетрагидрофуран, 1,4-диоксан или 1,2-диметоксиэтан; N-метилпирролидона; диметилсульфоксида; N,N-диметилформамида; сульфолана; N,N,N',N'-тетраметилмочевины; ароматических углеводородов, которые могут быть замещены одной или более алкильными группами или атомами хлора, таких как хлорбензол или ксилол; и пиридина. Предпочтительными растворителями являются пиридин, тетрагидрофуран, N,N,N',N'-тетраметилмочевина и 1,4-диоксан (пиридин и тетрагидрофуран особенно предпочтительны). Количество используемого растворителя обычно составляет от 1 до 10 мл (предпочтительно от 4 до 8 мл) на грамм соединения формулы (III).
Процесс обычно осуществляют в автоклаве или другом закупоренном сосуде.
Температура реакции обычно равна от 50 до 250°С, предпочтительно от 120 до 200°С. Реакцию обычно проводят с применением от 1 до 20 молярных эквивалентов (предпочтительно от 4 до 8 молярных эквивалентов) источника гидразина.
Для повышения скорости реакции необязательно может быть использован катализатор, и если он присутствует, его выбирают из фторидов щелочных и щелочноземельных металлов, таких как фторид калия. Количество используемого катализатора обычно составляет от 0,05 до 2 молярных эквивалентов (предпочтительно от 0,5 до 1 молярного эквивалента). Реакция также может быть эффективной в присутствии меди или соли меди, предпочтительно хлорида меди (I).
Способ изобретения для получения замещенных фенилгидразинов формулы (II) и их кислотно-аддитивных солей в определенных аспектах значительно лучше по сравнению с ранее известным. Способ (В), в частности, применим для получения ценного промежуточного продукта 3,5-дихлорфенилгидразина из 1,3,5-трихлорбензола, поскольку реакция идет с высоким выходом и изомерной чистотой и вместе с другими способами данного изобретения дает эффективный способ получения синтетически ценных промежуточных соединений.
Более того, если способ (В) применяют для получения 3,5-дихлорфенилгидразина из 1,3,5-трихлорбензола, реакция протекает с отличной региоселективностью.
Согласно еще одной особенности изобретения способы (А) и (В) могут быть объединены для получения замещенного анилина формулы (I) или его кислотно-аддитивной соли из соединения формулы (III).
Следующие нелимитирующие примеры иллюстрируют изобретение. Показано, что каждый продукт идентичен известным описанным образцам соединений.
Пример 1. Получение 3,5-дихлоранилина из 3,5-дихлорфенилгидразина. Никель Ренея (2 г суспензии в воде) прибавляли к раствору 3,5-дихлорфенилгидразина (1 г) в метаноле (5 мл) и нагревали при 60°С 2 ч. Охлажденную смесь отфильтровывали и упаривали, получая указанное в заголовке соединение с выходом 100%.
Пример 2. Получение 3,5-дихлоранилииа из 3,5-дихлорфенилгидразина по методике примера 1 повторяли, но с применением двух эквивалентов никеля Ренея и нагреванием при 60°С 3 ч с образованием указанного в заголовке соединения с выходом >90%.
Пример 3. Получение 3,5-дихлорфенилгидразина. Смесь 1,3,5-трихлорбензола (2,53 г), гидразингидрата (3,48 г, 5 молярных эквивалентов) и пиридина (12 мл) нагревали в автоклаве (заполненном аргоном) 6 ч при 180°С. Смесь охлаждали, избыток гидразина декантировали и органическую фазу упаривали в вакууме, получая указанное в заголовке соединение с выходом 60%. Показано, что использовано 65% исходного материала, что свидетельствует о том, что реакция идет с высокой селективностью.
Пример 4. Получение 3,5-дихлорфенилгидразина. Методику примера 3 повторяли, но с использованием 6 эквивалентов гидразингидрата, получая указанное в заголовке соединение с выходом 63%. Показано, что использовано 77% исходного материала. Это свидетельствует о том, что реакция идет с хорошей селективностью.
Пример 5. Получение 3,5-дихлорфенилгидразина. Методику примера 3 повторяли, но с использованием 6 эквивалентов гидразингидрата, получая через 10 ч при 180°С указанное в заголовке соединение с выходом 76%. Показано, что использовано 77% исходного материала, что свидетельствует о том, что реакция идет с высокой селективностью.
Пример 6. Получение 3,5-дихлорфенилгидразима. Методику примера 3 повторяли, но с использованием 6 эквивалентов гидразингидрата, получая через 6 ч при 200°С указанное в заголовке соединение с выходом 82%. Показано, что использовано 83% исходного материала, что свидетельствует о том, что реакция идет с высокой селективностью.
Изобретение относится к улучшенному способу получения соединений формулы (I)
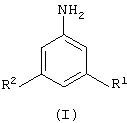
где каждый R1 и R2 независимо означает атом галогена, или его кислотно-аддитивной соли, которые могут найти применение при получении сельскохозяйственного фунгицидного соединения. Способ заключается в том, что подвергают гидрогенолизу фенилгидразин формулы (II)
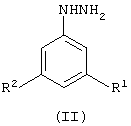
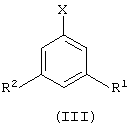
где R1 и R2 определены выше, или его кислотно-аддитивную соль в восстановительных условиях с применением никеля Ренея. Фенилгидразин формулы (II) или его кислотно-аддитивную соль получают реакцией соединения формулы (III) с гидразингидратом. 2 н. и 2 з.п. ф-лы.
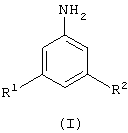
где каждый R1 и R2 независимо означает атом галогена;
или его кислотно-аддитивной соли, который включает гидрогенолиз замещенного фенилгидразина формулы (II)
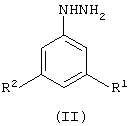
где R1 и R2 определены выше;
или его кислотно-аддитивной соли в восстановительных условиях с применением никеля Ренея.
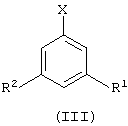
где R1 и R2 представляют хлор;
Х означает атом галогена,
с гидразингидратом.
| US 4508922A,02.04.1985 | |||
| US 3903090A ,02.09.1975 | |||
| WO9511062A1,27.04.1995 | |||
| US 4343812 A,10.08.1982 | |||
| BE 869481А, 05.02.1979 | |||
| Способ приготовления сернистого красителя защитного цвета | 1915 |
|
SU63A1 |
| HOUBEN-WEYL | |||
| Methoden der Organischen Chemie | |||
| Способ приготовления консистентных мазей | 1919 |
|
SU1990A1 |
| HOUBEN-WEYL | |||
| Methoden der Organischen Chemie | |||
| Способ приготовления консистентных мазей | 1919 |
|
SU1990A1 |
| П.САЙКС | |||
| Механизмы реакций в органической химии | |||
| - М.: Химия, 1979, с.155-157 | |||
| G.H.WOTIZ et al | |||
| Low temperature amination of aomatic polihalides | |||
| Journal of Organic chemystry | |||
| Автоматический сцепной прибор американского типа | 1925 |
|
SU1959A1 |
| Синтезы фторорганических соединений | |||
| Под ред | |||
| академика И.П.КНУНЯНЦА и профессора Г.Г.ЯКОБСОНА | |||
| - М.: Химия, 1973, с.198** | |||
| NAGARAJAN K | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Indian Journal of Chemistry | |||
| Колосниковая решетка с чередующимися неподвижными и движущимися возвратно-поступательно колосниками | 1917 |
|
SU1984A1 |
Авторы
Даты
2004-12-27—Публикация
2000-05-11—Подача