Изобретение относится к химии фосфорорганических соединений, а именно к новому способу получения N-замещенных фосфорилированных имидатов, имеющих в структуре цианэтильную группу, общей формулы
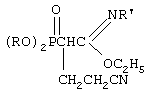
где R=С3-С4 - алкил или изоалкил;
R’=С(O)СН3, С(O)С6Н5, Si(CH3)3;
которые являются новыми по структуре фосфорорганическими соединениями и могут служить исходными в получении биологически активных соединений для нужд медицины и сельского хозяйства. Осуществление предложенного способа оказалось возможным благодаря наличию в исходных N-замещенных этил-(2-диалкоксифосфорил) этанимидатах высоких С-Н-кислотных свойств активированной метиленовой группы.
Известно присоединение нитрила диалкоксифосфорилуксусной кислоты к эфирам непредельных карбоновых кислот с получением бифункциональных соединений сложной структуры, содержащих нитрильную и сложноэфирную группировки. Реакции проводились в присутствии алкоголятов щелочных металлов в безводных спиртах при нагревании реакционных смесей до 4 часов на кипящей водяной бане (А.Н. Пудовик, Н.М. Лебедева. ЖОХ, 1955, т.25, с.1920-1924. А.Н. Пудовик, Н.М. Лебедева. ЖОХ, 1955, т.25, с.2235-2240).
Недостатками данного метода являются невысокие выходы (менее 17-71%) продуктов присоединения. А также в результате получают соединения иной структуры, чем в предлагаемом изобретении.
Известен метод присоединения эфира диалкоксифосфорилуксусной кислоты к акрилонитрилу в присутствии в качестве катализатора этилата натрия с получением С-цианэтилированных эфиров диалкоксифосфорилуксусной кислоты. Процессы проводились в растворе этилового спирта, общий выход нитрилов составил 50% от теоретического (Присоединение фосфонуксусного эфира и его гомологов к непредельным электрофильным реагентам. А.Н. Пудовик, Н.М. Лебедева. ЖОХ, т.22, № 12, 1952, с.228-2132). Недостатком данного метода является невысокий выход нитрилов.
Вышеописанным методом получают соединения совершенно иной структуры по сравнению с предлагаемым изобретением.
Задачей предлагаемого изобретения является разработка нового технологичного малостадийного метода синтеза N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов.
Техническим результатом является расширение арсенала химических соединений, получение новых N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов с высоким выходом (более 75%) перспективных для получения биологически активных соединений для нужд медицины и сельского хозяйства.
Указанный технический результат достигается разработкой нового способа получения N-замещенных этил-(2-диалкокси-фосфорил-4-циано)бутанимидатов формулы
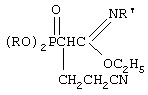
где R=С3-С4-алкил или изоалкил;
R’=С(O)СН3, С(O)С6Н5, Si(СН3)3;
заключающийся во взаимодействии N-замещенных этил-(2-диалкоксифосфорил) этанимидатов с акрилонитрилом в присутствии катализатора этилата натрия в среде диоксана при мольном соотношении N-замещенный этил-(2-диалкоксифосфорил)этанимидат : акрилонитрил : этилат натрия (1:1,05-1,15:0.1-0,15) соответственно и температуре 40-60°С.
Химическая схема предложенного способа получения N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов:
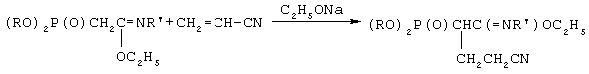
где R=C3-C4 – алкил или изоалкил;
R’=C(O)CH3,C(O)C6H5, Si(CH3)3;
Нуклеофильное присоединение N-замещенных алкил(диалкоксифосфорил) этанимидатов к акрилонитрилу происходит по β-углеродному атому. На основании изучения литературных данных механизм взаимодействия N-замещенного этил(диалкоксифосфорил)этанимидата с акрилонитрилом можно представить следующим образом:
Вначале реакции образуется амбидентный анион из этанимидата под действием алкокси-аниона
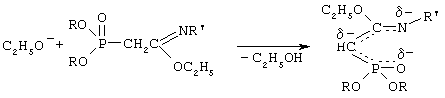
Затем образовавшийся анион нуклеофильно атакует молекулу акрилонитрила с образованием мезомерного аниона.
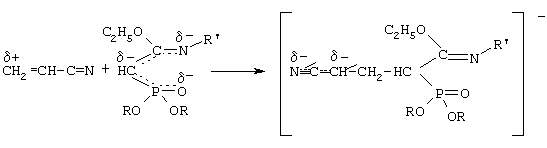
Этот мезомерный анион является сильным основанием и способен отрывать протон от молекулы этилового спирта.
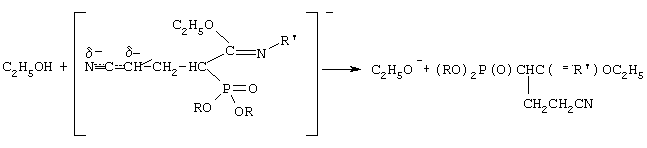
Не исключено, что в качестве донора протона выступает метиленовая группа N-замещенного алкил(диалкоксифосфорил)этанимидата.
При выборе растворителя для проведения реакций присоединения к акрилонитрилу нами были учтены следующие требования к растворителю: создание гомогенной реакционной массы, поддержание необходимого температурного режима и инертность по отношению к реагирующим компонентам. Всем этим требованиям отвечает диоксан, в нем растворяется этилат натрия и другие реагенты, есть возможность повышения температуры до 60°С и более, а также он абсолютно инертен по отношению к реагентам. Последнее требование исключает возможность использования этилового спирта, так как он вступает во взаимодействие с акрилонитрилом, понижая выход целевого соединения.
В начальный момент взаимодействия нет необходимости в дополнительном нагреве, так как реакция начинается самопроизвольно даже при комнатной температуре. Затем для повышения степени превращения исходных реагентов и ускорения реакции проводили дополнительное нагревание реакционной массы до 40-60°С.
Использование в данном процессе 5-15% избытка акрилонитрила по сравнению со стехиометрическим количеством необходимо из-за взаимодействия его со следами этилового спирта, вносимого в реакционную массу с катализатором. Предложенный метод получения N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов характеризуется простотой эксперимента, осуществляется в достаточно мягких условиях и обеспечивает высокий (более 75%) выход целевых соединений.
Способ осуществляется следующим образом.
Для синтеза N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов к смеси, состоящей из N-замещенного этил-(2-диалкоксифосфорил)этанимидата и акрилонитрила, взятых в мольных количествах 1:1,05-1,15 соответственно и растворенных в осушенном диоксане, при комнатной температуре и перемешивании прибавляли небольшими порциями катализатор - этилат натрия. Количество катализатора составляло 10-15 мол.% от количества N-замещенного имидата. Процесс протекает с небольшим разогревом реакционной массы, и для завершения его рекомендуется нагревание реакционной смеси при 50-60°С в течение 2 часов. После чего реакционную смесь охлаждали до комнатной температуры, отфильтровывали катализатор, а из фильтрата в вакууме водоструйного насоса отгоняли растворитель. Остатки растворителя удаляли путем вакуумирования (Рост 1-2 гПа) в течение 1 часа при 50-60°С. Выход N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов составляет более 75%. Для получения химически чистых соединений осуществляли дополнительную очистку полученных соединений методом колоночной адсорбционной хроматографии на силикагеле марки μLC 5/40. Идентификация синтезированных соединений проводилась по данным элементного анализа, молекулярной рефракции, определения молекулярной массы, ИК-спектроскопии. Для лучшего понимания сущности предложенного технического решения приводятся конкретные примеры синтезов.
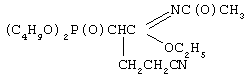
Пример 1. Этил-N-ацетил-(2-диизопропоксифосфорил-4-циано)бутанимидат,
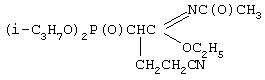
К смеси 4,0 г (0,0136 моль) этил-N-ацетил-(2-диизопропокси-фосфорил)этанимидата, 0,8 г (0,0150 моль, 10% изб. мольн.) акрилонитрила и 16 мл сухого диоксана при температуре 20-25°С и интенсивном перемешивании небольшими порциями прибавляли катализатор - этилат натрия - в количестве 0,14 г (0,00204 моль, 15% от количества исходного имидата). Затем реакционную массу нагревали до 60°С и перемешивали в течение 2 часов, после чего охлаждали, отфильтровывали катализатор, а из фильтрата в вакууме водоструйного насоса отгоняли растворитель. Остаток вакуумировали в течение 1 часа при температуре 50-60°С и 2 гПа. Получили 4,15 г этил-N-ацетил-(2-диизопропоксифосфорил-4-циано)бутанимидата. Выход 88%. Для получения химически чистого вещества его очищали методом колоночной адсорбционной хроматографии на силикагеле марки μLC 5/40, элюент диэтиловый эфир : ацетон (1:1 об.); Rf 0,68. n
ИК-спектр, ν, см-1: 775, 980-1020 (РОС); 1124 (СОС); 1248 (Р=O); 1660 (C=N); 1720 (NC=O); 2240 (C≡N).
Пример 2. Этил-N-триметилсилил-(2-дибутоксифосфорил-4-циано)бутанимидат,
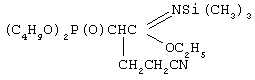
К смеси 5,0 г (0,0142 моль) этил-N-триметилсилил-(2-дибутоксифосфорил)этанимидата, 0,85 г (0,0156 моль, 10% изб. мольн.) акрилонитрила и 18 мл сухого диоксана при температуре 20-25°С и интенсивном перемешивании небольшими порциями прибавляли катализатор - этилат натрия - в количестве 0,145 г (0,00213 моль, 15% от количества исходного имидата). Затем реакционную массу нагревали до 60°С и перемешивали в течение 2 часов, после чего охлаждали, отфильтровывали катализатор, а из фильтрата в вакууме водоструйного насоса отгоняли растворитель. Остаток вакуумировали в течение 1 часа при температуре 50-60°С и 2 гПа. Получили 4,3 г этил-N-триметилсилил-(2-дибутоксифосфорил-4-циано)бутанимидата. Выход 75%. Для получения химически чистого вещества его очищали методом колоночной адсорбционной хроматографии на силикагеле марки μLC 5/40, элюент диэтиловый эфир : ацетон (1:1 об.); Rf 0,73. n
ПК-спектр, ν, см-1: 760 (Si-N); 775, 980-1010 (РОС); 1120 (СОС); 1252 (Р=O); 1666 (C=N); 2248 (C≡N).
Пример 3. Этил-N-ацетил-(2-дибутоксифосфорил-4-циано)бутанимидат,
К смеси 4,5 г (0.0140 моль) этил-N-ацетил-(2-дибутокси-фосфорил)этанимидата, 0,9 г (0.0161 моль, 15% изб. мольн.) акрилонитрила и 16 мл сухого диоксана при температуре 20-25°С и интенсивном перемешивании небольшими порциями прибавляли катализатор - этилат натрия - в количестве 0,095 г (0,0014 моль, 10% от количества исходного имидата). Затем реакционную массу нагревали до 40°С и перемешивали в течение 2 часов, после чего охлаждали, отфильтровывали катализатор, а из фильтрата в вакууме водоструйного насоса отгоняли растворитель. Остаток вакуумировали в течение 1 часа при температуре 50-60°С и 2 гПа. Получили 4,1 г этил-N-ацетил-(2-дибутоксифосфорил-4-циано)бутанимидата. Выход 78%. Для получения химически чистого вещества его очищали методом колоночной адсорбционной хроматографии на силикагеле марки μLC 5/40, элюент диэтиловый эфир : ацетон (1:1 об.); Rf 0,70. n
ИК-спектр, ν, см-1: 775, 990-1104 (РОС); 1116 (СОС); 1248 (Р=0); 1656 (C=N); 1720 (NC=0); 2252 (C≡N).
Пример 4. Этил-N-бензоил-(2-диизопропоксифосфорил-4-циано)бутанимидат,
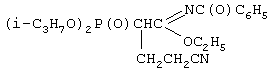
К смеси 6,0 г (0,0169 моль) этил-N-бензоил-(2-диизопро-поксифосфорил)этанимидата, 0,96 г (0,0177 моль, 5% изб. мольн.) акрилонитрила и 20 мл сухого диоксана при температуре 20-25°С и интенсивном перемешивании небольшими порциями прибавляли катализатор - этилат натрия - в количестве 0,116 г (0,0017 моль, 10% от количества исходного имидата). Затем реакционную массу нагревали до 50°С и перемешивали в течение 2 часов, после чего охлаждали, отфильтровывали катализатор, а из фильтрата в вакууме водоструйного насоса отгоняли растворитель. Остаток вакуумировали в течение 1 часа при температуре 50-60°С и 2 гПа. Получили 5,5 г этил-N-бензоил-(2-диизопропоксифосфорил-4-циано)бутанимидата. Выход 80%. Для получения химически чистого вещества его очищали методом колоночной адсорбционной хроматографии на силикагеле марки μLC 5/40, элюент диэтиловый эфир : ацетон (1:1 об.); Rf,63. n
ИК-спектр, ν, см-1: 775, 980-1104 (РОС); 1116 (СОС); 1260 (Р=O); 1595 (С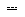 Car); 1676 (C=N); 1736 (NC=O); 2250 (C≡N).
Car); 1676 (C=N); 1736 (NC=O); 2250 (C≡N).
Предложенный метод позволяет осуществлять синтез N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов из соответствующих этанимидатов, что оказалось возможным вследствие высоких С-Н-кислотных свойств активированной метиленовой группы последних.
Метод заключается во взаимодействии N-замещенных этил-(2-диалкоксифосфорил)этанимидатов с акрилонитрилом в присутствии этилата натрия в качестве катализатора с образованием N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов. Достоинством разработанного метода является простота технологии и универсальность, так как он позволяет из соответствующих исходных этанимидатов получать С-цианэтилированные их гомологи.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ АЛКИЛ-(2-ДИАЛКОКСИФОСФОРИЛ)АЛКИЛИМИДАТОВ | 2001 |
|
RU2203284C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ (2-ДИАЛКОКСИФОСФОРИЛ-4-ЦИАНО)БУТАНАМИДИНОВ | 2009 |
|
RU2385870C1 |
| СПОСОБ ПОЛУЧЕНИЯ С-ФОСФОРИЛИРОВАННЫХ АЛКИЛАМИДИНОВ | 2007 |
|
RU2334752C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ (2-ТРИМЕТИЛСИЛИЛ-2-ДИАЛКОКСИФОСФОРИЛ)АЦЕТАМИДИНОВ | 2010 |
|
RU2427583C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ (2-БЕНЗОЛСУЛЬФОНИЛ-2-ДИАЛКОКСИФОСФОРИЛ)АЦЕТАМИДИНОВ | 2013 |
|
RU2529199C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ БИС[ДИАЛКОКСИФОСФОРИЛ]АЦЕТАМИДИНОВ | 2009 |
|
RU2415861C1 |
| СПОСОБ ПОЛУЧЕНИЯ N, N-ДИАЛКИЛ, N'-АЦИЛ-(АЦИЛДИАЛКОКСИФОСФОРИЛ)ЭТАНАМИДИНОВ | 2008 |
|
RU2374258C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-АЦИЛИРОВАННЫХ АЛКИЛ-(2-АЦЕТИЛ-2-ДИАЛКОКСИФОСФОРИЛ)ЭТАНИМИДАТОВ | 2001 |
|
RU2203283C1 |
| С-ФОСФОРИЛИРОВАННЫЕ АЦЕТАМИДИНЫ, СОДЕРЖАЩИЕ РЕАКЦИОННОСПОСОБНУЮ СН-КИСЛОТНУЮ МЕТИЛЕНОВУЮ ГРУППУ, В КАЧЕСТВЕ ИСХОДНЫХ СОЕДИНЕНИЙ ДЛЯ ПОЛУЧЕНИЯ БРОМПРОИЗВОДНЫХ С-ФОСФОРИЛИРОВАННЫХ АЦЕТАМИДИНОВ | 2007 |
|
RU2334753C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-(ФУРИЛ-2)-1,3-ДИОКСАНОВ | 1995 |
|
RU2086550C1 |
Изобретение относится к химии фосфорорганических соединений, а именно к новому способу получения N-замещенных фосфорилированных имидатов, имеющих в структуре цианэтильную группу. Описывается способ получения N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов
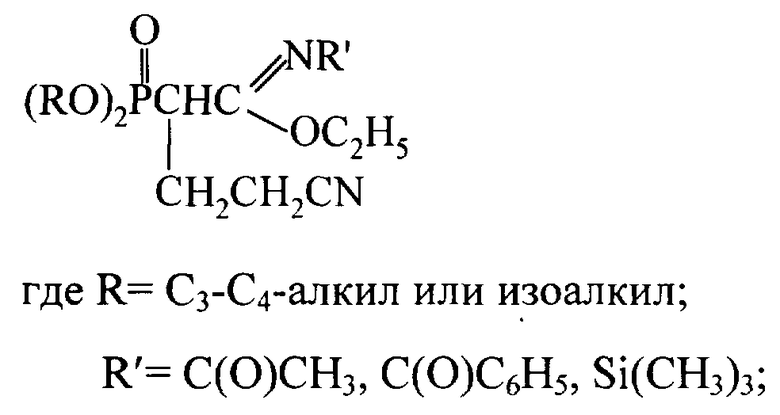
заключающийся во взаимодействии N-замещенных этил-(2-диалкоксифосфорил)этанимидатов с акрилонитрилом в присутствии катализатора этилата натрия в среде диоксана при мольном соотношении N-замещенный этил-(2-диалкоксифосфорил)этанимидат : акрилонитрил : этилат натрия (1:1,05-1,15:0,1-0,15) соответственно и температуре 40-60°С. Технический результат – получение новых химических соединений перспективных для получения биологически активных соединений для нужд медицины и сельского хозяйства.
Способ получения N-замещенных этил-(2-диалкоксифосфорил-4-циано)бутанимидатов
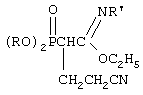
где R-C3-C4-алкил или изоалкил;
R’-C(O)CH3, C(O)C6H5, Si(CH3)3,
заключающийся во взаимодействии N-замещенных этил-(2-диалкоксифосфорил)этанимидатов с акрилонитрилом в присутствии катализатора-этилата натрия в среде диоксана при мольном соотношении N-замещенный этил-(2-диалкоксифосфорил)этанимидат:акрилонитрил:этилат натрия (1:1,05-1,15:0,1-0,15) соответственно и температуре 40-60°С.
| ПУДОВИК А.Н | |||
| и др | |||
| ЖОХ | |||
| Двухступенное или многоступенное гидравлическое инжекционное устройство для сжатия воздуха и других газов, с применением насосов для постоянного поддержания циркуляции в нем жидкости | 1925 |
|
SU1955A1 |
| ПУДОВИК А.Н | |||
| и др | |||
| ЖОХ | |||
| Приспособление для отвешивания жидкости без предварительного определения веса тары | 1925 |
|
SU1952A1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ АЛКИЛ-(2-ДИАЛКОКСИФОСФОРИЛ)АЛКИЛИМИДАТОВ | 2001 |
|
RU2203284C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-АЦИЛИРОВАННЫХ АЛКИЛ-(2-АЦЕТИЛ-2-ДИАЛКОКСИФОСФОРИЛ)ЭТАНИМИДАТОВ | 2001 |
|
RU2203283C1 |
Авторы
Даты
2004-09-20—Публикация
2003-04-29—Подача