Настоящее изобретение относится к кислотным аддитивным солям 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина (предпочтительно гидрохлориду или малеату), которые обладают превосходной пероральной абсорбцией, метаболизмом в активное соединение и активностью при ингибировании агрегации тромбоцитов и пригодны в качестве терапевтических или профилактических агентов при заболеваниях, обусловленных тромбозом или эмболией.
В ЕР-542411 (публикация японской заявки на патент № Hei 6-411239) описано, что 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридин и его производные, которые являются антагонистами рецепторов аденозиндифосфата (далее здесь обозначаемого АДФ), обладают превосходной активностью при ингибировании агрегации тромбоцитов и пригодны в качестве антитромботических или противоэмболических агентов.
В течение многих лет заявители активно исследовали фармакологическую активность различных производных гидропиридина для того, чтобы обнаружить соединения, имеющие превосходную активность при ингибировании агрегации тромбоцитов. Заявители обнаружили, что кислотные аддитивные соли 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина (предпочтительно гидрохлорида или малеата) обладают превосходной пероральной абсорбцией, метаболизмом в активное соединение, активностью при ингибировании агрегации тромбоцитов, низкой токсичностью и превосходной стабильностью при хранении и использовании и пригодны в качестве лекарственных средств (предпочтительно пригодны в качестве терапевтических или профилактических агентов, предпочтительно терапевтических агентов) при заболеваниях, вызываемых образованием тромбов или вызываемых эмболией (предпочтительно тромбоз или эмболия).
Настоящее изобретение обеспечивает кислотные аддитивные соли 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина (предпочтительно гидрохлорид или малеат), которые обладают превосходной активностью при ингибировании агрегации тромбоцитов; способы их получения и лекарственные средства на их основе, которые являются пригодными терапевтическими или профилактическими агентами (предпочтительно терапевтическими) при заболеваниях, вызванных тромбозом или вызванных эмболией, и предпочтительно пригодны в качестве терапевтических или профилактических агентов (предпочтительно терапевтических агентов) при тромбозе или эмболии.
Описание изобретения
Настоящее изобретение относится к кислотным аддитивным солям 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина (гидрохлориду или малеату) и относится к лекарственным средствам, содержащим кислотные аддитивные соли 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина (гидрохлорид или малеат) в качестве активного ингредиента.
Кислотный фрагмент кислотных аддитивных солей 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина является, например, неорганической кислотой, такой как серная кислота, соляная кислота, азотная кислота, фосфорная кислота, или органической кислотой, такой как трифторуксусная кислота, малеиновая кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и предпочтительно соляная кислота или малеиновая кислота.
2-Ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина гидрохлорид по настоящему изобретению имеет следующую формулу:
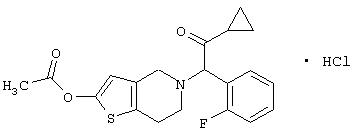
2-Ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина малеат имеет следующую формулу:
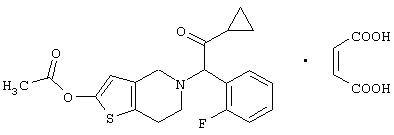
Кислотные аддитивные соли 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина имеют в молекуле асимметрический атом углерода и в каждом соединении могут присутствовать два изомера, имеющие R и S конфигурацию. Настоящее изобретение охватывает индивидуальные изомеры и смеси этих изомеров в произвольных соотношениях. Оптически активный изомер кислотных аддитивных солей 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина по настоящему изобретению может быть получен при использовании оптически активного исходного материала или выделен из рацемической смеси синтетически полученных кислотных аддитивных солей 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина обычным оптическим разделением.
В некоторых случаях, когда кислотным аддитивным солям 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина позволяют контакт с воздухом или перекристаллизовываться, они могут абсорбировать воду или могут впитывать воду с образованием гидрата. Настоящее изобретение включает эти гидраты.
Кислотные аддитивные соли 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина получают в присутствии или в отсутствие инертного растворителя (предпочтительно в инертном растворителе) добавлением 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина, который синтезируют по способу, описанному в ЕР 542411, к кислоте (предпочтительно к соляной кислоте, хлороводороду (газ) или малеиновой кислоте, более предпочтительно к концентрированной соляной кислоте или малеиновой кислоте, наиболее предпочтительно к концентрированной соляной кислоте) или в присутствии, или в отсутствие инертного растворителя (предпочтительно в инертном растворителе) прикапыванием или добавлением кислоты (предпочтительно соляной кислоты, хлороводорода (газ) или малеиновой кислоты, более предпочтительно концентрированной соляной кислоты или малеиновой кислоты, наиболее предпочтительно концентрированной соляной кислоты) один или несколько раз к 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридину. В этом способе, если необходимо, могут добавляться затравочные кристаллы указанной соли.
Растворитель, используемый в указанной выше реакции, не имеет особых ограничений, и подбирается таким образом, чтобы он не оказывал неблагоприятного воздействия на реакцию и мог до некоторой степени растворять исходный материал. Примеры таких растворителей включают алифатические углеводороды, такие как гексан, циклогексан, гептан, лигроин или петролейный эфир; ароматические углеводороды, такие как бензол, толуол или ксилол; галогенированные углеводороды, такие как дихлорметан, хлороформ, тетрахлорметан, 1,2-дихлорэтан, хлорбензол или дихлорбензол; производные простых эфиров, такие как диэтиловый эфир, диизопропиловый эфир, тетерагидрофуран, диоксан, диметоксиэтан или диэтиленгликольдиметиловый эфир; кетонные производные, такие как ацетон, метилэтилкетон или диэтилкетон; сложноэфирные производные, такие как этилацетат, пропилацетат или бутилацетат; производные карбоновых кислот, такие как уксусная кислота или пропионовая кислота, или нитрильные производные, такие как ацетонитрил или пропионитрил. Для получения гидрохлорида предпочтительными растворителями являются производные простых эфиров, производные кетонов, производные сложных эфиров, производные карбоновых кислот или нитрильные производные; более предпочтительными растворителями являются тетрагидрофуран, диоксан, ацетон, метилэтилкетон, этилацетат, уксусная кислота или ацетонитрил; еще более предпочтительными растворителями являются тетрагидрофуран, диоксан, уксусная кислота или ацетон. Наиболее предпочтителен ацетон. С другой стороны, для получения малеата предпочтительные растворители являются производными простых эфиров, производными кетонов, производными сложных эфиров или производными нитрилов; более предпочтительными растворителями являются тетрагидрофуран, диоксан, ацетон, метилэтилкетон, этилацетат или ацетонитрил; еще более предпочтительными растворителями являются тетрагидрофуран, диоксан или ацетон. Наиболее предпочтительным является ацетон.
Температура реакции изменяется в зависимости от реагента, растворителя и т.п. и обычно изменяется от -20 до 100°С, предпочтительно от 0 до 70°С. В случае гидрохлорида температура реакции предпочтительно составляет от 30 до 60°С и более предпочтительно от 40 до 55°С.
Время реакции изменяется в зависимости от реагента, растворителя, температуры реакции и т.п. и обычно составляет от 5 минут до 10 часов, предпочтительно от 10 минут до 5 часов.
В случае получения малеата реакцию предпочтительно осуществляют путем добавления 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина к раствору малеиновой кислоты в ацетоне при температуре в интервале от 0 до 70°С с последующим выдерживанием при указанной температуре в течение от 1 часа до 3 часов.
В случае получения гидрохлорида реакцию предпочтительно осуществляют путем добавления или прикапывания требуемого количества концентрированной соляной кислоты (обычно эквимолярной по отношению к тиенопиридиновому производному) к раствору 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина в ацетоне при температуре в интервале от 0 до 70°С (предпочтительно от 35 до 60°С) с последующим выдерживанием при указанной температуре в течение периода времени от 30 минут до 3 часов.
Более предпочтительно реакцию осуществляют путем добавления прикапыванием половины требуемого количества концентрированной соляной кислоты (обычно эквимолярной по отношению к тиенопиридиновому производному) к раствору тиенопиридинового производного в ацетоне при температуре в интервале от 35 до 60°С (предпочтительно от 40 до 55°С) в течение периода времени от 2 минут до 10 минут с добавлением при необходимости затравочных кристаллов указанной соли с последующим выдерживанием при указанной температуре в течение периода времени от 30 минут до 2 часов и затем дополнительным добавлением прикапыванием оставшегося требуемого количества концентрированной соляной кислоты к реакционной смеси в течение периода времени от 30 минут до 2 часов с последующим выдерживанием при указанной температуре в течение от 1 часа до 3 часов.
После реакции кислотные аддитивные соли 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина могут быть выделены из реакционной смеси обычными способами. Например, после реакции полученные кристаллы отделяют фильтрацией для получения заданного продукта или упаривают растворитель реакционной смеси с получением заданного продукта. Если необходимо, продукт может быть очищен перекристаллизацией, повторным осаждением или хроматографией.
Кислотные аддитивные соли 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина по настоящему изобретению проявляют превосходную пероральную абсорбцию, метаболизм в активное соединение и активность при ингибировании агрегации тромбоцитов, низкую токсичность и, кроме того, стабильны при хранении и использовании, таким образом, они пригодны в качестве профилактических или терапевтических средств (предпочтительно терапевтических средств) при заболеваниях, вызванных тромбообразованием или эмболией, более предпочтительны в качестве профилактических или терапевтических средств (предпочтительно терапевтических средств) при тромбозе или эмболии. Лекарственные препараты, описанные выше, предпочтительно используют для теплокровных животных, предпочтительно для людей.
В случае, когда кислотные аддитивные соли 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина по настоящему изобретению используют в качестве терапевтических или профилактических средств для описанных выше болезней, они могут назначаться как сами по себе, так и в смеси с фармацевтически пригодными эксципиентами, разбавителями и т.п., в различных формах дозировки, таких как таблетки, капсулы, гранулы, порошки, сиропы и т.п. для перорального назначения, и инъекции, суппозитории и т.п. для парентерального назначения.
Каждый из вышеописанных составов может быть получен хорошо известными способами при использовании добавок для составов, таких как эксципиенты, смазочные материалы, связующие, разрыхлители, эмульгаторы, стабилизаторы, улучшители вкуса (корреганты) и разбавители.
Примеры эксципиентов включают органические эксципиенты, например производные сахаров, такие как лактоза, сахароза, глюкоза, маннит или сорбит; производные крахмала, такие как кукурузный крахмал, картофельный крахмал, α-крахмал или декстрин; производные целлюлозы, такие как, кристаллическая целлюлоза; гуммиарабик; декстран; пуллюлан, и неорганические эксципиенты, например силикатные производные, такие как ангидрид кремниевой кислоты, синтетический алюмосиликат, силикат кальция или алюминат метасиликат магния; фосфорные производные, такие как гидрофосфат кальция; карбонатные производные, такие как карбонат кальция; сульфатные производные, такие как сульфат кальция и т.п.
Примеры смазочных материалов включают стеариновую кислоту; металлопроизводные стеаратов, такие как стеарат кальция или стеарат магния; тальк; воски, такие как пчелиный воск или спермацет; борную кислоту; адипиновую кислоту, сульфатные производные, такие как сульфат натрия; гликоль; фумаровую кислоту; бензоат натрия; DL-лейцин; производные лаурилсульфата, такие как лаурилсульфат натрия или лаурилсульфат магния; производные кремниевой кислоты, такие как ангидрид кремниевой кислоты или гидрат кремниевой кислоты, и описанные выше в эксципиентах производные крахмала.
Примеры связующих включают гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, поливинилпирролидон, macrogol (торговая марка) или эксципиенты, как описано выше в эксципиентах.
Примеры разрыхлителей включают производные целлюлозы, такие как гидроксипропилцеллюлоза, с низкой степенью замещения, карбоксиметилцеллюлоза, кальцийкарбоксиметилцеллюлоза или сшитая натрийкарбкосиметилцеллюлоза; химически модифицированный крахмал или производные целлюлозы, такие как карбоксиметилкрахмал или натрийкарбоксиметилкрахмал; сшитый поливинилпирролидин и производные крахмала, как описано выше.
Примеры эмульгаторов включают коллоидные глины, такие как бентонит или веегам; гидроксиды металлов, такие как гидроксид магния или гидроксид алюминия; анионные поверхностно-активные вещества, такие как лаурилсульфат натрия или стеарат кальция; катионные поверхностно-активные вещества, такие как бензалконийхлорид; неионные поверхностно-активные вещества, такие как полиоксиэтилен алкил простые эфиры, сложные эфиры полиоксиэтиленсорбита и жирных кислот или сложные эфиры сахарозы и жирных кислот.
Примеры стабилизаторов включают производные сложных эфиров пара-гидроксибензойной кислоты, такие как метилпарабен или пропилпарабен; производные спиртов, такие как хлорбутанол, бензиловый спирт или фенэтиловый спирт; бензалконийхлорид; производные фенола, такие как фенол или крезол; тимеросол; дегидроуксусная кислота или сорбиновая кислота.
Примеры корригентов включают подсластители, подкисляющие агенты, ароматизирующие вещества и т.п., которые обычно используются.
Конкретная доза соединения по настоящему изобретению изменяется в зависимости от серьезности симптомов пациента, возраста и т.п. Для перорального назначения количество активного ингредиента в единичной дозировке может быть от 0,1 мг (предпочтительно 1 мг) до 1000 мг (предпочтительно 500 мг). Единичная дозировка для внутривенного назначения может быть в диапазоне от 0,01 мг (предпочтительно 0,1 мг) до 500 мг (предпочтительно 250 мг) соединения по настоящему изобретению.
Единичная дозировка может назначаться взрослому человеку от 1 до 7 раз в день в течение от 1 до 7 дней в зависимости от серьезности симптомов пациента.
Следующие примеры, ссылочные примеры, примеры испытаний и примеры составов, предназначены для дополнительной иллюстрации настоящего изобретения и не предназначены для ограничений области действия изобретения.
Пример 1
2-Ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина гидрохлорид (кристалл А)
К раствору 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина (10 г), полученному согласно ссылочному примеру 1, в ацетоне (150 мл) добавляют прикапыванием концентрированную соляную кислоту (36%, 2,71 г) при перемешивании при комнатной температуре (25°С). Небольшое количество затравочных кристаллов заданного продукта (кристалл А получен по другому способу) добавляют к раствору и затем смесь перемешивают в течение 90 минут при той же температуре. Полученные кристаллы отделяют фильтрацией, кристаллы промывают небольшим количеством ацетона и затем сушат при 50°С при пониженном давлении в течение 4 часов с получением соединения, указанного в заголовке, в виде белых кристаллов (8,1 г, выход 74%) (кристалл А), т.пл. 133-136°С.
1H ЯМР (CDCl3) δ м.д.: 0.92-0.99 (1H, м), 1.05-1.16 (2H, м), 1.23-1.34 (1H, м), 1.84-1.95 (1H, м), 2.26 (3H, с), 3.07-3.23 (2H, м), 3.57-4.39 (4H, м), 6.04 (1H, с), 6.45 (1H, уш.с.), 7.37 - 7.57 (3H, м), 7.66-7.75 (1H, м).
Масс-спектр (CI, m/z): 374 (M++1).
ИК (KBr), νmax, cм-1: 1762, 1720.
Пример 2
2-Ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина малеат
К раствору малеиновой кислоты (4,43 г) в ацетоне (60 мл) добавляют 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридин (15,0 г), полученный согласно ссылочному примеру 1, затем смесь перемешивают при комнатной температуре (25оС) в течение 2 часов. Полученные кристаллы отделяют фильтрацией, промывают небольшим количеством ацетона и затем сушат при 50°С при пониженном давлении в течение 4 часов с получением соединения, указанного в заголовке, в виде белых кристаллов (17,1 г, выход 92%), т.пл. 171-172°C.
1H ЯМР (CD3OD) δ м.д.: 0,89–0,97 (1H, м), 1,02–1,09 (2H, м), 1,14–1,23 (1H, м), 1,94–2,03 (1H, м), 2,25 (3H, с), 3,00–3,09 (2H, м), 3,33–3,50 (2H, м), 3,88 (1H, д, J=14,9 Гц), 4.05 (1H, д, J=14,9 Гц), 5,70 (1H, с), 6,25 (2H, с), 6,40 (1H, с), 7,30-7,42 (2H, м), 7,45-7,52 (1H, м), 7,56-7,66 (1H, м).
Масс-спектр (CI, m/z): 374 (M++1).
ИК (KBr), νmax, cм-1: 1782, 1713.
Пример 3
2-Ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина гидрохлорид (кристалл В1)
К раствору 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина (10 г), полученному согласно ссылочному примеру 1, в ацетоне (100 мл) добавляют прикапыванием концентрированную соляную кислоту (36%, 2,71 г) при перемешивании в течение 1 минуты при 40°С. Реакционную смесь перемешивают в течение 60 минут при той же температуре (кристаллы начинают осаждаться после 10 минут после добавления концентрированной соляной кислоты). Полученные кристаллы отделяют фильтрацией, промывают ацетоном (20 мл) и затем сушат при 60°С при пониженном давлении в течение 2 часов с получением соединения, указанного в заголовке, в виде белых кристаллов (9,72 г, выход 89%) (кристалл В1), которые более стабильны при хранении, чем кристалл А, т.пл. 166-174°С.
Масс-спектр (CI, m/z): 374 (M++1).
ИК (KBr), νmax, cм-1: 1758, 1690.
Пример 4
2-Ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина гидрохлорид (кристалл В2)
К раствору 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина (50 г), полученному согласно ссылочному примеру 1, в ацетоне (750 мл) добавляют прикапыванием концентрированную соляную кислоту (36%, 6,78 г) при перемешивании в течение 5 минут при 40°С. Кристаллы В1 (0,1 г), полученные в примере 3, добавляют к реакционной смеси в качестве затравочных кристаллов и полученную смесь перемешивают при той же температуре в течение 60 минут. К полученной смеси дополнительно добавляют прикапыванием концентрированную соляную кислоту (36%, 6,10 г) в течение 60 минут и смесь перемешивают при той же температуре в течение 120 минут. Полученные кристаллы отделяют фильтрацией, промывают ацетоном (100 мл) и затем сушат при 70°С при пониженном давлении в течение 3 часов с получением соединения, указанного в заголовке, в виде белых кристаллов (47,8 г, выход 92%) (кристалл В2), которые характеризовались большей стабильностью при хранении, чем кристалл В1, полученный в примере 3, т.пл. 165-178°С.
Масс-спектр (CI, m/z): 374 (M++1).
ИК (KBr), νmax, cм-1: 1758, 1690.
Пример 5
2-Ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина малеат
К раствору малеиновой кислоты (932 г) в ацетоне (15 л), нагретому до 40°С, добавляют 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридин (3000 г), полученному согласно ссылочному примеру 1. Смесь перемешивают при комнатной температуре в течение 2 часов. Полученные кристаллы отделяют фильтрацией и промывают ацетоном (4 л) и затем сушат при 60°С при пониженном давлении в течение 8 часов с получением соединения, указанного в заголовке, в виде белых кристаллов (3538 г, выход 90%), т.пл. 172-173°C.
Масс-спектр (CI, m/z): 374 (M++1).
ИК (KBr), νmax, cм-1: 1782, 1713.
Пример 6
2-Ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина гидрохлорид (кристалл В2)
К раствору 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина (50 г), полученному согласно ссылочному примеру 1, в ацетоне (750 мл) добавляют прикапыванием концентрированную соляную кислоту (36%, 6,78 г) при перемешивании в течение 5 минут при 55°С. Кристаллы В1 (0,1 г), полученные в примере 3, добавляют к реакционной смеси в качестве затравочных кристаллов и полученную смесь перемешивают при той же температуре в течение 60 минут. К полученной смеси дополнительно добавляют прикапыванием концентрированную соляную кислоту (36%, 6,08 г) в течение 60 минут и смесь перемешивают при той же температуре в течение 120 минут. Полученные кристаллы отделяют фильтрацией, промывают ацетоном (100 мл) и затем сушат при 70°С при пониженном давлении в течение 3 часов с получением соединения, указанного в заголовке, в виде белых кристаллов (46,2 г, выход 89%) (кристалл В2), т.пл. 164-178°С.
Масс-спектр (CI, m/z): 374 (M++1).
ИК (KBr), νmax, cм-1: 1758, 1690.
Ссылочный пример
2-Ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридин
(а) Циклопропил-2-фторбензилкетон
К суспензии порошкообразного магния (7,2 г) в безводном диэтиловом простом эфире добавляют раствор 2-фторбензилбромида (30 мл) в диэтиловом эфире (30 мл), затем смесь перемешивают при комнатной температуре в течение 1 часа. Реакционную смесь добавляют прикапыванием к раствору циклопропилцианида (18,2 мл) в диэтиловом эфире (120 мл) в течение 100 минут. После перемешивания в течение 30 минут при комнатной температуре, перемешиваемую смесь нагревают при кипячении с обратным холодильником в течение 1 часа. После реакции реакционную смесь разделяют между этилацетатом и насыщенным раствором хлорида аммония. Слой этилацетата последовательно промывают водой, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия, сушат над безводным сульфатом натрия и затем упаривают при пониженном давлении. Осадок очищают хроматографией на силикагелевой колонке при использовании толуола в качестве элюента для получения заданного продукта (23 г, содержащие растворитель) в виде желтой жидкости.
1H ЯМР (CDCl3) δ м.д.: 0,82–0,98 (2H, м), 1,03–1,17 (2H, м), 1,92–2,06 (1H, м), 3,86 (2H, с), 7,10–7,30 (4H, м).
Масс-спектр (CI, m/z): 179 (M++1).
(b) 5-(α-Циклопропилкарбонил-2-фторбензил)-2-оксо-2,4,5,6,7,7а-гексагидротиено[3,2-c]пиридин
К раствору циклопропил-2-фторбензилкетона (8,7 г), полученному в ссылочном примере 1(а), в тетрахлориде метана (80 мл) добавляют N-бромсукцинимид (9,6 г) и бензоилпероксид (0,5 г), затем смесь нагревают при кипячении с обратным холодильником в течение 6 часов. После реакции к реакционной смеси добавляют толуол и полученное твердое вещество отфильтровывают. Фильтрат концентрировали при пониженном давлении. Остаток очищают хроматографией на силикагелевой колонке при использовании толуола в качестве элюента для получения α-циклопропилкарбонил-2-фторбензилбромида (8,5 г) в виде желтого масла.
К раствору α-циклопропилкарбонил-2-фторбензилбромида (6,0 г), полученному выше, в диметилформамиде (20 мл) добавляют 2-оксо-2,4,5,6,7,7а-гексагидротиено[3,2-c]пиридина гидрохлорид (4,8 г), который получают согласно способу, описанному в ЕР 192535 (публикация японской заявки на патент № Sho 61-246186), и бикарбонат калия (7,0 г). После перемешивания смеси при комнатной температуре в течение 2 часов реакционную смесь разделяют между этилацетатом и водой. Этилацетатный слой промывают насыщенным водным раствором хлорида натрия, сушат над безводным сульфатом натрия и упаривают при пониженном давлении. После очистки остатка хроматографией на силикагелевой колонке при использовании в качестве элюента толуол/этилацетата=3/1 продукт кристаллизуют из диизопропилового простого эфира для получения желаемого продукта (2,6 г, выход 35%) в виде светло-коричневых кристаллов, т.пл. 123-125°C.
1H ЯМР (CDCl3) δ м.д.: 0,75–0,96 (2H, м), 0,99-1,14 (2H, м), 1,83–2,01 (1H, м), 2,02–2,17 (1H, м), 2,25–2,45 и 2,47–2,62 (все 2H, каждый м), 2,85 и 3,10 (все 2H, каждый д, J=12,0 Гц), 3,88–4,01 и 4,03-4,16 (все 2H, каждый м), 4,85 и 4,89 (все 1H, каждый с), 6,03 и 6,06 (все 1H, каждый с), 7,10–7,45 (4H, м).
Масс-спектр (CI, m/z): 332 (M++1), 262.
Аналитически рассчитано для C18H18FNO2S, %: C 65,23; H 5,48; N 4,23.
Обнаружено, %: C 65,09; H 5,55; N 4,20.
(с) 2-Ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридин
К раствору 5-(α-циклопропилкарбонил-2-фторбензил)-2-оксо-2,4,5,6,7,7а-гексагидротиено[3,2-c]пиридина (2,6 г), полученному в ссылочном примере 1(b), в виде смеси с диметилформамидом (10 мл) и уксусным ангидридом (5 мл), охлажденной на ледяной бане, добавляют гидрид натрия (60% дисперсия в минеральном масле, 0,35 г), затем смесь перемешивают при той же температуре в течение 30 минут и далее при комнатной температуре в течение 3 часов. После реакции, смесь экстрагируют этилацетатом и экстракт промывают насыщенным водным раствором хлорида натрия, затем сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. После очистки остатка хроматографией на силикагелевой колонке при использовании толуол/этилацетата=3/1 в качестве элюента, продукт кристаллизуют из диизопропилового простого эфира для получения желаемого соединения (1,88 г, выход 65%) в виде белых кристаллов, т.пл. 120-122°C.
1H ЯМР (CDCl3) δ м.д.: 0,80-0,95 (2H, м), 0,99-1,16 (2H, м), 2,27 (3H, с), 2,21-2,34 (1H, м), 2,70-2,95 (4H, м), 3,47 (1H, д, J=15,0 Гц), 3,57 (1H, д, J=15,0 Гц), 4,83 (1H, с), 6,27 (1H, с), 7,10-7,55 (4H, м).
ИК (KBr), νmax, cм-1: 1758, 1704.
Масс-спектр (CI, m/z): 374 (M++1), 304.
Аналитически рассчитано для C20H20FNO3S, %: C 64,32; H 5,40; N 3,75.
Обнаружено, %: C 64,46; H 5,39; N 3,73.
Пример испытания 1
Концентрация метаболита в плазме собак
После перорального введения испытываемого соединения кобелям породы бигль (вес тела около 10 кг, продаваемые Kasho Co., Ltd. и Nippon Nosan Kogyo K.K.) измеряли концентрацию метаболита в плазме. (2Z)-[1-[α-Циклопропилкарбонил-2-фторбензил]-4-метилтио-3-пиперидинилиден]уксусную кислоту (далее здесь обозначаемую как “S-метильная форма”) использовали в качестве контрольного метаболита. Эта S-метильная форма является основным метаболитом 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина в плазме людей, собак и крыс. Ранее сообщалось, что S-метильная форма является показателем количества активного метаболита 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено-[3,2-c]пиридина, поскольку она образуется при последующем метаболизме активного метаболита [Annu. Rep. Sankyo Res. Lab., 51, 1 (1999)].
Через тридцать минут после кормления собак специальным кормом для собак, каждое испытываемое соединение (10 мг/кг), упакованное в желатиновые капсулы, перорально вводили каждой из собак. Отбирали образец крови объемом 3 мл шприцом, обработанным гепарином, из брахиальной подкожной вены каждой собаки после 15, 30, 45, 60, 90 и 120 минут после введения. Сразу после отбора образцов цельную кровь центрифугировали для получения плазмы. Образцы плазмы хранили до анализа при –30°С. К 0,5 мл размороженной плазмы добавляют 0,25 мл 2-гидроксиацетофенона (1 мкг/мл, в качестве внутреннего стандартного вещества), 0,25 мл 10 мМ буфера фосфата калия (рН 4,5) и 0,5 мл метанола. Смесь перемешивают при 20±3°С.
После добавления 8 мл смеси изопропиловый спирт/хлороформ (1/9) смесь встряхивают для экстрагирования S-метильной формы и внешнего стандартного соединения в фазу растворителя. Экстракт разделяют на водную фазу и фазу растворителя при использовании низкоскоростного центрифугирования (1500×g в течение 15 минут). Подходящую аликвоту базовой фазы растворителя сушат досуха при использовании газообразного азота и затем повторно растворяют в 0,25 мл мобильной фазы ВЭХЖ. Отдельно известное количество S-метильной формы добавляют к контрольной плазме собак с последующей сходной экстракцией. Калибровочную кривую получают нанесением соотношения площади пиков S-метильной формы и соединения внутреннего стандарта по оси Y напротив соответствующей концентрации добавляемой S-метильной формы по оси Х. Концентрацию S-метильной формы в образце рассчитывают по калибровочной кривой.
Условия ВЭХЖ
Колонка: YMC A302 (4,6×150 мм).
Мобильная фаза: ацетонитрил/изопропиловый спирт/вода/ трифторуксусная кислота (10/12/78/0,01).
Скорость потока 1,0 мл/мин.
Регистрация: УФ 220 нм.
Впрыскиваемое количество 30 мкл.
Результаты показаны в таблице 1. В этой таблице площадь под концентрацией плазмы – кривая зависимости от времени, которая является показателем количества, получаемого in vivo, и максимальная концентрация в плазме, которые являются фармокинетическими параметрами, имеют аббревиатуры AUC и Cmax соответственно. В этой таблице термин “гидрохлорид” означает 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина гидрохлорид, полученный в примере 1, тогда как “свободная форма” означает 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридин.
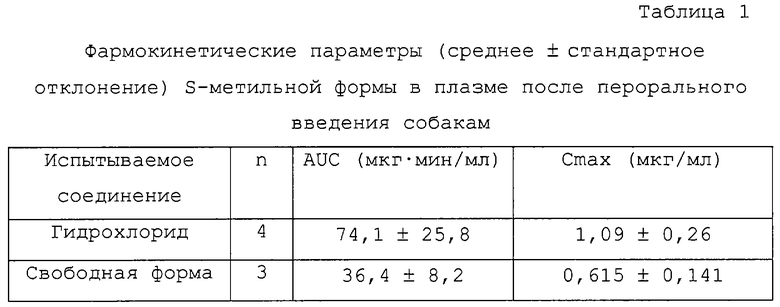
Результаты показывают, что как значения AUC, так и Сmax увеличиваются при конверсии 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина в его гидрохлорид.
Пример испытания 2
Ингибирующее действие на агрегацию тромбоцитов (кормление)
Для данного испытания использовали кобелей породы бигль (вес тела около 10 кг, продаваемые Kasho Co., Ltd. и Nippon Nosan Kogyo K.K.). Одна группа состояла из 5 или 6 собак. Агрегацию тромбоцитов измеряли при использовании автоматического аггрегометра тромбоцитов (“PAM-6C”, торговое название; изделие Mebanix Corporation) в соответствии со способом Born et al. (J. Physiol., 168, 178 (1963)) с небольшой модификацией.
Через каждые 2,5 часа и 4,5 часа после кормления отбирали 5,4 мл крови из головной вены каждой собаки при использовании цитрата натрия (0,6 мл, 3,8% (вес./об.) в качестве антикоагулянта. Кровь с добавлением цитрата центрифугировали (240 g, 20 минут) для отделения плазмы, обогащенной тромбоцитами (здесь далее обозначаемой как PRP), и плазмы, с низким содержанием тромбоцитов (далее здесь обозначаемой как РРР). После подсчета тромбоцитов в PRP автоматическим гематологическим анализатором (“К-1000”, торговое название; изделие Sysmex Corporation) добавляют PPP для установления числа тромбоцитов до 3×108/мл. PRP (240 мкл), диспергированную в кювете, помещали в автоматический агрегометр тромбоцитов. После предварительного нагревания (при 37°С) в течение 1 минуты добавляют 10 мкл АДФ (конечная концентрация 20 мкМ) для агрегации тромбоцитов. В течение 10 минут измеряли агрегацию тромбоцитов и максимальную агрегацию тромбоцитов определяли для получения значения до введения.
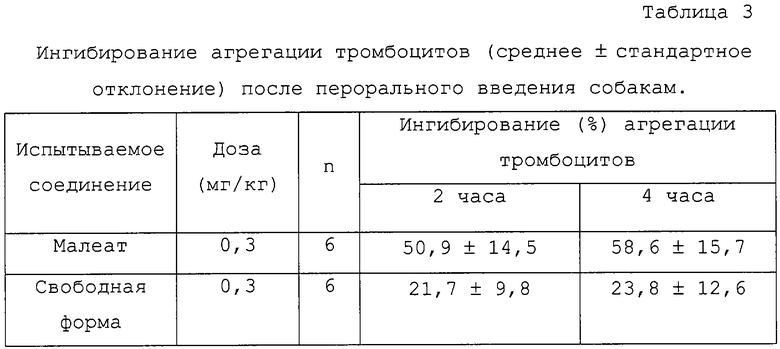
На следующий день, через 30 минут после кормления, испытываемое соединение в виде желатиновой капсулы вводили перорально собакам. Кровь отбирали через каждые 2 и 4 часа после введения. Измеряли агрегацию тромбоцитов PRP, посредством чего определяли максимальную агрегацию. Ингибирование (%) агрегации тромбоцитов испытываемым соединением рассчитывали путем сравнения его со значением перед введением. Результаты представлены в таблицах 2 и 3.
В этих таблицах термин “гидрохлорид” означает 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина гидрохлорид, полученный в примере 1, тогда как “свободная форма” означает 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридин и “малеат” означает 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина малеат, полученный в примере 2.
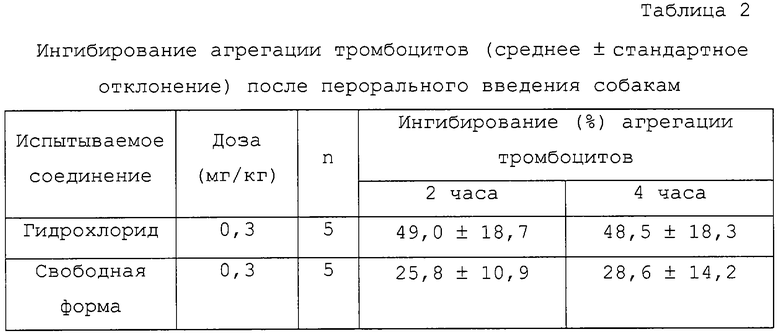
Пример испытания 3
Ингибирующее действие на агрегацию тромбоцитов (натощак)
Для данного испытания использовали кобелей породы бигль (вес тела около 10 кг, продаваемые Kasho Co., Ltd. и Nippon Nosan, Kogyo K.K.). Одна группа состояла из 3 собак. Агрегацию тромбоцитов измеряли при использовании автоматического агрегометра тромбоцитов (“PAM-6C”, торговое название; изделие Mebanix Corporation) в соответствии со способом Born et al. (J. Physiol., 168, 178 (1963)) с небольшой модификацией.
Из головной вены каждой собаки, которая не получала пищу в течение ночи, отбирали 5,4 мл крови при использовании цитрата натрия (0,6 мл, 3,8% (вес./об.)) в качестве антикоагулянта. Полученную кровь с добавлением цитрата центрифугировали (240 g, 20 минут) для отделения плазмы, обогащенной тромбоцитами (здесь далее обозначаемой как PRP), и плазмы с низким содержанием тромбоцитов (далее здесь обозначаемой как РРР). После подсчета тромбоцитов в PRP автоматическим гематологическим анализатором (“К-1000”, торговое название; изделие Sysmex Corporation) добавляют PPP для установления числа тромбоцитов до 3×108/мл. PRP (240 мкл), диспергированную в кювете, помещали в автоматический агрегометр тромбоцитов. После предварительного нагревания (при 37°С) в течение 1 минуты добавляют 10 мкл АДФ (конечная концентрация 20 мкМ) для агрегации тромбоцитов. В течение 10 минут измеряли агрегацию тромбоцитов и максимальную агрегацию тромбоцитов определяли для получения значения до введения.
На следующий день испытываемое соединение в желатиновой капсуле вводили перорально собакам. Кровь отбирали через каждые 2 и 4 часа после введения. Измеряли агрегацию тромбоцитов PRP, посредством чего определяли максимальную агрегацию. Ингибирование (%) агрегации тромбоцитов испытываемым соединением рассчитывали путем сравнения его со значением перед введением. Результаты представлены в таблице 4.
В этой таблице термин “малеат” означает 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина малеат, полученный в примере 2, тогда как термин “свободная форма” означает 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридин.

Результаты испытаний 2 и 3 показывают, что ингибирующее действие 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина гидрохлорида и малеата на АДФ-индуцированную агрегацию тромбоцитов сильнее, чем для 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина, и 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина гидрохлорид и малеат оба проявляют превосходную фармакологическую активность по сравнению с 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридином.
Пример состава 1
Твердая капсула
Порошок 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина гидрохлорида (50 мг), лактозу (128,7 мг), целлюлозу (70 мг) и стерат магния (1,3 мг) смешивают, пропускают через сито (60 меш) и заполняют твердую желатиновую капсулу (№3, 250 мг).
Пример состава 2
Таблетка
Порошок 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина гидрохлорида (50 мг), лактозу (124 мг), целлюлозу (25 мг) и стерат магния (1 мг) смешивают и прессуют в таблетировочной машине с получением таблетки весом 200 мг, которая при желании может иметь покрытие.
Пример состава 3
Твердая капсула
Порошок 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина малеата (50 мг), лактозу (128,7 мг), целлюлозу (70 мг) и стерат магния (1,3 мг) смешивают, пропускают через сито (60 меш) и заполняют твердую желатиновую капсулу (№3, 250 мг).
Пример состава 4
Таблетка
Порошок 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина малета (50 мг), лактозу (124 мг), целлюлозу (25 мг) и стерат магния (1 мг) смешивают и прессуют в таблетировочной машине с получением таблетки весом 200 мг, которая при желании может иметь покрытие.
| название | год | авторы | номер документа |
|---|---|---|---|
| МЕДИЦИНСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ АСПИРИН | 2001 |
|
RU2262933C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОЧИСТОГО ПРАЗУГРЕЛЬ ГИДРОХЛОРИДА | 2008 |
|
RU2435776C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКООЧИЩЕННОГО ПРАСУГРЕЛЯ ИЛИ ЕГО КИСЛОТНО-АДДИТИВНОЙ СОЛИ | 2007 |
|
RU2424243C2 |
| ПРОИЗВОДНЫЕ ТЕТРАГИДРОТИЕНО(3,2-С)ПИРИДИНА ИЛИ ИХ ФУРО-АНАЛОГИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2089553C1 |
| КРИСТАЛЛЫ ГИДРОБРОМАТА ПРАСУГРЕЛЯ | 2010 |
|
RU2484094C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2001 |
|
RU2281757C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2270695C2 |
| ПРОИЗВОДНОЕ СЛОЖНОГО ЭФИРА ТИЕНОПИРИДИНА, СОДЕРЖАЩЕЕ ЦИАНОГРУППУ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ЕГО ПРИМЕНЕНИЕ И КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2011 |
|
RU2526624C2 |
| ЦИКЛИЧЕСКИЕ АМИНОПРОИЗВОДНЫЕ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ И ПРЕДУПРЕЖДЕНИЯ ЗАБОЛЕВАНИЙ | 1997 |
|
RU2163596C2 |
| СПОСОБ ПОЛУЧЕНИЯ КЛОПИДОГРЕЛЯ И ЕГО ПРОИЗВОДНЫХ | 2009 |
|
RU2469039C2 |
Настоящее изобретение относится к кислотным аддитивным солям – гидрохлориду и малеату 2-ацетокси-5-(α-циклопропилкарбонил-2-фторбензил)-4,5,6,7-тетрагидротиено[3,2-c]пиридина. Описан также способ их получения, лекарственное средство на основе солей и применение. Кислотные аддитивные соли тетрагидротиенопиридиновых производных демонстрируют превосходную пероральную абсорбцию, метаболизм в активное соединение и ингибирующее действие при агрегации тромбоцитов, низкую токсичность, превосходную стабильность при хранении и использовании. Они пригодны в качестве терапевтических или профилактических агентов (предпочтительно терапевтических агентов) при тромбозе или эмболии. 9 c. и 19 з.п. ф-лы, 4 табл.
| Способ получения производных тетрагидро(фуро- или тиено)-[2,3-с]пиридина или их гидрохлоридов или четвертичных солей с метилйодидом | 1988 |
|
SU1657064A3 |
Авторы
Даты
2004-10-20—Публикация
2001-07-03—Подача