Настоящее изобретение относится к вводимой орально лекарственной композиции, предназначенной для контролируемого высвобождения из нее опиоидного, обладающего анальгезирующим действием активного вещества.
Из уровня техники известен целый ряд содержащих анальгезирующие средства композиций, обеспечивающих контролируемое высвобождение активного вещества. Так, в частности, в заявке ЕР-А 0647448 уже описан обладающий анальгезирующим действием препарат с замедленным, постепенным выделением активного вещества, в состав которого входят несколько представленных в ретардированной форме, содержащих опиоиды субстратов с диаметром от 0,1 до 3 мм, и который предназначен для введения в качестве суточной дозы. Пригодные для использования в этом препарате субстраты могут быть представлены в форме сфероидов, микрошариков, сферических гранул и обычных гранул. Для получения субстратов подобного типа требуются, как правило, связанные с относительно высокими затратами технологические операции, как, например, приготовление и нанесение покрытия на сферические гранулы или экструзия, сферонизация для получения сфероидов и придания им соответствующей формы.
С другой стороны, многие опиоидные активные вещества в процессе их получения образуются в виде кристаллов, а это в свою очередь создает проблему, связанную с возможностью их непосредственного, т.е. без проведения указанных дорогостоящих технологических операций, применения при изготовлении лекарственных средств.
С учетом вышеизложенного в основу настоящего изобретения была положена задача разработать предназначенный для орального введения препарат с контролируемым высвобождением по меньшей мере одного опиоидного активного вещества, в котором можно было бы непосредственно, т.е. без проведения связанных с высокими затратами технологических операций, использовать кристаллы, образующиеся в процессе получения активных веществ.
Согласно изобретению указанная задача решается благодаря созданию предназначенного для орального введения препарата с контролируемым высвобождением опиоидного анальгетика в форме кристаллов с размером частиц от 10 мкм до 3 мм, имеющих по меньшей мере одну ретардирующую (способствующую замедленному выделению) оболочку. Предпочтительно размер кристаллических частиц составляет от 50 мкм до 1 мм.
В качестве анальгетического активного вещества препараты по изобретению содержат в своем составе по меньшей мере один опиоид в кристаллической форме. В качестве опиоидов могут применяться гидроморфон, оксикодон, морфин, леворфанол, метадон, дигидрокодеин, кодеин, дигидроморфин, петидин, фентанил, пиритрамид, бупренорфин, тилидин, трамадол, их соответствующие соли или их смеси. К наиболее предпочтительным анальгетикам относятся трамадол, трамадолгидрохлорид, морфин, морфингидрохлорид и/или морфинсульфат.
Активное кристаллическое вещество в препаратах по изобретению может представлять собой монокристаллы либо иметь поликристаллическую структуру.
Наряду с вышеназванными опиоидными анальгетиками в состав препарата согласно изобретению могут входить и неопиоидные анальгезирующие средства, которые при определенных условиях проявляют вместе с опиоидными анальгетиками синергетический эффект. К числу таких неопиоидных анальгетиков относятся среди прочих ибупрофен, кетопрофен, флурбипрофен, пропифеназон, парацетамол, напроксен, ацеметацин, ацетилсалициловая кислота, метамизол и их соли, все предпочтительно в форме кристаллов.
Предлагаемые для применения согласно изобретению препараты отличаются контролируемым, предпочтительно постепенным выделением содержащихся в их составе анальгетиков. Этот эффект достигается за счет нанесения на кристаллы активного вещества по меньшей мере одной ретардирующей оболочки. Благодаря такой оболочке обеспечивается контролируемое замедленное, пролонгированное высвобождение активного вещества в течение определенного промежутка времени. Таким образом удается целенаправленно регулировать продолжительность действия предлагаемых в изобретении препаратов в отличие от традиционных лекарственных форм, т.е. форм, не имеющих указанного ретардирующего покрытия. При этом предусматривается, что для выделения активного вещества препарат достаточно вводить максимум два раза в сутки, предпочтительно даже только один раз.
В качестве покрывных материалов, т.е. материалов для оболочки, можно использовать все фармацевтически приемлемые для таких целей материалы, известные специалисту в данной области техники. Предпочтительно использовать природные, а при определенных условиях модифицированные или синтетические полимеры. К таковым относятся, например, такие полимеры, как простые эфиры целлюлозы или акриловые смолы. Наиболее предпочтительны водонерастворимые либо водонабухаемые производные целлюлозы, такие как алкилцеллюлоза, предпочтительно этилцеллюлоза, или водонерастворимые акриловые смолы, такие как поли(мет)акриловая кислота и/или ее производные, в частности ее соли, амиды или эфиры. В качестве покрывного материала пригодны также водонерастворимые воски. Все эти материалы известны из уровня техники, например из публикации В. Bauer, Lehmann, Osterwald, Rothgang "Ueberzogene Arzneiformen", изд-во Wissenschaftliche Verlagsgesellschaft mbH, Штутгарт, 1998, стр. 69 и далее, и включены в настоящее описание в качестве ссылки.
Кроме водонерастворимых полимеров и восков, для регуляции скорости высвобождения активного вещества при необходимости можно использовать также в количестве до 30 мас.% и не обладающие ретардирующей способностью, предпочтительно водорастворимые полимеры, такие, например, как поливинилпирролидон, или водорастворимые производные целлюлозы, такие как гидроксиэтилцеллюлоза, гидроксипропилметилцеллюлоза либо гидроксипропилцеллюлоза, и/или известные пластификаторы.
Помимо ретардирующей оболочки на кристаллы активного вещества можно наносить еще и иные покрытия. Такое покрытие при этом, выполненное, например, из материала, отличного от ретардирующей оболочки, может быть нанесено на поверхность кристаллов в виде неретардирующего разделительного слоя. В качестве покрывных материалов для этого разделительного слоя приемлемы предпочтительно простой эфир целлюлозы, поливидоны, полиакрилаты, равно как и полимерные природные вещества.
Другая возможность, альтернативная вышеописанной, состоит в том, что на оболочку, предпочтительно ретардирующую, наносят еще одно покрытие из кристаллического активного вещества либо из другого, отличного от последнего, предпочтительно опиоидного анальгетика, который высвобождается из этого дополнительного покрытия без замедления, сразу же после орального введения препарата. Такое многослойное покрытие должно обеспечить после введения препарата соответствующую быстродействующую начальную дозу анальгетика для снижения болей, при этом эффективность действия анальгетика в целом обеспечивается за счет последующего постепенного выделения активного вещества. В качестве покрывных материалов в указанных целях могут использоваться фармацевтически приемлемые материалы в сочетании с начальным активным веществом, как, например, простой эфир целлюлозы, поливидоны или полиакрилаты. В неретардирующем покрытии в качестве добавок к кристаллическому активному веществу либо вместо него или же вместо отличного от него другого, предпочтительно опиоидного, анальгетика можно предусмотреть иное фармацевтическое активное вещество.
Согласно другому варианту кристаллы активного вещества наряду с ретардирующей оболочкой могут иметь еще и другие покрытия, растворимость которых зависит от значения рН. Так, в частности, можно добиться того, что по меньшей мере часть кристаллов препарата проходит через желудочный тракт в нерастворенном виде и высвобождается только лишь при поступлении в кишечный тракт.
В другом предпочтительном варианте предусматривается, что предлагаемые в изобретении препараты наряду с имеющими ретардирующую оболочку и необязательно дополнительные покрытия кристаллами активного вещества, обеспечивающими контролируемое высвобождение активного вещества, содержат также кристаллы активного вещества с нанесенными на них одной либо несколькими неретардирующими покрытиями из числа вышеназванных.
Технология получения кристаллов опиоидного активного вещества известна. При этом кристаллы получают непосредственно в процессе требуемой в этих целях очистки.
На образующиеся непосредственно в процессе их получения, предпочтительно после перекристаллизации, кристаллы активного вещества наносят покрытия по обычным известным методам, например напылением растворов, дисперсий и/или эмульсий либо путем пульверизации. Приемлем также метод коацервации. Предпочтительно при этом сначала наносить на отдельные кристаллы соответствующий разделительный слой, причем данную операцию следует проводить по завершении последней стадии очистки, кристаллизации и сушки путем напыления лакового раствора или предпочтительно водной покрывной дисперсии. Затем на этот разделительный слой также напылением покрывной дисперсии и последующей сушкой наносят ретардирующую оболочку. Толщину этой оболочки можно варьировать в зависимости от требуемой продолжительности выделения активного вещества. Если предусматриваются еще и другие покрытия, то их предпочтительно наносить также с помощью выше описанного метода.
Объектом настоящего изобретения являются далее предназначенные для орального введения препараты в виде капсул, в которых содержатся кристаллы активного вещества с контролируемым высвобождением опиоидного анальгетика в соответствии с требуемой в каждом случае продолжительностью такого высвобождения и с предусматриваемым количеством выделяемого анальгетика.
Количество кристаллов активного вещества в одной капсуле выбирают при этом предпочтительно таким образом, чтобы обеспечить дозу, достаточную для двухкратного, предпочтительно однократного приема. Технология изготовления этой ретардирующей композиции также не требует существенных затрат, поскольку уже имеющие покрытие кристаллы нужно лишь поместить в капсулы. Согласно изобретению кристаллы активного вещества можно расфасовывать в соответствующей унифицированной дозировке во флакончики либо саше или осуществлять объемную дозировку с помощью соответствующего дозатора. Не исключается и добавление обычных вспомогательных веществ, таких как наполнители, смазки или вещества, способствующие разложению покрытия.
Предназначенные для орального введения препараты по изобретению могут изготавливаться, кроме того, в виде таблеток, при этом кристаллы активного вещества таблетируют в соответствии с предусматриваемыми для конкретных случаев продолжительностью их высвобождения и выделяемым количеством опиоидного анальгетика с использованием обычных вспомогательных веществ и добавок либо без таковых. И в этих случаях количество кристаллов активного вещества, из которых прессуют таблетки, предпочтительно выбирать таким образом, чтобы обеспечить требуемые продолжительность высвобождения и количество выделяемого анальгетика, достаточные для двухкратного, предпочтительно однократного суточного приема. Предпочтительно изготавливать таблетки с высокой долей вспомогательных веществ с целью сохранить активное вещество для индивидуального назначения. При быстром распаде таблеток кристаллы, из которых происходит затем постепенное высвобождение активного вещества, выделяются. В случае разделения таблетки на части такое пролонгированное выделение активного вещества также сохраняется.
Другая возможность изготовления таблеток предусматривает низкое содержание в них вспомогательных веществ. При этом в процессе таблетирования может происходить агрегация покрытых кристаллов активного вещества между собой, благодаря чему образуется дополнительная ретардирующая матрица. Подобные таблетки распадаются уже не спонтанно и, таким образом, пролонгированное действие проявляется более четко по сравнению с кристаллами, имеющими покрытие в каждом конкретном случае.
Предпочтительно общая концентрация трамадола в препаратах согласно изобретению в пересчете на гидрохлоридную соль составляет от 10 до 1000 мг, предпочтительно от 50 до 800 мг.
Примеры
Пример 1
В этом примере кристаллы трамадолгидрохлорида с поликристаллической структурой и размером частиц 250-500 мкм использовали после их получения и очистки без проведения последующей стадии приготовления композиции. Данные касательно количества этилцеллюлозы указаны в пересчете на сухую массу после нанесения водной дисперсии.

Указанные кристаллы трамадолгидрохлорида перемещали в аппарате с псевдоожиженным слоем с помощью нагретого воздуха и на эти кристаллы с помощью сопла для двухкомпонентных материалов медленно напыляли водную суспензию этилцеллюлозы, в которую предварительно при перемешивании добавляли дибутилсебакат. После нанесения суспензии кристаллы подвергали сушке.
Пример 2
Из покрытых в примере 1 кристаллов изготавливали капсулы. С этой целью покрытые кристаллы смешивали в кубическом смесителе с вышеуказанными вспомогательными веществами и с помощью капсулятора формировали капсулы с твердожелатиновой оболочкой размера 2.
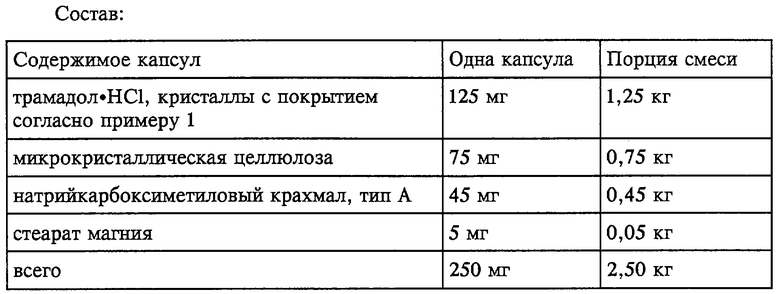
Пример 3
250 г кристаллов с нанесенным согласно примеру 1 покрытием смешивали с 344 г микрокристаллической целлюлозы и 6 г стеарата магния и из этой смеси прессовали быстро распадающиеся таблетки диаметром 10 мм и весом 300 мг.
Пример 4
В этом примере по завершении процесса их получения и очистки использовали кристаллы трамадолгидрохлорида поликристаллической структуры с размером частиц 250-500 мкм. Данные касательно промежуточного слоя, равно как и ретардирующей оболочки, указаны в пересчете на сухую массу после нанесения водной дисперсии.
Указанные кристаллы трамадолгидрохлорида перемещали в аппарате с псевдоожиженным слоем с помощью нагретого воздуха и сначала для образования промежуточного слоя на них напыляли водную дисперсию, после чего проводили сушку. Затем на кристаллы с помощью сопла для двухкомпонентных материалов медленно напыляли водную суспензию этилцеллюлозы, в которую предварительно при перемешивании добавляли дибутилсебакат. После нанесения суспензии кристаллы сушили.

| название | год | авторы | номер документа |
|---|---|---|---|
| АНАЛЬГЕТИК С КОНТРОЛИРУЕМЫМ ВЫСВОБОЖДЕНИЕМ АКТИВНОГО ВЕЩЕСТВА | 2000 |
|
RU2244541C2 |
| СИНЕРГИЧЕСКАЯ АНАЛЬГЕЗИРУЮЩАЯ КОМБИНАЦИЯ ОПИОИДНОГО АНАЛЬГЕЗИРУЮЩЕГО СРЕДСТВА И ИНГИБИТОРА ЦИКЛООКСИГЕНАЗЫ-2 | 1998 |
|
RU2232600C2 |
| СПОСОБ ПРЕДОТВРАЩЕНИЯ ЗЛОУПОТРЕБЛЕНИЯ СОДЕРЖАЩИМИ ОПИОИДЫ ЛЕКАРСТВЕННЫМИ ФОРМАМИ | 1998 |
|
RU2228180C2 |
| ЛЕКАРСТВЕННАЯ РЕТАРД-ФОРМА, СОДЕРЖАЩАЯ САХАРИНАТ ТРАМАДОЛА | 2000 |
|
RU2292877C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ОКРУГЛЫХ ГРАНУЛ | 2000 |
|
RU2221553C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2007 |
|
RU2445077C2 |
| ПЕРОРАЛЬНЫЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ | 2000 |
|
RU2240786C2 |
| ФАРМАЦЕВТИЧЕСКИЕ СОЛИ ТРАМАДОЛА | 2000 |
|
RU2292876C2 |
| ФАРМАЦЕВТИЧЕСКИЕ СОЛИ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2002 |
|
RU2309942C2 |
| ПРЕПАРАТЫ В ВИДЕ ПЕЛЛЕТ СФЕРИЧЕСКОЙ ФОРМЫ | 2003 |
|
RU2336863C2 |
Предложен новый предназначенный для орального введения препарат с контролируемым высвобождением опиоидного анальгетика в форме кристаллов с размером частиц от 10 мкм до 3 мм, предпочтительно от 50 мкм до 1 мм, имеющих по меньшей мере одну ретардирующую оболочку. Изобретение расширяет арсенал пероральных лекарственных форм опиоидных анальгетиков с замедленным выделением активного ингредиента. 15 з.п. ф-лы, 3 табл.
| WO 9901111 A1, 14.01.1999 | |||
| Устройство для секционирования тяговой цепи очистного комбайна | 1974 |
|
SU647448A1 |
| М.Д | |||
| МАШКОВСКИЙ | |||
| Лекарственные средства | |||
| - М.: Медицина, 1993, ч.1, с.181, 184, 188-190 | |||
| ВОДНАЯ СУСПЕНЗИЯ, СОДЕРЖАЩАЯ МИКРОКРИСТАЛЛЫ ФАРМАКОЛОГИЧЕСКИ АКТИВНОГО ВОДОНЕРАСТВОРИМОГО ЛЕКАРСТВЕННОГО ВЕЩЕСТВА, ПОКРЫТЫЕ МЕМБРАНООБРАЗУЮЩИМ ЛИПИДОМ (ВАРИАНТЫ), И ЛИОФИЛИЗИРОВАННЫЙ ПРЕПАРАТ ВОДНОЙ СУСПЕНЗИИ | 1992 |
|
RU2100030C1 |
Авторы
Даты
2004-11-10—Публикация
2000-01-17—Подача