Настоящее изобретение относится к лекарственным ретард-формам с ретардирующим покрытием, которые содержат в качестве действующего вещества трамадол в виде его сахарината, а также необязательно другие вспомогательные вещества.
Хорошо растворимый в воде гидрохлорид трамадола, т.е. гидрохлорид(1RS,2RS)-2-[(диметиламино)метил]-1-(3-метоксифенил)циклогексанола, часто применяют для снятия сильных болей и болей средней силы.
Введение гидрохлорида трамадола в виде ретард-препаратов позволяет улучшить терапевтический эффект этого действующего вещества. Ретардация (замедленное высвобождение) позволяет, в том числе и для этого действующего вещества с относительно коротким периодом полураспада в организме получить препарат с сохраняющимся в течение длительного времени действием, а за счет поддержания его концентрации в крови на более равномерном уровне позволяет также свести к минимуму побочные эффекты и создать условия для соблюдения пациентами предписанной схемы дозировки.
Ретардацию действующего вещества гидрохлорида трамадола можно обеспечить, например, нанесением ретардирующих пленочных покрытий на содержащие гидрохлорид трамадола лекарственные формы. Однако обеспечение ретардации этого действующего вещества с помощью пленочных покрытий связано с относительно высокими затратами, поскольку пленочные покрытия, наносимые из водных систем, часто создают недостаточно эффективный диффузионный барьер для таких хорошо растворимых в воде действующих веществ, а проницаемость этих пленочных покрытий для гидрохлорида трамадола при длительном хранении в большинстве случаев изменяется (Р.В.O'Donnell, J.W.McGinity, "Mechanical Properties of Polymeric Films, Prepared from Aqueous Polymeric Dispersions in Aqueous Polymeric Coatings for Pharmaceutical Dosage Forms", Drugs and the Pharmaceutical Science, т.79, под ред. J.W.McGinity, изд-во Marcel Decker, New York, Basel, Hong Kong, 1997).
Поэтому технология изготовления этих ретард-препаратов на основе гидрохлорида трамадола требует применения относительно сложных в осуществлении методов нанесения покрытий в виде многослойных пленок или длительных методов термической обработки, описанных, например, в публикациях US 5645858, соответственно US 5580578, US 5681585, US 5472712, а также у К.Bauer, "Coated Pharmaceutical Dosage Forms", изд-во Medpharm Scientific Publishers, Stuttgart, 1998, у В.Sutter, Диссертация, защищенная при Университете г.Дюссельдорф, 1987, или у F.N.Christensen, Proceed. Intern. Symp. Contr. Rel. Bioact. Mater., 17:124 (1990). Если такие покрытия наносят из растворов в органических растворителях, то связанные с этим расходы на охрану окружающей среды при утилизации остатков растворителей дополнительно удорожают технологию обеспечения ретардации гидрохлорида трамадола.
Исходя из вышеизложенного, в основу настоящего изобретения была положена задача разработать имеющую ретардирующее покрытие лекарственную ретард-форму с трамадолом в качестве действующего вещества, которая непосредственно после ее изготовления обладала бы стабильным при длительном хранении профилем высвобождения действующего вещества без необходимости осуществления сложных и дорогостоящих методов нанесения покрытия или длительной и тем самым связанной с высокими издержками термической обработки.
Согласно изобретению указанная задача решается с помощью лекарственных ретард-форм с ретардирующим покрытием, которые в качестве действующего вещества содержат трамадол в виде его сахарината, а также необязательно другие вспомогательные вещества.
При создании изобретения неожиданно было установлено, что предлагаемые в нем лекарственные ретард-формы обнаруживают уже непосредственно после их изготовления стабильный при длительном хранении профиль высвобождения действующего вещества, для достижения чего после обычной сушки ретардирующее покрытие не требуется подвергать термической обработке.
При получении сахарината трамадола этот трамадол, т.е. (1RS,2RS)-2-[(диметиламино)метил]-1-(3-метоксифенил)циклогексанол, и/или по крайней мере одну его соответствующую, предпочтительно водорастворимую, соль подвергают взаимодействию с сахарином и/или по крайней мере с одной его, предпочтительно водорастворимой, солью. В качестве соли трамадола предпочтительно применять его гидрохлорид, а в качестве соли сахарина предпочтительно использовать его натриевую, калиевую, кальциевую или аммониевую соль, более предпочтительно его натриевую соль.
Сахаринат трамадола может также образовываться in situ в процессе изготовления лекарственных ретард-форм.
Понятие "образование in situ" в контексте настоящего изобретения означает, что слабо растворимую в воде соль трамадола смешивают с растворимой в воде солью сахарина, многократно увлажняют и гранулируют, при необходимости экструдируют и/или перерабатывают в лекарственную форму при подводе иной энергии, предпочтительно под давлением и/или при подводе тепла.
Для образования сахарината трамадола in situ трамадол можно использовать в виде водорастворимой, фармацевтически приемлемой соли, предпочтительно в виде его гидрохлорида, а сахарин использовать в виде его водорастворимой, фармацевтически приемлемой соли, предпочтительно натриевой, калиевой, кальциевой или аммониевой соли, более предпочтительно в виде натриевой соли.
Предлагаемые в изобретении лекарственные формы с ретардирующим пленочным покрытием пригодны предпочтительно для перорального введения.
В одном из предпочтительных вариантов осуществления настоящего изобретения предлагаемые в изобретении лекарственные формы представлены в виде таблеток, капсул или суспензий.
В другом предпочтительном варианте осуществления настоящего изобретения предлагаемые в нем лекарственные формы представлены в состоящем из множества частиц виде, предпочтительно в виде микротаблеток, микрокапсул, микропеллетов, гранул, кристаллов действующих веществ или малых сферических гранул (пеллетов), необязательно расфасованных в капсулы или спрессованных в таблетки, либо в виде гидрофильной или липофильной жидкости, предпочтительно в виде гомогенной суспензии, наиболее предпочтительно в виде микстур или дисперсий для перорального введения.
Если предлагаемые в изобретении лекарственные формы представлены в виде гранул или пеллетов, то их размер предпочтительно составляет от 0,1 до 3 мм, более предпочтительно от 0,5 до 2 мм.
Если предлагаемые в изобретении лекарственные формы представлены в виде микротаблеток, то их диаметр предпочтительно составляет от 0,5 до 5 мм, более предпочтительно от 1 до 3 мм и наиболее предпочтительно от 1 до 2 мм.
Если предлагаемые в изобретении лекарственные формы представлены в виде кристаллов действующих веществ, микрочастиц, микропеллетов или микрокапсул, то их диаметр предпочтительно составляет от 10 мкм до 1 мм, более предпочтительно от 15 мкм до 0,5 мм и более предпочтительно от 30 до 200 мкм.
Помимо этого в состав предлагаемых в изобретении лекарственных форм в зависимости от формы их выпуска могут входить в качестве дополнительных компонентов обычные, хорошо известные специалистам вспомогательные вещества.
Если предлагаемые в изобретении лекарственные формы представлены в виде таблеток или микротаблеток, то в их состав в качестве других вспомогательных веществ предпочтительно включать микрокристаллическую целлюлозу, простой эфир целлюлозы, лактозу, крахмал и его производные, сахароспирты, гидрофосфат кальция, а также обычные, хорошо известные специалистам связующие, регуляторы текучести, смазывающие вещества и необязательно разрыхлители.
Если предлагаемые в изобретении лекарственные формы представлены в виде пеллетов, гранул или микропеллетов, то в их состав в качестве других вспомогательных веществ предпочтительно включать микрокристаллическую целлюлозу, простой эфир целлюлозы, лактозу, крахмал и его производные, сахароспирты, гидрофосфат кальция, алифатические спирты, сложные эфиры глицерина или эфиры жирных кислот.
Если предлагаемые в изобретении лекарственные формы представлены в виде микрокапсул или микрочастиц, то в зависимости от применяемой технологии их изготовления в их состав могут входить обычные, хорошо известные специалистам вспомогательные вещества.
Предлагаемые в изобретении лекарственные формы различных типов можно получать различными, хорошо известными специалистам методами.
Если предлагаемые в изобретении лекарственные формы представлены в виде таблеток, то их можно изготавливать, например, прессованием гранул, полученных путем влажного гранулирования, сухого гранулирования или гранулирования из расплава, либо непосредственным таблетированием сахарината трамадола, необязательно с дополнительными вспомогательными веществами. Кроме того, таблетки можно изготавливать прессованием снабженных покрытием пеллетов, кристаллов действующих веществ, микрочастиц или микрокапсул.
Предлагаемые в изобретении лекарственные формы в виде пеллетов можно изготавливать путем экструзии и сфероидизации путем послойного (нарастительного) гранулирования (пеллетирования) либо путем непосредственного пеллетирования в высокоскоростной мешалке или вихревом псевдоожиженном слое. Наиболее предпочтительно изготавливать пеллеты путем экструзии влажной массы с последующей сфероидизацией. Микрокапсулы изготавливают обычными методами микрокапсулирования, например распылительной сушкой, распылительной кристаллизацией (распылительным отверждением) или коацервацией.
В одном из предпочтительных вариантов осуществления изобретения в качестве основы ретардирующего пленочного покрытия, наносимого на предлагаемые лекарственные формы, предпочтительно использовать нерастворимый в воде, необязательно модифицированный природный и/или синтетический полимер либо природный, полусинтстический или синтетический воск, жир или алифатический спирт либо смесь по крайней мере двух указанных компонентов.
Для получения ретардирующего покрытия в качестве нерастворимых в воде полимеров для получения покрытия предпочтительно использовать поли(мет)акрилаты, более предпочтительно поли(С1-С4)алкил(мет)акрилаты, поли(С1-С4)диалкиламино-(С1-С4)алкил(мет)акрилаты и/или их сополимеры, наиболее предпочтительно сополимеры этилакрилата и метилметакрилата с молярным соотношением мономеров 2:1 (продукт Eudragit NE30D®), сополимеры этилакрилата, метилметакрилата и хлорида триметиламмонийэтилметакрилата с молярным соотношением мономеров 1:2:0,1 (продукт Eudragit RS®), сополимеры этилакрилата, метилметакрилата и хлорида триметиламмонийэтилметакрилата с молярным соотношением мономеров 1:2:0,2 (продукт Eudragit RL®) либо смесь по крайней мере двух указанных сополимеров. Эти материалы для покрытия поставляются на рынок в виде 30%-ных (по массе) водных латексных дисперсий, т.е. в виде продуктов Eudragit RS30D®, Eudragit NE30D®, соответственно Eudragit RL30D®, и их как таковые преимущественно используют в качестве материала покрытия.
В качестве нерастворимых в воде полимеров для получения ретардирующего покрытия у предлагаемых в изобретении лекарственных форм предпочтительно также использовать поливинилацетаты, необязательно в сочетании с другими вспомогательными веществами. Они поставляются на рынок в виде водной дисперсии, содержащей 27 мас.% поливинилацетата, 2,5 мас.% повидона и 0,3 мас.% натрийлаурилсульфата (продукт Kollicoat SR30D®).
В соответствии еще с одним предпочтительным вариантом осуществления изобретения в качестве основы ретардирующих покрытий предлагаемых в изобретении лекарственных форм можно использовать нерастворимые в воде производные целлюлозы, предпочтительно алкилцеллюлозы, такие как этилцеллюлоза, либо сложные эфиры целлюлозы, такие как ацетат целлюлозы. Покрытия из этилцеллюлозы или ацетата целлюлозы предпочтительно наносить из водной псевдолатексной дисперсии. Водные псевдолатсксные дисперсии этилцеллюлозы поставляются на рынок в виде 30%-ных (по массе) дисперсий (продукт Aquacoat®) или 25%-ных (по массе) дисперсий (продукт Surelease®).
В качестве природных, полусинтетических или синтетических типов воска, жиров, соответственно алифатических спиртов для ретардирующего покрытия предлагаемых в изобретении лекарственных форм предпочтительно использовать карнаубский воск, пчелиный воск, глицеринмоностеарат, глицеринмонобегенат (продукт Compritol ATO888®), глицериндитрипальмитостеарат (продукт Precirol ATO5®), микрокристаллический воск, цетиловый спирт, цетилстеариловый спирт либо смесь по крайней мере двух указанных компонентов.
Если в качестве основы ретардирующего покрытия используют нерастворимый в воде, необязательно модифицированный, природный и/или синтетический полимер, то с целью понизить минимальную температуру нанесения пленочного покрытия в состав дисперсии или раствора для нанесения покрытия помимо соответствующего полимера может дополнительно входить обычный, хорошо известный специалистам физиологически приемлемый пластификатор.
В качестве примера пригодных для этой цели пластификаторов можно назвать липофильные диэфиры алифатической или ароматической дикарбоновой кислоты с С6-С40 и алифатического спирта с C1-C8, например дибутилфталат, диэтилфталат, дибутилсебацат или диэтилсебацат, гидрофильные или липофильные эфиры лимонной кислоты, например триэтилцитрат, трибутилцитрат, ацетилтрибутилцитрат или ацетилтриэтилцитрат, полиэтиленгликоли, пропиленгликоль, сложные эфиры глицерина, например триацетин, продукт Myvacet® (ацетилированные моно- и диглицериды от С23Н44O5 до С25Н47O7), триглицериды со средней длиной цепи (продукт о Miglyol®), олеиновую кислоту или смеси по крайней мере двух указанных пластификаторов. В составе водных дисперсий продукта Eudragit RS® и необязательно продукта Eudragit RL® предпочтительно применять триэтилцитрат.
Предпочтительное количество пластификатора(ов) в составе ретардирующего покрытия предлагаемой в изобретении лекарственной формы составляет от 5 до 50 мас.%, более предпочтительно от 10 до 40 мас.% и наиболее предпочтительно от 10 до 30 мас.% в пересчете на количество используемого(ых) полимера(ов). В отдельных случаях, например при применении ацетата целлюлозы, пластификаторы можно также использовать в более высоких количествах, составляющих предпочтительно до 110 мас.%.
Помимо этого в состав ретардирующего покрытия могут входить и другие обычные, хорошо известные специалистам, вспомогательные вещества, например смазывающие вещества, предпочтительно тальк или глицеринмоностеарат, пигменты, предпочтительно оксиды железа или диоксид титана, или поверхностно-активные вещества, например продукт Tween 80®.
Профиль высвобождения трамадола, достигаемый непосредственно после изготовления предлагаемой в изобретении лекарственной формы, можно регулировать обычными, хорошо известными специалистам методами, например варьированием толщины покрытия или за счет применения других вспомогательных веществ в качестве компонентов покрытия. К пригодным для этой цели вспомогательным веществам относятся, например, гидрофильные или рН-зависимые порообразователи, например натрийкарбоксиметилцеллюлоза, ацетат-фталат целлюлозы, ацетат-сукцинат гидроксипропилметилцеллюлозы, лактоза, полиэтиленгликоль или маннит, либо водорастворимые полимеры, например поливинилпирролидон, или же водорастворимые типы целлюлозы, предпочтительно гидроксипропилметилцеллюлоза или гидроксипропилцеллюлоза.
Ретардирующее покрытие для дальнейшего повышения его ретардирующего действия может содержать также нерастворимые, соответственно липофильные вспомогательные вещества, например алкилированный диоксид кремния, который, например, поставляется на рынок как продукт Aerosil R972®, или стеарат магния.
Предлагаемые в изобретении лекарственные формы для высвобождения сахарината трамадола дополнительно могут иметь также стойкое к действию желудочного сока покрытие, растворимость которого зависит от величины рН. Благодаря такому покрытию предлагаемые в изобретении лекарственные формы проходят через желудок, не растворяясь в нем, и начинают высвобождать сахаринат трамадола только в кишечнике. Предпочтительно, чтобы стойкое к действию желудочного сока покрытие растворялось при значении рН от 5 до 7,5. Для получения стойкого к действию желудочного сока покрытия предпочтительно использовать сополимеры метакриловой кислоты и метилметакрилата с молярным соотношением мономеров 1:1 (продукт Eudragit L®), сополимеры метакриловой кислоты и метилметакрилата с молярным соотношением мономеров 1:2 (продукт Eudragit S®), сополимеры метакриловой кислоты и этилакрилата с молярным соотношением мономеров 1:1 (продукт Eudragit L30-D55®), сополимеры метакриловой кислоты, метилакрилата и метилметакрилата с молярным соотношением мономеров 7:3:1 (продукт Eudragit FS®), шеллак, ацетат-сукцинат гидроксипропилметилцеллюлозы, фталат-ацетат целлюлозы или смеси по крайней мере двух указанных компонентов, необязательно также в сочетании с описанными выше нерастворимыми в воде поли(мет)акрилатами, предпочтительно в сочетании с продуктом Eudragit NE30D® и/или продуктом Eudragit RL® и/или продуктом Eudragit RS®.
Покрытия предлагаемых в изобретении лекарственных форм можно наносить обычными, пригодными для получения каждого конкретного покрытия, хорошо известными специалистам методами, например напылением растворов, дисперсий или суспензий, методом нанесения из расплава или методом нанесения порошковых материалов. Указанные растворы, дисперсии или суспензии можно применять в виде водных или органических растворов или дисперсий. При этом предпочтительно применять водные дисперсии. В качестве органических растворителей можно использовать спирты, например этанол или изопропанол, кетоны, например ацетон, сложные эфиры, например этилацетат, хлорированные углеводороды, например дихлорметан, при этом предпочтительно применять спирты и кетоны. Можно также использовать смеси по крайней мере двух указанных выше растворителей. Такие методы нанесения покрытий известны из уровня техники, например из публикации Н. Sucker, изд-во Georg Thieme Verlag, 1991, стр.347 и далее. Все такие методы включены в настоящее описание в качестве ссылки.
Если предлагаемые в изобретении оральные лекарственные формы представлены в состоящем из множества частиц виде, то ретардирующее покрытие предпочтительно наносить таким образом, чтобы после изготовления на состоящие из множества частиц формы, содержащие сахаринат трамадола, можно было в псевдоожиженном слое наносить покрытие из соответствующих полимеров и необязательно других вспомогательных веществ из водных и/или органических сред, предпочтительно из водных сред, и сушить полученное покрытие, предпочтительно одновременно, при обычных температурах в псевдоожиженном слое, не подвергая покрытие последующей термической обработке. Сушку покрытия из поли(мет)акрилата предпочтительно проводить при температуре приточного воздуха в пределах от 30 до 50°С, более предпочтительно от 35 до 45°С.
Сушку покрытий на основе целлюлозы, например этилцеллюлозы или ацетата целлюлозы, предпочтительно осуществлять при температуре в пределах от 50 до 80°С, более предпочтительно от 55 до 65°С.
Восковые покрытия можно наносить из расплава в псевдоожиженном слое и после нанесения покрытия охлаждать до температуры ниже соответствующей температуры плавления воска с целью полного его отверждения. Наносить восковые покрытия можно также путем распыления их растворов в органических растворителях.
Для дальнейшей модификации профиля высвобождения действующего вещества предлагаемые в изобретении лекарственные ретард-формы могут содержать сахаринат трамадола также в ретардирующей матрице, предпочтительно в равномерно распределенном виде.
В качестве материалов матрицы можно использовать физиологически приемлемые гидрофильные материалы, хорошо известные специалистам в данной области. В качестве основы ретардирующей матрицы предпочтительно использовать простые эфиры целлюлозы, сложные эфиры целлюлозы и/или полиакрилаты. Наиболее предпочтительно использовать в качестве матрицы этилцеллюлозу, гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу, гидроксиметилцеллюлозу, поли(мет)акриловую кислоту и/или ее производные, такие как ее соли, амиды или эфиры.
Равным образом в качестве материалов матрицы предпочтительно использовать гидрофобные материалы, такие как гидрофобные полимеры, различные типы воска, жиры, жирные кислоты с длинной цепью, алифатические спирты или соответствующие сложные или простые эфиры либо их смеси. Наиболее предпочтительными гидрофобными материалами являются моно- или диглицериды жирных С12-С30кислот и/или алифатические С12-С30спирты и/или различные типы воска либо их смеси.
В качестве материала ретардирующей матрицы можно также использовать смеси указанных выше гидрофильных и гидрофобных материалов.
Ретардирующую матрицу можно получать обычными, хорошо известными специалистам методами.
Согласно еще одному предпочтительному варианту предлагаемые в изобретении лекарственные формы содержат действующее вещество трамадол как в ретардированном, так и неретардированном виде, например в виде гидрохлорида трамадола. Комбинирование с немедленно высвобождающимся действующим веществом позволяет ввести пациенту высокую начальную дозу для быстрого снятия боли. В последующем замедленное высвобождение действующего вещества из ретард-формы предотвращает ослабление анальгетического действия.
Назначаемая пациенту доза трамадола варьируется, например, в зависимости от веса пациента, показания к применению, а также от степени тяжести болей, соответственно заболевания. Дозу вводимого трамадола, а также профиль его высвобождения предпочтительно подбирать с таким расчетом, чтобы лекарственное средство требовалось принимать максимум дважды, предпочтительно только однократно, в сутки.
Содержание трамадола в предлагаемых в изобретении лекарственных формах, рассчитанных на однократный прием в день, предпочтительно составляет от 10 до 1200 мг, более предпочтительно от 20 до 1000 мг и наиболее предпочтительно от 100 до 800 мг.
Содержание трамадола в предлагаемых в изобретении лекарственных формах, рассчитанных на двукратный прием в день, предпочтительно составляет от 5 до 600 мг, более предпочтительно от 10 до 500 мг и наиболее предпочтительно от 50 до 400 мг трамадола.
Предлагаемые в изобретении лекарственные формы предпочтительно использовать для снятия болей или лечения таких заболеваний, как недержание мочи, кашель, воспалительные процессы, аллергические реакции, депрессии, абузус, алкоголизм, гастрит, диарея, сердечно-сосудистые заболевания, заболевания дыхательных путей, психические заболевания или эпилепсия, более предпочтительно для снятия болей или лечения недержания мочи или кашля.
Преимущество предлагаемых в изобретении лекарственных форм состоит в том, что они уже непосредственно после их изготовления характеризуются стабильным при хранении профилем высвобождения действующего вещества без необходимости подвергать полученную форму обычно следующей за сушкой термической обработке или наносить на нее покрытие сложным в осуществлении методом. Подобное преимущество позволяет сократить продолжительность, а тем самым и затраты на изготовление предлагаемых в изобретении лекарственных форм.
Кроме того, при создании изобретения неожиданно было установлено, что высвобождение действующего вещества трамадола из предлагаемых в изобретении лекарственных форм с нанесенным из водной среды ретардирующим покрытием происходит значительно медленнее по сравнению с лекарственными формами, которые снабжены ретардирующим покрытием идентичного состава или структуры, но которые содержат трамадол в качестве действующего вещества в виде его гидрохлорида. Помимо этого еще одно преимущество, связанное с нанесением ретардирующего пленочного покрытия из водной среды, состоит в отсутствии необходимости в сложной регенерации органических растворителей, а также в том, что предлагаемые в изобретении лекарственные формы не содержат более остаточных количеств растворителей.
Кроме того, предлагаемые в изобретении лекарственные формы отличаются тем, что характер высвобождения из них действующего вещества трамадола не зависит от обычно переменных условий высвобождения, например от ионной концентрации буфера, от наличия поверхностно-активных веществ или от изменения механической нагрузки.
Профиль высвобождения действующего вещества из предлагаемых в изобретении лекарственных форм определяли следующим образом.
Предлагаемую в изобретении лекарственную форму исследовали в корзиночном устройстве или в лопастной мешалке в соответствии с Европейской фармакопеей в течение 2 часов в 600 мл искусственного желудочного сока с рН 1,2 при температуре среды, в которую высвобождается действующее вещество, 37±0,5°С и при скорости вращения 100 об/мин, соответственно 50 об/мин при использовании лопастной мешалки. Затем лекарственную форму исследовали в течение 8 ч в 900 мл искусственного кишечного сока с рН 7,2. В каждом случае количество высвободившегося к определенному моменту времени сахарината трамадола определяли с помощью ЖХВР. В каждом опыте использовали по три образца и полученные для трех таких образцов результаты усредняли.
Ниже изобретение проиллюстрировано на примерах 1-11, которые не ограничивают его объем.
Примеры
Пример 1
Для получения сахарината трамадола эквимолярные количества трамадола, т.е. гидрохлорида (1RS,2RS)-2-[(диметиламино)метил]-1-(3-метоксифенил)циклогексанола, и натриевой соли сахарина либо дигидрата натриевой соли сахарина полностью растворяют при нагревании в минимально возможном количестве воды. После этого оба раствора путем перемешивания объединяют между собой. Сахаринат трамадола, который по истечении короткого интервала времени выкристаллизовывается при охлаждении из водного раствора, выделяют обычными методами и очищают с помощью этанола.
Получение пеллетов
2500 г сахарината трамадола и 2500 г микрокристаллической целлюлозы (Avicel PH 105 фирмы FMC) перемешивают в высокоскоростном смесителе Diosna P25 в течение 10 мин и затем гранулируют с использованием 3300 г деминерализованной воды в течение 10 мин. Далее влажный гранулят экструдируют в экструдере типа NICA E140 с экструзионной матрицей размером 1,0×2,0 мм и после этого влажный экструдат порциями по 2,7 кг сфероидизируют в сфероидизаторе типа NICA в течение 15 мин при скорости вращения 800 об/мин. Затем полученные пеллеты сушат в течение ночи в сушильном шкафу при 50°С. Выход пеллетов крупностью от 800 до 1250 мкм составляет более 90%.
Нанесение покрытия
На 3 кг полученных пеллетов (крупностью от 800 до 1250 мкм) наносят покрытие в псевдоожиженном слое (установка Hüttlin HKC05) из водной дисперсией указанного ниже состава при температуре продукта от 26 до 30°С до увеличения массы на 16 мас.% (в пересчете на исходную массу пеллетов). Это покрытие соответствует содержанию полимерного покрытия в 13 мас.% (в пересчете на исходную массу пеллетов). В завершение пеллеты сушат в псевдоожиженном слое в течение 10 мин при 45°С.
345 мг пеллетов с ретардирующим покрытием содержат 149 мг сахарината трамадола, что соответствует дозе гидрохлорида трамадола 100 мг.
Профиль высвобождения определяют вышеописанным методом в корзиночном устройстве, при этом полученные результаты приведены в таблице 1, а также на фиг.3.
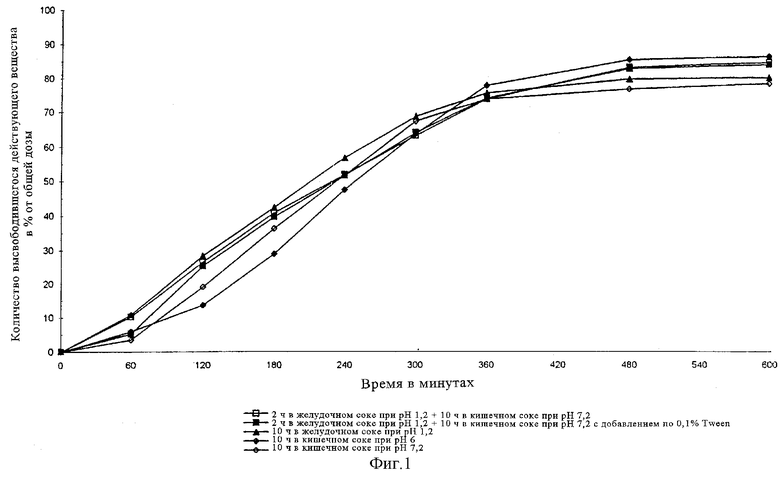
Кроме того, по описанному выше методу определяли также характеристики высвобождения действующего вещества из полученных таким путем пеллетов с ретардирующим покрытием в средах различного состава в условиях, указанных в таблице 2.
Полученные в этих опытах результаты представлены на фиг.1. Как следует их приведенных на фиг.1 графиков, различный состав среды, в которую высвобождается действующее вещество, практически не влияет на профиль высвобождения сахарината трамадола из содержащих его пеллетов с ретардирующим покрытием. Таким образом, ни величина рН, ни ионная сила, ни наличие поверхностно-активных веществ не влияют на профиль высвобождения действующего вещества из пеллетов с ретардирующим покрытием.
Сравнительный пример 1
Получение пеллетов, содержащих гидрохлорид трамадола
275 г сахарината трамадола, 75 г микрокристаллической целлюлозы (Avicel РН 105 фирмы FMC) и 105 г гидроксипропилцеллюлозы с низкой степенью замещения (1-НРС LH31®) перемешивают в планетарной мешалке Kennwood Chef в течение 10 мин, а затем гранулируют с использованием 250 г деминерализованной воды в течение 10 мин. Влажный гранулят экструдируют в экструдере типа NICA E140 с экструзионной матрицей размером 1,0×2,0 мм и после этого влажный экструдат сфероидизируют в сфероидизаторе NICA в течение 15 мин при скорости вращения 800 об/мин. Затем полученные пеллеты сушат в течение ночи в сушильном шкафу при 50°С. Выход пеллетов крупностью от 800 до 1250 мкм составляет более 90%.
Нанесение покрытия
На 320 г полученных пеллетов (крупностью от 800 до 1250 мкм) наносят покрытие в псевдоожиженном слое (установка Acromatic, Strea 1) из водной дисперсии указанного ниже состава при температуре продукта от 26 до 30°С до увеличения массы на 25 мас.% (в пересчете на исходную массу пеллетов). Это покрытие соответствует содержанию полимерного покрытия в 16 мас.% (в пересчете на исходную массу пеллетов). В завершение пеллеты сушат в псевдоожиженном слое в течение 10 мин при 45°С.
228 мг пеллетов с ретардирующим покрытием содержат 100 мг гидрохлорида трамадола.
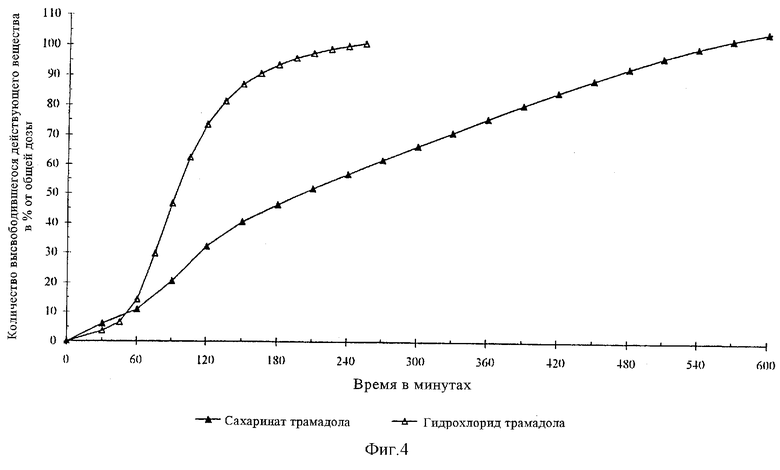
Профиль высвобождения определяли указанным выше методом в корзиночном устройстве. Полученные в этом опыте результаты, а также результаты, полученные для предлагаемых в изобретении пеллетов из примера 1, приведены на фиг.4.
Как следует из приведенных на фиг.4 графиков, действующее вещество сахаринат трамадола высвобождается из содержащих его пеллетов с ретардирующим покрытием в течение 10 ч, тогда как высвобождение действующего вещества гидрохлорида трамадола из содержащих его пеллетов с ретардирующим покрытием после непродолжительного времени задержки практически полностью завершается уже за 4 ч несмотря на более толстое полимерное покрытие и меньшую проницаемость полимерного состава этого покрытия.
Кроме того, определяли собственные характеристики высвобождения действующего вещества гидрохлорида трамадола, соответственно сахарината трамадола.
Характеристики собственного высвобождения действующего вещества и для гидрохлорида трамадола, и для сахарината трамадола определяют в деминерализованной воде (37°С±0,5°С) в соответствии с методом "<1087> intrinsic dissolution", опубликованному в USP 24-NF19, первое приложение (стр.2706 и далее). Для каждого из обоих действующих веществ собственное высвобождение рассчитывают по углу наклона касательной к кривой кумулятивного высвобождения действующего вещества вплоть до момента времени, в который высвобождение действующего вещества из спрессованного образца достигает 10%, и полученные результаты выражают в виде скорости высвобождения с размерностью мг-мин-1·см-2.
Собственное высвобождение в воде:
гидрохлорид трамадола: 21 мг-мин-1·см-2,
сахаринат трамадола: 2 мг-мин·см-2.
Различие в характеристиках собственного высвобождения действующих веществ однозначно свидетельствует о том, что сахаринат трамадола высвобождается из лекарственных форм значительно медленнее по сравнению с гидрохлоридом трамадола и поэтому также медленнее проникает сквозь диффузионные барьеры.
Пример 2
Получение пеллетов
505 г сахарината трамадола и 505 г микрокристаллической целлюлозы (Avicel РН 105® фирмы FMC) перемешивают в планетарной мешалке Kennwood Chef в течение 10 мин и затем гранулируют с использованием 630 г деминерализованной воды в течение 10 мин. Далее влажный гранулят экструдируют в экструдере типа NICA E140 с экструзионной матрицей размером 1,0×2,0 мм и после этого влажный экструдат сфероидизируют в сфероидизаторе типа NICA в течение 15 мин при скорости вращения 800 об/мин. Далее пеллеты сушат в течение ночи в сушильном шкафу при 50°С. Выход пеллетов крупностью от 800 до 1250 мкм составляет более 90%.
Нанесение покрытия
На 200 г полученных пеллетов (крупностью от 800 до 1250 мкм) наносят покрытие в псевдоожиженном слое (установка Aeromatic, Strea 1) из водной дисперсии указанного ниже состава при температуре продукта от 26 до 30°С до увеличения массы на 27 мас.% (в пересчете на исходную массу пеллетов). Это покрытие соответствует содержанию полимерного покрытия в 21 мас.% (в пересчете на исходную массу пеллетов). В завершение пеллеты с покрытием сушат в псевдоожиженном слое в течение 10 мин при 45°С.
379 мг пеллетов с ретардирующим покрытием содержат 149 мг сахарината трамадола, что соответствует дозе гидрохлорида трамадола 100 мг.
Профиль высвобождения определяли указанным выше методом в корзиночном устройстве, при этом полученные результаты приведены в таблице 3, а также на фиг.3. Однако в отличие от описанных выше условий пеллеты с покрытием исследовали в течение 10 ч в искусственном кишечном соке с рН 7,2.
Пример 3
Получение пеллетов
505 г сахарината трамадола и 505 г микрокристаллической целлюлозы (Avicel РН 105® фирмы FMC) перемешивают в планетарной мешалке Kennwood Chef в течение 10 мин и затем гранулируют с использованием 630 г деминерализованной воды в течение 10 мин. Далее влажный гранулят экструдируют в экструдере типа NICA E140 с экструзионной матрицей размером 1,0×2,0 мм и после этого влажный экструдат сфероидизируют в сфероидизаторе типа NICA в течение 15 мин при скорости вращения 800 об/мин. В завершение пеллеты сушат в течение ночи в сушильном шкафу при 50°С. Выход пеллетов крупностью от 800 до 1250 мкм составляет более 90%.
Нанесение покрытия
На 200 г полученных пеллетов (крупностью от 800 до 1250 мкм) наносят покрытие в псевдоожиженном слое (установка Aeromatic, Strea 1) из водной дисперсии указанного ниже состава при температуре продукта от 26 до 30°С до увеличения массы на 21 мас.% (в пересчете на исходную массу пеллетов). Это покрытие соответствует содержанию полимерного покрытия в 14 мас.% (в пересчете на исходную массу пеллетов). Затем пеллеты с покрытием подвергают исследованию на высвобождение действующего вещества либо непосредственно после нанесения покрытия и обычной сушки, либо после термической обработки, состоящей в выдержке в сушильном шкафу при 40°С в течение 15 ч.
361 мг пеллетов с ретардирующим покрытием содержат 149 мг сахарината трамадола, что соответствует дозе гидрохлорида трамадола 100 мг.
Соответствующие профили высвобождения определяли описанным выше методом в корзиночном устройстве, при этом полученные результаты приведены в таблице 4, а также на фиг.3 для пеллетов, не подвергнутых термической обработке.
Различия между показателями высвобождения действующих веществ из не подвергнутых и подвергнутых термической обработке форм составляют около 5%, что соответствует обычному разбросу результатов измерений. Таким образом, термическая обработка, проводимая после нанесения покрытия, не оказывает влияния на профиль высвобождения действующего вещества.
Пример 4
Получение пеллетов
252,5 г сахарината трамадола и 252,5 г микрокристаллической целлюлозы (Avicel РН 105® фирмы FMC) перемешивают в планетарной мешалке Kennwood Chef в течение 10 мин и затем гранулируют с использованием 338,0 г деминерализованной воды в течение 10 мин. Далее влажный гранулят экструдируют в экструдере типа NICA E140 с экструзионной матрицей размером 1,0×2,0 мм и после этого влажный экструдат сфероидизируют в сфероидизаторе типа NICA в течение 15 мин при скорости вращения 800 об/мин. В завершение пеллеты сушат в течение ночи в сушильном шкафу при 50°С. Выход пеллетов крупностью от 800 до 1250 мкм составляет более 90%.
Нанесение покрытия
На 170 г полученных пеллетов (крупностью от 800 до 1250 мкм) наносят покрытие в псевдоожиженном слое (установка Aeromatic, Strea 1) из водной дисперсии указанного ниже состава при температуре продукта от 26 до 30°С до увеличения массы на 28 мас.% (в пересчете на исходную массу пеллетов). Это покрытие соответствует содержанию полимерного покрытия в 20 мас.% (в пересчете на исходную массу пеллетов). Затем пеллеты с покрытием сушат в псевдоожиженном слое в течение 10 мин при 45°С.
381 мг пеллетов с ретардирующим покрытием содержат 149 мг сахарината трамадола, что соответствует дозе гидрохлорида трамадола 100 мг.
Профиль высвобождения определяли описанным выше методом в корзиночном устройстве, при этом полученные результаты приведены ниже в таблице 5, а также на фиг.3. Однако в отличие от описанных выше условий пеллеты с покрытием исследовали в течение 6 ч в искусственном кишечном соке с рН 7,2.
Пример 5
Получение пеллетов 505,0 г сахарината трамадола и 505,0 г микрокристаллической целлюлозы 20 (Avicel РН 105® фирмы FMC) перемешивают в планетарной мешалке Kennwood Chef в течение 10 мин и затем гранулируют с использованием 630,0 г деминерализованной воды в течение 10 мин. Далее влажный гранулят экструдируют в экструдере типа NICA E140 с экструзионной матрицей размером 1,0×2,0 мм и после этого влажный экструдат сфероидизируют в сфероидизаторе типа NICA в течение 15 мин при скорости вращения 800 об/мин. В завершение пеллеты сушат в течение ночи в сушильном шкафу при 50°С. Выход пеллетов крупностью от 800 до 1250 мкм составляет более 90%.
Нанесение покрытия
На 200 г полученных пеллетов (крупностью от 800 до 1250 мкм) наносят покрытие в псевдоожиженном слое (установка Aeromatic, Strea 1) из водной дисперсии указанного ниже состава при температуре продукта от 26 до 30°С до увеличения массы на 20 мас.% (в пересчете на исходную массу пеллетов). Это покрытие соответствует содержанию полимерного покрытия в 16 мас.% (в пересчете на исходную массу пеллетов). Затем пеллеты с покрытием сушат в псевдоожиженном слое в течение 10 мин при 45°С.
358 мг пеллетов с ретардирующим покрытием содержат 149 мг сахарината трамадола, что соответствует дозе гидрохлорида трамадола 100 мг.
Профиль высвобождения определяли указанным выше методом в корзиночном устройстве, при этом полученные результаты приведены в таблице 6, а также на фиг.3. Однако в отличие от описанных выше условий пеллеты с покрытием исследовали в течение 14 ч в искусственном кишечном соке с рН 7,2.
Пример 6
Исследование стабильности при хранении содержащих сахаринат трамадола пеллетов с ретардирующим покрытием
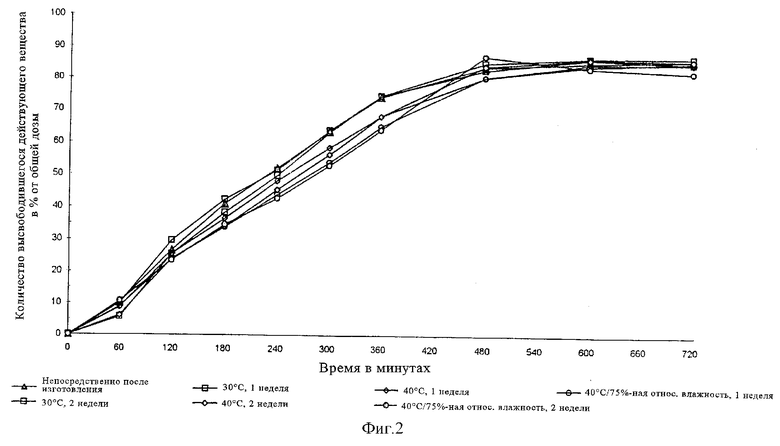
Полученные согласно примеру 1 пеллеты с ретардирующим покрытием выдерживали соответственно в закрытых стеклянных сосудах в течение 1, соответственно 2 недель либо при 30°С и 70%-ной относительной влажности воздуха, либо при 40°С в сухой атмосфере, либо при 40°С и 75%-ной относительной влажности воздуха и по истечении соответствующего времени хранения по описанному выше методу определяли профиль высвобождения действующего вещества. Однако в отличие от описанных выше условий пеллеты с покрытием исследовали в течение 10 ч в искусственном кишечном соке с рН 7,2.
Полученные в каждом из таких опытов результаты представлены на фиг.2. Как следует из приведенных на фиг.2 графиков, хранение при 30°С и 70%-ной относительной влажности воздуха, а также при 40°С в сухой атмосфере никак не сказывается на профиле высвобождения действующего вещества. Хранение при 40°С и 75%-ной относительной влажности воздуха также приводит лишь к незначительному замедлению высвобождения из частично слипшихся пеллетов. Поэтому предлагаемые в изобретении лекарственные формы с сахаринатом трамадола уже непосредственно после их изготовления обладают ретардирующим профилем высвобождения действующего вещества, который сохраняется при хранении и без термической обработки.
Пример 7
Получение пеллетов
250 г сахарината трамадола и 250 г микрокристаллической целлюлозы (Avicel PH 105® фирмы FMC) перемешивают в планетарной мешалке Kennwood Chef в течение 10 мин и затем гранулируют с использованием 443 г деминерализованной воды в течение 10 мин. Далее влажный гранулят экструдируют в экструдере типа NICA E140 с экструзионной матрицей размером 1,0×2,0 мм и после этого влажный экструдат сфероидизируют в сфероидизаторе типа NICA в течение 15 мин при скорости вращения 800 об/мин. В завершение пеллеты сушат в течение ночи в сушильном шкафу при 50°С. Выход пеллетов крупностью от 800 до 1250 мкм составляет более 90%.
Нанесение покрытия
На 170 г полученных пеллетов (крупностью от 800 до 1250 мкм) наносят покрытие в псевдоожиженном слое (установка Aeromatic, Strea 1) из водной дисперсии указанного ниже состава при температуре продукта от 35 до 40°С до увеличения массы на 5 мас.% (в пересчете на исходную массу пеллетов). Затем пеллеты с покрытием сушат в сушильном шкафу в течение 2 ч при 60°С.
*25%-ная псевдолатексная дисперсия этилцеллюлозы. Эта имеющаяся в продаже готовая дисперсия содержит дибутилсебацат в качестве пластификатора и диоксид кремния в качестве смазывающего вещества.
313 мг пеллетов с ретардирующим покрытием содержат 149 мг сахарината трамадола, что соответствует дозе гидрохлорида трамадола 100 мг.
Профиль высвобождения определяли описанным выше методом в корзиночном устройстве, при этом полученные результаты приведены в таблице 7, а также на фиг.3.
Пример 8
Изготовление таблеток
Состав из расчета на 1 таблетку:
Целлактозу и стеарат магния просеивают и затем в течение 10 мин перемешивают до гомогенности с сахаринатом трамадола в смесителе со свободным падением (Bohle, LM 40). Из этой смеси на эксцентриковом прессе типа Korsch EK0 с помощью пуансона прессуют круглые, выпуклые по типу драже таблетки диаметром 10 мм, высотой примерно 5 мм и радиусом выпуклости 8 мм.
Нанесение покрытия
На 2000 полученных таблеток наносят покрытие в псевдоожиженном слое (установка Aeromatic, Strea 1) из водной дисперсии указанного ниже состава при температуре продукта от 26 до 30°С до увеличения массы на 6,5 мас.% (в пересчете на исходную массу таблеток). Это покрытие соответствует содержанию полимерного покрытия в 5,0 мас.% (в пересчете на исходную массу таблеток). В завершение таблетки с покрытием сушат в сушильном шкафу в течение 10 мин при 40°С.
Профиль высвобождения определяли описанным выше методом в лопастной мешалке, при этом полученные результаты приведены в таблице 8.
Сравнительный пример 2
Изготовление таблеток
Состав из расчета на 1 таблетку:
Целлактозу и стеарат магния просеивают и затем в течение 10 мин перемешивают до гомогенности с гидрохлоридом трамадола в смесителе со свободным падением (Bohle, LM 40). Из этой смеси на эксцентриковом прессе Korsch EK0 с помощью пуансона прессуют круглые, выпуклые по типу драже таблетки диаметром 9 мм, высотой примерно 5 мм и радиусом выпуклости 8 мм.
Нанесение покрытия
На 2000 этих таблеток наносят покрытие в псевдоожиженном слое (установка Aeromatic, Strea 1) из водной дисперсии указанного ниже состава при температуре продукта от 26 до 30°С до увеличения массы на 6,5 мас.% (в пересчете на исходную массу таблеток). Это покрытие соответствует содержанию полимерного покрытия в 5,0 мас.% (в пересчете на исходную массу таблеток). В завершение таблетки с покрытием сушат в сушильном шкафу в течение 10 мин при 40°С.
Профиль высвобождения определяли описанным выше методом в лопастной мешалке, при этом полученные результаты приведены в таблице 8.
Если действующее вещество гидрохлорид трамадола высвобождается из таблеток с покрытием в течение 4 часов уже на >90%, то высвобождение сахарината трамадола из таблеток с покрытием происходит значительно медленнее и с постоянной скоростью, при этом через 12 часов высвобождается только 25% от общей дозы.
В данном случае также можно сделать вывод о том, что более медленное растворение сахарината трамадола при идентичных диффузионных барьерах приводит к существенно более выраженной ретардации по сравнению с высвобождением гидрохлорида трамадола и в отличие от него даже при меньшей толщине пленочного покрытия обеспечивает кинетику высвобождения 0-го порядка.
Пример 9
Получение пеллетов
500 г гидрохлорида трамадола, 345 г сахарината натрия и 845 г микрокристаллической целлюлозы (Avicel PH 101®) перемешивают в течение 10 мин и затем в течение 10 мин гранулируют с использованием деминерализованной воды в достаточном для гранулирования количестве. После гранулирования гранулят экструдируют в экструдере типа NICA E140 с экструзионной матрицей размером 0,8×1,6 мм и эктрудат вновь гранулируют с использованием достаточного количества воды с получением пластичной массы. Эту массу вновь экструдируют. Далее влажный экструдат сфероидизируют в сфероидизаторе NICA, тип S450. После сушки в сушильном шкафу пеллеты классифицируют, при этом выход пеллетов крупностью от 0,63 до 1,0 мм составляет >90%.
Нанесение покрытия
На 1000 г полученных пеллетов наносят покрытие в псевдоожиженном слое (установка Hüttlin HKC05) из водной дисперсии указанного ниже состава при температуре продукта от 26 до 30°С до увеличения массы на 20 мас.% (в пересчете на исходную массу пеллетов). Это покрытие соответствует содержанию полимерного покрытия в 16 мас.% (в пересчете на исходную массу пеллетов). В завершение пеллеты сушат в псевдоожиженном слое в течение 10 мин при 45°С.
Расфасовка пеллетов с покрытием в капсулы
406 мг пеллетов с ретардирующим покрытием (что соответствует дозе гидрохлорида трамадола 100 мг) расфасовывают на машине для сборки разъемных капсул Zanasi E6 в твердожелатиновые капсулы размера 0.
Профиль высвобождения определяли описанным выше методом в корзиночном устройстве, при этом полученные результаты приведены в таблице 9, а также на фиг.3. Однако в отличие от описанных выше условий пеллеты с покрытием исследовали в течение 10 ч в искусственном кишечном соке с рН 7,2.
Пример 10
Пеллеты получают аналогично примеру 4.
На 400 г этих пеллетов (крупностью от 800 до 1250 мкм) наносят покрытие в псевдоожиженном слое (установка Aeromatic, Strea 1) из водной дисперсии указанного ниже состава при температуре продукта от 26 до 30°С до увеличения массы на 25 мас.% (в пересчете на исходную массу пеллетов). Это покрытие соответствует содержанию полимерного покрытия в 20% (в пересчете на исходную массу пеллетов). В завершение пеллеты с покрытием сушат в псевдоожиженном слое в течение 10 мин при 40°С.
373 мг пеллетов с ретардирующим покрытием содержат 149 мг сахарината трамадола, что соответствует дозе гидрохлорида трамадола 100 мг.
Изготовление таблеток
Пеллеты с ретардирующим покрытием перемешивают в течение 5 мин в смесителе со свободным падением (Bohle, LM 40) с продуктом Kollidon CL® (сшитый поливинилпирролидон) и затем еще в течение 10 мин перемешивают с микрокристаллической целлюлозой (Avicel PH 101®) и стеаратом магния. Из этой смеси на таблетировочной машине (Fette, P 1200) прессуют круглые двоякоплоские таблетки диаметром 12 мм, массой по 500 мг каждая и твердостью от 100 до 130 Н.
В водной среде эти таблетки распадаются на отдельные пеллеты в течение 1-2 мин.
Профиль высвобождения определяли описанным выше методом в лопастной мешалке, при этом полученные результаты приведены в таблице 10, а также на фиг 3.
Пример 11
Пеллеты получают аналогично примеру 2.
На 200 г этих пеллетов (крупностью от 800 до 1250 мкм) наносят покрытие в псевдоожиженном слое (установка Aeromatic, Strea 1) из водной дисперсии указанного ниже состава при температуре продукта от 35 до 40°С до увеличения массы на 20 мас.% (в пересчете на исходную массу пеллетов). Это покрытие соответствует содержанию полимерного покрытия в 15 мас.% (в пересчете на исходную массу пеллетов). В завершение пеллеты с покрытием сушат в аппарате с псевдоожиженным слоем в течение 10 мин при 45°С.
358 мг пеллетов с ретардирующим покрытием содержат 149 мг сахарината трамадола, что соответствует дозе гидрохлорида трамадола 100 мг.
Профиль высвобождения определяли описанным выше методом в корзиночном устройстве, при этом полученные результаты приведены в таблице 11.
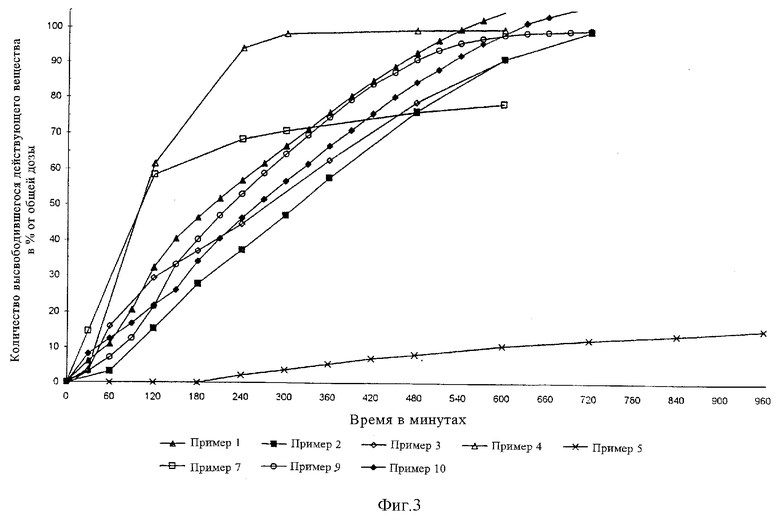
На фиг.3 представлены выборочные характеристики различных профилей высвобождения действующего вещества сахарината трамадола из экструдированных пеллетов, на которые наносили покрытие из водной дисперсии. Варьирование состава и толщины пленочного покрытия позволяет соответствующим образом регулировать профиль высвобождения действующего вещества из композиции, предназначенной для однократного приема в день, соответственно двукратного приема в день, а также сместить кинетику высвобождения с кинетики 1-го порядка в сторону кинетики 0-го порядка. Это свидетельствует о большом разнообразии достигаемых с помощью предлагаемого в изобретении решения показателей профиля высвобождения действующего вещества, при этом используют только коммерчески доступные полимерные дисперсии, перерабатываемые по рекомендуемой изготовителем технологии, без принятия дополнительных мер или применения особых добавок.
Изобретение относится к химико-фармацевтической промышленности и касается лекарственной формы трамадола с замедленным высвобождением. Лекарственная форма обладает высокой эффективностью при лечении болей различной этиологии и может применяться для лечения заболеваний, выбранных из группы: недержание мочи, кашля, воспалительные процессы и/или аллергические реакции, депрессивные состояния, абузус и/или алкоголизм, гастрит, диарея, сердечно-сосудистые заболевания, заболевания дыхательных путей, психические заболевания, эпилепсия. 37 з.п. ф-лы, 4 ил., 11 табл.
| RU 97111191 A1, 27.05.1999 | |||
| RU 99104404 A1, 27.03.1999 | |||
| ЕР 914823 A1, 12.05.1999 | |||
| RU 96116411 А, 10.11.1998. |
Авторы
Даты
2007-02-10—Публикация
2000-08-03—Подача