Изобретение относится к области ветеринарной вирусологии и биотехнологии и может быть использовано при разработке и изготовлении вакцинных препаратов для профилактики синдрома снижения яйценоскости-76 (ССЯ-76) птиц.
ССЯ-76 - вирусная болезнь кур-несушек, характеризующаяся резким, но непродолжительным снижением яичной продуктивности, появлением депигментированных яиц, яиц со слабой скорлупой и без скорлупы, а также увеличением процента боя и насечки.
Впервые болезнь была описана в 1976 году в Голландии. Позднее ССЯ-76 регистрировали во многих других странах Европы, Южной Америки, Австралии и Африки. В начале восьмидесятых годов прошлого века были выявлены случаи ССЯ-76 в нашей стране, что было подтверждено обнаруживанием в крови переболевших птиц антигемагглютининов к вирусу ССЯ-76.
Возбудителем болезни является ДНК-содержащий вирус, относящийся к семейству Adenoviridae, который в отличие от представителей других аденовирусов птиц способен агглютинировать эритроциты кур. К заболеванию восприимчивы куры-несушки всех пород в период наивысшей яйценоскости (180-240 сут), но возможно поражение птицы в любой период продуктивного цикла. Более восприимчивы к заболеванию куры высокопродуктивных мясояичных и мясных кроссов.
По данным многих зарубежных и отечественных исследователей экономический ущерб при ССЯ-76 складывается из потери от 5 до 30 яиц на курицу-несушку, а в племенных стадах с учетом выбраковки может доходить до 50 яиц.
Ущерб от болезни усугубляется затратами на оздоровительные мероприятия.
В настоящее время основным методом ликвидации ССЯ-76 птиц является вакцинопрофилактика заболевания [1].
Для специфической профилактики ССЯ-76 птиц широко используют инактивированные вакцины, приготовленные из различных штаммов вируса, репродуцированного в утиных эмбрионах (УЭ). Однако технология их изготовления обладает недостатками, устранение которых остается актуальной задачей и служит основной предпосылкой для проведения исследований по ее усовершенствованию и решения вопроса защиты птицеводства России от этой инфекции.
Известен способ изготовления инактивированной вакцины против ССЯ-76 птиц, включающий получение антигенного материала из штамма CNCM № 1043 гомологичного вируса, репродуцированного в УЭ, очистку антигенного материала от балластных примесей, инактивацию вируса, соединение антигенного материала с масляным адъювантом и последующий контроль целевого продукта [2, 3].
Известен способ изготовления инактивированной вакцины против ССЯ -76 птиц, включающий получение антигенного материала из штамма "В 8/78" гомологичного вируса, репродуцированного в УЭ, очистку антигенного материала от балластных примесей, инактивацию вируса бис-этилениминоэтилоксамидом, соединение антигенного материала с масляным адъювантом и последующий контроль целевого продукта [4].
Известен способ изготовления инактивированной вакцины против ССЯ-76 птиц, включающий получение антигенного материала из штамма ВГНКИ № 98 "Б-93" гомологичного вируса, репродуцированного в УЭ, очистку антигенного материала от балластных примесей, инактивацию вируса димером этиленимина, соединение антигенного материала с адъювантом и последующий контроль целевого продукта [5].
Известен способ изготовления инактивированной вакцины против ССЯ-76 птиц, включающий получение антигенного материала из штамма ВНИИВИП гомологичного вируса, репродуцированного в УЭ, очистку антигенного материала от балластных примесей, инактивацию вируса формалином, соединение антигенного материала с адъювантом и последующий контроль целевого продукта [6].
Наиболее близким к предлагаемому изобретению по совокупности существенных признаков является способ изготовления инактивированной вакцины против ССЯ-76 птиц, включающий получение антигенного материала из штамма "В 8/78" гомологичного вируса, репродуцированного в УЭ, очистку антигенного материала от балластных примесей, инактивацию вируса теотропином, соединение антигенного материала с масляным адъювантом и последующий контроль целевого продукта [7].
Общими существенными недостатками известных способов, как и способа-прототипа, являются низкая антигенная и гемаглютинирующая активность (ГА-активность) вакцинных препаратов по причине нестабильности при инактивации используемых для их изготовления штаммов вируса, а также необходимость культивирования вируса только в развивающихся УЭ.
В задачу создания настоящего изобретения входила разработка способа изготовления инактивированной вакцины против ССЯ-76 птиц на основе нового производственного штамма гомологичного вируса, обладающего высокой антигенной и ГА-активностью, сохраняющего свои нативные иммунобиологические свойства при инактивации и пригодного для изготовления высокоэффективной инактивированной вакцины, для которой антиген можно получать как в развивающихся утиных, так и в куриных эмбрионах (КЭ).
Технический результат от использования предлагаемого изобретения заключается в повышении антигенной и ГА-активности и стабильности препарата и расширении арсенала средств специфической профилактики ССЯ-76 птиц, обеспечивающих напряженный и длительный иммунитет у привитой птицы.
Указанный технический результат достигнут созданием способа изготовления инактивированной вакцины против ССЯ-76 птиц, охарактеризованного следующей совокупностью признаков:
1. Способ изготовления инактивированной вакцины против ССЯ-76 птиц.
2. Получение антигенного материала из штамма гомологичного вируса, репродуцированного в чувствительной биологической системе.
3. Из штаммов возбудителя инфекции используют штамм "БИСС № 113" вируса ССЯ-76 птиц в эффективном количестве.
4. Из чувствительных биологических систем используют 9-11-суточные УЭ.
5. Используют антигенный материал из штамма "БИСС № 113" гомологичного вируса, репродуцированного в 9-11-суточных УЭ, с биологической активностью, по меньшей мере, 6,0 lg ЭИД50/0,2 см3.
6. Используют антигенный материал из штамма "БИСС № 113" гомологичного вируса, репродуцированного в 9-11-суточных УЭ, с ГА-активностью, по меньшей мере, 1:4096.
7. Из чувствительных биологических систем используют 9-11-суточные эмбрионы SPF-кур.
8. Используют антигенный материал из штамма "БИСС № 113" гомологичного вируса, репродуцированного в 9-11-суточных эмбрионах SPF-кур, с биологической активностью, по меньшей мере, 6,0 lg ЭИД50/0,2 см3.
9. Используют антигенный материал из штамма "БИСС № 113" гомологичного вируса, репродуцированного в 9-11-суточных эмбрионах SPF-кур, с ГА-активностью, по меньшей мере, 1:4096.
10. Очистка антигенного материала от балластных примесей.
11. Очищенный антигенный материал подвергают инактивации.
12. Из инактивантов используют аминоэтилэтиленимин (АЭЭИ).
13. АЭЭИ используют в виде 10% водного раствора.
14. АЭЭИ вносят в антигенный материал в концентрации 0,2-0,4%.
15. Инактивацию вируса ССЯ-76 ведут в течение 48 часов при 37,0± 0,5° С и при рН 7,4-7,8.
16. Соединение очищенного и авирулентного антигенного материала с масляным адъювантом.
17. Из масляных адъювантов используют масляный адъювант "Монтанид ИЗА-70".
18. Антигенный материал из штамма "БИСС № 113" вируса ССЯ-76 птиц соединяют с масляным адъювантом "Монтанид ИЗА-70" в соотношении, по меньшей мере, 3:7 - 2:3.
19. Контроль целевого продукта.
Предлагаемое изобретение включает следующую совокупность существенных признаков, обеспечивающих получение технического результата во всех случаях, на которые испрашивается правовая охрана:
1. Способ изготовления инактивированной вакцины против ССЯ-76 птиц.
2. Получение антигенного материала из штамма "БИСС № 113" вируса ССЯ-76 птиц, репродуцированного в чувствительной биологической системе.
3. Штамм "БИСС № 113" вируса ССЯ-76 птиц используют в эффективном количестве.
4. Очистка антигенного материала от балластных примесей.
5. Инактивация вируса.
6. Соединение очищенного и авирулентного антигенного материала из штамма "БИСС № 113" вируса ССЯ -76 с масляным адъювантом.
7. Контроль целевого продукта.
Предлагаемое изобретение характеризуется также другими признаками, выражающими конкретные формы выполнения или особые условия его использования:
1. Из чувствительных биологических систем используют 9-11-суточные УЭ.
2. Используют антигенный материал из штамма "БИСС № 113", репродуцированного в 9-11-суточных УЭ, с биологической активностью, по меньшей мере, 6,0 lg ЭИД50/0,2 см3.
3. Используют антигенный материал из штамма "БИСС № 113" гомологичного вируса, репродуцированного в 9-11-суточных УЭ, с ГА-активностью, по меньшей мере, 1:4096.
4. Из чувствительных биологических систем используют 9-11-суточные эмбрионы SPF-кур.
5. Используют антигенный материал из штамма "БИСС № 113" гомологичного вируса, репродуцированного в 9-11-суточных эмбрионах SPF -кур, с биологической активностью, по меньшей мере, 6,0 lg ЭИД50/0,2 см3.
6. Используют антигенный материал из штамма "БИСС № 113" гомологичного вируса, репродуцированного в 9-11-суточных эмбрионах SPF-кур, с ГА-активностью, по меньшей мере, 1:4096.
7. Из инактивантов используют АЭЭИ.
8. АЭЭИ используют в виде 10% водного раствора.
9. АЭЭИ вносят в антигенный материал в концентрации 0,2-0,4%.
10. Инактивацию вируса ССЯ-76 птиц ведут в течение 48 часов при 37,0±0,5° С и рН 7,4-7,8.
11. Из масляных адъювантов используют масляный адъювант "Монтанид ИЗА-70".
12. Антигенный материал из штамма "БИСС № 113" вируса ССЯ-76 птиц соединяют с масляным адъювантом "Монтанид ИЗА-70" в соотношении, по меньшей мере, 3:7 - 2:3.
Признаками изобретения, характеризующими предлагаемую вакцину и совпадающими с признаками прототипа, в том числе родовое понятие, отражающее назначение, являются:
1. Способ изготовления инактивированной вакцины против ССЯ-76 птиц.
2. Получение антигенного материала из штамма гомологичного вируса, репродуцированного в чувствительной биологической системе.
3. Очистка антигенного материала от балластных примесей.
4. Инактивация вируса.
5. Соединение очищенного и авирулентного антигенного материала с масляным адъювантом.
6. Контроль целевого продукта.
По сравнению со способом-прототипом существенными отличительными признаками изобретения являются:
1. Из штаммов возбудителя инфекции используют штамм "БИСС № 113" вируса ССЯ-76 птиц.
2. Штамм "БИСС № 113" вируса ССЯ-76 птиц используют в эффективном количестве.
Предлагаемое изобретение характеризуется также другими отличительными признаками, выражающими конкретные формы выполнения или особые условия его использования:
1. Из чувствительных биологических систем используют 9-11-суточные УЭ.
2. Используют антигенный материал из штамма "БИСС № 113", репродуцированного в 9-11-суточных УЭ, с биологической активностью, по меньшей мере, 6,0 lg ЭИД50/0,2 см3.
3. Используют антигенный материал из штамма "БИСС № 113" гомологичного вируса, репродуцированного в 9-11-суточных УЭ, с ГА-активностью, по меньшей мере, 1:4096.
4. Из чувствительных биологических систем используют 9-11-суточные эмбрионы SPF-кур.
5. Используют антигенный материал из штамма "БИСС № 113" гомологичного вируса, репродуцированного в 9-11-суточных эмбрионах SPF-кур, с биологической активностью, по меньшей мере, 6,0 lg ЭИД50/0,2 см3.
6. Используют антигенный материал из штамма "БИСС № 113" гомологичного вируса, репродуцированного в 9-11-суточных эмбрионах SPF-кур, с ГА-активностью, по меньшей мере, 1:4096.
7. Из инактивантов используют АЭЭИ.
8. АЭЭИ используют в виде 10% водного раствора.
9. АЭЭИ вносят в антигенный материал в концентрации 0,2-0,4%.
10. Инактивацию вируса ССЯ-76 птиц ведут в течение 48 часов при 37,0±0,5° С и рН 7,4-7,8.
11. Из масляных адъювантов используют масляный адъювант "Монтанид ИЗА-70".
12. Антигенный материал из штамма "БИСС № 113" вируса ССЯ-76 птиц соединяют с масляным адъювантом "Монтанид ИЗА-70" в соотношении, по меньшей мере, 3:7 - 2:3.
Инактивированная вакцина, полученная предлагаемым способом, обладает более высокой антигенной и ГА-активностью и стабильностью по сравнению с вакциной-прототипом и позволяет расширить арсенал средств специфической профилактики ССЯ-76 птиц.
Достижение технического результата от использования предлагаемого способа объясняется тем, что при изготовлении инактивированной вакцины против ССЯ-76 птиц используют антигенный материал из нового штамма "БИСС № 113" гомологичного вируса, обладающего высокой антигенной и ГА-активностью и стабильностью в нативном виде и после инактивации и обеспечивающего получение высокоиммуногенного и безвредного препарата, создающего напряженный и длительный иммунитет у привитой птицы.
Дополнительный технический результат от использования предлагаемого способа достигается за счет того, что инактивацию вируса осуществляют АЭЭИ, что позволяет значительно снизить трудо- и энергозатраты на изготовление вакцины и повысить качество антигенного материала.
Дополнительный технический результат от использования предлагаемого изобретения в части повышения антигенной и ГА-активности целевого продукта достигается также за счет использования в его составе масляного адъюванта "Монтанид ИЗА-70".
Исходный вирус для получения штамма "БИСС" вируса ССЯ-76 птиц выделен из органов репродуктивной системы курицы с признаками острой формы ССЯ-76 в 1999 году в Ульяновской области. Производственный штамм "БИСС" вируса ССЯ-76 получен путем проведения 4-х последовательных пассажей на развивающихся УЭ.
Полученный штамм депонирован во Всероссийской государственной коллекции штаммов микроорганизмов, используемых в ветеринарии и животноводстве, Всероссийского научно-исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов (ВГНКИ) МСХ РФ 5 октября 2000 г. под регистрационным шифром "БИСС № 113-ДЕП".
Штамм "БИСС № 113" вируса ССЯ-76 обладает высокой биологической и антигенной активностью в нативном виде и после инактивации. Экспериментально подтверждена его возможность использования для приготовления инактивированной вакцины против ССЯ-76 птиц, создающей эффективную защиту кур против указанного возбудителя заболевания.
Штамм "БИСС № 113" вируса ССЯ-76 птиц характеризуется следующими признаками и свойствами.
Морфологические свойства
Штамм "БИСС № 113" вируса ССЯ-76 относится к семейству Adenoviridae, роду Aviadenovirus, к 3 серологической группе. При электронно-микроскопическом исследовании штамм "БИСС № 113" представлен вирионами икосаэдрической формы, которые лишены суперкапсидной оболочки и не содержат липидов. Диаметр нуклеокапсида 70± 8 нм.
Антигенные свойства
По своим антигенным свойствам штамм "БИСС № 113" относится к 3 серологической группе птичьих аденовирусов. Вирус стабильно нейтрализуется гомологичной антисывороткой. В перекрестной реакции торможение гемаглютинации (РТГА) со специфическими сыворотками к штаммам "В 8/78", ВГНКИ № 98 "Б-93" и "БИСС № 113" вируса ССЯ - 76 и гетерологичными сыворотками к парамиксовирусу - 1 (болезнь Ньюкасла) (ПМВ-1), ортомиксовирусам 5-7 серотипов, штамм "БИСС № 113" был идентифицирован как вирус, аналогичный эталонному "В 8/78" и известному отечественному ВГНКИ № 98 "Б-93" штаммам вируса ССЯ-76 и отнесен к аденовирусам птиц 3 серологической группы.
Через 14-21 сут после заражения 120-суточных кур отмечают появление вируснейтрализующих и гемагглютинирующих антител. Гемагглютинирующий титр штамма достигает 18,0-21,0 лог2. Пробы экстраэмбриональной жидкости (ЭЭЖ) после расплодки штамма на УЭ исследовали в реакции гемагглютинации (РГА). Исследуемые пробы ЭЭЖ имели ГА-активность в разведении 1:32768-1:262144.
Биотехнологические характеристики
Штамм "БИСС № 113" предназначен для изготовления инактивированной вакцины против ССЯ-76 птиц. Штамм хорошо размножается в 9-11-суточных УЭ, зараженных в аллантоисную полость. Инфекционная активность штамма через 120 час при температуре 37,0± 0,5° С достигает 6,75+0,31 lg ЭИД50/0,2 см3.
Штамм также культивируется в КЭ и первичной культуре клеток утиных фибробластов, вызывая цитопатическое действие (ЦПД). Результаты культивирования вируса ССЯ-76 штамма "БИСС № 113" представлены в таблице 1. Штамм является генетически стабильным и сохраняет свои свойства на протяжении 10 пассажей.
Гемагглютинирующие свойства
Штамм "БИСС № 113" обладает выраженными гемагглютинирующими свойствами. Агглютинирует эритроциты кур и уток, вызывая образование среднезернистой реакции гемагглютинации (РГА) с предельным титром 21,0 лог2.
Инфекционные свойства
К штамму "БИСС № 113" восприимчивы куры, утки и гуси при интратрахеальном, оральном и внутримышечном заражениях. Начиная с 14 сут после введения вируса 120-суточным цыплятам, отмечают появление депигментированных лишенных скорлупы яиц. В течение четырех недель процент яиц с мягкой скорлупой и бесскорлупных составляет около 30% и более.
Клинических признаков болезни при экспериментальном и естественном заражениях вирус не вызывает. Патолого-анатомические изменения не выражены и определяются только гистологически по изменениям в репродуктивных органах.
Хемо-генотаксономическая характеристика
Сердцевина вириона содержит двухцепочечную молекулу ДНК и два внутренних белка. Масса нуклеиновой кислоты достигает 17,3% массы вириона.
Основная масса белков вируса ССЯ-76 птиц сосредоточена в капсидной оболочке вириона. На долю сердцевинных белков приходится до 20% всех протеинов вируса. Сердцевинный белок "1" с молекулярной массой 46х103 г/моль легко отделяется от внутреннего нуклеотида, содержащего ДНК в комплексе с богатым аргинином сердцевинным белком "2".
Гексон, основание пептона и его нить (фибер) вируса "БИСС № 113" построены из полипептидов с молекулярными массами 120× 103, 70× 103, 62× 103 г/моль соответственно.
Белковые структуры вируса штамма "БИСС № 113" формируют несколько антигенов. В составе структурного вирусного антигена у них обнаружены типоспецифические, группоспецифические, подгруппоспецифические антигены нити пектона. В составе структурного вирусного антигена выявлено три основных компонента, обозначенных А, В и С. Антиген А структурно связан с гексоном, антиген В - с пептоном, антиген С - с нитями вириона (фибера). Связанный с гексоном компонент А содержит группоспецифический антиген (a) и типоспецифический антиген (ε ). Антигенный фактор, связанный с пептоном, назван антигеном β , а с нитью вириона (фибер) - γ .
С помощью ПЦР и секвенирования апмлифицированных участков генома установлено, что аллантоисная жидкость от зараженных штаммов "БИСС" УЭ содержала геном вируса ССЯ-76.
Нуклеотидная последовательность амплифицированного консервативного фрагмента гена гексона штамма "БИСС" имела полную гомологию с референтными штаммами вируса ССЯ-76.
Физические свойства
Масса вириона - 252× 103 г/моль. Плавучая плотность 1,32-1,35 г/мл в градиенте С3С1. Константа седиментации зрелого вириона составляет 8-10×10-13-9-10×10-13 с.
Устойчивость к внешним факторам
Штамм "БИСС № 113" стабилен при рН в пределах 6,0-9,0. Устойчив к жирорастворителям. Инактивирует при 56° С.
Дополнительные признаки и свойства
Антигенная активность - 100%.
Патогенность выражена.
Вирулентность выражена.
Контагиозность выражена.
Онкогенность выражена.
Онкогенность отсутствует.
Свободен от контаминации бактериальной и грибковой флоры, микоплазмами и гемагглютинирующими вирусами.
На основании полученных данных можно утверждать, что штамм "БИСС № 113" по антигенному и иммунологическому спектрам является оригинальным, в таксономическом отношении новым, ранее неизвестным изолятом вируса СС-76 птиц.
Проведенный заявителем анализ уровня техники, включающий поиск по патентным и научно-техническим источникам информации и выявление источников, содержащих сведения об аналогах предлагаемого изобретения, позволил установить, что заявитель не обнаружил источники, характеризующиеся признаками, тождественными (идентичными) всем существенным признакам предлагаемого изобретения. Определение из перечня выявленных аналогов прототипа как наиболее близкого по совокупности существенных признаков аналога позволило установить совокупность существенных по отношению к усматриваемому заявителем техническому результату отличительных признаков предлагаемого способа, изложенных в независимом пункте формулы изобретения.
Следовательно, заявляемое изобретение соответствует условию патентоспособности "новизна".
Для проверки соответствия предлагаемого решения условию патентоспособности "изобретательский уровень" проведен дополнительный поиск известных решений для выявления признаков, включенных в отличительную часть независимого пункта формулы изобретения. Результаты поиска показали, что предлагаемое решение не вытекает для специалиста явным образом из известного уровня техники, изложенного в соответствующем разделе описания (не выявлены решения, имеющие признаки, совпадающие с отличительными признаками предлагаемого изобретения), а также не выявлено влияния предусматриваемых существенными признаками предлагаемого изобретения преобразований для достижения технического результата.
Следовательно, предлагаемый способ соответствует условию патентоспособности "изобретательский уровень".
Сущность предлагаемого изобретения пояснена примерами его исполнения.
Пример 1.
Исходный вирус для получения штамма "БИСС № 113" выделен из органов репродуктивной системы курицы с признаками острой формы ССЯ-76 в 1999 году в Ульяновской области. Вакцинный штамм получен во ВНИИ защиты животных путем проведения последовательных пассажей на развивающихся УЭ 9-11-суточного возраста. Для получения вируса первого пассажа зараженные эмбрионы инкубировали в термостате в течение 120 час при температуре 37,0±0,5° С. Гибель эмбрионов в течение первых 24 час после введения вируса считали неспецифичной. Через 120 час инкубации все эмбрионы охлаждали при температуре 4-8° С в течение 12-18 час и вскрывали. ЭЭЖ из полости эмбриона отбирали пипеткой и собирали в стеклянные флаконы. Вируссодержащую жидкость подвергали низкоскоростному центрифугированию для освобождения от крупнодисперсных частиц. Осветленную суспензию использовали для последующего пассирования.
Полученный вирус был подвергнут всестороннему контролю в соответствии с руководством МЭБ по стандартным диагностическим методам и вакцинам (1996) и на уровне 4 пассажа заложен на хранение в качестве матровой расплодки. Вирус матровой расплодки с титром инфекционной активности 6,75± 0,31 lg ЭИД50/0,2 см3, представленный в виде вируссодержащей ЭЭЖ, хранят при температуре минус 40° С.
Полученному штамму вируса ССЯ-76 птиц присвоено авторское наименование "БИСС".
Пример 2.
Для изготовления инактивированной эмульсионной вакцины используют производственный штамм "БИСС № 113" вируса ССЯ-76, получаемый из ВГНКИ. Указанный штамм используют для получения матровой расплодки. Для этого 3 ампулы лиофилизированного вируса растворяют в 30 см3 стерильного 0,9% раствора хлорида натрия, содержащего 200 Eg/см3 стрептомицина. Приготовленным вирусом заражают 150 УЭ или эмбрионов SPF-кур 9-11-суточного возраста путем его введения в аллантоисную полость в объеме 0,2 см3. Зараженные эмбрионы инкубируют при температуре 37,4±0,5° С и относительной влажности 60-70% в течение 96-120 час. Каждые 24 час эмбрионы овоскопируют. Через 96-120 час после заражения и инкубации эмбрионы используют для получения вируса. Перед вскрытием эмбрионы охлаждают при 4-8° С в течение 12-24 час. После этого из них через прокол в хориоаллантоисной оболочке стерильной пипеткой отбирают вируссодержащую жидкость. Собранную жидкость центрифугируют при 1000 об/мин в течение 15 мин и сливают по 50-100 см3 в стерильные флаконы емкостью по 100-200 см3. В стерильных условиях из каждого флакона отбирают по 3-5 см3 жидкости для контроля стерильности и ГА-активности. Полученная матровая расплодка должна быть стерильной и иметь ГА-активность не ниже 1:4096. Матровую расплодку хранят в замороженном виде при температуре не выше минус 40° С.
Матровую расплодку используют для получения производственной расплодки вируса. Для этого флаконы с матровым вирусом размораживают в водяной бане при 18-20° С, содержимое флаконов очищают хлороформом и центрифугируют при 2500 об/мин в течение 20 мин. Надосадочную жидкость отбирают в стерильные флаконы. Активность вируса определяют в РГА и производят корректировку объема путем разведения 0,9% раствором хлорида натрия до активности 2048-4096 ГАЕ/0,2 см3. Подготовленный таким образом матровый вирус используют для получения производственной расплодки вируса.
Полученным вирусом заражают партию УЭ или эмбрионы SPF-кур в количестве, обеспечивающем изготовление планируемого объема серии вакцины. Зараженные эмбрионы инкубируют при температуре 37,0± 0,5° C и относительной влажности 60-70% в течение 96-120 час. Через 96-120 час после заражения эмбрионы охлаждают 4-8° С в течение 12-24 час, производят вскрытие зараженных эмбрионов и сбор вируссодержащего материала. Полученный вируссодержащий материал подвергают первичной очистке путем центрифугирования. Центрифугирование проводят в течение 7-10 мин при 1000 об/мин и температуре 2-6° С. При этом аллантоисную жидкость освобождают от осколков скорлупы, клеток и эритроцитов. Очищенную вируссодержащую ЭЭЖ сливают в стеклянные 20 дм3 стерильные бутыли. Полученную ЭЭЖ подвергают инактивации АЭЭИ. Для этого вируссодержащую ЭЭЖ нагревают в водяной бане до 37,0+0,5° С. При перемешивании в суспензию добавляют 10% раствор АЭЭИ до конечной концентрации 0,2-0,4%. Инактивацию ведут в течение 48 час после добавления инактиванта при 37,0+0,5° С и рН 7,4-7,8 с периодическим перемешиванием. По окончании инактивации бутыли с полученным антигеном охлаждают при 4-8° С в течение 2 сут, периодически перемешивая суспензию. Затем из каждой бутыли отбирают пробу в количестве 20 см3 для определения титра в РГА, контроля, авирулентности, стерильности и рН. Инактивированный антиген должен быть стерильным и авирулентным, иметь ГА-титр не менее 1:8192 и рН в пределах 7,4-7,8. Антиген хранят при 4-8° С. Полученный антиген подвергают дополнительной отчистке от балластных примесей на проточной ультрацентрифуге и фильтровальной установке с элементом ЭПРС. После этого антигенный материал соединяют с масляным адъювантом в соотношении 30:70-40-60 по весу. Перед составлением вакцины проводят корректировку объема инактивированного антигена по титру гемагглютининов. ГА-активность инактивированного антигена в РГА инактивированного антигена в РТГА должна быть не меньше 1:4096. Для изготовления эмульсионной вакцины можно использовать как отечественные, так и зарубежные масляные адъюванты. В данном случае используют масляный адъювант фирмы "Сеппик" (Франция) "Монтанид ИЗА-70".
Изготовление инактивированной эмульсионной вакцины проводят следующим образом: в реактор со стерильным масляным адъювантом при включенной мешалке (250-300 об/мин) подают необходимый объем инактивированного материала со скоростью 2-3 дм3/мин (стадия предэмульсии).
Затем предэмульсию пропускают через гомогенизатор в течение 3 часов, получая в результате стабильную эмульсию типа "вода-масло". Учитывая термолабильность вирусного антигена, процесс эмульгирования проводят при температуре 4-8° С. При получении эмульсии контролируют некоторые ее характеристики: тип эмульсии, стабильность, вязкость и другие свойства. Готовую вакцину разливают во флаконы объемом 200-450 см3, которые герметично укупоривают и закатывают алюминиевыми колпачками. Полученную вакцину контролируют по следующим показателям: по внешнему виду и цвету, наличию посторонней примеси и дефектов флаконов, стабильности эмульсии, определению относительной вязкости, плотности инактивации вакцины и ее антигенной активности.
По внешнему виду препарат представляет собой однородную эмульсию белого цвета. При хранении допускается отслоение масла в верхней части флакона. При встряхивании однородность эмульсии восстанавливается.
Полученная вакцина против ССЯ-76 птиц имеет оптимальный компонентный состав:
Антигенный материал 30,0-40,0
АЭЭИ (10% водный раствор) 0,2-0,4
Масляный адъювант До 100,0
Содержание антигена в вакцине в указанных выше пределах является его эффективным количеством в препарате, обеспечивающим достижение технического результата.
Полученная вакцина предназначена для профилактической иммунизации молодняка кур против ССЯ-76. Вакцинации подлежит клинически здоровая птица в возрасте 90-120 суток, но не позднее, чем за один месяц до начала яйцекладки. Вакцину в дозе 0,5 см3 вводят птице однократно подкожно в среднюю треть шеи, внутримышечно в область груди или жировую складку хвоста. Вакцина вызывает иммунитет к инфекции не менее чем у 80% вакцинированных цыплят, индуцируя накопление в сыворотке крови антител к вирусу ССЯ-76 в титре 5 лог2 и выше в РТГА или более двух минимальных значений в ИФА. Продолжительность поствакцинального иммунитета составляет не менее 12 месяцев.
Пример 3.
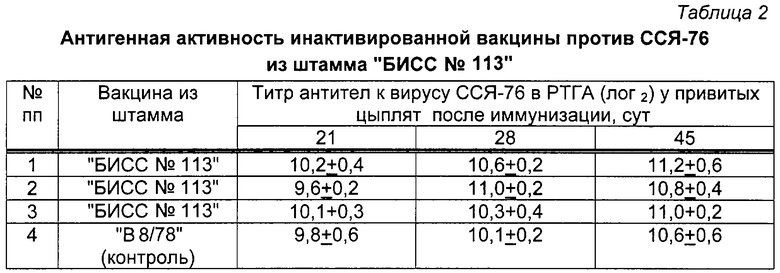
Описанным в примере 2 способом изготовлено 3 опытных образца инактивированной вакцины против ССЯ-76 птиц на основе штамма "БИСС № 113" и масляного адъюванта "Монтанид ИЗА-70". Инактивированный вирус ССЯ-76 перед компоновкой вакцины разводили 1:2 стерильным ФБР. В качестве контроля использовали образец серийной инактивированной вакцины против ССЯ-76, приготовленной из штамма "В 8/78". Все вакцины вводили цыплятам опытных и контрольных групп (в каждой группе по 20 голов). Результаты исследований по определению антигенной активности препаратов представлены в таблице 2.
Из данных таблицы 2 видно, что все три образца инактивированной вакцины против ССЯ-76, приготовленные из штамма "БИСС № 113", индуцировали у привитых цыплят образование антител к вирусу ССЯ-76 в высоких титрах. Вакцина из штамма "В 8/78" вызывала у иммунизированных цыплят образование антител к вирусу ССЯ-76 в титрах аналогичного уровня.
Пример 4.
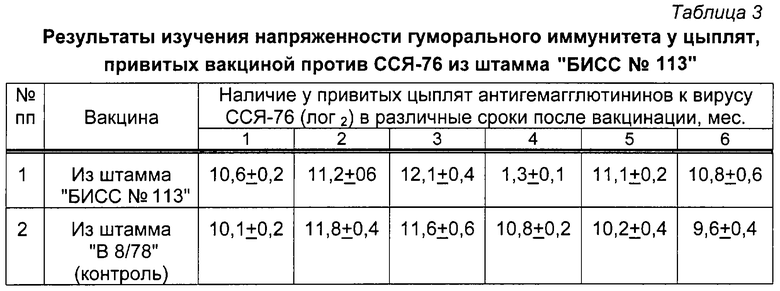
Описанным в примере 2 способом изготовлена инактивированная вакцина против ССЯ-76 птиц на основе штамма "БИСС № 113" и масляного адъюванта "Монтанид ИЗА-70". Проведены исследования по изучению напряженности и длительности иммунитета, создаваемого полученной вакциной. Для этого, начиная с 30 по 120 сут после прививки птицы данной вакциной, с периодичностью 1 раз в месяц оценивали напряженность гуморального иммунитета в РТГА. Полученные результаты представлены в таблице 3.
Согласно представленным в таблице 3 данным следует, что в интервале от 1 до 6 месяцев вакцинированная птица обеих групп имела антитела к вирусу ССЯ-76 в высоких титрах. Существенных различий в уровне поствакцинального иммунитета, вызванного вакцинами из штаммов "БИСС № 113" и "В 8/78", не было установлено. Полученные данные позволили сделать заключение, что однократная вакцинация цыплят инактивированным препаратом из штамма "БИСС № 113" в дозе 0,5 см3 обеспечивала формирование напряженного уровня антител к вирусу ССЯ-76 в течение всего срока исследования.
Пример 5.
Проведена сравнительная оценка антигенной активности инактивированной вакцины против ССЯ-76 птиц на основе штамма "БИСС № 113" и инактивированной вакцины против ССЯ-76 на основе штамма "В 8/78". Вакцины готовили с масляным адъювантом "Монтанид ИЗА-70" в соотношении адъюванта с антигеном 7:3 по весу. Антигены разводили предварительно фосфатно-буферным раствором (ФБР) в соотношении 1:3.
Активность цельного антигена в РГА была следующей:
штамм "БИСС" - 21 лог2;
штамм "В 8/78" (образец № 9) - 19 лог2;
штамм "В 8/78" (образец № 11) - 19 лог2;
штамм "В 8/78" (образец № 16) - 19 лог2;
штамм "В 8/78" (образец № 17) - 19 лог2.
Вакцины эмульгировали в течение 3 мин при 3000 об/мин.
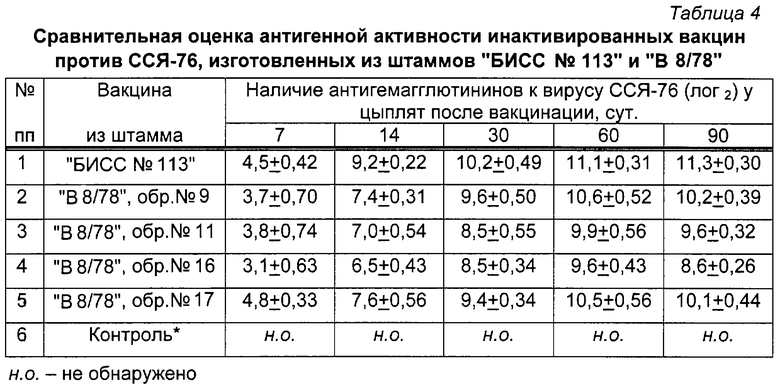
Вакцины проверяли на антигенную активность, прививая птиц в возрасте 100 сут внутримышечно в дозе 0,5 см3, а при проверке безвредности вакцины вводили в дозе 1,5 см3 и птиц выдерживали в течение 10-12 сут. Все вакцины не вызывали никаких отклонений у птицы как в поведении, так и в местах введения препаратов. Сыворотки крови отбирали через 7, 11, 30, 60 и 90 сут после вакцинации и исследовали в РТГА, а результаты выражали в лог2. Результаты исследований приведены в таблице 4.
Согласно данным таблицы 4 следует, что наиболее высокой антигенной активностью обладают вакцина из штамма "БИСС № 113" и образцы № 9 и № 17 вакцины из штамма "В 8/78".
Пример 6.
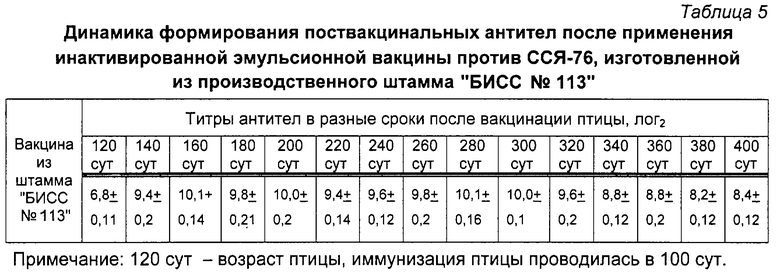
Описанным в примере 2 способом изготовлена инактивированная вакцина против ССЯ-76 птиц. Проведены исследования на предмет определения динамики формирования поствакцинальных антител у птицы, привитой полученным препаратом. Результаты исследований приведены в таблице 5.
Пример 7.
Описанным в примере 2 способом изготовлена инактивированная вакцина против ССЯ-76 птиц. Проведены исследования по оценке антигенной активности полученного препарата. Результаты исследований приведены в таблице 6.
Таким образом, приведенная выше информация свидетельствует о выполнении при использовании предлагаемого изобретения следующей совокупности условий:
- способ изготовления вакцины против ССЯ-76 птиц, воплощающий предлагаемое изобретение, предназначен для использования в сельском хозяйстве, а именно в ветеринарной вирусологии и биотехнологии;
- для предлагаемого изобретения в том виде, как оно охарактеризовано в независимом пункте формулы изобретения, подтверждена возможность его осуществления с помощью описанных в заявке или известных до даты приоритета средств и методов;
- при использовании предлагаемого способа достигнут технический результат, заключающийся в повышении антигенной и ГА-активности и стабильности препарата и расширении арсенала средств профилактики ССЯ-76 птиц, обеспечивающих напряженный и длительный иммунитет у привитой птицы.
Следовательно, предлагаемое изобретение соответствует условию патентоспособности "промышленная применимость".
Источники информации
1. Сюрин В.Н. и др. Вирусные болезни животных. - М.: ВНИТИБП, 1998, 846-870.
2. Пат. Франции № 2382500; С 12 К 5/00, А 61 К 39/32; 29.09.78.
3. Baxendale J., Lutticken D. and al. The results of field trials conducted with an inactivated vaccine against the Egg Drop Syndrome-76 (EDS-76). Avian Pathology, 1980, V.9, № 1, 77-91.
4. Пат. РФ № 1809836, С 12 N 7/00, А 61 К 39/00; 15.04.93.
5. Пат. РФ № 2097066, А 61 К 39/12, С 12 N 7/00, А 61 К 39/235; 27.11.97.
6. Пат. РФ № 2155030, А 61 К 9/127, 39/00, 39/235; 27.08.2000.
7. Пат. РФ № 2183968, А 61 К 39/12; 26.06.2002 (прототип).


| название | год | авторы | номер документа |
|---|---|---|---|
| ИНАКТИВИРОВАННАЯ ВАКЦИНА ПРОТИВ СИНДРОМА СНИЖЕНИЯ ЯЙЦЕНОСКОСТИ-76 ПТИЦ | 2003 |
|
RU2233671C1 |
| ВАКЦИНА АССОЦИИРОВАННАЯ ПРОТИВ НЬЮКАСЛСКОЙ БОЛЕЗНИ ПТИЦ, ИНФЕКЦИОННОГО БРОНХИТА КУР, СИНДРОМА СНИЖЕНИЯ ЯЙЦЕНОСКОСТИ-76, ИНФЕКЦИОННОЙ БУРСАЛЬНОЙ БОЛЕЗНИ И РЕОВИРУСНОГО ТЕНОСИНОВИТА ПТИЦ ИНАКТИВИРОВАННАЯ ЭМУЛЬСИОННАЯ | 2010 |
|
RU2443429C2 |
| ШТАММ "БИСС № 113" ВИРУСА СИНДРОМА СНИЖЕНИЯ ЯЙЦЕНОСКОСТИ - 76 ПТИЦ ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИННЫХ ПРЕПАРАТОВ | 2002 |
|
RU2221865C1 |
| ИНАКТИВИРОВАННАЯ ЭМУЛЬСИОННАЯ ВАКЦИНА ПРОТИВ СИНДРОМА ГИДРОПЕРИКАРДИТА КУР | 2002 |
|
RU2216351C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ИНАКТИВИРОВАННОЙ ЭМУЛЬСИОННОЙ ВАКЦИНЫ ПРОТИВ СИНДРОМА ГИДРОПЕРИКАРДИТА КУР | 2002 |
|
RU2213576C1 |
| ИНАКТИВИРОВАННАЯ ЭМУЛЬСИОННАЯ ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОГО ЛАРИНГОТРАХЕИТА ПТИЦ | 2003 |
|
RU2257225C1 |
| ВАКЦИНА ПРОТИВ ГРИППА ПТИЦ ИНАКТИВИРОВАННАЯ ЭМУЛЬСИОННАЯ | 2006 |
|
RU2323741C2 |
| ИНАКТИВИРОВАННАЯ СОРБИРОВАННАЯ ВАКЦИНА ПРОТИВ ИНФЕКЦИОННОГО ЛАРИНГОТРАХЕИТА ПТИЦ | 2003 |
|
RU2259845C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ИНАКТИВИРОВАННОЙ ЭМУЛЬГИРОВАННОЙ ВАКЦИНЫ ПРОТИВ ГРИППА ПТИЦ И ВАКЦИНА ИНАКТИВИРОВАННАЯ ЭМУЛЬГИРОВАННАЯ ПРОТИВ ГРИППА ПТИЦ | 2008 |
|
RU2358760C1 |
| ВАКЦИНА АССОЦИИРОВАННАЯ ПРОТИВ НЬЮКАСЛСКОЙ БОЛЕЗНИ, РЕОВИРУСНОГО ТЕНОСИНОВИТА И МЕТАПНЕВМОВИРУСНОЙ ИНФЕКЦИИ ПТИЦ ИНАКТИВИРОВАННАЯ ЭМУЛЬСИОННАЯ | 2011 |
|
RU2480238C1 |
Изобретение относится к ветеринарной вирусологии и биотехнологии. Способ включает получение антигенного материала из штамма “БИСС № 113-ДЕП” (коллекция ВГНКИ) вируса ССЯ-76 птиц, репродуцированного в 9-11-суточных утиных эмбрионах (УЭ) или эмбрионах SPF-кур, с биологической активностью, по меньшей мере, 6,0 lg ЭИД50/0,2 см3 и гемагглютинирующей активностью, по меньшей мере, 1:4096. Полученный вирус очищают от балластных примесей известным образом. Затем в вируссодержащую суспензию вносят аминоэтилэтиленимин (АЭЭИ) в концентрации 0,2-0,4% для инактивации вируса. Очищенный и авирулентный антигенный материал соединяют с масляным адъювантом в эффективном соотношении. Готовый препарат подвергают контролю в соответствии с требованиями ТУ. Вакцина обладает высокой антигенной и гемагглютирующей активностью, стабильна, обеспечивает напряженный и длительный иммунитет у привитой птицы. 12 з.п. ф-лы, 6 табл.
| RU 2183968 C1, 26.06.2002.RU 2097066 C1, 27.11.1997.FR 2382500 A, 29.09.1978. |
Авторы
Даты
2004-11-10—Публикация
2003-01-04—Подача