Изобретение относится к медицине, а именно к лечению тканей бронхиальной раны у больных с различными заболеваниями бронхолегочной системы, перенесших реконструктивно-пластические операции на трахее и бронхах.
Реконструктивно-пластические операции на трахее и бронхах остаются одним из наиболее актуальных разделов легочной хирургии, поскольку позволяют максимально сохранить легочную ткань и восстановить просвет воздухоносных путей. Несмотря на высокую потребность в этих операциях, отношение к ним остается сдержанным из-за значительного числа послеоперационных осложнений. Все имеющиеся способы формирования межбронхиальных анастомозов не лишены недостатков, и после операций у части больных развивается ряд серьезных осложнений (несостоятельность швов, стенозирование, разрастание грануляций, образование бронхоартериальных свищей). Как известно, наиболее грозным осложнением здесь является несостоятельность трахеобронхиальных швов, которая при гнойно-деструктивных заболеваниях легких достигает 50%. В связи с этим проблема поиска эффективных мер профилактики и лечения этого осложнения является чрезвычайно актуальной. Известно, что при благоприятных условиях заживление межбронхиального анастомоза протекает по типу первичного натяжения, в неблагоприятных же ситуациях анастомоз заживает вторичным натяжением, что обуславливает присоединение осложнений, а иногда и гибель больного.
Известно использование лазерного излучения различной мощности в медицине. Это так называемая фотодинамическая терапия, применяющаяся в неврологии, кардиологии, урологии, пульмонологии, хирургии, гастроэнтерологии и основанная на антибактериальном, противовоспалительном и стимулирующем эффектах лазерного излучения (см., например, патент RU №2112569, МПК A 61 N 5/06).
Однако использование лазерного воздействия для лечения тканей бронхиальной раны после реконструктивно-пластических операций в легочной хирургии для профилактики послеоперационных осложнений неизвестно, как не известен и механизм такого воздействия.
Известны способы лечения тканей ран медикаментозным воздействием антибиотиками ("Раны и раневая инфекция"./Под ред. М.И.Кузина и др. - М.: Медицина, 1981, 416).
Известны способы лечения тканей бронхиальной раны у больных, перенесших реконструктивно-пластические операций на трахеобронхиальном дереве бронхолегочной системы, при которых проводят медикаментозное воздействие, например санацию трахеобронхиального дерева при проведении торакальных операций (патент RU №2145883, МПК А 61 В 17/00). Однако, как показывает практика применения таких способов, в большинстве случаев не происходит заживления бронхиального шва первичным натяжением, а как указывалось выше, известные способы лечения тканей бронхиальной раны направлены на достижение именно такого заживления. В ряде случаев в результате проведенного лечения происходит вторичное заживление бронхиального шва, что приводит к различным осложнениям.
Наиболее близким по технической сущности и достигаемому результату является способ лечения тканей бронхиальной раны у больных с различными заболеваниями бронхолегочной системы после пластических операций на трахее и бронхах, который решает задачу проведения лечения, исключающего несостоятельность швов, путем медикаментозного воздействия на ткани бронхиальной раны, а именно введением гепарина и орошением линии швов контрикалом в течение 5-7 дней после операции (см. патент RU №2065290, МПК А 61 В 17/00).
Однако этот способ в ряде случаев также неэффективен и не позволяет значительно ускорить лечение.
Заявляемое изобретение решает задачу создания способа лечения тканей бронхиальной раны у больных с различными заболеваниями бронхолегочной системы после пластических операций на трахее и бронхах, позволяющего ускорить заживление бронхиального шва.
Техническим результатом заявляемого изобретения является ускорение заживления тканей бронхиальной раны, уменьшение послеоперационных осложнений путем нормализации содержания гистамина и ДНК в тканях бронхиальной раны и, как следствие, ускорения течения репаративных процессов.
Этот технический результат достигается тем, что при лечении тканей бронхиальной раны после реконструктивно-пластических операций на трахеобронхиальном дереве путем медикаментозного воздействия на ткани бронхиальной раны в качестве медикаментозного средства используют антибиотики, после операции дополнительно на область раны воздействуют 4-5 раз лазерным излучением длиной волны 0,63 мкм и мощностью на выходе световода 3 мВт в течение 3 минут, причем первое лазерное воздействие осуществляют во время операции после наложения швов, второе в 1-й день после операции, а интервал между каждыми последующими лазерными воздействиями равен количеству дней, выбранным в возрастающем порядке из ряда нечетных последовательных чисел, начинающегося с единицы.
В результате использования заявляемого способа происходит полное заживление бронхиального шва первичным натяжением, при этом также нормализуется содержание гистамина и ДНК в тканях бронхиальной раны, что способствует ускорению течения репаративных процессов и обеспечивает надежную профилактику послеоперационных осложнений.
Использование заявляемого способа и его преимущества иллюстрируются проведенными исследованиями. Под наблюдением находился 31 больной в возрасте от 17 до 69 лет с заболеваниями бронхолегочной системы, которым были произведены реконструктивно-пластические операции на трахеобронхиальном дереве (средний возраст пациентов составил 44,6±2,4 лет). Из них мужчин было 43 (70,5%) и 18 (29,5%) женщин. На ткани бронхиальной раны после реконструктивно-пластических операций на трахеобронхиальном дереве воздействовали введением антибиотиков в соответствии с общепринятыми методиками, а также 4-5 раз лазерным излучением длиной волны 0,63 мкм и мощностью на выходе световода 3 мВт в течение 3 минут, причем первое лазерное воздействие осуществляли во время операции после наложения швов, второе в 1-й день после операции, а интервал между каждыми последующими лазерными воздействиями равен количеству дней, выбранным в возрастающем порядке из ряда нечетных последовательных чисел, начинающегося с единицы, то есть на 3-й, 7-й день. По показаниям облучение могло проводиться также на 13-й день после операции.
В качестве источника излучения использовали отечественный гелий-неоновый лазер ЛГ-75 с длиной волны 0,63 мкм и мощностью на выходе световода 3 мВт. Лазерное воздействие осуществляли через рабочий канал эндоскопа фирмы “Olympus” во время операции после наложения швов и на 1-, 3-, 7- и 13-й дни послеоперационного периода в течение 3 минут.
Контроль за эффективностью лечебных мероприятий осуществляли по клиническим данным, фибробронхоскопическим исследованиям, а также при помощи гистологических и гистохимических методик.
Фибробронхоскопия применялась для контроля за состоянием слизистой оболочки бронха в области раны. Исследования проводили на эндоскопе фирмы “Olympus” по общепринятой методике.
Люминесцентно-гистохимическим методом Кросса исследовали содержание гистамина в тканях. Количественно концентрацию гистамина в структурах слизистой оболочки бронхов оценивали с помощью цитоспектрофлуориметрии, осуществляемой на люминесцентном микроскопе с применением микрофлуориметрической насадки ФМЭЛ. Наблюдение велось на вольтметре при напряжении 800 вольт с зондом 0,5 мм.
Окраску акридиновым оранжевым для количественных исследований ДНК проводили по Р.Риглер (1966 г.) модификации П.Н.Карнауховой (1985 г.). Депарафинированные срезы фиксировали в растворе Карнуа. После фосфатно-цитратного буфера с рН 4,2 их окрашивали в растворе акридинового оранжевого. После заключения в парафин срезы рассматривали под люминесцентным микроскопом с длиной возбуждающего света 435 нм (светофильтры ФС, СЗС, БС) и запирающими светофильтрами ЖС-18-0,5, фильтры 8, 9 и 15.
Окраска гематоксилин-эозином по Р.Ромейс использовалась для оценки глубины поврежденных тканей и заживления в послеоперационном периоде. Окраску по Ван-Гизону применяли для определения степени пораженности эластических элементов в слизистой и подслизистой оболочках бронхиального шва.
Концентрация гистамина и интенсивность люминесценции ДНК в тканевых структурах выражались в условных единицах согласно показаниям цифрового вольтметра. Полученные цифровые данные обрабатывались статистически по специально разработанной программе “Статистика” на компьютере IBM совместимом - Pentium 166 ММХ Microsoft office (Word и Excel). Статистическую достоверность полученных данных определяли по критерию Стьюдента.
Послеоперационный период у больных, получавших лечение в соответствии с заявленным способом, протекал достаточно легко, кашель с мокротой наблюдались редко, как и субфебрилитет, слабость. Бронхообструктивный синдром был кратковременным (1-3 дня) и незначительным, быстрее стабилизировались анализы крови. Нормализация общего состояния отмечалась уже через 7-10 дней. Осложнения возникли у 1 больного (3,3%) в виде пневмонии.
При исследовании бронхоскопической картины линии бронхиального шва в 1-е сутки послеоперационного периода отек слизистой был менее выраженным, хотя наблюдались гиперемия и наложения фибрина.
На 3-и сутки после операции отек слизистой был незначительным, фибрин встречался местами тонким слоем, четко прослеживалась линия анастомоза.
На 7-е сутки послеоперационного периода бронхоскопически в области линии шва наблюдалась незначительная гиперемия слизистой, отсутствие фибрина, слегка выделялась линия шва.
К 13-м суткам отмечалось полное восстановление слизистой, линия шва не определялась.
Таким образом, при сопоставлении данных способа-прототипа и заявляемого способа можно сделать вывод о том, что макроскопический процесс заживления бронхиальной раны в способе-прототипе завершался в основном к 13 дню, тогда как после эндобронхиального лазерного воздействия практически полное заживление бронхиального шва наблюдалось уже на 7-е сутки послеоперационного периода.
Гистологическая картина тканей бронхиального шва в 3-, 7- и 13-й дни послеоперационного периода соответствовала макроскопическим изменениям.
Динамика содержания гистамина в тканевых структурах бронхиального шва у больных приведена в таблице 1.
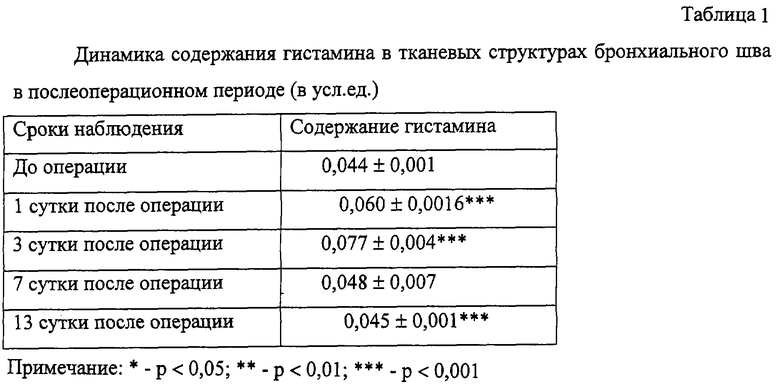
После эндобронхиальной лазеротерапии во время операции и в послеоперационном периоде содержание гистамина в тканях бронхиального шва увеличилось в 1-е сутки на 40% и составило 0,060±0,002 усл.ед. Наибольшее количество этого амина также отмечалось в эпителии, в собственной же пластинке слизистой оно было неравномерным.
К 3-м суткам после операции уровень гистамина увеличивался во всех структурах раневой поверхности на 75% по сравнению с исходными значениями и соответствовал 0,077±0,004 усл.ед. Увеличение содержания этого амина, очевидно, было связано с постепенным нарастанием острого воспалительного процесса.
К 7-м суткам его содержание возвращалось к дооперационному уровню во всех структурах слизистой оболочки (0,048±0,007 усл.ед.) и к 13-м суткам сохранялось на том же уровне (0,045±0,001 усл.ед.). Установлено, что гистамин способствует повышению проницаемости сосудов, увеличивая перфорированность базальной мембраны и фенестрированность эпителия. В этой ситуации остающиеся около раны тканевые структуры и остатки веществ попадали в кровь и через нее выводились из организма. Кроме того, гистамин принимает участие в реакции “антиген-антитело”, способствуя дифференцировке Т-лимфоцитов, доводя их до плазмоцитов. На остатках тканей в области операционной раны концентрировались плазмоциты и соответствующие антитела, которые связывались с антигенами. Эти комплексы поступали в кровь и через нее выводились из организма. Происходило очищение бронхиальной раны. После очищения раны воспалительная реакция затихала, уровень гистамина снижался. Процесс заживления у этих больных мы наблюдали уже на 7-е сутки.
Данные исследования гистамина позволяют сделать вывод о том, что использование заявленного способа приводит к быстрому очищению бронхиальной раны и сдерживает иммуннологические процессы, гармонизируя содержание гистамина в тканях.
Изменения интенсивности люминесценции ДНК в тканях бронхиальной раны отражены в таблице 2.
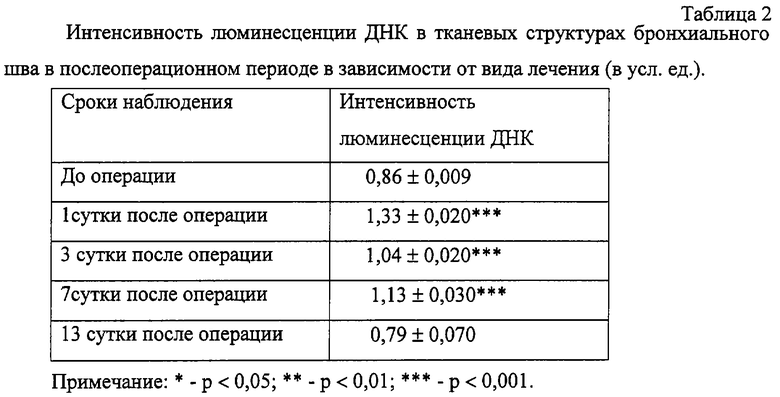
Интенсивность люминесценции ДНК в структурах слизистой оболочки бронхиального шва в 1-е сутки увеличивалась на 55% в сравнении с дооперационным уровнем и составляла 1,33±0,020 усл.ед. Наибольшее содержание этого вещества наблюдалось в эпителии. В собственной пластинке слизистой оболочки люминесценция ДНК возрастала только в областях шва. На 3-е сутки степень люминесценции ее во всех структурах раневой поверхности уменьшилась до 1,04±0,020 усл.ед., хотя и превышала исходные значения (0,86±0,009 усл.ед.). К 7-м суткам люминесценция ДНК вновь увеличивалась до 1,13±0,030 усл.ед., а к 13-му дню снижалась до уровня дооперационных значений и составляла 0,79±0,020 усл.ед.
В проведенных исследованиях было обнаружено, что после лазерного воздействия в тканях бронхиальной раны разрушения ДНК не наблюдалось, синтез белков шел более интенсивно, в то время как без лазерного воздействия, в результате затягивания воспалительного процесса, как правило, отмечается нарушение этого синтеза.
Таким образом, установлено, что использование заявляемого способа снижает интенсивность воспалительной реакции тканей, улучшает микроциркуляцию в зоне повреждения, стимулирует репаративно-регенераторные процессы и, тем самым, препятствует формированию в зоне повреждения грубого рубца и развитию послеоперационных осложнений.
Заявляемый способ лечения способствует нормализации содержания гистамина в тканях бронхиального шва без увеличения числа лимфоцитов и полиморфноядерных нейтрофилов, нормализует синтез ДНК в тканях бронхиальной раны, ускоряя процессы репарации, обеспечивая полное заживление бронхиального шва первичным натяжением уже к 7-м суткам после хирургического вмешательства, снижая количество послеоперационных осложнений в 3 раза.
Эффективность предложенных разработок иллюстрируется также следующими клиническими примерами.
Пример 1. Выписка из истории болезни больного Ц., 54 лет. Поступил в хирургическое торакальное отделение РКБ №1 с жалобами на кашель с мокротой, содержащей примесь свежей крови, боли в нижних отделах левой половины грудной клетки сзади, повышение температуры, общую слабость, потливость. Считает себя больным в течение 15-20 лет с тех пор, как перенес двухстороннюю пневмонию. Обострения были частыми, после легкого переохлаждения. Неоднократно госпитализировался в терапевтический стационар, получал антибактериальное и симптоматическое лечение. В последние 2-3 года отмечает появление прожилок крови в мокроте. Данное ухудшение состояния около недели связывает с переохлаждением. Кровохарканье - второй день.
При осмотре - состояние средней тяжести. Кожные покровы бледноваты. Грудная клетка правильной формы, обе половины симметричны в дыхании. ЧДД 28 в минуту. Перкуторный звук легочный, дыхание везикулярное. Область сердца не изменена, границы относительной сердечной тупости в пределах нормы. Тоны сердца приглушены, ритмичны. Пульс 70 в минуту. АД - 160/100 мм рт.ст. Живот мягкий, безболезненный. Печень выступает из-под края реберной дуги на 1-2 см, эластической консистенции. Селезенка не пальпируется. Область почек не изменена, симптом Пастернацкого отрицательный с обеих сторон. Физиологические отправления в норме.
В анализе крови от 30.08 - умеренный лейкоцитоз. Анализ мочи без особенностей. ВК и атипичные клетки в мокроте не обнаружены. В коагулограмме - умеренная гиперкоагуляция. Сахар крови, биохимические анализы, белковые фракции крови без изменений.
Спирограмма от 01.09: Легкие нарушения вентиляции обструктивного типа.
Кинетокардиограмма от 01.09: Легочная гипертензия 1 степени.
ЭКГ от 01.09 без особенностей
Фибробронхоскопия от 06.09: При осмотре ТБД обнаружено наличие серой густой мокроты в нижней доле правого легкого, деформация нижнедолевого бронха справа. Слева на шпоре верхнедолевого бронха обнаружено наличие “плюс”-ткани.
Клинический диагноз: Опухоль верхнедолевого бронха слева. Гипертоническая болезнь.
Произведена операция резекции верхней доли слева с клиновидной резекцией бронха. Наложен межбронхиальный анастомоз, который облучен лазером в течение 3 минут. При гистологическом исследовании макропрепарата верифицирована гроздьевидная гемангиома.
Течение послеоперационного периода гладкое: в течение 7 дней сохранялись субфебрильная температура, кашель с небольшим количеством мокроты с примесью крови, общая слабость, боли в области послеоперационной раны. Заживление операционной раны первичным натяжением.
При бронхоскопии в 1-е сутки в правом бронхиальном дереве определялся гнойный секрет, слева по линии анастомоза выраженная отечность и яркая гиперемия слизистой, линия анастомоза через световод, проведенный через рабочий канал бронхоскопа, облучена лазером в течение 3 минут. На 3-й день в правом бронхиальном дереве имелось умеренное количество слизисто-гнойной мокроты, слева по линии анастомоза определялось наличие фибрина (типа валика) желтоватого цвета. Отек анастомоза был незначительным. Произведено удаление мокроты и фибрина, после чего линия анастомоза через световод, проведенный через рабочий канал бронхоскопа, облучена лазером в течение 3 минут. На 7-е сутки в правом бронхиальном дереве незначительное количество мокроты. Слева анастомоз проходим, отечности нет, линия анастомоза прослеживается, в просвет бронха не выступает. Сегментарные бронхи без особенностей. Бронхи промыты раствором канамицина. Анастомоз облучен лазером 3 мин. На 13-й день также было проведено облучение лазером 3 мин.
В послеоперационном периоде больной получал ристомицин. Выписан на 14-й день после операции в удовлетворительном состоянии.
При контрольной явке через 1,5 месяца изменений в области анастомоза не выявлено. Все последующие годы продолжал работать на прежнем месте, легочных кровотечений не наблюдалось. Как видно из приведенной истории болезни, больному Ц. была произведена резекция верхней доли слева с клиновидной резекцией бронха по поводу доброкачественной опухоли бронха. В послеоперационном периоде кроме традиционной терапии ему осуществляли воздействие низкоинтенсивным гелий-неоновым лазером с длиной волны 0,63 мкм и мощностью на выходе световода 3 мВт в течение 3 минут (4 сеанса). Заживление бронхиального шва наблюдалось уже на 7-е сутки после операции.
Пример 2. Больной М., 57 лет, находился на лечении в хирургическом торакальном отделении Республиканской клинической больницы №МЗ ЧР по поводу туберкулезного цирроза верхней и средней долей правого легкого с мелкими кавернами.
Кашель беспокоит более 20 лет (курильщик). В течение месяца наблюдаются повышение температуры до 38-38,5°С, слабость, одышка, усиление кашля. При рентгенологическом исследовании выявлено уменьшение объема правого легкого, наличие запавшей верхушки и сужение межреберных промежутков в верхних отделах, смещение органов средостения вправо. Кроме того, определялось негомогенное затемнение верхней и средней долей с участками просветления, присутствие дополнительной тени в правом корне.
Произведена операция верхняя билобэктомия справа. С целью сохранения нижней доли произведено наложение межбронхиального анастомоза. Перед наложением последних швов анастомоз облучен лазером. Нижняя доля включена в вентиляцию, воздушна. Анастомоз герметичен. Плевральная полость промыта раствором фурацилина, введен 1,0 г канамицина. Дренирование плевральной полости в 3 и 7 межреберьях. Рана послойно ушита.
График лазерного воздействия:
1) на операционном столе непосредственно после выполнения операции;
2) на 1-е сутки послеоперационного периода;
3) на 3-и сутки послеоперационного периодa;
4) на 7-е сутки послеоперационного периода;
5) на 13-е сутки послеоперационного периода.
Послеоперационный период без осложнений. Заживление первичное. Выписан в удовлетворительном состоянии на 17-й день после операции.
Пример 3. Больная П., 25 лет, и/б №133/11, находилась на лечении в хирургическом торакальном отделении Республиканской клинической больницы №1 МЗ ЧР по поводу гиноплазии нижней доли левого легкого с нагноившимися бронхоэктазами. Больна более 10 лет. Заболевание связывает с перенесенной пневмонией, беспокоит постоянный кашель, усиливающийся при малейшем переохлаждении. При бронхографическом исследовании слева в бронхах базальных сегментов выявлены мешотчатые и цилиндрические бронхоэктазы. Направлена на хирургическое лечение.
Произведена операция резекция нижней доли левого легкого (безкультевым методом). Часть нижнедолевого бронха освобождена от гипертрофированных лимфатических узлов до отхождения язычкового бронха. Произведено иссечение стенок нижнедолевого бронха до бронха язычковых сегментов. Из просвета удалено большое количество вязкой мокроты. Наложены капроновые швы между хрящевой и мембранозной частями бронха, легкое включено в вентиляцию. Плевральная полость промыта фурациллином. При наложении швов произведено облучение тканей лазером в течение 3 минут. Выполнено дренирование плевральной полости в 7-м межреберье. Рана послойно ушита.
График последующего лазерного воздействия:
на 1-е сутки послеоперационного периода;
на 3-и сутки послеоперационного периода;
на 7-е сутки послеоперационного периода;
на 13-е сутки послеоперационного периода.
Послеоперационный период без осложнений. Рана зажила первичным натяжением.
Выписана из отделения в удовлетворительном состоянии на 16-й день после операции.
Приведенные клинические примеры наглядно демонстрируют преимущество заявленного способа перед известными способами и способом-прототипом. При использовании заявленного способа выздоровление наступает, как правило, на 14-16-е сутки, а в тяжелых случаях - на 17-е сутки, в то время как при использовании способа-прототипа только на 19-20-е.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ БРОНХОМИОПЛАСТИКИ ПОСЛЕ БЕСКУЛЬТЕВОЙ ОБРАБОТКИ ПРАВОГО ГЛАВНОГО БРОНХА | 2018 |
|
RU2692989C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ РУБЦОВЫХ СТЕНОЗОВ ГОРТАНИ И ТРАХЕИ | 2009 |
|
RU2388477C1 |
| СПОСОБ НАЛОЖЕНИЯ БРОНХИАЛЬНОГО АНАСТОМОЗА | 1999 |
|
RU2189787C2 |
| Способ соединения трахеи с бронхом | 1982 |
|
SU1114401A1 |
| СПОСОБ ОБРАБОТКИ КУЛЬТИ ГЛАВНОГО БРОНХА | 2004 |
|
RU2271155C2 |
| ИНДИКАТОРНОЕ СРЕДСТВО И СПОСОБ КОНТРОЛЯ ПНЕВМОСТАЗА В ТОРАКАЛЬНОЙ ХИРУРГИИ | 2011 |
|
RU2489971C2 |
| СПОСОБ ЛЕЧЕНИЯ АТРЕЗИИ ПИЩЕВОДА | 2000 |
|
RU2199958C2 |
| СПОСОБ ЗАКРЫТИЯ КУЛЬТИ БРОНХА | 1993 |
|
RU2045934C1 |
| СПОСОБ НАЛОЖЕНИЯ ТРАХЕО-БРОНХИАЛЬНОГО И МЕЖБРОНХИАЛЬНОГО АНАСТОМОЗОВ | 1994 |
|
RU2112437C1 |
| Способ хирургического лечения ранней несостоятельности короткой культи бронха | 2020 |
|
RU2758678C1 |
Изобретение относится к медицине и предназначено для лечения тканей бронхиальной раны у больных с различными заболеваниями бронхолегочной системы, перенесших реконструктивно-пластические операции на трахее и бронхах. Больным вводят антибиотики и дополнительно на область раны воздействуют 4-5 раз лазерным излучением длиной волны 0,63 мкм и мощностью на выходе световода 3 мВт. Время облучения 3 мин. Первое лазерное воздействие осуществляют во время операции после наложения швов, второе - в 1-й день после операции, а интервал между каждыми последующими лазерными воздействиями равен количеству дней, выбранным в возрастающем порядке из ряда нечетных последовательных чисел, начинающегося с единицы. Способ позволяет ускорить заживление тканей бронхиальной раны, уменьшить послеоперационные осложнения путем нормализации содержания гистамина и ДНК в тканях бронхиальной раны и, как следствие, ускорения течения репаративных процессов. 2 табл.
Способ лечения тканей бронхиальной раны после реконструктивно-пластических операций на трахеобронхиальном дереве путем медикаментозного воздействия на ткани бронхиального шва, отличающийся тем, что в качестве медикаментозного средства используют антибиотики, а после операции дополнительно на область раны воздействуют 4-5 раз лазерным излучением длиной волны 0,63 мкм и мощностью на выходе световода 3 мВт в течение 3 мин, причем первое лазерное воздействие осуществляют во время операции после наложения швов, второе в 1-й день после операции, а интервал между каждыми последующими лазерными воздействиями равен количеству дней, выбранным в возрастающем порядке из ряда нечетных последовательных чисел, начинающегося с единицы.
| КАШИНЦЕВА Л.А | |||
| Эндоскопическая оценка результатов и реабилитации больных после бронхопластических операций | |||
| Автореферат диссертации | |||
| - Уфа, 1999, с.5-18 | |||
| ЧЕРЕМИСИНА О.В | |||
| Эндоскопическая лазерная профилактика и лечение послеоперационных эндобронхиальных осложнений | |||
| Автореферат диссертации | |||
| - Томск, 1997, с.4-19 | |||
| КОЗЛОВ В.И., БУЙЛИН В.А | |||
| Лазеротерапия с применением АЛТ “Мустанг” | |||
| - М.: Аспект-пресс, 1995, с.90-91. |
Авторы
Даты
2004-11-10—Публикация
2003-08-18—Подача