Изобретение относится к новым химическим биологически активным веществам из ряда гетероциклических соединений формулы (1а-в),
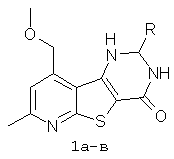
где (1a) R=5-бромфурил-2; (1б) R=фурил-2; (1в) R=циклогексил,
проявляющим свойство ослаблять токсическое действие гербицида гормонального действия 2,4-дихлорфеноксиуксусной кислоты (2,4-Д) на проростках подсолнечника.
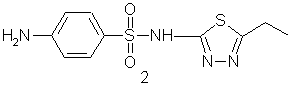
Антидотной активностью по отношению к 2,4-Д обладает 2-(n-аминобензолсульфамидо)-5-этил-1,3,4-тиадиазол формулы (2), принятый в качестве прототипа по свойствам (патент №2040898 Антидот гербицида гормонального действия 2,4-дихлорфенокси-уксусной кислоты // Стрелков В.Д., Исакова Л.И., Калита М.И., Литвинова Л.Н., Чубенко Т.И. МКИ А 01 N 25/32, 43/82, опубл. 09.08.95. БИ №22).
Структурным аналогом синтезированных соединений (1а-в) может служить 3-амино-6-метил-4-метоксиметил-2-(4-нитрофенил)тиено[2,3-b]-пиридин (3)
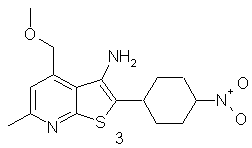
[Ye. A. Kaigorodova, V.K. Vasilin, L.D. Konyushkin, Ye.B. Usova, G.D. Krapivin Synthesis and Reactions of Substituted 3-amino-2-furyl(benzyl)-hieno[2,3-b]pyridines // Molecules. 2000. - №5. -Р.1085-1093 // http://www.mdpi.org.
Задачей настоящего изобретения является расширение арсенала биологически активных веществ, полученных синтетическим путем, для использования в сельском хозяйстве с целью защиты сельскохозяйственных культур от отрицательного действия гербицидов.
Это достигается применением 1,2,3,4-тетрагидропиридо[3’,2’:4,5]-тиено[3,2-d]пиримидин-4-онов (1а-в) путем обработки проросших семян подсолнечника.
Соединения (1а-в) получали реакцией конденсации 3-амино-6-метил-4-метоксиметилтиено[2,3-b]пиридин-2-карбоксамида 4 с альдегидами в толуоле в присутствии n-толуолсульфокислоты:

(1a) R=5-бромфурил-2; (1б) R=фурил-2; (1в) R=циклогексил.
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение 6-метил-4-метоксиметил-2-(5-бромфурил-2)-1,2,3,4-тетрагидропиридо[3’,2’:4,5]тиено[3,2-d]пиримидин-4-она (1а)
2,5 г (0,01 моль) тиенопиридина 4 растворяли в 50 мл толуола, добавляли 1,92 г (0,011 моль) 5-бромфурфурола и затем вносили на кончике шпателя n-толуолсульфокислоту. Кипятили реакционную смесь с обратным холодильником в течение 3 часов, после чего упаривали растворитель на треть. Кристаллический осадок отделяли и промывали 10 мл холодного этанола. Перекристаллизовывали из диметилформамида. Выход соединения (1а) составил 3,4 г (83%). Тпл=210-212°С (с разл.).
Элементный анализ для С16Н14ВrN3O3S: Найдено, %: С 47,17; Н 3,44; N 10,26. Вычислено, %: С 47,07; Н 3,46; N 10,29. Спектр ЯМР 1Н (DMSO-d6, 500 МГц): 2,58 (3Н, с, СН3), 3,42 (3Н, с, ОСН3), 4,83 (2Н, с, ОСН2), 5,87-5,94 (1Н, м, СН), 6,30 (1Н, д, 3-НFur3J=3,4 Гц), 6,37 (1Н, д, 4-НFur, 3J=3,4 Гц), 6,98 (1Н, д, NНАмид, J=3,4 Гц), 7,17 (1Н, с, НРу), 8,2 (1Н, уш.с, NНАмин). Масс-спектр, m/z (относительная интенсивность пиков в % от максимального): 407 (48), 328 (88), 296 (12), 235 (100), 219 (98), 203 (27), 175 (27), 163 (21), 42 (20), 39 (16).
Пример 2. Получение 6-метил-4-метоксиметил-2-(фурил-2)-1,2,3,4-тетрагидропиридо[3’,2’:4,5]тиено[3,2-d]пиримидин-4-она (1б)
2,5 г (0,01 моль) тиенопиридина 4 растворяли в 50 мл толуола, добавляли 0,9 мл (0,011 моль) фурфурола и затем вносили на кончике шпателя n-толуолсульфокислоту. Кипятили реакционную смесь с обратным холодильником в течение 3 часов, после чего упаривали растворитель на треть. Кристаллический осадок отделяли и промывали 10 мл холодного этанола. Перекристаллизовывали из диметилформамида. Выход соединения (1б) составил 2,57 г (78%). Тпл=259-260°С.
Элементный анализ для С16Н15N3O3S: Найдено, %: С 58,47; Н 4,56; N 12,70. Вычислено, %: С 58,35; Н 4,59; N 12,76. Спектр ЯМР 1Н (DMSO-d6, 500 МГц): 2,57 (3Н, с, СН3), 3,39 (3Н, с, ОСН3), 4,85 (2Н, с, ОСН2), 5,93-5,99 (1Н, м, СН), 6,30-6,35 (2Н, м, 3,4-HFur), 6,99 (1Н, д, NHАмид, J=3,4 Гц), 7,24 (1Н, с, НРу), 7,55 (1Н, д, 5НFur, J=1,8), 8,21 (1H, уш.с, NНАмин).
Масс-спектр, m/z (относительная интенсивность пиков в % от максимального): 329 (83), 312 (13), 296 (18), 235 (100), 230 (10), 219 (89), 203 (25), 175 (23), 163 (22), 135 (10), 94 (22), 73 (23), 42 (21), 39 (27).
Пример 3. Получение 6-метил-4-метоксиметил-2-циклогексил-1,2,3,4-тетрагидропиридо[3’,2’:4,5]тиено[3,2-d]пиримидин-4-она (1в)
2,5 г (0,01 моль) тиенопиридина (4) растворяли в 50 мл толуола, добавляли 1,3 мл (0,011 моль) циклогексанкарбальдегида и затем вносили на кончике шпателя n-толуолсульфокислоту. Кипятили реакционную смесь с обратным холодильником в течение 3 часов, после чего упаривали растворитель на две трети, остаток разбавляли 20 мл петролейного эфира. Образовавшийся осадок отделяли и перекристаллизовывали из этанола. Выход соединения (1б) составил 2,56 г (74%). Тпл=225-226°С.
Элементный анализ для C18H23N3О2S: Найдено, %: С 62,72; Н 6,67; N 12,11. Вычислено, %: С 62,58; Н 6,71; N 12,16. Спектр ЯМР 1Н (DMSO-d6, 500 МГц): 1,08-1,92 (10Н, м, Hцг), 2,61 (3Н, с, СН3), 3,41 (3Н, с, ОСН3), 4,78 (2Н, с, ОСН2), 4,52-4,58 (1Н, м, СН), 6,28 (1Н, д, NHАмид, J=3,4 Гц), 7,09 (1Н, с, НРу), 7,54 (1Н, уш.с, NНАмин).
Масс-спектр, m/z (относительная интенсивность пиков в % от максимального): 345 (65), 262 (17), 296 (18), 235 (100), 230 (10), 219 (92), 203 (25), 175 (23), 163 (22), 94 (34), 73 (33), 42 (29), 39 (33).
Пример 4. Изучение антидотной активности 1,2,3,4-тетрагидропиридо-[3’,2’:4,5]тиено[3,2-d|пиримидин-4-онов (1а-в) к 2,4-Д
Антидотную активность 1,2,3,4-тетрагидропиридо[3’,2’:4,5]тиено-[3,2-d]пиримидин-4-онов (1а-в) к 2,4-Д 500 ВР БАСФАГ (ГР №582313-1) изучали в лабораторных условиях на проростках подсолнечника сорта ВНИИМК-8883. Заявляемые соединения, прототип по свойству 2-(n-аминобензолсульфамидо)-5-этил-1,3,4-тиадиазол и аналог по структуре (3) испытывали в виде растворов, содержание спирта составляло соответственно 0,2%, содержание заявляемого соединения и прототипа составляло 10-2-10-5% (по массе).
Проросшие семена подсолнечника подвергали воздействию 2,4-Д и антидота. Часть семян обрабатывали только гербицидом (эталон сравнения). Контролем служили семена, обработанные водой. Дальнейшее проращивание семян проводили при температуре 28°С в течение 3 суток, измеряли длину гипокотиля и корня проростков подсолнечника.
Антидотную активность оценивали по увеличению длины корня и гипокотиля проростков в варианте гербицид + антидот в сравнении с гербицидным вариантом (эталон). Параллельно проводили испытание прототипа -2-(n-аминобензолсульфамидо)-5-этил-1,3,4-тиадиазола и аналога по структуре (3).
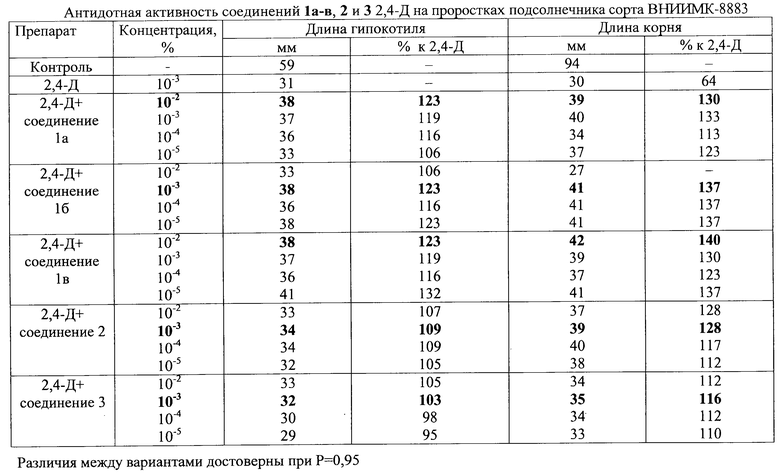
Статистическая обработка экспериментальных данных проведена с использованием t-критерия Стьюдента при уровне вероятности Р=0,95. Результаты испытаний представлены в таблице.
Как следует из таблицы, заявляемые соединения (1а-в) снижают токсичность 2,4-Д для проростков подсолнечника, превосходя прототип (2) и аналог по структуре (3). Так, соединение (1а) в оптимальной концентрации 10-2% увеличивает длину гипокотиля на 23%, корня - на 30% в сравнении с 2,4-Д. Соединение (1б) в оптимальной концентрации 10-3% увеличивает длину гипокотиля на 23%, корня - на 37% в сравнении с 2,4-Д. Соединение (1в) в оптимальной концентрации 10-2% увеличивает длину гипокотиля на 23%, корня - на 40% в сравнении с 2,4-Д. В то время как прототип (2) в оптимальной концентрации 10-3% увеличивает длину гипокотиля на 9% и длину корня на 28% в сравнении с 2,4-Д.
Аналог по структуре (3) в оптимальной концентрации 10-3% увеличивает длину гипокотиля на 3%, корня - на 16% по отношению к 2,4-Д.
Таким образом, соединения (1а-в) проявляют свойства антидота и могут быть использованы в практике сельского хозяйства для снятия токсического воздействия гербицида 2,4-Д на растения и активации их роста.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО ДЛЯ СНИЖЕНИЯ ТОКСИЧЕСКОГО ДЕЙСТВИЯ ГЕРБИЦИДА 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ НА ПОДСОЛНЕЧНИКЕ | 2003 |
|
RU2242123C1 |
| ЗАМЕЩЕННЫЕ 6а,11-ДИГИДРО-5H-БЕНЗО[4,5][1,3]ОКСАЗИНО[2,3-α]ИЗОИНДОЛ-11-ОНЫ-АНТИДОТЫ ГЕРБИЦИДА ГОРМОНАЛЬНОГО ДЕЙСТВИЯ 2,4-ДИХЛОР-ФЕНОКСИУКСУСНОЙ КИСЛОТЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2007 |
|
RU2345083C1 |
| 2-ТИОАЛКИЛПИРИДИНЫ И ТИЕНО[2,3-B]ПИРИДИНЫ-АНТИДОТЫ ГЕРБИЦИДА ГОРМОНАЛЬНОГО ДЕЙСТВИЯ 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ | 2003 |
|
RU2232762C1 |
| 2-АРИЛ-4,4-ДИФЕНИЛ-3,4-ДИГИДРОХИНАЗОЛИНЫ - АНТИДОТЫ ГЕРБИЦИДА ГОРМОНАЛЬНОГО ДЕЙСТВИЯ 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ | 2014 |
|
RU2574067C1 |
| (2-БЕНЗОИЛ-6-МЕТИЛ-4-МЕТОКСИМЕТИЛТИЕНО[2,3-B]ПИРИДИНИЛ-3)-ИМИНОТРИФЕНИЛФОСФОРАН- АНТИДОТ ГЕРБИЦИДА ГОРМОНАЛЬНОГО ДЕЙСТВИЯ 2.4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ | 2003 |
|
RU2232765C1 |
| N-Арил-3-(1,3-диоксоизоиндолин-2-ил)тиено[2,3-b]пиридин-2-карбоксамиды в качестве антидотов 2,4-Д на подсолнечнике | 2023 |
|
RU2811272C1 |
| N-алкилзамещенные бензо- и (пиридо[2,3-b]тиено)пирроло[1,2-a][1,4]диазепин-6-оны - антидоты гербицида гормонального действия 2,4-дихлорфеноксиуксусной кислоты на подсолнечнике | 2016 |
|
RU2607629C1 |
| 2-(1Н-БЕНЗИМИДАЗОЛ-2-ИЛ)-5'-НИТРОБЕНЗОЙНАЯ КИСЛОТА - АНТИДОТ ГЕРБИЦИДА ГОРМОНАЛЬНОГО ДЕЙСТВИЯ 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2012 |
|
RU2492647C1 |
| Способ получения производных 2-арил(гетарил)-7-метил-1,2,3,4-тетрагидропиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-она | 2016 |
|
RU2634351C1 |
| 7-(2-Арил-1-циановинил)-3-фенил-1,2,3,4-тетрагидропиразоло[1,5-a][1,3,5]триазин-8-карбонитрилы в качестве антидотов 2,4-Д на подсолнечнике | 2023 |
|
RU2803727C1 |
Описываются 1,2,3,4-тетрагидропиридо[3',2':4,5]тиено[3,2-d]пиримидин-4-оны формулы 1
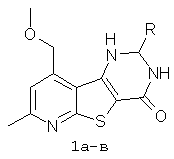
где (la) R=5-бромфурил-2; (1б) R=фурил-2; (1в) R=циклогексил. Технический результат заключается в получении новых соединений, используемых в сельском хозяйстве с целью защиты сельскохозяйственных культур от отрицательного действия 2,4-дихлорфеноксиуксусной кислоты. 1 табл.
1,2,3,4-Тетрагидропиридо[3'2':4,5]тиено[3,2-d]пиримидин-4-оны формулы 1
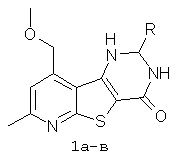
la R=5-бромфурил-2;
1б R=фурил-2;
1 в R=циклогексил,
проявляющие антидотную активность к гербициду гормонального действия 2,4-дихлорфеноксиуксусной кислоте на проростках подсолнечника.
| Molecules | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| АППАРАТ, СЛУЖАЩИЙ ДЛЯ ОДНОВРЕМЕННОГО ВОСПРОИЗВЕДЕНИЯ С ОДНОЙ И ТОЙ ЖЕ ЛЕНТЫ ЗВУКА, ЦВЕТА И СТЕРЕОСКОПИЧНОСТИ ДВИЖУЩЕГОСЯ ПРЕДМЕТА | 1921 |
|
SU1085A1 |
Авторы
Даты
2004-11-27—Публикация
2003-07-24—Подача