Настоящее изобретение относится к соединениям общей формулы
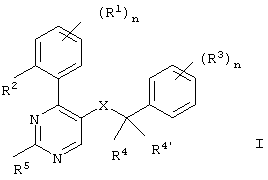
где
R1 означает водород или галоген,
R2 означает водород, галоген, низший алкил или низший алкокси,
R1 и R2 вместе с двумя атомами углеродного цикла могут означать группу -СН=СН-СН=СН-,
R3 означает галоген, трифторметил, низший алкил или низший алкокси,
R4/R4’ независимо друг от друга каждый означает водород или низший алкил,
R5 означает низший алкил, низший алкокси, амино, фенил, гидрокси(низш.)алкил, циано(низш.)алкил, карбамоил(низш.)алкил, пиридил, пиримидил, -(СН2)n-пиперазинил, необязательно замещенный одной или двумя низшими алкильными группами или гидрокси(низш.)алкилом, -(СН2)n-морфолинил, -(СН2)n-пиперидинил, -(СН2)n+1-имидазолил, (низш.)алкилсульфанил, (низш.)алкилсульфонил, бензиламино, -NH-(СН2)n+1N(R4’’)2 -(СH2)n+1N(R4’’)2, -O-(СН2)n+1-морфолинил, -O-(СН2)n+1-пиперидинил или -O-(СН2)n+1N(R4’’)2, где R4’’ означает водород или (низш.)алкил, и
n означает 0-2,
Х означает -C(O)N(R4’’)- или -N(R4’’)C(O)-;
и к их фармацевтически приемлемым кислотно-аддитивным солям.
Соединения формулы I и их соли отличаются ценными терапевтическими свойствами. При создании изобретения неожиданно было установлено, что соединения по настоящему изобретению являются антагонистами рецептора нейрокинина 1 (NK-1, вещество Р). Вещество Р представляет собой встречающийся в естественных условиях ундекапептид, принадлежащий к пептидам из семейства тахикининов, последние так называются из-за быстрого сократительного действия на внесосудистую ткань гладкой мускулатуры.
Рецептор вещества Р является представителем надсемейства связанных с протеином G рецепторов.
Нейропептидные рецепторы вещества Р (NK-1) широко распространены в нервной системе млекопитающих (прежде всего в головном мозге и спинальных ганглиях), кровеносной системе и периферических тканях (прежде всего в двенадцатиперстной кишке и тощей кишке), и они участвуют в регуляции многочисленных разнообразных биологических процессов.
Установлено, что центральное и периферическое действие тахикинина млекопитающих, т.е. вещества Р, связано с многочисленными воспалительными состояниям, включая мигрень, ревматоидный артрит, астму и воспалительное заболевание кишечника, а также выявлена его роль в качестве медиатора рвотного рефлекса и модулятора нарушений центральной нервной системы (ЦНС), таких как болезнь Паркинсона (Neurosci. Res. 7, 187-214, 1996), состояние тревоги (Can. J. Phys., 75, 612-621, 1997) и депрессия (Science, 281, 1640-1645,1998).
Данные о возможности применения антагонистов рецептора тахикинина для лечения боли, головной боли, прежде всего мигрени, болезни Альцгеймера, рассеянного склероза, ослабления синдрома отказа от морфина, сердечно-сосудистых изменений, отека, такого как отек, вызванный термическим повреждением, хронических воспалительных заболеваний, таких как ревматоидный артрит, астма/бронхиальная гиперреактивность и другие респираторные заболевания, включая аллергический ринит, воспалительные заболевания кишечника, включая язвенный колит и болезнь Крона, повреждения глаза и глазных воспалительных заболеваний, обобщены в статье "Tachykinin Receptor and Tachykinin Receptor Antagonists" J. Auton. Pharmacol., 13, 23-93, 1993.
Кроме того, антагонисты рецептора нейрокинина 1 разрабатывают с целью лечения многочисленных физиологических нарушений, связанных с избытком или с нарушением баланса тахикининов, в частности вещества Р. Примеры состояний, которые связаны с веществом Р, включают нарушения центральной нервной системы, такие как состояние тревоги, депрессия и психоз (WO 95/16679, WO 95/18124 и WO 95/23798).
Антагонисты рецептора нейрокинина-1, кроме того, могут применяться для лечения состояния укачивания и индуцированной лекарственным средством рвоты.
Кроме того, в журнале The New England Journal of Medicine, том 34, №3, 190-195, 1999 описано уменьшение индуцированной цисплатином рвоты с помощью избирательных антагонистов рецептора нейрокинина-1.
В патенте US 5972938 также описан способ лечения психоиммунологического или психосоматического нарушения путем введения антагониста рецептора тахикинина, такого как рецептор NK-1.
Объектами настоящего изобретения являются соединения формулы I и их фармацевтически приемлемые соли, способ получения вышеупомянутых соединений, содержащие их лекарственные средства и способ их изготовления, а также применение вышеупомянутых соединений для лечения и профилактики заболеваний, прежде всего заболеваний и расстройств типа приведенных выше, или для производства соответствующих лекарственных средств.
Наиболее предпочтительными показаниями по настоящему изобретению являются такие, которые включают расстройства центральной нервной системы, например необходимость терапии или профилактики некоторых депрессивных состояний или рвоты при введении антагонистов NK-1 рецептора. Основной приступ депрессии определяют как период по крайней мере в течение двух недель, во время которого, в течение большинства дней или почти каждый день, наблюдается подавленное настроение или потеря интереса или отсутствие удовлетворения от любого или почти от любого вида активной деятельности.
Общие термины, используемые в контексте настоящего изобретения, имеют следующие значения, независимо от того, применяются эти термины индивидуально или в различных сочетаниях.
Используемый в описании термин "(низш.)алкил" означает линейную или разветвленную алкильную группу, содержащую от 1 до 7 атомов углерода, например, метил, этил, пропил, изопропил, н-бутил, изобутил, трет-бутил и т.п. Предпочтительны (низш.)алкильные группы, содержащие от 1 до 4 углеродных атомов.
Термин "(низш.)алкокси" означает группу, в которой алкильные остатки имеют значения, указанные выше, причем алкил присоединен через атом кислорода.
Термин "галоген" означает хлор, йод, фтор и бром. Термин "фармацевтически приемлемые кислотно-аддитивные соли" означает соли неорганических и органических кислот, таких как хлористоводородная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, паратолуолсульфоновая кислота и т.п.
Предпочтительными являются соединения, у которых Х означает -C(O)N(R4’’)-, где R4’’ означает метил, a R5 означает пиперазинил, необязательно замещенный одной или двумя метильными группами, например, нижеуказанные соединения:
(3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид(3R,5S)-4-(2-бромфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид(3R,5S)-4-(2-хлорфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-пиперазин-1-ил-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(2-метоксифенил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-димeтилпиперазин-1-ил)-4-(2-фторфенил)пиримидин-5-карбоновой кислоты,
(3,5-бис-триф)торметилбензил)метиламид 4-(4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фтор-2-метилфенил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-нафталин-1-ил-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты и
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты.
Кроме того, предпочтительны соединения, у которых Х означает -C(O)N(R4’’)-, где R4’’ означает метил, a R5 означает морфолинил или -O(СН2)2-морфолинил.
Примерами таких соединений являются:
(3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-морфолин-4-илэтокси)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-метоксифенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-морфолин-4-ил-4-нафталин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты.
Кроме того, предпочтительны соединения, у которых Х означает
-C(O)N(R4’’)-, R4’’ означает метил, a R5 означает –NH(CH2)2N(CH3)2, -O(СН2)2N(СН3)2 или –O(CH2)3N(CH3)2, например следующие соединения:
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтиламино)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтокси)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(3-диметиламинопропокси)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-карбоновой кислоты или
(3,5-бис-трифторметилбензил)метиламид 2-(3-диметиламинопропокси)-4-о-толилпиримидин-5-карбоновой кислоты.
Кроме того, предпочтительны соединения, у которых Х означает
-N(R4’’)C(O)-, R4’’ означает метил, а R5 означает морфолинил или пиперазинил, необязательно замещенный группой низший алкил, например, следующие соединения:
2-(3,5-бис-трифторметилфенил)-N-метил-N-[2-(4-метилпиперазан-1-ил)-4-о-толилпиримидин-5-ил] изобутирамид и
2-(3,5-бис-трифторметилфенил)-N-метил-N-(2-морфолин-4-ил-4-о-толилпиримидин-5-ил) изобутирамид.
Настоящие соединения формулы I и их фармацевтически приемлемые соли могут быть получены по известным в данной области техники методам, например описанным ниже способом, который включает
а) взаимодействие соединения формулы
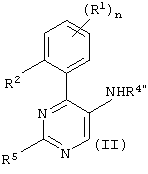
с соединением формулы
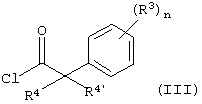
с образованием соединения формулы
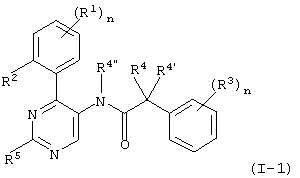
где R1-R5 и n имеют значения, указанные выше, или б) взаимодействие соединения формулы
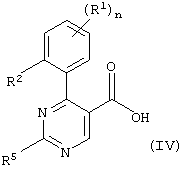
с соединением формулы
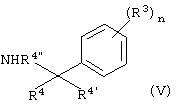
с образованием соединения формулы
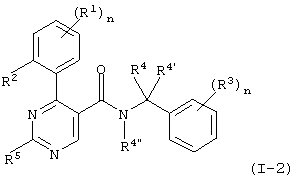
где R1-R5 и n имеют значения, указанные выше, или
в) модификацию одного или более заместителей R1-R5, имеющих значения, указанные выше, и, если необходимо, перевод полученного соединения в его фармацевтически приемлемую кислотно-аддитивную соль.
По способу а) к смеси соединения формулы II, например метил [6-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-3-ил] амина и соединения формулы III, например, 2-(3,5-бис-трифторметилфенил)-2-метилпропионил-хлорида, добавляют DIPEA (N-этилдиизопропиламин) и смесь перемешивают при температуре от 35 до 40°С. Требуемое соединение формулы I-1 получают после очистки с высоким выходом.
Способ б) описывает взаимодействие соединения формулы IV с соединением формулы V с образованием соединения формулы I-2. Реакцию проводят в обычных условиях, например, в растворителе, таком как дихлорметан, в присутствии триэтиламина, EDCI (гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида) и НОВТ (1-гидроксибензотриазола). Полученную смесь перемешивают при 20°С в течение 12 ч.
Получение соли проводят при комнатной температуре по известным в данной области техники методам. При этом имеются ввиду соли как с неорганическими, так и органическими кислотами. Примерами таких солей являются гидрохлориды, гидробромиды, сульфаты, нитраты, цитраты, ацетаты, малеаты, сукцинаты, метансульфонаты, пара-толуолсульфонаты и т.п.
Нижеуказанные схемы 1-6 более подробно иллюстрируют способы получения соединений формулы I. Исходные материалы формул V, VIII, X, XIV и XVIII являются известными соединениями и могут быть получены по известным в данной области техники методам.
На схемах используются следующие сокращения:
ТГФ - тетрагидрофуран
DIPEA - N-этилдиизопропиламин
НОВТ - 1-гидроксибензотриазол
EDCI - гидрохлорид N-(3-диметиламинопропил)-N’-этилкарбодиимида
м-ХНБК - мета-хлорнадбензойная кислота
ДФФА - дифенилфосфорилазид
ДМФ - диметилформамид
ТЭА - триэтиламин
Схема 1
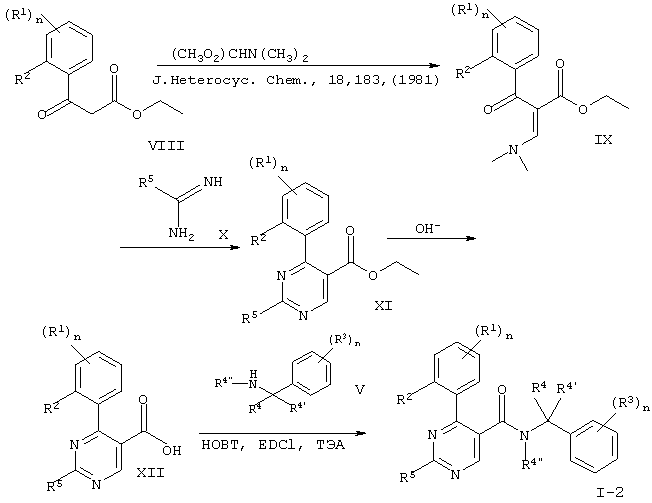
Заместители имеют значения, указанные выше.
Схема 2
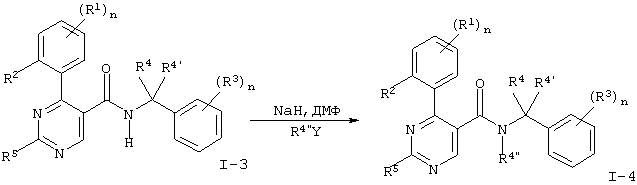
Y=галоген
R4”(низш.)алкил
Заместители имеют значения, указанные выше.
Схема 3
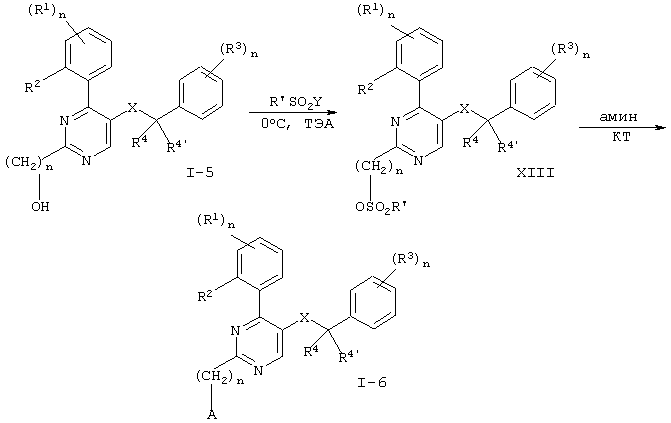
R’ означает (низш.)алкил, Y означает галоген, А означает аминогруппу, такую, как -N(R4)2, пиперазинил, морфолинил, пиперидинил или имидазолил. Остальные заместители имеют значения, указанные выше.
Схема 4
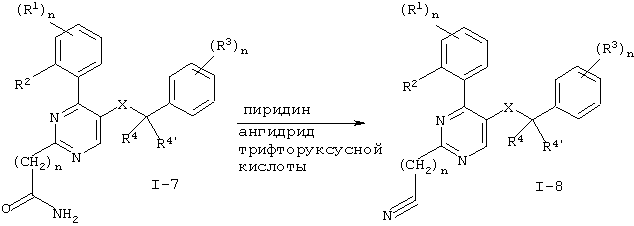
Заместители имеют значения, указанные выше.
Схема 5
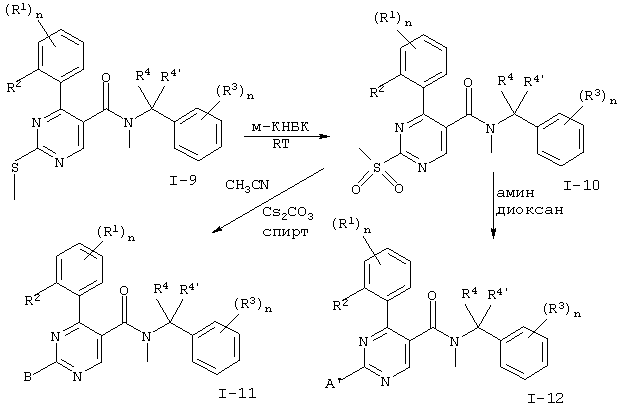
Тип реакции описан в журнале Bioorg. and Med. Chem., vol.5, №2, 437-444 (1997).
R1-R4 и n имеют значения, указанные выше, В означает (низш.)алкокси, -O-(CH2)n+1N(R4)2, -O-(СН2)n+1-морфолинил или -O-(СН2)n+1-пиперидинил, а А’ означает аминогруппу, такую как -N(R4)2, необязательно замещенный пиперазинил, морфолинил, пиперидинил, имидазолил, бензиламин или -NH-(CH)n+1N(R4)2.
Схема 6
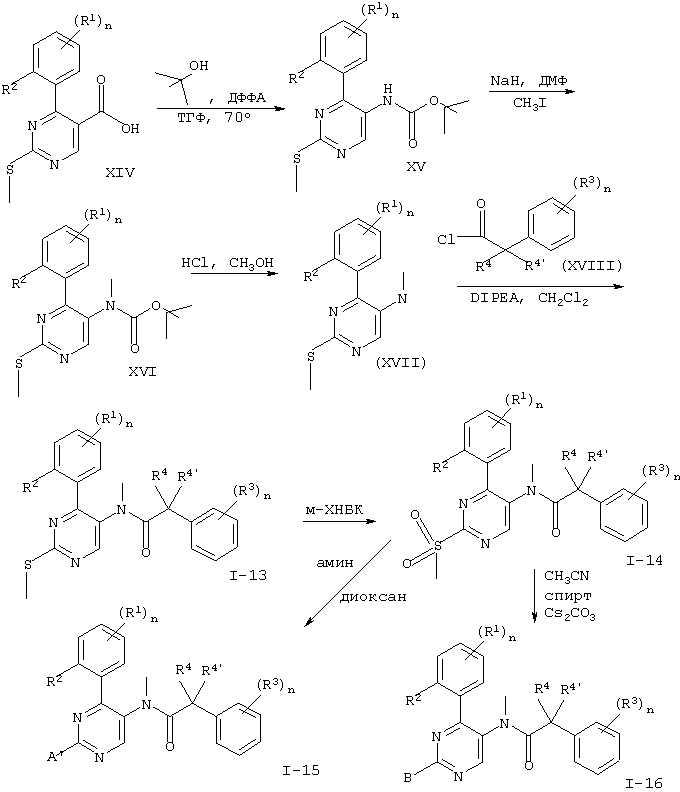
R1-R4 и n имеют значения, указанные выше, В означает (низш.)алкокси, -O-(CH2)n+1N(R4)2 -O-(СН2)n+1-морфолинил или -O-(СН2)n+1-пиперидинил, а А’ означает аминогруппу, такую как -N(R4)2, необязательно замещенный пиперазинил, морфолинил, пиперидинил, имидазолил, бензиламин или -NH-(CH2)n+1N(R4)2.
Как отмечалось ранее, соединения формулы I и их фармацевтически приемлемые аддитивные соли обладают ценными фармакологическими свойствами. Установлено, что соединения по настоящему изобретению являются антагонистами рецептора нейрокинина 1 (NK-1, вещество Р).
Соединения формулы I были изучены с помощью приведенных ниже тестов.
Сродство тестируемых соединений к NK1-рецептору оценивали с использованием человеческих NK1-рецепторов в СНО-клетках, инфицированных человеческим NК1-рецептором (с использованием экспрессионной системы вируса Semliki) и в присутствии радиоактивно меченного с помощью [3Н]-вещества Р (конечная концентрация 0,6 нМ). Опыты по связыванию проводили в HEPES-буфере (50 мМ, рН 7,4), содержащим БСА (бычий сывороточный альбумин) (0,04%), леупептин (8 мкг/мл), MnCl2 (3 мМ) и фосфорамидон (2 мкМ). В опытах по связыванию использовали 250 мкл суспензии мембран (1,25×105 клеток/пробирку для анализа), 0,125 мкл буфера, включающего замещающий агент, и 125 мкл [3Н]-вещества Р. Для получения кривых замещения использовали по меньшей мере 7 концентраций соединения. Пробирки для анализа инкубировали в течение 60 мин при комнатной температуре, после чего содержимое пробирки быстро фильтровали под вакуумом через фильтры типа GF/C, которые предварительно в течение 60 мин пропитывали PEI (0,3%) с двумя промывками, для каждой из которых использовали по 2 мл HEPES-буфера (50 мМ, рН 7,4). Радиоактивность, сохранившуюся на фильтрах, оценивали с помощью сцинцилляционного счетчика. Все опыты проводили в трех повторностях по меньшей мере в двух различных экспериментах.
Для предпочтительных соединений их сродство к NК1-рецептору, выраженное в виде значения рКi, составляло 8,00-9,20. Примерами таких соединений являются:

Соединения формулы I, а также их фармацевтически приемлемые кислотно-аддитивные соли могут применяться в качестве лекарственных средств, например, в форме фармацевтических композиций. Фармацевтические композиции могут вводиться перорально, например, в форме таблеток, филмтаблеток, драже, желатиновых капсул с твердым или мягким покрытием, растворов, эмульсий или суспензий. Однако введение также может быть осуществлено ректально, например, в форме суппозиториев, или парентерально, например, в форме инъецируемых растворов.
Соединения формулы I и их фармацевтически приемлемые кислотно-аддитивные соли могут быть подвергнуты обработке вместе с фармацевтически инертными неорганическими или органическими эксципиентами для приготовления таблеток, филмтаблеток, драже и желатиновых капсул с твердым покрытием. В качестве таких эксципиентов для приготовления, например, таблеток, драже и желатиновых капсул с твердым покрытием могут использоваться лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли и т.д.
Приемлемыми эксципиентами для приготовления желатиновых капсул с мягким покрытием являются, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и т.д.
Приемлемыми эксципиентами для приготовления растворов и сиропов являются, например, вода, полиолы, сахароза, инвертный сахар, глюкоза и т.д.
Приемлемыми эксципиентами для инъецируемых растворов являются, например, вода, спирты, полиолы, глицерин, растительные масла и т.д.
Приемлемыми эксципиентами для суппозиториев являются, например, природные или гидрогенизированные масла, воски, жиры, полутвердые или жидкие полиолы.
Кроме того, фармацевтические композиции могут содержать консерванты, солюбилизаторы, стабилизаторы, смачивающие агенты, эмульгаторы, подслащивающие вещества, красители, корригенты, соли для изменения осмотического давления, буферы, маскирующие агенты или антиоксиданты. Они также могут содержать и другие терапевтически ценные вещества.
Дозы могут варьироваться в широких пределах и, естественно, должны быть подобраны в зависимости от индивидуальных требований в каждом конкретном случае. В целом, в случае перорального введения суточная доза для пациента может находиться в диапазоне примерно от 10 до 1000 мг соединения формулы I, однако при необходимости верхний предел может быть превышен.
Ниже настоящее изобретение проиллюстрировано примерами, не ограничивающими его объем.
Пример 1
(3,5-бис-трифторметилбензил)метиламид 2-метил-4-фенилпиримидин-5-карбоновой кислоты
а) 3,5-бис-трифторметилбензиламид 2-метид-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,50 г (2,33 ммоля) 2-метил-4-фенилпиримидин-5-карбоновой кислоты, 0,65 мл (4,47 ммоля) триэтиламина, 0,44 г (2,33 ммоля) 1-гидроксибензотриазола и 0,44 г (2,33 ммоля) гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида в 40 мл CH2Cl2 добавляли 0,68 г (2,8 ммоля) 3,5-бис-трифторметилбензиламина и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь разбавляли 20 мл CH2Cl2, промывали 50 мл 0,5 н. НСl, 50 мл Н2О и проводили обратную экстракцию водных слоев 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, этилацетат), при этом получали 0,80 г (78%) 3,5-бис-трифторметилбензиламида 2-метил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 188,5-189,5°С.
б) (3,5-Бис-трифторметидбензил)метиламид 2-метил-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,67 г (1,52 ммоля) 3,5-бис-трифторметилбензиламида 2-метил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл N,N-диметилформамида добавляли 0,08 г (1,98 ммоля) гидрида натрия (60%-ная дисперсия в минеральном масле) и реакционную смесь перемешивали в течение 1 ч. Затем при 0°С добавляли 0,15 мл (2,4 ммоля) метилиодида и реакционную смесь перемешивали при комнатной температуре (КТ) в течение 3 ч. Реакционную смесь распределяли между 50 мл Н2О, 50 мл солевого раствора и 50 мл СН2Сl2. Фазы разделяли и водный слой дважды промывали 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, этилацетат/гексан, 4:1), при этом получали 0,50 г (72%) (3,5-бис-трифторметилбензил)метиламида 2-метил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(EI):453 (М+).
Пример 2
(3,5-Дихлорбензил)метиламид 2-метид-4-фенилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 1а), из 2-метил-4-фенилпиримидин-5-карбоновой кислоты и 3,5-дихлорбензиламина получали 3,5-дихлорбензиламид 2-метил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 194-195°С, который метилировали аналогично тому, как описано в примере 1б), при этом получали (3,5-дихлорбензил)метиламид 2-метил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(EI):385 (M+).
Пример 3
(3,5-Бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-метидпиримидин-5-карбоновой кислоты
а) Этиловый эфир 2-(2-бромбензоил)-3-диметиламиноакриловой кислоты
К раствору 25,9 г (95,5 ммоля) этилового эфира 3-(2-бромфенил)-3-оксопропионовой кислоты в 200 мл толуола в течение 1 ч добавляли 18,21 г (152 ммоля) диметилацеталя N,N-диметилформамида, растворенного в 100 мл толуола, и реакционную смесь перемешивали при 100°С в течение 1,5 ч. Растворитель выпаривали, полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 40:1), при этом получали 25 г (80%) этилового эфира 2-(2-бромбензоил)-3-диметиламиноакриловой кислоты в виде твердого вещества светло-коричневого цвета.
б) Этиловый эфир 4-(2-бромфенил)-2-метидпиримидин-5-карбоновой кислоты
К свежеприготовленному раствору алкоголята натрия [полученному из 0,77 г (33,7 ммоля) натрия, добавленного к 100 мл этанола] добавляли 3,18 г (33,7 ммоля) гидрохлорида ацетамидина. Через 10 мин добавляли раствор 10,0 г (30,6 ммоля) этилового эфира 2-(2-бромбензоил)-3-диметиламиноакриловой кислоты в 120 мл этанола и реакционную смесь нагревали при 80°С в течение 16 ч. Растворитель выпаривали, остаток распределяли между 100 мл Н2О и 100 мл СН2Сl2. Водную фазу дважды экстрагировали 100 мл СН2Сl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 40:1), при этом получали 8,3 г (84%) этилового эфира 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты в виде масла светло-коричневого цвета.
в) 4-(2-бромфенил)-2-метилпиримидин-5-карбоновая кислота
К раствору 8,3 г (25,8 ммоля) этилового эфира 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты в 10 мл этанола добавляли 1,55 г (38,6 ммоля) NaOH в 20 мл Н2О. После перемешивания в течение 1 ч реакционную смесь промывали 100 мл диэтилового эфира. Водную фазу подкисляли 25%-ной НСl до рН 1 и дважды экстрагировали 200 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали, при этом получали 7,0 г (92%) 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты в виде пены светло-желтого цвета.
г) (3,5-Бис-трифторметилбензид)метиламид 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты
К раствору 0,5 г (1,71 ммоля) 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты, 0,47 мл (3,41 ммоля) триэтиламина, 0,26 г (1,71 ммоля) 1-гидроксибензотриазола и 0,32 г (1,71 ммоля) гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида в 40 мл СН2Сl2 добавляли 0,52 г (2,0 ммоля) (3,5-бис-трифторметилбензил)метиламина и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь разбавляли 20 мл СН2Сl2, промывали 50 мл 0,5н. НСl, 50 мл Н2О и проводили обратную экстракцию водных слоев 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, этилацетат), при этом получали 0,7 г (77%) (3,5-бис-трифторметилбензил)метиламида 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 121,5-122,5°С.
Пример 4
3,5-Бис-трифторметилбензиламид
4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты
К раствору 0,5 г (1,71 ммоля) 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты, 0,47 мл (3,41 ммоля) триэтиламина, 0,26 г (1,71 ммоля) 1-гидроксибензотриазола и 0,32 г (1,71 ммоля) гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида в 40 мл CH2Cl2 добавляли 0,49 г (2,05 ммоля) 3,5-бис-трифторметилбензиламина и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь разбавляли 20 мл СН2Сl2, промывали 50 мл 0,5н. НСl, 50 мл Н2О и проводили обратную экстракцию водных слоев 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH), при этом получали 0,4 г (45%) 3,5-бис-трифторметилбензиламида 4-(2-бромфенил)-2-метилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 137,5-138,5°С.
Пример 5
(3,5-Бис-трифторметилбензил)метиламид 2,4-дифенилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 1а), из 2,4-дифенилпиримидин-5-карбоновой кислоты и 3,5-бис-трифторметилбензиламина получали 3,5-бис-трифторметилбензиламид 2,4-дифенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл>220°C, который метилировали, как описано в примере 1б), при этом получали (3,5-бис-трифторметилбензил)метиламид 2,4-дифенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):516,2 (M+H+).
Пример 6
(3,5-Дихлорбензил)метиламид 2,4-дифенидпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 1а), из 2,4-дифенилпиримидин-5-карбоновой кислоты и 3,5-дихлорбензиламина получали 3,5-дихлорбензиламид 2,4-дифенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл>220°С, который метилировали, как описано в примере 1б), при этом получали (3,5-дихлорбензил)метиламид 2,4-дифенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):448 (M+H+).
Пример 7
(3,5-Дихлорбензил)метиламид 4-фенил-2-пропилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 1а), из 4-фенил-2-пропилпиримидин-5-карбоновой кислоты и 3,5-дихлорбензиламина получали 3,5-дихлорбензиламид 4-фенил-2-пропилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 183°С, который метилировали, как описано в примере 1б), при этом получали (3,5-дихлорбензил)метиламид 4-фенил-2-пропилпиримидин-5-карбоновой кислоты в виде бесцветного масла, МС(ЕI):413 (М+).
Исходное соединение, 4-фенил-2-пропилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3б), из этилового эфира 2-бензоил-3-диметиламиноакриловой кислоты и гидрохлорида бутирамидина, с последующим гидролизом, как описано в примере 3в), до 4-фенил-2-пропилпиримидин-5-карбоновой кислоты.
Пример 8
(3,5-Бис-трифторметилбензил)метиламид 4-фенил-2-пропилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 1а), из 4-фенил-2-пропилпиримидин-5-карбоновой кислоты и 3,5-бис-трифторметилбензиламина получали 3,5-бис-трифторметилбензиламид 4-фенил-2-пропилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 194-195°С, который метилировали, как описано в примере 1б), при этом получали (3,5-бис-трифторметилбензил)метиламид 4-фенил-2-пропилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):482,3 (M+H+).
Пример 9
(3,5-Бис-трифторметилбензил)метидамид 4-фенил-2-пиридин-4-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 3г), из 4-фенил-2-пиридин-4-илпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-фенил-2-пиридин-4-илпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 143-144°С.
Исходное соединение, 4-фенил-2-пиридин-4-илпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3б), из этилового эфира 2-бензоил-3-диметиламиноакриловой кислоты и гидрохлорида изоникотинамидина, с последующим гидролизом, как описано в примере 3в), до 4-фенил-2-пиридин-4-илпиримидин-5-карбоновой кислоты.
Пример 10
(3,5-Бис-трифторметилбензил)метиламид 4-фенил [2,2’] бипиримидинид-5-карбоновой кислоты
Аналогично тому, как описано в примере 3г), из 4-фенил-[2,2’] бипиримидинил-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-фенил- [2,2’]бипиримидинил-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 172-173°С.
Исходное соединение, 4-фенил[2,2’]бипиримидинил-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3б), из этилового эфира 2-бензоил-3-диметиламиноакриловой кислоты и гидрохлорида пиримидин-2-карбоксамидина, с последующим гидролизом, как описано в примере 3в), до 4-фенил[2,2’]бипиримидинил-5-карбоновой кислоты.
Пример 11
3,5-Бис-трифторметидбензидамид 2-метил-4-нафталин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 1а), из 2-метил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и 3,5-бис-трифторметилбензиламина получали 3,5-бис-трифторметилбензиламид 2-метил-4-нафталин-1-илпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 146,7-146,9°С.
Исходное соединение, 2-метил-4-нафталин-1-илпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3а)-3в), из этилового эфира 3-нафталин-1-ил-3-оксопропионовой кислоты и диметилацеталя N,N-диметилформамида.
Пример 12
(3,5-Бис-трифторметилбензил)метиламид 2-метил-4-нафталин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 1б), из 3,5-бис-трифторметилбензиламида 2-метил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и метилиодида получали (3,5-бис-трифторметилбензил)метиламид 2-метил-4-нафталин-1-илпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 164,9-165,2°С.
Пример 13
(3,5-Бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-метилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 3г), из 4-(2-метоксифенил)-2-метилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-метилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 140-141°С.
Исходное соединение, 4-(2-метоксифенил)-2-метилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3а)-3в), из этилового эфира 3-(2-метоксифенил)-3-оксопропионовой кислоты и диметилацеталя N,N-диметилформамида.
Пример 14
(3,5-Бис-трифторметидбензил)метиламид 2-метилсудьфанил-4-фенилпиримидин-5-карбоновой кислоты
К раствору 3 г (12,18 ммоля) 2-метилсульфанил-4-фенилпиримидин-5-карбоновой кислоты, 3,32 мл (24,36 ммоля) триэтиламина, 1,84 г (12,18 ммоля) 1-гидроксибензотриазола и 2,33 г (12,81 ммоля) гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида в 170 мл СН2Сl2 добавляли 3,76 г (14,62 ммоля) (3,5-бис-трифторметилбензил) метиламина и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь разбавляли 100 мл СН2Сl2, промывали 100 мл 0,5н. НСl, 100 мл Н2О и проводили обратную экстракцию водных слоев 100 мл СН2Сl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/этилацетат), при этом получали 4,15 г (67%) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфанил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 119,1-119,8°С.
Пример 15
(3,5-Бис-трифторметилбензил)метиламид 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты
К раствору 4,15 г (85,5 ммоля) (3,5-бис-трифторметилбензил)метиламида2-метилсульфанил-4-фенилпиримидин-5-карбоновой кислоты в 170 мл CH2Cl2 при 5°С добавляли 5,27 г (21,4 ммоля) 3-хлорнадбензойной кислоты (70%) и реакционную смесь перемешивали при КТ в течение 3 ч. Затем добавляли 150 мл насыщенного раствора NаНСО3, слои разделяли, органическую фазу промывали насыщенным раствором NaHCO3, сушили (Nа2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/метанол, 40:1), при этом получали 4,20 г (95%) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, MC(EI):517 (M+).
Пример 16
(3,5-Бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,97 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,27 мл (2,42 ммоля) 1-метилпиперазина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл СН2Сl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/метанол, 9:1), при этом получали 0,4 г (77%) (3,5-бис-трифторметилбензил)метиламида 2-(4-метилпиперазин-1-ил)-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):538,3 (М+Н+).
Пример 17
(3,5-Бис-трифторметилбензил)метиламид 2-бензиламино-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,4 г (0,77 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,21 мл (1,923 ммоля) бензиламина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/метанол, 40:1), при этом получали 0,2 г (47%) (3,5-бис-трифторметил-бензил)метиламида 2-бензиламино-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 117,2-118,1°С.
Пример 18
(3,5-Бис-трифторметилбензид)метиламид 2-морфолин-4-ил-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,4 г (0,77 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,17 мл (1,93 ммоля) морфолина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл СН2Сl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/метанол, 40:1), при этом получали 0,21 г (52%) (3,5-бис-трифторметилбензил)метиламида 2-морфолин-4-ил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 168,1-168,4°С.
Пример 19
(3,5-Бис-трифторметилбензил)метиламид 4-фенид-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,208 г (2,15 ммоля) пиперазина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл СН2Сl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/метанол, 40:1), при этом получали 0,42 г (83%) (3,5-бис-трифторметилбензил)метиламида 4-фенил-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):524,1 (M+H+).
Пример 20
(3,5-Бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-фенидпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,276 г (2,15 ммоля) цис-2,6-диметилпиперазина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл СН2Сl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/метанол, 40:1), при этом получали 0,51 г (96%) (3,5-бис-трифторметилбензил)метиламида (2R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):552,1 (M+H+).
Пример 21
(3,5-Бис-трифторметилбензил)метиламид 2-(2-диметиламиноэтиламино)-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,4 г (0,77 ммоля) (3,5-бис-трифторметилбензил)метиламида2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,211 мл (1,93 ммоля) 2-диметиламиноэтиламина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/метанол/NH4OH, 140:10:1), при этом получали 0,22 г (54%) (3,5-бис-трифторметилбензил)метиламида 2-(2-диметиламиноэтиламино)-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 109,5-110,3°С.
Пример 22
(3,5-Бис-трифтоометилбензил)метиламид 4-фенил-2-пиперидин-1-илпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,183 г (2,15 ммоля) пиперидина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл СН2Сl2, объединенные органические экстракты сушили (MgSО4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/этилацетат, 20:1), при этом получали 0,48 г (95%) (3,5-бис-трифторметилбензил)метиламида 4-фенил-2-пиперидин-1-илпиримидин-5-карбоновой кислоты в виде воскообразного вещества светло-желтого цвета, MC(ISP):523,2 (M+H+).
Пример 23
(3,5-Бис-трифторметилбензил)метиламид 2-[4-(2-гидроксиэтил)пиперазин-1-ил]-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл диоксана добавляли 0,28 г (2,15 ммоля) N-(2-гидроксиэтил)пиперазина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл СН2Сl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 6:1), при этом получали 0,43 г (78%) (3,5-бис-трифторметил-бензил)метиламида2-[4-(2-гидроксиэтил)пиперазин-1-ил]-4-фенилпиримидин-5-карбоновой кислоты в виде воскообразного вещества светло-желтого цвета. MC(ISP):568,2 (M+H+).
Пример 24
(3,5-Бис-трифторметилбензил)метиламид 2-(2-морфолин-4-илэтокси)-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 20 мл ацетонитрила добавляли 0,15 г (1,16 ммоля) N-(2-гидроксиэтил)морфолина, 1,57 г (4,83 ммоля) Cs2CO3, и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 40:1), при этом получали 0,39 г (68%) (3,5-бис-трифторметилбензил)метиламида 2-(2-морфолин-4-илэтокси)-4-фенилпиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(ISP):569,2 (M+H+).
Пример 25
(3,5-Бис-трифторметилбензид)метиламид 4-фенил-2-(2-пиперидин-1-илэтокси)пиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 20 мл ацетонитрила добавляли 0,15 г (1,16 ммоля) N-(2-гидроксиэтил)пиперидина, 1,57 г (4,83 ммоля) Cs2CO3, и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4OH, 200:10:1), при этом получали 0,47 г (85%) (3,5-бис-трифторметилбензил)метиламида 4-фенил-2-(2-пиперидин-1-илэтокси)пиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(ISP):567,2 (М+Н+).
Пример 26
(3,5-Бис-трифторметилбензил)метиламид 2-(2-диметиламиноэтокси)-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 20 мл ацетонитрила добавляли 0,10 г (1,16 ммоля) 2-диметиламиноэтанола, 1,57 г (4,83 ммоля) Сs2СО3, и реакционную смесь перемешивали в течение 16 ч.
После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4OH, 110:10:1), при этом получали 0,43 г (82%) (3,5-бис-трифторметилбензил)метиламида2-(2-диметиламиноэтокси)-4-фенилпиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(ISP):527,2 (М+Н+).
Пример 27
(3,5-Бис-трифторметилбензил)метиламид 2-(3-диметиламинопропокси)-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,5 г (0,96 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 20 мл ацетонитрила добавляли 0,14 мл (1,16 ммоля) 2-диметиламинопропанола, 1,57 г (4,83 ммоля) Cs2CO3, и реакционную смесь перемешивали в течение 16 ч.
После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4OH, 110:10:1), при этом получали 0,50 г (95%) (3,5-бис-трифторметилбензил)метиламида 2-(3-диметиламинопропокси)-4-фенилпиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(ISP):541,2 (M+H+).
Пример 28
(3,5-Бис-трифторметилбензил)метиламид 2-метокси-4-фенилпиримидин-5-карбоновой кислоты
К суспензии 0,4 г (0,77 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-фенилпиримидин-5-карбоновой кислоты в 10 мл метанола добавляли 0,10 г (1,93 ммоля) метанолята натрия (95%) и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 40:1), при этом получали 0.23 г (63%) (3,5-бис-трифторметилбензил)метиламида 2-метокси-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 101,2-102°С.
Пример 29
(3,5-Бис-трифторметидбензил)метиламид 2-карбамоилметил-4-фенилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 3г), из 2-карбамоилметил-4-фенилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 2-карбамоилметил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 161-163°С.
Исходное соединение, 2-карбамоилметил-4-фенилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3б), из этилового эфира 2-бензоил-3-диметиламиноакриловой кислоты и гидрохлорида малонамидина, с последующим гидролизом, как описано в примере 3в), до 2-карбамоилметил-4-фенилпиримидин-5-карбоновой кислоты.
Пример 30
(3,5-Бис-трифторметилбензил)метиламид 2-цианометил-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,50 г (1,01 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-карбамоилметил-4-фенилпиримидин-5-карбоновой кислоты и 0,17 мл пиридина в 10 мл диоксана добавляли 0,15 мл (1,06 ммоля) ангидрида трифторуксусной кислоты и полученную реакционную смесь перемешивали при 50°С в течение 1 ч. Затем реакционную смесь выливали в смесь льда с водой и трижды экстрагировали 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSО4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 30:1), при этом получали 0,25 г (51%) (3,5-Бис-трифторметилбензил)метиламида2-цианометил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 114-116°С.
Пример 31
(3,5-Бис-трифторметилбензид)метиламид 2-гидроксиметил-4-фенилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 3г), из 2-гидроксиметил-4-фенилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 2-гидроксиметил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, МС(ЕI):469 (M+).
Исходное соединение, 2-гидроксиметил-4-фенилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3б), из этилового эфира 2-бензоил-3-диметиламиноакриловой кислоты и гидрохлорида 2-гидроксиацетамидина, с последующим гидролизом, как описано в примере 3в), до 2-гидроксиметил-4-фенилпиримидин-5-карбоновой кислоты.
Пример 32
(3,5-Бис-трифторметилбензид)метидамид 2-диметиламинометил-4-фенилпиримидин-5-карбоновой кислоты
а) 5-[(3,5-Бис-трифторметилбензил)метилкарбамоил]-4-фенилпиримидин-2-илметиловый эфир метансульфоновой кислоты
К раствору 2,64 г (5,62 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-гидроксиметил-4-фенилпиримидин-5-карбоновой кислоты и 1,17 мл (8,44 ммоля) триэтиламина в 30 мл CH2Cl2 при 0°С добавляли 0,479 мл (6,19 ммоля) метансульфонилхлорида и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь выливали в насыщенный раствор NаНСО3 и трижды экстрагировали 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/этилацетат, 8:1), при этом получали 2,30 г (74%) 5-[(3,5-бис-трифторметилбензил)метилкарбамоил]-4-фенилпиримидин-2-илметиловый эфир метансульфоновой кислоты в виде вязкого бесцветного масла, MC(ISP):548,1 (М+Н+).
б) (3,5-Бис-трифторметилбензил)метиламид 2-диметидаминометил-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,40 г (0,73 ммоля) 5-[(3,5-бис-трифторметилбензил)метилкарбамоил]-4-фенилпиримидин-2-илметилового эфира метансульфоновой кислоты в 5 мл СН2Сl2 добавляли 1 мл 5,6М раствора диметиламина в этаноле и реакционную смесь перемешивали при КТ в течение 16 ч. Затем реакционную смесь выливали в Н2О и трижды экстрагировали 50 мл СН2Сl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 20:1), при этом получали 0,33 г (90%) (3,5-бис-трифторметилбензил)метиламида2-диметиламинометил-4-фенилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):497,2 (М+Н+).
Пример 33
(3,5-Бис-трифторметилбензил)метиламид 2-морфолин-4-илметид-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,40 г (0,73 ммоля) 5-[(3,5-бис-трифторметилбензил)метилкарбамоил]-4-фенилпиримидин-2-илметилового эфира метансульфоновой кислоты в 5 мл СН2Сl2 добавляли 0,095 мл (1,10 ммоля) морфолина и реакционную смесь перемешивали при КТ в течение 16 ч. Затем реакционную смесь выливали в Н2О и трижды экстрагировали 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 10:1), при этом получали 0,33 г (88%) (3,5-бис-трифторметилбензил)метиламида 2-морфолин-4-илметил-4-фенилпиримидин-5-карбоновой кислоты в виде воскообразного твердого вещества светло-желтого цвета, MC(ISP):539,3 (M+H+).
Пример 34
(3,5-Бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-илметил)-4-фенилпиримидин-5-карбоновой кислоты
К раствору 0,40 г (0,73 ммоля) 5-[(3,5-бис-трифторметилбензил)метилкарбамоил]-4-фенилпиримидин-2-илметилового эфира метансульфоновой кислоты в 5 мл CH2Cl2 добавляли 0,12 мл (1,1 ммоля) N-метилпиперазина. Реакционную смесь перемешивали при КТ в течение 16 ч, затем выливали в Н2О и трижды экстрагировали 50 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 10:1), при этом получали 0,31 г (77%) (3,5-бис-трифторметилбензил)метиламида 2-(4-метилпиперазин-1-илметил)-4-фенилпиримидин-5-карбоновой кислоты в виде воскообразного твердого вещества светло-желтого цвета, MC(ISP):552,2 (M+H+).
Пример 35
(3,5-Бис-трифторметилбензил)метидамид 4-фенил-2-пиперидин-1-илметилпиримидин-5-карбоновой кислоты
К раствору 0,40 г (0,73 ммоля) 5-[(3,5-бис-трифторметилбензил)метилкарбамоил]-4-фенилпиримидин-2-илметилового эфира метансульфоновой кислоты в 5 мл CH2Cl2 добавляли 0,11 мл (1,1 ммоля) пиперидина. Реакционную смесь перемешивали при КТ в течение 16 ч, затем выливали в Н2О и трижды экстрагировали 50 мл СН2Сl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 10:1), при этом получали 0,32 г (81%) (3,5-бис-трифторметилбензил)метиламида 4-фенил-2-пиперидин-1-илметилпиримидин-5-карбоновой кислоты в виде воскообразного твердого вещества светло-желтого цвета, MC(ISP):537,2 (M+H+).
Пример 36
(3,5-Бис-трифторметилбензил)метиламид 2-имидазол-1-илметил-4-фенилпиоимидин-5-карбоновой кислоты
К раствору 0,40 г (0,73 ммоля) 5-[(3,5-бис-трифторметилбензил)метилкарбамоил]-4-фенилпиримидин-2-илметилового эфира метансульфоновой кислоты и 0,04 г (0,80 ммоля) метанолята натрия в 15 мл N,N-диметилформамида добавляли 0,59 г (0,88 ммоля) имидазола и реакционную смесь перемешивали при КТ в течение 16 ч. Затем реакционную смесь упаривали и остаток распределяли между Н2О и СН2Сl2. Водный слой дважды экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 10:1), при этом получали 0,24 г (63%) (3,5-бис-трифторметилбензил)метиламида 2-имидазол-1-илметил-4-фенилпиримидин-5-карбоновой кислоты в виде твердого вещества светло-желтого цвета, MC(ISP):520.2 (М+Н+).
Пример 37
(3,5-Бис-трифторметилбензид)метиламид 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
а) Этиловый эфир 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
К суспензии 3,81 г (46,54 ммоля) ацетата натрия и 6,47 г (23,27 ммоля) сульфата S-метилизотиомочевины в 100 мл N,N-диметилформамида одной порцией добавляли раствор 6,90 г (21,15 ммоля) этилового эфира 2-(2-бромбензоил)-3-диметиламиноакриловой кислоты в 20 мл N,N-диметилформамида и реакционную смесь перемешивали при 90°С в течение 16 ч. Затем растворитель выпаривали, остаток распределяли между 100 мл CH2Cl2 и 100 мл Н2О. Водную фазу дважды экстрагировали 100 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали.
Полученный остаток очищали хроматографией (SiO2, СН2Сl2), при этом получали 5,20 г (69%) этилового эфира 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде масла светло-зеленого цвета.
б) 4-(2-Бромфенил)-2-метилсульфанилпиримидин-5-карбоновая кислота
К раствору 5,10 г (14,4 ммоля) этилового эфира 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в 10 мл этанола добавляли 10 мл 2 н. раствора NaOH. После перемешивания в течение 1 ч к раствору желтого цвета добавляли 50 мл Н2О и 50 мл CH2Cl2, водную фазу подкисляли 25%-ной НСl до рН 1. Фазы разделяли и водную фазу дважды экстрагировали 200 мл СН2Сl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали, при этом получали 4,60 г (98%) 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде твердого вещества грязно-белого цвета.
в) (3,5-Бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
К раствору 2 г (6,15 ммоля) 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты, 1,71 мл (12,3 ммоля) триэтиламина, 0,94 г (6,15 ммоля) 1-гидроксибензотриазола и 1,17 г (6,15 ммоля) гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида в 70 мл СН2Сl2 добавляли 1,63 г (6,34 ммоля) (3,5-бис-трифторметилбензил) метиламина и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь разбавляли 50 мл СН2Сl2, промывали 50 мл 0,5 н. НСl, 50 мл Н2О, и проводили обратную экстракцию водных слоев 75 мл СН2Сl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 40:1), при этом получали 3,0 г (86%) (3,5-бис-трифторметилбензил) метиламида 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):566, 564 (М+Н+).
Пример 38
(3,5-Бис-трифторметилбензил)метидамид 4-(2-бромфенил)-2-метансульфонилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил) метиламида 4-(2-бромфенил)-2- метилсульфанилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-метансульфонилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):598, 596 (М+Н+).
Пример 39
(3,5-Бис-трифторметилбензил)метиламид 2-амино-4-(2-бромфенил)пиримидин-5-карбоновой кислоты
Через раствор 0,42 г (0,7 ммоля) (3,5-бис-трифторметилбензил)метиламида 4-(2-бромфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты в 30 мл N,N-диметилформамида пропускали NH3 в течение 10 мин и реакционную смесь перемешивали в течение 4 ч. Затем растворитель выпаривали, остаток распределяли между 20 мл CH2Cl2 и 20 мл Н2О. Водную фазу дважды экстрагировали 30 мл СН2Сl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4ОH, 140:10:1), при этом получали 0,29 г (77%) (3,5-бис-трифторметилбензил)метиламида 2-амино-4-(2-бромфенил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):535,1, 533,1 (М+Н+).
Пример 40
(3,5-Бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-(4-метидпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил)метиламида 4-(2-бромфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):618,1, 616,1 (М+Н+), из которого после взаимодействия по известному способу с фумаровой кислотой получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-(2-бромфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты (1:1), tпл 179-180°С.
Пример 41
(3,5-Бис-трифторметилбензил)метиламид(3R,5S)-4-(2-бромфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметил-бензил)метиламида 4-(2-бромфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил)метиламид (3R,5S)-4-(2-бромфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):632,0, 630,0 (М+Н+).
Пример 42
(3,5-Бис-трифторметилбензил)метиламид 4-(2-бромфенид)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида 4-(2-бромфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):603,9, 601,9 (М+Н+).
Пример 43
(3,5-Бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-морфолин-4-идпиримидин-5-кароновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметил-бензил)метиламида 4-(2-бромфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):605, 603 (М+Н+).
Пример 44
(3,5-Бис-трифторметилбензилметиламид 4-(2-хдорфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 4-(2-хлорфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил)метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(EI):519 (М+).
Исходное соединение, 4-(2-хлорфенил)-2-метилсульфанилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 37а), б), из этилового эфира 2-(2-хлорбензоил)-3-диметиламиноакриловой кислоты и сульфата S-метилизотиомочевины, с последующим гидролизом до 4-(2-хлорфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты, полученной в виде пены белого цвета.
Пример 45
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-метансульфонилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметил-бензил)метиламида 4-(2-хлорфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-метансульфонилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):552,0 (М+Н+).
Пример 46
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметил-бензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):572,1 (M+H+), из которого после взаимодействия по известному способу с фумаровой кислотой получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты (1:1), tпл 174,8-175,8°С.
Пример 47
(3,5-Бис-трифторметидбензил)метиламид (3R,5S)-4-(2-хлорфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил)метиламид (3R,5S)-4-(2-хлорфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):586,1 (М+Н+).
Пример 48
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):558,2 (М+Н+), из которого после взаимодействия по известному способу с фумаровой кислотой получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты (1:1), tпл 123-126°С.
Пример 49
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):559,1 (M+H+).
Пример 50
(3,5-Бис-трифторметидбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтиламино)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 21, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 2-диметиламиноэтиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтиламино)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):560,2 (M+H+).
Пример 51
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-морфолин-4-илэтокси)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 24, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и N-(2-гидроксиэтил) морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-морфолин-4-илэтокси)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):603,0 (M+H+).
Пример 52
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтокси)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 26, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 2-диметиламиноэтанола получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтокси)пиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):561,2 (M+H+).
Пример 53
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(3-диметиламинопропокси)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 27, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлорфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 2-диметиламинопропанола получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(3-диметиламинопропокси)пиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):575,1 (M+H+).
Пример 54
(3,5-Бис-трифторметилбензил)метиламид 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметил-бензил)метиламид 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС(ЕI):499 (M+).
Исходное соединение, 2-метилсульфанил-4-о-толилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 37а), б), из этилового эфира 2-(2-метилбензоил)-3-диметиламиноакриловой кислоты и сульфата S-метилизотиомочевины, с последующим гидролизом до 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты, полученной в виде пены белого цвета.
Пример 55
(3,5-Бис-трифторметилбензил)метиламид 2-метилсудьфонил-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)метиламид 2-метилсульфонил-4-о-толилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):532,1 (M+H+).
Пример 56
(3,5-Бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-о-толил-пиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):552,1 (М+Н+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида 2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты (1:1), tпл 151,5-152,5°C.
Пример 57
(3,5-Бис-трифторметидбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-о-толилпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил)метиламид (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):566,3 (M+H+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты (1:0,5), tпл 203,5-204,5°С.
Пример 58
(3,5-Бис-трифторметилбензил)метиламид 2-пиперазин-1-ил-4-о-тодидпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида2-метилсульфонил-4-о-толилпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил)метиламид 2-пиперазин-1-ил-4-о-толилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP): 538,3 (М+Н+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида2-пиперазин-1-ил-4-о-толилпиримидин-5-карбоновой кислоты (1:1), tпл 149,5-151,5°С.
Пример 59
(3,5-Бис-трифторметилбензил)метидамид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-о-толилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(EI):538 (M+).
Пример 60
(3,5-Бис-трифторметилбензил)метиламид 2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 26, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-о-толилпиримидин-5-карбоновой кислоты и 2-диметиламиноэтанола получали (3,5-бис-трифторметилбензил)метиламид 2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):541,2 (M+H+).
Пример 61
(3,5-Бис-трифторметилбензил)метиламид 2-(3-диметиламинопропокси)-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 27, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-о-толилпиримидин-5-карбоновой кислоты и 2-диметиламинопропанола получали (3,5-бис-трифторметилбензил)метиламид 2-(3-диметиламинопропокси)-4-о-толилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):555,2 (М+Н+).
Пример 62
(3,5-Бис-трифторметилбензил)метидамид 4-(2-метоксифенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 4-(2-метоксифенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(EI):515 (M+).
Исходное соединение, 4-(2-метоксифенил)-2-метилсульфанилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 37а), б), из этилового эфира 2-(2-метоксибензоил)-3-диметиламиноакриловой кислоты и сульфата S-метилизотиомочевины с последующим гидролизом до 4-(2-метоксифенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты, полученной в виде пены белого цвета.
Пример 63
(3,5-Бис-трифторметидбензил)метиламид 4-(2-метоксифенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил)метиламида 4-(2-метоксифенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)-метиламид 4-(2-метоксифенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):548,1 (M+H+).
Пример 64
(3,5-Бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил)метиламида 4-(2-метоксифенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):568,5(M+H+).
Пример 65
(3,5-Бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(2-метоксифенил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметилбензил)метиламида 4-(2-метоксифенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил)-метиламид (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(2-метоксифенил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):582,2 (M+H+).
Пример 66
(3,5-Бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-пиперазин-1-идпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида 4-(2-метоксифенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):554,2(М+Н+).
Пример 67
(3,5-Бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил)метиламида 4-(2-метоксифенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, tпл 190,8-192,0°С.
Пример 68
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 4-(4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС(ЕI):503 (M+).
Пример 69
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил)метиламида 4-(4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(EI):535 (M+).
Пример 70
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил) метиламида 4-(4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-(4-метилпиперазин-1-ил) пиримидин-5-карбоновой кислоты в виде пены белого цвета, МС(Е1):555 (M+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-(4-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты (1:1), tпл 144,5-145,5°C.
Пример 71
(3,5-Бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фторфенил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметилбензил)метиламида 4-(4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фторфенил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):570,2 (М+Н+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фторфенил)пиримидин-5-карбоновой кислоты (1:0,5), tпл 220-223°C.
Пример 72
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил) метиламида 4-(4-фторфенил)-2-метилсульфонил-пиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС (ISP):542,2 (М+Н+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил) метиламида 4-(4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты (1:1), tпл 155-158°С.
Пример 73
(3,5-Бис-трифторметидбензил)метиламид 4-(4-фторфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил) метиламида 4-(4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):543,2 (М+Н+).
Пример 74
(3,5-Бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 4-(2-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде твердого вещества белого цвета, tпл 109,5-110°С.
Исходное соединение, 4-(2-фторфенил)-2-метилсульфанилпиримидин-5-карбоновую кислоту, получали, как описано в примере 37а), б), из этилового эфира 2-(2-фторбензоил)-3-диметиламиноакриловой кислоты и сульфата S-метилизотиомочевины с последующим гидролизом до 4-(2-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты, полученной в виде пены белого цвета.
Пример 75
(3,5-Бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил)метиламида 4-(2-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):536,2 (М+Н+).
Пример 76
(3,5-Бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-(4-метидпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил)метиламида 4-(2-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил) метиламид 4-(2-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):556,1 (М+Н+).
Пример 77
(3,5-Бис-трифторметилбензил)метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(2-фторфенил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметилбензил)метиламида 4-(2-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил)метиламид (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(2-фторфенил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):570,2 (M+H+).
Пример 78
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида 4- (2-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС (ISP):542,2 (М+Н+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-(2-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты (1:1), tпл 124,8-125,1°С.
Пример 79
(3,5-Бис-трифторметидбензид)метидамид 4-(2-фторфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил)метиламида 4-(2-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС(ЕI):542 (М+).
Пример 80
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 4-(4-фтор-2-метилфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде твердого вещества белого цвета, МС(ЕI):517 (М+). Исходное соединение, 4-(4-фтор-2-метилфенил)-2-метилсульфанилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 37а), б), из этилового эфира 2-(4-фтор-2-метилбензоил)-3-диметиламиноакриловой кислоты и сульфата S-метилизотиомочевины с последующим гидролизом до 4-(4-фтор-2-метилфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты, полученной в виде пены белого цвета.
Пример 81
(3,5-Бис-трифторметилбензил)метидамид 4-(4-фтор-2-метилфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил)метиламида 4-(4-фтор-2-метилфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)-метиламид 4-(4-фтор-2-метилфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС(ЕI):549 (М+).
Пример 82
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил)метиламида 4-(4-фтор-2-метилфенил)2-метилсульфонилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):570,2 (M+H+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-(4-фтор-2-метилфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты (1:1), tпл 185,0-186,5°С.
Пример 83
(3,5-Бис-трифторметилбензил)метиламид (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фтор-2-метилфенил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметилбензил)метиламида 4-(4-фтор-2-метилфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил)-метиламид(3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фтор-2-метилфенил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):548,1 (M+H+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фтор-2-метилфенил)пиримидин-5-карбоновой кислоты (1:0,5), tпл 228-230°С.
Пример 84
(3,5-Бис-трифторметилбензил)метиламид 4-(4-фтор-2-метидфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида 4-(4-фтор-2-метилфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-Бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):556,1 (М+Н+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-(4-фтор-2-метилфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты (1:1), tпл 143-145°C.
Пример 85
(3,5-Бис-трифторметилбензил) метиламид 4-(4-фтор-2-метилфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил)метиламида 4-(4-фтор-2-метилфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):557,1 (M+H+).
Пример 86
(3,5-бис-трифторметилбензил)метиламид 2-метилсульфанил-4-нафталин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 2-метилсульфанил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 2-метилсульфанил-4-нафталин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС(ЕI):535 (М+).
Исходное соединение, 2-метилсульфанил-4-нафталин-1-илпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 37а), б), из этилового эфира 3-диметиламино-2-(нафталин-1-карбонил)акриловой кислоты и сульфата S-метилизотиомочевины с последующим гидролизом до 2-метилсульфанил-4-нафталин-1-илпиримидин-5-карбоновой кислоты, полученной в виде пены белого цвета.
Пример 87
(3,5-Бис-трифторметилбензил)метиламид 2-метилсульфонид-4- нафталин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфанил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)метиламид 2-метилсульфонил-4-нафталин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):568,1 (M+H+).
Пример 88
(3,5-Бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил) метиламид 2-(4-метилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты в виде твердого вещества белого цвета, tпл 170,6-170,9°С.
Пример 89
(3,5-Бис-трифторметилбензил)метиламид (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 20, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и цис-2,6-диметилпиперазина получали (3,5-бис-трифторметилбензил) метиламид (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):602,1 (M+H+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты (1:0,5), tпл 247-249°С.
Пример 90
(3,5-Бис-трифторметилбензил)метиламид 4-нафталин-1-ил-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил) метиламид 4-нафталин-1-ил-2-пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, МС (ISP):574,2 (М+Н+), из которого при взаимодействии с фумаровой кислотой по известному способу получали фумарат (3,5-бис-трифторметилбензил)метиламида 4-нафталин-1-ил-2-пиперазин-1-илпиримидин-5-карбоновой кислоты (1:1), tпл 176-178°С.
Пример 91
(3,5-Бис-трифторметилбензил)метиламид 2-морфолин-4-ил-4-нафтадин-1 -илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил)метиламида 2-метилсульфонил-4-нафталин-1-илпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 2-морфолин-4-ил-4-нафталин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):575,1 (М+Н+).
Пример 92
(3,5-Бис-трифторметилбензил)метиламид 4-фенил-2-пиридин-3-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 3г), из 4-фенил-2-пиридин-3-илпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-фенил-2-пиридин-3-илпиримидин-5-карбоновой кислоты в виде бесцветного твердого вещества, tпл 127-128°C.
Исходное соединение, 4-фенил-2-пиридин-3-илпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 3б), из этилового эфира 2-бензоил-3-диметиламиноакриловой кислоты и гидрохлорида 3-амидинопиридина с последующим гидролизом, как описано в примере 3в), до 4-фенил-2-пиридин-3-илпиримидин-5-карбоновой кислоты, МС(Е1):277 (М+).
Пример 93
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 37в), из 4-(2-хлор-4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и (3,5-бис-трифторметилбензил) метиламина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):538,1 (M+H+).
Исходное соединение, 4-(2-хлор-4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновую кислоту, получали аналогично тому, как описано в примере 37а), б), из этилового эфира 2-(2-хлор-4-фторбензоил)-3-диметиламиноакриловой кислоты и сульфата S-метилизотиомочевины с последующим гидролизом до 4-(2-хлор-4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты, полученной в виде пены белого цвета.
Пример 94
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенид)-2-метилсульфонилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 15, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлор-4-фторфенил)-2-метилсульфанилпиримидин-5-карбоновой кислоты и 3-хлорнадбензойной кислоты получали (3,5-бис-трифторметилбензил)-метиламид 4-(2-хлор-4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):570,1 (M+H+).
Пример 95
(3,5-Бис-трифторметидбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлор-4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):590,1 (M+H+).
Пример 96
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлор-4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):577,0 (M+H+).
Пример 97
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 19, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлор-4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и пиперазина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2- пиперазин-1-илпиримидин-5-карбоновой кислоты в виде пены белого цвета, MC(ISP):576,0 (М+Н+).
Пример 98
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(2-диметиламиноэтокси)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 26, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлор-4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 2-диметиламиноэтанола получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(2-диметиламиноэтокси)пиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):579,1 (M+H+).
Пример 99
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(3-диметиламинопропокси)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 27, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлор-4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и 2-диметиламинопропанола получали (3,5-бис-трифторметилбензил) метиламид 4-(2-хлор-4-фторфенил)-2-(3-диметиламинопропокси)пиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):593,1 (M+H+).
Пример 100
(3,5-Бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(2-морфолин-4-илэтокси)пиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 24, из (3,5-бис-трифторметилбензил)метиламида 4-(2-хлор-4-фторфенил)-2-метилсульфонилпиримидин-5-карбоновой кислоты и N-(2-гидроксиэтил)-морфолина получали (3,5-бис-трифторметилбензил)метиламид 4-(2-хлор-4-фторфенил)-2-(2-морфолин-4-илэтокси)пиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(ISP):621,0 (М+Н+).
Пример 101
(3,5-Диметоксибензил)метиламид 2-метидсульфанил-4-о-толилпиримидин-5-карбоновой кислоты
К раствору 3,00 г (11,52 ммоля) 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты в 70 мл СН2Сl2 добавляли 3,21 мл (23,05 ммоля) триэтиламина, 1,55 г (11,52 ммоля) 1-гидроксибензотриазола, 2,20 г (11,52 ммоля) гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида, 2,29 г (12,68 ммоля) (3,5-диметоксибензил) метиламина и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь разбавляли 100 мл СН2Сl2. промывали 100 мл 0,5н. НСl, 100 мл Н2О и проводили обратную экстракцию водных слоев 100 мл СН2Сl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH), при этом получали 4,20 г (86%) (3,5-диметоксибензил)метиламида 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):424,1 (M+H+).
Пример 102
(3,5-Диметоксибензил)метиламид 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты
К раствору 4,00 г (9,44 ммоля) (3,5-диметоксибензил)метиламида 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты в 100 мл СН2Сl2 при 5°С добавляли 5,82 г (23,61 ммоля) 3-хлорнадбензойной кислоты (70%) 30 и реакционную смесь перемешивали при КТ в течение 3 ч. После добавления 100 мл насыщенного раствора NаНСО3 слои разделяли, органическую фазу промывали насыщенным раствором NаНСО3, сушили (Na2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, СН2Сl2/этилацетат, 4:1), при этом получали 2,00 г (46%) (3,5-диметоксибензил)метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты в виде бесцветной пены, MC(ISP):456,5 (M+H+).
Пример 103
(3,5-Диметоксибензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толидпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-диметоксибензил) метиламида 2-метансульфонил-4-о-толилпиримидин-5-10 карбоновой кислоты и 1-метилпиперазина получали (3,5-диметоксибензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты в виде бесцветного масла, MC(ISP):476,3 (M+H+).
Пример 104
(3,5-Диметоксибензил)метиламид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-диметоксибензил) метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-диметоксибензил)метиламид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты в виде 20 бесцветной пены, MC(ISP):463,3 (M+H+).
Пример 105
(3,5-Диметоксибензил)метиламид 2-(2-диметиламиноэтиламино)-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 21, из (3,5-диметоксибензил) метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты и 2-диметиламиноэтиламина получали (3,5-диметоксибензил)метиламид 2-(2-диметиламиноэтиламино)-4-о-толилпиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(ISP):464,4 (M+H+).
Пример 106
(3,5-Диметоксибензил)метиламид 2-(2-диметиламиноэтокси)-4-о-толидпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 26, из (3,5-диметоксибензил)метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты и 2-диметиламиноэтанола получали (3,5-диметоксибензил)метиламид 2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, МС(ЕI):465,3 (M+H+).
Пример 107
(3,5-Диметилбензил)метиламид 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты
К раствору 2,60 г (9,99 ммоля) 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты, 2,78 мл (19,98 ммоля) триэтиламина, 1,34 г (9,99 ммоля) 1-гидроксибензотриазола и 1,91 г (9,99 ммоля) гидрохлорида N-(3-диметиламинопропил)-N’-этилкарбодиимида в 70 мл CH2Cl2 добавляли 1,78 г (11,99 ммоля) (3,5-диметоксибензил) метиламина, и реакционную смесь перемешивали в течение 16 ч. Затем реакционную смесь разбавляли 100 мл CH2Cl2, промывали 100 мл 0,5н. НСl, 100 мл Н2О и проводили обратную экстракцию водных слоев 100 мл CH2Cl2. Объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH, 40:1), при этом получали 3,20 г (82%) (3,5-диметилбензил)метиламида 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(EI):391 (M+).
Пример 108
(3,5-Диметилбензил)метиламид 2-метансульфонил-4-о-толил-пиримидин -5-карбоновой кислоты
К раствору 3,20 г (8,17 ммоля) (3,5-диметилбензил)метиламида 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты в 70 мл CH2Cl2 при 5°С добавляли 3,52 г (20,43 ммоля) 3-хлорнадбензойной кислоты (70%) и реакционную смесь перемешивали при КТ в течение 3 ч. После добавления 100 мл насыщенного раствора NаНСО3 слои разделяли, органическую фазу промывали насыщенным раствором NаНСО3, сушили (Na2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/этилацетат, 4:1), при этом получали 2,55 г (73%) (3,5-диметилбензил)метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты в виде бесцветной пены, MC(EI):423 (М+).
Пример 109
(3,5-Диметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 16, из (3,5-диметилбензил) метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты и 1-метилпиперазина получали (3,5-диметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толил-пиримидин-5-карбоновой кислоты в виде бесцветной пены, MC(ISP):444,5 (М+Н+).
Пример 110
(3,5-Диметил6ензил)метиламид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 18, из (3,5-диметилбензил) метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты и морфолина получали (3,5-диметилбензил)-метиламид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты в виде бесцветной пены, MC(EI):430 (M+).
Пример 111
(3,5-Диметилбензил)метиламид 2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-карбоновой кислоты
Аналогично тому, как описано в примере 26, из (3,5-диметилбензил) метиламида 2-метансульфонил-4-о-толилпиримидин-5-карбоновой кислоты и 2-диметиламиноэтанола получали (3,5-диметилбензил) метиламид 2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-карбоновой кислоты в виде масла светло-желтого цвета, MC(ISP):433,5 (М+Н+).
Пример 112
2-(3,5-Бис-трифторметилфенил)-N-метил-N-(2-метилсульфанил-4-о-толилпиримидин-5-ил)изобутиоамид
а) Трет-бутидовый эфир (2-метилсульфанил-4-о-толилпиримидин-5-ил)карбаминовой кислоты
К раствору 2,33 г (8,95 ммоля) 2-метилсульфанил-4-о-толилпиримидин-5-карбоновой кислоты, 1,25 мл триэтиламина (8,95 ммоля) и 1,68 мл (17,9 ммоля) трет-бутанола в 30 мл ТГФ добавляли 1,97 мл (8,95 ммоля) дифенилфосфорилазида и полученный раствор кипятили с обратным холодильником в течение 12 ч. После выпаривания растворителя остаток распределяли между CH2Cl2 и Н2О. Водную фазу дважды экстрагировали CH2Cl2, объединенные органические экстракты сушили (Na2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/этилацетат, 15:1), при этом получали 1,95 г (65%) трет-бутилового эфира (2-метилсульфанил-4-о-толилпиримидин-5-ил)карбаминовой кислоты в виде бесцветного твердого вещества, MC(TSP):331 (M+).
б) Трет-бутиловый эфир метил(2-метилсульфанил-4-о-толилпиримидин-5-ил)карбаминовой кислоты
К раствору 1,9 г (5,73 ммоля) трет-бутилового эфира (2-метилсульфанил-4-о-толилпиримидин-5-ил)карбаминовой кислоты в 15 мл N,N-диметилформамида добавляли 0,29 г (7,45 ммоля) гидрида натрия (60%-ная дисперсия в минеральном масле) и реакционную смесь перемешивали в течение 1 ч. После добавления при 0°С 0,57 мл (9,17 ммоля) метилиодида реакционную смесь перемешивали в течение 3 ч. Затем реакционную смесь распределяли между 75 мл Н2О, 75 мл солевого раствора и 75 мл CH2Cl2. Фазы разделяли и водный слой дважды промывали 75 мл CH2Cl2. Объединенные органические экстракты сушили (Na2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/этилацетат, 15:1), при этом получали 1,95 г (98%) трет-бутилового эфира метил(2-метилсульфанил-4-о-толилпиримидин-5-ил)карбаминовой кислоты в виде бесцветного масла, MC(TSP):345 (M+).
в) Метил(2-метилсульфанил-4-о-толидпиримидин-5-ил)амин
Раствор 1,95 г (5,64 ммоля) трет-бутилового эфира метил(2-метилсульфанил-4-о-толилпиримидин-5-ил)карбаминовой кислоты в 30 мл 30 МеОН/2 н. НСl перемешивали при 50°С в течение 3 ч. После выпаривания растворителя остаток распределяли между 40 мл 1 н. NaOH и 40 мл CH2Cl2. Фазы разделяли, водный слой дважды промывали 50 мл CH2Cl2. Объединенные органические экстракты сушили (Na2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/этилацетат, 10:1), при этом получали 1,30 г (94%) метил(2-метилсульфанил-4-о-толилпиримидин-5-ил)амина в виде твердого вещества белого цвета, МС(ЕI):245 (М+).
г) 2-(3.5-Бис-трифторметилфенил)-N-метил-N-(2-метилсульфанил-4-о-толилпиримидин-5-ил)изобутирамид
К раствору 1,30 г (5,3 ммоля) метил(2-метилсульфанил-4-о-толилпиримидин-5-ил)амина и 1,36 мл (7,95 ммоля) N-этилдиизопропиламина в 15 мл CH2Cl2 добавляли раствор 1,30 г (5,3 ммоля) 2-(3,5-бис-трифторметилфенил)-2-метилпропионилхлорида в 5 мл CH2Cl2 и реакционную смесь перемешивали при КТ в течение 24 ч. Затем реакционную смесь выливали в 50 мл 0,5 н. NаОН. Фазы разделяли и водный слой дважды промывали 50 мл CH2Cl2. Объединенные органические экстракты сушили (Na2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/этилацетат, 10:1), при этом получали 2,30 г (82%) 2-(3,5-бис-трифторметилфенил)-N-метил-N-(2-метилсульфанил-4-о-толилпиримидин-5-ил)изобутирамида в виде твердого вещества белого цвета, tпл 124-125°С, MC(TSP):528,2 (M+H+).
Пример 113
2-(3,5-Бис-трифторметилфенил)-N-(2-метансульфонил-4-о-толидпиримидин-5-ил)-N-метилизобутирамид
К раствору 2,20 г (4,17 ммоля) (3,5-бис-трифторметилбензил)метиламида 2-метилсульфанил-4-фенилпиримидин-5-карбоновой кислоты в 50 мл CH2Cl2 при 5°С добавляли 2,57 г (10,43 ммоля) 3-хлорнадбензойной кислоты (70%) и реакционную смесь перемешивали при КТ в течение 3 ч. После добавления 100 мл насыщенного раствора NаНСО3 слои разделяли, органичекую фазу промывали насыщенным раствором NaHCO3, сушили (Na2SO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/этилацетат, 10:1), при этом получали 2,30 г (98%) 2-(3,5-бис-трифторметилфенил)-N-(2-метансульфонил-4-о-толилпиримидин-5-ил)-N-метилизобутирамида в виде бесцветной пены, MC(ISP):560,2 (M+H+).
Пример 114
2-(3,5-Бис-трифторметилфенил)-N-метил-N-[2-(4-метилпиперазин-1-ил)-4-о-тодидпиримидин-5-ид]изобутирамид
К раствору 0,5 г (0,89 ммоля) 2-(3,5-бис-трифторметилфенил)-N-(2-метансульфонил-4-о-толилпиримидин-5-ил)-N-метилизобутирамида в 10 мл диоксана добавляли 0,25 мл (2,23 ммоля) 1-метилпиперазина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4OH, 110:10:1), при этом получали 0,37 г (71%) 2-(3,5-бис-трифторметилфенил)-N-метил-N-(2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-ил]изобутирамида в виде бесцветного твердого вещества, tпл 149-151°С, MC(ISP):580,1 (M+H+).
Пример 115
2-(3,5-Бис-трифторметилфенил)-N-метил-N-(2-морфолин-4-ил-4-о-толилпиримидин-5-ил)изобутирамид
К раствору 0,4 г (0,71 ммоля) 2-(3,5-бис-трифторметилфенил)-N-(2-метансульфонил-4-о-толилпиримидин-5-ил)-N-метил-изобутирамида в 10 мл диоксана добавляли 0,19 мл (2,14 ммоля) морфолина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл CH2Cl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/этилацетат), при этом получали 0,34 г (84%) 2-(3,5-бис-трифторметилфенил)-N-метил-N-(2-морфолин-4-ил-4-о-толилпиримидин-5-ил)изобутирамида в виде бесцветного твердого вещества, tпл 151-152°C, MC(ISP):567,1 (M+H+).
Пример 116
2-(3,5-Бис-триФторметидфенил)-N-[2-(2-диметидаминоэтиламино)-4-о-толилпиримидин-5-ил]-N-метидизобутирамид
К раствору 0,35 г (0,63 ммоля) 2-(3,5-бис-трифторметилфенил)-N-(2-метансульфонил-4-о-толилпиримидин-5-ил)-N-метилизобутирамида в 10 мл диоксана добавляли 0,20 мл (1,88 ммоля) 2-диметиламиноэтиламина и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 50 мл СН2Сl2 и 50 мл Н2О. Водный слой экстрагировали 50 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4OH), при этом получали 0,23 г (64%) 2-(3,5-бис-трифторметилфенил)-N-[2-(2-диметиламиноэтиламино)-4-о-толилпиримидин-5-ил]-N-метилизобутирамида в виде бесцветного твердого вещества, tпл 143-144°C, MC(ISP):568,3 (M+H+).
Пример 117
2-(3,5-Бис-трифторметилфенил)-N-[2-(2-диметиламиноэтокси)-4-о-толидпиримидин-5-ил]-N-метилизобутирамид
К раствору 0,4 г (0,71 ммоля) 2-(3,5-бис-трифторметилфенил)-N-(2-метансульфонил-4-о-толилпиримидин-5-ил)-N-метилизобутирамида в 15 мл ацетонитрила добавляли 0,09 мл (0,93 ммоля) 2-диметиламиноэтанола, 1,17 г (3,57 ммоля) Cs2CO3, и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 40 мл CH2Cl2 и 40 мл Н2О. Водный слой экстрагировали 40 мл СН2Сl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4OH, 110:10:1), при этом получали 0,36 г (88%) 2-(3,5-бис-трифторметилфенил)-N-[2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-ил]-N-метилизобутирамида в виде бесцветного твердого вещества, tпл 140-141°С, MC(ISP):569,2 (M+H+).
Пример 118
2-(3,5-Бис-трифторметилфенил)-N-метил-N-[2-(2-морфолин-4-илэтокси)-4-о-толилпиримидин-5-ил] изобутирамид
К раствору 0,4 г (0,71 ммоля) 2-(3,5-бис-трифторметилфенил)-N-(2-метансульфонил-4-о-толилпиримидин-5-ил)-N-метилизобутирамида в 15 мл ацетонитрила добавляли 0,12 г (0,93 ммоля) N-(2-гидроксиметил)морфолина, 1,17 г (3,57 ммоля) Сs2СО3 и реакционную смесь перемешивали в течение 16 ч. После выпаривания растворителя остаток распределяли между 40 мл СН2Сl2 и 40 мл Н2О. Водный слой экстрагировали 40 мл CH2Cl2, объединенные органические экстракты сушили (MgSO4), фильтровали и упаривали. Полученный остаток очищали хроматографией (SiO2, CH2Cl2/MeOH/NH4OH, 110:10:1), при этом получали 0,35 г (80%) 2-(3,5-бис-трифторметилфенил)-N-метил-N-[2-(2-морфолин-4-илэтокси)-4-о-толилпиримидин-5-ил]изобутирамида в виде бесцветной пены, MC(ISP):611,1 (M+H+).
Пример А
Таблетки следующего состава приготавливают обычным методом, мг/табл.:
Действующее вещество 5
Лактоза 45
Кукурузный крахмал 15
Микрокристаллическая целлюлоза 34
Стеарат магния 1
Масса таблетки 100
Пример Б
Приготавливают капсулы следующего состава, мг/капс.:
Действующее вещество 10
Лактоза 155
Кукурузный крахмал 30
Тальк 5
Масса содержимого капсулы 200
Действующее вещество, лактозу и кукурузный крахмал сначала перемешивают в смесителе, а затем обрабатывают в измельчающей машине. Смесь возвращают в смеситель, добавляют тальк и тщательно перемешивают. Смесью с помощью машины заполняют желатиновые капсулы с твердым покрытием.
Пример В
Приготавливают суппозитории следующего состава, мг/суппоз.:
Действующее вещество 15
Масса наполнителя суппозитория 1285
Всего 1300
Массу наполнителя суппозитория расплавляют в стеклянном или стальном резервуаре, тщательно перемешивают и охлаждают до 45°С. Затем к ней добавляют тонкоизмельченное действующее вещество и перемешивают до полного диспергирования. Смесью заполняют пресс-формы для суппозиториев требуемого размера, дают остыть, затем суппозитории удаляют из пресс-форм и упаковывают по отдельности в вощеную бумагу или металлическую фольгу.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ 5-ФЕНИЛПИРИМИДИНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2244710C2 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2001 |
|
RU2284997C2 |
| ПРОИЗВОДНЫЕ ДИФЕНИЛА И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2000 |
|
RU2238266C2 |
| ПРОИЗВОДНЫЕ ПИРИДИНА И ПИРИМИДИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ | 2003 |
|
RU2293731C2 |
| МОДУЛЯТОРЫ АДЕНОЗИНОВЫХ РЕЦЕПТОРОВ | 2001 |
|
RU2277911C2 |
| ПИРИМИДИНГИДРАЗИДНЫЕ СОЕДИНЕНИЯ КАК ИНГИБИТОРЫ PGDS | 2008 |
|
RU2464262C2 |
| ПИРИМИДИНАМИДНЫЕ СОЕДИНЕНИЯ КАК ИНГИБИТОРЫ PGDS | 2006 |
|
RU2420519C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ ERK2 И ИХ ИСПОЛЬЗОВАНИЕ | 2002 |
|
RU2300377C2 |
| ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ JNK | 2007 |
|
RU2493155C2 |
| ПРИМЕНЕНИЕ АНТАГОНИСТОВ РЕЦЕПТОРА NK-1 ДЛЯ ЛЕЧЕНИЯ ЧЕРЕПНО-МОЗГОВОЙ И СПИННОМОЗГОВОЙ ТРАВМЫ ИЛИ ПОВРЕЖДЕНИЯ НЕРВНОЙ ТКАНИ | 2002 |
|
RU2304435C2 |
Изобретение относится к новым производным 4-фенилпиримидина и их фармацевтически приемлемым кислотно-аддитивным солям, которые обладают свойствами антагонистов рецептора нейрокинина(NK-1), и могут быть использованы для лечения заболеваний, опосредствованных NK-1 рецептором, например, головная боль, болезнь Альцгеймера, рассеянный склероз, сердечно-сосудистых изменений, отека, хронических воспалительных заболеваний и т.д. Соединения изобретения соответствуют общей формуле
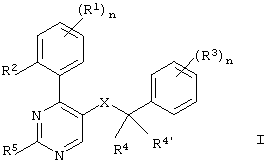
где R1 означает водород или галоген, R2 означает водород, галоген, низший алкил или низший алкокси, R1 и R2 вместе с двумя атомами углеродного цикла могут означать группу -СН=СН-СН=СН-, R3 означает галоген, трифторметил, низший алкил или низший алкокси, R4/R4’ независимо друг от друга каждый означает водород или низший алкил, R5 означает низший алкил, низший алкокси, амино, фенил, гидрокси(низший)алкил, циано(низший)алкил, карбамоил(низший)алкил, пиридил, пиримидил, -(CH2)n-пиперазинил, необязательно замещенный одной или двумя низшими алкильными группами или гидрокси(низшим)алкилом,-(CH2)n-морфолинил, -(CH2)n-пиперидинил, -(CH2)n+1-имидазолил, низший алкилсульфанил, низший алкилсульфонил, бензиламино, -NH-(CH2)n+1N(R4’’)2, -(CH2)n+1N(R4’’)2, -O-(CH2)n+1-морфолинил, -O-(CH2)n+1-пиперидинил или -O-(СН2)n+1N(R4’’)2, где R4’’ означает водород или низший алкил, и n означает 0-2,Х означает -C(O)N(R4’’)- или -N(R4’’)C(O)-. Изобретение также относится к фармацевтической композиции. 2 н. и 9 з.п. ф-лы.
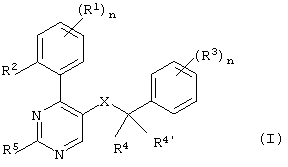
где R1 означает водород или галоген;
R2 означает водород, галоген, низший алкил или низший алкокси;
R1 и R2 вместе с двумя атомами углеродного цикла могут означать группу -СН=СН-СН=СН-;
R3 означает галоген, трифторметил, низший алкил или низший алкокси;
R4, R4’ независимо друг от друга каждый означает водород или низший алкил,
R5 означает низший алкил, низший алкокси, амино, фенил, гидрокси(низший)алкил, циано(низший)алкил, карбамоил(низший)алкил, пиридил, пиримидил, -(СH2)n-пиперазинил, необязательно замещенный одной или двумя низшими алкильными группами или гидрокси(низшим)алкилом, -(СH2)n-морфолинил, -(СH2)n-пиперидинил, -(СH2)n+1-имидазолил, низший алкилсульфанил, низший алкилсульфонил,бензиламино,-NH-(CH2)n+1 N(R4’’)2, -(CH2)n+1N(R4’’)2, -O-(CH2)n+1-морфолинил, -O-(CH2)n+1-пиперидинил или -O-(СН2)n+1N(R4’’)2,где R4’’ означает водород или низший алкил, где n = 0-2;
Х означает -C(O)N(R4’’)- или -N(R4’’)C(O)-,
и их фармацевтически приемлемые кислотно-аддитивные соли.
(3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид (3R,5S)-4-(2-бромфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-пиперазин-1 -илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид (3R,5S)-4-(2-хлорфенил)-2-(3,5-диметилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид (3R,5S)-2-(3,5-диметилпиперазин-1-ил)-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-пиперазин-1-ил-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид (3R,5R)-2-(3,5-диметилпиперазин-1-ил)-4-(2-метоксифенил) пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-фторфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид (3R,5R)-2-(3,5-диметилпиперазин-1-ил)-4-(2-фторфенил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фторфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-(4-метилпиперазин-1-ил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил) метиламид (3R,5R)-2-(3,5-диметилпиперазин-1-ил)-4-(4-фтор-2-метилфенил)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-пиперазин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-(4-метилпиперазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид (3R,5S)-2-(3,5-диметилпи-перазин-1-ил)-4-нафталин-1-илпиримидин-5-карбоновой кислоты и
(3,5-бис-трифторметилбензил)метиламид 4-нафталин-1-ил-2-пиперазин-1-илпиримидин-5-карбоновой кислоты.
(3,5-бис-трифторметилбензил)метиламид 4-(2-бромфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-морфолин-4-илэтокси)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-морфолин-4-ил-4-о-толилпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-метоксифенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(4-фтор-2-метилфенил)-2-морфолин-4-илпиримидин-5-карбоновой кислоты и
(3,5-бис-трифторметилбензил)метиламид 2-морфолин-4-ил-4-нафталин-1-илпиримидин-5-карбоновой кислоты.
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтиламино)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(2-диметиламиноэтокси)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 4-(2-хлорфенил)-2-(3-диметиламинопропокси)пиримидин-5-карбоновой кислоты,
(3,5-бис-трифторметилбензил)метиламид 2-(2-диметиламиноэтокси)-4-о-толилпиримидин-5-карбоновой кислоты или
(3,5-бис-трифторметилбензил)метиламид 2-(3-диметиламинопропокси)-4-о-толилпиримидин-5-карбоновой кислоты.
2-(3,5-бис-трифторметилфенил)-N-метил-N-[2-(4-метилпиперазин-1-ил)-4-о-толилпиримидин-5-ил]изобутирамид и
2-(3,5-бис-трифторметилфенил)-N-метил-N-(2-морфолин-4-ил-4-о-толилпиримидин-5-ил)изобутирамид.
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
Авторы
Даты
2004-12-27—Публикация
2000-05-24—Подача