Настоящее изобретение относится к химическим агентам и композициям, предназначенным для улучшения фертильности животных, особенно женских особей, обычно человека.
Ингибиторы DP-IV
Дипептидилпептидаза IV (DP-IV, а также дипептидиламинопептидаза IV, DPP-IV, DAP-IV, ЕС 3.4.14.5) представляет собой сериновую пептидазу, которая отщепляет аминоконцевой дипептид от пептидов и протеинов. Она распознает субстраты, в которых N-терминальная последовательность представляет собой Х-Рrо или Х-АIа. Ингибиторы DP-IV были предложены для использования в качестве терапевтических агентов, предназначенных для лечения воспалительных заболеваний и синдрома приобретенного иммунодефицита (СПИД). Обычно известные ингибиторы DP-IV представляют собой аналоги субстрата. Примерами ингибиторов DP-IV могут служить вещества, раскрытые в DD 296075 А5 (Neubert с сотр., ноябрь 1991), WO 91/16339 (Bachovchin с сотр., октябрь 1991), WO 93/08259 (Bachovchin с сотр., апрель 1993), WO 95/15309 (Jenkins с сотр., июнь 1995), WO 98/19998 (Villhauer, май 1998), WO 99/46272 (Scharpe с сотр., сентябрь 1999) и WO 99/61431 (Demuth с сотр., декабрь 1999). Пролекарства некоторых из указанных ингибиторов описаны также в WO 99/67278 и WO 99/67279 (обе заявки Demuth с сотр., декабрь 1999).
В следующих ниже схемах представлены основные типы соединений, являющихся ингибиторами DP-IV, а также конкретные примеры тех соединений, которые являются предпочтительными веществами настоящего изобретения; в схемах также даны ссылки на патентные документы, в которых раскрыт обширный ряд соединений, из которых выбраны указанные выше типы и примеры. Следует отметить, что все ингибиторы DP-IV, раскрытые в описаниях цитированных DD и WO заявок, могут использоваться в настоящем изобретении, и ссылки на указанные известные патентные документы приведены для полной информации, касающейся общих и более конкретных формул и рассматриваемых индивидуальных соединений. Так, например, указанные в следующей ниже таблице пирролидиновые и тиазолидиновые кольца могут быть заменены большим числом других гетероциклов с различными размерами кольца и/или, как отмечается в упомянутых публикациях, указанные аминоацильные фрагменты могут быть заменены на большое число других групп, с получением других ингибиторов DP-IV, предназначенных для использования в настоящем изобретении.
Аминоацилпирролидиды и тиазолидиды (см. DD 296075 А5), например
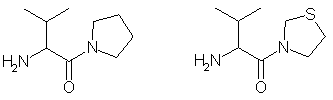
Аминоацил пирролидинальдегиды (см. DD 296075 А5 и WO 95/15309), например

Аминоацилпирролидинбороновые кислоты (см. WO 91/16339 и
WO 93/08259), например

нитрилы аминоацилпирролидина (см. WO 95/15309 и WO 98/19998), например
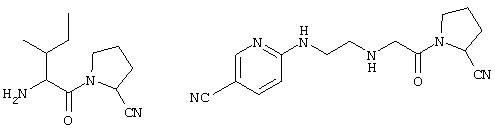
Синдром поликистоза яичников
Синдром поликистоза яичников (PCOS, синдром Штейна Левенталя) представляет собой болезненное состояние, характеризующееся уплотнением овариальной капсулы и образованием множественных фолликулярных кист. Указанное заболевание может приводить к бесплодию и аменорее. В результате нарушаются уровни циркуляции гормонов - повышается количество лютеинизирующего гормона (LH) и стероидов и понижается содержание фолликулостимулирующего гормона. Хотя предполагается, что это явление есть следствие аномальной секреции гонадотропинвысвобождающего гормона (GnRH) из гипоталамуса, физиологический дефект, лежащий в основе PCOS, остается предметом обсуждения. Применение лечебных схем, регулирующих уровни содержания LH и FSH, может приводить к успешно завершаемому оплодотворению, однако такие схемы достаточно сложны и дорогостоящи. Авторы настоящего изобретения установили, что ингибиторы DP-IV могут применятьсядля лечения PCOS.
Первый аспект настоящего изобретения относится к фармацевтической композиции, предназначенной для лечения бесплодия, причем рассматриваемая композиция отличается тем, что она включает в себя ингибитор DP-IV. Второй аспект настоящего изобретения относится к новому применению ингибиторов DP-IV для лечения бесплодия, особенно женского бесплодия, связанного с PCOS. Третий аспект настоящего изобретения относится к улучшенной схеме, обеспечивающей оплодотворение у субъектов с PCOS, причем такая схема включает в себя прием указанным субъектом композиции, содержащей ингибитор DP-IV.
Такой способ применения ингибиторов DP-IV обладает многими преимуществами над традиционными схемами лечения, включающими в себя применение агонистов GnRH, а также FSH и LH. LH и FSH представляют собой крупные пептиды, которые выделяют из природных источников (обычно из женской мочи в постклимактерический период) или готовят в культурной среде с использованием рекомбинантных клеток. При выделении из мочи необходимо обращать внимание на опасность передачи заболевания и наличие антигенных белковых примесей. В случае рекомбинантных гормонов вероятность передачи человеческих патогенов уменьшается, однако такие материалы все еще могут быть загрязнены антигенным белком, и они существенно более дорогостоящие, чем мочевые белки. Кроме этого, рекомбинантные пептиды обычно не дают картину полностью “очеловеченного” гликозилирования, что должно приводить к антигенности и пониженной эффективности. GnRH-агонисты обычно представляют собой декапептиды, получение которых требует многостадийного синтеза. В отличие от указанных выше материалов, ингибиторы DP-IV представляют собой небольшие молекулы, которые легко доступны с помощью стандартных синтетических методов. Рассматриваемые материалы не являются антигенными, их легко очищать и они характеризуются низкой стоимостью.
Другое преимущество состоит в том, что во многих случаях ингибиторы DP-IV являются биологически активными веществами при пероральном применении. Это отличает их от агонистов GnRH, FSH и LH, которые следует применять путем инъекций. Следовательно, применение ингибиторов DP-IV может осуществляться по менее инвазивной схеме, вызывающей меньший стресс у пациента.
Фармацевтическая композиция согласно настоящему изобретению особенно эффективна для лечения женского бесплодия. Предпочтительно, чтобы причиной указанного бесплодия служил синдром поликистоза яичников. Указанная композиция характеризуется тем, что она включает в себя ингибитор DP-IV. Кроме этого, рассматриваемая композиция может включать в себя такие известные в данной области фармацевтически применимые эксципиенты, как разбавители, носители, наполнители, связующие вещества, диспергаторы, стабилизаторы и т.д.
В контексте настоящего изобретения соединение считаетсяингибитором DP-IV, если оно ингибирует действие фермента при концентрации 1 мкм. Предпочтительно, когда рассматриваемое соединение ингибирует действие DP-IV при концентрации ниже 100 нМ и не ингибирует другие ферменты при концентрации ниже 1 мкМ. В следующих ниже схемах представлены основные типы ингибиторов DP-IV, а также их конкретные примеры, которые предпочтительно применять в настоящем изобретении; в схемах также приведены ссылки на патентные источники, из широкой сферы которых, касающейся раскрытых соединений, взяты указанные типы и примеры. Следует подчеркнуть, что ингибиторы DP-IV, раскрытые в описаниях цитированных DD и WO заявок, могут применяться в настоящем изобретении, и на эти документы непосредственно ссылаются для полной информации по общим и более конкретным вопросам, касающимся формул и рассматриваемых индивидуальных соединений. Так, например, в представленных ниже схемах указанные пирролидиновые и тиазолидиновые кольца могут быть заменены большим числом других гетероциклов с различными размерами кольца и/или указанные аминоацильные фрагменты, в соответствии с указанными публикациями, могут быть заменены большим числом других групп, с получением других ингибиторов DP-IV, предназначенных для использования в настоящем изобретении.
Аминоацилпирролидиды и тиазолидиды (см. DD 296075 А5), например

Аминоацилпирролидинальдегиды (см. DD 296075 А5 и WO 95/15309), например
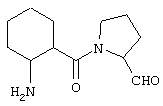
Аминоацилпирролидинбороновые кислоты (см. WO 91/16339 и
WO 93/08259), например
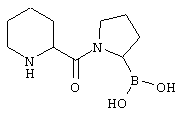
Нитрилы аминоацилпирролидина (см. WO 95/15309 и WO 98/19998), например

Согласно предпочтительному воплощению настоящего изобретения, ингибитор DP-IV представляет собой нитрил аминоацилпирролидина. Особенно предпочтительными веществами такого типа могут служить нитрилы аминоацилпирролидина, раскрытые в WO 95/15309 и WO 98/19998.
Композиции настоящего изобретения могут быть сформированы для применения на человеке любым известным методом, включая пероральное применение, введение через слизистые оболочки (например, трансбуккальное, сублингвальное, интраназальное,вагинальное и ректальное применение), трансдермальное применение или применение в виде инъекций (включая внутривенную, внутримышечную и подкожную инъекции). Предпочтительным путем применения является пероральный прием. В этом случае композицию формируют в виде таблетки или капсулы.
Настоящее изобретение предусматривает новое применение соединений, являющихся известными ингибиторами DP-IV, в качестве терапевтических агентов для лечения бесплодия, особенно женского бесплодия, связанного с синдромом поликистоза яичников.
Настоящее изобретение предусматривает улучшенный способ лечения бесплодия, особенно женского бесплодия, связанного с PCOS, согласно которому на пациенте применяют фармацевтическую композицию, включающую в себя терапевтически эффективное количество ингибитора DP-IV. Рассматриваемое лечение может включать в себя индивидуальное применение указанных соединений или их совместное применение с упомянутыми выше другими агентами. Применение может проводиться в виде разовой дозы, или в виде раздельных доз с интервалом, например, в 2-6 часов. Курс лечения может составлять один день или несколько дней или недель до достижения требуемого клинического эффекта. Примерами подходящих конечных показателей лечения могут служить оплодотворение яйцеклетки (в случае естественного оплодотворения), а также успешное образование неоплодотворенных яйцеклеток или успешная имплантация эмбриона(в случае искусственного оплодотворения). Детали, касающиеся дозировки и длительности лечения, будут определяться лечащим врачом.
Примеры
Пример 1. Приготовление ингибиторов.
Ингибиторы DP-IV могут быть получены с использованием методов, описанных в литературе. Синтез нитрилов аминоацилпирролидина описан в WO 95/15309 и WO 98/19998. Ниже описан способ, служащий иллюстрацией указанных методов.
Пример 1А - Синтез (2S)-N-изолейцилпирролидин-2-карбонитрила.
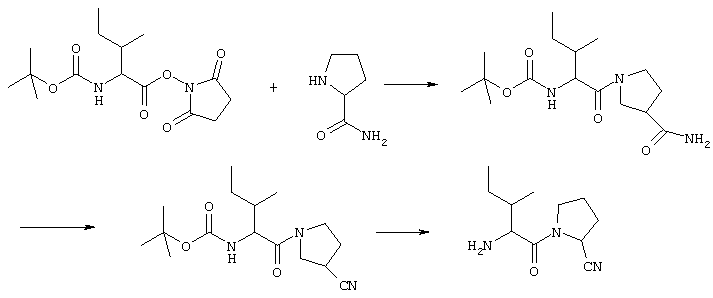
(а) трет-Бутилоксикарбонил-изолейцилпролинамид
К перемешиваемой суспензии гидрохлорида пролинамида (225 мг, 1,50 ммоля) в сухом дихлорметане (15 мл) добавляли диизопропилэтиламин с получением прозрачного основного (рН 9) раствора. В систему в виде одной порции добавляли N-(трет-бутилоксикарбонилизолейцилокси)сукцинимид (328 мг, 1,0 ммоль), и полученную смесь перемешивали в течение 16 часов при комнатной температуре в атмосфере азота. Растворитель выпаривали в вакууме, и полученный остаток распределяли между этилацетатом и 0,3 н раствором бисульфата калия. Органический слой промывали насыщенным раствором бикарбоната натрия, водой и рассолом, сушили над сульфатом натрия и концентрировали в вакууме. Полученный остаток очищали фильтрацией через тонкий слой силикагеля, проводя элюирование сначала смесью гексан/этилацетат (10:90) и затем этилацетатом. В результате концентрирования элюата, содержащего продукт, получали целевое соединение в виде бесцветной вспененной стеклообразной массы; 301 мг (92%).
Спектр 1H ЯМР (СDСl3): δ 6,90(1Н, шир.с); 5,51(1Н, шир. с); 5,18(1H,d, J=9,6 Гц); 4,62(1Н,дд, J=2,6 и 7,0 Гц); 4,29(1Н,дд, J=8,4 и 9,2 Гц); 3,79-3,58 (2Н, м); 2,36(1Н,м); 2,09-1,57(5Н,м); 1,43(9Н,с); 1,17(1Н,м); 0,95(3Н,д, J=6,6 Гц); 0,90(3Н,т, J=7,3 Гц) ч/млн.
(b) (2S)-N-(трет-Бутилоксикарбонилизолейцил)пирролидин-2-карбонитрил.
К перемешиваемому раствору амида, полученного в разделе (а) (203 мг, 0,62 ммоля), в сухом пиридине (10 мл) и в атмосфере азота добавляли имидазол (84 мг, 1,24 ммоля). Полученную смесь охлаждали до -35°С, после чего прикапывали оксихлорид фосфора (0,25 мл, 2,48 ммоля). Полученную смесь перемешивали в течение 1 часа, при этом температуре давали повышаться до -20°С, после чего растворитель удаляли в вакууме. Остаток очищали методом хроматографии на силикагеле с получением целевого соединения в виде бесцветного масла; выход 180 мг (94%).
Спектр 1H ЯМР (СDСl3): δ 5,14 (1Н, д, J=9,2 Гц); 4,80 (1Н, дд, J=2,6 и 7,1 Гц); 4,22 (1Н, дд, J=7,9 и 9,1 Гц); 3,81 (1Н, м); 3,71 (1Н, м); 2,30-2,12 (4Н, м); 1,75 (1Н, м); 1,60 (1Н, м); 1,42 (9Н, с); 1,19 (1Н, м); 0,97 (3Н, д, J=6,9 Гц); 0,91 (3H, т, J=7,3 Гц) ч/млн.
Спектр 13С ЯМР (CDCl3): δ 171,7; 155,6; 118,0; 79,6; 56,0; 46,5; 46,0; 37,8; 29,6; 28,1; 25,0; 24,2; 15,2; 10,9 ч/млн.
(с) Трифторацетат (2S)-N-(изолейцил)пирролидин-2-карбонитрила
Нитрил из раздела (b) растворяли в трифторуксусной кислоте, и полученный раствор перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в вакууме, и остаток растворяли в воде. Полученный раствор лиофилизировали с получением целевого соединения в виде белого пушистого твердого вещества; выход 60 мг.
Масс-спектр FAB: вычислено m/е 209,3; найдено 210,2 (M+H)+
Спектр 1H ЯМР (D2O): δ 4,3 (1Н, м); 3,64 (1H, д, J=5,6 Гц), 3,16 (2Н, м), 1,86-1,48 (5Н, м); 0,98 (1Н, м), 0,68 (1Н, м), 0,51 (3Н, д, J=6,9 Гц); 0,38 (3Н, т, J=7,3 Гц) ч/млн.
Спектр 13С ЯМР (D2O): δ 169,7; 119,7; 57,3; 48,6; 48,1; 36,9; 30,2; 25,8; 24,5; 15,4; 11,5; ч/млн.
Пример 1В - Синтез (2S)-N-((2’S)-2’-амино-3’,3’-диметил-бутаноил)пирролидин-2-карбонитрила
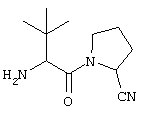
Указанное вещество получали, следуя методике, описанной в примере 1А, в результате замены производного изолейцина на соответствующее производное трет-бутилглицина.
Спектр 1H ЯМР (CD3OD): δ 4,86-4,81 (1Н, м); 4,04 (1Н, с); 3,77-3,71 (2Н, м); 3,34 (2Н, с); 2,34-2,08 (4Н, м); 1,14(9Н, с) ч/млн.
Спектр 13С ЯМР (СD3ОD): δ 167,40, 117,99, 58,78, 46,53, 34,21, 29,54, 25,22, 25,03 ч/млн.
Пример 2. Животная модель человеческого бесплодия
Диабетические жирные крысы Zucker (ZDF) считаются подходящей моделью для демонстрации потенциальной применимости терапевтических агентов в области человеческой фертильности, особенно в том, что касается PCOS. Гормональный статус рассматриваемых животных изменяется по мере того, как они начинают страдать от ожирения, что аналогично человеческим заболеваниям, в которых предполагается взаимосвязь между ожирением и PCOS.
Животные
Самцов и самок, страдающих от ожирения диабетических крыс Zucker, а также фертильных тощих самок и самцов крыс помещали в индивидуальные клетки и кормили Purina 5008 (6,5% жира). Ожиревших крыс в возрасте 6,5 недель рандомизировали на три группы:
1. Контрольная группа - страдающие ожирением крысы ZDF (n=8), получавшие носитель.
2. Лечебная группа с ежедневным приемом лекарства, страдающие ожирением крысы ZDF (n=8), получавшие перорально один раз в день соединение примера 1В (10 мг/кг/день).
3. Лечебная группа с двукратным ежедневным приемом лекарства - страдающие ожирением крысы ZDF (n=8), получавшие перорально дважды в день соединение примера 1В (10 мг/кг/день).
Методы
К концу исследования собирали образцы крови и гипофиза тощих и страдающих от ожирения крыс. Методом радиоиммунологического анализа измеряли концентрации гипофизарного LH и тестостерона в плазме крови. Эстральную цикличность оценивали исследованием вагинального мазка.
2.1 - Гипофизарный LH
Гипофизы крыс, страдающих от ожирения, содержали большее количество LH, чем гипофизы худых крыс (8,1±0,6 мг/гипофиз против 6,3±0,6 мг/гипофиз, для ожиревших и худых крыс, соответственно; р<0,05). Применение соединения Примера 1В на крысах, страдающих ожирением, нормализует содержание гипофизарного LH до значения, характерного для тощих крыс (8,1±0,6 мг/гипофиз против 5,2±0,4 мг/гипофиз для контрольных и обработанных ожиревших крыс, соответственно, р<0,05).
2.2 - Тестостерон плазмы
Уровни содержания тестостерона в плазме самцов крыс с ожирением были ниже, чем у самцов худых крыс (1145+328 нг/мл против 2410+239 нг/мл, для крыс с ожирением и худых крыс, соответственно; р<0,05). Обработка крыс с ожирением соединением примера 1В нормализует уровни тестостерона в плазме до значений, наблюдаемых у худых крыс (2410±239 нг/мл против 2392±759 нг/мл, для худых крыс и крыс, страдающих ожирением, соответственно, NS).
2.3 - Цикличность
Самки крыс, страдающих ожирением, имели аномальную эстральную цикличность в сравнении с худыми крысами. Обработка соединением примера 1В нормализует эстральную цикличность у самок крыс, страдающих ожирением.
Представленные выше результаты показывают, что ингибиторы DP-IV являются полезными веществами для лечения бесплодия у объектов как мужского, так и женского полов, в особенности при симптомах PCOS.
Пример 3. Фармацевтическая рецептура
3А - 50 мг таблетка
Таблетки, содержащие эквивалент, соответствующий 50 мг соединения примера 1А, в качестве активного агента, готовили из следующих ингредиентов:
Соединение Примера 1А (в виде соли трифторуксусной кислоты) 154,5 г
Пшеничный крахмал 53,5 г
Гидроксипропилцеллюлоза 13,5 г
Карбоксиметилцеллюлоза кальция 11,0 г
Стеарат магния 2,0 г
Лактоза 165
Всего 400,0 г
Указанные материалы смешивали и затем прессовали с получением 2000 таблеток по 200 мг, каждая из которых содержала эквивалент, соответствующий 50 мг соединения примера 1А в виде свободного основания.
3В - 100 мг вагинальные свечи
Свечи, подходящие для вагинального применения и содержащие эквивалент, соответствующий 100 мг соединения Примера 1А в качестве активного агента, готовили из следующих ингредиентов:
Соединение Примера 1А (в виде соли трифторуксусной кислоты) 154,5 г
Пшеничный крахмал 210,0 г
Коллоидный оксид кремния 2,5 г
Povidone 30 49,0 г
Стеарат магния 23,0 г
Адипиновая кислота 57,0 г
Бикарбонат натрия 43,0 г
Лаурилсульфат натрия 5,0 г
Лактоза 456,0
Всего 1000,0 г
Перечисленные материалы смешивали друг с другом и затем прессовали с получением 1000 свечей массой в 1 г, каждая из которых содержала эквивалент, соответствующий 100 мг соединения Примера 1А в виде свободного основания.
Приведенные выше примеры лишь иллюстрируют изобретение, раскрытое в настоящем документе, и не носят ограничительного характера. Некоторые расширения, рассматриваемые специалистом в данной области как эквивалентные, охватываются сферой настоящего изобретения и формулы изобретения, которая дополнительно определяет сферу притязаний.
Один или более ингибиторов DP-IV могут использоваться в качестве единого компонента, обладающего активностью, касающейся указанных предназначений рассматриваемой композиции и способа настоящего изобретения.
Изобретение относится к химико-фармацевтической промышленности и касается применения ингибитора дипептидилпептидазы IV при получении терапевтической композиции для усиления фертильности, лечения бесплодия при наличии синдрома поликистоза яичников. Заявляемые соединения обладают высокой эффективностью при лечении бесплодия, вызванного синдромом поликистоза яичников, при эффективном количестве активного ингредиента 1 мкМ. При введении ингибитора дипептидилпептидазы IV происходит нормализация уровня лютеинизирующего гормона и тестостерона в крови, заявленные соединения являются малотоксичными для теплокровных животных и человека. 6 з.п. ф-лы.
| Д.А.Харкевич, “Фармакология”, М.: “Медицина”, 1987г., стр | |||
| Способ очищения сернокислого глинозема от железа | 1920 |
|
SU47A1 |
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| реф | |||
| Bongers J, Lambros Т, Ahmad М, Heimer ЕР, Kinetics of dipeptidyl peptidase IV proteolysis of growth hormone-releasing factor and anaogs | |||
| Biochim Biophys Acta | |||
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
| RU 96122010 А, 20.01.1999. | |||
Авторы
Даты
2005-02-27—Публикация
2000-03-21—Подача