Настоящее изобретение относится к соединениям формулы I:
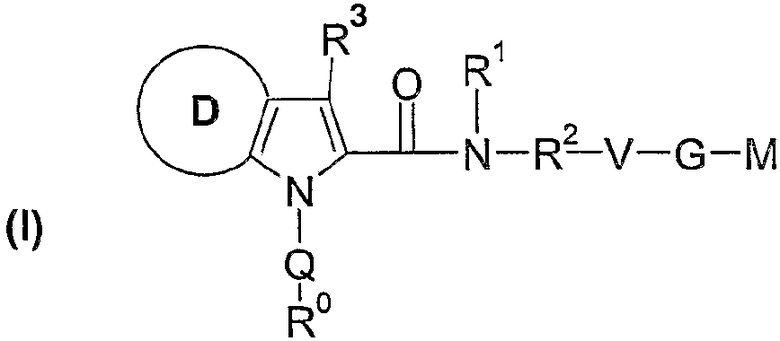
где R0; R1; R2; R3; Q; V, G и M имеют значения, указанные ниже. Соединения формулы I представляют собой ценные фармакологически активные соединения. Они проявляют сильный антитромботический эффект и подходят, например, для лечения и профилактики сердечно-сосудистых расстройств, подобных тромбоэмболическим заболеваниям или рестенозам. Они представляют собой обратимо действующие ингибиторы ферментов свертывания крови фактора Xa (FXa) и/или фактора VIIa (FVIIA), и могут в целом применяться при состояниях, при которых присутствует нежелательная активность фактора Xa и/или фактора VIIa, или для лечения или предотвращения которых предполагается ингибирование фактора Xa и/или фактора VIIa. Изобретение, кроме того, относится к способам получения соединений формулы I, их применению, в частности, в качестве активных ингредиентов в фармацевтических средствах и к фармацевтическим препаратам, включающим их.
Нормальный гемостаз является результатом сложного баланса между процессом инициации, образования тромба и растворения тромба. Сложные взаимодействия между клетками крови, специфическими белками плазмы и сосудистой поверхностью поддерживают текучесть крови до тех пор, пока не происходит повреждение и потеря крови (ЕР-А-987274). Многие существенные патологические состояния связаны с аномальным гемостазом. Например, локальное формирование тромба вследствие разрыва атеросклеротической бляшки является основной причиной острого инфаркта миокарда и нестабильной стенокардии. Лечение окклюзивного коронарного тромба либо тромболитической терапией, либо чрескожной ангиопластикой может сопровождаться острым тромботическим повторным закрытием пораженного сосуда.
Сохраняется потребность в безопасных и эффективных антикоагулянтах для ограничения или предотвращения образования тромба. Наиболее желательно создать средства, которые ингибируют свертывание, не оказывая прямого ингибирующего действия на тромбин, но путем ингибирования других стадий в каскаде свертываемости, подобных активности фактора Ха и/или фактора VIIa. В настоящее время считается, что ингибиторы фактора Ха связаны с более низким риском кровотечения, чем ингибиторы тромбина (A.E.P.Adang & J.B.M.Rewinkel, Drugs of the Future 2000, 25, 369-383).
Специфичные для фактора Ха ингибиторы свертывания крови с низкой молекулярной массой, которые эффективны, но не вызывают нежелательные побочные эффекты, были описаны, например, в документе WO-A-95/29189. Однако кроме эффективности в качестве специфичного для фактора Ха ингибитора свертывания крови, желательно, чтобы такие ингибиторы также имели дополнительные преимущественные свойства, например устойчивость в плазме и печени и избирательность, по сравнению с другими протеазами серина, ингибирование которых не предполагается, такими как тромбин. Сохраняется потребность в дополнительных специфичных для фактора Ха ингибиторах свертывания крови с низкой молекулярной массой, которые эффективны, а также имеют указанные выше преимущества.
Специфичное ингибирование каталитического комплекса фактора VIIa/тканевого фактора с использованием моноклональных антител (WO-A-92/06711) или белка, такого как фактор VIIa, инактивированного хлорметилкетоном (WO-A-96/12800, WO-A-97/47651), представляет собой крайне эффективное средство борьбы с образованием тромба, вызванным острым повреждением артерий или с тромботическими осложнениями, связанными с бактериальной септицемией. Имеется также экспериментальное доказательство, свидетельствующее о том, что ингибирование фактора VIIa/тканевого фактора ингибирует рестеноз после баллонной ангиопластики. Исследования кровотечения, проводимые у бабуинов, указывают на то, что ингибирование комплекса фактора VIIa/тканевого фактора имеет самый широкий диапазон безопасности в отношении терапевтической эффективности и риска кровотечения любого испытанного подхода с использованием антикоагулянтов, включая ингибирование тромбина, тромбоцитов и фактора Ха. Определенные ингибиторы фактора VIIa были уже описаны. В документе ЕР-А-987274, например, раскрываются соединения, содержащие трипептидную единицу, которые ингибируют фактор VIIa. Однако профиль свойств этих соединений еще не идеален, и сохраняется потребность в дальнейших имеющих низкую молекулярную массу ингибиторах свертываемости крови, ингибрующих фактор VIIa.
Настоящее изобретение удовлетворяет этим потребностям предоставлением новых соединений формулы I, которые проявляют более высокую ингибирующую активность в отношении фактора Ха/фактора VIIa и представляют собой благоприятные средства с высокой биологической доступностью.
(1) Таким образом, настоящее изобретение относится к соединениям формулы I,

где R0 представляет собой
1) моноциклический или бициклический 6-14-членный арил, где арил является моно-, ди- или тризамещенным, независимо друг от друга, R8,
2) моноциклический или бициклический 4-15-членный гетероциклил, выбранный из группы бензимидазолила, 1,3-бензодиоксолила, бензофуранила, бензоксазолила, бензотиазолила, бензотиофенила, циннолинила, хроманила, индазолила, индолила, изохроманила, изоиндолила, изохинолинила, фенилпиридила, фталазинила, птеридинила, пуринила, пиридила, пиридоимидазолила, пиридопиридинила, пиридопиримидинила, пиримидинила, хиназолинила, хинолила, хиноксалинила или 1,4,5,6-тетрагидропиридазинила, где указанный гетероциклил является моно-, ди- или тризамещенным, независимо друг от друга, R8, или
3) моноциклический или бициклический 4-15-членный гетероциклил, содержащий 1, 2, 3 или 4 гетероатома, выбранных из азота, серы или кислорода, где указанный гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8, и который является дополнительно замещенным моноциклическим или бициклическим 4-15-членным гетероциклилом, содержащим 1, 2, 3 или 4 гетероатома, выбранных из азота, серы или кислорода, где
гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8,
R8 представляет собой
1) галоген,
2) -NO2,
3) -CN,
4) -C(O)-NH2,
5) -OH,
6) -NH2,
7) -O-CF3
8) моноциклический или бициклический 6-14-членный арил, где арил является моно-, ди- или тризамещенным, независимо друг от друга галогеном или -O-(C1-C8)-алкилом,
9) -(C1-C8)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, галогеном, NH2, -ОН или метоксиостатком,
10) -O-(C1-C8)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, галогеном, NH2, -ОН или метоксиостатком,
11) -SO2-CH3 или
12) -SO2-CF3,
при условии, что R8 представляет собой, по меньшей мере, один из галогена, -C(O)-NH2 или -O-(C1-C8)-алкильного остатка, если R0 представляет собой моноциклический или бициклический 6-14-членный арил,
подструктура

в формуле I представляет собой
4-8-членную насыщенную, частично ненасыщенную или ароматическую циклическую группу, содержащую 0, 1, 2, 3 или 4 гетероатома, выбранных из азота, серы или кислорода, незамещенную или замещенную 1, 2, 3, 4, 5 или 6 R3, или замещенную 1 или 2 =О, при условии, что указанная циклическая группа не является фенильным остатком,
Q представляет собой прямую связь, -(C0-C2)-алкилен-C(O)-NR10-, -NR10-C(O)-NR10-, -NR10-C(O)-, -SO2-, -(C1-C6)-алкилен, -(CH2)m-NR10-C(O)-NR10-(CH2)n-, -(CH2)m-NR10-C(O)-(CH2)n-, -(CH2)m-S-(CH2)n-, -(CH2)m-C(O)-(CH2)n-, -(CH2)m-SO2-NR10-(CH2)n-, -(CH2)m-NR10-SO2-(CH2)n-, -(CH2)m-NR10-SO2-NR10-(CH2)n-, -(CH2)m-CH(OH)-(CH2)n-, -(CH2)m-O-C(O)-NR10-(CH2)n-, -(C2-C3)-алкилен-O-(C0-C3)-алкилен, -(C2-C3)-алкилен-S(O)-, -(C2-C3)-алкилен-S(O)2-, -(CH2)m-NR10-C(O)-О-(CH2)n-, -(C2-C3)-алкилен-S(O)2-NH-(R10)-, -(C2-C3)-алкилен-N-(R10)- или -(C0-C3)-алкилен-C(O)-O-(CH2)m-,
где R10 имеет значения, определенные ниже, и n и m независимо друг от друга являются одинаковыми или различными и представляют собой целые числа 0, 1, 2, 3, 4, 5 или 6, где алкиленовые остатки, которые образованы -(CH2)m- или -(CH2)n-, являются незамещенными или моно-, ди- или тризамещенными независимо друг от друга галогеном, -NH2 или -ОН; или -(C3-C6)-циклоалкиленом, где циклоалкилен является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, галогеном, -NH2 или -ОН;
R1 представляет собой атом водорода, -(C1-C4)-алкил, где алкил является незамещенным или замещенным 1-3 раза R13; -(C1-C3)-алкилен-C(O)-NH-R0, -(C1-C3)-алкилен-C(O)-O-R10, моноциклический или бициклический 6-14-членный арил, где арил является моно-, ди- или тризамещенным, независимо друг от друга, R8, где R8 имеет значения, определенные выше; моноциклический или бициклический 4-15-членный гетероциклил, содержащий 1, 2, 3 или 4 гетероатома, выбранных из азота, серы или кислорода; -(C1-C3)-перфторалкилен, -(C1-C3)-алкилен-S(O)-(C1-C4)-алкил, -(C1-C3)-алкилен-S(O)2-(C1-C3)-алкил, -(C1-C3)-алкилен-S(O)2-N(R4')-R5', -(C1-C3)-алкилен-O-(C1-C4)-алкил, -(C0-C3)-алкилен-(C3-C8)-циклоалкил, или -(C0-C3)-алкилен-het, где het представляет собой 3-7-членный циклический остаток, содержащий до 1, 2, 3 или 4 гетероатомов, выбранных из азота, серы или кислорода, где указанный циклический остаток является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
R4'и R5' независимы друг от друга и являются одинаковыми или различными и представляют собой атом водорода или -(C1-C4)-алкил,
R2 представляет собой прямую связь или -(C1-C4)-алкилен, или
R1 и R3 вместе с атомами, с которыми они связаны, могут образовать 6-8-членную циклическую группу, содержащую 1, 2, 3 или 4 гетероатома, выбранных из азота, серы или кислорода, где указанная циклическая группа является незамещенной или моно-, ди- или тризамещенной, независимо друг от друга, R14, или
R1-N-R2-V могут образовать 4-7-членную циклическую группу, содержащую 1, 2, 3 или 4 гетероатома, выбранных из азота, серы или кислорода, где указанная циклическая группа является незамещенной или моно-, ди- или тризамещенной, независимо друг от друга, еще одним R14,
R14 представляет собой галоген, -OH, =O, -(C1-C8)-алкил, -(C1-C4)-алкокси, -NO2-, -C(O)-OH-, -CN, -NH2, -C(O)-O-(C1-C4)-алкил, -(C0-C8)-алкил-SO2-(C1-C4)-алкил, -(C0-C8)-алкил-SO2-(C1-C3)-перфторалкил, -(C0-C8)-алкил-SO2-N(R18)-R21, -C(O)-NH-(C1-C8)-алкил, -C(O)-N-[(C1-C8)-алкил]2, NR18-C(O)-NH-(C1-C8)-алкил, -C(O)-NH2, -S-R18, или NR18-C(O)-NH-[(C1-C8)-алкил]2,
где R18 и R21 представляют собой, независимо друг от друга, атом водорода, -(C1-C3)-перфторалкил или -(C1-C6)-алкил,
V представляет собой
1) 3-7-членный циклический остаток, содержащий 1-4 гетероатома, выбранных из азота, серы или кислорода, где указанный циклический остаток является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
2) 6-14-членный арил, где арил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14, или
3) моноциклический или бициклический 4-15-членный гетероциклил, где указанный гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
G представляет собой прямую связь, -(CH2)m-NR10-SO2-NR10-(CH2)n-, -(CH2)m-CH(OH)-(CH2)n-, -(CH2)m-, -(CH2)m-O-(CH2)n-, -(CH2)m-C(O)-NR10-(CH2)n-, -(CH2)-SO2-(CH2)n-, -(CH2)m-NR10-C(O)-NR10-(CH2)n-, -(CH2)m-NR10-C(O)-(CH2)n-, -(CH2)m-C(O)-(CH2)n-, -(CH2)-S-(CH2)n-, -(CH2)m-SO2-NR10-(CH2)n-, -(CH2)m-NR10-SO2-(CH2)n-, -(CH2)m-NR10-, -(CH2)m-O-C(O)-NR10-(CH2)n- или -(CH2)m-NR10-C(O)-O-(CH2)n-,
n и m независимо друг от друга являются одинаковыми или различными и представляют собой целые числа 0, 1, 2, 3, 4, 5 или 6,
М представляет собой
1) атом водорода,
2) -(C1-C8)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
3) -C(O)-N(R11)-R12,
4) -(CH2)m-NR10,
5) 6-14-членный арил, где арил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
6) моноциклический или бициклический 4-15-членный гетероциклил, где гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
7) -(C3-C8)-циклоалкил, где указанный циклоалкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
8) 3-7-членный циклический остаток, содержащий 1, 2, 3 или 4 гетероатома, выбранных из азота, серы или кислорода, где указанный циклический остаток является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14, где R14 имеет значения, определенные выше,
R3 представляет собой
1) атом водорода,
2) галоген,
3) -(C1-C4)-алкил, где указанный алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
4) -(C1-C3)-перфторалкил,
5) фенил, где фенил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
6) -(C0-C4)-алкилен-O-R19, где R19 представляет собой
а) атом водорода,
b) -(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
с) -CF3 или
d) -CHF2,
7) -NO2,
8) -CN,
9) -SOs-R11, где s равно 1 или 2,
10) -SOt-N(R11)-R12, где t равно 1 или 2,
11) -(C0-C4)-алкилен-С(O)-R11,
12) -(C0-C4)-алкилен-С(O)-O-R11,
13) -(C0-C4)-алкилен-С(O)-N(R11)-R12,
14) -(C0-C4)-алкилен-N(R11)-R12,
15) -NR10-SO2-R10,
16) -S-R10,
17) -(C0-C2)-алкилен-С(O)-O-(C2-C4)-алкилен-O-С(O)-(C1-C4)-алкил,
18) -C(O)-O-C(R15, R16)-O-C(O)-R17,
19) -(C0-C2)-алкилен-С(O)-O-(C2-C4)-алкилен-O-С(O)-O-(C1-C6)-алкил,
20) -C(O)-O-C(R15, R16)-O-C(O)-O-R17,
21) -(C0-C4)-алкилен-(C6-C14)-арил, где арил является моно-, ди- или тризамещенным, независимо друг от друга, R13,
22) -(C0-C4)-алкилен-(C4-C15)-гетероциклил, где гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
23) -(C0-C4)-алкилен-(C3-C8)-циклоалкил, где циклоалкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
24) -(C0-C4)-алкилен-het, где het является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
25) -(C0-C3)-алкилен-O-CH2-(C1-C3)-перфторалкилен-CH2-O-(C0-C4)-алкил,
26) -SOw-N(R11)-R13, где w равно 1 или 2,
27) -(C0-C4)-алкилен-C(O)-N(R11)-R13,
28) -(C0-C4)-алкилен-N(R11)-R13, или
29) остаток из следующего перечня
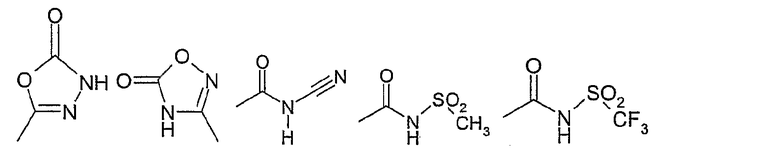
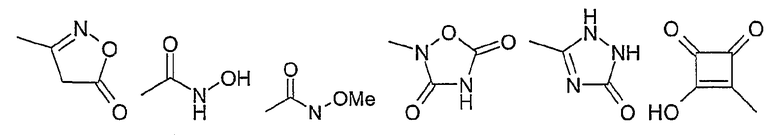
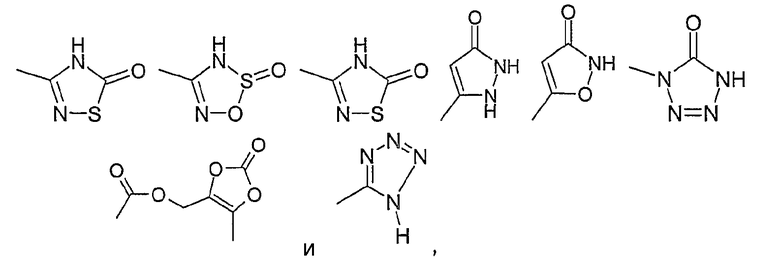
где Ме представляет собой метил, или
если 2 остатка -OR19 присоединены к соседним атомам, они могут образовывать вместе с атомами, к которым они присоединены, 5- или 6-членное кольцо, которое является незамещенным или замещенным от 1 до 4 R13,
R11 и R12 независимо друг от друга являются одинаковыми или различными и представляют собой
1) атом водорода,
2) -(C1-C6)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
3) -(C0-C6)-алкил-(C3-C6)-циклоалкил,
4) -SOt-R10, где t равно 1 или 2,
5) -(C0-C6)-алкил-(C6-C14)-арил, где алкил и арил независимо друг от друга являются незамещенными или моно-, ди- или тризамещенными R13,
6) -(C1-C3)-перфторалкил,
7) -O-R17, или
8) -(C0-C6)-алкил-(C4-C15)-гетероциклил, где алкил и гетероциклил имеют значения, определенные выше, и являются независимо друг от друга незамещенными или моно-, ди- или тризамещенными R13, или
R11 и R12 вместе с атомом азота, с которым они связаны, образуют 4-7-членное моноциклическое гетероциклическое кольцо которое, в дополнение к атому азота, может содержать 1 или 2 одинаковых или различных кольцевых гетероатома, выбранных из кислорода, серы и азоты; где указанное гетероциклическое кольцо является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
R13 представляет собой галоген, -NO2, -CN, =O, -OH, -CF3, -C(O)-O-R10, -C(O)-N-(R10)-R20, -N(R10)-R20, -(C3-C8)-циклоалкил, -(C0-C3)-алкилен-O-R10, -Si-(CH3)3, -N(R10)-S(O)u-R10, где u равно 1 или 2, -S-R10, -SOr-R10, где r равно 1 или 2, -S(O)v-N(R10)- R20, где v равно 1 или 2, -C(O)-R10, -(C1-C8)-алкил, -(C1-C8)-алкокси, фенил, фенилокси-, O-CF3, -(C0-C4)-алкил-C(O)-O-C(R15, R16)-O-C(O)-R17, -(C1-C4)-алкоксифенил, -(C0-C4)-алкил-C(O)-O-C(R15, R16)-O-C(O)-R17, -(C1-C3)-перфторалкил, -O-R15, -NH-C(O)-NH-R10, -NH-C(O)-O-R10, или остаток из следующего перечня
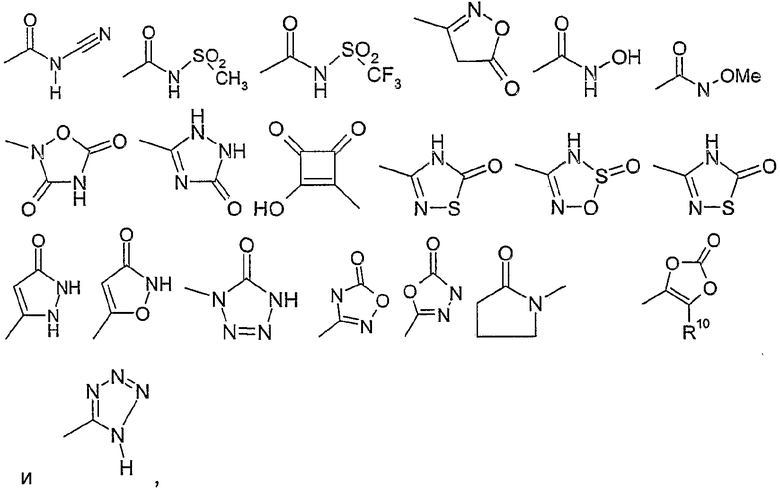
где Ме представляет собой метил,
R10 и R20 представляют собой, независимо друг от друга, водород, -(C1-C6)-алкил, -(C0-C4)-алкил-ОН, -(C0-C4)-алкил-О-(C1-C4)-алкил или -(C1-C3)-перфторалкил,
R15 и R16 представляют собой, независимо друг от друга, водород, -(C1-C6)-алкил, или вместе с атомом углерода, с которым они связаны, могут образовывать 3-6-членное карбоциклическое кольцо, которое является незамещенным или замещенным от 1 до 3 R10, и
R17 представляет собой -(C1-C6)-алкил, -(C1-C6)-алкил-ОН, -(C1-C6)-алкил-О-(C1-C6)-алкил, -(C3-C8)-циклоалкил, -(C1-C6)-алкил-О-(C1-C8)-алкил-(C3-C8)-циклоалкил, -(C1-C6)-алкил-(C3-C8)-циклоалкил, где указанное циклоалкильное кольцо является незамещенным или замещенным 1, 2 или 3 -ОН,
-О-(C1-C4)-алкил или R10,
во всех его стереоизомерных формах в любом соотношении и его физиологически приемлемые соли.
(2) Таким образом, настоящее изобретение относится к соединениям формулы I, где
R0 представляет собой
1) моноциклический или бициклический 6-14-членный арил, выбранный из фенила, нафтила, бифенилила, антрила или флуоренила, где арил является моно-, ди- или тризамещенным, независимо друг от друга, R8.
2) гетероциклил, выбранный из бензимидазолила, 1,3-бензодиоксолила, бензофуранила, бензоксазолила, бензотиазолила, бензотиофенила, циннолинила, хроманила, индазолила, индолила, изохроманила, изоиндолила, изохинолинила, фенилпиридила, фталазинила, птеридинила, пуринила, пиридила, пиридоимидазолила, пиридопиридинила, пиридопиримидинила, пиримидинила, хиназолинила, хинолила, хиноксалинила или 1,4,5,6-тетрагидропиридазинила, где указанный гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8, или
3) гетероциклил, где гетероциклил выбран из группы, состоящей из акридинила, азабензимидазолила, азаспиродеканила, азепинила, азетидинила, азиридинила, бензимидазолила, бензофуранила, бензотиофуранила, бензотиофенила, бензоксазолила, бензтиазолила, бензтриазолила, бензтетразолила, бензизоксазолила, бензизотиазолила, карбазолила, 4аН-карбазолила, карболинила, хроманила, хроменила, циннолинила, декагидрохинолинила, 4,5-дигидрооксазолинила, диоксазолила, диоксазинила, 1,3-диоксоланила, 1,3-диоксоленила, 6Н-1,5,2-дитиазинила, дигидрофтор[2,3-b]-тетрагидрофуранила, фуранила, фуразанила, имидазолидинила, имидазолинила, имидазолила, 1Н-индазолила, индолинила, индолизинила, индолила, 3Н-индолила, изобензофуранила, изохроманила, изоиндазолила, изоиндолинила, изоиндолила, изохинолинила, изотиазолила, изотиазолидинила, изотиазолинила, изоксазолила, изоксазолинила, изоксазолидинила, 2-изоксазолинила, кетопиперазинила, морфолинила, нафтиридинила, октагидроизохинолинила, оксадиазолила, 1,2,3-оксадиазолила, 1,2,4-оксадиазолила, 1,2,5-оксадиазолила, 1,3,4-оксадиазолила, 1,2-оксатиепанила, 1,2-оксатиоланила, 1,4-оксазепанила, 1,2-оксазинила, 1,3-оксазинила, 1,4-оксазинила, оксазолидинила, оксазолинила, оксазолила, фенантридинила, фенантролинила, феназинила, фенотиазинила, феноксатиинила, феноксазинила, фталазинила, пиперазинила, пиперидинила, птеридинила, пуринила, пиранила, пиразинила, пиразолидинила, пиразолинила, пиразолила, пиридазинила, пиридооксазолила, пиридоимидазолила, пиридотиазолила, пиридила, пиримидинила, пирролидинила, пирролидинонила, пирролинила, 2Н-пирролила, пирролила, хиназолинила, хинолинила, 4Н-хинолизинила, хиноксалинила, хинуклидинила, тетрагидрофуранила, тетрагидроизохинолинила, тетрагидрохинолинила, 1,4,5,6-тетрагидропиридазинила, тетрагидропиридинила, тетрагидротиофенила, тетразинила, тетразолила, 6Н-1,2,5-тиадиазинила, 1,2,3-тиадиазолила, 1,2,4-тиадиазолила, 1,2,5-тиадиазолила, 1,3,4-тиадиазолила, тиантренила, 1,2-тиазинила, 1,3-тиазинила, 1,4-тиазинила, 1,3-тиазолила, тиазолила, тиазолидинила, тиазолинила, тиенила, тиетанила, тиенотиазолила, тиенооксазолила, тиеноимидазолила, тиетанила, тиоморфолинила, тиофенолила, тиофенила, тиопиранила, 1,2,3-триазинила, 1,2,4-триазинила, 1,3,5-триазинила, 1,2,3-триазолила, 1,2,4-триазолила, 1,2,5-триазолила, 1,3,4-триазолила и ксантенила,
где указанный гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8, и
который дополнительно замещен гетероциклилом, выбранным из группы, состоящей из акридинила, азабензимидазолила, азаспиродеканила, азепинила, азетидинила, азиридинила, бензимидазолила, бензофуранила, бензотиофуранила, бензотиофенила, бензоксазолила, бензтиазолила, бензтриазолила, бензтетразолила, бензизоксазолила, бензизотиазолила, карбазолила, 4аН-карбазолила, карболинила, хроманила, хроменила, циннолинила, декагидрохинолинила, 4,5-дигидрооксазолинила, диоксазолила, диоксазинила, 1,3-диоксоланила, 1,3-диоксоленила, 6Н-1,5,2-дитиазинила, дигидрофтор[2,3-b]-тетрагидрофуранила, фуранила, фуразанила, имидазолидинила, имидазолинила, имидазолила, 1Н-индазолила, индолинила, индолизинила, индолила, 3Н-индолила, изобензофуранила, изохроманила, изоиндазолила, изоиндолинила, изоиндолила, изохинолинила, изотиазолила, изотиазолидинила, изотиазолинила, изоксазолила, изоксазолинила, изоксазолидинила, 2-изоксазолинила, кетопиперазинила, морфолинила, нафтиридинила, октагидроизохинолинила, оксадиазолила, 1,2,3-оксадиазолила, 1,2,4-оксадиазолила, 1,2,5-оксадиазолила, 1,3,4-оксадиазолила, 1,2-оксатиепанила, 1,2-оксатиоланила, 1,4-оксазепанила, 1,2-оксазинила, 1,3-оксазинила, 1,4-оксазинила, оксазолидинила, оксазолинила, оксазолила, фенантридинила, фенантролинила, феназинила, фенотиазинила, феноксатиинила, феноксазинила, фталазинила, пиперазинила, пиперидинила, птеридинила, пуринила, пиранила, пиразинила, пиразолидинила, пиразолинила, пиразолила, пиридазинила, пиридооксазолила, пиридоимидазолила, пиридотиазолила, пиридила, пиримидинила, пирролидинила, пирролидинонила, пирролинила, 2Н-пирролила, пирролила, хиназолинила, хинолинила, 4Н-хинолизинила, хиноксалинила, хинуклидинила, тетрагидрофуранила, тетрагидроизохинолинила, тетрагидрохинолинила, 1,4,5,6-тетрагидропиридазинила, тетрагидропиридинила, тетрагидротиофенила, тетразинила, тетразолила, 6Н-1,2,5-тиадиазинила, 1,2,3-тиадиазолила, 1,2,4-тиадиазолила, 1,2,5-тиадиазолила, 1,3,4-тиадиазолила, тиантренила, 1,2-тиазинила, 1,3-тиазинила, 1,4-тиазинила, 1,3-тиазолила, тиазолила, тиазолидинила, тиазолинила, тиенила, тиетанила, тиенотиазолила, тиенооксазолила, тиеноимидазолила, тиетанила, тиоморфолинила, тиофенолила, тиофенила, тиопиранила, 1,2,3-триазинила, 1,2,4-триазинила, 1,3,5-триазинила, 1,2,3-триазолила, 1,2,4-триазолила, 1,2,5-триазоила, 1,3,4-триазолила и ксантенила,
где гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8,
R8 представляет собой
1) галоген,
2) -NO2,
3) -CN,
4) -C(O)-NH2,
5) -OH,
6) -NH2,
7) -O-CF3,
8) моноциклический или бициклический 6-14-членный арил, где арил имеет значения, определенные выше, и арил является моно-, ди- или тризамещенным, независимо друг от друга, галогеном или -О-(C1-C8)-алкилом,
9) -(C1-C8)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, галогеном, NH2, -OH или метоксиостатком, или
10) -О-(C1-C8)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, галогеном, NH2, -OH или метоксиостатком,
11) -SO2-CH3 или
12) -SO2-CF3,
при условии, что R8 представляет собой, по меньшей мере, один из галогенов, -C(O)-NH2 или -О-(С1-С8)-алкильного остатка, если R0 представляет собой моноциклический или бициклический 6-14-членный арил, где арил имеет значения, определенные выше,
подструктура D представляет собой остаток, выбранный из группы, состоящей из азетидина, азетина, азокана, азокан-2-она, циклобутила, циклооктана, циклооктена, циклопентила, циклогексила, циклогептила, циклооктила, 1,4-диазепана, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, [1,4]диазокана, [1,2]диазокан-3-она, [1,3]диазокан-2-она, диоксазола, диоксазина, диоксола, 1,3-диоксолена, 1,3-диоксолана, фурана, имидазола, имидазолина, имидазолидина, изотиазола, изотиазолидина, изотиазолина, изоксазола, изоксазолина, изоксазолидина, 2-изоксазолина, кетопиперазина, морфолина, 1,2-оксатиепана, 1,2-оксатиолана, 1,2-оксазина, 1,3-оксазина, 1,4-оксазина, оксазола, [1,4]оксазокана, [1,3]оксазокан-2-она, оксетана, оксокана, оксокан-2-она, пиперазина, пиперидина, пирана, пиразина, пиразола, пиразолина, пиразолидина, пиридазина, пиридина, пиримидина, пиррола, пирролидина, пирролидинона, пирролина, 5,6,7,8-тетрагидро-1Н-азоцин-2-она, тетрагидрофурана, тетрагидропирана, тетрагидропиридина, тетразина, тиадиазина, тиадиазола, 1,2-тиазина, 1,3-тиазина, 1,4-тиазина, 1,3-тиазола, тиазола, тиазолидина, тиазолина, тиетана, тиокана, тиокан-1,1-диоксида, тиокан-1-оксида, тиокан-2-она, тиоморфолина, тиофена, тиопирана, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола или 1,2,4-триазола, и является незамещенным или замещенным от 1 до 6 R3, или замещенным 1 или 2 =О,
Q представляет собой прямую связь, -(C0-C2)-алкилен-C(O)-NR10-, -NR10-C(O)-NR10-, -NR10-C(O)-, -SO2-, -(C1-C6)-алкилен, -(CH2)m-NR10-C(O)-NR10-(CH2)n-, -(CH2)m-NR10-C(O)-(CH2)n-, -(CH2)m-S-(CH2)n-, -(CH2)m-C(O)-(CH2)n-, -(CH2)m-SO2-NR10-(CH2)n-, -(CH2)m-NR10-SO2-(CH2)n-, -(CH2)m-NR10-SO2-NR10-(CH2)n-, -(CH2)m-CH(OH)-(CH2)n-, -(CH2)m-O-C(O)-NR10-(CH2)n-, -(C2-C3)-алкилен-O-(C0-C3)-алкилен, -(C2-C3)-алкилен-S(O)-, -(C2-C3)-алкилен-S(O)2-, -(CH2)m-NR10-C(O)-О-(CH2)n-, -(C2-C3)-алкилен-S(O)2-NH-(R10)-, -(C2-C3)-алкилен-N-(R10)- или -(C0-C3)-алкилен-C(O)-O-,
где R10 имеет значения, определенные ниже, и где n и m независимо друг от друга являются одинаковыми или различными и представляют собой целые числа 0, 1, 2, 3, 4, 5 или 6, где алкиленовые остатки, образованные -(CH2)m- или -(CH2)n-, являются незамещенными или моно-, ди- или тризамещенными независимо друг от друга галогеном, -NH2 или -ОН; или -(C3-C6)-циклоалкиленом, где циклоалкилен является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, галогеном, -NH2 или -ОН;
R1 представляет собой атом водорода, -(C1-C4)-алкил, где алкил является незамещенным или замещенным 1-3 раза R13; -(C1-C3)-алкилен-C(O)-NH-R0, -(C1-C3)-алкилен-C(O)-O-R15, арил, выбранный из фенила, нафтила, бифенилила, антрила или флуоренила, где арил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8, где R8 имеет значения, определенные выше;
моноциклический или бициклический 4-15-членный гетероциклил, который имеет значения, определенные выше;
-(C1-C3)-перфторалкилен, -(C1-C3)-алкилен-S(O)-(C1-C4)-алкил, -(C1-C3)-алкилен-S(O)2-(C1-C3)-алкил, -(C1-C3)-алкилен-S(O)2-N(R4')-R5', -(C1-C3)-алкилен-O-(C1-C4)-алкил, -(C0-C3)-алкилен-(C3-C8)-циклоалкил, или -(C0-C3)-алкилен-het, где het представляет собой остаток, выбранный из азепина, азетидина, азиридина, азирина, 1,4-диазепана, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, диазиридина, диазирина, диоксазола, диоксазина, диоксола, 1,3-диоксолена, 1,3-диоксолана, фурана, имидазола, имидазолина, имидазолидина, изотиазола, изотиазолидина, изотиазолина, изоксазола, изоксазолина, изоксазолидина, 2-изоксазолина, кетопиперазина, морфолина, 1,4-оксазепана, 1,2-оксатиепана, 1,2-оксатиолана, 1,2-оксазина, 1,3-оксазина, 1,4-оксазина, оксазола, оксазиридина, оксирана, пиперазина, пиперидина, пирана, пиразина, пиразола, пиразолина, пиразолидина, пиридазина, пиридина, пиримидина, пиррола, пирролидина, пирролидинона, пирролина, тетрагидропиридина, тетразина, тетразола, тиадиазина, тиадиазола, 1,2-тиазина, 1,3-тиазина, 1,4-тиазина, 1,3-тиазола, тиазола, тиазолидина, тиазолина, тиенила, тиетана, тиоморфолина, тиопирана, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола или 1,2,4-триазола, где указанная циклическая группа является незамещенной или моно-, ди- или тризамещенной, независимо друг от друга, R14,
R4'и R5' независимы друг от друга и являются одинаковыми или различными и представляют собой атом водорода или -(C1-C4)-алкил,
R2 представляет собой прямую связь или -(C1-C4)-алкилен,
R1 и R3 вместе с атомами, с которыми они связаны, могут образовать 6-8-членный циклический остаток, выбранный из группы, состоящей из азокана, азокан-2-она, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, [1,4]диазокана, [1,2]диазокан-3-она, [1,3]диазокан-2-она, диоксазина, [1,4]диоксокана, диоксола, кетопиперазина, морфолина, 1,2-оксазина, 1,3-оксазина, 1,4-оксазина, оксокана, оксокан-2-она, пиперазина, пиперидина, пирана, пиразина, пиридазина, пиридина или 5,6,7,8-тетрагидро-1Н-азоцин-2-она, где указанная циклическая группа является незамещенной или моно-, ди- или тризамещенной, независимо друг от друга, R14, или
R1-N-R2-V могут образовать 4-7-членную циклическую группу, выбранную из группы азепина, азетидина, диоксазола, диоксазина, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, имидазола, имидазолина, имидазолидина, изотиазола, изотиазолидина, изотиазолина, изоксазола, изоксазолина, изоксазолидина, 2-изоксазолина, кетопиперазина, морфолина, оксазола, пиперазина, пиперидина, пиразина, пиразола, пиразолина, пиразолидина, пиридазина, пиридина, пиримидина, пиррола, пирролидина, пирролидинона, пирролина, тетрагидропиридина, тетразина, тетразола, тиазола, тиадиазола, тиазолидина, тиазолина, тиоморфолина, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола или 1,2,4-триазола, где указанная циклическая группа является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
R14 представляет собой фтор, хлор, бром, иод, -OH, =O, -(C1-C8)-алкил, -(C1-C4)-алкокси, -NO2-, -C(O)-OH-, -CN, -NH2, -C(O)-O-(C1-C4)-алкил, -(C0-C8)-алкил-SO2-(C1-C4)-алкил, -(C0-C8)-алкил-SO2-(C1-C3)-перфторалкил, -(C0-C8)-алкил-SO2-N(R18)-R21, -C(O)-NH-(C1-C8)-алкил, -C(O)-N-[(C1-C8)-алкил]2, NR18-C(O)-NH-(C1-C8)-алкил, -C(O)-NH2, -S-R18 или NR18-C(O)-NH-[(C1-C8)-алкил]2,
где R18 и R21 представляют собой, независимо друг от друга, атом водорода, -(C1-C3)-перфторалкил или -(C1-C6)-алкил,
V представляет собой
1) моноциклический или бициклический 6-14-членный арил, выбранный из группы, состоящей из фенила, нафтила, бифенилила, антрила или флуоренила, где арил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
2) гетероциклил, выбранный из группы акридинила, 8-азабицикло[3,2,1]окт-3-ила, азаиндол(1Н-пирролопиридина); азабензимидазолила, азаспиродеканила, азепинила, азетидинила, азиридинила, бензимидазолила, бензофуранила, бензотиофуранила, бензотиофенила, бензоксазолила, бензтиазолила, бензтриазолила, бензтетразолила, бензизоксазолила, бензизотиазолила, карбазолила, 4аН-карбазолила, карболинила, хроманила, хроменила, циннолинила, декагидрохинолинила, 1,4-диазепана, 4,5-дигидрооксазолинила, диоксазолила, диоксазинила, 1,3-диоксоланила, 1,3-диоксоленила, 6Н-1,5,2-дитиазинила, дигидрофтор[2,3-b]-тетрагидрофуранила, фуранила, фуразанила, имидазолидинила, имидазолинила, имидазолила, 1Н-индазолила, индолинила, индолизинила, индолила, 3Н-индолила, изобензофуранила, изохроманила, изоиндазолила, изоиндолинила, изоиндолила, изохинолинила, изотиазолила, изотиазолидинила, изотиазолинила, изоксазолила, изоксазолинила, изоксазолидинила, 2-изоксазолинила, кетопиперазинила, морфолинила, нафтиридинила, октагидроизохинолинила, оксадиазолила, 1,2,3-оксадиазолила, 1,2,4-оксадиазолила, 1,2,5-оксадиазолила, 1,3,4-оксадиазолила, 1,2-оксатиепанила, 1,2-оксатиоланила, 1,4-оксазепанила, 1,2-оксазинила, 1,3-оксазинила, 1,4-оксазинила, оксазолидинила, оксазолинила, оксазолила, фенантридинила, фенантролинила, феназинила, фенотиазинила, феноксатиинила, феноксазинила, фталазинила, пиперазинила, пиперидинила, птеридинила, пуринила, пиранила, пиразинила, пиразолидинила, пиразолинила, пиразолила, пиридазинила, пиридооксазолила, пиридоимидазолила, пиридотиазолила, пиридила, пиримидинила, пирролидинила, пирролидинонила, пирролинила, 2Н-пирролила, пирролила, хиназолинила, хинолинила, 4Н-хинолизинила, хиноксалинила, хинуклидинила, тетрагидрофуранила, тетрагидроизохинолинила, тетрагидрохинолинила, 1,4,5,6-тетрагидропиридазинила, тетрагидропиридинила, тетрагидротиофенила, тетразинила, тетразолила, 6Н-1,2,5-тиадиазинила, 1,2,3-тиадиазолила, 1,2,4-тиадиазолила, 1,2,5-тиадиазолила, 1,3,4-тиадиазолила, тиантренила, 1,2-тиазинила, 1,3-тиазинила, 1,4-тиазинила, 1,3-тиазолила, тиазолила, тиазолидинила, тиазолинила, тиенила, тиетанила, тиенотиазолила, тиенооксазолила, тиеноимидазолила, тиетанила, тиоморфолинила, 1λ6-тиоморфолинила, тиофенила, тиопиранила, 1,2,3-триазинила, 1,2,3-триазолила, 1,2,4-триазолила, 1,2,5-триазолила, 1,3,4-триазолила и ксантенила,
где указанный гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
G представляет собой прямую связь, -(CH2)m-NR10-SO2-NR10-(CH2)n-, -(CH2)m-CH(OH)-(CH2)n-, -(CH2)m-, -(CH2)m-O-(CH2)n-, -(CH2)m-C(O)-NR10-(CH2)n-, -(CH2)-SO2-(CH2)n-, -(CH2)m-NR10-C(O)-NR10-(CH2)n-, -(CH2)m-NR10-C(O)-(CH2)n-, -(CH2)m-C(O)-(CH2)n-, -(CH2)-S-(CH2)n-, -(CH2)m-SO2-NR10-(CH2)n-, -(CH2)m-NR10-SO2-(CH2)n-, -(CH2)m-NR10-, -(CH2)m-O-C(O)-NR10-(CH2)n- или -(CH2)m-NR10-C(O)-O-(CH2)n-,
n и m независимо друг от друга являются одинаковыми или различными и представляют собой целые числа 0, 1, 2, 3, 4, 5 или 6,
М представляет собой
1) атом водорода,
2) -(C1-C8)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
3) -C(O)-N-(R11)-R12,
4) -(CH2)m-NR10,
5) -(C6-C14)-арил, где арил имеет значения, определенные выше, и является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
6) -(C4-C15)-гетероциклил, где гетероциклил имеет значения, определенные выше, и является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14, или
7) -(C3-C8)-циклоалкил, где указанный циклоалкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
R3 представляет собой
1) атом водорода,
2) галоген,
3) -(C1-C4)-алкил, где указанный алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
4) -(C1-C3)-перфторалкил,
5) фенил, где фенил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
6) -(C0-C4)-алкилен-O-R19, где R19 представляет собой
а) атом водорода,
b) -(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
с) -CF3 или
d) -CHF2,
7) -NO2,
8) -CN,
9) -SOs-R11, где s равно 1 или 2,
10) -SOt-N(R11)-R12, где t равно 1 или 2,
11) -(C0-C4)-алкилен-С(O)-R11,
12) -(C0-C4)-алкилен-С(O)-O-R11,
13) -(C0-C4)-алкилен-С(O)-N(R11)-R12,
14) -(C0-C4)-алкилен-N(R11)-R12,
15) -NR10-SO2-R10,
16) -S-R10,
17) -(C0-C2)-алкилен-С(O)-O-(C2-C4)-алкилен-O-С(O)-(C1-C4)-алкил,
18) -C(O)-O-C(R15, R16)-O-C(O)-R17,
19) -(C0-C2)-алкилен-С(O)-O-(C2-C4)-алкилен-O-С(O)-O-(C1-C6)-алкил,
20) -C(O)-O-C(R15, R16)-O-C(O)-O-R17,
21) -(C0-C4)-алкилен-(C6-C14)-арил, где арил является моно-, ди- или тризамещенным, независимо друг от друга, R13,
22) -(C0-C4)-алкилен-(C4-C15)-гетероциклил, где гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
23) -(C0-C4)-алкилен-(C3-C8)-циклоалкил, где циклоалкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
24) -(C0-C4)-алкилен-het, где het является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
25) -(C0-C4)-алкилен-O-CH2-(C1-C3)-перфторалкилен-CH2-O-(C0-C3)-алкил,
26) -SOw-N(R11)-R13, где w равно 1 или 2,
27) -(C0-C4)-алкилен-C(O)-N(R11)-R13,
28) -(C0-C4)-алкилен-N(R11)-R13, или
29) остаток из следующего перечня
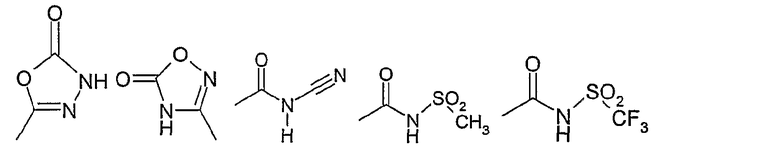
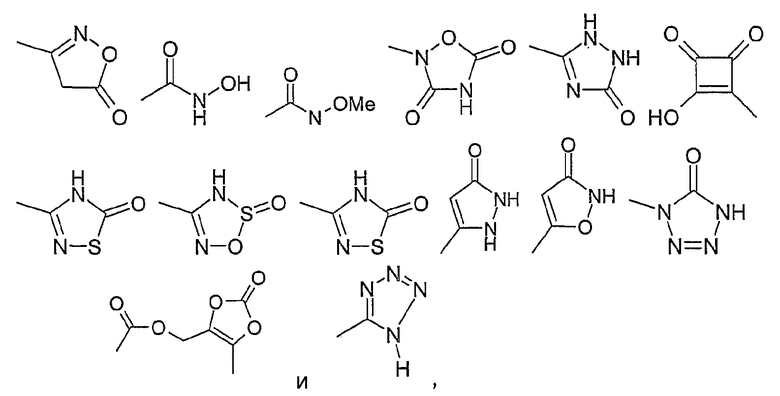
где Ме представляет собой метил, или
если 2 остатка -OR19 присоединены к соседним атомам, они могут образовывать вместе с атомами, к которым они присоединены, 1,3-диоксольное или 2,3-дигидро-[1,4]диоксиновое кольцо, которое замещено от 1 до 4 R13,
R11 и R12 независимо друг от друга являются одинаковыми или различными и представляют собой
1) атом водорода,
2) -(C1-C6)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
3) -(C0-C6)-алкил-(C3-C6)-циклоалкил,
4) -SOt-R10, где t равно 1 или 2,
5) -(C0-C6)-алкил-(C6-C14)-арил, где алкил и арил независимо друг от друга являются незамещенными или моно-, ди- или тризамещенными R13,
6) -(C1-C3)-перфторалкил,
7) -O-R17, или
8) -(C0-C6)-алкил-(C4-C15)-гетероциклил, где алкил и гетероциклил являются независимо друг от друга незамещенными или моно-, ди- или тризамещенными R13, или
R11 и R12 вместе с атомом азота, с которым они связаны, образуют гетероциклическое кольцо, выбранное из группы азепина, азетидина, диоксазола, диоксазина, 1,4-диазепана, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, имидазола, имидазолина, имидазолидина, изотиазола, изотиазолидина, изотиазолина, изоксазола, изоксазолина, изоксазолидина, 2-изоксазолина, кетопиперазина, морфолина, [1,4]оксазепана, оксазола, пиперазина, пиперидина, пиразина, пиразола, пиразолина, пиразолидина, пиридазина, пиридина, пиримидина, пиррола, пирролидина, пирролидинона, пирролина, тетрагидропиридина, тетразина, тетразола, тиазола, тиадиазола, тиазолидина, тиазолина, тиоморфолина, тиофена, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола или 1,2,4-триазола, где указанное гетероциклическое кольцо является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
R13 представляет собой галоген, -NO2, -CN, =O, -OH, -CF3, -C(O)-O-R10, -C(O)-N(R10)-R20, -N(R10)-R20, -(C3-C8)-циклоалкил, -(C0-C3)-алкилен-O-R10, -Si-(CH3)3, -N(R10)-S(O)u-R10, где u равно 1 или 2, -S-R10, -SOr-R10, где r равно 1 или 2, -S(O)v-N(R10)-R20, где v равно 1 или 2, -C(O)-R10, -(C1-C8)-алкил, -(C1-C8)-алкокси, фенил, фенилокси-, O-CF3, -(C0-C4)-алкил-C(O)-O-C(R15, R16)-O-C(O)-R17, -(C1-C4)-алкоксифенил, -(C0-C4)-алкил-C(O)-O-C(R15, R16)-O-C(O)-О-R17, -(C1-C3)-перфторалкил, -O-R15, -NH-C(O)-NH-R10, -NH-C(O)-O-R10, или остаток из следующего перечня
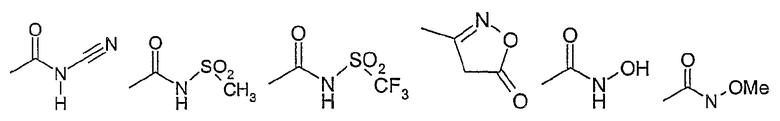
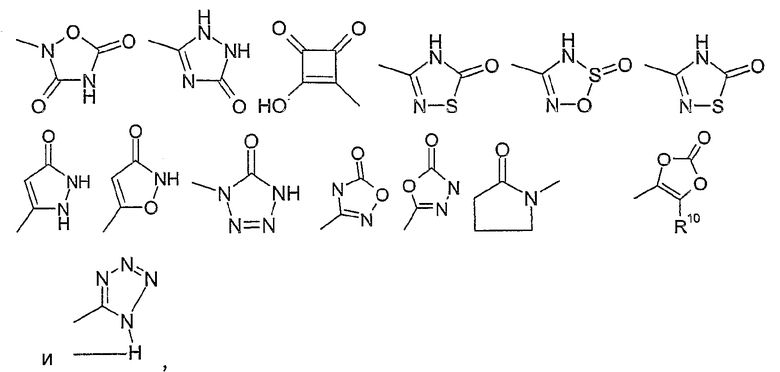
где Ме представляет собой метил,
R10 и R20 представляют собой, независимо друг от друга, водород, -(C1-C6)-алкил, -(C0-C4)-алкил-ОН, -(C0-C4)-алкил-О-(C1-C4)-алкил или -(C1-C3)-перфторалкил,
R15 и R16 представляют собой, независимо друг от друга, водород, -(C1-C6)-алкил, циклопропил, циклобутил, циклопентил или циклогексил, где каждое кольцо является незамещенным или замещенным от 1 до 3 R10, и
R17 представляет собой -(C1-C6)-алкил, -(C1-C6)-алкил-ОН, -(C1-C6)-алкил-О-(C1-C6)-алкил, -(C3-C8)-циклоалкил, -(C1-C6)-алкил-О-(C1-C8)-алкил-(C3-C8)-циклоалкил, -(C1-C6)-алкил-(C3-C8)-циклоалкил, где указанное циклоалкильное кольцо является незамещенным или замещенным 1, 2 или 3 -ОН,
-О-(C1-C4)-алкил или R10,
во всех его стереоизомерных формах и смесях в любом соотношении и его физиологически приемлемые соли.
(3) Настоящее изобретение также относится к соединениям формулы I, где
где R0 представляет собой
1) моноциклический или бициклический 6-14-членный арил выбран из группы фенила, нафтила, бифенила, антрила или флуоренила, где арил является моно-, ди- или тризамещенным, независимо друг от друга, R8,
2) гетероциклил, выбранный из группы бензимидазолила, 1,3-бензодиоксолила, бензофуранила, бензоксазолила, бензотиазолила, бензотиофенила, циннолинила, хроманила, индазолила, индолила, изохроманила, изоиндолила, изохинолинила, фенилпиридила, фталазинила, птеридинила, пуринила, пиридила, пиридоимидазолила, пиридопиридинила, пиридопиримидинила, пиримидинила, хиназолинила, хинолила, хиноксалинила или 1,4,5,6-тетрагидропиридазинила, где указанный гетероциклил является моно-, ди- или тризамещенным, независимо друг от друга, R8, или
3) гетероциклил, выбранный из группы азабензимидазолила, бензимидазолила, 1,3-бензодиоксолила, бензофуранила, бензотиазолила, бензотиофенила, бензоксазолила, хроманила, циннолинила, 2-фурила, 3-фурила, имидазолила, индолила, индазолила, изохроманила, изоиндолила, изохинолинила, изотиазолила, изоксазолила, оксазолила, фталазинила, птеридинила, пуринила, пиразинила, пиразолила, пиридазинила, пиридоимидазолила, пиридопиридинила, пиридопиримидинила, 2-пиридила, 3-пиридила, 4-пиридила, пиримидинила, пирролила, 2-пирролила, 3-пирролила, хинолинила, хиназолинила, хиноксалинила, тетразолила, тиазолила, 2-тиенила или 3-тиенила,
который дополнительно замещен гетероциклилом, выбранным из группы акридинила, азабензимидазолила, азаспиродеканила, азепинила, азетидинила, азиридинила, бензимидазолила, бензофуранила, бензотиофуранила, бензотиофенила, бензоксазолила, бензтиазолила, бензтриазолила, бензтетразолила, бензизоксазолила, бензизотиазолила, карбазолила, 4аН-карбазолила, карболинила, хроманила, хроменила, циннолинила, декагидрохинолинила, 4,5-дигидрооксазолинила, диоксазолила, диоксазинила, 1,3-диоксоланила, 1,3-диоксоленила, 6Н-1,5,2-дитиазинила, дигидрофтор[2,3-b]-тетрагидрофуранила, фуранила, фуразанила, имидазолидинила, имидазолинила, имидазолила, 1Н-индазолила, индолинила, индолизинила, индолила, 3Н-индолила, изобензофуранила, изохроманила, изоиндазолила, изоиндолинила, изоиндолила, изохинолинила (бензимидазолила), изотиазолила, изотиазолидинила, изотиазолинила, изоксазолила, изоксазолинила, изоксазолидинила, 2-изоксазолинила, кетопиперазинила, морфолинила, нафтиридинила, октагидроизохинолинила, оксадиазолила, 1,2,3-оксадиазолила, 1,2,4-оксадиазолила, 1,2,5-оксадиазолила, 1,3,4-оксадиазолила, 1,2-оксатиепанила, 1,2-оксатиоланила, 1,4-оксазепанила, 1,2-оксазинила, 1,3-оксазинила, 1,4-оксазинила, оксазолидинила, оксазолинила, оксазолила, фенантридинила, фенантролинила, феназинила, фенотиазинила, феноксатиинила, феноксазинила, фталазинила, пиперазинила, пиперидинила, птеридинила, пуринила, пиранила, пиразинила, пиразолидинила, пиразолинила, пиразолила, пиридазинила, пиридооксазолила, пиридоимидазолила, пиридотиазолила, пиридила, пиримидинила, пирролидинила, пирролидинонила, пирролинила, 2Н-пирролила, пирролила, хиназолинила, хинолинила, 4Н-хинолизинила, хиноксалинила, хинуклидинила, тетрагидрофуранила, тетрагидроизохинолинила, тетрагидрохинолинила, 1,4,5,6-тетрагидропиридазинила, тетрагидропиридинила, тетрагидротиофенила, тетразинила, тетразолила, 6Н-1,2,5-тиадиазинила, 1,2,3-тиадиазолила, 1,2,4-тиадиазолила, 1,2,5-тиадиазолила, 1,3,4-тиадиазолила, тиантренила, 1,2-тиазинила, 1,3-тиазинила, 1,4-тиазинила, 1,3-тиазолила, тиазолила, тиазолидинила, тиазолинила, тиенила, тиетанила, тиенотиазолила, тиенооксазолила, тиеноимидазолила, тиетанила, тиоморфолинила, тиофенила, тиопиранила, 1,2,3-триазинила, 1,2,3-триазолила, 1,2,4-триазолила, 1,2,5-триазолила, 1,3,4-триазолила и ксантенила,
где указанный гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8,
R8 представляет собой
1. фтор, хлор или бром,
2. -NO2,
3. -CN,
4. -C(O)-NH2,
5. -OH,
6. -NH2,
7. -OCF3,
8. моноциклический или бициклический 6-14-членный арил, где арил имеет значения, определенные выше, и является моно-, ди- или тризамещенным, независимо друг от друга, галогеном или -O-(C1-C8)-алкилом,
9. -(C1-C8)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, галогеном, NH2, -ОН или метоксиостатком, или
10. -O-(C1-C8)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, галогеном, NH2, -ОН или метоксиостатком,
11. -SO2CH3 или
12. -SO2CF3,
при условии, что R8 представляет собой, по меньшей мере, один из галогенов, -C(O)-NH2 или -O-(C1-C8)-алкильного остатка, если R0 представляет собой арил или гетероциклил, которые имеют значения, определенные выше,
подструктура D представляет собой остаток, выбранный из группы пиридила, пиридил-N-оксидпиридила, пирролила, фурила, тиенила, имидазолила, пиразолила, оксазолила, иозоксазолила, тиазолила, триазолила, изотиазолила, тиадиазолила, пиримидинила, пиридазинила, пиразинила и является незамещенным или замещенным от 1 до 4 R3, или замещенным 1 или 2 =О,
Q представляет собой прямую связь, -(C0-C2)-алкилен-C(O)-NR10-, -NR10-C(O)-NR10-, -NR10-C(O)-, -SO2-, -(C1-C6)-алкилен,
R1 представляет собой атом водорода, -(C1-C4)-алкил, где алкил является незамещенным или замещенным 1-3 раза R13; -(C1-C3)-алкилен-C(O)-NH-R0, -(C1-C3)-алкилен-C(O)-O-R15, -(C1-C3)-перфторалкилен, -(C1-C3)-алкилен-S(O)-(C1-C4)-алкил, -(C1-C3)-алкилен-S(O)2-(C1-C3)-алкил, -(C1-C3)-алкилен-S(O)2-N(R4')-R5', -(C1-C3)-алкилен-O-(C1-C4)-алкил, -(C0-C3)-алкилен-(C3-C8)-циклоалкил, или -(C0-C3)-алкилен-het, где het представляет собой остаток, выбранный из группы азепина, азетидина, азиридина, 1,4-диазепана, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, диазиридина, диазирина, диоксазола, диоксазина, диоксола, 1,3-диоксолена, 1,3-диоксолана, фурана, имидазола, имидазолина, имидазолидина, изотиазола, изотиазолидина, изотиазолина, изоксазола, изоксазолина, изоксазолидина, 2-изоксазолина, кетопиперазина, морфолина, 1,2-оксатиепана, 1,2-окстиолана, 1,4-оксазепана, 1,2-оксазина, 1,3-оксазина, 1,4-оксазина, оксазола, оксазиридина, оксирана, пиперазина, пиперидина, пирана, пиразина, пиразола, пиразолина, пиразолидина, пиридазина, пиридина, пиримидина, пиррола, пирролидина, пирролидинона, пирролина, тетрагидропиридина, тетразина, тетразола, тиадиазина, тиадиазола, 1,2-тиазина, 1,3-тиазина, 1,4-тиазина, 1,3-тиазола, тиазола, тиазолидина, тиазолина, тиенила, тиетана, тиоморфолина, тиопирана, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола или 1,2,4-триазола, где het является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
R4'и R5' независимы друг от друга и являются одинаковыми или различными и представляют собой атом водорода или -(C1-C4)-алкил,
R2 представляет собой прямую связь или -(C1-C4)-алкилен, или
R1-N-R2-V образует 4-7-членную циклическую группу, выбранную из группы азепина, азетидина, 1,4-диазепана, диоксазола, диоксазина, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, имидазола, имидазолина, имидазолидина, изотиазола, изотиазолидина, изотиазолина, изоксазола, изоксазолина, изоксазолидина, 2-изоксазолина, кетопиперазина, морфолина, 1,4-оксазепана, оксазола, пиперазина, пиперидина, пиразина, пиразола, пиразолина, пиразолидина, пиридазина, пиридина, пиримидина, пиррола, пирролидина, пирролидинона, пирролина, тетрагидропиридина, тетразина, тетразола, тиазола, тиадиазола, тиазолидина, тиазолина, тиоморфолина, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола или 1,2,4-триазола, где указанная циклическая группа является незамещенной или моно-, ди- или тризамещенной, независимо друг от друга, R14,
R14 представляет собой фтор, хлор, бром, иод, -OH, =O, -(C1-C8)-алкил, -(C1-C4)-алкокси, -NO2-, -C(O)-OH-, -CN, -NH2, -C(O)-O-(C1-C4)-алкил, -(C0-C8)-алкил-SO2-(C1-C4)-алкил, -(C0-C8)-алкил-SO2-(C1-C3)-перфторалкил, -(C0-C8)-алкил-SO2-N(R18)-R21, -C(O)-NH-(C1-C8)-алкил, -C(O)-N-[(C1-C8)-алкил]2, NR18-C(O)-NH-(C1-C8)-алкил, -C(O)-NH2, -S-R18, или NR18-C(O)-NH-[(C1-C8)-алкил]2,
где R18 и R21 представляют собой независимо друг от друга атом водорода, -(C1-C3)-перфторалкил или -(C1-C6)-алкил,
V представляет собой
1) остаток het выбранный из группы азаиндол(1Н-пирролопиридина), азепина, азетидина, азиридина, азирина, 1,4-диазепана, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, диазиридина, диазирина, диоксазола, диоксазина, диоксола, 1,3-диоксолена, 1,3-диоксолана, фурана, имидазола, имидазолина, имидазолидина, изотиазола, изотиазолидина, изотиазолина, изоксазола, изоксазолина, изоксазолидина, 2-изоксазолина, кетопиперазина, морфолина, 1,2-оксатиепана, 1,2-оксатиолана, 1,4-оксазепана, 1,2-оксазина, 1,3-оксазина, 1,4-оксазина, оксазола, оксазиридина, оксирана, пиперазина, пиперидина, пирана, пиразина, пиразола, пиразолина, пиразолидина, пиридазина, пиридина, пиримидина, пиррола, пирролидина, пирролидинона, пирролина, тетрагидропиридина, тетразина, тетразола, тиадиазина, тиадиазола, 1,2-тиазина, 1,3-тиазина, 1,4-тиазина, 1,3-тиазола, тиазола, тиазолидина, тиазолина, тиенила, тиетана, тиоморфолина, тиопирана, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола или 1,2,4-триазола, которая имеет значения, определенные выше, и где het является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14, или
2) фенил, где фенил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
G представляет собой прямую связь, -(CH2)m-NR10-SO2-NR10-(CH2)n-, -(CH2)m-CH(OH)-(CH2)n-, -(CH2)m-, -(CH2)m-O-(CH2)n-, -(CH2)m-C(O)-NR10-(CH2)n-, -(CH2)-SO2-(CH2)n-, -(CH2)m-NR10-C(O)-NR10-(CH2)n-, -(CH2)m-NR10-C(O)-(CH2)n-, -(CH2)m-C(O)-(CH2)n-, -(CH2)-S-(CH2)n-, -(CH2)m-SO2-NR10-(CH2)n-, -(CH2)m-NR10-SO2-(CH2)n-, -(CH2)m-NR10-, -(CH2)m-O-C(O)-NR10-(CH2)n- или -(CH2)m-NR10-C(O)-O-(CH2)n-,
n и m являются независимо друг от друга одинаковыми или различными и представляют собой целые числа 0, 1, 2, 3, 4, 5 или 6,
М представляет собой
1) атом водорода,
2) -(C1-C8)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
3) -C(O)-N-(R11)-R12,
4) -(CH2)m-NR10,
5) фенил или нафтил, где фенил или нафтил являются незамещенными или моно-, ди- или тризамещенными, независимо друг от друга, R14,
6) гетероциклил, где гетероциклил представляет собой остаток из группы, которую можно получить из азепана, азепина, 1,4-диазепана, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, имидазола, изотиазола, изоксазола, изоксазолидина, 2-изоксазолина, кетоморфолина, кетопиперазина, морфолина, оксазола, [1,4]-оксазепана, пиперазина, пиперазинона, пиперидина, пиперидинона, пиразина, пиридазина, пиридазинона, пиридина, пиридона, пиримидина, пирролидина, пирролидинона, тетрагидропирана, 1,4,5,6-тетрагидропиридазинила, тетразина, тетразола, тиадиазола, тиазола, тиофена, тиоморфолина, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола или 1,2,4-триазола, где указанный гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14, или
7) -(C3-C8)-циклоалкил, где указанный циклоалкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
R3 представляет собой
1) атом водорода,
2) галоген,
3) -(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
4) -(C1-C3)-перфторалкил,
5) фенил, где фенил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
6) -(C0-C4)-алкилен-O-R19, где R19 представляет собой
а) атом водорода,
b) -(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
с) -CF3, или
d) -CHF2,
7) -CN,
8) -(C0-C4)-алкилен-(C4-C15)-гетероциклил, где гетероциклил имеет значения, определенные выше, и является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
9) -SOs-R11, где s равно 1 или 2,
10) -SOt-N(R11)-R12, где t равно 1 или 2,
11) -(C0-C4)-алкилен-С(O)-R11,
12) -(C0-C4)-алкилен-С(O)-O-R11,
13) -(C0-C4)-алкилен-С(O)-N(R11)-R12,
14) -(C0-C4)-алкилен-N(R11)-R12,
15) -NR10-SO2-R10,
16) -(C0-C4)-алкилен-het, где het имеет значения, определенные выше, и является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
17) -(C0-C2)-алкилен-С(O)-O-(C2-C4)-алкилен-O-С(O)-(C1-C4)-алкил,
18) -C(O)-O-C(R15, R16)-O-C(O)-R17,
19) -(C0-C2)-алкилен-С(O)-O-(C2-C4)-алкилен-O-С(O)-O-(C1-C6)-алкил,
20) -C(O)-O-C(R15, R16)-O-C(O)-O-R17,
21) -(C0-C4)-алкилен-(C6-C14)-арил, где арил имеет значения, определенные выше, и является моно-, ди- или тризамещенным, независимо друг от друга, R13,
22) -(C0-C4)-алкилен-(C3-C8)-циклоалкил, где циклоалкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
23) -(C0-C3)-алкилен-O-CH2-CF2-CH2-O-(C0-C3)-алкил,
24) -(C0-C3)-алкилен-O-CH2-CF2-CF2-CH2-O-(C0-C3)-алкил,
25) -(C0-C3)-алкилен-O-CH2-(C1-C3)-перфторалкилен-CH2-OH,
26) -SOw-N(R11)-R13, где w равно 1 или 2,
27) -(C0-C4)-алкилен-C(O)-N(R11)-R13,
28) -(C0-C4)-алкилен-N(R11)-R13, или
29) остаток из следующего перечня

где Ме представляет собой метил, или
если 2 остатка -OR19 присоединены к соседним атомам, они могут образовывать вместе с атомами, к которым они присоединены, 1,3-диоксольное кольцо или 2,3-дигидро-[1,4]диоксиновое кольцо, замещенное от 1 до 4 R13,
R11 и R12 независимо друг от друга являются одинаковыми или различными и представляют собой
1) атом водорода,
2) -(C1-C6)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
3) -(C0-C6)-алкил-(C6-C14)-арил, где арил имеет значения, определенные выше, и где алкил и арил являются, независимо друг от друга, незамещенными или моно-, ди- или тризамещенными R13,
4) -O-R17, или
5) -(C0-C6)-алкил-(C4-C15)-гетероциклил, где алкил и гетероциклил являются, независимо друг от друга, незамещенными или моно-, ди- или тризамещенными R13, или
R11 и R12 вместе с атомом азота, с которым они связаны, могут образовать кольцо, выбранное из группы азепина, азетидина, 1,4-диазепана, диоксазола, диоксазина, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, имидазола, имидазолина, имидазолидина, изотиазола, изотиазолидина, изотиазолина, изоксазола, изоксазолина, изоксазолидина, 2-изоксазолина, кетопиперазина, морфолина, [1,4]оксазепана, оксазола, пиперазина, пиперидина, пиразина, пиразола, пиразолина, пиразолидина, пиридазина, пиридина, пиримидина, пиррола, пирролидина, пирролидинона, пирролина, тетрагидропиридина, тетразина, тетразола, тиазола, тиадиазола, тиазолидина, тиазолина, тиоморфолина, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола или 1,2,4-триазола, которое является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
R13 представляет собой фтор, хлор, бром, иод, -NO2, -CN, =O, -OH, -CF3, -C(O)-O-R10, -C(O)-N(R10)-R20, -N(R10)-R20, -(C0-C3)-алкилен-O-R10, -Si-(CH3)3, -N(R10)-S(O)2-R10, -S-R10, -SO2-R10, -S(O)2-N(R10)-R20, -C(O)-R10, -(C1-C8)-алкил, -(C1-C8)-алкокси, фенил, фенилокси-, O-CF3, -(C1-C3)-перфторалкил, -(C0-C4)-алкил-C(O)-O-C(R15,R16)-O-C(O)-R17, -(C1-C4)-алкоксифенил, -(C0-C4)-алкил-C(O)-O-C(R15,R16)-O-C(O)-О-R17, -O-R15, -NH-C(O)-NH-R10, -NH-C(O)-O-R10, или остаток из следующего перечня
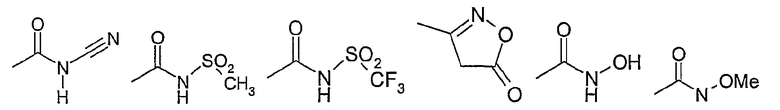
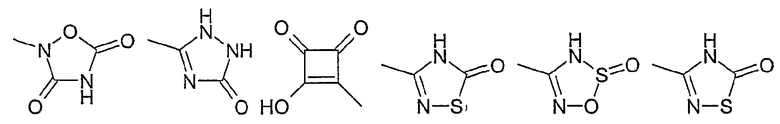
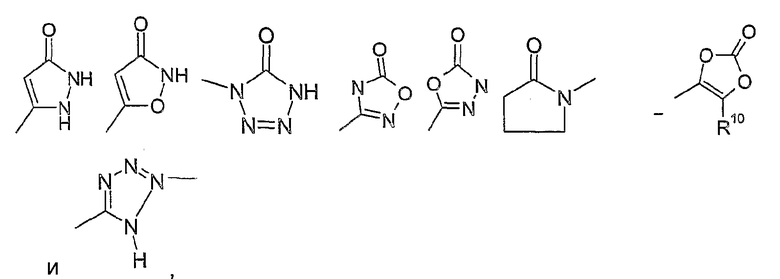
где Ме представляет собой метил,
R10 и R20 представляют собой, независимо друг от друга, водород, -(C1-C6)-алкил, -(C0-C4)-алкил-ОН, -(C0-C4)-алкил-О-(C1-C4)-алкил или -(C1-C3)-перфторалкил,
R15 и R16 представляют собой независимо друг от друга водород, -(C1-C6)-алкил, или вместе образуют кольцо, выбранное из группы циклопропила, циклобутила, циклопентила или циклогексила, где каждое кольцо является незамещенным или замещенным от 1 до 3 R10, и
R17 представляет собой -(C1-C6)-алкил, -(C1-C6)-алкил-ОН, -(C1-C6)-алкил-О-(C1-C6)-алкил, -(C3-C8)-циклоалкил, -(C1-C6)-алкил-О-(C1-C8)-алкил-(C3-C8)-циклоалкил, -(C1-C6)-алкил-(C3-C8)-циклоалкил, где указанное циклоалкильное кольцо является незамещенным или замещенным 1, 2 или 3 -ОН,
-О-(C1-C4)-алкил или R10,
во всех его стереоизомерных формах и смесях в любом соотношении и его физиологически приемлемые соли.
(4) Настоящее изобретение также относится к соединениям формулы I, где
R0 представляет собой
1) фенил, где фенил является незамещенным или моно-, ди- или тризамещеным, независимо друг от друга, R8.
2) гетероциклил, выбранный из группы бензимидазолила, 1,3-бензодиоксолила, бензофуранила, бензоксазолила, бензотиазолила, бензотиофенила, циннолинила, хроманила, индазолила, индолила, изохроманила, изоиндолила, изохинолинила, фенилпиридила, фталазинила, птеридинила, пуринила, пиридила, пиридоимидазолила, пиридопиридинила, пиридопиримидинила, пиримидинила, хиназолинила, хинолила, хиноксалинила или 1,4,5,6-тетрагидропиридазинила, где указанный гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8, или
3) гетероциклил, выбранный из группы пиридила, 2-пиридила, 3-пиридила, 4-пиридила, пирролила, 2-пирролила, 3-пирролила, фурила, 2-фурила, 3-фурила, тиенила, 2-тиенила, 3-тиенила, имидазолила, пиразолила, оксазолила, изоксазолила, тиазолила, тиадиазолила, изотиазолила, триазолила, тетразолила, пиридазинила и пиразинила, где указанный гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8,
и дополнительно замещен остатком, выбранным из группы пиридила, 2-пиридила, 3-пиридила, 4-пиридила, пирролила, 2-пирролила, 3-пирролила, фурила, 2-фурила, 3-фурила, тиенила, 2-тиенила, 3-тиенила, имидазолила, пиразолила, оксазолила, изоксазолила, тиазолила, тиадиазолила, изотиазолила, триазолила, тетразолила, пиридазинила и пиразинила, где указанный остаток является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8,
R8 представляет собой
1. F, Cl, Br или I,
2. -C(O)-NH2,
3. -(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, галогеном, -OH или метоксиостатком, или
4. -О-(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, галогеном или метоксиостатком, при условии, что R8 представляет собой, по меньшей мере, один из галогена, -C(O)-NH2 или -О-(С1-С8)-алкильного остатка, если R0 представляет собой арил или гетероциклил, которые имеют значения, определенные выше,
подструктура D представляет собой остаток, выбранный из группы пиридила, пиридил-N-оксида, пирролила, фурила, тиенила, имидазолила, пиразолила, оксазолила, изоксазолила, тиазолила, изотиазолила, тиадиазолила, пиримидинила, пиридазинила, пиразинила и является незамещенным или замещенным от 1 до 4 R3, или замещенным 1 или 2 =О,
Q представляет собой прямую связь, -C(O)-; -SO2- или -(C1-C6)-алкилен, -(C0-C2)-алкилен-C(O)-NR10-,
R1 представляет собой атом водорода, -(C1-C2)-алкил, -(C1-C3)-алкилен-C(O)-NH-RO, -(C1-C3)-перфторалкилен, -(C1-C3)-алкилен-С(O)-OR15, -(C1-C3)-алкилен-S(O)2-(C1-C3)-алкил или -(C1-C3)-алкилен-S(O)2-N(R4')-R5', где R4'и R5' независимы друг от друга и являются одинаковыми или различными и представляют собой атом водорода или -(C1-C4)-алкил,
R2 представляет собой прямую связь или -(C1-C2)-алкилен,
R1-N-R2-V могут образовать 4-7-членную циклическую группу, выбранную из группы азетидина, азетидинона, пиперидина, пиперазина, пиридина, пиримидина, пирролидина, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола, 1,2,4-триазола, тетразина, тетразола, 1,4-диазепана, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, азепина, кетопиперазина, 1,4-оксазепана, оксазола, изоксазола, изоксазолидина, 2-изоксазолина, морфолина, тиазола, изотиазола, тиадиазола или тиоморфолина, где указанная циклическая группа является незамещенной или моно-, ди- или тризамещенной, независимо друг от друга, R14,
R14 представляет собой фтор, хлор, -OH, =O, -(C1-C8)-алкил, -C(O)-OH-, -CN, -NH2, -C(O)-O-(C1-C4)-алкил, -C(O)-NH-(C1-C8)-алкил, -C(O)-N-[(C1-C8)-алкил]2, -C(O)-NH2 или -N(R18)- R21,
где R18 и R21 представляют собой, независимо друг от друга, атом водорода, -(C1-C3)-перфторалкил или -(C1-C4)-алкил,
V представляет собой
1. циклический остаток, выбранный из группы, содержащей соединения, полученные из азаиндола(1Н-пирролпиридина), азиридина, азирина, азетидина, азетидинона, 1,4-диазепана, пиррола, пирролидина, пиридонила, имидазола, пиразола, 1,2,3-триазола, 1,2,4-триазола, тетразола, пиридина, пиримидина, пиразина, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, тетразина, тетразола, азепина, диазирина, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, пиридазина, пиперидина, пиперазина, пирролидинона, кетопиперазина, фурана, пирана, диоксола, 1,4-оксазепана, оксазола, изоксазола, 2-изоксазолина, изоксазолидина, морфолина, оксирана, оксазиридина, 1,3-диоксолена, 1,3-диоксолана, 1,2-оксазина, 1,3-оксазина, 1,4-оксазина, оксазиридина, тиофена, тиопирана, тиетана, тиазола, изотиазола, изотиазолина, изотиазолидина, 1,2-оксатиолана, тиодиазола, тиопирана, 1,2-тиазина, 1,3-тиазола, 1,3-тиазина, 1,4-тиазина, тиадиазина или тиоморфолина, где указанный циклический остаток является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14, или
2. фенил, где фенил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14, или
G представляет собой прямую связь, -(CH2)m- или -(CH2)m-NR10-, где m представляет собой целые числа 0, 1, 2, 3 или 4,
М представляет собой
1. атом водорода,
2. гетероциклил, где гетероциклил представляет собой остаток, выбранный из группы, которую можно получить из азепана, азепина, 1,4-диазепана, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, имидазола, изотиазола, изоксазола, изоксазолидина, 2-изоксазолина, кетоморфолина, кетопиперазина, морфолина, оксазола, [1,4]-оксазепана, пиперазина, пиперазинона, пиперидина, пиперидинона, пиразина, пиридазина, пиридазинона, пиридина, пиридона, пиримидина, пирролидина, пирролидинона, тетрагидропирана, 1,4,5,6-тетрагидропиридазинила, тетразина, тетразола, тиадиазола, тиазола, тиоморфолина, тиофена, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола или 1,2,4-триазола, где указанный гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
3. -(C1-C6)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
4. -(C3-C6)-циклоалкил или
5. -C(O)-N(R11)-R12,
R3 представляет собой
1) атом водорода,
2) галоген,
3) -(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
4) -(C1-C3)-перфторалкил,
5) фенил, где фенил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
6) -(C0-C4)-алкилен-O-R19, где R19 представляет собой
а) атом водорода,
b) -(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
с) -CF3 или
d) -CF2,
7) -CN,
8) -NR10-SO2-R10,
9) -SOs-R11, где s равно 1 или 2,
10) -SOt-N(R11)-R12, где t равно 1 или 2,
11) -(C0-C4)-алкилен-С(O)- R11,
12) -(C0-C4)-алкилен-С(O)-О-R11,
13) -(C0-C4)-алкилен-С(O)-N(R11)-R12,
14) -(C0-C4)-алкилен-N(R11)-R12,
15) -(C0-C2)-алкилен-С(O)-O-(C2-C4)-алкилен-O-С(O)-(C1-C4)-алкил,
16) -C(O)-O-C(R15, R16)-O-C(O)-R17,
17) -(C0-C2)-алкилен-С(O)-O-(C2-C4)-алкилен-O-С(O)-O-(C1-C6)-алкил,
18) -C(O)-O-C(R15, R16)-O-C(O)-O-R17,
19) -(C0-C3)-алкилен-O-CH2-CF2-CH2-O-(C0-C3)-алкил,
20) -(C0-C3)-алкилен-O-CH2-CF2-CF2-CH2-O-(C0-C3)-алкил,
21) -(C0-C3)-алкилен-O-CH2-(C1-C3)-перфторалкилен-CH2-OH,
22) -SOw-N(R11)-R13, где w равно 1 или 2,
23) -(C0-C4)-алкилен-C(O)-N(R11)-R13,
24) -(C0-C4)-алкилен-N(R11)-R13, или
25) остаток из следующего перечня
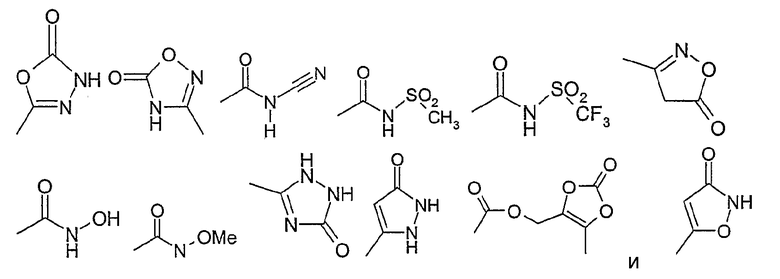
где Ме представляет собой метил,
если 2 остатка -OR19 присоединены к соседним атомам, они могут образовывать вместе с атомами, к которым они присоединены, 1,3-диоксольное кольцо или 2,3-дигидро-[1,4]диоксиновое кольцо, которое является замещенным от 1 до 4 R13,
R11 и R12 вместе с атомом азота, с которым они связаны, могут образовать кольцо, выбранное из группы азепина, азетидина, 1,4-диазепана, диоксазола, диоксазина, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, имидазола, имидазолина, имидазолидина, изотиазола, изотиазолидина, изотиазолина, изоксазола, изоксазолина, изоксазолидина, 2-изоксазолина, кетопиперазина, морфолина, [1,4]-оксазепана, оксазола, пиперазина, пиперидина, пиразина, пиразола, пиразолина, пиразолидина, пиридазина, пиридина, пиримидина, пиррола, пирролидина, пирролидинона, пирролина, тетрагидропиридина, тетразина, тетразола, тиазола, тиадиазола, тиазолидина, тиазолина, тиоморфолина, тиофена, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола или 1,2,4-триазола, где указанное кольцо является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
R13 представляет собой фтор, хлор, -NO2, -CN, =O, -OH, -CF3, -C(O)-O-R10, -C(O)-N(R10)-R20, -N(R10)-R20, -(C0-C3)-алкилен-O-R10, -Si-(CH3)3, -N(R10)-S(O)2-R10, -S-R10, -SO2-R10, -S(O)2-N(R10)-R20, -C(O)-R10, -(C1-C8)-алкил, -(C1-C8)-алкокси, фенил, фенилокси-, O-CF3, перфторалкил, -NH-C(O)-NH-R10, -(C0-C4)-алкил-C(O)-O-С(R15, R16)-O-C(O)-R17, -(C1-C4)-алкоксифенил, -(C0-C4)-алкил-C(O)-O-С(R15, R16)-O-C(O)-О-R17, -O-R15, -NH-C(O)-O-R10, или остаток из следующего перечня
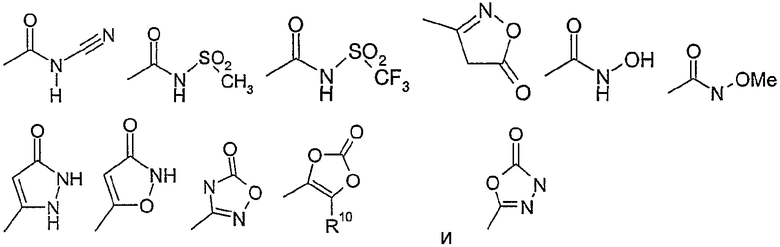
где Ме представляет собой метил,
R10 и R20 представляют собой независимо друг от друга водород, -(C1-C6)-алкил, -(C0-C4)-алкил-ОН, -(C0-C4)-алкил-О-(C1-C4)-алкил или -(C1-C3)-перфторалкил,
R15 и R16 представляют собой независимо друг от друга водород, -(C1-C6)-алкил, или вместе образуют кольцо, выбранное из группы циклопропила, циклобутила, циклопентила или циклогексила, где каждое кольцо является незамещенным или замещенным от 1 до 3 R10, и
R17 представляет собой -(C1-C6)-алкил, -(C1-C6)-алкил-ОН, -(C1-C6)-алкил-О-(C1-C6)-алкил, -(C3-C8)-циклоалкил, -(C1-C6)-алкил-О-(C1-C8)-алкил-(C3-C8)-циклоалкил, -(C1-C6)-алкил-(C3-C8)-циклоалкил, где указанное циклоалкильное кольцо является незамещенным или замещенным 1, 2 или 3 -ОН,
-О-(C1-C4)-алкил или R10,
во всех его стереоизомерных формах и смесях в любом соотношении и его физиологически приемлемые соли.
(5) Настоящее изобретение также относится к соединениям формулы I, где
R0 представляет собой
1) фенил, где фенил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8.
2) гетероциклил, выбранный из группы индолила, изоиндолила, бензофуранила, бензотиофенила, 1,3-бензодиоксолила, индазолила, бензимидазолила, бензоксазолила, бензотиазолила, хинолинила, изохинолинила, хроманила, изохроманила, циннолинила, хиназолинила, хиноксалинила, фталазинила, пиридоимидазолила, пиридопиридинила, пиридопиримидинила, пиридила, пуринил и птеридинила,
где указанный гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8,
3) гетероциклил, выбранный из группы пиридила, 2-пиридила, 3-пиридила, 4-пиридила, пирролила, 2-пирролила, 3-пирролила, фурила, 2-фурила, 3-фурила, тиенила, 2-тиенила, 3-тиенила, имидазолила, пиразолила, оксазолила, изоксазолила, тиазолила, тиадиазолила, изотиазолила, триазолила, тетразолила, пиридазинила и пиразинила, где указанный гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8,
и дополнительно замещенный остатком, выбранным из группы пиридила, 2-пиридила, 3-пиридила, 4-пиридила, пирролила, 2-пирролила, 3-пирролила, фурила, 2-фурила, 3-фурила, тиенила, 2-тиенила, 3-тиенила, имидазолила, пиразолила, оксазолила, изоксазолила, тиазолила, тиадиазолила, изотиазолила, триазолила, тетразолила, пиридазинила и пиразинила, где указанный остаток является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8,
R8 представляет собой
1. F, Cl, Br или I,
2. -C(O)-NH2,
3. -(C1-C4)-алкил, где алкил является незамещенным моно-, ди- или тризамещенным, независимо друг от друга, галогеном, -OH или метоксиостатком, или
4. -О-(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, галогеном или метоксиостатком, при условии, что R8 представляет собой, по меньшей мере, один из галогена, -C(O)-NH2 или -О-(С1-С8)-алкильного остатка, если R0 представляет собой арил или гетероциклил, которые имеют значения, определенные выше,
подструктура D представляет собой остаток, выбранный из группы, состоящей из пиридила, пиридил-N-оксида, пирролила, фурила, тиенила, имидазолила, пиразолила, оксазолила, изоксазолила, тиазолила, триазолила, изотиазолила, тиадиазолила, пиримидинила, пиридазинила, пиразинила и является незамещенным или замещенным от 1 до 4 R3, или замещенным 1 или 2 =О,
Q представляет собой прямую связь, -C(O)-; -SO2- или -(C1-C6)-алкилен, -(C0-C2)-алкилен-C(O)-NR10-,
R1 представляет собой атом водорода или -(C1-C2)-алкил,
R2 представляет собой прямую связь или -(C1-C2)-алкилен, или
R1-N-R2-V могут образовать 4-7-членную циклическую группу, выбранную из пиперидина, пиридина, пиримидина, пирролидина, пирролидинона, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола, 1,2,4-триазола, тетразина, тетразола, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, азепина, кетопиперазина, оксазола, изоксазола, изоксазолидина, 2-изоксазолина, морфолина, тиазола, изотиазола, тиадиазола или тиоморфолина, где указанная циклическая группа является незамещенной или моно-, ди- или тризамещенной, независимо друг от друга, R14,
R14 представляет собой фтор, хлор, =O, -(C1-C4)-алкил или -NH2,
V представляет собой
1. циклический остаток из группы, содержащей соединения, которые получены из азаиндолила(1Н-пирролпиридина), азетидина, азепина, азиридина, азирина, 1,4-диазепана, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, диазирина, 1,3-диоксолана, диоксолана, фурана, имидазола, изохинолина, изотиазола, изотиазолидина, изотиазолина, изоксазола, 2-изоксазолина, изоксазолидина, кетопиперазина, морфолина, 1,2-оксазина, 1,3-оксазина, 1,4-оксазина, оксазола, 1,2-оксатиолана, пиперидина, пирана, пиразина, пиразола, пиридазина, пиперазина, пиридина, пиридона, пиримидина, пиррола, пирролидина, пирролидинона, хиназолина, хинолина, тетразина, тетразола, тиадиазина, 1,2-тиазина, 1,3-тиазина, 1,4-тиазина, 1,3-тиазола, тиетана, тиоморфолина, тиофена, тиопирана, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола или 1,2,4-триазола,
где указанный циклический остаток является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14, или
2. фенил, где фенил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
G представляет собой прямую связь, -(CH2)m- или -(CH2)m-NR10-, где m представляет собой целые числа 0, 1, 2, 3 или 4,
М представляет собой
1. атом водорода,
2. гетероциклил, где гетероциклил представляет собой остаток из группы, которую можно получить из 1,4-диазепана, кетоморфолина, тиофена, пиридазона, пиперидина, пиперазина, пиридина, пиримидина, пирролидина, пирролидинона, пиридонила, имидазола, пиридазина, пиразина, 1,2,3-триазина, 1,2,4-триазина, 1,3,5-триазина, 1,2,3-триазола, 1,2,4-триазола, тетразина, тетразола, 1,2-диазепина, 1,3-диазепина, 1,4-диазепина, азепина, кетопиперазина, оксазола, изоксазола, изоксазолидина, 2-изоксазолина, морфолина, тиазола, изотиазола, тетрагидропирана, 1,4,5,6-тетрагидропиридазинила, тиадиазола или тиоморфолина, где указанный гетероциклил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14,
3. -(C1-C6)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R14, или
4. -(C3-C6)-циклоалкил,
R3 представляет собой
1) атом водорода,
2) галоген,
3) -(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
4) -(C1-C3)-перфторалкил,
5) фенил, где фенил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
6) -(C0-C4)-алкилен-O-R19, где R19 представляет собой
а) атом водорода,
b) -(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
с) -CF3 или
d) -CHF2,
7) -CN,
8) -NR10-SO2-R10,
9) -SOs-R11, где s равно 1 или 2,
10) -SOt-N(R11)-R12, где t равно 1 или 2,
11) -(C0-C4)-алкилен-С(O)-R11,
12) -(C0-C4)-алкилен-С(O)-О-R11,
13) -(C0-C4)-алкилен-С(O)-N(R11)-R12,
14) -(C0-C4)-алкилен-N(R11)-R12,
15) -(C0-C2)-алкилен-С(O)-O-(C2-C4)-алкилен-O-С(O)-(C1-C4)-алкил,
16) -C(O)-O-C(R15, R16)-O-C(O)-R17,
17) -(C0-C2)-алкилен-С(O)-O-(C2-C4)-алкилен-O-С(O)-O-(C1-C6)-алкил,
18) -C(O)-O-C(R15, R16)-O-C(O)-O-R17, или
19) остаток из следующего перечня
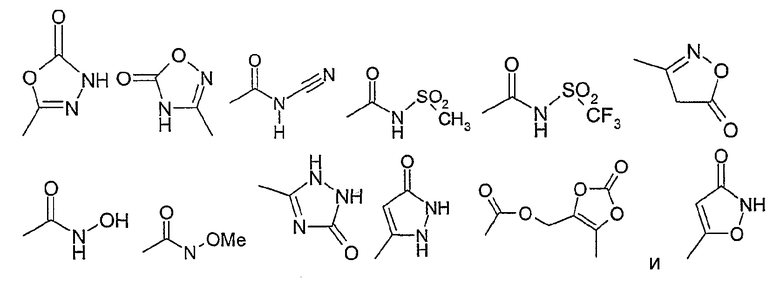
где Ме представляет собой метил,
R11 и R12 являются независимо друг от друга одинаковыми или различными и представляют собой
1) атом водорода,
2) -(C1-C6)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
3) -(C0-C6)-алкил-(C3-C6)-циклоалкил,
4) -O-R17, или
5) -(C0-C6)-алкил-(C4-C15)-гетероциклил, где алкил и гетероциклил независимо друг от друга являются незамещенными или моно-, ди- или тризамещенными R13, и где гетероциклил выбран из группы азетидина, циклопропила, циклобутила, 4,5-дигидрооксазола, имидазолидина, морфолина, (1,4)-оксазепана, оксазолидина, пиперидина, пиперазина, пирролидина, тетрагидротиофена, тиазолидина или тиоморфолина, или
R11 и R12 вместе с атомом азота, с которым они связаны, образуют гетероциклическое кольцо, выбранное из группы азетидина, циклопропила, циклобутила, 4,5-дигидрооксазола, имидазолидина, мофролина, (1,4)-оксазепана, оксазолидина, пиперидина, пиперазина, пирролидина, тетрагидротиофена, тиазолидина или тиоморфолина,
R13 представляет собой фтор, -CN, =O, -OH, -CF3, -C(O)-O-R10, -C(O)-N(R10)-R20, -N(R10)-R20, -(C3-C6)-циклоалкил, -(C0-C3)-алкилен-O-R10, -Si-(CH3)3, -S-R10, -SO2-R10, -(C1-C3)-перфторалкил, или остаток из следующего перечня
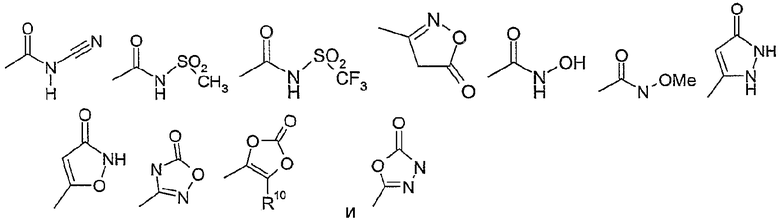
где Ме представляет собой метил,
R10 и R20 представляют собой независимо друг от друга водород, -(C1-C4)-алкил или -(C1-C3)-перфторалкил,
R15 и R16 представляют собой, независимо друг от друга, водород, -(C1-C6)-алкил, или вместе образуют кольцо, выбранное из циклопропила, циклобутила, циклопентила или циклогексила, где каждое кольцо является незамещенным или замещенным от 1 до 3 R10, и
R17 представляет собой -(C1-C6)-алкил, -(C1-C6)-алкил-ОН, -(C1-C6)-алкил-О-(C1-C6)-алкил, -(C1-C6)-алкил-О-(C1-C8)-алкил-(C3-C8)-циклоалкил, -(C0-C6)-алкил-(C3-C8)-циклоалкил, где указанное циклоалкильное кольцо является незамещенным или замещенным 1, 2 или 3 -ОН,
-О-(C1-C4)-алкил или R10,
во всех его стереоизомерных формах и смесях в любом соотношении и его физиологически приемлемые соли.
(6) Настоящее изобретение также относится к соединениям формулы I, где
R0 представляет собой
1. фенил, где фенил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8.
2. пиридил или бензотиофенил, где пиридил или бензотиофенил являются незамещенными или моно-, ди- или тризамещенными, независимо друг от друга, R8, или
3. гетероциклил, выбранный из тиенила, тиадиазолила, изоксазолила и тиазолила, где указанный гетероциклил замещен остатком, выбранным из тиенила, 2-тиенила и 3-тиенила, где указанный остаток является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R8,
R8 представляет собой F, Cl, Br, -OCH3 или -C(O)-NH2,
подструктура D представляет собой остаток, выбранный из пиридила, пиридил-N-оксида, пирролила, тиенила, имидазолила, пиразолила, оксазолила, изоксазолила, тиазолила, изотиазолила, тиадиазолила, пиримидинила, пиридазинила или пиразинила и является незамещенной или замещенной 1, 2, 3, или 4 R3, или замещенной 1 или 2 =О,
Q представляет собой прямую связь, -C(O)-; -SO2-, CH2-C(O)-NH-, метилен или этилен,
R1 представляет собой атом водорода,
R2 представляет собой прямую связь или метилен,
R1-N-R2-V могут образовать 4-7-членную циклическую группу, выбранную из азетидина, пирролидина, пиперидина и,
R14 представляет собой фтор, хлор, =O, метил, этил или -NH2,
V представляет собой
1. циклический остаток из группы, содержащей соединения, которые получены из азаиндолила(1Н-пирролопиридина), азетидина, 1,4-диазепана, изоксазола, изохинолина, пиперазина, пиперидина, пиразина, пиридазина, пиримидина, пирролидина, хиназолина, хинолина или тетрагидропирана,
где указанный циклический остаток является незамещенным или моно-, или дизамещенным, независимо друг от друга, R14, или
2. фенил, где фенил является незамещенным или моно- или дизамещенным, независимо друг от друга, R14,
G представляет собой прямую связь, -(CH2)m- или -(CH2)m-NR10-, где m представляет собой целые числа 1 или 2,
М представляет собой атом водорода, -(C2-C4)-алкил, азепанил, циклопропил, циклобутил, циклопентил, циклогексил, имидазолил, кетоморфолинил, [1,4]оксазепанил, пиперидинил, пиперидонил, пиразинил, пиразолил, пиридазинил, пиридил, пиримидил, пирролидинил, 1,4,5,6-тетрагидропиридазинил или тетрагидропиранил, где остатки являются незамещенными или моно-, или дизамещенными независимо друг от друга R14
R3 представляет собой
1) атом водорода,
2) фтор, хлор,
3) -(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
4) -(C1-C3)-перфторалкил,
5) фенил, где фенил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
6) -(C0-C4)-алкилен-O-R19, где R19 представляет собой
а) атом водорода,
b) -(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
с) -CF3 или
d) -CHF2,
7) -CN,
8) -NR10-SO2-R10,
9) -SOs-R11, где s равно 1 или 2,
10) -SOt-N(R11)-R12, где t равно 1 или 2,
11) -(C0-C4)-алкилен-С(O)- R11,
12) -(C0-C4)-алкилен-С(O)-О-R11,
13) -(C0-C4)-алкилен-С(O)-N(R11)-R12,
14) -(C0-C4)-алкилен-N(R11)-R12,
15) -(C0-C2)-алкилен-С(O)-O-(C2-C4)-алкилен-O-С(O)-(C1-C4)-алкил,
16) -C(O)-O-C(R15, R16)-O-C(O)-R17,
17) -(C0-C2)-алкилен-С(O)-O-(C2-C4)-алкилен-O-С(O)-O-(C1-C6)-алкил или
18) -C(O)-O-C(R15, R16)-O-C(O)-O-R17,
R11 и R12 являются независимо друг от друга одинаковыми или различными и представляют собой
1) атом водорода,
2) -(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
3) -(C0-C6)-алкил-(C3-C6)-циклоалкил,
4) -O-R17 или
5) -(C0-C6)-алкилгетероциклил, где алкил и гетероциклил являются независимо друг от друга незамещенными или моно-, ди- или тризамещенными R13, и где гетероциклил выбран из азетидина, имидазолидина, морфолина, (1,4)-оксазепана или пирролидина, или
R11 и R12 вместе с атомом азота, с которым они связаны, могут образовывать кольцо, которое выбрано из группы азетидина, имидазолидина, морфолина, (1,4)-оксазепана, пиперазина, пиперидина, пирролидина или тиоморфолина,
R13 представляет собой фтор, -CN, =O, -OH, -CF3, -C(O)-O-R10, -C(O)-N(R10)-R20, -N(R10)-R20, -(C3-C6)-циклоалкил, -(C0-C3)-алкилен-O-R10, -Si-(CH3)3, -S-R10, -SO2-R10, или -(C1-C3)-перфторалкил,
R10 и R20 представляют собой, независимо друг от друга, водород, -(C1-C4)-алкил или -(C1-C3)-перфторалкил,
R15 и R16 представляют собой независимо друг от друга водород, -(C1-C4)-алкил, или вместе образуют кольцо, выбранное из циклопропила, циклобутила, циклопентила или циклогексила, где каждое кольцо является незамещенным или замещенным от 1 до 3 R10, и
R17 представляет собой -(C1-C6)-алкил, -(C1-C6)-алкил-ОН, -(C1-C6)-алкил-О-(C1-C6)-алкил, -(C1-C6)-алкил-О-(C1-C8)-алкил-(C3-C8)-циклоалкил, -(C0-C6)-алкил-(C3-C8)-циклоалкил, где указанное циклоалкильное кольцо является незамещенным или замещенным 1, 2 или 3 -ОН, -О-(C1-C4)-алкилом или R10,
во всех его стереоизомерных формах и смесях в любом соотношении и его физиологически приемлемые соли.
(7) Настоящее изобретение также относится к соединениям формулы I, где
R0 представляет собой
1. пиридил или бензотиофенил, где пиридил или бензотиофенил являются незамещенными или моно- или дизамещенными независимо друг от друга R8, или
2. гетероциклил, выбранный из группы тиенила, тиадиазолила, изоксазолила и тиазолила, где указанный гетероциклил является замещенным, независимо друг от друга, остатком, выбранным из тиенила, 2-тиенила и 3-тиенила, где указанный остаток является незамещенным или моно- или дизамещенным, независимо друг от друга, R8,
R8 представляет собой F, Cl, Br, -OCH3 или -C(O)-NH2,
подструктура D представляет собой пиридил и является незамещенной или замещенной 1, 2, 3, или 4 R3, или замещенной одним или двумя =О,
Q представляет -CH2-C(O)-NH- или метилен,
R1 представляет собой атом водорода,
R2 представляет собой прямую связь,
R14 представляет собой фтор, хлор, =O, метил, этил или -NH2,
V представляет собой пиперидин, где пиперидин является незамещенным или моно- или дизамещенным, независимо друг от друга, R14, или
G представляет собой прямую связь,
М представляет собой атом водорода, -(C2-C4)-алкил, изопропил или пиридил, где остаток является незамещенным или моно- или ди- замещенным, независимо друг от друга, R14,
R3 представляет собой
1) атом водорода,
2) фтор, хлор,
3) -(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
4) -(C0-C2)-алкилен-O-R19, где R19 представляет собой
а) атом водорода или
b) -(C1-C4)-алкил, где алкил является незамещенным или моно-, ди- или тризамещенным, независимо друг от друга, R13,
5) -(C0-C4)-алкилен-С(O)-R11,
6) -(C0-C4)-алкилен-С(O)-N(R11)-R12,
R11 и R12 независимы друг от друга и являются одинаковыми или различными и представляют собой
1) водород или
2) -(С1-С4)-алкил, где алкил является моно-, ди- или тризамещенным, независимо друг от друга, R13, или
R11 и R12 вместе с атомом азота, с которым они связаны, могут образовать кольцо, выбранное из группы азетидина, имидазолидина, морфолина, (1,4)-оксазепана, пиперазина, пиперидина, пирролидина или тиоморфолина,
R13 представляет собой фтор, =O, -OH, -CF3, -C(O)-O-R10, -C(O)-N(R10)-R20, -N(R10)-R20, или -(C0-C3)-алкилен-O-R10,
R10 и R20 представляют собой независимо друг от друга водород, -(C1-C4)-алкил или -(C1-C3)-перфторалкил,
во всех его стереоизомерных формах и смесях в любом соотношении и его физиологически приемлемые соли.
(8) Настоящее изобретение также относится к соединениям формулы I, которые представляют собой
(1-изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пиррол[2,3-b]пиридин-2-карбоновой кислоты,
сложный метиловый эфир 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[2,3-b]пиридин-5-карбоновой кислоты,
1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[2,3-b]пиридин-5-карбоновую кислоту,
2-[(1-изопропилпиперидин-4-ил)амид] 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пиррол[2,3-b]пиридин-2,5-дикарбоновой кислоты,
(1-изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты,
1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[3,2-b]пиридин-5-карбоновую кислоту,
(1-изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-оксо-4,5-дигидро-1Н-пиррол[3,2-b]пиперидин-2-карбоновой кислоты,
сложный метиловый эфир 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(3,4,5,6-тетрагидро-2Н-[1,4']бипиридинил-4-илкарбамоил)-1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты,
1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(3,4,5,6-тетрагидро-2Н-[1,4']бипиридинил-4-илкарбамоил)-1Н-пиррол[3,2-b]пиридин-5-карбоновую кислоту,
(1-изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-c]пиридин-2-карбоновой кислоты,
(1-изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-(2-гидроксиэтокси)-1Н-пиррол[2,3-c]пиридин-2-карбоновой кислоты,
(1-изопропилпиперидин-4-ил)амид 1-[(5-хлорпиридин-2-илкарбамоил)метил]-5-(2-метиоксиэтокси)-1Н-пиррол[2,3-c]пиридин-2-карбоновой кислоты,
(1-изопропилпиперидин-4-ил)амид 1-[(5-хлорпиридин-2-илкарбамоил)метил]-5-(2-гидроксиэтокси)-1Н-пиррол[2,3-c]пиридин-2-карбоновой кислоты,
(1-изопропилпиперидин-4-ил)амид 1-[(6-хлорбензо[b]тиофен-2-илметил)-5-(2-метоксиэтокси)-1Н-пиррол[2,3-c]пиридин-2-карбоновой кислоты или
(1-изопропилпиперидин-4-ил)амид 1-[(6-хлорбензо[b]тиофен-2-илметил)-5-(2-гидроксиэтокси)-1Н-пиррол[2,3-c]пиридин-2-карбоновой кислоты.
Используемый в настоящем описании термин "алкил" следует понимать в самом широком смысле для обозначения углеводородных остатков, которые могут быть линейными или разветвленными, и которые могут быть ациклическими или циклическими остатками, или включать любую комбинацию ациклических и циклических субъединиц. Кроме того, используемый в настоящем описании термин "алкил" ясно включает насыщенные группы, а также ненасыщенные группы, где последние группы содержат одну или несколько, например, 1, 2 или 3, двойных связей и/или тройных связей при условии, что двойные связи не расположены внутри циклической алкильной группы таким образом, что получается ароматическая система. Все эти указания также относятся к ситуации, если алкильная группа встречается как заместитель на другом остатке, например, в алкоксиостатке, алкокосикарбонильном остатке или арилалкильном остатке. Примеры "-(С1-С8)-алкила" или "-(С1-С8)-алкилена" представляют собой алкильные остатки, содержащие от 1 до 8 атомов углерода, представляют собой метил, метилен, этил, этилен, пропил, пропилен, бутил, бутилен, пентил, пентилен, гексил, гептил или октил, н-изомеры всех этих остатков, изопропил, изобутил, 1-метилбутил, изопентил, неопентил, 2,2-диметилбутил, 2-метилпентил, 3-метилпентил, изогексил, втор-бутил, трет-пентил, трет-бутил, трет-пентил. Термин "-(С0-С6)-алкил" или "-(С0-С8)-алкилен" представляет собой углеводородный остаток, содержащий от 1 до 8 атомов углерода. Термин "-С0-алкил" или "С0-алкилен" представляет собой ковалентную связь.
Ненасыщенные алкильные остатки представляют собой, например, алкенильные остатки, такие как винил, 1-пропенил, 2-пропенил (=аллил), 2-бутенил, 3-бутенил, 2-метил-2-бутенил, 3-метил-2-бутенил, 5-гексенил или 1,3-пентадиенил, или алкинильные остатки, такие как этинил, 1-пропионил, 2-пропионил (=пропаргил) или 2-бутинил. Алкильные остатки могут также быть ненасыщенными, когда они замещены. Примерами -(С3-С8)-циклоалкильных циклических алкильных остатков являются циклоалкильные остатки, содержащие от 3 до 8 кольцевых атомов углерода, подобных циклопропилу, циклобутилу, циклопентилу, циклогексилу, циклогептилу или циклооктилу, которые могут также быть замещенными и/или ненасыщенными. Ненасыщенные циклические алкильные группы и ненасыщенные циклоалкильные группы, подобные, например, циклопентилу или циклогексенилу, могут быть связаны через любой атом углерода.
Подразумевается, что термины "моноциклический или бициклический 6-14-членный арил" или "-(С6-С14)-арил" означают ароматические углеводородные радикалы, содержащие от 6 до 14 атомов в кольце. Примерами -(С6-С14)-арильных радикалов являются фенил, нафтил, например, 1-нафтил и 2-нафтил, бифенилил, например, 2-бифенилил, 3-бифенилил и 4-бифенилил, антрил или флуоренил. Бифенильные радикалы, нафтильные радикалы и, в частности, фенильные радикалы представляют собой предпочтительные арильные радикалы.
Термины "моноциклический или бициклический 4-15-членный гетероциклил" или "-(С4-С15)-гетероциклил" относятся к гетероциклам, в которых один или несколько из 4-15 атомов углерода замещены гетероатомами, такими как азот, кислород или сера.
Примерами являются акридинил, 8-азабицикло[3.2.1]окт-3-ил, азаиндол(1Н-пирролопиридинил), азабензимидазолил, азаспиродеканил, азепинил, азетидинил, азиридинил, бензимидазолил, бензофуранил, бензотиофуранил, бензотиофенил, бензоксазолил, бензтиазолил, бензтриазолил, бензтетразолил, бензизоксазолил, бензизотиазолил, карбазолил, 4аН-карбазолил, карболинил, хроманил, хроменил, циннолинил, декагидрохинолинил, 4,5-дигидрооксазолинил, диоксазолил, диоксазинил, 1,3-диоксоланил, 1,3-диоксоленил, 6Н-1,5,2-дитиазинил, дигидрофтор[2,3-b]-тетрагидрофуранил, фуранил, фуразанил, имидазолидинил, имидазолинил, имидазолил, 1Н-индазолил, индолинил, индолизинил, индолил, 3Н-индолил, изобензофуранил, изохроманил, изоиндазолил, изоиндолинил, изоиндолил, изохинолинил(бензимидазолил), изотиазолил, изотиазолидинил, изотиазолинил, изоксазолил, изоксазолинил, изоксазолидинил, 2-изоксазолинил, кетопиперазинил, морфолинил, нафтиридинил, октагидроизохинолинил, оксадиазолил, 1,2,3-оксадиазолил, 1,2,4-оксадиазолил, 1,2,5-оксадиазолил, 1,3,4-оксадиазолил, 1,2-оксатиепанил, 1,2-оксатиоланил, 1,4-оксазепанил, 1,2-оксазинил, 1,3-оксазинил, 1,4-оксазинил, оксазолидинил, оксазолинил, оксазолил, оксетанил, оксоканил, фенантридинил, фенантролинил, феназинил, фенотиазинил, феноксатиинил, феноксазинил, фталазинил, пиперазинил, пиперидинил, птеридинил, пуринил, пиранил, пиразинил, пиразолидинил, пиразолинил, пиразолил, пиридазинил, пиридооксазолил, пиридоимидазолил, пиридотиазолил, пиридил, пиримидинил, пирролидинил, пирролидинонил, пирролинил, 2Н-пирролил, пирролил, хиназолинил, хинолинил, 4Н-хинолизинил, хиноксалинил, хинуклидинил, тетрагидрофуранил, тетрагидроизохинолинил, тетрагидрохинолинил, тетрагидрофуранил, тетрагидропиранил, тетрагидропиридинил, тетрагидротиофенил, тетразинил, тетразолил, 6Н-1,2,5-тиадиазинил, 1,2,3-тиадиазолил, 1,2,4-тиадиазолил, 1,2,5-тиадиазолил, 1,3,4-тиадиазолил, тиантренил, 1,2-тиазинил, 1,3-тиазинил, 1,4-тиазинил, 1,3-тиазолил, тиазолил, тиазолидинил, тиазолинил, тиенил, тиетанил, тиенотиазолил, тиенооксазолил, тиеноимидазолил, тиетанил, тиоморфолинил, 1λ6-тиоморфолинил, тиофенолил, тиофенил, тиопиранил, 1,2,3-триазинил, 1,2,4-триазинил, 1,3,5-триазинил, 1,2,3-триазолил, 1,2,4-триазолил, 1,2,5-триазолил, 1,3,4-триазолил и ксантенил.
Предпочтительными являются гетероциклы, такие как бензимидазолил, 1,3-бензодиоксолил, бензофуранил, бензотиазолил, бензотиофенил, бензоксазолил, хроманил, циннолинил, 2-фурил, 3-фурил, имидазолил, индолил, индазолил, изохроманил, изоиндолил, изохинолинил, изотиазолил, изоксазолил, оксазолил, фталазинил, птеридинил, пуринил, пиразинил, пиразолил, пирадизинил, пиридоимидазолил, пиридопиридинил, пиридопиримидинил, 2-пиридил, 3-пиридил, 4-пиридил, пиримидинил, пирролил; 2-пирролил, 3-пирролил, хинолинил, хиназолинил, хиноксалинил, тетразолил, тиазолил, 2-тиенил и 3-тиенил.
Предпочтительными являются также:
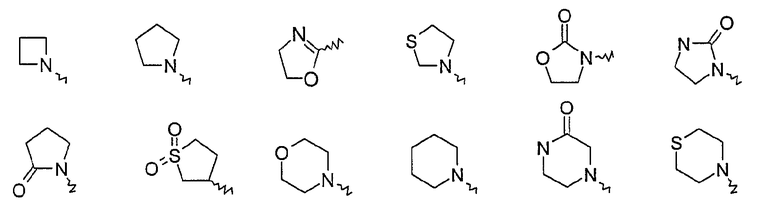
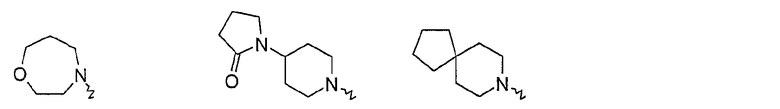
Термины "het" или "3-7-членный циклический остаток, содержащий до 1, 2, 3 или 4 гетероатомов", относятся к структурам гетероциклов, которые могут быть получены из соединений, таких как азепин, азетидин, азиридин, азирин, 1,4-диазепан, 1,2-диазепин, 1,3-диазепин, 1,4-диазепин, диазиридин, диазирин, диоксазол, диоксазин, диоксол, 1,3-диоксолен, 1,3-диоксолан, фуран, имидазол, имидазолин, имидазолидин, изотиазол, изотиазолидин, изотиазолин, изоксазол, изоксазолин, изоксазолидин, 2-изоксазолин, кетоморфолин, кетопиперазин, морфолин, 1,2-оксатиепан, 1,2-оксатиолан, 1,4-оксазепан, 1,2-оксазин, 1,3-оксазин, 1,4-оксазин, оксазол, оксазиридин, оксетан, оксиран, пиперазин, пиперидин, пиран, пиразин, пиразол, пиразолин, пиразолидин, пиридазин, пиридин, пиримидин, пиррол, пирролидин, пирролидинон, пирролин, тетрагидрофуран, тетрагидропиран, тетрагидропиридин, тетразин, тетразол, тиадиазин, тиадиазол, 1,2-тиазин, 1,3-тиазин, 1,4-тиазин, 1,3-тиазол, тиазол, тиазолидин, тиазолин, тиенил, тиетан, тиоморфолин, тиопиран, 1,2,3-триазин, 1,2,4-триазин, 1,3,5-триазин, 1,2,3-триазол или 1,2,4-триазол.
Термин "группа R1-N-R2-V может образовывать 4-7-членную циклическую группу" или "R11 и R12 вместе с атомом азота, с которым они связаны, могут образовывать 4-7-членное моноциклическое гетероциклическое кольцо, которое, в дополнение к атому азота, могут содержать 1 или 2 одинаковых или различных кольцевых гетероатома, выбранных из кислорода, серы и азота" относятся к структурам гетероциклов, которые могут быть получены из таких соединений как азепан, азепин, азетидин, диоксазол, диоксазин, 1,4-диазепан, 1,2-диазепин, 1,3-диазепин, 1,4-диазепин, имидазол, имидазолин, имидазолидин, изотиазол, изотиазолидин, изотиазолин, изоксазол, изоксазолин, изоксазолидин, 2-изоксазолин, кетопиперазин, морфолин, [1,4]оксазепан, оксазол, пиперазин, пиперидин, пиразин, пиразол, пиразолин, пиразолидин, пиридазин, пиридин, пиримидин, пиррол, пирролидин, пирролидинон, пирролин, тетрагидропиридин, тетразин, тетразол, тиазол, тиадиазол, тиазолидин, тиазолин, тиоморфолин, 1,2,3-триазин, 1,2,4-триазин, 1,3,5-триазин, 1,2,3-триазол или 1,2,4-триазол.
Термин "R15 и R16 вместе с атомом углерода, с которым они связаны, могут образовывать 3-6-членное карбоциклическое кольцо" относится к структурам, которые могут быть получены из соединений, таких как циклопропил, циклобутил, циклопентил или циклогексил.
Термин "подструктура
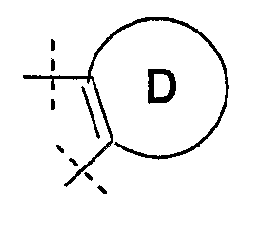
в формуле I" или " подструктура D" представляет собой
4-8-членную насыщенную, частично ненасыщенную или ароматическую циклическую группу, содержащую 0, 1, 2, 3 или 4 гетероатома, выбранных из азота, серы или кислорода" относится к структурам, которые могут быть получены из соединений, таких как азепан, азетидин, азетин, азокан, азокан-2-он, циклобутил, циклооктан, циклооктен, циклопентил, циклогексил, циклогептил, циклооктил, 1,2-диазепан, 1,2-диазепин, 1,3-диазепин, 1,4-диазепин, [1,4]диазокан, [1,2]диазокан-3-он, [1,3]диазокан-2-он, диоксазол, диоксазин, диоксол, 1,3-диоксолен, 1,3-диоксолан, фуран, имидазол, имидазолин, имидазолидин, изотиазол, изотиазолидин, изотиазолин, изоксазол, изоксазолин, изоксазолидин, 2-изоксазолин, кетопиперазин, морфолин, 1,4-оксаазепан, 1,2-оксатиепан, 1,2-оксатиолан, 1,2-оксазин, 1,3-оксазин, 1,4-оксазин, оксазол, [1,4]оксазокан, [1,3]оксазокан-2-он, оксетан, оксокан, оксокан-2-он, пиперазин, пиперидин, фенил, пиран, пиразин, пиразол, пиразолин, пиразолидин, пиридазин, пиридин, пиримидин, пиррол, пирролидин, пирролидинон, пирролин, 5,6,7,8-тетрагидро-1Н-азоцин-2-он, тетрагидрофуран, тетрагидропиран, тетрагидропиридин, тетразин, тиадиазин, тиадиазол, 1,2-тиазин, 1,3-тиазин, 1,4-тиазин, 1,3-тиазол, тиазол, тиазолидин, тиазолин, тиетан, тиокан, тиокан-1,1-диоксид, тиокан-1-оксид, тиокан-2-он, тиоморфолин, тиопиран, 1,2,3-триазин, 1,2,4-триазин, 1,3,5-триазин, 1,2,3-триазол или 1,2,4-триазол.
Термин "подструктура D" представляет собой 5-6-членную насыщенную, частично ненасыщенную или ароматическую циклическую группу, содержащую 0, 1, 2, 3 или 4 гетероатома, выбранных из азота, серы или кислорода" относится к структурам, которые могут быть получены из соединений, таких как циклопентил, циклогексил, диоксазол, диоксазин, диоксол, 1,3-диоксолен, 1,3-диоксолан, фуран, имидазол, имидазолин, имидазолидин, изотиазол, изотиазолидин, изотиазолин, изоксазол, изоксазолин, изоксазолидин, 2-изоксазолин, кетоморфолин, кетопиперазин, морфолин, 1,2-оксатиолан, 1,2-оксазин, 1,3-оксазин, 1,4-оксазин, оксазол, пиперазин, пиперидин, фенил, пиран, пиразин, пиразол, пиразолин, пиразолидин, пиразин, пиразинон, пиридазин, пиридазон, пиридин, пиридон, пиримидин, пиримидон, пиррол, пирролидин, пирролидинон, пирролин, тетрагидрофуран, тетрагидропиран, тетрагидропиридин, тетразин, тетразол, тиадиазин, тиадиазол, 1,2-тиазин, 1,3-тиазин, 1,4-тиазин, 1,3-тиазол, тиазол, тиазолидин, тиазолин, тиоморфолин, тиопиран, тетразин, тетразол, 1,2,3-триазин, 1,2,4-триазин, 1,3,5-триазин, 1,2,3-триазол или 1,2,4-триазол.
Термин "R1 и R3 вместе с атомами, с которыми они связаны, могут образовать 6-8-членную циклическую группу, содержащую 1, 2, 3 или 4 гетероатома, выбранных из азота, серы или кислорода" относится к структурам гетероциклов, которые могут быть получены из соединений, таких как азокан, азокан-2-он, циклогептил, циклогексил, циклооктан, циклооктен, 1,4-диазепан, 1,2-диазепин, 1,3-диазепин, 1,4-диазепин, [1,4]диазокан, [1,2]диазокан-3-он, [1,3]диазокан-2-он, диоксазин, [1,4]диоксокан, диоксол, кетопиперазин, морфолин, 1,2-оксатиепан, 1,4-оксазепан, 1,2-оксазин, 1,3-оксазин, 1,4-оксазин, [1,4]оксазокан, [1,3]оксазокан-2-он, оксокан, оксокан-2-он, фенил, пиперазин, пиперидин, пиран, пиразин, пиридазин, пиримидин, 5,6,7,8-тетрагидро-1Н-азоцин-2-он или тиоморфолин.
То, что многие из перечисленных выше названий гетероциклов представляют собой химические названия ненасыщенных или ароматических кольцевых систем, не подразумевает, что 4-15-членная моно- или полициклическая группа может быть получена только из соответствующей ненасыщенной кольцевой системы. Названия в настоящем описании служат только для описания кольцевой системы в отношении размера кольца и количества гетероатомов и их относительных положений. Как объяснено выше, 4-15-членная моно- или полициклическая группа может быть насыщенной или частично ненасыщенной или ароматической и, таким образом, в случае пригодности, может быть получена не только из самих перечисленных выше гетероциклов, но также из всех их частично или полностью гидрогенизированных аналогов, а также из их более высоко ненасыщенных аналогов. В качестве примеров полностью или частично гидрогенизированных аналогов перечисленных выше гетероциклов, из которых может быть получена эта группа, можно упомянуть следующие: пирролин, пирролидин, тетрагидрофуран, тетрагидротиофен, дигидропиридин, тетрагидропиридин, пиперидин, 1,3-диоксолан, 2-имидазолин, имидазолидин, 4,5-дигидро-1,3-оксазол, 1,3-оксазолидин, 4,5-дигидро-1,3-тиазол, 1,3-тиазолидин, пергидро-1,4-диоксан, пиперазин, пергидро-1,4-оксазин (=морфолин), пергидро-1,4-тиазин (=тиоморфолин), пергидроазепин, индолин, изоиндолин, 1,2,3,4-тетрагидрохинолин или 1,2,3,4-тетрагидроизохинолин.
Термин "-(С1-С3)-перфторалкил" представляет собой частично или полностью фторированный алкильный остаток, который можно получить из остатков, таких как -CF3, -CHF2, -CH2F, -CHF-CF3, -CHF-CHF2, -CHF-CH2F, -CH2-CF3, -CH2-CHF2, -CH2-CH2F, -CF2-CF3, -CF2-CHF2, -CF2-CH2F, -CH2-CHF-CF3, -CH2-CHF-CHF2, -CH2-CHF-CH2F, -CH2-CH2-CF3, -CH2-CH2-CHF2, -CH2-CH2-CH2F, -CH2-CF2-CF3, -CH2-CF2-CHF2, -CH2-CF2-CH2F, -CHF-CHF-CF3, -CHF-CHF-CHF2, -CHF-CHF-CH2F, -CHF-CH2-CF3, -CHF-CH2-CHF2, -CHF-CH2-CH2F, -CHF-CF2-CF3, -CHF-CF2-CHF2, -CHF-CF2-CH2F, -CF2-CHF-CF3, -CF2-CHF-CHF2, -CF2-CHF-CH2F, -CF2-CH2-CF3, -CF2-CH2-CHF2, -CF2-CH2-CH2F, -CF2-CF2-CF3, -CF2-CF2-CHF2 или -CF2-CF2-CH2F.
Термин "-(С1-С3)-перфторалкилен" представляет собой частично или полностью фторированный алкиленовый остаток, который можно получить из остатков, таких как -CF2-, -CHF-, -CHF-CHF2-, -CHF-CHF-, -CH2-CF2-, -CH2-CHF-, -CF2-CF2-, -CF2-CHF-, -CH2-CHF-CF2-, -CH2-CHF-CHF-, -CH2-CH2-CF2-, -CH2-CH2-CHF, -CH2-CF2-CF2-, -CH2-CF2-CHF-, -CHF-CHF-CF2-, -CHF-CHF-CHF-, -CHF-CH2-CF2-, -CHF-CH2-CHF-, -CHF-CF2-CF2-, -CHF-CF2-CHF-, -CF2-CHF-CF2-, -CF2-CHF-CHF-, -CF2-CH2-CF2-, -CF2-CH2-CHF-, -CF2-CF2-CF2- или -CF2-CF2-CHF.
Термин "оксо-остаток" или "=О" относится к остаткам, таким как карбонил (-С(О)-) или нитрозо (-N=O). Галоген представляет собой фтор, хлор, бром или иод, предпочтительно, фтор, хлор или бром, особенно предпочтительно хлор или бром.
Оптически активные атомы углерода, присутствующие в соединениях формулы I, могут независимо друг от друга иметь конфигурацию R или конфигурацию S. Соединения формулы I могут присутствовать в форме чистых энантиомеров или чистых диастереомеров или в форме смесей энантиомеров и/или диастереомеров, например, в форме рацематов. Настоящее изобретение относится к чистым энантиомерам и смесям энантиомеров, а также к чистым диастереомеров и смесям диастереомеров. Изобретение включает смеси двух или более двух стереоизомеров формулы I, и оно включает все соотношения стереоизомеров в смесях. В случае, когда соединения формулы I могут присутствовать в виде Е-изомеров или Z-изомеров (или цис-изомеров или транс-изомеров), изобретение относится и к чистым Е-изомерам, и к чистым Z-изомерам и к E/Z смесям во всех соотношениях. Изобретение также включает все таутомерные формы соединений формулы I.
Диастереомеры, включая E/Z изомеры, можно разделить на отдельные изомеры, например, хроматографией. Рацематы можно разделить на 2 энантиомера обычными способами, например, хроматографией, на хиральные фазы или разделением, например, кристаллизацией диастереомерных солей, полученных с оптически активными кислотами или основаниями. Стереохимически однородные соединения формулы I можно также получить использованием стереохимически однородных исходных материалов или использованием стереоселективных реакций.
Физиологически приемлемые соли соединений формулы I представляют собой нетоксичные соли, которые являются физиологически приемлемыми, в частности, фармацевтически используемыми солями. Такие соли соединений формулы I, содержащие кислотные группы, например, карбоксильную группу СООН, представляют собой, например, соли щелочных металлов или соли щелочноземельных металлов, такие как соли натрия, соли калия, соли магния и соли кальция, а также соли с физиологически приемлемыми ионами четвертичного аммония, такими как тетраметиламмоний или тетраэтиламмоний, и кислотно-аддитивные соли с аммонием и физиологически приемлемыми органическими аминами, такими как метиламин, диметиламин, триметиламин, этиламин, триэтиламин, этаноламин или трис-(2-гидроксиэтил)амин. Основные группы, содержащиеся в соединениях формулы I, например, аминогруппы или гуанидиногруппы, образуют кислотно-аддитивные соли, например, с неорганическими кислотами, такими как хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота или фосфорная кислота, или с органическими карбоновыми кислотами и сульфоновыми кислотами, такими как муравьиная кислота, уксусная кислота, щавелевая кислота, лимонная кислота, молочная кислота, яблочная кислота, янтарная кислота, малоновая кислота, бензойная кислота, малеиновая кислота, фумаровая кислота, винная кислота, метансульфоновая кислота или пара-толуолсульфоновая кислота. Соединения формулы I, которые одновременно содержат основную группу и кислотную группу, например, гуанидиногруппу и карбоксильную группу, могут также присутствовать в виде цвиттерионов (бетаинов), которые аналогичным образом включены в настоящее изобретение.
Соли соединений формулы I можно получить обычными способами, известными специалистам в данной области, например, объединением соединения формулы I с неорганической или органической кислотой или основанием в растворителе или диспергирующем веществе, или из других солей катионным или анионным обменом. Настоящее изобретение также включает все соли соединений формулы I, которые, ввиду низкой физиологической переносимости, прямо не подходят для использования в лекарственных средствах, но подходят, например, в качестве промежуточных соединений для проведения дальнейших химических модификаций соединений формулы I или в качестве исходных материалов для получения физиологически приемлемых солей.
Настоящее изобретение, кроме того, включает все растворители соединений формулы I, например гидраты или аддукты со спиртами.
Изобретение также включает производные и модификации соединений формулы I, например, пролекарства, защищенные формы и другие физиологически приемлемые производные, а также активные метаболиты соединений формулы I. Изобретение относится, в частности, к пролекарствам и защищенным формам соединений формулы I, которые могут быть превращены в соединения формулы I в физиологических условиях. Подходящие пролекарства для соединений формулы I, т.е. химически модифицированные производные соединений формулы I, имеющие свойства, которые улучшаются желательным образом, например, в отношении растворимости, биологической доступности или длительности действия, известны специалистам в данной области. Более подробную информацию, относящуюся к пролекарствам, можно найти в стандартной литературе, подобной, например, Design of Prodrugs, H. Bundgaard (ed.), Elsevier, 1985; Fleisher et al., Advanced Drug Delivery Reviews 19 (1996) 115-130; или H. Bundgaard, Drugs of the Future 16 (1991) 443, которые все включены в настоящее описание в качестве ссылки. Подходящие пролекарства для соединений формулы I представляют собой, в частности, ацильные пролекарства и карбаматные пролекарства ацилатируемых содержащих азот групп, таких как аминогруппы и гуанидиногруппы, а также сложноэфирные пролекарства и амидные пролекарства групп карбоновых кислот, которые могут присутствовать в соединениях формулы I. В ацильных пролекарствах и карбаматных пролекарствах один или несколько, например, 1 или 2, атома водорода на атомах азота в таких группах замещены ацильной группой или карбаматом, предпочтительно, -(С1-С6)-алкилоксикарбонильной группой. Подходящие ацильные группы и карбаматные группы для ацильных пролекарств и карбаматных пролекарств представляют собой, например, пролекарства Rp1-CO- и Rp2-О-CO-, где Rp1 представляет собой (C1-C18)-алкил, (C1-C8)-циклоалкил, (C3-C8)-циклоалкил-(C1-C4)-алкил, (C6-C14)-арил, Het-, (C6-C14)-арил-(C1-C4)-алкил, или Het-(C1-C4)-алкил и в которых Rp2 имеет значения, указанные для Rp1, за исключением водорода.
Особенно предпочтительные соединения формулы I представляют собой те, в которых 2 или более остатков определены, как указано выше, для предпочтительных соединений формулы I, или остатки могут иметь один или некоторые из специфических определений остатков, представленных в их общих определениях или в представленных выше определениях предпочтительных соединений. Все возможные комбинации определений, представленных для предпочтительных определений определенных обозначений остатков, определенно являются предметом настоящего изобретения.
Также в отношении всех предпочтительных соединений формулы I, все их стереоизомерные формы и их смеси в любом соотношении и их физиологически приемлемые соли определенно являются предметом настоящего изобретения, а также их пролекарства. Аналогичным образом, также во всех предпочтительных соединениях формулы I все остатки, которые присутствуют более одного раза в молекуле, являются независимыми друг от друга и могут быть одинаковыми или различными.
Соединения формулы I можно получить использованием процедур и методик, которые сами по себе известны и понятны специалисту в данной области. Исходные материалы или образующие блоки для использования в общих синтетических процедурах, которые можно применить при получении соединений формулы I, легко доступны специалисту в данной области. Во многих случаях они имеются в продаже или были описаны в литературе. Иначе их можно получить из легко доступных соединений-предшественников аналогично процедурам, описанным в литературе, или по процедурам или аналогично процедурам, описанным в настоящей заявке.
В целом, соединения формулы I можно получить, например в ходе конвергентного синтеза, связыванием двух или более фрагментов, которые могут быть получены ретросинтетически из соединений формулы I. Конкретнее, подходяще замещенные исходные азаиндольные производные используются в качестве образующих блоков при получении соединений формулы I. Хотя различные синтетические аспекты химии азаиндолов значительно отличаются от химии индолов, многие процедуры, описывающие синтез и функционализацию индолов, могут быть модифицированы и приспособлены специалистами в данной области. Поэтому литература, описывающая трансформации и синтез индолов, высоко инструктивна и применима к химии азаиндолов. Если такие азаиндольные производные отсутствуют в продаже, их можно получить в соответствии с хорошо известными стандартными процедурами для образования азаиндольной кольцевой системы, такой как, например, индольный синтез Фишера, индольный синтез Бишлера или индольный синтез Рейссерта. Путем выбора подходящих молекул-предшественников, эти виды индольного синтеза обеспечивают возможность введения разнообразных заместителей в различные положения азаиндольной системы, которую можно затем химически модифицировать для окончательного получения молекулы формулы I, имеющей желательный тип заместителя. В качестве одного из всеобъемлющих обзоров по химии индолов и по синтетическим процедурам для их получения, находится ссылка W.J. Houlihan (ed.), "Indoles, Part One", volume 25, 1972, из серии "The Chemistry of Heterocyclic Compounds", A. Weissberger and E.C. Taylor (ed.), John Wiley & Sons; R.E. Willette, Advances in Heterocyclic Chemistry 9 (1968) 27; J.-Y. Merour Curr. Org. Chem. 5 (2001) 471; H. Döpp et al. in Houben-Weyl, "Methoden der Organischen Chemie" (Methods of Organic Chemistry), Georg Thieme Verlag, Stuttgart, Germany 1994, Vol E6a,b part 2a Hetarene I.
Если предстоит синтезировать исходные азаиндольные производные, то это может быть сделано, например, в соответствии с хорошо известным упомянутым выше азаиндольным синтезом. В следующем описании дано его краткое объяснение, однако, они представляют собой стандартные процедуры, всесторонне обсужденные в литературе, и они хорошо известны специалисту в данной области.
Индольный синтез Фишера включает кислотную циклизацию гетероарилгидразонов, например, общей формулы 2,
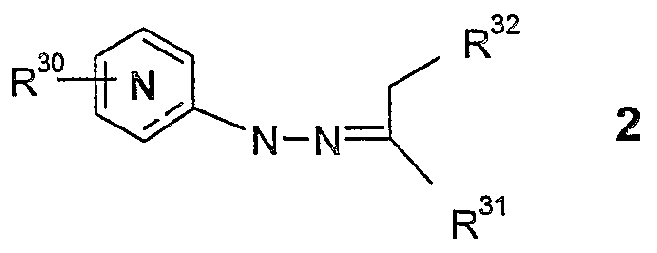
которые можно получить различными способами, и в которых R30, R31 и R32 могут иметь широкое разнообразие определений. Кроме водорода и алкила, R31 и R32 могут, в частности, обозначать сложноэфирные группы, или метильные, или этильные группы, или 2,2,2-трифторэтильные группы, несущие сложноэфирную группу в качестве заместителя, таким образом, обеспечивая возможность введения в азаиндольную молекулу части (CH2)p-CO, встречающейся в группах R2 и/или R3 в соединениях формулы I. В качестве примеров многочисленных литературных ссылок, описывающих синтез азаиндольных производных, в соответствии с синтезом Фишера, кроме указанной выше книги, изданной Houlihan, упоминаются следующие статьи: F.G. Salituro et al., J. Med. Chem. 33 (1990) 2944; N.M. Gray et al., J. Med. Chem. 34 (1991) 1283; J. Sh. Chikvaidze et al., Khim. Geterotsikl. Soedin. (1991) 1508; S.P. Hiremath et al., Indian J. Chem. 19 (1980) 770; J. Bornstein, J. Amer. Chem. Soc. 79 (1957) 1745; S. Wagaw, B. Yang и S. Buchwald, J. Am. Chem. Soc. 121 (1999) 10251 или by Y. Murakami, Y. Yokoyama, T. Miura, H. Hirasawa Y. Kamimura и M. Izaki, Heterocycles 22 (1984) 1211; D. L. Hughes, Org. Prep. Proc. 25 (1993) 607.
Индольный синтез Рейссерта включает восстановительную циклизацию о-нитрофенилпировиноградных кислот или их сложных эфиров, например, общей формулы 3
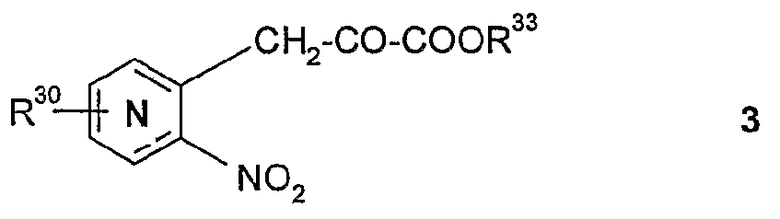
в которой R30 может иметь широкое разнообразие определений и может присутствовать во всех положениях ароматического кольца. Индольный синтез Рейссерта ведет к получению производных азаиндол-2-карбоновых кислот. Производные пировиноградной кислоты формулы 3 можно получить конденсацией сложных эфиров щавелевой кислоты замещенными о-нитрометилазабензолов. В качестве литературных источников, кроме указанной выше книги, изданной Houlihan, и указанных в настоящем описании литературных ссылок, упоминаются, например, статьи: H.G. Lindwall и G.J. Mantell, J. Org. Chem. 18 (1953) 345 или H. Burton и J.L. Stoves, J. Chem. Soc. (1937) 1726 или W. Noland, F. Baude, Org. Synth Coll. Vol. V, J. Wiley, New York, (1973) 567.
Другой способ достижения селективного в отношении области доступа к азаиндольной структуре включает палладиевый катализ, например, о-галоанилины (X=Cl, Br, I) или о-трифторметансульфонилоксианилины (X=Otf) общей формулы 4 могут быть циклизованы в азаиндолы с использованием нескольких алкинов принятием процедур, описанных J. Ezquerra, C Pedregal. C Lamas, J. Barluenga, M. Perez, M. Garcia-Martin, J. Gonzalez, J. Org. Chem. 61 (1996) 5805; или F. Ujjainwalla, D. Warner, Tetrahedron Lett. 39 (1998) 5355 и, кроме того, A. Rodriguez, C. Koradin, W. Dohle, P. Knochel, Angew. Chem. 112 (2000) 2607; или R. Larock, E. Yum, M. Refvik, J. Org. Chem. 63 (1998) 7653; R. Larock, E. Yum, J. Am. Chem. Soc. 113 (1991) 6689; K. Roesch; R. Larock, J. Org. Chem. 66 (2001) 412.
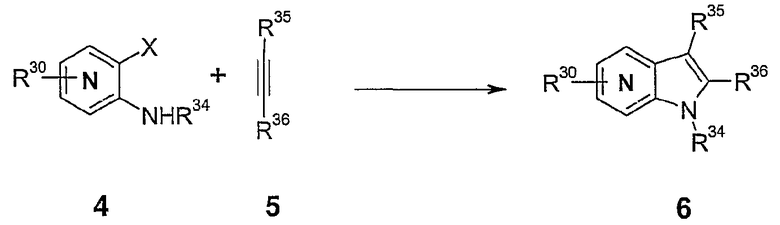
Альтернативно, азаиндольную структуру можно создать использованием разнообразных кетонов в условиях палладиевого катализа принятием и модификацией процедуры, описанной C.Chen, D. Liebermann, R.Larsen, T.Verhoeven и P.Reider J. Org. Chem. 62 (1997) 2676, как указано ниже, где X = Cl, Br, I или Otf:
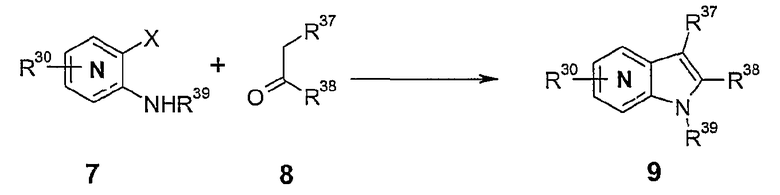
В соответствии с индольным синтезом Бишлера, А-аза-анилинкетоны, например, общей формулы 10,

могут быть циклизованы в азаиндольные производные.
Еще один путь к специфически замещенным азаиндольным производным проходит через 2,3-дигидроазаиндолы (азаиндолины), которые могут быть легко получены восстановлением азаиндолов, например, гидрогенизацией или циклизацией подходящих азафенилэтиламиновых производных. Азаиндолины могут подвергаться разнообразной электрофильной ароматической реакции замещения, обеспечивающей возможность введения различных заместителей в ароматическое ядро, которое не может быть непосредственно введено в ароматическое ядро азаиндольной молекулы. Затем азоиндолы могут быть дегидрогенизированы в соответствующие азаиндолы, например, реагентами, подобными хлоранилу или палладию, вместе с акцептором водорода. И снова, детали по этим способам синтеза можно обнаружить в указанной выше книге под редакцией Houlihan.
Более того, 2-Н-азаиндолы могут быть превращены в соответствующие карбоновые кислоты или сложные эфиры карбоновых кислот введением лития в положение 2 азаиндолов общей формулы 13 и последующим взаимодействием с двуокисью углерода или алкилхлорформиатом в соответствии с I. Hasan, E. Marinelli, L. Lin, F. Fowler, A. Levy, J. Org. Chem. 46 (1981) 157; T. Kline J. Heterocycl. Chem. 22 (1985) 505; J.-R. Dormoy, A. Heymes, Tetrahedron 49, (1993) 2885; E. Desarbre, S. Coudret, C. Meheust, J.-Y. Merour, Tetrahedron 53 (1997) 3637, как указано ниже:
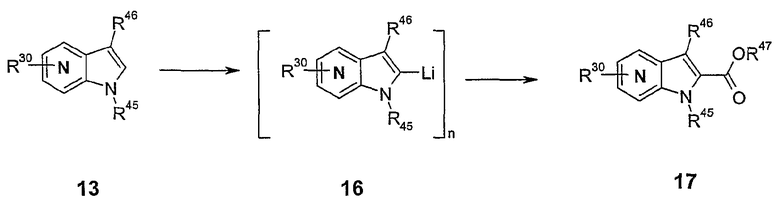
где R45 обозначает водород или защитную группу, подобную, например, бензолсульфонилу или трет-бутоксикарбонилу.
Ниже перечислены и вкратце приведены в виде ссылок дальнейшие процедуры, представляющие особый интерес для осуществления настоящего изобретения, однако они представляют собой стандартные процедуры, всесторонне обсужденные в литературе, и они хорошо известны специалисту в данной области.
1) T. Sakamoto et al., Chem. Pharm. Bull. 34 (1986) 2362.

a) I. Mahadevan et al., J. Heterocycl. Chem. 29 (1992) 359
b) J.-R. Dormoy et al., Tetrahedron 49 (1993) 2885
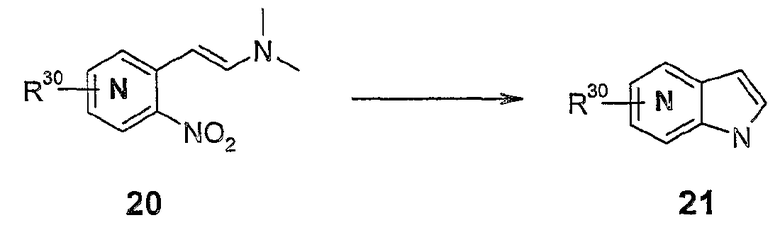
3) a) L. Estel et al., J. Org. Chem. 53 (1988) 2740
b) D. Hands et al., Synthesis (1996) 877
c) T. Kumiko et al., Bioorg. Med. Chem. Lett. 20 (2000) 2347
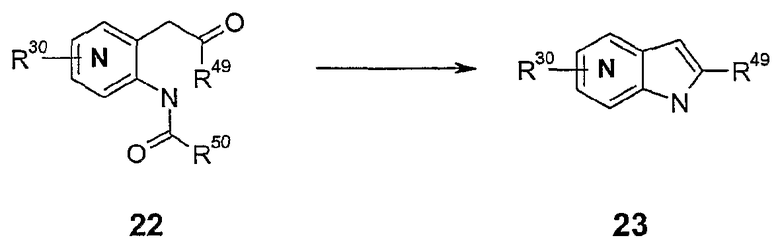
4) a) S. Clemo et al., J. Chem. Soc. (1945) 603
b) R. Okuda, J. Org. Chem. 24 (1959) 1008
c) J. Turner, J. Org. Chem. 48 (1983) 3401
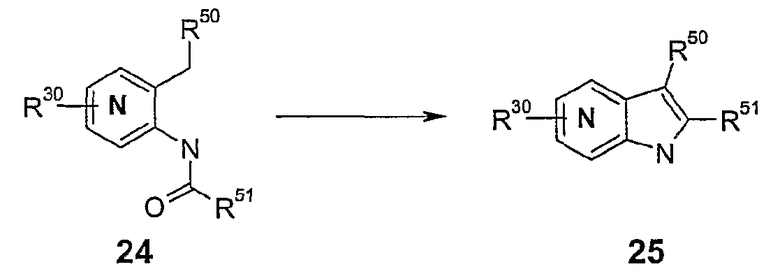
5) a) M. Davis et al., Tetrahedron 48 (1992) 939
b) C. Martin et al., Tetrahedron Lett. 30 (1989) 935
c) S. Ball et al., J. Organomet. Chem. 550 (1998) 457

В зависимости от заместителей в исходных материалах, в определенных видах синтеза азаиндолов могут быть получены смеси позиционных изомеров, которые, однако, можно отделить современными методиками отделения, подобными, например, препаративной ВЭЖХ.
Кроме того, для получения желательных заместителей в ядре азаиндольной кольцевой системы в формуле I функциональные группы, введенные в кольцевую систему во время азаиндольного синтеза, могут быть химически модифицированы. Например, азаиндолы, несущие атом водорода в положении 2 и положении 3, можно также получить омылением и последующим декарбоксилированием азаиндолов, несущих сложноэфирную группу в соответствующем положении. Группы карбоновых кислот и группы уксусных кислот в положении 2 и положении 3 могут быть превращены в их гомологи обычными реакциями для удлинения цепи карбоновых кислот. Атомы галогена можно ввести в положение 2 и положение 3, например, взаимодействием соответствующего азаиндолинона с галогенизирующим агентом, таким как пентахлорид фосфора, аналогично способу, описанному J.C.Powers, J. Org. Chem. 31 (1966) 2627. Исходные азаиндолиноны для такого синтеза можно получить из 2-аминогетероарилуксусных кислот. Исходные азаиндольные производные для получения соединений формулы I, несущих галогеновый заместитель в положении 3, можно также получить в соответствии с процедурами, описанными в литературе, подобными следующим. Для фторирования производных сложного этилового эфира 1Н-азаиндол-2-карбоновой кислоты в положении 3 трифлат N-фтор-2,4,6-триметилпиридиния представляет собой реагент выбора (T. Umemoto, S. Fukami, G. Tomizawa, K. Harasawa, K. Kawada, K. Tomita J. Am. Chem. Soc. 112 (1990) 8563). Хлорирование производных сложного этилового эфира 1Н-азаиндол-2-карбоновой кислоты в положении 3 взаимодействием сульфурилхлорида в бензоле дает сложный этиловый эфир 3-хлор-1Н-азаиндол-2-карбоновой кислоты (Chem. Abstr. 1962, 3441i-3442b); такой же результат можно получить средствами NCS (D. Comins, M. Killpack, Tetrahedron Lett. 33 (1989) 4337; M. Brennan, K. Erickson, F. Szmlac, M. Tansey, J. Thornton, Heterocycles 24 (1986) 2879). Бромирование производных сложного этилового эфира 1Н-азаиндол-2-карбоновой кислоты в положении 3 может быть достигнуто взаимодействием с NBS (M. Tani, H. Ikegami, M. Tashiro, T. Hiura, H. Tsukioka, Heterocycles 34 (1992) 2349). Аналогично процедурам, описанным выше, NIS можно использовать по существу для иодирования производных сложного этилового эфира 1Н-азаиндол-2-карбоновой кислоты в положении 3. Кроме того, иодирование производных сложного этилового эфира 1Н-азаиндол-2-карбоновой кислоты в положении 3 эффективно использование иода (T. Sakamoto, T. Nagano, Y. Kondo, H. Yamanaka Chem. Pharm. Bull. 36 (1988) 2248).
В частности, группы, присутствующие в азаиндольной кольцевой системе, могут быть модифицированы разнообразными реакциями и, таким образом, могут быть получены желательные остатки R3a и R30. Например, нитрогруппы могут быть восстановлены в аминогруппы различными восстанавливающими агентами, такими как сульфиды, дитиониты, сложные гидриды, или каталитическим гидрированием. Восстановление нитрогруппы можно также провести на более поздней стадии синтеза соединения формулы I, и восстановление нитрогруппы в аминогруппу может также происходить спонтанно реакцией, осуществляемой на другой функциональной группе, например, при взаимодействии группы, подобной цианогруппе, с гидросульфидом, или при гидрировании группы. Для введения или получения остатков R3a и R30 аминогруппы могут затем быть модифицированы в соответствии со стандартными процедурами для алкилирования, например, взаимодействием с (замещенными) алкилгалогенидами или восстановительным аминированием карбонильных соединений, в соответствии со стандартными процедурами для алкилирования, например, взаимодействием с активированными производными карбоновых кислот, такими как хлориды кислот, ангидриды, активированные сложные эфиры, или взаимодействием с карбоновыми кислотами в присутствии активирующего агента, или в соответствии с процедурами для сульфонилирования, например, взаимодействием с сульфонилхлоридами. Карбоновые кислоты, хлориды карбоновых кислот или сложные эфиры карбоновых кислот могут быть введены процедурами, описанными F. Santangelo, C. Casagrande, G. Norcini, F. Gerli, Synth. Commun. 23 (1993) 2717; P. Beswick, C. Greenwood, T. Mowlem, G. Nechvatal, D. Widdowson, Tetrahedron 44 (1988) 7325; V. Collot, M. Schmitt, P. Marwah, J. Bourguignon, Heterocylces 51 (1999) 2823. Галогены или гидроксигруппы - посредством трифлата или нонафлата - или первичные амины - посредством их диазониевой соли - или после взаимопревращения в соответствующий станнан, или бороновая кислота, присутствующая в азаиндольной структуре, могут быть превращены в разнообразные другие функциональные группы, например, -CN, -CF3, простые эфиры, кислоты, сложные эфиры, амиды, амины, алкильные или арильные группы, опосредованные посредством переходных металлов, а именно, катализом палладием или никелем или солями меди и реагентами, например, указанными ниже (F. Diederich, P. Stang, Metal-catalyzed Cross-coupling Reactions, Wiley-VCH, 1998; или M. Beller, C. Bolm, Transition Metals for Organic Synthesis, Wiley-VCH, 1998; J. Tsuji, Palladium Reagents и Catalysts, Wiley, 1996; J. Hartwig, Angew. Chem. 110 (1998) 2154; B. Yang, S. Buchwald, J. Organomet. Chem. 576 (1999) 125; T. Sakamoto, K. Ohsawa, J. Chem. Soc. Perkin Trans I, (1999), 2323; D. Nichols, S. Frescas, D. Marona-Lewicka, X. Huang, B. Roth, G. Gudelsky, J. Nash, J. Med. Chem, 37 (1994), 4347; P. Lam, C. Clark, S. Saubern, J. Adams, M. Winters, D. Chan, A. Combs, Tetrahedron Lett., 39 (1998) 2941; D. Chan, K. Monaco, R. Wang, M. Winters, Tetrahedron Lett. 39 (1998) 2933; V. Farina, V. Krishnamurthy, W. Scott, The Stille Reaction, Wiley, 1994; A. Klaspars, X. Huang, S. Buchwald, J. Am. Chem. Soc. 124 (2002) 7421; F. Kwong, A. Klapars, S. Buchwald, Org. Lett. 4 (2002) 581; M Wolter, G. Nordmann, G. Job, S. Buchwald, 4 (2002) 973).
Сложноэфирные группы, присутствующие в азаиндольном ядре, могут быть гидролизованы в соответствующие карбоновые кислоты, которые после активации могут затем взаимодействовать с аминами или спиртами в стандартных условиях. Кроме того, эти сложноэфирные или кислотные группы могут быть восстановлены в соответствующие спирты разнообразными стандартными процедурами. Группы простого эфира, присутствующие в азаиндольном ядре, например, бензилоксигруппы или другие легко расщепляемые группы простых эфиров, могут расщепляться для получения гидроксигрупп, которые затем могут взаимодействовать с разнообразными агентами, например, агентами этерификации или активирующими агентами, обеспечивающими возможность замещения гидроксигрупп другими группами. Содержащие серу группы могут взаимодействовать аналогичным образом.
В ходе синтеза для модификации групп R54 или R8', присоединенных к азаиндольной кольцевой системе, с применением методологии параллельного синтеза, кроме разнообразных реакций, крайне полезным может быть катализ солью палладия или меди. Такие реакции описаны, например, в F. Diederich, P. Stang, Metal-catalyzed Cross-coupling Reactions, Wiley-VCH, 1998; или M. Beller, C. Bolm, Transition Metals for Organic Synthesis, Wiley-VCH, 1998; J. Tsuji, Palladium Reagents and Catalysts, Wiley, 1996; J. Hartwig, Angew. Chem. 110 (1998), 2154; B. Yang, S. Buchwald, J. Organomet. Chem. 576 (1999) 125; P. Lam, C Clark, S. Saubern, J.Adams, M. Winters, D. Chan, A. Combs, Tetrahedron Lett. 39 (1998) 2941; D.Chan, K. Monaco, R. Wang, M. Winters, Tetrahedron Lett. 39 (1998) 2933; J. Wolfe, H. Tomori, J. Sadight, J. Yin, S. Buchwald, J. Org. Chem. 65 (2000) 1158; V. Farina, V. Krishnamurthy, W. Scott, The Stille Reaction, Wiley, 1994; A. Klaspars, X. Huang, S. Buchwald, J. Am. Chem. Soc. 124 (2002) 7421; F. Kwong, A. Klapars, S. Buchwald, Org. Lett. 4 (2002) 581; M Wolter, G. Nordmann, G. Job, S. Buchwald, 4 (2002) 973).
Ранее упомянутые реакции для превращения функциональных групп, кроме того, в целом, исключительно описаны в руководствах по органической химии, подобных M. Smith, J. March, March's Advanced Organic Chemistry, Wiley-VCH, 2001 и в учебниках, подобных Houben-Weyl, "Methoden der Organischen Chemie" (Methods of Organic Chemistry), Georg Thieme Verlag, Stuttgart, Germany, или "Organic Reactions", John Wiley & Sons, New York, или R. C. Larock, "Comprehensive Organic Transformations", Wiley-VCH, 2nd ed (1999), B. Trost, I. Fleming (eds.), Comprehensive Heterocyclic Chemistry II, Elsevier Science, 1996), в которых можно найти детали по реакциям и литературные первоисточники. Ввиду того, что в настоящем случае функциональные группы присоединены к азаиндольной системе, в определенных случаях может стать необходимым специальное приспособление условий взаимодействия или выбрать специфические реагенты из разнообразных реагентов, которые могут в принципе использоваться при реакции превращения, или принять специфические меры для достижения желательного превращения, например, использование методик защитных групп. Однако обнаружение подходящих вариантов взаимодействия и условий реакции в таких случаях не вызывает никаких проблем для специалиста в данной области.
Структурные элементы, присутствующие в остатках в положении 1 азаиндольного кольца в соединениях формулы I, и в группе COR8', присутствующей в положении 2 и/или в положении 3 азаиндольного кольца, можно ввести в исходное азаиндольное производное, которое можно получить, как указано выше, последовательными стадиями взаимодействия с использованием методологий синтеза, подобных методологиям, описанным ниже, с использованием процедур, которые сами по себе хорошо известны специалисту в данной области.
Остатки R8', которые можно ввести в формулу 29, например, конденсацией соответствующей карбоновой кислоты формулы 29 соединением формулы HR8', т.е. амином формулы HN(R1')R2'-V-G-M для получения соединения формулы 30. Полученное таким образом соединение формулы 30 может уже содержать желательные конечные группы, т.е. группы R8'и R54 могут представлять собой группы -N(R1)R2-V-G-M и R0-Q-, как определено в формуле I, или необязательно в соединении формулы 30, полученном таким образом; затем остаток или остатки R8' и остаток R54 превращаются соответственно в остатки N(R1)R2-V-G-M и R0-Q- для получения желательного соединения формулы I.
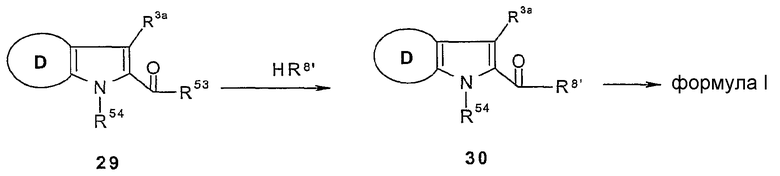
Таким образом, остатки R8' и соответственно остатки R1' и R2'-V-G-M, содержащиеся в них, могут иметь представленные выше обозначения, соответственно, R1 и R2-V-G-M или в дополнение к остаткам функциональные группы R1' и R2'-V-G-M могут также присутствовать в форме групп, которые могут в последующем трансформироваться в конечные группы R1 и R2-V-G-M, т.е. функциональные группы могут присутствовать в форме групп-предшественников или производных, например, в защищенной форме. В ходе получения соединений формулы I в целом может быть предпочтительно или необходимо ввести функциональные группы, которые восстанавливают или предотвращают нежелательные взаимодействия или побочные реакции на соответствующей стадии синтеза, в форме групп-предшественников, которые позднее превращаются в желательные функциональные группы, или для временной блокировки функциональных групп стратегией защитных групп, подходящих для проблемы синтеза. Такие стратегии хорошо известны специалистам в данной области (см., например, Greene and Wuts, Protective Groups in Organic Synthesis, Wiley, 1991, or P. Kocienski, Protecting groups, Thieme 1994). В качестве примеров групп-предшественников, можно упомянуть цианогрупп и нитрогруппы. Цианогруппы могут на более поздней стадии быть превращены в производные карбоновых кислот или восстановлением в аминометильные группы, или нитрогруппы, которые могут быть трансформированы восстановлением, подобным каталитической гидрогенизации в аминогруппы. Защитные группы могут также иметь значение твердой фазы, и расщепление из твердой фазы означает удаление защитной группы. Использование таких методик известно специалистам в данной области (Burgess K (Ewd.) Solid Phase Organic Synthesis, New York; Wiley, 2000). Например, фенольная гидроксигруппа может быть присоединена к тритил-полистирольной смоле, которая служит в качестве защитной группы, и молекула отщепляется от этой смолы обработкой TFA (трифторуксусной кислотой) на более поздней стадии синтеза.
Остаток R54 в соединениях формул 29 и 30 может обозначать группу -Q-R0, как определено выше, которая в конечном счете должна присутствовать в желательной молекуле-мишени формулы I, или он может обозначать группу, которая может быть в последующем трансформирована в группу -Q-R0, например, группу-предшественницу или производное группы -Q-R0, в которой функциональные группы присутствуют в защищенной форме, или R54 может обозначать атом водорода или защитную группу для атома азота азаиндольного кольца. Аналогичным образом, остатки R3a и R30 в формулах 29 и 30 имеют соответствующие определения R3 в формуле I, как определено выше, однако, для синтеза соединений формулы I эти остатки также могут в принципе присутствовать на стадии конденсации соединения формулы 29 с соединением формулы HR8', давая соединение формулы 30 в форме групп-предшественниц или в защищенной форме.
Остатки R53 в соединениях формулы 29, которые могут быть одинаковыми или различными, могут представлять собой, например, гидрокси или (С1-С4)-алкокси, т.е. группы COR53,присутствующие в соединениях формулы 29, могут представлять собой, например, свободные карбоновые кислоты или их сложные эфиры, подобные сложным алкиловым эфирам, какими могут быть группы COR8' в соединениях формулы I. Группы COR53 могут также представлять собой любое другое активированное производное карбоновой кислоты, которое обеспечивает возможность образования амида, образования сложного эфира или образования сложного тиоэфира с соединением формулы HR8'. Группа COR53 может также представлять собой, например, хлорид кислоты, активированный сложный эфир, подобный замещенному сложному фениловому эфиру, азолид, подобный имидазолиду, азид или смешанный ангидрид, например, смешанный ангидрид со сложным эфиром карбоновой кислоты или с сульфоновой кислотой, где все производные можно получить из карбоновой кислоты стандартными процедурами, и они могут взаимодействовать с амином, спиртом или меркаптаном формулы HR8' в стандартных условиях. Группу карбоновой кислоты СООН, представляющая COR53, в соединении 29, можно получить, например, из группы сложного эфира, введенной в азаиндольную систему во время синтеза азаиндола, стандартными процедурами гидролиза.
Соединения формулы I, в которых группа COR8 представляет собой группу сложного эфира, можно также получить из соединений формулы 29, в которых COR53 представляет собой группу карбоновой кислоты, обычными реакциями этерификации, подобными, например, взаимодействию кислоты со спиртом в условиях кислотного катализа, или алкилированию соли карбоновой кислоты с электрофилом, подобным алкилгалогениду, или трансэтерификацией из другого сложного эфира. Соединения формулы I, в которой группа COR8 представляет собой амидную группу, можно получить из аминов и соединений формулы 29, в которых COR53 представляет собой группу карбоновой кислоты или ее сложный эфир, обычными реакциями аминирования. В частности, для получения амидов соединения формулы 29, в которых COR53 представляет собой группу карбоновой кислоты, могут быть конденсированы в стандартных условиях с соединениями формулы HR8', которые представляют собой амины, посредством обычных реагентов соединения, используемых в пептидном синтезе. Такие реагенты соединения представляют собой, например, карбодиимиды, подобные дициклогексилкарбодиимиду (DCC) или диизопропилкарбодиимиду, карбонилдиазолы, подобные карбонилдиимидазолу (CDI) и аналогичным реагентам, пропилфосфоновый ангидрид, тетрафторборат О-((циано(этоксикарбонил)метилен)амино)-N,N,N',N'-тетраметилурония (TOTU), диэтилфосфорилцианид (DEPC) или хлорид бис-(2-оксо-3-оксазолидинил)фосфорила (BOP-Cl) и многие другие.
Если остаток -Q-R0, присутствующий в азаиндоле формулы I, или остаток R54, присутствующий в азаиндоле формулы 29, или остаток, в котором функциональные группы внутри остатка -Q-R0 или R54, присутствуют в защищенной форме или в форме группы-предшественницы, уже не были введены во время предыдущей стадии, например, во время синтеза азаиндольного ядра, то эти остатки могут, например, быть введены в положение 1 азаиндольной системы обычными описанными в литературе процедурами, хорошо известными специалисту в области N-алкилирования, восстановительного аминирования, N-арилирования, N-ацилирования или N-сульфонилирования, кольцевых атомов азота гетероциклов. Исходное азаиндольное производное, которое следует использовать в такой реакции, несет атом водорода в положении 1. N-алкилирование кольцевого атома азота можно, например, выполнить в стандартных условиях, предпочтительно, в присутствии основания, используя алкилирующее соединение формулы LG-Q-R0 или формулы R54-LG, где атом в группе Q или в группе R54, связанной с группой LG, в этом случае представляет собой алифатический атом углерода алкильной части, а LG представляет собой уходящую группу, например, галоген, подобный хлору, брому или иоду, или сульфонилоксигруппу, подобную тозилокси, мезилокси или трифторметилсульфонилокси. LG может, например, также представлять собой гидроксигруппу, которая для достижения реакции алкилирования активируется обычным активирующим агентом. Для получения соединений, в которых А представляет собой прямую связь, и ароматическая группа прямо связана с положением 1 азаиндольной системы, могут использоваться обычные процедуры арилирования. Например, арилфториды, подобные фторбензоатам алкила и метилсульфонам 4-фторфенила, можно использовать в качестве арилирующих агентов. Такие процессы описаны, например, S. Stabler, Jahangir, Synth. Commun. 24 (1994) 123; I. Khanna, R. Weier, Y. Yu, X. Xu. F. Koszyk, J. Med. Chem. 40 (1997) 1634. Альтернативно, широкое разнообразие замещенных арилиодидов, арилбромидов или арилтрифлатов могут служить в качестве арилирующих агентов в положении 1 азаиндольной системы при реакции, опосредованной солью меди или палладием в соответствии с R. Sarges, H. Howard, K. Koe, A. Weissmann, J. Med. Chem, 32 (1989) 437; P. Unangst, D. Connor, R. Stabler, R. Weikert, J. Heterocycl. Chem, 24 (1987) 811; G. Tokmakov, I. Grandberg, Tetrahedron 51 (1995) 2091; D. Old, M. Harris, S. Buchwald, Org. Lett. 2 (2000) 1403, G. Mann, J. Hartwig, M. Driver, C. Fernandez-Rivas, J. Am. Chem. Soc. 120 (1998) 827; J. Hartwig, M. Kawatsura, S. Hauk, K. Shaughnessy, L J. Org. Chem. 64 (1999) 5575. Более того, такие реакции арилирования могут осуществляться взаимодействием широкого диапазона замещенных арилбороновых кислот, как продемонстрировано, например, W. Mederski, M. Lefort, M. Germann, D. Kux, Tetrahedron 55 (1999) 12757.
В ходе синтеза во многих случаях может быть благоприятным или даже требоваться использование микроволнового содействия для ускорения, облегчения или обеспечения возможности взаимодействий. Некоторые реакции, например, описаны J.L Krstenansky, I. Cotteril, Curr: Opin. Drug. Disc. & Development, 4(2000), 454; P. Lidstrom, J. Tierney, B. Wathey, J. Westman, Tetrahedron, 57(2001), 9225; M. Larhed, A. Hallberg, Drug Discovery Today, 8 (2001) 406; S. Caddick, Tetrahedron, 51 (1995) 10403.
Предпочтительные способы включают, но не ограничиваются ими, способы, описанные в примерах. Соединения настоящего изобретения представляют собой ингибиторы серин-протеазы, которые ингибируют активность ферментных факторов свертывания крови - фактора Ха и/или фактора VII. В частности, они представляют собой высокоактивные ингибиторы фактора Ха. Они представляют собой специфические ингибиторы серин-протеазы, пока они существенно не ингибируют активность других протеаз, ингибирование которых нежелательно. Активность соединений формулы I можно определить, например, в анализах, описанных ниже, или в других анализах, известных специалистам в данной области. В отношении ингибирования фактора Ха, предпочтительный вариант осуществления изобретения включает соединения, которые имеют Ki<1 мМ для ингибирования фактора Ха, по данным определения в описанном ниже анализе с сопутствующим ингибированием фактора VIIa или без ингибирования, и которые предпочтительно по существу не ингибируют активность других протеаз, участвующих в свертывании и фибринолизе, ингибирование которых нежелательно (с использованием такой же концентрации ингибитора). Соединения изобретения ингибируют каталитическую активность фактора Ха или прямо, в пределах комплекса протромбиназы, или в виде растворимой субъединицы, или косвенно ингибированием сборки фактора Ха в комплекс протромбиназы.
В качестве ингибиторов фактора Ха и/или фактора VIIa, соединения формулы I и их физиологически приемлемые соли и их пролекарства в целом подходят для лечения и профилактики состояний, при которых активность фактора Ха и/или фактора VIIa играет роль или имеет нежелательную степень, или на которые может оказывать благоприятное влияние ингибирование фактора Ха и/или фактора VIIa или снижение их активности, или для предотвращения, облегчения или излечения которых врач желает ингибировать фактор Ха и/или фактор VIIa или снизить их активность. Поскольку ингибирование фактора Ха и/или фактора VIIa влияет на свертывание крови и фибринолиз, соединения формулы I и их физиологически приемлемые соли и их пролекарства в целом подходят для снижения свертывания крови, или для лечения и профилактики состояний, при которых активность фактора Ха и/или фактора VIIa играет роль или имеет нежелательную степень, или на которые может оказывать благоприятное влияние снижение свертываемости крови, или для предотвращения, облегчения или излечения которых врач желает снизить активность системы свертывания крови. Таким образом, специфическим предметом настоящего изобретения являются снижение или ингибирование нежелательного свертывания крови, в частности у индивидуума, введением эффективного количества соединения формулы I или его физиологически приемлемой соли или пролекарства, а также его фармацевтических препаратов.
Настоящее изобретение также относится к соединениям формулы I и их физиологически приемлемым солям и/или к их пролекарствам для применения в качестве фармацевтических средств (или лекарственных средств), к применению соединений формулы I и их физиологически приемлемых солей и/или их пролекарств для производства фармацевтических средств для ингибирования фактора Ха и/или фактора VIIa или для воздействия на свертывание крови, воспалительную реакцию или фибринолиз или для лечения или профилактики указанных выше или ниже заболеваний, например, для производства фармацевтических средств для лечения и профилактики сердечно-сосудистых расстройств, тромбоэмболических заболеваний или рестенозов. Изобретение также относится к применению соединений формулы I и их физиологически приемлемых солей и/или их пролекарств для ингибирования фактора Ха и/или фактора VIIa или для воздействия на свертывание крови или фибринолиз или для лечения или профилактики указанных выше или ниже заболеваний, например, для применения при лечении и профилактике сердечно-сосудистых расстройств, тромбоэмболических заболеваний или рестенозов и к способам лечения, направленным на такие цели, включая способы указанных видов лечения и профилактики. Настоящее изобретение также относится к фармацевтическим препаратам (или фармацевтическим композициям), которые содержат эффективное количество, по меньшей мере, одного соединения формулы I и его физиологически приемлемых солей и/или его пролекарств в дополнение к обычному фармацевтически приемлемого носителя, т.е. одного или нескольких фармацевтически приемлемых веществ-носителей или эксципиентов и/или вспомогательных веществ или добавок.
Изобретение также относится к лечению патологических состояний, таких как аномальное формирование тромба, острый инфаркт миокарда, нестабильная стенокардия, тромбоэмболия, острая окклюзия сосудов, связанная с тромболитической терапией или чрескожной транслюминальной коронарной ангиопластикой (РТСА), транзиторные ишемические приступы, инсульт, перемежающаяся хромота или аорто-коронарное шунтирование коронарных или периферических артерий, сужение просвета сосудов, рестеноз после коронарной или венозной ангиопластики, поддержание проходимости сосудистого доступа у пациентов, получающих длительный гемодиализ, патологическое образование тромба, происходящее в венах нижних конечностей, после операций на брюшной полости, коленном или тазобедренном суставе, риск тромбоэмболии легочной артерии или диссеминированная системная внутрисосудистая коагулопатия, возникающая в сосудистой системе, во время септического шока, определенных вирусных инфекциях или раке. Соединения настоящего изобретения можно также применять для снижения воспалительной реакции. Примерами конкретных расстройств, для лечения или профилактики которых можно применять соединения формулы I, являются коронарная болезнь сердца, инфаркт миокарда, стенокардия, сосудистый рестеноз, например, рестеноз после ангиопластики, подобной РТСА, респираторный дистресс-синдром взрослых, многоорганная недостаточность и расстройство в виде диссеминированного внутрисосудистого свертывания. Примерами относящихся к проблеме осложнений, связанных с операциями, являются тромбозы, подобные тромбозу глубоких вен и проксимальных вен, который может возникнуть после операции.
Соединения формулы I и их физиологически приемлемые соли и их пролекарства можно вводить животным, предпочтительно, млекопитающим, и, в частности, людям в виде фармацевтических средств для лечения или профилактики. Их можно вводить отдельно или в смесях друг с другом или в форме фармацевтических препаратов, которые обеспечивают возможность энтерального или парентерального введения.
Фармацевтические средства можно вводить перорально, например, в форме пилюль, таблеток, лакированных таблеток, покрытых таблеток, гранул, твердых и мягких желатиновых капсул, растворов, сиропов, эмульсий, суспензий или аэрозольных смесей. Однако введение можно проводить ректально, например, в форме суппозиторий, или парентерально, например, внутривенно, внутримышечно или подкожно, в форме растворов для инъекций или растворов для вливаний, микрокапсул, имплантатов или стержней, или чрескожно или место, например, в форме мазей, растворов или настоек, или другими путями, например, в форме аэрозолей или назальных спреев.
Фармацевтические препараты в соответствии с изобретением получают способом, известным самим по себе, и знакомым специалисту в данной области, где фармацевтически приемлемые инертные неорганические и/или органические носители используются в дополнение к соединению (соединениям) формулы I и/или его (их) фармацевтически приемлемым солям и/или его (их) пролекарствам. Для производства пилюль, таблеток, покрытых таблеток и твердых желатиновых капсул можно использовать, например, лактозу, кукурузный крахмал или его производные, тальк, стеариновую кислоту или ее соли и т.д. Носители для мягких желатиновых капсул и суппозиторий представляют собой, например, жиры, воски, полутвердые и жидкие полиолы, естественные или отвержденные масла и т.д. Подходящие носители для производства растворов, например, растворов для инъекций, или эмульсий или сиропов, представляют собой, например, воду, солевой раствор, спирты, глицерин, полиолы, сахарозу, инвертированный сахар, глюкозу, растительные масла и т.д. Подходящие носители для микрокапсул, имплантатов или стержней представляют собой, например, сополимеры гликолевой кислоты и молочной кислоты. Фармацевтические препараты обычно содержат примерно от 0,5% до 90 мас.% соединений формулы I и/или их физиологически приемлемых солей и/или их пролекарств. Количество активного ингредиента формулы I и/или его физиологически приемлемых солей и/или его пролекарств в фармацевтических препаратах обычно составляет от примерно 0,5 мг до примерно 1000 мг, предпочтительно, от примерно 1 мг до примерно 500 мг.
В дополнение к активным ингредиентам формулы I и/или их физиологически приемлемым солям и/или их пролекарствам и к веществам-носителям, фармацевтические препараты могут содержать добавки, такие как, например, наполнители, разрыхлители, связывающие вещества, смазывающие вещества, смачивающие агенты, стабилизаторы, эмульгаторы, консерванты, подслащивающие вещества, красители, ароматизаторы, загустители, разбавители, буферные вещества, растворители, солюбилизаторы, агенты для достижения депо эффекта, соли для изменения осмотического давления, покрывающие агенты или антиоксиданты. Они могут также содержать 2 или более соединений формулы I и/или их физиологически приемлемые соли и/или их пролекарства. В случае, когда фармацевтический препарат содержит 2 или более соединений формулы I, выбор отдельных соединений может быть нацелен на конкретный общий фармакологический профиль фармацевтического препарата. Например, высокоактивное соединение с более короткой продолжительностью действия можно объединить с длительно действующим соединением с более низкой активностью. Гибкость, допускаемая в отношении выбора заместителей соединений формулы I, обеспечивает возможность значительного контроля биологических и физико-химических свойств соединений и, таким образом, обеспечивает возможность выбора таких желательных соединений. Кроме того, в дополнение, по меньшей мере, к одному соединению формулы I и/или его физиологически приемлемой соли и/или его пролекарству, фармацевтические препараты могут также содержать один или несколько других терапевтически или профилактически активных ингредиентов. При использовании соединений формулы I дозу можно менять в широких пределах, и, как обычно делается и известно врачу, ее подбирают для индивидуальных состояний в каждом отдельном случае. Это зависит, например, от конкретного используемого соединения, от природы и тяжести подлежащего лечению заболевания, от вида и схемы введения, или от того, лечится ли острое или хроническое состояние, или от того, проводится ли профилактика. Соответствующую дозировку можно установить, используя клинические подходы, хорошо известные в области медицины. В целом, суточная доза для достижения желательных результатов у взрослого с массой тела примерно 75 кг составляет от 0,01 мг/кг до 100 мг/кг, предпочтительно, от 0,1 мг/кг до 50 мг/кг, в частности, от 0,1 мг/кг до 10 мг/кг, (в каждом случае в мг на 1 кг массы тела). Суточную дозу можно разделить, в частности, в случае введения относительно больших количеств, на несколько, например, 2, 3 или 4 частичных введений. Обычно, в зависимости от индивидуального поведения, может быть необходимо отклониться вверх или вниз от указанной суточной дозы.
Соединение формулы I можно также преимущественно испоьзовать в виде антикоагулянта вне индивидуума. Например, эффективное количество соединения изобретения может контактировать со свежевзятым образцом крови для предотвращения свертывания образца крови. Кроме того, соединение формулы I или его соли можно использовать для диагностических целей, например, при диагностике in vivo, и в качестве вспомогательного средства при биохимических исследованиях. Например, соединение формулы I можно использовать в анализе для идентификации присутствия фактора Ха и/или фактора VIIa или для выделения фактора Ха и/или фактора VIIa по существу в очищенной форме. Соединение изобретения может быть меченым, например, радиоизотопом, и затем меченое соединение, связанное с фактором Ха и/или фактором VIIa, выявляется с использованием обычного способа, применяемого для выявления конкретной метки. Таким образом, соединение формулы I или его соль можно использовать в качестве зонда для выявления локализации количества активности фактора Ха и/или фактора VIIa in vivo, in vitro или ex vivo.
Кроме того, соединения формулы I можно использовать в качестве промежуточных соединений синтеза для получения других соединений, в частности, других фармацевтически активных ингредиентов, которые можно получить из соединений формулы I, например, введением заместителей или модификацией функциональных групп.
В целом, синтетические последовательности для получения соединений, которые можно использовать в настоящем изобретении, представлены в приведенных ниже примерах. И объяснение, и реальная процедура различных аспектов настоящего изобретения описаны в соответствующих местах описания. Следующие примеры предназначены просто для иллюстрации настоящего изобретения, а не для его ограничения ни по объему, ни по сущности. Специалисты в данной области легко поймут, что известные вариации состояний и способов, описанных в примерах, можно использовать для синтеза соединений настоящего изобретения.
Понятно, что изменения, которые существенно не воздействуют на активность различных вариантов осуществления изобретения, включены в раскрытое в настоящем описании изобретение. Таким образом, следующие примеры предназначены для иллюстрации, а не ограничения настоящего изобретения.
ПРИМЕРЫ
Когда на конечной стадии синтеза соединения использовалась кислота, такая как трифторуксусная кислота или уксусная кислота, например, когда трифторуксусная кислота использовалась для удаления группы tBu, или когда соединение очищалось хроматографией с использованием элюентов, которые содержали такую кислоту, в некоторых случаях, в зависимости от процедуры разработки, например, деталей способа лиофилизации, соединение получали частично или полностью в форме соли используемой кислоты, например, в форме соли уксусной кислоты или соли трифторуксусной кислоты или соли хлористоводородной кислоты.
Пример 1
(1-Изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пиррол[2,3-b]пиридин-2-карбоновой кислоты
(i) Сложный метиловый эфир 1Н-пиррол[2,3-b]пиридин-2-карбоновой кислоты
0,495 г (1,64 ммоль) 1-бензолсульфонил-1Н-пиррол[2,3-b]пиридин-2-карбоновой кислоты растворяют в 5 мл метанола и 3 мл 2 н водной гидроокиси натрия. Реакционную смесь перемешивают при 40°С в течение 8 ч. Растворитель удаляют при пониженном давлении. Остаточные летучие вещества удаляют двойным совместным дистиллированием с толуолом. Остаток суспендируют в метанольной хлористоводородной кислоте и перемешивают в течение 16 ч при RT. Растворитель удаляют при пониженном давлении. Остаток растворяют в этилацетате и промывают насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия. Органическую фазу сушат сульфатом натрия, фильтруют и растворитель удаляют при пониженном давлении.
Выход 0,201 г. MC (Cl+): m/e=177 (M+H-).
(ii) 1-[5-(5-Хлортиофен-2-ил)-изоксазол-3-илметил]-1Н-пиррол[2,3-b]пиридин-2-карбоновая кислота
0,195 г (1,1 ммоль) сложного метилового эфира 1Н-пиррол[2,3-b]пиридин-2-карбоновой кислоты растворяют в 4 мл DMF и добавляют 48,7 мг (1,2 ммоль) гидрида натрия (60% в минеральном масле). Реакционную смесь перемешивают при КТ в течение 20 мин, охлаждают до -78°С, затем добавляют 324 мг (1,2 ммоль) 3-бромметил-5-(5-хлортиофен-2-ил)изоксазола [полученного приспособлением процедуры, описанной Ewing, William R.; Becker, Michael R.; Choi-Sledeski, Yong Mi; Pauls, Heinz W.; He, Wei; Condon, Stephen M.; Davis, Roderick S.; Hanney, Barbara A.; Spada, Alfred P.; Burns, Christopher J.; Jiang, John Z.; Li, Aiwen; Myers, Michael R.; Lau, Wan F.; Poli, Gregory B; PCT Int. Appl. (2001) 460 pp. WO 0107436 A2]. Реакционной смеси дают возможность согреться до КТ в течение ночи. Добавляют 0,3 мл 2 н водной гидроокиси натрия и затем реакционную смесь перемешивают при КТ в течение 24 ч. Продукт очищают препаративной ВЭЖХ в обращенной фазе, элюируя градиентом 0-100% ацетонитрила в воде (+0,01% трифторуксусная кислота). После лиофилизации продукт получают в виде твердого вещества.
Выход 280 мг. MC (TOF MC ES+): m/e=359 (M+).
(iii) Сложный трет-бутиловый эфир (1-изопропилпиперидин-4-ил)карбаминовой кислоты
К раствору 5,0 г сложного трет-бутилового эфира пиперидин-4-илкарбаминовой кислоты в 15 мл метанола добавляют 7,34 мл ацетона, 3,14 г Na(CN)BH3 и 0,3 мл уксусной кислоты. После перемешивания в течение 16 ч при КТ растворитель удаляют при пониженном давлении и остаток секционируют между 30 мл воды и 30 мл этилацетата. Органический слой промывают насыщенным раствором Na2CO3, водой и затем сушат над Na2SO4. После фильтрации растворитель удаляют при пониженном давлении для получения белого твердого вещества.
Выход: 4,8 г. MC (ES+): m/e=243.
(iv) 1-Изопропилпиперидин-4-иламин
К 4,8 г сложного трет-бутилового эфира (1-изопропилпиперидин-4-ил)карбаминовой кислоты в 15 мл метанола добавляют 20 мл метанольной хлористоводородной кислоты (8М) и смесь перемешивают в течение 16 ч. Удаление растворителя при пониженном давлении дает белое твердое вещество, которое совместно выпаривают дважды с 20 мл толуола. Продукт получают в виде его гидрохлорида.
Выход: 5,42 г. MC (ES+): m/e=143.
(v)(1-Изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пиррол[2,3-b]пиридин-2-карбоновой кислоты
0,135 г (0,4 ммоль) 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пиррол[2,3-b]пиридин-2-карбоновой кислоты, 0,432 г (3,8 ммоль) NEM и 135 мг (0,4 ммоль) TOTU растворяют в 3 мл DMF и перемешивают при RY в течение 20 мин. 89 мг (0,4 ммоль) дигидрохлорида 1-изопропилпиперидин-4-иламина добавляют к реакционному раствору и перемешивают при КТ в течение 4 ч. Продукт очищают препаративной ВЭЖХ в обращенной фазе, элюируя градиентом 0-100% ацетонитрила в воде (+0,01% трифторуксусная кислота). После лиофилизации получают продукт в виде твердого вещества.
Выход: 156 мг. MC (TOF MC ES+): m/e=484 (M+).
Пример 2
Сложный метиловый эфир 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[2,3-b]пиперидин-5-карбоновой кислоты
(i) Сложный метиловый эфир 6-аминоникотиновой кислоты
К раствору 10 г 6-аминоникотиновой кислоты в 100 мл МеОН добавляют 0,8 мл концентрированной H2SO4 и смесь нагревают до 60°С в течение 12 ч. Затем реакционную смесь концентрируют при пониженном давлении. После добавления 50 мл ледяной воды рН смеси доводят до 8 добавлением K2CO3. Водную фазу экстрагируют этилацетатом (3×100 мл) и объединенные органические слои сушат над MgSO4. Удаление растворителя дает 5,5 г желательного продукта, который подвергают следующей реакции без дальнейшей очистки.
Выход: 5,5 г.
(ii) Сложный метиловый эфир 6-амино-5-иодникотиновой кислоты
К 5 г сложного метилового эфира 6-аминоникотиновой кислоты и 16,2 г тетрафторбората бис(пиридин)иодиния(I) в 250 мл DCM добавляют по каплям 7,6 мл трифторметансульфоновой кислоты при 0°С. Смесь перемешивают в течение 24 ч при RT. Затем добавляют дополнительные 3,2 г тетрафторбората бис(пиридин)иодиния(I) и 1,5 мл трифторметансульфоновой кислоты. После перемешивания в течение 2 ч при КТ реакционную смесь концентрируют при пониженном давлении и затем собирают концентрированным водным раствором Na2SO3, и доводят до рН 8 концентрированным водным аммиаком. Смесь экстрагируют этилацетатом (2×150 мл). Объединенные органические слои промывают солевым раствором и затем сушат над MgSO4. После фильтрации растворитель удаляют при пониженном давлении и остаток совместно дистиллируют со 100 мл толуола.
Выход: 9,6 г.
(iii) Сложный 5-метиловый эфир 1Н-пиррол[2,3-b]пиридин-2,5-дикарбоновой кислоты
Раствор 5,6 г сложного метилового эфира 6-амино-5-иодникотиновой кислоты, 5,3 г 2-оксопропионовой кислоты, 11,1 г NEt3 4,2 г трифенилфосфина и 1,1 г Pd(OAc)2 в 100 мл DMF нагревают в атмосфере аргона до 100°С. Через 10 ч реакционную смесь концентрируют при пониженном давлении и остаток перемешивают с 250 мл воды в течение 1 ч. Осажденный продукт отфильтровывают и промывают водой. Неочищенный продукт подвергают следующей стадии реакции без дальнейшей очистки.
Выход: 10 г.
(iv) Сложный метиловый эфир 2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[2,3-b]пиридин-5-карбоновой кислоты
К раствору 9,5 г сложного 5-метилового эфира 1Н-пиррол[2,3-b]пиридин-2,5-дикарбоновой кислоты в 120 мл DMF и 23,9 мл Net3, добавляют 9,2 г гидрохлорида 1-изопропилпиперидин-4-иламина и 11 г BOP-Cl при КТ и смесь перемешивают в течение 3 ч. После добавления 20 мл воды реакционную смесь экстрагируют этилацетатом (3×150 мл). Объединенные органические слои промывают солевым раствором (1×50 мл) и сушат над MgSO4. После фильтрации растворитель удаляют при пониженном давлении и остаток очищают хроматографией на силикагеле, элюируя EtOAc/MeOH 9:7→EtOAc/MeOH/NH3 (водн.) 6:4:0,4. Фракции, содержащие продукт, выпаривают и совместно дистиллируют с толуолом.
Выход 7,2 г.
(v) Сложный метиловый эфир 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиридин-4-илкарбамоил)-1Н-пиррол[2,3-b]пиридин-5-карбоновой кислоты
К раствору 1,2 г сложного метилового эфира 2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[2,3-b]пиридин-5-карбоновой кислоты в 20 мл DMF добавляют 91 мг гидрида натрия (95%) при 0°С. Затем реакционную смесь согревают до КТ и перемешивают в течение 30 мин. После охлаждения снова до 0°С добавляют 967 мг 3-бромметил-5-(5-хлортиофен-2-ил)изоксазола [полученный приспособлением процедуры, описанной Ewing, William R.; Becker, Michael R.; Choi-Sledeski, Yong Mi; Pauls, Heinz W.; He, Wei; Condon, Stephen M.; Davis, Roderick S.; Hanney, Barbara A.; Spada, Alfred P.; Burns, Christopher J.; Jiang, John Z.; Li, Aiwen; Myers, Michael R.; Lau, Wan F.; Poli, Gregory B; PQ Int. Appl. (2001), 460 pp. WO 0107436 A2] и смесь перемешивают в течение 2 ч при RT. Затем добавляют 50 мл воды и осадок отфильтровывают для получения 630 мг чистого продукта. Фильтрат концентрируют при пониженном давлении и остаток очищают препаративной ВЭЖХ в обращенной фазе, элюируя градиентом 0-100% ацетонитрила в воде (+0,01% трифторуксусной кислоты). После лиофилизации получают еще 371 мг продукта в виде твердого вещества.
Выход: 1,0 г. MC (ES+): m/e=542, хлор-тип.
Пример 3
1-[5-(5-Хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[2,3-b]пиридин-5-карбоновая кислота
К раствору 630 мг сложного метилового эфира 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[2,3-b]пиридин-5-карбоновой кислоты в 60 мл МеОН добавляют 8,7 мл 1М водного раствора NaOH. Реакционную смесь нагревают до 60°С в течение 3 ч. После охлаждения до КТ добавляют 8,8 мл 1М водной HCl и растворители удаляют при пониженном давлении. Остаток перемешивают с водой/MeCN 2:1 и осажденный продукт отфильтровывают.
Выход: 276 мг. MC (ES+): m/e=528, хлор-тип.
Пример 4
2-[(1-Изопропилпиперидин-4-ил)амид] 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пиррол[2,3-b]пиридин-2,5-дикарбоновой кислоты
К раствору 100 мг 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[2,3-b]пиридин-5-карбоновой кислоты в 1 мл DMF добавляют 62 мг TOTU, 0,2 мл DIPEA и 10 мг NH4Cl при КТ и перемешивают в течение 16 ч. Затем растворитель удаляют при пониженном давлении и неочищенный материал очищают препаративной ВЭЖХ (колонка С18 обращенной фазы, элюирование градиентом H2O/MeCN 0,1% TFA). Фракции, содержащие продукт, выпаривают и лиофилизируют для получения белого твердого вещества. Продукт получают в виде его трифторуксусной соли.
Выход: 16 мг. MC (ES+): m/e=527, хлор-тип.
Пример 5
(1-Изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты
(i) 1Н-Пиррол[3,2-b]пиридин-2-карбоновая кислота
1,22 мл 2-оксопропионовой кислоты, 0,26 г ацетата палладия и 3,20 мл триэтиламина добавляют к раствору 1,00 г 2-бромпиридин-3-иламина и 1,21 г трифенилфосфина в 10 мл N,N-диметилформамида. Реакционную смесь перемешивают в течение 4 ч при 100°С. После удаления растворителя при пониженном давлении остаток очищают колоночной хроматографией на силикагеле дихлорметаном/метанолом в качестве элюента.
Выход: 260 мг. MC (ES+): m/e=163.
1H-ЯМР (400 МГц, ДМСО/TMS): δ = 13,30 (с, 1H); 12,00 (с, 1H); 8,45 (д, 1H); 7,82 (д, 1H); 7,25 (дд, 1H); 7,14(с, 1H).
(ii) Сложный метиловый эфир 1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты
Раствор 130 мг 1Н-пиррол[2,3-b]пиридин-2-карбоновой кислоты в 5 мл 8 н раствора хлористоводородной кислоты в метаноле перемешивают при 60°С в течение 6 ч. Удаление растворителя при пониженном давлении дает белое твердое вещество, которое совместно выпаривают дважды с 5 мл толуола. Продукт получают в виде его гидрохлорида.
Выход: 150 мг. MC (ES+): m/e=177.
1H-ЯМР (400 МГц, ДМСО/TMS): δ = 13,60 (с, 1H); 8,86 (д, 1H); 8,59 (д, 1H); 7,82 (дд, 1H); 7,41 (с, 1H); 3,99 (с, 3H).
(iii) Сложный метиловый эфир 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты
К раствору 150 мг сложного метилового эфира 1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты в 2 мл N,N-диметилформамида добавляют 20,4 мг гидрида натрия (95%) при 0°С. После перемешивания при 0°С в течение 10 мин добавляют 261 мг 3-бромэтил-5-(5-хлортиофен-2-ил)изоксазола. Реакционной смеси дают возможность согреться до комнатной температуры и перемешивают в течение 2 ч. После удаления растворителя при пониженном давлении остаток очищают хроматографией на силикагеле, элюируя градиентом дихлорметана/метанола.
Выход: 80 мг. MC (ES+): m/e=374, хлор-тип.
1H-ЯМР (400 МГц, ДМСО/TMS): δ = 8,54 (д, 1H); 8,13 (д, 1H); 7,58 (д, 1H); 7,43 (с, 1H); 7,39 (дд, 1H); 7,26 (д, 1H); 7,73 (с, 1H); 5,98 (с, 2H); 3,90 (с, 3H),
(iv) 1-[5-(5-Хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пиррол[3,2-b]пиридин-2-карбоновая кислота
Раствор 75 мг сложного метилового эфира 1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты и 9,6 мг гидроокиси лития в смеси 3 мл тетрагидрофурана и 1 мл воды перемешивают в течение 2 ч при комнатной температуре. После подкисления 6 н хлористоводородной кислотой до рН 2 растворитель смеси удаляют при пониженном давлении. Полученный остаток очищают хроматографией на силикагеле, элюируя градиентом этилацетата/метанола с 0,1% водой.
Выход: 50 мг. MC (ES+): m/e=360, хлор-тип.
1H-ЯМР (400 МГц, ДМСО/TMS): δ = 8,45 (д, 1H); 7,84 (д, 1H); 7,53 (д, 1H); 7,22 (д, 1H); 7,15 (дд, 1H); 6,94 (с, 1H); 6,60 (с, 1H); 6,14 (с, 2H).
(v) (1-Изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты
К суспензии 50 мг 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты добавляют 36 мг гидрохлорида 1-изопропилпиперидин-4-иламина и 35 мг бис(2-оксо-3-оксазолидинил)фосфонового хлорида в 1 мл дихлорметане, 77 мкл триэтиламина при комнатной температуре и смесь перемешивают в течение 16 ч. После удаления растворителя при пониженном давлении остаток очищают препаративной ВЭЖХ (колонка С18 обращенной фазы, элюирование градиентом воды/ацетонитрила с 0,1% трифторуксусной кислоты). Фракции, содержащие продукт, выпаривают и лиофилизируют для получения белого остатка, который секционируют между 5 мл водного 0,1 н раствора гидроокиси натрия и 5 мл этилацетата. Органический слой промывают дополнительной водой и затем сушат над сульфатом натрия. После фильтрации и удаления растворителя при пониженном давлении получают белое твердое вещество.
Выход: 10 мг. MC (ES+): m/e=484, хлор-тип.
1H-ЯМР (500 МГц, ДМСО/TMS): δ = 8,53 (д, 1H); 8,46 (д, 1H); 8,03 (д, 1H); 7,57 (д, 1H); 7,32 (с, 1H); 7,28 (дд, 1H); 7,26 (д, 1H); 6,65 (с, 1H); 5,93 (с, 2H); 3,75 (м, 1H); 2,80 (м, 2H); 2,70 (м, 1H); 2,17 (м, 2H); 1,80 (м, 2H); 1,53 (м, 2H); 0,96 (д, 6H).
Пример 6
1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[3,2-b]пиридин-5-карбоновая кислота
(i) Сложный метиловый эфир 5-амино-6-бромпиридин-2-карбоновой кислоты
К раствору 5,00 г сложного метилового эфира 5-аминопиридин-2-карбоновой кислоты в 75 мл 48% водного раствора бромистоводородной кислоты добавляют 3,39 мл 32% водного раствора перекиси водорода. Смесь перемешивают при комнатной температуре в течение 2 ч, затем добавляют дополнительные 0,80 мл раствора перекиси водорода. После перемешивания в течение 1 ч реакционную смесь охлаждают и ее рН доводят до 8 добавлением концентрированного водного аммиака. Смесь экстрагируют 300 мл этилацетата. Водный слой промывают дополнительным этилацетатом и затем объединенные органические фазы сушат над сульфатом натрия. После фильтрации растворитель удаляют при пониженном давлении, и остаток очищают хроматографией на силикагеле, элюируя градиентом н-гептана/этилацетата.
Выход: 2,83 г. MC (ES+): m/e=231.
1H-ЯМР (400 МГц, ДМСО/TMS): δ = 7,80 (д, 1H); 7,10 (д, 1H); 6,37 (с, 2H); 3,80 (с, 3H).
(ii) Сложный 5-метиловый эфир 1Н-пиррол[3,2-b]пиридин-2,5-дикарбоновой кислоты
Следующее соединение получают по аналогии с примером 5 с использованием сложного метилового эфира 5-амино-6-бромпиридин-2-карбоновой кислоты вместо 2-бромпиридин-3-иламина.
MC (ES+): m/e=221.
1H-ЯМР (400 МГц, ДМСО/TMS): δ = 11,80 (с, 1H); 7,89 (д, 1H); 7,84 (д, 1H); 6,93 (с, 1H); 3,88 (с, 3H).
(iii) Сложный метиловый эфир 2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[3,2-b]пиридин-5-карбоновой кислоты
К раствору 140 мг сложного 5-метилового эфира 1Н-пиррол[3,2-b]пиридин-2,5-дикарбоновой кислоты в 1,4 мл N,N-диметилформамида и 0,35 мл триэтиламина добавляют 164 мг гидрохлорида 1-изопропилпиперидин-4-иламина и 161 мг бис(2-оксо-3-оксазолидинил)фосфонового хлорида при комнатной температуре и смесь перемешивают в течение 1 ч. После удаления растворителя при пониженном давлении остаток очищают препаративной ВЭЖХ (колонка С18 обращенной фазы, элюирование градиентом воды/ацетонитрила с 0,1% трифторуксусной кислотой). Фракции, содержащие продукт, выпаривают и лиофилизируют для получения белого твердого вещества. Продукт получают в виде трифторуксусной соли.
Выход: 112 мг. MC (ES+): m/e=345.
1H-ЯМР (400 МГц, ДМСО/TMS): δ = 12,20 (с, 1H); 9,10 (с, 1H); 8,79 (д, 1H); 7,93 (м, 2H); 7,42 (с, 1H); 4,14 (м, 1H); 3,90 (с, 3H); 3,47 (м, 3H); 3,15 (м, 2H); 2,15 (м, 2H); 1,88 (м, 2H); 1,28 (д, 6H).
(iv) Сложный метиловый эфир 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[3,2-b]пиридин-5-карбоновой кислоты
К раствору 60 мг сложного метилового эфира 2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[3,2-b]пиридин-5-карбоновой кислоты в 2 мл N,N-диметилформамида добавляют 4 мг гидрида натрия (95%) при 0°С. После перемешивания при 0°С в течение 10 мин добавляют 53 мг 3-бромметил-5-(5-хлортиофен-2-ил)изоксазола и смесь перемешивают в течение 2 ч при комнатной температуре. После удаления растворителя при пониженном давлении остаток очищают препаративной ВЭЖХ (колонка С18 обращенной фазы, элюирование градиентом воды/ацетонитрила с 0,1% трифторуксусной кислотой). Фракции, содержащие продукт, выпаривают и лиофилизируют для получения белого твердого вещества. Продукт получают в виде трифторуксусной соли.
Выход: 50 мг. MC (ES+): m/e=542, хлор-тип.
1H-ЯМР (400 МГц, ДМСО/TMS): δ = 8,93 (м, 2H); 8,25 (д, 1H); 8,04 (д, 1H); 7,55 (д, 1H); 7,42 (с, 1H); 7,28 (д, 1H); 6,69 (с, 1H); 5,97 (с, 2H); 4,07 (м, 1H); 3,91 (с, 3H); 3,45 (м, 2H); 3,10 (м, 2H); 2,10 (м, 3H); 1,83 (м, 2H); 1,25 (м, 6H).
(v) 1-[5-(5-Хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[3,2-b]пиридин-5-карбоновая кислота
К раствору 50 мг сложного метилового эфира 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[3,2-b]пиридин-5-карбоновой кислоты в 2 мл ТГФ и 1 мл воды добавляют 3,6 мг гидроокиси лития и смесь перемешивают при комнатной температуре в течение 2 ч. Затем реакционную смесь подкисляют 6 н хлористоводородной кислотой до рН 3 и растворитель удаляют при пониженном давлении. Полученный остаток очищают препаративной ВЭЖХ (колонка С18 обращенной фазы, элюирование градиентом воды/ацетонитрила с 0,1% трифторуксусной кислотой). Фракции, содержащие продукт, выпаривают и лиофилизируют для получения белого твердого вещества. Продукт получают в виде трифторуксусной соли.
Выход: 25 мг. MC (ES+): m/e=528, хлор-тип.
1H-ЯМР (500 МГц, ДМСО/TMS): δ = 13,00 (с, 1H); 8,90 (м, 2H); 8,23 (д, 1H); 8,03 (д, 1H); 7,56 (д, 1H); 7,42 (с, 1H); 7,28 (д, 1H); 6,69 (с, 1H); 5,98 (с, 2H); 4,07 (м, 1H); 3,45 (м, 2H); 3,10 (м, 2H); 2,10 (м, 3H); 1,83 (м, 2H); 1,25 (д, 6H).
Пример 7
(1-Изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-оксо-4,5-дигидро-1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты
(i) Сложный метиловый эфир 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-4-окси-1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты
К раствору 80 мг сложного метилового эфира 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты в 1 мл дихлорметана добавляют раствор 52,8 мг 3-хлорпероксибензойной кислоты (70%, влажная с водой) в 1 мл дихлорметана при 0°С. После перемешивания при 0°С в течение 1 ч реакционной смеси дают возможность согреться до комнатной температуры и перемешивают в течение 16 ч. Раствор промывают водным 0,1 н раствором гидроокиси натрия. Органический слой промывают дополнительной водой и затем сушат над безводным сульфатом натрия. После концентрации при пониженном давлении остаток непосредственно подвергают последующему взаимодействию без дальнейшей очистки.
Выход: 100 мг. MC (ES+): m/e=390, хлор-тип.
(ii) Сложный метиловый эфир 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-оксо-4,5-дигидро-1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты
Раствор 100 мг сложного метилового эфира 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-4-окси-1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты в 5 мл уксусного ангидрида нагревают в течение 4 ч при 100°С. После охлаждения до комнатной температуры растворитель смеси удаляют при пониженном давлении. После совместного выпаривания дважды с 5 мл толуола остаток растворяют в 5 мл метанола и добавляют 17,6 мг карбоната калия. Суспензию перемешивают в течение 16 ч при комнатной температуре. После концентрации при пониженном давлении остаток очищают препаративной ВЭЖХ (колонка С18 обращенной фазы, элюирование градиентом воды/ацетонитрила с 0,1% трифторуксусной кислотой). Продукт получают в виде трифторуксусной соли.
Выход: 20 мг. MC (ES+): m/e=390, хлор-тип.
1H-ЯМР (400 МГц, ДМСО/TMS): δ = 11,65 (с, 1H), 7,90 (д, 1H); 7,60 (д, 1H); 7,28 (д, 1H); 6,71 (с, 1H); 6,67 (с, 1H); 6,35 (д, 1H); 5,87 (с, 2H); 3,81 (с, 3H).
(iii) 1-[5-(5-Хлортиофен-2-ил)изоксазол-3-илметил]-5-оксо-4,5-дигидро-1Н-пиррол[3,2-b]пиридин-2-карбоновая кислота
Раствор 20 мг сложного метилового эфира 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-оксо-4,5-дигидро-1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты и 1,9 мг гидроокиси лития в смеси 2 мл тетрагидрофурана и 1 мл воды перемешивают в течение 2 ч при комнатной температуре. Растворитель удаляют при пониженном давлении и остаток совместно выпаривают дважды с толуолом. Остаток непосредственно подвергают последующему взаимодействию без дальнейшей очистки.
Выход: 20 мг. MC (ES+): m/e=376, хлор-тип.
(iv) (1-Изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-оксо-4,5-дигидро-1Н-пиррол[3,2-b]пиридин-2-карбоновой кислоты
К суспензии 19,9 мг 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-оксо-4,5-дигидро-1Н-5-пиррол[3,2-b]пиридин-2-карбоновой кислоты и 13,5 мг бис(2-оксо-3-оксазолидинил)фосфинового хлорида в 1 мл дихлорметана добавляют 7,4 мкл триэтиламина при комнатной температуре и смесь перемешивают в течение 2 ч. Реакционную смесь обрабатывают 5 мл водного 0,1 н раствора гидроокиси натрия и промывают ацетилацетатом. Органический слой сушат над безводным сульфатом натрия. После фильтрации и удаления растворителя при пониженном давлении остаток растворяют в смеси 2 мл ацетонитрила и 1 мл воды. Лиофилизация раствора дает белое твердое вещество.
Выход: 8 мг. MC (ES+): m/e=500, хлор-тип.
1H-ЯМР (500 МГц, ДМСО/TMS): δ = 11,70 (с, 1H); 8,36 (д, 1H); 7,83 (д, 1H); 7,59 (д, 1H); 7,28 (д, 1H); 6,76 (с, 1H); 6,63 (с, 1H); 6,22 (д, 1H); 5,85 (с, 2H); 3,68 (с, 1H); 2,78 (м, 2H); 2,68 (м, 1H); 2,14 (м, 2H); 1,75 (м, 2H); 1,51 (м, 2H); 0,98 (д, 6H).
Пример 8
Сложный метиловый эфир 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(3,4,5,6-тетрагидро-2Н-[1,4']бипиридил-4-илкарбамоил)-1Н-пиррол[3,2-b]пиридин-5-карбоновой кислоты
(i) Сложный метиловый эфир 2-(3,4,5,6-тетрагидро-2Н-[1,4']бипиридил-4-илкарбамоил)-1Н-пиррол[3,2-b]пиридин-5-карбоновой кислоты
К раствору 450 мг сложного 5-метилового эфира 1Н-пиррол[3,2-b]пиридин-2,5-дикарбоновой кислоты в 9 мл дихлорметана и 1,13 мл триэтиламина добавляют 614 мг дигидрохлорида 3,4,5,6-тетрагидро-2Н-[1,4']бипиридил-4-иламина и 520 мг бис(2-оксо-3-оксазолидинил)фосфонового хлорида при комнатной температуре и смесь перемешивают в течение 2 ч. После обработки реакционной смеси 5 мл насыщенного водного раствора карбоната калия осадок отфильтровывают и совместно выпаривают дважды с толуолом. Осадок непосредственно повергают последующей реакции без дальнейшей очистки.
Выход: 300 мг. MC (ES+): m/e=380.
1H-ЯМР (400 МГц, ДМСО/TMS): δ = 8,30 (м, 1H); 8,15 (д, 2H); 7,68 (д, 2H); 7,04 (с, 1H); 6,85 (д, 2H); 4,10 (м, 1H); 3,95 (м, 2H); 3,84 (с, 3H); 3,00 (м, 2H); 1,91 (м, 2H); 1,53 (м, 2H).
(ii) Сложный метиловый эфир 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(3,4,5,6-тетрагидро-2Н-[1,4']бипиридил-4-илкарбамоил)-1Н-пиррол[3,2-b]пиридин-5-карбоновой кислоты
К раствору 150 мг сложного метилового эфира 2-(3,4,5,6-тетрагидро-2Н-[1,4']бипиридил-4-илкарбамоил)-1Н-пиррол[3,2-b]пиридин-5-карбоновой кислоты добавляют 2 мл N,N-диметилформамида, 9,5 мг гидрида натрия (96%) при 0°С. После перемешивания при 0°С в течение 10 мин добавляют 121 мг 3-бромметил-5-(5-хлортиофен-2-ил)изоксазола и смесь перемешивают в течение 50 ч при комнатной температуре. 2 мл воды добавляют к реакционной смеси и полученный осадок отфильтровывают. Остаток растворяют в 2 мл N,N-диметилформамида и очищают препаративной ВЭЖХ (колонка С18 обращенной фазы, элюирование градиентом воды/ацетонитрила с 0,1% трифторуксусной кислотой). Фракции, содержащие продукт, выпаривают и лиофилизируют для получения белого твердого вещества. Продукт получают в виде трифторуксусной соли.
Выход: 27 мг. MC (ES+): m/e=577, хлор-тип.
Пример 9
1-[5-(5-Хлортиофен-2-ил)изоксазол-3-илметил]-2-(3,4,5,6-тетрагидро-2Н-[1,4']бипиридил-4-илкарбамоил)-1Н-пиррол[3,2-b]пиридин-5-карбоновая кислота
К раствору сложного метилового эфира 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пиррол[3,2-b]пиридин-5-карбоновой кислоты в 0,5 мл тетрагидрофурана и 0,25 мл воды добавляют 2,4 мг гидроокиси лития и смесь перемешивают при комнатной температуре в течение 16 ч. После удаления растворителя при пониженном давлении полученный остаток очищают препаративной ВЭЖХ (колонка С18 обращенной фазы, элюирование градиентом воды/ацетонитрила с 0,1% трифторуксусной кислотой). Фракции, содержащие продукт, выпаривают и лиофилизируют для получения белого твердого вещества. Продукт получают в виде трифторуксусной соли.
Выход: 14,3 мг. MC (ES+): m/e=563, хлор-тип.
1H-ЯМР (500 МГц, ДМСО/TMS): δ = 13,25 (с, 1H); 13,00 (с, 1H); 8,73 (д, 1H); 8,24 (м, 3H); 8,03 (д, 1H); 7,57 (д, 1H); 7,39 (с, 1H); 7,26 (м, 3H); 6,69 (с, 1H); 5,98 (с, 2H); 4,25 (м, 3H); 2,00 (м, 2H); 1,59 (м, 2H).
Пример 10
(1-Изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты
(i) 2-(2-Метоксиэтокси)-4-метил-5-нитропиридин
К 20 мл 2-метоксиэтанола добавляют 243 мг NaH (6,09 ммоль, 60% суспензия в масле) и смесь перемешивают в течение 15 мин в атмосфере аргона. Добавляют 1 г (5,8 ммоль) 2-хлор-4-метил-5-нитропиридина и реакционную смесь перемешивают в течение 3 ч при комнатной температуре. После добавления 40 мл воды и простого метил-трет-бутилового эфира фазы разделяют и органическую фазу промывают насыщенным раствором NaHCO3 и водой и сушат над Na2SO4. После фильтрации растворитель удаляют в вакууме и остаток очищают флэш-хроматографией на силикагеле с использованием гептана/этилацетата=8/2. 2-(2-метоксиэтокси)-4-метил-5-нитропиридин выделяют в виде бесцветного масла.
Выход: 0,73 г.
(ii) Калиевая соль сложного этилового эфира 3-[2-(2-метоксиэтокси)-5-нитропиридин-4-ил]-2-оксопропионовой кислоты
К 265 мг (6,78 ммоль) калия в 20 мл абсолютного простого диэтилового эфира медленно добавляют 2,5 мл этанола. Смесь охлаждают до 0°С и добавляют раствор 720 мг (3,39 ммоль) 2-(2-метоксиэтокси)-4-метил-5-нитропиридина в 2,5 мл абсолютного простого диэтилового эфира и 0,5 мл этанол. По каплям в течение 45 мин добавляют 3,966 г (27,14 ммоль) сложного диэтилового эфира щавелевой кислоты в 15 мл толуола. Реакционную смесь перемешивают при комнатной температуре в течение 4 ч. Осадок фильтруют, промывают простым диэтиловым эфиром/н-гептаном 1/1 и сушат в вакууме. Калиевую соль сложного этилового эфира 1,4 г 3-[2-(2-метоксиэтокси)-5-нитропиридин-4-ил]-2-оксопропионовой кислоты выделяют в виде красного твердого вещества и используют на следующей стадии без дальнейшей очистки.
(iii) Сложный этиловый эфир 5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты
0,8 мл кислотной кислоты добавляют к раствору высушенной калиевой соли сложного этилового эфира 3-[2-(2-метоксиэтокси)-5-нитропиридин-4-ил]-2-оксопропионовой кислоты в 20 мл метанола и раствор гидрогенизируют с использованием 199 мг Pd(OH)2 (20% на активированном угле). Через 3 ч смесь концентрируют и остаток распределяют между насыщенным раствором NaHC3 и этилацетатом. Фазы разделяют и органическую фазу сушат над MgSO4. После фильтрации растворитель удаляют в вакууме и получают желательный продукт в виде бледно-желтого твердого вещества.
Выход: 660 мг.
(iv) Сложный этиловый эфир 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты
105 мг (4,16 ммоль) NaH (96%) добавляют к раствору сложного этилового эфира 5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты в 50 мл абсолютного DMF и смесь перемешивают в течение 30 мин при комнатной температуре. К смеси добавляют 1,05 г (3,78 ммоль) 3-бромметил-5-(5-хлортиофен-2-ил)изоксазола и перемешивание продолжают в течение 3 ч. После добавления 21 мг (0,832 ммоль) NaH (96%) и 210 мг (0,756 ммоль) 3-бромметил-5-(5-хлортиофен-2-ил)изоксазола и стояния в течение ночи смесь концентрируют в вакууме. Остаток растворяют в CH2Cl2 и раствор промывают насыщенным раствором NaHCO3. Растворитель удаляют в вакууме и остаток очищают флэш-хроматографией на силикагеле с использованием н-гептана/этилацетата=3/2 в качестве растворителя. Фракции, содержащие продукт, концентрируют.
Выход 1,3 г.
(v) 1-[5-(5-Хлортиофен-2-ил)изоксазол-3-илметил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновая кислота
К раствору 1,3 г (2,814 ммоль) сложного этилового эфира 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты в 30 мл THF и 15 мл MeOH добавляют 11,26 мл 1М LiOH и смесь перемешивают при 50°С в течение 3 ч. Органические растворители удаляют в вакууме, добавляют 50 мл воды и рН доводят до 2 раствором 1 н HCl. Желательный продукт осаждают и фильтруют. Промывают водой и сушат над P2O5.
Выход 1,11 г.
(vi) (1-Изопропилпиперидин-4-ил)амидгидрохлорид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты
К раствору 1,11 г (2,55 ммоль) 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты и 0,55 г (2,55 ммоль) дигидрохлорида 1-изопропилпиперидин-4-иламина в 20 мл абсолютного DMF добавляют 837 мг (2,55 ммоль) TOTU и 1,34 мл (7,67 ммоль) DIPEA и смесь перемешивают при комнатной температуре в течение 4 ч. Растворитель удаляют в вакууме, остаток растворяют в CH2Cl2 и фазу CH2Cl2 промывают насыщенным раствором NaHCO3. Органическую фазу концентрируют и остаток очищают хроматографией через силикагель с использованием CH2Cl2/MeOH/HOAc/H2O=90/10/1/1 в качестве элюента. Фракции, содержащие продукт, объединяют и концентрируют. Продукт выделяют в виде его гидрохлорида лиофилизиацией с использованием 2,5 эквивалентов 1 н HCl в H2O/AcCN.
Выход 1,2 г. MC (ES+): m/e=558, хлор-тип.
Пример 11
(1-Изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-(2-гидроксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты
К раствору 600 мг (1,01 ммоль) (1-изопропилпиперидин-4-ил)амидгидрохлорида 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты (пример 10 (vi)) в 50 мл CH2Cl2 добавляют 2 мл (2,02 ммоль) 1М раствора BBr3 в CH2Cl2. Смесь перемешивают при комнатной температуре в течение 6 ч. После стояния в течение ночи растворитель удаляют в вакууме и остаток очищают препаративной ВЭЖХ (элюент: CH3CN/H2O/0,1% CF3COOH). Фракции, содержащие продукт, объединяют и концентрируют в вакууме. Остаток растворяют в CH2Cl2 и промывают 0,1 н раствором NaOH. Раствор удаляют в вакууме и остаток лиофилизируют 2,5 эквивалентами 1 н HCl, получая 464 мг (79%) гидрохлорида желательного продукта.
MC (LC-MC-ES+): m/e=544, хлор-тип.
Пример 12
(1-Изопропилпиперидин-4-ил)амид 1-[(5-хлорпиридин-2-илкарбамоил)метил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты
(i) 5-(2-Метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновая кислота
К раствору 1 г (3,784 ммоль) сложного этилового эфира 5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты (пример 10 (iii)) в 50 мл THF и 25 мл MeOH добавляют 15,14 мл 1M LiOH. Смесь перемешивают в течение 2 ч при комнатной температуре. Органические растворители удаляют в вакууме, раствор подкисляют и концентрируют в вакууме. Остаток очищают флэш-хроматографией через силикагель с использованием H2Cl2/MeOH/HOAc/H2O=90/10/1/1 в качестве элюента. Фракции продукта объединяют, концентрируют в вакууме и лиофилизируют.
Выход: 820 мг.
(ii) (1-Изопропилпиперидин-4-ил)амид 5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты
К раствору 820 мг (3,47 ммоль) 5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты и 745 мг (3,47 ммоль) дигидрохлорида 1-изопропилпиперидин-4-иламина в 30 мл абсолютного DMF добавляют 1,13 г (3,47 ммоль) TOTU и 1,81 мл (10,41 ммоль) DIPEA и смесь перемешивают в течение 4 ч при комнатной температуре. Растворитель удаляют в вакууме, остаток растворяют в H2Cl2 и фазу CH2Cl2 промывают насыщенным раствором NaHCO3. Органическую фазу концентрируют и остаток очищают хроматографией через силикагель с использованием CH2Cl2/MeOH/HOAc/H2O=90/10/1/1 в качестве элюента. Фракции, содержащие продукт, объединяют и концентрируют. Остаток растворяют в H2Cl2 и фазу CH2Cl2 промывают насыщенным раствором NaHCO3. Фазы разделяют и органическую фазу сушат над Na2SO4. После фильтрации растворитель удаляют в вакууме. Выход 461 мг.
(iii) 2-Бром-N-(5-хлорпиридин-2-ил)ацетамид
К раствору 5 г 5-хлорпиридин-2-иламина и 1,5 мл пиридина в 30 мл толуола по каплям добавляют 8 г бромацетилбромида, растворенного в 10 мл толуола в условиях охлаждения льдом. Через 2 ч осадок выделяют фильтрацией и рекристаллизуют из толуола для получения белого твердого вещества.
Выход: 12 г.
(iv) (1-Изопропилпиперидин-4-ил)амид 1-[(5-хлорпиридин-2-илкарбамоил)метил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты
К раствору 461 мг (1,27 ммоль) (1-изопропилпиперидин-4-ил)амида 5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты в 20 мл абсолютного DMF добавляют 46 мг (1,91 ммоль) NaH (96%) в атмосфере аргона. Смесь перемешивают в течение 15 мин при комнатной температуре. Добавляют 479 мг (1,91 ммоль) 2-бром-N-(5-хлорпиридин-2-ил)ацетамида и смесь перемешивают в течение 3 ч при комнатной температуре. Растворитель удаляют в вакууме, остаток растворяют в H2Cl2 и фазу CH2Cl2 промывают Н2О, и сушат над Na2SO4. После фильтрации органическую фазу концентрируют и остаток очищают хроматографией через силикагель с использованием CH2Cl2/MeOH/HOAc/H2O=90/10/1/1 в качестве элюента с последующей препаративной ВЭЖХ (элюент: CH3CN/H2O/0,1% CF3COOH). Фракции, содержащие продукт, объединяют и концентрируют в вакууме. Остаток лиофилизируют 2 эквивалентами 1 н HCl в смеси H2O/CH3CN, давая гидрохлорид желательного продукта.
Выход: 545 мг. MC (LC-MC-ES+): m/e=529, хлор-тип.
Пример 13
(1-Изопропилпиперидин-4-ил)амид 1-[(5-хлорпиридин-2-илкарбамоил)метил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты
Соединение получают, как описано в примере 11. Из 446 мг (0,789 ммоль) (1-изопропилпиперидин-4-ил)амидгидрохлорида 1-[(5-хлорпиридин-2-илкарбамоил)метил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты получают 286 мг желательного продукта.
MC (LC-MC-ES+): m/e=515, хлор-тип.
Пример 14
(1-Изопропилпиперидин-4-ил)амид 1-(6-хлорбензо[b]тиофен-2-илметил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты
(i) Сложный этиловый эфир 1-(6-хлорбензо[b]тиофен-2-илметил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты
К раствору 660 мг (2,497 ммоль) сложного этилового эфира 5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты в 15 мл абсолютного DMF добавляют 24 мг (2,497 ммоль) NaH (96%) в атмосфере аргона. Смесь перемешивают в течение 30 мин при комнатной температуре. 623 мг (2,497 ммоль) 2-бромметил-6-хлорбензо[b]тиофена [полученного приспособлением процедуры, описанной Ewing, William R. et al. in PCT Int. Appl. (1999), 300 pp. WO 9937304 A1; и Ewing, William R. et al. PCT Int. Appl. (2001), 460 pp. WO 0107436 A2] и смесь перемешивают в течение 1 ч при комнатной температуре. Растворитель удаляют в вакууме и остаток очищают препаративной ВЭЖХ (элюент: CH3CN/H2O/0,1% CF3COOH). Фракции, содержащие продукт, объединяют, концентрируют в вакууме и лиофилизируют.
Выход: 900 мг.
(ii) 1-(6-Хлорбензо[b]тиофен-2-илметил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновая кислота
8 мл 1М раствора LiOH добавляют к раствору 890 мг (2 ммоль) сложного этилового эфира 1-(6-хлорбензо[b]тиофен-2-илметил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты в 30 мл THF и 15 мл MeOH, и смесь перемешивают в течение 1 ч при 50°С. Добавляют 16 мл 1 н HCl, органический растворитель удаляют в вакууме, и остаток экстрагируют этилацетатом. Органическую фазу сушат над MgSO4. После фильтрации растворитель выпаривают, получая желательный продукт.
Выход: 810 мг.
(iii) (1-Изопропилпиперидин-4-ил)амид 1-(6-хлорбензо[b]тиофен-2-илметил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты
К раствору 800 мг (1,92 ммоль) 1-(6-хлорбензо[b]тиофен-2-илметил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты и 413 мг (1,92 ммоль) дигидрохлорида 1-изопропилпиперидин-4-иламина в 20 мл абсолютного DMF добавляют 628 мг (1,92 ммоль) TOTU и 1,0 мл (5,757 ммоль) DIPEA, и смесь перемешивают при комнатной температуре в течение 1 ч. Растворитель удаляют в вакууме и остаток очищают препаративной ВЭЖХ (элюент: CH3CN/H2O/0,1% CF3COOH) и хроматографией через силикагель с использованием CH2Cl2/MeOH/HOAc/H2O=85/15/1,5/1,5 в качестве элюента. Фракции, содержащие продукт, объединяют и концентрируют. Выход: 870 мг (69%), соответствующий трифторацетат. 60 мг трифторацетата лиофилизируют с использованием 2,5 эквивалентов 1 н HCl в Н2О и выделяют в виде гидрохлорида.
MC (LC-MS-ES+): m/e=541, хлор-тип.
Пример 15
(1-Изопропилпиперидин-4-ил)амид 1-(6-хлорбензо[b]тиофен-2-илметил]-5-(2-гидроксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты
К раствору 810 мг (1,236 ммоль) (1-изопропилпиперидин-4-ил)амидгидрохлорид 1-(6-хлорбензо[b]тиофен-2-илметил]-5-(2-метоксиэтокси)-1Н-пиррол[2,3-с]пиридин-2-карбоновой кислоты в 80 мл CH2Cl2 добавляют 2,472 мл 1М раствора BBr3 в CH2Cl2. Смесь перемешивают при комнатной температуре в течение 30 мин. Растворитель удаляют в вакууме и лиофилизируют. Остаток очищают препаративной ВЭЖХ (элюент: CH3CN/H2O/0,1% CF3COOH). Фракции, содержащие продукт, объединяют, концентрируют в вакууме и лиофилизируют с 2,5 эквивалентами 1 н HCl, получая гидрохлорид желательного продукта.
Выход: 594 мг. MC (LC-MC-ES+): m/e=527, хлор-тип.
Фармакологическое тестирование
Способность соединений формулы I ингибировать фактор Ха или фактор VIIa или другие ферменты, подобные тромбину, плазмину или трипсину, можно оценить определением концентрации соединения формулы I, которое ингибирует ферментную активность на 50%, т.е. величины IC50, которая была связана с константой ингибирования Ki. Очищенные ферменты используют в хромогенных анализах. Концентрацию ингибитора, которая вызывает уменьшение на 50% скорости гидролиза субстрата, определяют линейной регрессией после нанесения на график относительных скоростей гидролиза (по сравнению с неингибированным контролем) в зависимости от логарифма концентрации соединения формулы I. Для расчета константы ингибирования Ki величину IC50 корригируют на конкуренцию с субстратом, используя формулу
Ki=IC50/{1+(концентрация субстрата/Km)},
где Km представляет собой константу Michaelis-Menten (Chen and Prusoff, Biochem. Pharmacol. 22 (1973), 3099-3108; I. H. Segal, Enzyme Kinetics, 1975, John Wiley & Sons, New York, 100-125; которые включены в настоящее описание в качестве ссылки).
А) Анализ фактора Ха
В анализе для определения ингибирования активности фактора Ха используют буфер TBS-PEG (50 мМ Tris-HCl, рН 7,8, 200 мМ NaCl, 0,05% (мас./об.) PEG-8000, 0,02% (мас./об.) NaN3). IC50 определяют объединением содержимого соответствующих лунок титровочной микропланшеты половинной площади Costar, включающих 25 мкл человеческого фактора Ха (Enzyme Research Laboratories, Inc.; South Bend, Indiana) в TBS-PEG; 40 мкл 10% (об./об.) DMSO в TBS-PEG (ингибированный контроль) или различные концентрации соединения, которое предстоит тестировать, разводят в 10% (об./об.) DMSO в TBS-PEG; и субстрат S-2765 (N(α)-бензилоксикарбонил-D-Arg-Gly-L-Arg-пара-нитроанилид, Kabi Pharmacia, Inc.; Franklin, Ohio) в TBS-PEG.
Анализ выполняют предварительной инкубацией соединения формулы I плюс фермента в течение 10 мин. Затем анализ начинают добавлением субстрата для получения конечного объема 100 мкл. Исходную скорость гидролиза хромогенного субстрата измеряют изменением спектральной поглощательной способности при 405 нм с использованием приборов кинетического считывания планшет (Cerer UV900HDi) при 25°С в течение линейной части течения во времени (обычно через 1,5 мин после добавления субстрата). Концентрация фермента составляет 0,5 нМ, а концентрация субстрата составляет 140 мкМ.
b) Анализ фактора VIIa
Ингибирующую активность в отношении фактора VIIa/тканевого фактора определяют с использованием хромогенного анализа. По существу, как описано ранее (публикация J.A.Ostrem et al., Biochemistry 37 (1998) 1053-1059), которая включена в настоящее описание в качестве ссылки). Кинетические анализы проводят при 25°С в титровочных микропланшетах половинной площади (Costar Corp., Cambridge, Massachusetts), используя с использованием прибора кинетического считывания планшет (Molecular Devices Spectramax 250). Типичный анализ состоит из 25 мкл человеческого фактора VIIa и TF (соответствующая конечная концентрация 5 нМ и 10 нМ) в комбинации с 40 мкл разведений ингибитора в буфере 10% DMSO/TBS-PEG (50 мМ Tris, 15 мМ NaCl, 5 мМ CaCl2, 0,05% PEG 8000, pH 8,15). После 15 мин периода предварительной инкубации анализ начинают добавлением 35 мкл хромогенного субстрата S-2288 (D-Ile-Pro-Arg-пара-нитроанилида, Pharmacia Hepar Inc., конечная концентрация 500 мкл). Результаты (константы ингибирования Ki (FXa) для ингибирования фактора Ха) показаны в таблице.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА Ха | 2004 |
|
RU2346944C2 |
| ИНДОЛ-2-КАРБОКСАМИДЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА Ха И/ИЛИ VIIa, ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2002 |
|
RU2299881C2 |
| ТАРТРАТНЫЕ ПРОИЗВОДНЫЕ ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА СВЕРТЫВАНИЯ КРОВИ IXA | 2007 |
|
RU2446160C2 |
| ИЗОСЕРИНОВЫЕ ПРОИЗВОДНЫЕ ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА СВЕРТЫВАНИЯ КРОВИ IXA | 2007 |
|
RU2446157C2 |
| ПИРАЗОЛОПИРИМИДИНОВЫЕ СОЕДИНЕНИЯ-ИНГИБИТОРЫ JAK И СПОСОБЫ | 2009 |
|
RU2539568C2 |
| ЗАМЕЩЕННЫЕ ИНДОЛЫ | 2000 |
|
RU2255087C2 |
| НОВЫЕ ДИАМИДЫ ПИРИМИДИН-4,6-ДИКАРБОНОВОЙ КИСЛОТЫ ДЛЯ СЕЛЕКТИВНОГО ИНГИБИРОВАНИЯ КОЛЛАГЕНАЗ | 2003 |
|
RU2344129C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСАЗОЛОВ КОНДЕНСАЦИЕЙ АРОМАТИЧЕСКИХ АЛЬДЕГИДОВ С АЛЬФА-КЕТОКСИМАМИ С ОБРАЗОВАНИЕМ N-ОКСИДОВ И ПОСЛЕДУЮЩИМ ВЗАИМОДЕЙСТВИЕМ С АКТИВИРОВАННЫМИ ПРОИЗВОДНЫМИ КИСЛОТ | 2005 |
|
RU2402537C2 |
| МОЧЕВИНА И СУЛЬФАМИДНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ TAFIA | 2007 |
|
RU2459619C2 |
| ЛЕЧЕНИЕ СОСТОЯНИЙ, АССОЦИИРОВАННЫХ С ГИПЕРИНСУЛИНЕМИЕЙ | 2015 |
|
RU2722179C2 |
Изобретение относится к соединениям формулы I и их физиологически приемлемым солям в качестве ингибиторов фактора Ха, к лекарственному средству на их основе, а также к способу их получения и применения. Соединения могут найти применение для воздействия на свертывание крови, воспалительную реакцию или фибринолиз их лечения и профилактики заболеваний, опосредованных фактором Ха, например, сердечно-сосудистых расстройств, тромбоэмболических заболеваний или рестенозов. В общей формуле I
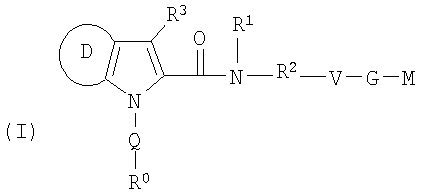
R0 представляет собой моноциклический или бициклический 6-9-членный гетероциклил, выбранный из группы бензотиофенила, пиридила, или моноциклический 5-членный гетероциклил, содержащий 1, 2 гетероатома, выбранных из азота или кислорода, где указанный гетероциклил является монозамещен R8, и который дополнительно замещен моноциклическим 5-членным гетероциклилом, содержащим 1 гетероатом, выбранный из серы, где гетероциклил монозамещен R8, R8 представляет собой галоген, подструктуру  , которая в формуле I представляет собой 6-членную, частично ненасыщенную или ароматическую циклическую группу, содержащую 1 гетероатом, выбранный из азота, и которая замещена 1 группой R23 или оксогруппой, при условии, что указанная циклическая группа не является фенильным остатком, Q представляет собой прямую связь, -(С0-С2)-алкилен-С(O)-NR10-, -(С1-С6)-алкилен, -R1 представляет собой атом водорода, R2 представляет собой прямую связь, V представляет собой 6-членный циклический остаток, содержащий 1 гетероатом, выбранный из азота, где указанный циклический остаток является незамещенным, бициклический 12-членный гетероциклил, содержащий 1-2 гетероатома, выбранных из азота, где указанный гетероциклил является незамещенным, G представляет собой прямую связь, М представляет собой атом водорода, -(С1-С8)-алкил, где алкил является незамещенным, R3 представляет собой атом водорода, R23 представляет собой атом водорода, -(С0-С4)-алкилен -O-R19 (где R19 представляет собой а) атом водорода, b) -(С1-С4)-алкил, где алкил является незамещенным или монозамещенным R13), -(С0-С4)-алкилен-С(O)-R11, -(С0-С4)-алкилен-С(O)-R11, R11 и R12 независимо друг от друга являются одинаковыми или различными и представляют собой атом водорода, -(С1-С6)-алкил, -O-R17 или R13 представляет собой -C(O)-O-R10, R10 и R20 представляют собой, независимо друг от друга, водород, -(С1-С6)-алкил, R17 представляет собой -(С1-С6)-алкил, и его физиологически приемлемые соли. 4 н. и 7 з.п. ф-лы, 1 табл.
, которая в формуле I представляет собой 6-членную, частично ненасыщенную или ароматическую циклическую группу, содержащую 1 гетероатом, выбранный из азота, и которая замещена 1 группой R23 или оксогруппой, при условии, что указанная циклическая группа не является фенильным остатком, Q представляет собой прямую связь, -(С0-С2)-алкилен-С(O)-NR10-, -(С1-С6)-алкилен, -R1 представляет собой атом водорода, R2 представляет собой прямую связь, V представляет собой 6-членный циклический остаток, содержащий 1 гетероатом, выбранный из азота, где указанный циклический остаток является незамещенным, бициклический 12-членный гетероциклил, содержащий 1-2 гетероатома, выбранных из азота, где указанный гетероциклил является незамещенным, G представляет собой прямую связь, М представляет собой атом водорода, -(С1-С8)-алкил, где алкил является незамещенным, R3 представляет собой атом водорода, R23 представляет собой атом водорода, -(С0-С4)-алкилен -O-R19 (где R19 представляет собой а) атом водорода, b) -(С1-С4)-алкил, где алкил является незамещенным или монозамещенным R13), -(С0-С4)-алкилен-С(O)-R11, -(С0-С4)-алкилен-С(O)-R11, R11 и R12 независимо друг от друга являются одинаковыми или различными и представляют собой атом водорода, -(С1-С6)-алкил, -O-R17 или R13 представляет собой -C(O)-O-R10, R10 и R20 представляют собой, независимо друг от друга, водород, -(С1-С6)-алкил, R17 представляет собой -(С1-С6)-алкил, и его физиологически приемлемые соли. 4 н. и 7 з.п. ф-лы, 1 табл.
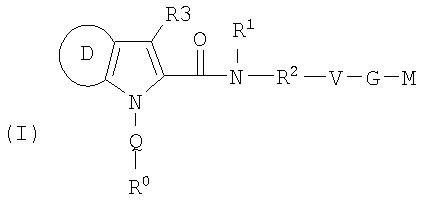
где R0 представляет собой
моноциклический или бициклический 6-9-членный гетероциклил, выбранный из группы бензотиофенила, пиридила, или
моноциклический 5-членный гетероциклил, содержащий 1, 2 гетероатома, выбранных из азота или кислорода, где указанный гетероциклил является монозамещен R8, и который дополнительно замещен моноциклическим 5-членным гетероциклилом, содержащим 1 гетероатом, выбранный из серы,
где гетероциклил монозамещен R8,
R8 представляет собой
галоген,
подструктура
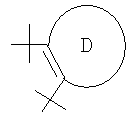
которая в формуле I представляет собой 6-членную, частично ненасыщенную или ароматическую циклическую группу, содержащую 1 гетероатом, выбранный из азота, и которая замещена 1 группой R23 или оксогруппой,
при условии, что указанная циклическая группа не является фенильным остатком,
Q представляет собой прямую связь, -(С0-С2)-алкилен-С(O)-NR10-, -(С1-С6)-алкилен,
R1 представляет собой атом водорода,
R2 представляет собой прямую связь,
V представляет собой
6-членный циклический остаток, содержащий 1 гетероатом, выбранный из азота, где указанный циклический остаток является незамещенным,
бициклический 12-членный гетероциклил, содержащий 1-2 гетероатома, выбранных из азота, где указанный гетероциклил является незамещенным,
G представляет собой прямую связь,
М представляет собой
атом водорода,
-(С1-С8)-алкил, где алкил является незамещенным,
R3 представляет собой
атом водорода,
R23 представляет собой
атом водорода,
-(С0-С4)-алкилен -O-R19, где R19 представляет собой
a) атом водорода,
b) -(С1-С4)-алкил, где алкил является незамещенным или монозамещенным R13,
-(C0-C4)-алкилен-C(O)-R11,
-(С0-С4)-алкилен-С(O)-O-R11,
R11 и R12 независимо друг от друга являются одинаковыми или различными и представляют собой
атом водорода,
-(С1-С6)-алкил,
-O-R17 или
R13 представляет собой -C(O)-O-R10,
R10 и R20 представляют собой, независимо друг от друга, водород, -(С1-С6)-алкил,
R17 представляет собой -(С1-С6)-алкил, и его физиологически приемлемые соли.
где R0 представляет собой
гетероциклил, выбранный из группы бензотиофенила, пиридила, или гетероциклил, где гетероциклил выбран из группы дигидрофтор[2,3-b]тетрагидрофуранила, фуранила, имидазолидинила, имидазолинила, имидазолила, изоксазолила, изоксазолинила, изоксазолидинила, 2-изоксазолинила, оксазолинила, оксазолила, пиразолидинила, пиразолинила, пиразолила, 2Н-пирролила, пирролила, тетрагидрофуранила, где указанный гетероциклил монозамещен R8, и
который дополнительно замещен гетероциклилом, выбранным из группы тиенила, где гетероциклил монозамещен R8,
R8 представляет собой
галоген,
подструктура D представляет собой остаток, выбранный из группы пиридина, замещенный 1 группой R23, или оксогруппой,
Q представляет собой прямую связь, -(С0-С2)-алкилен-С(O)-NR10-, -(С1-С6)-алкилен,
R1 представляет собой атом водорода,
R2 представляет собой прямую связь,
V представляет собой
гетероциклил, выбранный из группы пиперидинила, пиридила, хинолинила, 4Н-хинолизинила, тетрагидроизохинолинила, тетрагидрохинолинила, тетрагидропиридинила, где указанный гетероциклил является незамещенным,
М представляет собой
атом водорода,
-(С1-С8)-алкил, где алкил является незамещенным,
R3 представляет собой
атом водорода,
R23 представляет собой
атом водорода,
-(С0-С4)-алкилен -O-R19, где R19 представляет собой
a) атом водорода,
b) -(С1-С4)-алкил, где алкил является незамещенным или монозамещенным R13,
-(С0-С4)-алкилен-С(O)-R11,
-(C0-C4)-алкилен-C(O)-O-R11,
R11 и R12 независимо друг от друга являются одинаковыми или различными и представляют собой
атом водорода,
-(С1-С6)-алкил,
-O-R17 или
R13 представляет собой -C(O)-O-R10,
R10 и R20 представляют собой, независимо друг от друга, водород, -(С1-С6)-алкил,
R17 представляет собой -(С1-С6)-алкил.
где R0 представляет собой
гетероциклил, выбранный из группы бензотиофенила, пиридила, или
гетероциклил, выбраный из группы 2-фурила, 3-фурила, имидазолила, изоксазолила, оксазолила, пиразолила, пирролила, 2-пирролила, 3-пирролила,
который дополнительно замещен гетероциклилом, выбранным из группы тиенила, где гетероциклил монозамещен R8,
R8 представляет собой
фтор, хлор или бром,
подструктура D представляет собой остаток, выбранный из группы пиридила, замещенный 1 группой R23, или оксогруппой,
Q представляет собой прямую связь, -(С0-С2)-алкилен-С(O)-NR10-, (С1-С6)-алкилен,
R1 представляет собой атом водорода,
R2 представляет собой прямую связь,
V представляет собой
гетероциклил, выбранный из пиперидина, пиридина, тетрагидропиридина, и где гетероциклил является незамещенным,
М представляет собой
атом водорода,
-(С1-С8)-алкил, где алкил является незамещенным, независимо друг от друга, R14,
R3 представляет собой
атом водорода,
R23 представляет собой
атом водорода,
-(С0-С4)-алкилен -O-R19, где R19 представляет собой
a) атом водорода,
b) -(С1-С4)-алкил, где алкил является незамещенным или монозамещен R13,
-(С0-С4)-алкилен-С(O)-R11,
-(С0-С4)-алкилен-С(O)-O-R11,
R11 и R12 независимо друг от друга являются одинаковыми или различными и представляют собой
атом водорода,
-(С1-С6)-алкил,
-O-R17 или
R13 представляет собой -C(O)-O-R10,
R10 и R20 представляют собой, независимо друг от друга, водород, -(С1-С6)-алкил,
R17 представляет собой -(С1-С6)-алкил.
где R0 представляет собой
гетероциклил, выбранный из группы бензотиофенила, пиридила, или
гетероциклил, выбраный из группы пирролила, 2-пирролила, 3-пирролила, фурила, 2-фурила, 3-фурила, имидазолила, пиразолила, оксазолила и изоксазолила, где гетероциклил является монозамещен R8,
и дополнительно замещен остатком тиенила, 2-тиенила, 3-тиенила, где указанный остаток является является монозамещен R8,
R8 представляет собой
F, Cl, Br или I,
подструктура D представляет собой остаток, выбранный из группы пиридила, замещенный 1 группой R23, или оксогруппой,
Q представляет собой прямую связь, -(С1-С6)-алкилен или -(С0-С2)-алкилен-С(O)-NR10-,
R1 представляет собой атом водорода,
R2 представляет собой прямую связь,
V представляет собой
циклический остаток из группы, содержащей соединения, которые являются производными пиридина, где указанный гетероциклил является незамещенным, М представляет собой атом водорода,
-(С1-С6)-алкил, где алкил является незамещенным,
R3 представляет собой
1) атом водорода,
R23 представляет собой
атом водорода,
-(С0-С4)-алкилен-О-R19, где R19 представляет собой
a) атом водорода,
b) -(С0-С4)-алкил, где алкил является незамещенным или монозамещен R13,
-(С0-С4)-алкилен-C(O)-R11,
-(С0-С4)-алкилен-С(O)-O-R11,
R13 представляет собой -C(O)-O-R10,
R10 и R20 представляют собой, независимо друг от друга, водород, -(С1-С6)-алкил,
R17 представляет собой -(С1-С6)-алкил.
где R0 представляет собой
гетероциклил, выбранный из группы бензотиофенила, пиридила, или
гетероциклил, выбраный из группы пирролила, 2-пирролила, 3-пирролила, фурила, 2-фурила, 3-фурила, имидазолила, пиразолила, оксазолила, изоксазолила и пиразинила, где гетероциклил монозамещен R8,
и дополнительно замещен остатком, выбранным из группы тиенила, 2-тиенила, 3-тиенила, где указанный остаток является монозамещен R8,
R8 представляет собой
F, Cl, Br или I,
подструктура D представляет собой остаток, выбранный из группы пиридила, и является замещенной 1 группой R23, или оксогруппой,
Q представляет собой прямую связь, -(С1-С6)-алкилен или -(С0-С2)-алкилен-С(O)-NR10-,
R1 представляет собой атом водорода,
R2 представляет собой прямую связь,
V представляет собой
циклический остаток из группы, содержащей соединения, которые являются производными азиродина, изохинолина, морфолина, пиперидина, пиридина, хинолина, где указанный циклический остаток является незамещенным,
М представляет собой
атом водорода,
-(С1-С8)-алкил, где алкил является незамещенным,
R3 представляет собой атом водорода,
R23 представляет собой
атом водорода,
-(С0-С4)-алкилен -O-R19, где R19 представляет собой
a) атом водорода,
b) -(С1-С4)-алкил, где алкил является незамещенным или монозамещен R13,
-(С0-С4)-алкилен-C(O)-R11,
-(С0-С4)-алкилен-С(O)-O-R11,
R11 и R12 независимо друг от друга являются одинаковыми или различными и представляют собой
атом водорода,
-(С1-С6)-алкил,
-O-R17 или
R13 представляет собой -C(O)-O-R10,
R10 и R20 представляют собой, независимо друг от друга, водород, -(С1-С6)-алкил, и
R17 представляет собой -(С1-С6)-алкил.
где R0 представляет собой
пиридил или бензотиофенил, или
гетероциклил, выбранный из изоксазолила, где указанный гетероциклил является замещенным остатком, выбранным из тиенила, 2-тиенила и 3-тиенила, где указанный остаток является монозамещен R8,
R8 представляет собой F, Cl, Br,
подструктура D представляет собой остаток, выбранный из пиридила, замещенный 1 группой R23 или оксогруппой,
Q представляет собой прямую связь, -CH2-C(O)-NH, метилен или этилен,
R1 представляет собой атом водорода,
R2 представляет собой прямую связь,
V представляет собой
остаток, выбранный из группы, содержащей соединения, которые являются производными пиперидина, хиназолина, хинолина,
где указанный циклический остаток является незамещенным,
М представляет собой атом водорода, (С2-С4)-алкил, где алкил является незамещеным,
R3 представляет собой
атом водорода,
R23 представляет собой
атом водорода,
-(С0-С2)-алкилен -O-R19, где R19 представляет собой
a) атом водорода,
b) -(С1-С4)-алкил, где алкил является незамещенным или монозамещен R13,
-(С0-С4)-алкилен-С(O)-R11,
-(С0-С4)-алкилен-C(O)-O-R11,
R11 и R12 независимо друг от друга являются одинаковыми или различными и представляют собой
атом водорода,
-(С1-С4)-алкил,
-O-R17 или
R13 представляет собой -C(O)-O-R10,
R10 и R20 представляют собой, независимо друг от друга, водород, -(С1-С6)-алкил, R17 представляет собой -(С1-С6)-алкил.
где R0 представляет собой
пиридил или бензотиофенил, или
гетероциклил, выбранный из изоксазолила, где указанный гетероциклил является замещенным остатком, выбранным из тиенила, 2-тиенила и 3-тиенила, где указанный остаток является монозамещен R8,
R8 представляет собой F, Cl, Br,
подструктура D представляет собой остаток, выбранный из пиридила, замещенный 1 группой R23 или оксогруппой,
Q представляет собой -CH2-C(O)-NH или метилен,
R1 представляет собой атом водорода,
R2 представляет собой прямую связь,
V представляет собой пиперидин, где пиперидин является незамещенным,
G представляет собой прямую связь,
М представляет собой атом водорода, (С2-С4)-алкил, где алкил является незамещенным,
R3 представляет собой
атом водорода,
R11 и R12 независимо друг от друга являются одинаковыми или различными и представляют собой
атом водорода или
-(С1-С4)-алкил,
R13 представляет собой -C(O)-O-R10,
R10 и R20 представляют собой, независимо друг от друга, водород, -(С1-С4)-алкил.
(1-изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пирроло[2,3-b]пиридин-2-карбоновой кислоты,
метиловый эфир 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пирроло[2,3-b]пиридин-5-карбоновой кислоты,
1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пирроло[2,3-b]пиридин-5-карбоновую кислоту,
2-[(1-изопропилпиперидин-4-ил)амид]5-амида 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пирроло[2,3-b]пиридин-2,5-дикарбоновой кислоты,
(1-изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-1Н-пирроло[3,2-b]пиридин-2-карбоновой кислоты,
1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(1-изопропилпиперидин-4-илкарбамоил)-1Н-пирроло[3,2-b]пиридин-5-карбоновую кислоту,
(1-изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-оксо-4,5-дигидро-1Н-пирроло[3,2-b]пиперидин-2-карбоновой кислоты,
метиловый эфир 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(3,4,5,6-тетрагидро-2Н-[1,4']бипиридинил-4-илкарбамоил)-1Н-пирроло[3,2-b]пиридин-5-карбоновой кислоты,
1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-2-(3,4,5,6-тетрагидро-2Н-[1,4']бипиридинил-4-илкарбамоил)-1H-пирроло[3,2-b]пиридин-5-карбоновую кислоту,
(1-изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-(2-метоксиэтокси)-1Н-пирроло[2,3-с]пиридин-2-карбоновой кислоты,
(1-изопропилпиперидин-4-ил)амид 1-[5-(5-хлортиофен-2-ил)изоксазол-3-илметил]-5-(2-гидроксиэтокси)-1Н-пирроло[2,3-с]пиридин-2-карбоновой кислоты,
(1-изопропилпиперидин-4-ил)амид 1-[(5-хлорпиридин-2-илкарбамоил)метил]-5-(2-метоксиэтокси)-1Н-пирроло[2,3-с]пиридин-2-карбоновой кислоты,
(1-изопропилпиперидин-4-ил)амид 1-[(5-хлорпиридин-2-илкарбамоил)метил]-5-(2-гидроксиэтокси)-1H-пирроло[2,3-с]пиридин-2-карбоновой кислоты,
(1-изопропилпиперидин-4-ил)амид 1-[(6-хлорбензо[b]тиофен-2-илметил)-5-(2-метоксиэтокси)-1Н-пирроло[2,3-с]пиридин-2-карбоновой кислоты или
(1-изопропилпиперидин-4-ил)амид 1-[(6-хлорбензо[b]тиофен-2-илметил)-5-(2-гидроксиэтокси)-1Н-пирроло[2,3-с]пиридин-2-карбоновой кислоты.

где остаток R8' имеет значение -N(R1)-R2-V-G-M, где R1,R2,V,G и М имеют значения, как указано в пп.1-8, остаток R54 означает группу -Q-R0 или водород, и где группа -C(O)-R53 может представлять собой группу карбоновой кислоты или ее эфир, а группы R3a в формулах 29 и 30 имеют соответствующие определения R3 в формуле I, как определено в п.1 и фукциональные группы, не участвующие в реакции при необходимости могут быть защищены, и если в полученном соединении R54 означает Н, трансформируют его в соединение с группой -Q-R0; с удалением при необходимости защитных групп.
| ПРОИЗВОДНЫЕ ИМИДАЗО[1,5-А]ПИРИДИНА КАК ИНГИБИТОРЫ СЕРИНПРОТЕАЗ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1996 |
|
RU2175327C2 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
Авторы
Даты
2008-08-10—Публикация
2004-05-05—Подача