Настоящее изобретение относится к новым синергетическим гербицидным композициям избирательного действия для борьбы с травянистыми растениями и сорняками в посевах культурных растений, в частности, в посевах кукурузы и зерновых культур, эти композиции содержат гербицид 3-гидрокси-4-(4-метилфенил)-5-оксопиразолин, обладающее синергетической активностью количество по меньшей мере одного второго гербицида, а также необязательно масляную добавку и/или защитный агент (антидот), а также к применению этих композиций для борьбы с сорняками в посевах культурных растений.
При внесении гербицидов культурные растения также могут подвергаться серьезным повреждениям в зависимости, например, от таких факторов, как концентрация гербицида и метод внесения, особенности самого сельскохозяйственного растения, состав почвы и климатические условия, такие как характеристики освещенности, температура и количество осадков. Для решения этой и аналогичных проблем уже было предложено применять различные соединения в качестве антидотов, способных противодействовать вредному воздействию гербицида на культурное растение, т.е. защищать от него культурное растение, сохраняя при этом практически без уменьшения гербицидное воздействие на сорняки, подлежащие уничтожению.
Однако было обнаружено, что предложенные антидоты часто обладают очень специфичным действием не только в отношении культурных растений, но и в отношении гербицида, что в некоторых случаях также зависит от метода внесения, т.е. конкретный антидот часто может оказаться пригодным только для конкретного культурного растения и конкретного класса гербицидов или конкретного гербицида. Например, было установлено, что антидоты клохинтоцет и клохинтоцет-мексил и мефенпир и мефенпир-диэтил, описанные в ЕР-А-0191736 (соединение 1.316) и в WO 91/07874 (пример 3), а также описанные в The Pesticide Manual, 11-е изд., British Crop Protection Council, Entry No. 154 и 462, обладают способностью защищать культурные растения от фитотоксичного действия определенных 3-гидрокси-(4-метилфенил)-5-оксопиразолиновых производных, однако в некоторых случаях они снижают гербицидное действие в отношении сорняков.
В US-A-4834908 описаны некоторые комбинации масляных добавок, которые повышают гербицидное действие соединений из класса циклогександионов, бензотиадиазинондиоксидов, гербицидов, которые представляют собой дифениловые эфиры, и гербицидов, которые относятся к арилоксифеноксипроизводным.
Хотя 3-гидрокси-(4-метилфенил)-5-оксопиразолиновые производные по структуре совершенно отличны от соединений, которые описаны в US-A-4834980, сочетание таких масляных добавок с указанными 3-гидрокси-(4-метилфенил)-5-оксопиразолиновыми производными также приводит к повышению гербицидной активности, но при этом культурное растение также в значительной степени повреждается. Таким образом, смесь гербицида/масляной добавки нельзя применять для избирательной борьбы с сорняками в посевах культурных растений.
При создании изобретения неожиданно было установлено, что с сорняками можно очень успешно избирательно бороться при использовании определенных 3-гидрокси-(4-метилфенил)-5-оксопиразолиновых гербицидов, не повреждая при этом культурные растения, путем внесения этих соединений в сочетании с обладающим синергетической активностью количеством по меньшей мере одного второго гербицида, и необязательно также в сочетании с добавкой, включающей масло растительного или животного происхождения или минеральное масло, их сложные алкиловые эфиры или смеси этих масел и масляных производных, и с антидотами клохинтоцетом или мефенпиром.
Таким образом, изобретение относится к гербицидной композиции избирательного действия, содержащей наряду с обычными в препаративных формах инертными добавками, такими как носители, растворители и смачивающие агенты, в качестве действующего вещества смесь, включающую
а) гербицидно эффективное количество соединения формулы I
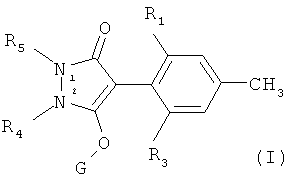
где
R1 и R3 каждый независимо друг от друга обозначает галоген, нитро, циано, С1-С4алкил, С2-С4алкенил, С2-С4алкинил, С1-С4галоалкил, С2-С6галоалкенил, С3-С6циклоалкил, галозамещенный С3-С6циклоалкил, С2-С6алкоксиалкил, С2-С6алкилтиоалкил, гидрокси, меркапто, C1-С6алкокси, С3-С6алкенилокси, С3-С6алкинилокси, карбонил, карбоксил, С1-С4алкилкарбонил, С1-С4гидроксиалкил, С1-С4алкоксикарбонил, С1-С4алкилтио, С1-С4алкилсульфинил, C1-С4алкилсульфонил, амино, С1-С4алкиламино или ди(С1-С4алкил)амино;
R4 и R5 вместе обозначают группу
-C-R6(R7)-O-C-R8(R9)-C-R10(R11)-C-R12(R13)- (Z1),
-C-R14(R15)-C-R16(R17)-O-C-R18(R19)-C-R20(R21)- (Z2) или
-C-R22(R23)-C-R24(R25)-C-R26(R27)-O-C-R28(R29)- (Z3),
где R6, R7, R8, R9, R10, R11, R12, R13, R14, R15, R16, R17, R18, R19, R20, R21, R22, R23, R24, R25, R26, R27, R28 и R29 каждый независимо друг от друга обозначает водород, галоген, С1-С4алкил или С1-С4галоалкил, причем алкиленовое кольцо, которое вместе с атомами углерода групп Z1, Z2 или Z3 содержит от 2 до 6 атомов углерода и которое может включать кислород, может быть либо анеллировано, либо связано посредством спиросвязи с атомами углерода групп Z1, Z2 или Z3, или это алкиленовое кольцо может быть соединено мостиком по меньшей мере с одним кольцевым атомом групп Z1, Z2 или Z3;
G обозначает водород, -С(Х1)-R30, -С(Х2)-Х3-R31, -C(X4)-N(R32)-R33, -SO2-R34, катион щелочного металла, щелочно-земельного металла, сульфония или аммония или -Р(Х5)(R35)-R36 или -СН2-Х6-R37;
X1, Х2, Х3, Х4, X5 и Х6 каждый независимо друг от друга обозначает кислород или серу;
R30, R31, R32 и R33 каждый независимо друг от друга обозначает водород, C1-С10алкил, C1-С10галоалкил, C1-С10цианалкил, C1-С10нитроалкил, C1-С10аминоалкил, С1-С5алкиламино-С1-С5алкил, С2-С8диалкиламино-С1-С5алкил, С3-С7циклоалкил-С1-С5алкил, С2-С10алкоксиалкил, С4-С10алкенилоксиалкил, С4-С10алкинилоксиалкил, С2-С10алкилтиоалкил, С1-С5алкилсульфоксил-С1-С5алкил, С1-С5алкилсульфонил-С1-С5алкил, С2-С8алкилиденаминоокси-С1-С5алкил, C1-С5алкилкарбонил-С1-С5алкил, С1-С5алкоксикарбонил-С1-С5алкил, С1-С5аминокарбонил-С1-С5алкил, С2-С8диалкиламинокарбонил-С1-С5алкил, C1-С5алкилкарбониламино-С1-С5алкил, С2-С5алкилкарбонил-(С1-С5алкил)аминоалкил, С3-С6триалкилсилил-С1-С5алкил, фенилС1-С5алкил, гетероарилС1-С5алкил, феноксиС1-С5алкил, гетероарилоксиС1-С5алкил, С2-С5алкенил, С2-С5галоалкенил, С3-С8циклоалкил, фенил или C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный фенил или гетероарил или гетероариламино, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный гетероариламино, дигетероариламино, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный дигетероариламино, фениламино, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано или нитрозамещенный фениламино, дифениламино, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано или нитрозамещенный дифениламино, С3-С7циклоалкиламино, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный С3-С7циклоалкиламино, диС3-С7циклоалкиламино, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный диС3-С7циклоалкиламино, С3-С7циклоалкокси или C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный С3-С7циклоалкокси;
R34, R35 и R36 обозначают водород, C1-С10алкил, C1-С10галоалкил, C1-С10цианалкил, C1-С10нитроалкил, C1-С10аминоалкил, С1-С5алкиламино-С1-С5алкил, С2-С8диалкиламино-С1-С5алкил, С3-С7циклоалкил-С1-С5алкил, С2-С10алкоксиалкил, С4-С10алкенилоксиалкил, С4-С10алкинилоксиалкил, С2-С10алкилтиоалкил, С1-С5алкилсульфоксил-С1-С5алкил, С1-С5алкилсульфонил-С1-С5алкил, С2-С8алкилиденаминоокси-С1-С5алкил, С1-С5алкилкарбонил-С1-С5алкил, С1-С5алкоксикарбонил-С1-С5алкил, С1-С5аминокарбонил-С1-С5алкил, С2-С8диалкиламинокарбонил-С1-С5алкил, С1-С5алкилкарбониламино-С1-С5алкил, С2-С5алкилкарбонил-(С1-С5алкил)аминоалкил, С3-С6триалкилсилил-C1-С5алкил, фенилС1-С5алкил, гетероарилС1-С5алкил, феноксиС1-С5алкил, гетероарилоксиС1-С5алкил, С2-С5алкенил, С2-С5галоалкенил, С3-С8циклоалкил, фенил или C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный фенил или гетероарил или гетероариламино, C1-С3алкил-, C1-С3 галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный гетероариламино, дигетероариламино, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный дигетероариламино, фениламино, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный фениламино, дифениламино, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный дифениламино, С3-С7циклоалкиламино, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный С3-С7циклоалкиламино, диС3-С7циклоалкиламино, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный диС3-С7циклоалкиламино, С3-С7циклоалкокси, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный С3-С7циклоалкокси, C1-С10алкокси, C1-С10галоалкокси, С1-С5алкиламино, С2-С8диалкиламино и бензилокси или фенокси, причем бензильная и фенильная группы сами могут быть замещены C1-С3алкилом, C1-С3галоалкилом, C1-С3алкокси-, C1-С3галоалкоксигруппой, галогеном, цианогруппой, формилом, ацетилом, пропионилом, карбоксилом, С1-С5алкоксикарбонилом, метилтио-, этилтио- или нитрогруппой;
и R37 обозначает C1-С10алкил, C1-С10галоалкил, C1-С10цианалкил, C1-С10нитроалкил, C1-С10аминоалкил, С1-С5алкиламино-С1-С5алкил, С2-С8диалкиламино-С1-С5алкил, С3-С7циклоалкил-С1-С5алкил, С2-С10алкоксиалкил, С4-С10алкенилоксиалкил, С4-С10алкинилоксиалкил, С2-С10алкилтиоалкил, С1-С5алкилсульфокси-С1-С5алкил, С1-С5алкилсульфонил-С1-С5алкил, С2-С8алкилиденаминоокси-С1-С5алкил, С1-С5алкилкарбонил-С1-С5алкил, C1-С5алкоксикарбонил-С1-С5алкил, С1-С5аминокарбонил-С1-С5алкил, С2-С8диалкиламинокарбонил-С1-С5алкил, С1-С5алкилкарбониламино-С1-С5алкил, С2-С5алкилкарбонил-(С1-С5алкил)аминоалкил, С3-С6триалкилсилил-С1-С5алкил, фенилС1-С5алкил, гетероарилС1-С5алкил, феноксиС1-С5алкил, гетероарилоксиС1-С5алкил, С2-С5алкенил, С2-С5галоалкенил, С3-С8циклоалкил, фенил или C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный фенил или гетероарил или гетероариламино, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный гетероариламино, дигетероариламино, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный дигетероариламино, фениламино, C1-С3алкил-, С1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный фениламино, дифениламине, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный дифениламинo, С3-С7циклоалкиламино, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный С3-С7циклоалкиламино, диС3-С7циклоалкиламино, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный диС3-С7циклоалкиламино, С3-С7циклоалкокси, C1-С3алкил-, C1-С3галоалкил-, C1-С3алкокси-, C1-С3галоалкокси-, гало-, циано- или нитрозамещенный С3-С7циклоалкокси или C1-С10алкилкарбонил; и солей и диастереомеров соединений I, при условии, что R1 и R3 одновременно не обозначают метил; и
б) обладающее гербицидной синергетической активностью количество по меньшей мере одного гербицида, выбранного из классов феноксифеноксипропионовых кислот, гидроксиламинов, сульфонилмочевин, имидазолинонов, пиримидинов, триазинов, мочевин, РРО, хлорацетанилидов, феноксиуксусных кислот, триазинонов, динитроанилинов, азинонов, карбаматов, оксиацетамидов, тиолкарбаматов, азолмочевин, бензойных кислот, анилидов, нитрилов, трионов и сульфонамидов, а также из таких гербицидов, как амитрол, бенфуресат, бентазон, цинметилин, кломазон, хлопиралид, дифензокват, дитиопир, этофумесат, флурохлоридон, инданофан, изоксабен, оксазикломефон, пиридат, пиридафол, квинхлорак, квинмерак, тридифан и флампроп; и необязательно
в) эффективное для предотвращения вредного действия гербицида количество антидота, выбранного из группы, включающей клохинтоцет, катион, такой как щелочной металл, щелочно-земельный металл, сульфоний или аммоний клохинтоцета, клохинтоцет-мексил, мефенпир, катион, такой как щелочной металл, щелочно-земельный металл, сульфоний или аммоний мефенпира, и мефенпир-диэтил; и/или
г) добавку, включающую масло растительного или животного происхождения или минеральное масло, их алкиловые эфиры или смеси этих масел и производных масел.
В контексте настоящего описания понятие галоген включает фтор, хлор, бром или йод, предпочтительно фтор, хлор или бром. Встречающиеся в определениях заместителей алкильные группы обозначают, например, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил или трет-бутил и пентильные и гексильные изомеры. Приемлемые циклоалкильные заместители содержат от 3 до 6 атомов углерода и представляют собой, например, циклопропил, циклобутил, циклопентил или циклогексил. Они могут быть замещены одним или несколькими атомами галогена, предпочтительно фтора, хлора или брома. Под алкенилом понимают, например, винил, аллил, металлил, 1-метилвинил или бут-2-ен-1-ил. Алкинил обозначает, например, этинил, пропаргил, бут-2-ин-1-ил, 2-метилбутан-2-ил или бут-3-ин-2-ил. Галоалкильные группы предпочтительно имеют цепь, состоящую из 1-4 атомов углерода. Галоалкил обозначает, например, фторметил, дифторметил, трифторметил, хлорметил, дихлорометил, трихлорметил, 2,2,2-трифторэтил, 2-фторэтил, 2-хлорэтил, пентафлорэтил, 1,1-дифтор-2,2,2-трихлорэтил, 2,2,3,3-тетрафторэтил или 2,2,2-трихлорэтил, предпочтительно трихлорметил, дифторхлорметил, дифторметил, трифторметил или дихлорфторметил. Приемлемые галоалкенильные радикалы включают алкенильные группы, замещенные одним или несколькими атомами галогена, где галоген обозначает фтор, хлор, бром или йод и предпочтительно фтор или хлор, например, 2,2-дифтор-1-метилвинил, 3-фторпропенил, 3-хлорпропенил, 3-бромпропенил, 2,3,3-трифторпропенил, 2,3,3-трихлорпропенил и 4,4,4-трифторбут-2-ен-1-ил. Из С2-С6алкенильных групп, замещенных 1, 2 или 3 атомами галогена, предпочтительными являются группы, имеющую цепь, состоящую из 3-5 атомов углерода. Алкоксигруппы предпочтительно имеют цепь, состоящую из 1-6 атомов углерода. Алкоксигруппа обозначает, например, метокси, этокси, пропокси, изопропокси, н-бутоки, изобутокси, втор-бутокси или трет-бутокси или изомеры пентилокси- или гексилоксигрупп, предпочтительно метокси или этокси. Алкилкарбонил предпочтительно обозначает ацетил или пропионил. Алкоксикарбонил обозначает, например, метоксикарбонил, этоксикарбонил, пропоксикарбонил, изопропоксикарбонил, н-бутоксикарбонил, изобутоксикарбонил, втор-бутоксикарбонил или трет-бутоксикарбонил, предпочтительно метоксикарбонил или этоксикарбонил. Алкилтиогруппы предпочтительно имеют цепь, состоящую из 1-4 атомов углерода. Алкилтио обозначает, например, метилтио, этилтио, пропилтио, изопропилтио, н-бутилтио, изобутилтио, втор-бутилтио или трет-бутилтио, предпочтительно метилтио или этилтио. Алкилсульфинил обозначает, например, метилсульфинил, этилсульфинил, пропилсульфинил, изопропилсульфинил, н-бутилсульфинил, изобутилсульфинил, втор-бутилсульфинил или трет-бутилсульфинил, предпочтительно метилсульфинил или этилсульфинил. Алкилсульфонил обозначает, например, метилсульфонил, этилсульфонил, пропилсульфонил, изопропилсульфонил, н-бутилсульфонил, изобутилсульфонил, втор-бутилсульфонил или трет-бутилсульфонил, предпочтительно метилсульфонил или этилсульфонил. Алкиламино обозначает, например, метиламино, этиламино, н-пропиламино, изопропиламино или бутиламиновый изомер. Диалкиламино обозначает, например, диметиламино, метилэтиламино, диэтиламино, н-пропилметиламино, дибутиламино или диизопропиламино, Алкоксиалкильные группы предпочтительно имеют от 2 до 6 атомов углерода. Алкоксиалкил обозначает, например, метоксиметил, метэтоксиэтил, этоксиметил, этоксиэтил, н-пропоксиметил, н-пропоксиэтил, изопропоксиметил или изопропоксиэтил. Алкилтиоалкил обозначает, например, метилтиометил, метилтиоэтил, этилтиометил, этилтиоэтил, н-пропилтиометил, н-пропилтиоэтил, изопропилтиометил, изопропилтиоэтил, бутилтиометил, бутилтиоэтил или бутилтиобутил. Фенил может находиться в замещенной форме, в каждом случае заместители могут находиться в орто-, мета- и/или пара-положении. Предпочтительными положениями заместителей являются орто- и пара-положения относительно точки присоединения к кольцу.
Гетероарильные группы обычно представляют собой ароматические гетероциклы, которые содержат предпочтительно от 1 до 3 гетероатомов, выбранных из азота, кислорода и серы. Примерами приемлемых гетероциклов и гетероароматических соединений являются: пирролидин, пиперидин, пиран, диоксан, азетидин, оксетан, пиридин, пиримидин, триазин, тиазол, тиадиазол, имидазол, оксазол, изоксазол и пиразин, фуран, морфолин, пиперазин, пиразол, бензоксазол, бензотиазол, хиноксалин и хинолин. Указанные гетероциклы и гетероароматические соединения могут быть дополнительно замещены, например, галогеном, алкилом, алкоксигруппой, галоалкилом, галоалкокси-, нитро-, цианогруппой, тиоалкилом, алкиламиногруппой или фенил. С2-С10алкенил- и -алкинильные группы R34 могут быть моно- или полиненасыщенными. Они содержат предпочтительно от 2 до 12 атомов углерода, в частности от 2 до 6 атомов углерода.
Катионы щелочного металла, щелочно-земельного металла или аммония, служащие в качестве заместителя G, обозначают, например, катионы натрия, калия, магния, кальция и аммония. Предпочтительными катионами сульфония являются, в частности, катионы триалкилсульфония, в которых все алкильные радикалы содержат предпочтительно от 1 до 4 атомов углерода.
Левосторонняя свободная валентность групп Z1, Z2 и Z3 связана с положением 1, а правосторонняя свободная валентность связана с положением 2 пиразолинового кольца.
Соединения формулы I, в которых алкиленовое кольцо может быть анеллировано или связано посредством спиросвязи с группами Z1, Z2 или Z3, при этом от 2 до 6 атомов углерода связано с атомами углерода групп Z1, Z2 и Z3, имеют, например, следующее строение:
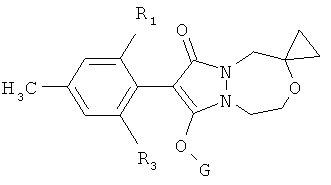
(спиросвязь) или
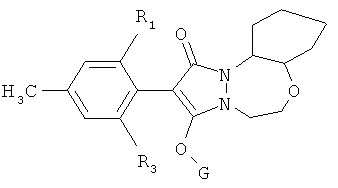
(анеллировано).
Соединения формулы I, в которых алкиленовое кольцо в группах Z1, Z2 или Z3 соединено мостиком по меньшей мере с одним кольцевым атомом групп Z1, Z2 или z3, имеют, например, следующее строение:
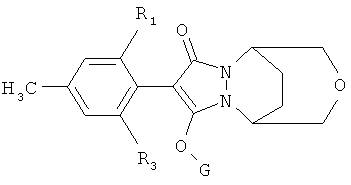
(связь с помощью мостика).
В гербицидах формулы I, которые являются предпочтительными для включения в композиции по изобретению, R1 и R3 каждый независимо друг от друга обозначает этил, галоэтил, этинил, С1-С2алкокси или С1-С2галоалкокси.
Предпочтительными также являются композиции по изобретению, в которых в формуле I R4 и R5 вместе обозначают группу Z2, т.е. -C-R14(R15)-C-R16(R17)-O-C-R18(R19)-C-R20(R21)-, где наиболее предпочтительно R14, R15, R16, R17, R18, R19, R20 и R21 обозначают водород.
Кроме того, в предпочтительной группе композиций по изобретению в формуле I R30, R31, R32 и R33 каждый независимо друг от друга обозначает водород, C1-С8алкил, С1-С8галоалкил, С1-С8цианалкил, С1-С8нитроалкил, C1-С8аминоалкил, С2-С5алкенил, С2-С5галоалкенил, С3-С8циклоалкил, C1-С5алкиламино-С1-С5алкил, С2-С8диалкиламино-С1-С5алкил, С3-С7циклоалкил-С1-С5алкил, С2-С4алкоксиалкил, С4-С6алкенилоксиалкил, С4-С6алкинилоксиалкил, С2-С4алкилтиоалкил, С1-С4алкилсульфинил-С1-С2алкил, С1-С2алкилсульфонил-С1-С2алкил, С2-С4алкилиденаминоокси-С1-С2алкил, C1-С5алкилкарбонил-С1-С2алкил, С1-С5алкоксикарбонил-С1-С2алкил, С1-С5аминокарбонил-С1-С2алкил, С2-С8диалкиламинокарбонил-С1-С2алкил, C1-С5алкилкарбониламино-С1-С2алкил, С2-С5алкилкарбонил-(С1-С2алкил)аминоалкил, С3-С6триалкилсилил-С1-С5алкил, фенилС1-С2алкил, гетероарилС1-С2алкил, феноксиС1-С2алкил, гетероарилоксиС1-С2алкил, фенил или гетероарил;
R34 R35 и R36 каждый независимо друг от друга обозначает водород, C1-С8алкил, С1-С8 галоалкил, С1-С8циануалкил, С1-С8нитроалкил, С1-C8аминоалкил, С2-С5алкенил, С2-С5 галоалкенил, С3-С8циклоалкил, С1-С5алкиламино-С1-С5алкил, С2-С8диалкиламино-С1-С5алкил, С3-С7циклоалкил-С1-С5алкил, C2-С4алкоксиалкил, С4-C6алкенилоксиалкил, С4-С6алкинилоксиалкил, С2-С4алкилтиоалкил, С1-С4алкилсульфинил-С1-С2алкил, С1-С2алкилсульфонил-С1-С2алкил, С2-С4алкилиденаминоокси-С1-С2алкил, С1-С5алкилкарбонил-С1-С2алкил, С1-С5алкоксикарбонил-С1-С2алкил, С1-С5аминокарбонил-С1-С2алкил, С2-С8диалкиламинокарбонил-С1-С2алкил, С1-С5алкилкарбониламино-С1-С2-алкил, С2-С5алкилкарбонил-(С1-С2алкил)аминоалкил, С3-С6триалкилсилил-C1-С5алкил, фенилС1-С2алкил, гетероарилС1-С2алкил, феноксиС1-С2алкил, гетероарилоксиС1-С2алкил, фенил или гетероарил, бензилокси или фенокси, причем сами бензильные и фенильные группы могут быть замещены галогеном, нитро-, циано-, амино-, диметиламино-, гидрокси-, метокси-, этокси-, метилтио-, этилтиогруппой, формилом, ацетилом, пропионилом, карбоксилом, C1-С5алкоксикарбонилом или C1- или С2галоалкилом; и
R37 обозначает С1-С8алкил, С1-С8галоалкил, С1-С8цианалкил, С1-С8нитроалкил, С1-С8аминоалкил, С2-С5алкенил, С2-С5галоалкенил, С3-С8циклоалкил, С1-С5алкиламино-С1-С5алкил, С2-С8диалкиламино-С1-С5алкил, С3-С7циклоалкил-С1-С5алкил, С2-С4алкоксиалкил, С4-С6алкенилоксиалкил, С4-С6алкинилоксиалкил, С2-С4алкилтиоалкил, С1-С4алкилсульфинил-С1-С2алкил, С1-С2алкилсульфонил-С1-С2алкил, С2-С4алкилиденаминоокси-С1-С2алкил, C1-С5алкилкарбонил-С1-С2алкил, С1-С5алкоксикарбонил-С1-С2алкил, C1-С5аминокарбонил-С1-С2алкил, С2-С8диалкиламинокарбонил-С1-С2алкил, C1-С5алкилкарбониламино-С1-С2алкил, С2-С5алкилкарбонил-(С1-С2алкил)аминоалкил, С3-С6триалкил-С1-С5алкил, фенилС1-С2алкил, гетероарилС1-С2алкил, феноксиС1-С2алкил, гетероарилоксиС1-С2алкил, фенил или гетероарил, бензилокси или фенокси, причем сами бензильные и фенильные группы могут быть замещены галогеном, нитро-, циано-, амино-, диметиламино-, гидрокси-, метокси-, этокси-, метилтио-, этилтиогруппой, формилом, ацетилом, пропионилом, карбоксилом, С1-С2алкоксикарбонилои или С1- или С2галоалкилом; или R37 обозначает С1-С8алкилкарбонил.
Особенно предпочтительными являются такие композиции по изобретению, в которых в формуле I R30, R31, R32 и R33 каждый независимо друг от друга обозначает водород, С1-С8алкил, С1-С8галоалкил, С2-С5алкенил, С2-С5галоалкенил, С3-С8циклоалкил, С3-С7циклоалкил-С1-С2алкил, С2-С4алкоксиалкил, фенил, гетероарил, фенилС1-С2алкил, гетероарилС1-С2алкил, феноксиС1-С2алкил, гетероарилоксиС1-С2алкил;
R34, R35 и R36 каждый независимо друг от друга обозначает водород, C1-С8алкил, С1-С8галоалкил, С2-С5алкенил, С2-С5галоалкенил, С3-С8циклоалкил, С3-С7циклоалкил-С1-С2алкил, С2-С4алкоксиалкил, фенил, гетероарил, фенилС1-С2алкил, гетероарилС1-С2алкил, феноксиС1-С2алкил, гетероарилоксиС1-С2алкил, C1-С6алкокси, C1-С3алкиламино или ди(С1-С3алкил)амино; и
R37 обозначает C1-С8алкил, С1-С8галоалкил, С2-С5алкенил, С2-С5галоалкенил, С3-С8циклоалкил, С3-С7циклоалкил-С1-С2алкил, С2-С4алкоксиалкил, фенил, гетероарил, фенилС1-С2алкил, гетероарилС1-С2алкил, феноксиС1-С2алкил, гетероарилоксиС1-С2алкил, C1-С6алкокси, C1-С3алкиламино, ди(С1-С3алкил)амино или С1-С8алкилкарбонил.
Среди композиций по изобретению особенно предпочтительными являются композиции, которые содержат в качестве обладающего гербицидной активностью компонента смесь соединения формулы I и обладающее синергетической активностью количество по меньшей мере одного гербицида, выбранного из группы, включающей диклофоп-метил, флуазифоп-П-бутил-, квизалафоп-П-этил, пропаквизафоп, клодинафоп-П-пропаргил, цигалофоп-бутил, феноксапроп-П-этил, галоксифоп-метил, галоксифоп-этоэтил, сетоксидим, аллоксидим, клетодим, клефоксидим, циклоксидим, тепралкоксидим, тралкоксидим, бутроксидим, амидосульфурон, азимсульфурон, бенсульфурон-метил, хлоримурон-этил, циносульфурон, хлорсульфурон, хлоримурон, циклосульфамурон, этаметсульфурон-метил, этоксисульфурон, флуазасульфурон, флупирсульфурон, имазосульфурон, йодсульфурон (CAS RN 144550-36-7 и 185119-76-0), метсульфурон-метил, никосульфурон, оксасульфурон, примисульфурон, пиразосульфурон-этил, сульфосульфурон, римсульфурон, тифенсульфурон-метил, триасульфурон, трибенурон-метил, трифлусульфурон-метил, просульфурон, флукарбазон, тритосульфурон (CAS RN 142469-14-5), имазетапир, имазаметабенз, имазаметапир, имазаквин, имазамокс, имазапир, пиритиобак-натрий, пириминобак, биспирибак-натрий, атразин, бутрацил, симазин, симетрин, тербутрин, тербутилазин, тримексифлам, изопротурон, хлортолурон, диурон, димрон, флуометурон, линурон, метабензтиазурон, глифосат, сульфосат, глуфосинат, нитрофен, бифенокс, ацифлуорфен, лактофен, оксифлуорфен, этоксифен, флуоргликофен, фомесафен, галосафен, азафенидин (CAS RN.-68049-83-2), бензфендизон (CAS RN 158755-95-4), бутафенацил (CAS RN 158755-95-4)=CGA 2768S54, карфентразон-этил, цинидон-этил (CAS RN 142891-20-1), флумиклорак-пентил, флумиоксазин, флутиацет-метил, оксадиаргил (CAS RN 39807-15-3), оксадиазон, пентоксазон (CAS RN 110956-75-7), сулфентразон, флуазолат (CAS RN 174514-07-9), пирафлуфен-этил, алахлор, ацетохлор, бутахлор, диметахлор, диметенамид, S-диметенамид, метазахлор, метолахлор, S-метолахлор, претилахлор, пропахлор, пропизохлор, тенилхлор, пентоамид (CAS RN 106700-29-2), 2,4-Д, флуроксипир, МСРА, МСРР, МСРВ, трихлорпир, мекропоп-П, гексазинон, метамитрон, метрибузин, оризалин, пендиметалин, трифлуралин, хлоридазон, норфлуразон, хлорпрофам, десмедифам, фенметифам, профам, мефенацет, флутиацет, бутилат, циклоат, диаллат, ЭПТК, эспрокарб, молинат, просульфокарб, тиобенкарб, триаллат, фентразамид (CAS RN 158237-07-1), кафенстрол, дикамба, пиклорам, дифлуфеникан, пропанил, бромоксинил, дихлобенил, иоксинил, сулкотрион, мезотрион (CAS RN 104206-82-8), изоксафлутол, изоксахлортол (CAS RN 141112-06-3), флукарбазон (CAS RN 181274-17-9), пропоксикарбазон (CAS RN 145026-81-9 и 181274-15-7 (натриевая соль)), форамсульфурон (CAS RN 173159-57-4), пеноксулам (CAS RN 219714-96-2), трифлоксисульфурон (CAS RN 145099-21-4 и 199119-58-9 (натриевая соль)), пирифталид (CAS RN 135186-78-6), трифлоксисульфурон (CAS RN 145099-21-4 и 199119-58-9 (натриевая соль)), пирифталид (CAS RN 135186-78-6), флуфенпир-этил (CAS RN 188489-07-8), профлуазол (CAS RN 190314-43-3), пираклонил (CAS RN 158353-15-2), бенфлуамид (CAS RN 113604-08-7), пиколинафен (CAS RN 137641-05-5), амикарбазон (CAS RN 129909-90-6), флуфенпир-этил (CAS RN 188489-07-8), профлуазол (CAS RN 190314-43-3), пираклонил (CAS RN 158353-15-2), бенфлуамид (CAS RN 113604-08-7). пикалинафен (CAS RN 137641-05-5), амикарбазон (CAS RN 129909-90-6), хлорасулам, диклосулам (CAS RN 145701-21-9), флорасулам, флуметсулам, метосулам, амитрол, бенфуресат, бентазон, цинметилин, кломазон, хлопиралид, дифензокват, дитиопир, этофумесат, флурохлоридон, инданофан, изоксабен, оксазикломефон (CAS RN 153197-14-9), пиридат, пиридафол (CAS RN 40020-01-7), квинхлораквинхлорак, квинмерак, тридифан и флампроп. Сокращение CAS RN обозначает регистрационный номер в Chemical Abstracts.
Композиции по изобретению предпочтительно содержат
а) гербицид формулы I в сочетании с:
б) обладающим гербицидной синергетической активностью количеством второго гербицида по изобретению,
в) антидотом и
г) масляной добавкой.
Из обладающих синергетической активностью гербицидов б) предпочтительными являются представители класса сульфонилмочевин и феноксифеноксипропионовых кислот, особенно предпочтительным гербицидом является, например, клодинафоп-пропаргил, описанный в The Pesticide Manual, 11-е изд., British Crop Protection Council, регистрационный No. 147, и триасульфурон, описанный в The Pesticide Manual, 11-е изд., British Crop Protection Council, регистрационный No. 723. Особенно предпочтительным антидотом в) в композиции по изобретению является клохинтоцет-мексил. В качестве приемлемой масляной добавки предпочтительными согласно изобретению являются MERGE® и Actiprom®.
Если не указано иное, то вышеуказанные компоненты, представляющие собой соединения формулы I, описаны в The Pesticide Manual, одиннадцатое изд., 1997, ВСРС. Компоненты, представляющие собой соединение формулы 1, при необходимости могут также присутствовать в форме их сложных эфиров или солей, перечисленных, например, в The Pesticide Manual, одиннадцатое изд., 1997, ВСРС. Бутафенацил описан в US-A-5.183.492. Петоамид имеет регистрационный номер CAS 106700-29-2. Мезотрион описан в US-A-5006158.
Композиции по изобретению могут также включать соли соединений формулы I, которые могут быть образованы с кислотами. Приемлемыми кислотами для получения кислотно-аддитивных солей являются как органические, так и неорганические кислоты. Примеры таких кислот включают соляную кислоту, бромистоводородную кислоту, азотную кислоту, фосфорную кислоту, серную кислоту, уксусную кислоту, пропионовую кислоту, масляную кислоту, валериановую кислоту, щавелевую кислоту, малоновую кислоту, фумаровую кислоту, органические сульфоновые кислоты, молочную кислоту, винную кислоту, лимонную кислоту и салициловую кислоту. Соли соединений формулы I, которые имеют кислый водород, также представляют собой соли щелочных металлов, например соли натрия и калия; соли щелочно-земельных металлов, например соли кальция и магния; соли аммония, в том числе незамещенные соли аммония и моно- или полизамещенные соли аммония, или соли других органических азотсодержащих оснований. Предпочтительные солеобразующие вещества из гидроксидов щелочных металлов и гидроксидов щелочно-земельных металлов включают предпочтительно гидроксиды лития, натрия, калия, магния или кальция, но особенно предпочтительными из них являются гидроксиды натрия или калия.
Примерами аминов, которые пригодны для образования солей аммония, являются не только аммиак, но и первичные, вторичные и третичные C1-С18алкиламины, С1-С4гидроксиалкиламины и С2-С4алкоксиалкиламины, например, метиламин, этиламин, н-пропиламин, изопропиламин, четыре изомера бутиламина, н-амиламин, изоамиламин, гексиламин, гептиламин, октиламин, нониламин, дециламин, пентадециламин, гексадециламин, гептадециламин, октадециламин, метилэтиламин, метилизопропиламин, метилэтиламин, метилнониламин, метилпентадециламин, метилоктадециламин, этилбутиламин, этилгептиламин, этилоктиламин, гексилгептиламин, гексилоктиламин, диметиламин, диэтиламин, ди-н-пропиламин, диизопропиламин, ди-н-бутиламин, ди-н-амиламин, диизоамиламин, дигексиламин, дигептиламин, диоктиламин, этаноламин, н-пропаноламин, изопропаноламин, N,N-диэтаноламин, N-этилпропаноламин, N-бутилэтаноламин, аллиламин, н-бутенил-2-амин, н-пентенил-2-амин, 2,3-диметилбутенил-2-амин, дибутенил-2-амин, н-гексенил-2-амин, пропилендиамин, триметиламин, триэтиламин, три-н-пропиламин, триизопропиламин, три-н-бутиламин, триизобутиламин, три-втор-бутиламин, три-н-амиламин, метоксиэтиламин и этоксиэтиламин; гетероциклические амины, например, пиридин, хинолин, изохинолин, морфолин, пиперидин, пирролидин, индолин, хинуклидин и азепин; первичные ариламины, например, анилины, метоксианилины, этоксианилины, орто-, мета-, пара-толуидины, фенилендиамины, бензидины, нафтиламины и орто-, мета-, пара-хлоранилины; но особенно предпочтительными являются триэтиламин, изопропиламин и диизопропиламин.
Если применяют нехиральные исходные продукты, то асимметрично замещенные соединения формулы I, полученные согласно процессам, приведенным в настоящем описании, как правило, имеют форму рацематов. Стереоизомеры можно разделить на основе их физико-химических свойств с помощью известных методов, таких, например, как фракционированная кристаллизация с последующим образованием солей с оптически чистыми основаниями, кислотами или комплексами металлов, или с помощью хроматографических методов, таких, например, как жидкостная хроматография высокого давления (ЖХВД) на ацетилцеллюлозе. В контексте настоящего описания под "соединениями формулы I" понимают как концентрированные, так и оптически чистые формы стереизомеров по изобретению и рацематы и диастереоизомеры. Если специально не упоминаются индивидуальные оптические антиподы, то следует понимать, что формула по изобретению относится к рацемическим смесям, которые получают с помощью указанного способа получения. Если присутствует алифатическая двойная связь С=С, то может иметь место геометрическая изомеризация.
Соединения формулы I также могут в зависимости от природы заместителей присутствовать в виде геометрических и/или оптических изомеров и смесей изомеров и в виде таутомеров и смесей таутомеров. Например, соединения формулы I, в которых группа G обозначает водород, могут присутствовать в виде таутомеров, находящихся в указанном состоянии равновесия:
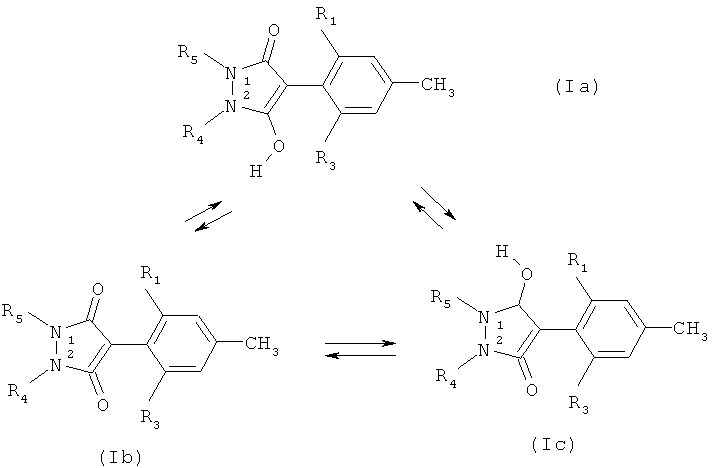
Когда G имеет значение, отличное от водорода, и Z обозначает группу Z1 или Z3 или когда G имеет значение, отличное от водорода, и Z2 является асимметрично замещенным, сконденсированным или связанным посредством спиросвязи, то соединения формулы I могут присутствовать в виде изомера формулы Id
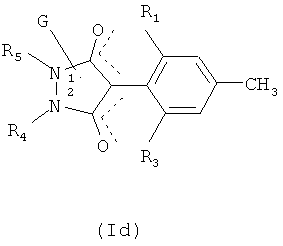
Способы получения соединений, отличных от соединений формулы I по настоящему изобретению в отношении значений заместителей R4 и R5, описаны, например, в WO 96/21652. Соединения формулы I по настоящему изобретению можно получать с помощью процессов, аналогичных описанным в WO 96/21652.
Соединения формулы II
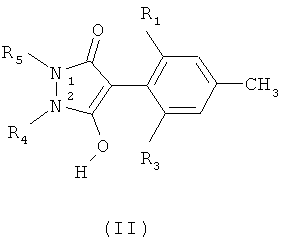
где R1, R3, R4 и R5 имеют значения, указанные для формулы I, применяемые в качестве исходных продуктов для таких процессов, можно получать, например, путем взаимодействия соединения формулы III
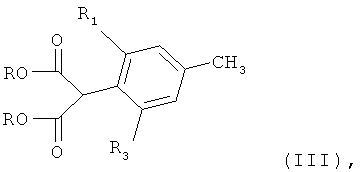
где R обозначает C1-С6алкил, C1-С6 галоалкил, предпочтительно метил, этил или трихлорэтил, и R1 и R3 имеют значения, указанные для формулы I, в инертном органическом растворителе, необязательно в присутствии основания, с соединением формулы IV или IVa
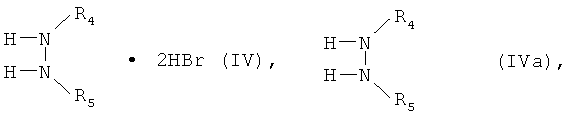
где R4 и R5 имеют значения, указанные для формулы I. Другие процессы получения, с помощью которых можно получить соединения формулы II, также описаны, например, в WO 92/16510.
Соединения формулы III либо являются известными, либо их можно получить с помощью известных методов. Методы получения соединений формулы III и их взаимодействие с гидразинами описаны, например, в WO 97/02243. Соединения формулы III, в которых R обозначает C1-С6алкил, C1-С6галоалкил, предпочтительно метил, этил или трихлорэтил и R1, R2 и R3 имеют значения, указанные для формулы I, можно получать с помощью аналогичных методов, которые известны специалисту в данной области. Например, соединения формулы III, в которых R обозначает C1-С6алкил или C1-С6галоалкил, предпочтительно метил, этил или трихлорэтил, и R1, R2 и R3 каждый независимо друг от друга обозначает С1-С4алкил, С2-С4алкенил или С2-С4алкинил, можно получать с помощью метода поперечного сочетания, описанного у Stille (J.K.Stille, Angew. Chem. 1986. 98, 504-519), Sonogashira (К.Sonogashira и др., Tetrahedron Lett. 1975, 4467-4470), Suzuki (N.Miyaura, A.Suzuki, Chem. Rev. 1995, 95, 2457-2483) или Heck (R.F.Heck, Org. React. 1982, 27, 345-390), и необязательно последующего гидрирования. Этот процесс проиллюстрирован на следующей реакционной схеме:
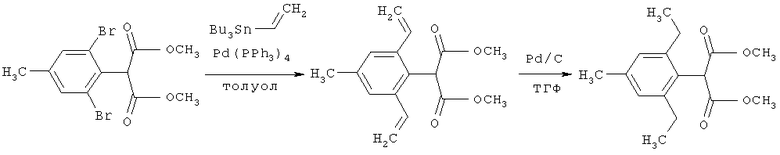
Соединения формул IV и IVa либо являются известными, либо их можно получать с помощью методов, аналогичных известным. Методы получения соединений формулы IV описаны, например, в WO 95/00521. Эти соединения можно получать, например, нагреванием соединения формулы V
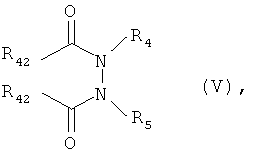
где R42 обозначает водород, С1-С4алкил, C1-С6алкокси, C1-С6галоалкокси или бензилокси, предпочтительно водород, метил, метокси, этокси, трихлорэтокси, трет-бутокси или бензилокси, и R4 и r5 имеют значения, указанные для формулы I, в инертном растворителе в присутствии основания или кислоты. Соединения формулы V, в которых R42 обозначает водород, С1-С4алкил, C1-С6алкокси, C1-С6галоалкокси или бензилокси, предпочтительно водород, метил, метокси, этокси, трихлорэтокси, трет-бутокси или бензилокси, и R4 и R5 имеют значения, указанные для формулы I, можно получать, например, путем взаимодействия соединения формулы VI
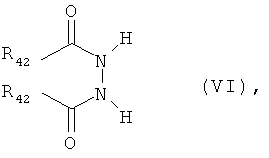
где R42 обозначает водород, С1-С4алкил, C1-С6алкокси, C1-С6галоалкокси или бензилокси, предпочтительно водород, метил, метокси, этокси, трихлорэтокси, трет-бутокси или бензилокси, в присутствии основания и инертного растворителя, с соединением формулы VII
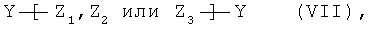
где Y обозначает галоген, алкил/арилсульфонат -OSO2R43, предпочтительно бром, хлор, йод, мезилат (R43=СН3), трифлат (R43=СF3) или тозилат (R43 = пара-толил), и Z1, Z2, и Z3 имеют значения, указанные для формулы I. В формуле VII свободные валентности групп Z1, Z2 и Z3 в каждом случае связаны с группой Y. Соединения формулы VI и VII являются известными или их можно получать аналогично методам, известным специалисту в данной области. Соединения формулы IV, в которых R4 и R5 вместе обозначают группу Z2, т.е. -C-R14(R15)-C-R16(R17)-O-C-R18(R19)-C-R20(R21)-, где R14, R15, R16, R17, R18, R19, R20 и R21 обозначают водород, можно получать, например, согласно следующей реакционной схеме:
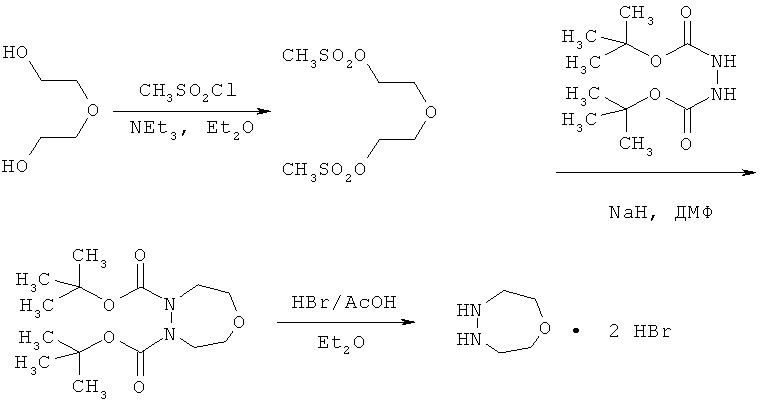
Конечные продукты формулы I можно выделять общепринятым методом путем концентрирования и/или выпаривания растворителя и путем кристаллизации или растирания твердого остатка в растворителях, в которых они не полностью растворимы, таких как простые эфиры, алканы, ароматические углеводороды или хлорированные углеводороды, или можно очищать с помощью хроматографии. Соли соединений формулы I можно получать хорошо известным методом. Такие методы получения описаны, например, в WO 96/21652.
Примеры получения.
Пример Р1: Получение
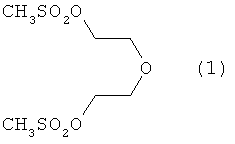
Раствор, содержащий 177,6 г метансульфонилхлорида в 400 мл диэтилового эфира, добавляют по каплям в течение 1 ч к охлажденному до -10°С раствору, содержащему 80,6 г (0,76 моля) диэтиленгликоля и 159,9 г (1,58 моля) триэтиламина в 1500 мл диэтилового эфира, поддерживая температуру на уровне ниже 5°С. После перемешивания в течение 30 мин при температуре 0°С охлаждение прекращают. Через 2 ч добавляют 12 мл триэтиламина и 12 мл метансульфонилхлорида при температуре 20°С и смесь перемешивают в течение еще 4 ч. Образовавшуюся суспензию белого цвета затем переносят на вакуум-фильтр и остаток промывают трижды 300 мл диэтилового эфира. Остаток на фильтре растворяют в 2000 мл этилацетата и суспензию перемешивают в течение 30 мин при комнатной температуре и вновь фильтруют. Полученный фильтрат концентрируют упариванием и остаток применяют в следующей реакции без дополнительной очистки. Получают 216,5 г требуемого неочищенного продукта (1) в форме кристаллов белого цвета.
Пример Р2.
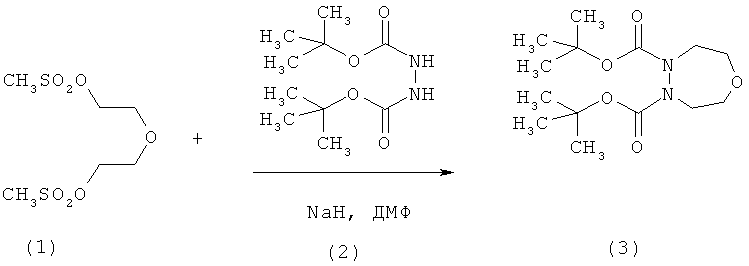
Раствор, содержащий 68,78 г (0,30 моля) соединения (2) в 140 мл диметилформамида, добавляют по каплям в течение 30 мин к охлажденной до 5°С суспензии, содержащей 23,9 г (0,60 моля) 60%-ного гидрида натрия в 500 мл диметилформамида. Охлаждение прекращают и осуществляют перемешивание до достижения температуры реакционной смеси 20°С. Затем смесь быстро нагревают до температуры 30-40°С с целью завершения элиминирования водорода.
После охлаждения до температуры 0-5°С добавляют по каплям в течение 30 мин раствор, содержащий 80 г (0,305 моля) (1) в 160 мл диметилформамида, поддерживая температуру на уровне от 0 до 5°С. После прекращения охлаждения и перемешивания в течение 3 ч при комнатной температуре и в течение 45 мин при температуре примерно 40°С реакционную смесь сливают на смесь, содержащую насыщенный раствор хлорида аммония, лед и метил-трет-бутиловый эфир; фазы разделяют и затем органическую фазу промывают водой (дважды). После сушки органической фазы над сульфатом натрия, концентрирования и упаривания и дополнительной сушки при температуре 40°С в вакууме получают 92,2 г (3) в форме масла светло-желтого цвета. Неочищенный продукт используют в следующей реакции без дополнительной очистки.
Пример Р3.
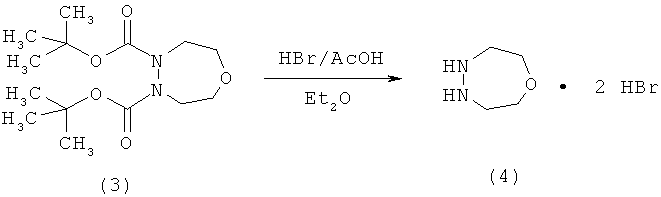
160,5 мл 33%-ного раствора бромистого водорода в ледяной уксусной кислоте добавляют по каплям в течение 30 мин к охлажденному до 0°С раствору, содержащему 92,2 г (0,305 моля) соединения (3) в 1200 мл диэтилового эфира. После прекращения охлаждения и последующего перемешивания в течение 22 ч при 20°С и перемешивания в течение 27 ч при температуре дефлегмации образовавшуюся суспензию белого цвета переносят в вакуум-фильтр; затем осуществляют промывку диэтиловым эфиром и остаток на фильтре затем сушат над P2O5 в вакууме при температуре от 50 до 60°С. Получают продукт (4) в форме твердого вещества белого цвета, выход 52,9 г.
Пример Р4.
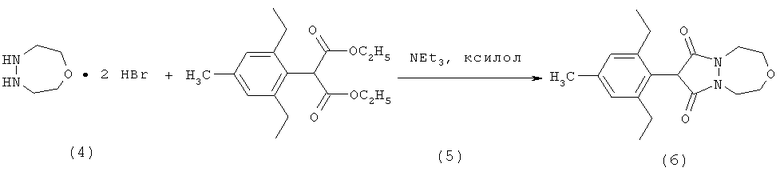
10,61 мл (76 ммолей) триэтиламина добавляют к суспензии, содержащей 4,4 г (16,5 ммоля) соединения (4) в 175 мл ксилена и осуществляют дегазирование (4 × вакуум/аргон). Суспензию желтого цвета затем нагревают до температуры 60°С и перемешивают в течение 3 ч. Затем добавляют 5,07 г (16,5 ммоля) соединения (5) и нагревают в бане с температурой 140°С для того, чтобы непрерывно отгонять избыток триэтиламина и образующийся этанол. Через 3 ч реакционную смесь охлаждают до температуры 40°С и сливают на 100 мл смеси лед/вода. Реакционную смесь подщелачивают с помощью водного 1 н. раствора гидроксида натрия и водную фазу (содержащую продукт) промывают дважды этилацетатом. Затем после двукратной промывки органической фазы водным 1 н. раствором гидроксида натрия водные фазы объединяют, оставшийся ксилен отгоняют и значение рН объединенных водных фаз доводят при охлаждении до 2-3 с помощью 4 н. НСl. Осадившийся продукт переносят в вакуум-фильтр, остаток на фильтре промывают водой и быстро гексаном и остаток на фильтре затем сушат в вакууме при температуре 60°С над P2O5. Получают 4,08 г твердого вещества (6), имеющего температуру плавления 189-191°С (разложение).
Пример Р5.
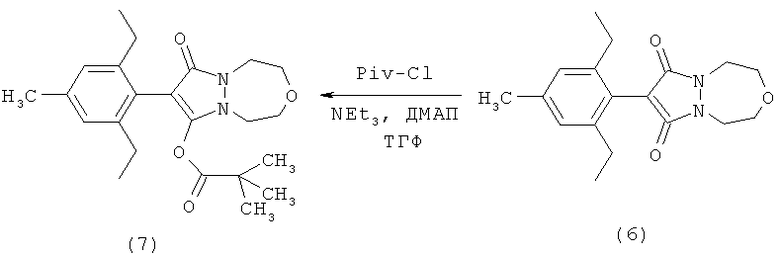
Каталитическое количество 4-диметиламинопиридина добавляют к охлажденному до температуры 0°С раствору, содержащему 1 г (3,2 ммоля) соединения (6) и 0,65 г (6,4 ммоля) триэтиламина в 30 мл тетрагидрофурана. Затем по каплям добавляют 0,49 г (4,1 ммоля) пивалоилхлорида. После перемешивания в течение 30 мин при температуре 0°С охлаждение прекращают и перемешивание осуществляют в течение еще 60 мин. Затем реакционную смесь сливают на насыщенный водный раствор хлорида натрия и органическую фазу отделяют. Органическую фазу сушат над сульфатом магния, фильтруют и концентрируют упариванием. После очистки хроматографией и перекристаллизации из диэтилового эфира получают 1,07 г соединения (7) с температурой плавления от 122 до 123°С.
Пример Р6: Получение
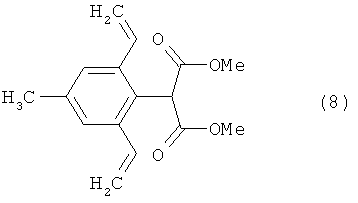
К раствору, содержащему 20 г диметилового эфира 2-(2,6-дибром-4-метилфенил)малоновой кислоты (известного из WO 96/35664) (52,6 ммоля) в 400 мл толуола (дегазированного трижды, вакуум/аргон), добавляют сначала 36,7 г (0,116 моля) трибутилвинилстаннана, а затем 2 г тетракис(трифенилфосфин)палладия. Затем реакционную смесь перемешивают в течение 9 ч при температуре от 90 до 95°С. После фильтрации через фильтр типа Hyflo и концентрирования с помощью роторного испарителя и после очистки хроматографией получают 15,3 г соединения (8) в форме масла желтого цвета, которое используют на следующей стадии без дополнительной очистки.
Пример Р7.
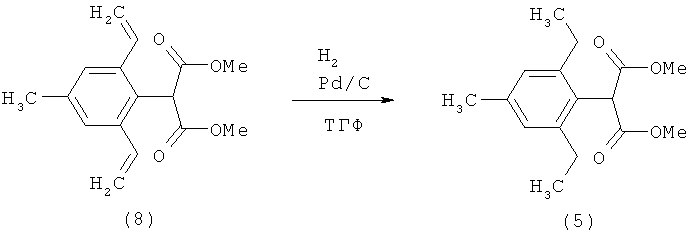
15,2 г соединения (8), полученного согласно примеру Р6, гидрируют с помощью водорода в присутствии палладиевого катализатора (уголь в качестве носителя, 7 г 5%-ного Pd/C) в 160 мл тетрагидрофурана при температуре от 20 до 25°С. После завершения гидрирования продукт фильтруют через фильтр типа Hyflo и полученный фильтрат концентрируют с помощью роторного испарителя. Получают 13,7 г соединения (5) в форме кристаллов желтого цвета с температурой плавления от 47 до 49°С.
Пример Р8.
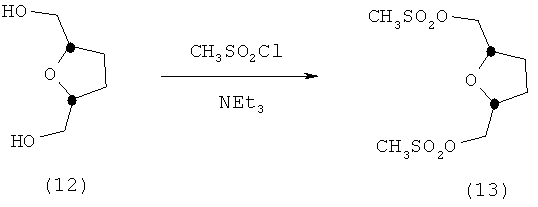
67,8 г (0,59 моля) метансульфохлорида добавляют по каплям к охлажденному до 0-3°С раствору, содержащему 37,1 г (0,28 моля) цис-2,5-бис(гидроксиметил)тетрагидрофурана (12) и 65,3 г (0,65 моля) триэтиламина в 400 мл метиленхлорида, поддерживая температуру на уровне ниже 7°С. Затем осуществляют перемешивание в течение ночи при температуре 20°С. Образовавшуюся суспензию белого цвета переносят в вакуум-фильтр, остаток промывают метиленхлоридом и фильтрат концентрируют упариванием. Остаток растворяют в этилацетате, промывают водой (дважды) и насыщенным водным раствором хлорида натрия (однократно), сушат (Nа2SO4) и концентрируют. Получают 72,7 г димезилатного производного (13) в форме неочищенного масла, которое используют в следующей реакции без дополнительной очистки.
Исходный продукт (12) описан в литературе: см., например, у К.Naemura и др., Tetrahedron Asymmetry, 1993, 4, 911-918.
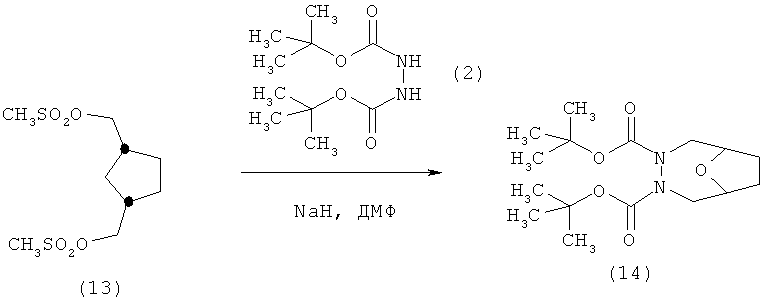
Пример Р9.
Работая аналогично примеру получения Р2, используя в качестве исходных продуктов 21,0 г (0,53 моля) 60%-ного NaH, 58,4 г (0,25 моля) соединения (2) и 72,5 г (0,25 моля) димезилата (13) в общем объеме 840 мл диметилформамида, получают соединение (14) в форме неочищенного мала коричневого цвета. После очистки хроматографией получают 53,7 г чистого соединения (14) в форме твердого вещества белого цвета с температурой от 81 до 83°С.
Пример P10.
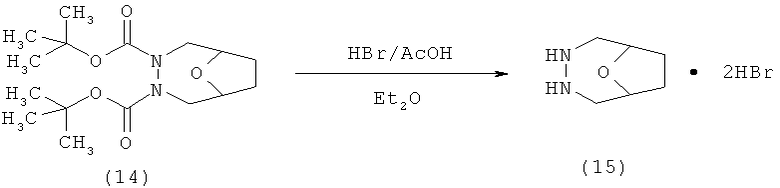
Работая аналогично примеру получения Р3, используя в качестве исходных продуктов 53,5 г (0,16 моля) соединения (14) в 800 мл диэтилового эфира и 90 мл 33%-ного раствора бромистого водорода в концентрированной уксусной кислоте, получают 36,5 г бициклического гидразина (15) в форме твердого вещества с температурой плавления от 262 до 264°С.
Пример Р11.
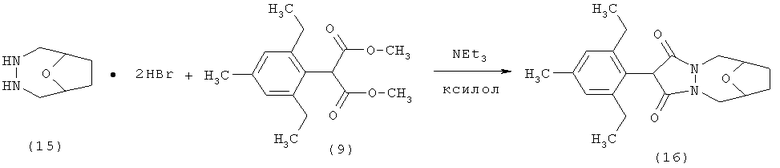
Работая аналогично примеру получения Р4, используя в качестве исходных продуктов 0,105 моля малоната (9) и 30,4 г (0,105 моля) гидразина (15), получают 29,7 г соединения (16) в форме твердого вещества с температурой плавления 287°С.
Пример Р12.
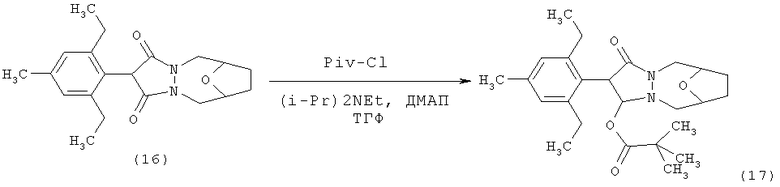
Работая аналогично примеру получения Р9, используя в качестве исходных продуктов 1,1 г (3,2 моля) соединения (16), получают 0,83 г пивалоилового эфира (17) в форме твердого веществ с температурой плавления 141-143°С.
Ниже в таблице, в приведенной в качестве заместителя G формуле, левая сторона формулы является местом присоединения атома кислорода гетероцикла. Другие концевые валентные структуры представляют собой метальные группы.
Соединения формулы Iе:
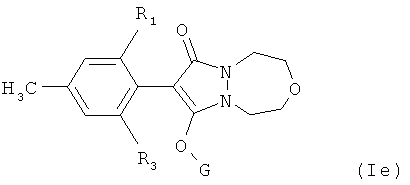


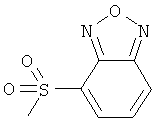


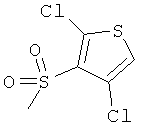
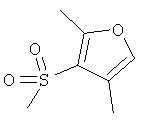
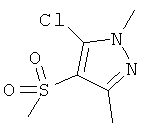
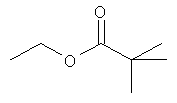
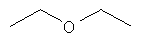
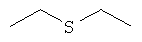
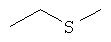
Изобретение относится также к способу избирательной борьбы с сорняками в культурах полезных растений, который предусматривает обработку полезных растений, их семян или рассады или их посевных площадей а) гербицидно эффективным количеством гербицида формулы I, б) обладающим гербицидной синергетической активностью количеством по меньшей мере одного гербицида, выбранного из классов феноксифеноксипропионовых кислот, гидроксиламинов, сульфонилмочевин, имидазолинонов, пиримидинов, триазинов, мочевин, РРО, хлорацетанилидов, феноксиуксусных кислот, триазинонов, динитроанилинов, азинонов, карбаматов, оксиацетамидов, тиолкарбаматов, азолмочевин, бензойных кислот, анилидов, нитрилов, трионов и сульфонамидов, а также из таких гербицидов, как амитрол, бенфуресат, бентазон, цинметилин, кломазон, хлопиралид, дифензокват, дитиопир, этофумесат, флурохлоридон, инданофан, изоксабен, оксазикломефон, пиридат, пиридафол, квинхлорак, квинмерак, тридифан, флампроп и глуфосинат; и необязательно в) эффективным для предотвращения вредного действия гербицида количеством антидота, выбранного из группы, включающей клохинтоцет, катион, такой как щелочной металл, щелочно-земельный металл, сульфоний или аммоний клохинтоцета, клохинтоцет-мексил, мефенпир, катион, такой как щелочной металл, щелочно-земельный металл, сульфоний или аммоний мефенпира, и мефенпир-диэтил; и/или г) добавкой, включающей масло растительного или животного происхождения, минеральное масло, его алкиловые эфиры или смеси этих масел и производных масел.
Культурные растения, которые можно защищать от вредного воздействия указанных выше гербицидов с помощью антидота, выбранного из группы, включающей клохинтоцет, катион, такой как щелочной металл, щелочно-земельный металл, сульфоний или аммоний клохинтоцета, клохинтоцет-мексил, мефенпир, катион, такой как щелочной металл, щелочно-земельный металл, сульфоний или аммоний мефенпира, и мефенпир-диэтил, предпочтительно представляют собой зерновые культуры, хлопчатник, сою, сахарную свеклу, сахарный тростник, плантационные культуры, рапс, кукурузу и рис, более предпочтительно кукурузу и злаковые культуры. Кроме того, следует понимать, что полезные культуры также могут обозначать культуры, у которых создали устойчивость к гербицидам или к определенным классам гербицидов с помощью общепринятых методов селекции или методов генной инженерии, такие, например, как IMI-кукуруза, Poast Protected-кукуруза (толерантность к сетоксидию). Liberty Link-кукуруза, В.t./Liberty Link-кукуруза, IMI/Liberty Link-кукуруза, IMI/Liberty Link /В.t.-кукуруза, Roundup Ready-кукуруза и Roundup Ready/B.t-кукуруза.
Сорняки, подлежащие уничтожению, могут представлять собой либо двудольные, либо предпочтительно однодольные сорные растения, например Avena, Agrostis, Phalaris, Lolium, Bromus, Alopecurus, Setaria, Digitaria, Brachiaria, Echinochloa, Panicum, Sorghum hal./bic., Rottboellia, Cyperus, Brachiaria, Echinochloa, Scirpus, Monochoria и Sagittaria, и двудольные сорные растения, такие как Sinapis, Chenopodium, Stellaria, Galium, Viola, Veronica, Matricaria, Papaver, Solanum, Abutilon, Sida, Xanthium, Amaranthus, Ipomoea и Chrysanthemum.
Под "посевными площадями" следует понимать участки почвы, на которые уже посажены культурные растения или их семена, а также площади, предназначенные для посадки этих культурных растений.
В зависимости от конечной цели антидот по изобретению можно использовать для предварительной обработки семян культурного растения (протравливание семян или обработка рассады), или он может быть внесен в почву до или после посева. Кроме того, он может быть внесен отдельно или вместе с гербицидом и масляной добавкой после всхода растений. Следовательно, обработку растений или семян антидотом в принципе можно осуществлять независимо от времени обработки гербицидом. Однако растение также можно обрабатывать путем одновременного внесения гербицида, масляной добавки и антидота (например, в виде баковой смеси (смеси, приготовленной в одном резервуаре)). Нормы расхода антидота относительно гербицида прежде всего зависят от типа обработки. Для обработки культур в незащищенном грунте, которую проводят либо с использованием смеси, приготовленной в резервуаре, в которую входит комбинация антидота и гербицида, либо путем раздельного внесения антидота и гербицида, соотношение между гербицидом и антидотом, как правило, составляет от 100:1 до 1:10, предпочтительно от 20:1 до 1:1. Для обработки культур в незащищенном грунте, как правило, вносят от 0,001 до 1,0 кг/га, предпочтительно от 0,001 до 0,25 кг антидота/га.
Норма расхода гербицида, как правило, составляет от 0,001 до 2 кг/га, но предпочтительно от 0,005 до 1 кг/га.
В композиции по изобретению массовое соотношение соединения формулы I и второго гербицида составляет от 1:100 до 1000:1.
В композиции по изобретению количество масляной добавки, как правило, составляет от 0,01 до 2% в пересчете на массу смеси для опрыскивания. Масляную добавку можно, например, вводить в резервуар для опрыскивания в требуемой концентрации после приготовления смеси для опрыскивания.
Предпочтительные масляные добавки представляют собой минеральные масла или масла растительного происхождения, такие, например, как рапсовое масло, оливковое масло или подсолнечное масло, алкиловые эфиры масла растительного происхождения, такие, например, как метильные производные, или масло животного происхождения, такое как рыбий жир или говяжий маргарин.
Особенно предпочтительные масляные добавки представляют собой алкиловые эфиры высших жирных кислот (C8-C22), прежде всего метиловые производные жирных С12-С18кислот, например, метиловые эфиры лауриновой кислоты, пальмитиновой кислоты и олеиновой кислоты. Эти эфиры известны как метиллаурат (CAS-111-82-0), метилпальмитат (CAS-112-39-0) и метилолеат (CAS-112-62-9).
Применение и действие масляных добавок можно улучшать, объединяя их с поверхностно-активными веществами, такими как неионогенные, анионогенные или катионогенные поверхностно-активные вещества. Примеры приемлемых анионогенных, неионогенных и катионогенных поверхностно-активных веществ приведены в WO 97/34485 на стр.7 и 8.
Предпочтительными поверхностно-активными веществами являются анионогенные поверхностно-активные вещества типа додецилбензолсульфонатов, особенно их кальциевые соли, а также неионогенные поверхностно-активные вещества типа этоксилатов жирного спирта. Особенно предпочтительными являются этоксилированные жирные С12-С22спирты, имеющие степень этоксилирования от 5 до 40. Примерами имеющихся в продаже предпочтительных поверхностно-активных веществ являются вещества, относящиеся к типам Genapol (Clariant AG, Муттенз, Швейцария).
Концентрация поверхностно-активных веществ в пересчете на общую массу добавки обычно составляет от 1 до 30 мас.%.
Примерами масляных добавок, представляющих собой смеси масел или минеральных масел или их производных с поверхностно-активными веществами, являются Edenor ME SU®, Emery 2231® (Henkel Tochtergesellschaft Cognis GMBH, Германия, Turbocharge® (Zeneca Agro, Stoney Creek, Ontario, Канада) или наиболее предпочтительно Actipron® (BP Oil UK Limited, Великобритания).
Введение органического растворителя в смесь масляной добавки/поверхностно-активного вещества может также дополнительно усилить ее действие. Приемлемыми растворителями являются, например, растворители типа Solvesso® (ESSO) или Aromatic Solvent® (Exxon Corporation).
Концентрация этих растворителей может составлять от 10 до 80% в пересчете на общую массу.
Такие масляные добавки, которые также описаны, например, в US-A-4834908, являются особенно предпочтительными для композиции по изобретению. Особенно предпочтительная масляная добавка, известная под названием MERGE®, может быть получена от фирмы BASF Corporation, и она в целом описана, например, в US-A-4834908 в колонке 5 в качестве примера СОС-1. Еще одной масляной добавкой, которая является предпочтительной согласно изобретению, является SCORE® (Novartis Crop Protection Canada.)
Обработку с помощью предлагаемой композиции можно осуществлять всеми приемлемыми методами, например, применять на предвсходовой стадии, послевсходовой стадии и для протравливания семенного материала.
Для протравливания семян, как правило, используют от 0,001 до 10 г антидота/кг семян, предпочтительно от 0,05 до 6 г антидота/кг семян. Если антидот применяют в жидкой форме незадолго до времени посева, то для более эффективного всасывания целесообразно применять растворы антидота, содержащие действующее вещество в концентрации от 1 до 10000 част./млн, предпочтительно от 100 до 1000 част./млн.
Для обработки предпочтительно использовать антидоты по изобретению или комбинации этих антидотов с гербицидами формулы I и масляными добавками вместе с вспомогательными веществами, обычно применяемыми в технологии приготовления препаративных форм, например, с получением эмульгирующихся концентратов, покрывных паст, готовых к применению распыляемых или разбавляемых растворов, разбавленных эмульсий, смачивающихся порошков, растворимых порошков, дустов, гранул или микрокапсулированных препаратов.
Такие композиции описаны, например, в WO 97/34485 на стр.9-13. Композиции готовят обычным методом, например, путем гомогенного смешения и/или измельчения действующих веществ совместно с жидкими или твердыми вспомогательными веществами, например, с растворителями или твердыми носителями. Кроме того, для получения композиций могут дополнительно использоваться поверхностно-активные вещества (ПАВ). Растворители и твердые носители, которые можно применять для этой цели, указаны, например, в WO 97/ 34485 на стр.6.
В зависимости от природы действующего вещества формулы I, входящего в состав композиции, пригодными поверхностно-активными веществами являются неионогенные, катионогенные и/или анионогенные поверхностно-активные вещества, а также смеси поверхностно-активных веществ, обладающие высокими эмульгирующими, диспергирующими и смачивающими свойствами. Примеры пригодных для применения анионогенных, неионогенных и катионогенных поверхностно-активных веществ описаны, например, в WO 97/34485 на стр.7 и 8. Кроме того, для приготовления гербицидных композиций по изобретению также можно применять поверхностно-активные вещества, которые обычно применяют для приготовления препаративных форм, которые, в частности, описаны в: "Mc Cutcheon's Detergents and Emulsifiers Annual" MC Publishing Corp., Ridgewood New Jersey, 1981, Stache, H., "Tensid-Taschenbuch", Carl Hanser Verlag, Munich/Vienna, 1981 и у М. и J. Ash, "Encyclopedia of Surfactants", том I-III, Chemical Publishing Co., New York, 1980-81.
Гербицидные композиции обычно содержат от 0,1 до 99 мас.%, в частности, от 0,1 до 95 мас.% смеси действующих веществ, включающей соединение формулы I, второй обладающий синергетической активностью гербицид и необязательно антидот по изобретению, от 0 до 2 мас.% масляной добавки по изобретению и от 1 до 99,9 мас.%, твердого или жидкого вспомогательного вещества для препаративной формы и от 0 до 25 мас.%, предпочтительно от 0,1 до 25 мас.% поверхностно-активного вещества. Несмотря на то, что в качестве поставляемых в продажу композиций наиболее предпочтительны концентрированные составы, конечный потребитель, как правило, использует разбавленные композиции.
Композиции могут также содержать другие добавки, такие как стабилизаторы, например, при необходимости эпоксидированные растительные масла (эпоксидированное кокосовое масло, рапсовое масло или соевое масло); антивспениватели, например, силиконовое масло; консерванты; регуляторы вязкости; связующие вещества; прилипатели, а также удобрения или другие действующие вещества. Для внесения антидотов по изобретению или содержащих их композиций для защиты культурных растений от нежелательных воздействий гербицидов формулы I можно применять различные методы и технологии, например, описанные ниже методы:
I) Протравливание семян
а) Протравливание семян композицией в виде смачивающегося порошка, содержащей в качестве действующего вещества антидот по изобретению, путем встряхивания в сосуде до тех пор, пока он не распределится равномерно по поверхности семян (сухая обработка). С этой целью для обработки 100 кг семян используют от 1 до 500 г применяемых в качестве действующего вещества антидотов (от 4 г до 2 кг смачивающегося порошка).
б) Протравливание семян эмульгирующимся концентратом антидотов по изобретению в соответствии с методом а) (влажная обработка).
в) Протравливание путем погружения семян в смесь, содержащую 100-1000 част./млн антидотов по изобретению на 1-72 часа, оставляя их влажными или подвергая их далее сушке (замачивание семян).
Протравливание семян или обработка проросшей рассады, как очевидно, являются предпочтительными методами обработки, так как обработка действующим веществом полностью сконцентрирована на целевой культуре. Обычно применяют от 1 до 1000 г антидота, предпочтительно от 5 до 250 г антидота на 100 кг семян, однако в зависимости от применяемого метода, который также дает возможность использовать другие действующие вещества или микроэлементы, возможны отклонения от указанных предельных концентраций как в большую, так и в меньшую сторону (кратность пропитки).
II) Внесение в виде смеси, приготовленной в резервуаре (баковой смеси)
Применяют жидкую композицию смеси антидота и гербицида (взаимное соотношение от 20:1 до 1:100), норма расхода гербицида составляет от 0,005 до 5,0 кг/га. В смесь в резервуаре можно добавлять масляную добавку предпочтительно в количестве от 0,01 до 2 мас.%. Эти приготовленные в одном резервуаре смеси вносят до или после посева.
III) Внесение в борозду
Антидот в виде эмульгирующегося концентрата, смачивающегося порошка или гранул вносят в открытую борозду, в которую были высеяны семена. После закрытия борозды гербицид, необязательно в сочетании с масляной добавкой, применяют обычным методом на предвсходовой стадии.
IV) Контролируемое высвобождение действующего вещества
Антидот наносят в растворе на минеральные гранулированные субстраты или на полимеризованные грануляты (мочевина/формальдегид) и дают высохнуть. При необходимости на гранулы можно нанести покрытие (гранулы с покрытием), благодаря чему обеспечивается контролируемое высвобождение действующего вещества в течение определенного периода времени.
Предпочтительные композиции имеют, в частности, следующий состав: (% обозначает мас.%; «смесь действующих веществ» обозначает смесь соединения формулы I с обладающим синергетической активностью вторым гербицидом и необязательно с антидотами по изобретению и/или масляными добавками).
Эмульгирующиеся концентраты:
смесь действующих веществ: от 1 до 90%, предпочтительно от 5 до 20%
поверхностно-активное вещество: от 1 до 30%, предпочтительно от 10 до 20%
жидкий носитель: от 5 до 94%, предпочтительно от 70 до 85%
Дусты:
смесь действующих веществ: от 0,1 до 10%, предпочтительно от 0,1 до 5%
твердый носитель: от 99,9 до 90%, предпочтительно от 99,9 до 99%
Суспензионные концентраты:
смесь действующих веществ: от 5 до 75%, предпочтительно от 10 до 50%
вода: от 94 до 24%, предпочтительно от 88 до 30%
поверхностно-активное вещество: от 1 до 40%, предпочтительно от 2 до 30%
Смачивающиеся порошки:
смесь действующих веществ: от 0,5 до 90%, предпочтительно от 1 до 80%
поверхностно-активное вещество: от 0,5 до 20%, предпочтительно от 1 до 15%
твердый носитель: от 5 до 95%, предпочтительно от 15 до 90%
Гранулы:
смесь действующих веществ: от 0,1 до 30%, предпочтительно от 0,1 до 15%
твердый носитель: от 99,5 до 70%, предпочтительно от 97 до 85%.
Ниже изобретение более подробно проиллюстрировано на примерах, не ограничивающих его объем.
Примеры композиций на основе смесей гербицидов и при необходимости антидотов и масляной добавки (% обозначает мас.%)
Действующие вещества тщательно смешивают с адъювантами и эту смесь измельчают в пригодной мельнице, получая смачивающиеся порошки, которые могут быть разбавлены водой до получения суспензий любой требуемой концентрации.
Действующее вещество растворяют в метиленхлориде, раствор распыляют на носитель и затем растворитель удаляют под вакуумом.
Тонкоизмельченное действующее вещество равномерно подают в смеситель к носителю, увлажненному полиэтиленгликолем, получая беспылевые гранулы с покрытием.
Действующее вещество смешивают с адъювантами и смесь размалывают, увлажняют водой, экструдируют и затем сушат в потоке воздуха.
Готовые к применению дусты получают путем смешения действующих веществ с носителями и измельчения смеси в пригодной мельнице.
Тонкоизмельченное действующее вещество равномерно смешивают с адъювантами, получая суспензионный концентрат, из которого суспензии любой требуемой концентрации могут быть получены путем разбавления водой.
Часто более предпочтительно изготавливать отдельные препаративные формы на основе гербицидов (необязательно в сочетании с масляной добавкой) и на основе антидотов и смешивать их в воде непосредственно перед внесением в машину для внесения ядохимикатов в нужном соотношении компонентов смеси в виде "баковой смеси" (смеси, приготовленной в одном резервуаре). На основе гербицидов и антидотов можно готовить различные препаративные формы и непосредственно перед применением вносить вместе в машину для внесения ядохимикатов в нужном соотношении компонентов смеси в виде "баковой смеси" (смеси, приготовленной в резервуаре) в воде, после чего вносить масляную добавку.
Эффективность композиций по изобретению в качестве гербицидов избирательного действия проиллюстрирована в следующих примерах.
Биологические примеры
Пример В1: Опыт по определению эффективности на послевсходовой стадии развития растений
Опытные растения выращивают в условиях теплицы в горшках до появления всходов. В качестве субстрата для выращивания используют стандартную почву. На послевсходовой стадии опытные растения или культурные растения, выращенные из семян, протравленных антидотом, обрабатывают либо только гербицидами, либо смесью гербицидов с антидотами и/или масляными добавками. Обработку осуществляют с использованием эмульсии (полученной из эмульгирующегося концентрата (пример F1, в)) тестируемых соединений. Нормы расхода зависят от оптимальных доз, определенных в незащищенном грунте и в условиях теплицы. Эффективность обработки оценивают через 2-4 недели после начала опытов (за 100% принимают полную деструкцию, за 0% - отсутствие фитотоксичного действия).
В качестве масляной добавки используют ACTIPRON® в концентрации 0,5% в пересчете на массу смеси для опрыскивания.
Послевсходовое гербицидное действие в отношении Alopecurus
Из этих опытов видно, что при использовании в качестве гербицида клодинафоп-пропаргила в сочетании с антидотом клохинтоцет-мексилом и масляной добавкой ACTIPRON® достигается только 40%-ный уровень гербицидной активности в отношении Alopecurus при общей норме расхода гербицида/антидота 40 г/га. При применении соединения формулы I (nо. 1.007) в сочетании с антидотом клохинтоцет-мексилом и масляной добавкой ACTIPRON® гербицидное действие в отношении Alopecurus вообще не обнаружено при использовании 4 изученных норм расхода, и обнаружено только 40%-ное действие при использовании наиболее высокой нормы расхода (125+31,25 г/га). Однако при создании изобретения неожиданно установлено, что композиция по изобретению, включающая гербицид формулы I (nо. 1.007) в сочетании с клодинафоп-пропаргилом, антидотом клохинтоцет-мексилом и масляной добавкой ACTIPRON® приводит к практически полному уничтожению Alopecurus при использовании всех изученных норм расхода (эффективность на уровне 92-99%).
Аналогичное действие выявлено, когда в качестве масляной добавки вместо ACTIPRON® используют масляную добавку MERGE®.
Пример В2: Опыт по определению эффективности на послевсходовой стадии развития растений:
Опытные растения выращивают в условиях теплицы в горшках до появления всходов. В качестве субстрата для выращивания используют стандартную почву. На послевсходовой стадии опытные растения или культурные растения, выращенные из семян, протравленных антидотом, обрабатывают либо только гербицидами, либо смесью гербицидов с антидотами и/или масляными добавками. Обработку осуществляют с использованием эмульсии (полученной из эмульгирующегося концентрата (пример F1, в)) тестируемых соединений. Нормы расхода зависят от оптимальных доз, определенных в незащищенном грунте и в условиях теплицы. Эффективность обработки оценивают через 2-4 недели после начала опытов (за 100% принимают полную деструкцию, за 0% - отсутствие фитотоксичного действия).
В качестве масляной добавки используют MERGE® в концентрации 0,7% в пересчете на массу смеси для опрыскивания.



Послевсходовая гербицидная активность в отношении сорняков в посевах пшеницы, согербицид: тралкоксидим:
соединение 1.008 (30 г/га + клохинтоцет-мексил (8 г/га) + MERGE + тралкоксидим (125 г/га)
0
98
98
100
98
Из таблиц В2.1-В2.4 можно сделать заключение, что введение масляной добавки MERGE® в смесь, включающую два гербицида и один антидот, неожиданно повышает гербицидное действие в отношении сорняков, не оказывая вредное воздействие на культурные растения.
Тест 1
Исследуемые семена выращивали в теплице в 10 см горшочках на стандартной почве при соотношении приблизительно 30 растений травы или от 3 до 6 широколистных растений на горшочек до стадии 2-3 листьев.
Соединение А формулы
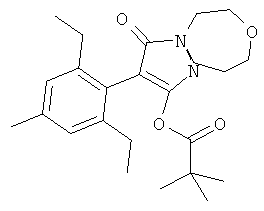
наносилось в количестве 7,5, 15 и 30 г действующего вещества на га концентрата эмульсии в 3 повторах на исследуемые виды. Каждая смесь гербицидов наносилась в дозе между 5 и 800 г действующего вещества на га в виде одного повтора на исследуемое растение. Обработку, растворение RO в воде (деионизированная посредством обратных осмотических способов) осуществляли с помощью спрея объемом 200 л/га. Обрабатывают листву трав и широколистных сорняков с использованием гусеничного спрея с одним калиброванным наконечником с плоским факелом распыла (11002VS), который обычно используется для нанесения гербицидов. После распыления растения помещали в холодную тепличную нишу с температурой 12/16°С. Визуальную оценку % гербицидного эффекта осуществляли спустя 21 день после обработки (0 = отсутствие эффекта и 100 = общая гибель). Данные для одного соединения А, которые охватывают более 3 повторов, представлены в таблице с результатами. После оценки наблюдаемые результаты были сравнены с ожидаемыми результатами с помощью метода "Colby". Для определения синергетического эффекта использовали формулу: "Ожидаемый" результат для (а+б)-(аб/100), где а и б являются наблюдаемыми результатами для а и б (Colby 1967).
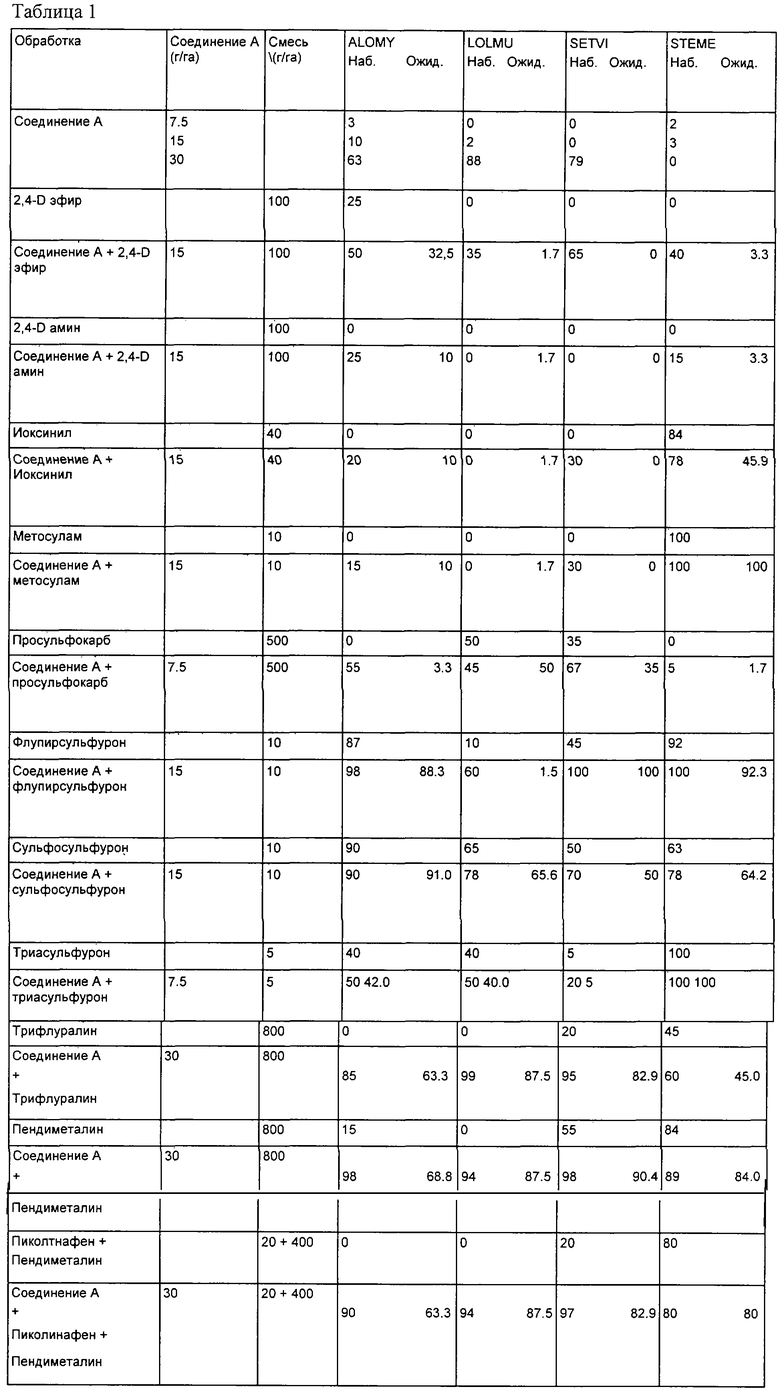
Эти данные суммированы в табл.1 [ALOMY (Alopecurus myosuroides), LOLMU (Lolium muliflorum), SETVI (Setaria viridis), STEME (Stellaria media). Наблюдаемые результаты (таблица 1) превышали ожидаемые результаты по Колби, а значит, наблюдается синергетический эффект.
Тест 2
Исследуемые семена выращивали в теплице в 10 см горшочках на стандартной почве при соотношении приблизительно 30 растений травы или от 3 до 6 широколистных растений на горшочек до стадии 2-3 листьев.
Соединение А формулы
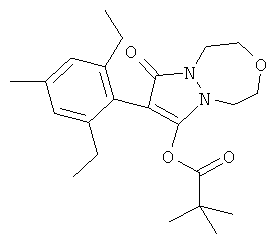
наносилось в количестве 7,5 и 15 г действующего вещества на га концентрата эмульсии в 3 повторах на исследуемые виды. Каждая смесь гербицидов наносилась в дозе между 5 и 400 г действующего вещества на га в виде одного повтора на исследуемое растение. Обработку, растворение RO в воде (деионизированная посредством обратных осмотических способов) осуществляли с помощью спрея объемом 200 л/га. Обрабатывают листву трав и широколистных сорняков с использованием гусеничного спрея с одним калиброванным наконечником с плоским факелом распыла (11002VS), который обычно используется для нанесения гербицидов. После распыления растения помещали в холодную тепличную нишу с температурой 12/16°С. Визуальную оценку % гербицидного эффекта осуществляли спустя 21 день после обработки (0 = отсутствие эффекта и 100 = общая гибель). Данные для одного соединения А, которые охватывают более 3 повторов, представлены в таблице с результатами.
После оценки наблюдаемые результаты были сравнены с ожидаемыми результатами с помощью метода "Colby". Для определения синергетического эффекта использовали формулу: "Ожидаемый" результат для (а+б)-(аб/100), где а и б являются наблюдаемыми результатами для а и б (Colby 1967).
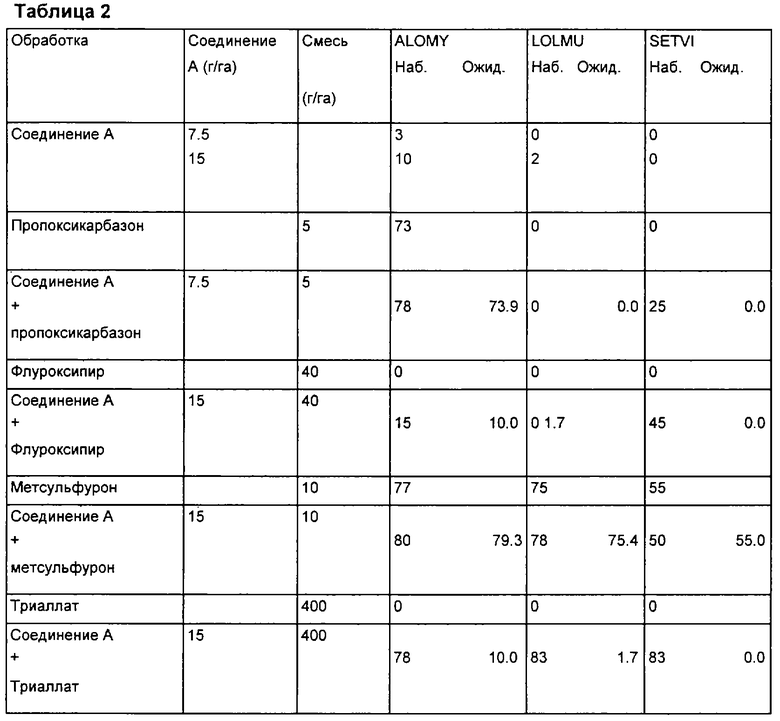
Эти данные суммированы в табл.2 [ALOMY (Alopecurus myosuroides), LOLMU (Lolium muliflorum), SETVI (Setaria viridis). Наблюдаемые результаты (таблица 2) превышали ожидаемые результаты по Колби, а значит, наблюдается синергетический эффект.
Тест 3
Исследуемые семена выращивали в теплице в 10 см. горшочках на стандартной почве при соотношении приблизительно 30 растений травы или от 3 до 6 широколистных растений на горшочек до стадии 2-3 листьев.
Соединение А формулы

наносилось в количестве 7,5, 15 и 30 г действующего вещества на га концентрата эмульсии в 3 повторах на исследуемые виды. Каждая смесь гербицидов наносилась в дозе между 5 и 100 г действующего вещества на га в виде одного повтора на исследуемое растение. Обработку, растворение RO в воде (деионизированная посредством обратных осмотических способов) осуществляли с помощью спрея объемом 200 л/га. Обрабатывают листву четырех трав и четырех широколистных сорняков с использованием гусеничного спрея с одним калиброванным наконечником с плоским факелом распыла (11002VS), который обычно используется для нанесения гербицидов. После распыления растения помещали в холодную тепличную нишу с температурой 12/16°С. Визуальную оценку % гербицидного эффекта осуществляли спустя 22 дня после обработки (0 = отсутствие эффекта и 100 = общая гибель). Данные для одного соединения А, которые охватывают более 3 повторов, представлены в таблице с результатами.
После оценки наблюдаемые результаты были сравнены с ожидаемыми результатами помощью метода "Colby". Для определения синергетического эффекта использовали формулу: "Ожидаемый" результат для (а+б)-(аб/100), где а и б являются наблюдаемыми результатами для а и б (Colby 1967).
Эти данные суммированы в табл.3 [ALOMY (Alopecurus myosuroides), LOLMU (Lolium muliflorum), SETVI (Setaria viridis)]. Наблюдаемые результаты превышали ожидаемые результаты по Колби, а значит, наблюдается синергетический эффект.
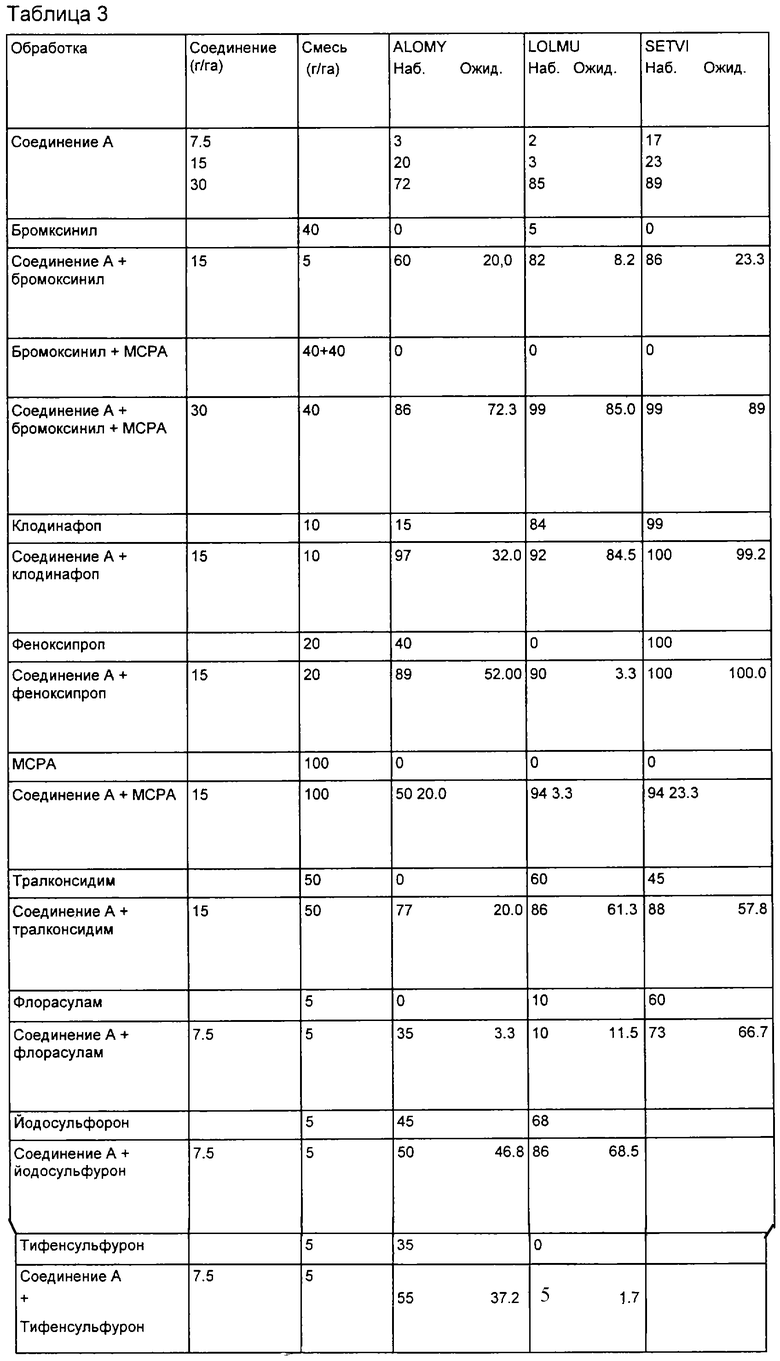
Тест 4
Исследуемые семена выращивали в теплице в 10 см. горшочках на стандартной почве при соотношении приблизительно 30 растений травы или от 3 до 6 широколистных растений на горшочек до стадии 2-3 листьев.
Соединение А формулы
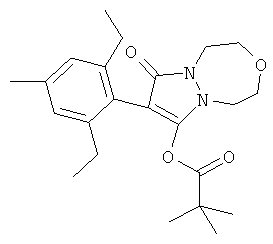
наносилось в количестве 7,5 и 15 г действующего вещества на га концентрата эмульсии в 3 повторах на исследуемые виды. Каждая смесь гербицидов наносилась в дозе между 5 и 100 г действующего вещества на га в виде одного повтора на исследуемое растение. Обработку, растворение RO в воде (деионизированная посредством обратных осмотических способов) осуществляли с помощью спрея объемом 200 л/га. Обрабатывают листву четырех трав и четырех широколистных сорняков с использованием гусеничного спрея с одним калиброванным наконечником с плоским факелом распыла.
После распыления растения помещали в холодную тепличную нишу с температурой 12/16°С. Визуальную оценку % гербицидного эффекта осуществляли спустя 22 дня после обработки (0 = отсутствие эффекта и 100 = общая гибель). Данные для одного соединения А, которые охватывают более 3 повторов, представлены в таблице с результатами.
После оценки наблюдаемые результаты были сравнены с ожидаемыми результатами с помощью метода "Colby". Для определения синергетического эффекта использовали формулу: "Ожидаемый" результат для (а+б)-(аб/100), где а и б являются наблюдаемыми результатами для а и б (Colby 1967).
Эти данные суммированы в табл.4 [Amaranthus retroflexus), VERPE (Veronica persica)]. Наблюдаемые результаты превышали ожидаемые результаты по Колби, а значит, наблюдается синергетический эффект.
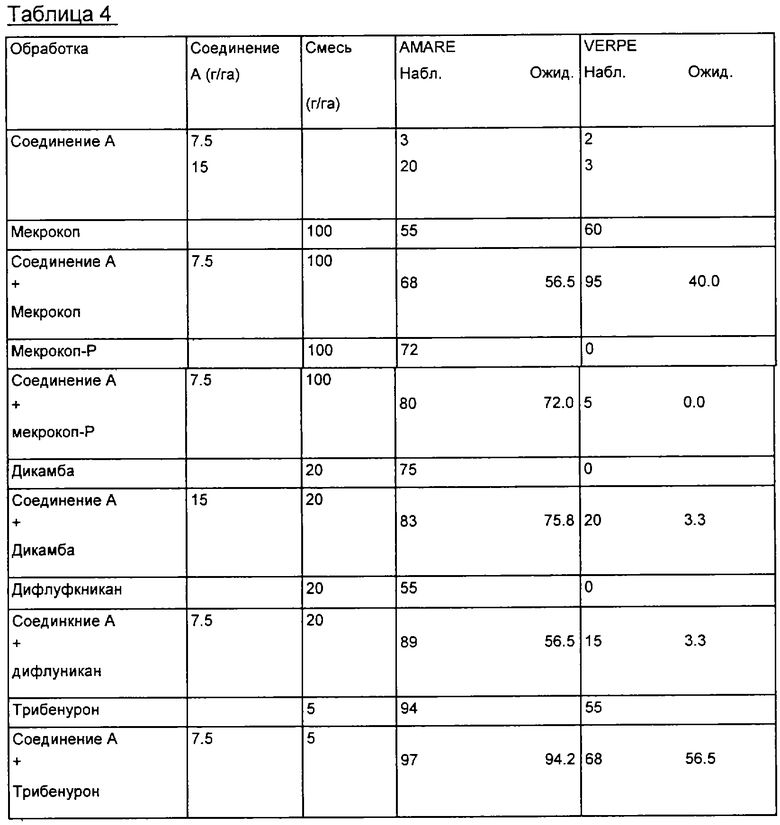
Тест 5
Исследуемые семена выращивали в теплице в 10 см горшочках на стандартной почве при соотношении приблизительно 30 растений травы на 1 горшочек или от 3 до б широколистных растений до стадии 2-3 листьев.
Соединение А формулы
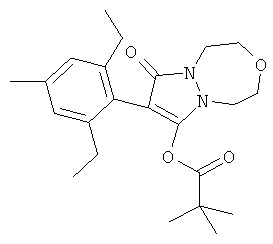
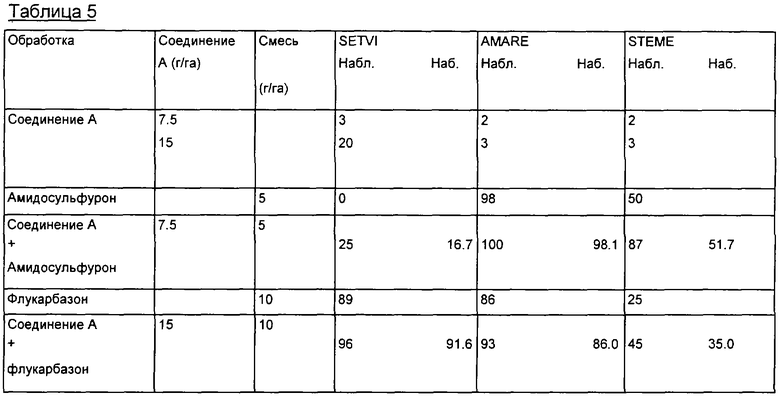
наносилось в количестве 7,5 на 15 г действующего вещества на га концентрата эмульсии в 3 повторах на исследуемые виды. Каждая смесь гербицидов наносилась в дозе между 5 и 100 г действующего вещества на га в виде одного повтора на исследуемое растение. Обработку, растворение RO в воде (деионизированная посредством обратных осмотических способов) осуществляли с помощью спрея объемом 200 л/га. Обрабатывают листву 4 трав и 4 широколистных сорняков с использованием гусеничного спрея с одним калиброванным наконечником с плоским факелом распыла. После распыления растения помещали в холодную тепличную нишу с температурой 12/16°С. Визуальную оценку % гербицидного эффекта осуществляли спустя 22 дня после обработки (0 = отсутствие эффекта и 100 = общая гибель). Данные для соединения А охватывают более 3 повторов, значения представлены в таблице с результатами. После оценки наблюдаемые результаты были сравнены с ожидаемыми результатами с помощью метода "Colby". Для определения синергетического эффекта использовали формулу: "Ожидаемый" результат для (а+б)-(аб/100), где а и б являются наблюдаемыми результатами для а и б (Colby 1967).
Эти данные суммированы в табл.5 [AMARE (Amaranthus retroflexus), VERPE (Veronica persica)]. Полученные результаты превышали ожидаемые результаты по Колби, а значит, наблюдается синергетический эффект.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ, СПОСОБ БОРЬБЫ С СОРНЫМИ И ТРАВЯНИСТЫМИ РАСТЕНИЯМИ | 2000 |
|
RU2262846C2 |
| ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ ИЗБИРАТЕЛЬНОГО ДЕЙСТВИЯ, СПОСОБ ИЗБИРАТЕЛЬНОЙ БОРЬБЫ С СОРНЫМИ И ТРАВЯНИСТЫМИ РАСТЕНИЯМИ | 2000 |
|
RU2249352C2 |
| КОМПОЗИЦИЯ ДЛЯ ОТПУГИВАНИЯ ПАРАЗИТОВ | 1999 |
|
RU2234219C2 |
| ПИРАЗОЛКАРБОКСАМИДНЫЕ И ПИРАЗОЛТИОАМИДНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ФУНГИЦИДОВ | 2000 |
|
RU2259356C2 |
| КОМПОЗИЦИЯ ДЛЯ ОТПУГИВАНИЯ ПАРАЗИТОВ | 1999 |
|
RU2226054C2 |
| ЦИКЛИЧЕСКИЕ ДИОНЫ В КАЧЕСТВЕ ГЕРБИЦИДНЫХ СОЕДИНЕНИЙ | 2020 |
|
RU2822391C2 |
| ГЕРБИЦИДНЫЕ СОЕДИНЕНИЯ | 2020 |
|
RU2839723C2 |
| ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С РОСТОМ НЕЖЕЛАТЕЛЬНОЙ РАСТИТЕЛЬНОСТИ | 2002 |
|
RU2276844C2 |
| ГЕРБИЦИДНЫЕ ЦИКЛОГЕКСАНДИОНОВЫЕ ПРОИЗВОДНЫЕ | 2020 |
|
RU2830286C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛИЧЕСКИХ ДИКЕТОНОВ | 2003 |
|
RU2316544C2 |
Описывается гербицидная композиция, которая помимо общепринятых инертных вспомогательных веществ содержит в качестве действующего вещества смесь, включающую а) гербицидно эффективное количество соединения формулы (I)

где R1 и R3 каждый независимо друг от друга обозначает C1-C4 алкил, R4 и R5 вместе обозначают группу -C-R6(R7)-O-C-R8(R9)-C-R10(R11)-C-R12(R13)-(Z1), -С-R14(R15)-C-R16(R17)-O-C-R18(R19)-C-R20(R21)-(Z2) или -C-R22(R23)-C-R24(R25)-C-R26(R27)-O-С-R28(R29)-(Z3), где R6-R29 каждый обозначает водород, G обозначает водород и -С(Х1)-R30, Х1 обозначает кислород, R30 обозначает C1-С10-алкил, б) обладающее гербицидной синергетической активностью количество по меньшей мере одного гербицида, выбранного из классов сульфонилмочевин, феноксиуксусных кислот, а также из таких гербицидов, как флорсулам, тралкоксидим, клодинафоп-пропаргил, феноксапроп-Р-этил, трифлурамин, пендиметалин, пиколинафен, пропоксикарбазон, флукарбазон, флуроксипир, триаллат, дифлуфеникан, метосулам, просульфокарб, иоксинил, бромоксинил. Композиция дополнительно может содержать эффективное для предотвращения вредного действия гербицида количество защитного агента - клохинтоцет-мексила и добавку, включающую минеральное масло или алкиловые эфиры C8-C22 жирной кислоты в количестве 0-2 мас.%. Описывается способ избирательной борьбы с сорными и травянистыми растениями в посевах культурных растений путем обработки культурных растений, их семян или рассады или мест их произрастания указанной композицией. Технический результат - повышение гербицидного действия в отношении сорняков. 2 н. и 3 з.п. ф-лы, 11 табл.
1. Гербицидная композиция, которая помимо общепринятых инертных вспомогательных веществ для композиций содержит в качестве действующего вещества смесь, включающую
а) гербицидно эффективное количество соединения формулы I

где
R1 и R3 каждый обозначает С1-С4алкил, R4 и R5 вместе обозначают группу
-C-R6(R7)-O-C-R8(R9)-C-R10(R11)-C-R12(R13)-(Z1),
-C-R14(R15)-C-R16(R17)-O-C-R18(R19)-C-R20(R21)-(Z2) или
-C-R22(R23)-C-R24(R25)-C-R26(R27)-O-C-R28(R29)-(Z3),
где R6, R7, R8, R9, R10, R11, R12, R13, R14, R15, R16, R17, R18, R19, R20, R21, R22, R23, R24, R25, R26, R27, R28 и R29 каждый обозначает водород;
G обозначает водород и -С(Х1)-R30;
X1 обозначает кислород;
R30 обозначает C1-С10алкил,
б) обладающее гербицидной синергетической активностью количество по меньшей мере одного гербицида, выбранного из классов сульфонилмочевин, феноксиуксусных кислот, а также из таких гербицидов, как флорсулам, тралкоксидим, клодинафоп-пропаргил, феноксапроп-Р-этил, трифлурамин, пендиметалин, пиколинафен, пропоксикарбазон, флукарбазон, флуроксипир, триаллат, дифлуфеникан, метосулам, просульфокарб, иоксинил, бромоксинил.
2. Композиция по п.1, которая дополнительно содержит эффективное для предотвращения вредного действия гербицида количество защитного агента (антидота), представляющего собой клохинтоцет-мексил.
3. Композиция по п.1, которая дополнительно содержит добавку, включающую минеральное масло или алкиловые эфиры C8-C22 жирной кислоты в количестве 0-2 мас.%.
4. Способ борьбы с сорными и травянистыми растениями в посевах культурных растений, который заключается в том, что культурные растения, их семена или рассаду или места их произрастания обрабатывают композицией по пп.1-3.
5. Способ по п.4, где культурные растения представляют собой злаковые культуры.
| WO 9621652 A1, 18.07.1996 | |||
| EP 508126 A1, 14.10.1992 | |||
| WO 9947525 A1, 23.09.1999 | |||
| DE 19728568 A1, 22.01.1998 | |||
| RU 2000125819 A1, 27.10.2002. |
Авторы
Даты
2005-05-10—Публикация
2000-09-05—Подача