Изобретение относится к химико-фармацевтической промышленности и может быть использовано при производстве готовых лекарственных форм инсулина человека пролонгированного действия с активностью 100 единиц на мл (далее - 100 МЕ/мл), в том числе и картриджных форм.
Известны препараты инсулина пролонгированного действия, в которых как действующее вещество использовалась субстанция свиного инсулина, как пролонгаторы ионы цинка и протаминсульфат, как изотонический агентг - лицерин, как консерванты - м-крезол и фенол, как вещество с буферной емкостью - натрий фосфорнокислый или уксуснокислый (“Современные гормональные средства”, Киев: Здоровье, 1994 год). Но такие препараты содержали большое количество вредных для здоровья человека примесей, которые вызывали нежелательные аллергические реакции и осложнения.
Более совершенными и наиболее близкими по составу к заявляемой готовой лекарственной форме инсулина пролонгированного действия являются лекарственные препараты по патенту США №5547930, 1996 года, “Кристаллы инсулина ASPВ28”, которые содержат как действующее вещество аналог субстанции инсулина ASPВ28 в количестве 3,55-4,375 г/л, как пролонгаторы - цинка хлорид в количестве 0,0323-0,0395 г/л и протаминсульфат в количестве 0,463-0,565 г/л, как изотонический агент глицерин в количестве 30-33 г/л, как консерванты - м-крезол в количестве 1,4-1,6 г/л и фенол в количестве 1,2-1,3 г/л, как агент с буферной емкостью - динатрийгидрогенфосфат в количестве 1,8-1,9 г/л и воду. К недостаткам этого медицинского препарата можно отнести большое содержание глицерина и протаминсульфата (30-33 г/л и 0,463-0,565 г/л по сравнению с 14-18 г/л и 0,238-0,318 г/л в заявляемом решении соответственно). И хотя авторы патента №5547930 не дают данных по химической стабильности препарата при хранении, но известно, что глицерин при хранении препарата увеличивает образование ковалентно прошитых димеров инсулина и дезамидоинсулинов (Fcta Pharm. Nord. 4(3), стр. 152), а протаминсульфаты способствуют образованию протамин-инсулинов, которые также относятся к высокомолекулярным соединениям и большое количество которых свидетельствует о химической нестабильности готовой лекарственной формы во времени, что, в свою очередь, приводит к увеличению частоты клинических аллергических реакций у больных диабетом. Кроме того, использование в прототипе как действующего вещества аналога субстанции инсулина ASPВ28 приводит к удлинению процесса приготовления готового лекарственного средства, потому что рост кристаллов по данным авторов патента №5547930 занимает 7 суток (по сравнению с 18-20 часами в заявляемом решении).
Задачей изобретения является создание готовой лекарственной формы инсулина человека пролонгированного действия, которая отличается химической и физической стабильностью при хранении, и обеспечение сокращения сроков ее приготовления.
Поставленная задача решается тем, что готовая лекарственная формула инсулина человека пролонгированного действия, содержащая высокоочищенную субстанцию инсулина человека, протаминсульфат, цинка хлорид, глицерин, м-крезол, фенол, динатрийгидрогенфосфат гептагидрат и воду, согласно изобретению отличается тем, что высокоочищенная субстанция инсулина человека имеет остаточную протеолитическую активность не более 0,005 абсорбционных единиц, а композиция содержит динатрийгидрогенфосфат гептагидрат или натрийдигидрогенфосфат дигидрат и дополнительно натрия хлорид и имеет рН 6,9-7,8 при следующем соотношении компонентов, г/л: высокоочищенная субстанция инсулина человека 3,214-3,928; протаминсульфат 0,238-0,318; цинка хлорид 0,014-0,0225; глицерин 14-18; м-крезол 1,4-1,6; фенол 0,5-0,7; натрийдигидрогенфосфат дигидрат 2,4-2,8 или динатрийгидрогенфосфат гептагидрат 2,0-2,3; натрий хлорид 0,15-0,3; вода - остальное.
В заявляемом решении как действующее вещество, то есть высокоочищенная субстанция инсулина человека, может быть использована полусинтетическая субстанция инсулина человека, полученная реакцией транспептидации свиного инсулина с сопутствующими родственными примесями, которая проводится в присутствии трипсина при молярном избытке ди-трет-бутилового эфира треонина, и постадийно очищенная хроматографией высокого давления, или субстанция инсулина человека, полученная по рекомбинантной технологии, причем обе субстанции инсулина человека должны характеризоваться остаточной протеолитической активностью не более 0,005 абсорбционных единиц. Как пролонгаторы в заявляемом решении могут использоваться протаминсульфат с остаточной протеолитической активностью тоже не более 0,005 абсорбционных единиц и цинка хлорид; в качестве изотонических агентов используются глицерин и натрия хлорид; консервантов - м-крезол и фенол; вещества с буферной емкостью - натрийдигидрогенфосфат дигидрат или динатрийгидрогенфосфат гептагидрат. Растворение субстанции инсулина человека и корректировка рН смеси до 6,9-7,8 реализуются известными способами с помощью НСl и NaOH соответственно.
Решение поставленной авторами задачи иллюстрируется примерами конкретного выполнения.
Пример 1.
3,571 г субстанции инсулина человека суспендировали в 150 мл воды, затем с помощью 1 М НСl рН суспензии довели до 3,1 для растворения кристаллов субстанции. 0,318 г протаминсульфата растворили в 25 мл воды и довели рН раствора до 3,1, добавляя 1 М НСl. 0,0225 г цинка хлорида добавили к раствору протаминсульфата. Потом смешали раствор субстанции инсулина человека и раствор, который содержал протаминсульфат и цинка хлорид.
После этого приготовили буферный раствор, который содержал 2,5 г натрийдигидрогенфосфата дигидрата, 1,5 г м-крезола, 0,6 г фенола, 16 г глицерина и 0,2 г натрия хлорида в объеме 800 мл и довели рН буферного раствора до 7,8, провели стерилизующую фильтрацию и профильтровали туда смесь кислых растворов субстанции инсулина человека, протаминсульфата и цинка хлорида. Полученную смесь выдерживали при перемешивании 18 часов при температуре 18°С для получения кристаллической суспензии готового лекарственного препарата. Готовый препарат разлили в асептических условиях в картриджи емкостью 1,5 и 3,0 мл. Готовый препарат проанализировали методом аналитической высокоэффективной жидкостной хроматографии (ВЭЖХ). Анализ показал практическое отсутствие инсулина в супернатанте при общем содержании инсулина 98 МЕ/мл. Содержание высокомолекулярных белков составило 0,2%. Форму и размер кристаллов определяли с помощью микроскопа при 400-кратном увеличении. Кристаллы имели тетрагональную форму и длину от 1 до 25 мкм.
Пример 2.
75% кристаллической доли лекарственной формы готовили, как в примере 1, за исключением того, что вместо натрийдигидрогенфосфата дигидрата брали динатрийгидрогенфосфат гептагидрат в количестве 2,0 г, а смесь всех компонентов выдерживали при перемешивании при такой же температуре 20 часов. 25% растворимой части лекарственной формы готовили следующим образом: 1,19 г субстанции инсулина человека суспендировали в 100 мл воды, с помощью 1 М НСl довели рН до 3,1. В 230 мл воды приготовили буферный раствор, который содержал 0,66 г динатрийгидрогенфосфата гептагидрата, 0,5 г м-крезола, 0,2 г фенола, 5,28 г глицерина и 0,066 г натрия хлорида. Буферный раствор смешали с раствором субстанции инсулина, откорректировали рН полученного раствора до 7,3 и провели стерилизующую фильтрацию в емкость с кристаллической частью готовой лекарственной формы. Смесь перемешивали в течение 1 часа и потом в асептических условиях провели разлив. Анализ готового препарата таким же методом, как в примере 1, показал общее содержание инсулина человека 97,3 МЕ/мл, содержание инсулина в супернатанте 24 МЕ/мл. Содержание высокомолекулярных белков составило 0,25%. Кристаллы имели тетрагональную форму и длину от 1 до 20 мкм.
Пример 3.
Готовое лекарственное средство получали, как в примере 1, но натрия хлорида брали 0,35 г. Общее содержание инсулина в медицинском препарате, определенное методом аналитической ВЭЖХ, составило 98 МЕ/мл, в супернатанте - 0,5 МЕ/мл. Содержание высокомолекулярных белков было 0,55%. Форма и размер кристаллов были, как в примере 1.
Пример 4.
Готовую лекарственную форму получали, как в примере 1, но натрия хлорида брали 0,1 г. Общее содержание инсулина в медицинском препарате, определенное методом аналитической ВЭЖХ, составило 96,8 МЕ/мл, в супернатанте - 0,8 МЕ/мл. Содержание высокомолекулярных белков составляло 0,6%. Форма и размер кристаллов были, как в примере 1.
Для определения химической и физической стабильности полученные образцы медицинских препаратов, которые на момент приготовления отвечали всем требованиям, предъявляемым к препаратам инсулина Европейской фармакопеей, выдерживались при температуре 4°С в течение 25 месяцев. После этого образцы были проанализированы аналитической системой ВЭЖХ на содержание высокомолекулярных соединений (ВМС). Внешний вид суспензии определялся визуально. Полученные данные сведены в таблицу, представленную ниже.
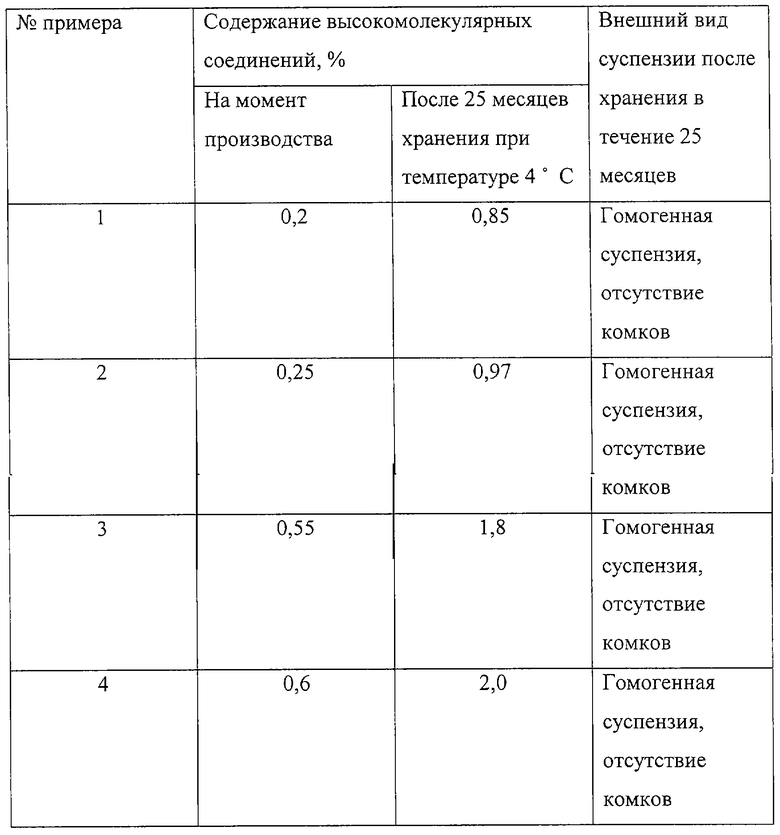
Таким образом, как видно из приведенных примеров и таблицы, химическая и физическая стабильность полученных в соответствии с изобретением образцов готовых лекарственных форм инсулина человека пролонгированного действия (примеры 1 и 2) более чем в три раза превышает данные, которые требуются Европейской фармакопеей, а их состав позволяет сократить производственный процесс более чем в семь раз.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГОТОВАЯ ЛЕКАРСТВЕННАЯ ФОРМА ИНСУЛИНА ЧЕЛОВЕКА КОРОТКОГО ДЕЙСТВИЯ | 2003 |
|
RU2252752C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ГОТОВОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ ИНСУЛИНА ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ | 2002 |
|
RU2252782C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМБИНИРОВАННОГО ПРЕПАРАТА ИНСУЛИНА ЧЕЛОВЕКА | 2002 |
|
RU2261108C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ СУСПЕНЗИИ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ НА ОСНОВЕ СУБСТАНЦИИ ГЕННО-ИНЖЕНЕРНОГО (РЕКОМБИНАНТНОГО) ИНСУЛИНА ЧЕЛОВЕКА | 2004 |
|
RU2281756C2 |
| ИНСУЛИНОВЫЕ ПРЕПАРАТЫ, СОДЕРЖАЩИЕ УГЛЕВОДЫ | 1997 |
|
RU2204411C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ СУСПЕНЗИИ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ НА ОСНОВЕ СУБСТАНЦИИ ГЕННО-ИНЖЕНЕРНОГО (РЕКОМБИНАНТНОГО) ИНСУЛИНА ЧЕЛОВЕКА | 2001 |
|
RU2185152C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ПРЕПАРАТА ПЕНСУЛИН СС СУСПЕНЗИИ ИНСУЛИНА ДЛЯ КАРТРИДЖА | 1999 |
|
RU2157698C1 |
| ПРЕПАРАТ ИНСУЛИНА, СОДЕРЖАЩИЙ NaCl, ПАРЕНТЕРАЛЬНАЯ ГОТОВАЯ ФОРМА, СПОСОБ ПОВЫШЕНИЯ ХИМИЧЕСКОЙ СТАБИЛЬНОСТИ ПРЕПАРАТА ИНСУЛИНА | 1997 |
|
RU2182015C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ГОТОВОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ ИНСУЛИНА КОРОТКОГО ДЕЙСТВИЯ | 2002 |
|
RU2261107C2 |
| КОМПЛЕКС АНАЛОГА ИНСУЛИНА И ПРОТАМИНА, СПОСОБ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ДИАБЕТА | 1995 |
|
RU2154494C2 |
Изобретение относится к химико-фармацевтической промышленности и может быть использовано в производстве готовых лекарственных форм инсулина человека пролонгированного действия. Лекарственная форма содержит высокоочищенную субстанцию инсулина человека, протаминсульфат, цинка хлорид, глицерин, м-крезол, фенол, натрийдигидрогенфосфат дигидрат или динатрийгидрогенфосфат гептагидрат, натрий хлорид и воду, имеет остаточную протеолитическую активность не более 0,005 адсорбционных единиц и рН 6,9-7,8. Технический результат - создание готовой лекарственной формы инсулина человека пролонгированного действия, которая отличается химической и физической стабильностью при хранении и обеспечивает сокращение сроков ее приготовления. 1 табл.
Готовая лекарственная форма инсулина человека пролонгированного действия, содержащая высокоочищенную субстанцию инсулина человека, протаминсульфат, цинка хлорид, глицерин, м-крезол, фенол и воду, отличающаяся тем, что высокоочищенная субстанция инсулина человека имеет остаточную протеолитическую активность не более 0,005 адсорбционных единиц, а композиция содержит натрийдигидрогенфосфат дигидрат или динатрийгидрогенфосфат гептагидрат и дополнительно натрий хлорид и имеет рН 6,9-7,8 при следующем соотношении компонентов, г/л:
высокоочищенная субстанция инсулина человека 3,214-3,928
протаминсульфат 0,238-0,318
цинка хлорид 0,014-0,0225
глицерин 14-18
м-крезол 1,4-1,6
фенол 0,5-0,7
натрийдигидрогенфосфат дигидрат 2,4-2,8
или динатрийгидрогенфосфат гептагидрат 2,0-2,3
натрия хлорид 0,15-0,3
вода остальное
| US 5547930 А, 20.08.1996 | |||
| СПОСОБ ПРИГОТОВЛЕНИЯ СУСПЕНЗИИ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ НА ОСНОВЕ СУБСТАНЦИИ ГЕННО-ИНЖЕНЕРНОГО (РЕКОМБИНАНТНОГО) ИНСУЛИНА ЧЕЛОВЕКА | 2001 |
|
RU2185152C1 |
| ПРОИЗВОДНОЕ ИНСУЛИНА, РАСТВОРИМАЯ ПРОЛОНГИРОВАННАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ПРОЛОНГИРОВАНИЯ ГИПОГЛИКЕМИЧЕСКОГО ДЕЙСТВИЯ ПРИ ЛЕЧЕНИИ ДИАБЕТА | 1994 |
|
RU2164520C2 |
| WO 9847489 A1, 29.10.1998 | |||
| KURTZ et al | |||
| Circulating IgG antibody to protamine in patients tretated with protamin-insulins | |||
| Diabetologia | |||
| Гребенчатая передача | 1916 |
|
SU1983A1 |
Авторы
Даты
2005-05-27—Публикация
2003-04-29—Подача