Область техники, к которой относится изобретение.
Данное изобретение касается применения CDP-холина для профилактического лечения церебральной ишемии.
Уровень техники.
Существует ряд факторов, участвующих в появлении и степени развития церебральных ишемических нарушений, вторичных относительно локальной ишемии. Данные факторы включают недостаток энергии и потерю гомеостаза нейромедиаторов и катионов; индукцию и нерегулируемую экспрессию ранних генов, а также мобилизацию цитокинов, которые изменяют функцию гематоэнцефалического барьера и участвуют в инфильтрации лейкоцитов; быструю гибель клеток в центральных зонах инфаркта и задержанную гибель, часто ассоциированную с апоптозом, в периферических и пограничных областях, а также индукцию или экспрессию трофических факторов и их рецепторов, которые способствуют компенсационно пластическому феномену и ангиогенезу.
Знание механизмов гибели клетки, возникшей в результате ишемии, представляет собой базовый аспект, поскольку их контроль делает возможным внешнетерапевтическое вмешательство. Генетический контроль запрограммированной гибели клетки в основном был исследован на нематоде Caenorhabditis elegans и имеет отношение к генам ced-3, ced-4 и ced-9. Каспазы, тип цистеин-зависимых протеаз млекопитающих, соответствуют ряду вариантов продукта гена ced-3 и являются важными элементами при развитии апоптоза. Каспазы различным образом включают в ряд моделей гибели клетки, и они действуют на различные базовые субстраты, определяющие выживаемость клеток, приводя к их дезинтеграции. Каспазы 1, 2, 3, 6 и 8 связаны с различными заболеваниями центральной нервной системы. В работах Т.Е. Andreoli (см. Am. J. Med., 107, 488-506, (1999)) и B.C. Albensi (см. Drug News Perspect., 12(8), 453-457, (1999)) подробно рассмотрен феномен апоптоза и роль каспаз.
В настоящее время имеется мало литературных данных относительно экспрессии каспаз после повреждения, индуцированного временной общей ишемией или фокальной ишемией. Современные исследования показали, что для каждой каспазы характерна вариабельная экспрессия в зависимости от времени действия и типов клеток. Заявителями обнаружено, что каспазы принимают участие в ишемическом эпизоде в обоих случаях - как в головном мозге человека, так и в модели фокальной ишемии на крысах, и что экспрессия каспаз, как доказано, является особенно заметной в пограничной зоне в течение первых дней после инфаркта.
CDP-холин (цитидин-дифосфат-холин, Цитиколин) является ключевым предшественником в синтезе мембранного фосфатидилхолина. В экспериментальных моделях экзогенное введение CDP-холина снижает разрушение клеточных мембран путем индукции повышения синтеза фосфатидилхолина и снижения уровней свободных жирных кислот. Показано, что лечение CDP-холином эффективно в ряде моделей ишемии или гипоксии на животных. Антиапоптотический, нейропротекторный и антиамнезический эффекты CDP-холина исследованы в экспериментах на крысах в работе Х.А. Alvarez и соавт. (см. Methods and Findings in Experimental and Clinical Pharmacology: 21(8), 535-540, (1999)). Нейропротекторный механизм CDP-холина полностью неизвестен. В настоящее время считают, что данный эффект связан со снижением уровня свободных жирных кислот, образованием свободных радикалов, стабилизацией мембран нервных клеток, снижением токсичности, индуцированной глутаматом, и повышением уровня выживаемости нервных клеток. Пока не выяснено, может ли положительный эффект CDP-холина при ишемических эпизодах быть связан со снижением уровня гибели клеток вследствие апоптоза в пограничной области после фокальной ишемии.
Неожиданно было обнаружено, что введение CDP-холина перед церебральным ишемическим эпизодом дает более сильный положительный эффект в плане профилактики тяжести последствий заболевания, чем введение CDP-холина после возникновения последствий.
Сущность изобретения.
Данное изобретение касается применения CDP-холина или его фармацевтически приемлемой соли для изготовления лекарственного средства для профилактического лечения церебральной ишемии.
Профилактическое лечение означает, что CDP-холин или его фармацевтически приемлемую соль вводят перед возможным развитием ишемического эпизода. В том случае, когда ишемический эпизод происходит, продолжение лечения является предпочтительным. В таком случае режим лечения может быть адаптирован в соответствии с нуждами пациента.
С точки зрения другого аспекта изобретение касается нейропротекторного лечения. Нейропротекция означает защиту ткани головного мозга от повреждения, в частности, от церебрального инфаркта.
Согласно другому аспекту, данное изобретение касается применения CDP-холина или его фармацевтически приемлемой соли для профилактики степени повреждения ткани головного мозга.
Согласно специфическому варианту осуществления данное изобретение касается вышеупомянутого применения, при котором повреждение ткани головного мозга и, в частности, церебральный инфаркт, связаны с церебральной ишемией.
Церебральная ишемия включает в себя церебральные ишемические события. Ишемическое событие можно определить как уменьшение кровоснабжения ткани. Церебральная ишемия может быть вызвана снижением или даже нарушением кровоснабжения из артерии, питающей головной мозг.
CDP-холин обладает ингибирующим эффектом на активацию каспазной цепи и снижает уровень апоптоза в нервных клетках в пограничной области.
Таким образом, в свете другого аспекта, данное изобретение относится к применению CDP-холина или его фармацевтически приемлемой соли для ингибирования активации каспазной цепи. Поскольку данный эффект был выше у предварительно пролеченных субъектов, то пришли к заключению, что CDP-холин вызывает профилактический нейропротекторный эффект при церебральных ишемических событиях. Вкратце, тот факт, что CDP-холин является более эффективным при введении перед ишемией, предполагает наличие предупреждающего действия на тяжесть ишемических осложнений. Наконец, профилактический способ, соответствующий данному изобретению, является значительно более эффективным, чем традиционное лечение после события.
Применение в соответствии с данным изобретением включает в себя способ профилактического лечения церебральной ишемии, предусматривающий введение нуждающемуся в этом субъекту эффективного количества CDP-холина или его фармацевтически приемлемой соли.
CDP-холин или его фармацевтически приемлемые соли или их смеси могут быть введены или необязательно совместно введены нуждающемуся в этом субъекту, обычно больному человеку, последовательно или одновременно с дополнительными терапевтическими агентами в фармацевтически приемлемой форме, например, в виде подходящих смесей с фармацевтическими носителями и/или наполнителями, в эффективном количестве, предпочтительно в суточных дозах, лежащих в интервале от 0,5 до 4 г по свободному CDP-холину, более предпочтительно от 1 до 2 г по свободному CDP-холину, как перорально, так и парентерально в зависимости от состояния пациента.
Перечень фигур чертежей и иных материалов.
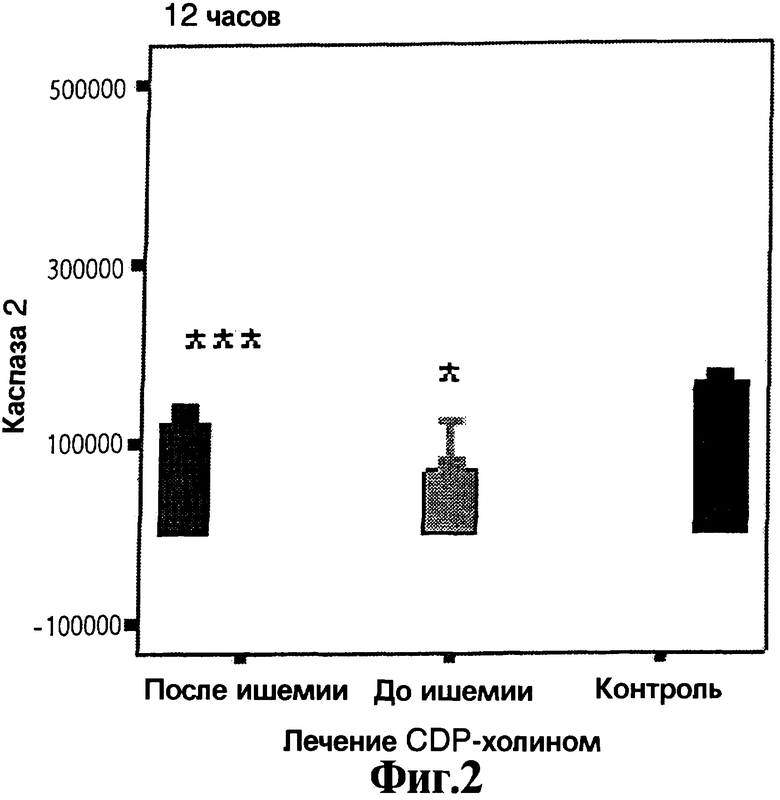
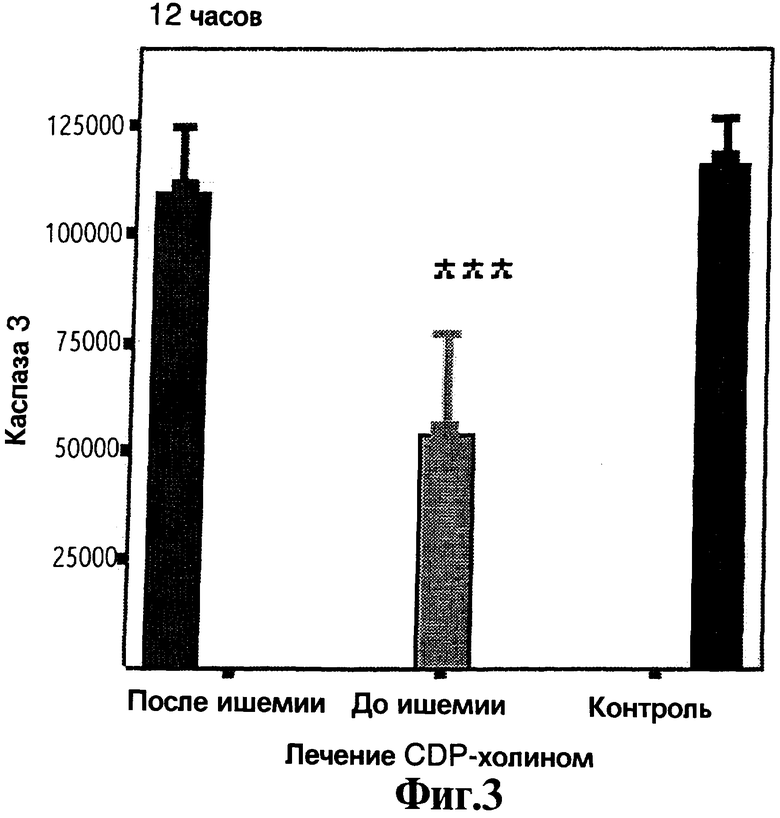
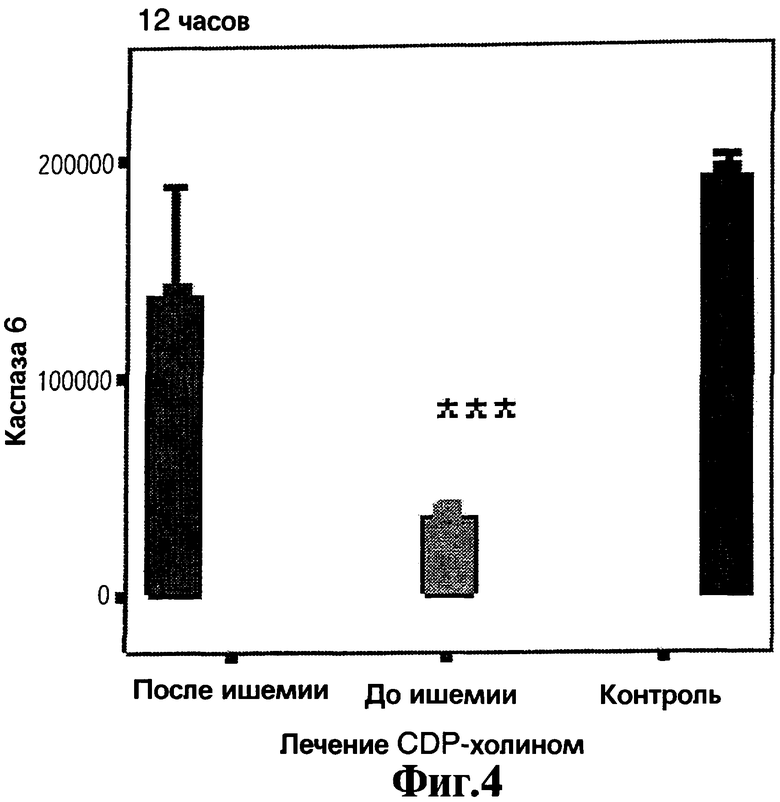
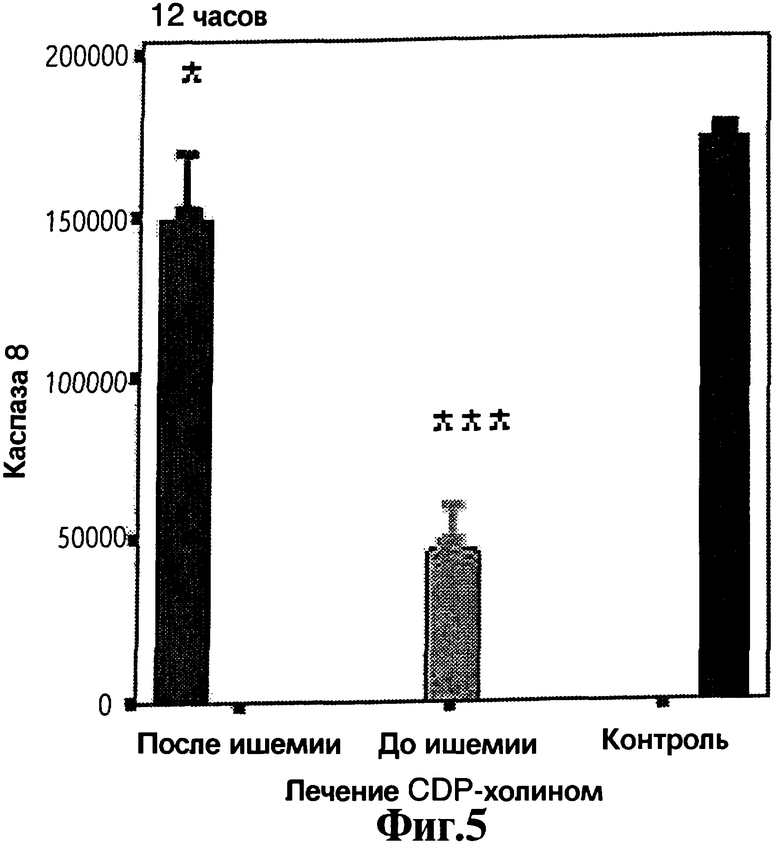
На Фигурах 1, 2, 3, 4 и 5 представлены графики в виде столбиков, отражающие средние значения измерения каспаз 1, 2, 3, 6 и 8, соответственно, в анализах с использованием иммунофлуоресценции. Доверительный интервал составляет 95% и статистическая значимость относительно контроля равна *р<0,05, **р<0,025, ***р<0,01.
Сведения, подтверждающие возможность осуществления изобретения.
Фармацевтически приемлемые соли CDP-холина включают в себя его соли, полученные при добавлении оснований, в частности соли щелочных или щелочноземельных металлов, такие как соли натрия, калия, кальция и магния, или соли присоединения, полученные при добавлении неорганических или органических кислот, таких как хлористоводородная кислота, бромистоводороднная кислота, серная кислота, уксусная кислота, трифторуксусная кислота, лимонная кислота, молочная кислота, малоновая кислота, винная кислота, акриловая кислота, метакриловая кислота, яблочная кислота, малеиновая кислота, фумаровая кислота, бензойная кислота, салициловая кислота, коричная кислота, метансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота и никотиновая кислота.
CDP-холин или его соли могут быть использованы в безводной или сольватированной, в частности, гидратированной форме.
Введение может быть пероральным в форме таблетки, капсулы, порошка, гранулы, облатки, лепешки, раствора, суспензии, эмульсии, сиропа, геля и т.п. или парентеральным в форме раствора, суспензии, эмульсии и т.п. для внутривенной или внутримышечной инъекции.
Субъекты, особенно нуждающиеся в лечении в соответствии с данным изобретением, представлены:
- Пациентами, подвергшимися основному хирургическому вмешательству, т.е. пациентами, которым будут делать, делают и особенно которым сделаны хирургические операции, когда являются вероятными или, в особенности, при которых происходили кровотечения, манипуляции с сосудами или индуцированная и поддерживаемая гипотензия (нейрохирургия, сердечно-сосудистая хирургия, трансплантаты органов, имплантат ортопедического протеза и т.п.). В данных случаях предпочтительно начать лечение за 24-48 часов до хирургической операции, например, при эффективных пероральных дозах 1-2 г/день. Введение лекарства продолжают во время хирургической операции в эффективных дозах, составляющих, например, 1-2 г, внутривенным путем во время анестезии и затем в течение 1 недели в эффективных дозах, составляющих, например, 1-2 г/день, перорально или внутривенно в зависимости от состояния пациента.
- Пациентами с высокой степенью риска развития острого ишемического события, такого как инсульт, вследствие нескольких известных факторов риска, таких как история предшествующих временных ишемических эпизодов, артериальная гипертензия, гиперхолестеринемия, курение, фибрилляция предсердий или другое эмболическое сердечное заболевание. В данном случае пациентов следует лечить эффективными дозами, например, 1-2 г/день при пероральном введении, как если бы пациент перенес гипотетический инсульт.
Примеры
Следующие примеры иллюстрируют препараты активного ингредиента, пригодные для применения в способе, соответствующем данному изобретению. Компетентные специалисты в данной области смогут сделать любое изменение при условии, что специфический вариант осуществления изобретения не будет модифицирован, и вследствие этого изобретение не ограничено специфическими деталями данных примеров.
ПРИМЕР 1: таблетки по 500 мг
CDP-холин, натриевая соль 522,5 мг
Тальк 30,9 мг
Стеарат магния 3,0 мг
Диоксид кремния 2,5 мг
Na-Кроскармеллоза 20,0 мг
Кукурузный крахмал 20,0 мг
Микрокристаллическая целлюлоза, s.q.* 780,0 мг
*s.q. - в достаточном количестве или сколько требуется.
ПРИМЕР 2: 25% раствор для перорального применения
CDP-холин, натриевая соль 26,12 г
70% сорбит 20,00 г
Метиловый эфир п-гидроксибензойной кислоты 0,16 г
Пропиловый эфир п-гидроксибензойной кислоты 0,04 г
Цитрат динатрия 0,60 г
Сахарина натриевая соль 0,02 г
Клубничная эссенция 0,04 г
Краситель Red Punzo 4R 0,50 г
Безводная лимонная кислота 0,05 г
Очищенная вода, s.q.* 100,00 мл
*s.q. - в достаточном количестве или сколько требуется.
ПРИМЕР 3: Раствор для внутривенной инъекции
CDP-холин, натриевая соль 522,50 мг
Хлористоводородная кислота, рН 6,0-6,5, q.s.
Вода q.s.* 4,00 мл
*q.s. - (quantum satis) в достаточном количестве или сколько требуется.
ПРИМЕР 4: Нейропротекторное действие
Эффект CDP-холина на отсроченную гибель нервных клеток (апоптоз) оценивают на модели кортикальной церебральной ишемии на крысах в соответствии со следующим протоколом эксперимента:
1) - Животные:
Все тесты на церебральный инфаркт проводят на самцах крыс Sprague-Dawley массы 220-270 г. Животных содержат при свободном доступе к корму и воде в помещениях с контролем температуры и влажности с циклом чередования света и темноты 12/12 час.
2) - Модель закупорки средней мозговой артерии:
Церебральную ишемию индуцируют путем постоянной непосредственной закупорки средней мозговой артерии с использованием электрокоагуляции. При глубокой анестезии на голову крысы накладывают зажимы и делают разрез между левым ухом и левым глазом. Затем обнажают череп, разрезая височную мышцу. Краниотомию проводят с использованием сверла диаметром 1-2 мм позади чешуйчатой борозды. Твердую мозговую оболочку просверливают, чтобы обнажить ветвь средней мозговой артерии, в которой проводят постоянную коагуляцию.
3) - Схемы лечения:
Крыс случайным образом делят на три группы:
(a) Группа, получающая лечение через 30 минут после ишемии; животных данной группы лечат CDP-холином (500 мг/кг) в 0,9% стерильном физиологическом солевом растворе (0,1 мл), который вводят внутрибрюшинно. Данная группа представлена на Фигурах 1-5, как "После ишемии".
(b) Группа, получающая лечение за 24 часа до ишемии и через 30 минут после ишемии; животные данной группы получают такое же лечение, как в группе (а). Данная группа представлена на Фигурах 1-5, как "До ишемии".
(c) Животных данной группы используют в качестве контроля. После ишемии их лечат 0,9% физиологическим солевым раствором (0,1 мл), который вводят внутрибрюшинно. Данная группа представлена на Фигурах 1-5, как "Контроль".
4) - Получение образцов для морфологического изучения.
Мечение фрагментированной ДНК и иммуногистохимический анализ каспазы:
Животным позволяют возвратиться к нормальному состоянию в различные периоды времени (30 мин и 1, 4, 8, 12, 24 и 48 час) перед тем, как их усыпляют этиловым эфиром. Затем в их головной мозг сразу же вводят PBS (фосфатно-буферный раствор) при 4°С, используя канюлю, введенную в сердце (левый желудочек) с последующим введением 4% параформальдегида. Головной мозг быстро удаляют и фиксируют путем погружения в тот же самый фиксирующий раствор на 24 час при 4°С. После криопротекции с использованием 30% сахарозы головной мозг замораживают в изопентане, охлажденном жидким азотом, а затем хранят при -70°С. С помощью криостата из головного мозга делают срезы толщиной 50 мкм. Срезы головного мозга хранят при -70°С, используя криопротектор. Данные препараты затем используют как образцы для иммуногистохимического анализа, изучения морфологии и мечения in situ апоптотических клеток. Морфологию инфаркта изучают на последовательных препаратах, включающих начало и конец инфаркта с использованием окрашивания гематоксилином и эозином и окрашивания по Нисслу (NissI) (крезил фиолетовым). Апоптотические клетки метят вариантами фрагментированной ДНК введением метки in situ. Иммуногистохимический анализ экспрессии каспазы проводят, используя метод с применением авидин-биотин-пероксидазы со специфическими первичными антителами против каспаз 1, 2, 3, 6 и 8, полученными от фирмы Santa Cruz Biotechnology.
5) - Гель-электрофорез и анализ методом вестерн-блоттинга:
Приготовление образцов в плане групп и периодов времени аналогично данной процедуре, описанной в разделе 4). Животных, которые находятся в состоянии глубокой анестезии, декапитируют и сразу удаляют головной мозг. В каждом из случаев делают срезы следующих областей: а) серого вещества в области инфаркта; б) белого вещества в области инфаркта; в) серого вещества в пограничной области и г) белого вещества в пограничной области. Для каждого случая получают образцы из контралатеральной и ипсилатеральной сторон. Данные образцы впоследствии используют для анализа методом вестерн-блоттинга с использованием антител против каспаз и антител против различных субстратов каспаз с целью исследования их возможной деградации после ишемического повреждения.
6) - Результаты
Для оценки эффекта лечения экспрессию каспаз 1, 2, 3, 6 и 8 как маркеров процесса апоптоза измеряют через 12 часов после индукции инфаркта, полученные результаты представляют на Фигурах 1, 2, 3, 4 и 5, соответственно. Заявители наблюдают наличие существенных различий между лечеными и контрольными животными в плане экспрессии данных маркеров. Кроме того, что более важно, данные различия являются более значительными у животных, получающих лечение до ишемии, чем у животных, получающих лечение после ишемии. Все эти эксперименты делают очевидным, что CDP-холин при введении до и после индукции инфаркта снижает уровень каспаз более значительно, чем при введении только после индукции инфаркта.
| название | год | авторы | номер документа |
|---|---|---|---|
| CDP-ХОЛИН-СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ СИНДРОМА АЛКОГОЛЬНОЙ АБСТИНЕНЦИИ И СПОСОБ ЛЕЧЕНИЯ С ЕГО ИСПОЛЬЗОВАНИЕМ | 2001 |
|
RU2251422C2 |
| ПРИМЕНЕНИЕ БЕТА-ГИДРОКСИБУТИРАТА ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ ДЛЯ ПРИГОТОВЛЕНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА, ОБЛАДАЮЩЕГО ЦИТОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ, ВКЛЮЧАЮЩЕЙ НЕЙРОПРОТЕКТОРНУЮ, КАРДИОПРОТЕКТОРНУЮ, ПРОТИВОИШЕМИЧЕСКУЮ, АНТИГИПОКСИЧЕСКУЮ, АНТИСТРЕССОРНУЮ, АКТОПРОТЕКТОРНУЮ И АДАПТОГЕННУЮ АКТИВНОСТИ, ЛЕКАРСТВЕННОЕ СРЕДСТВО И СПОСОБ ПРОФИЛАКТИКИ, КУПИРОВАНИЯ И ЛЕЧЕНИЯ С ПОМОЩЬЮ ЭТОГО ЛЕКАРСТВЕННОГО СРЕДСТВА | 2009 |
|
RU2426535C2 |
| ИНЪЕКЦИОННАЯ ФОРМА ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ (ВАРИАНТЫ) ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ НЕРВНОЙ СИСТЕМЫ И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2010 |
|
RU2448706C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИАПОПТОТИЧЕСКОЙ АКТИВНОСТЬЮ | 2018 |
|
RU2685428C1 |
| КОМБИНАЦИИ ЭДАРАВОНА ДЛЯ ЛЕЧЕНИЯ ИШЕМИЧЕСКИХ ПОВРЕЖДЕНИЙ МОЗГА | 2017 |
|
RU2693627C2 |
| НЕЙРОЗАЩИТНОЕ ДЕЙСТВИЕ РАСТВОРИМОЙ УРСОДЕЗОКСИХОЛЕВОЙ КИСЛОТЫ В МОДЕЛЯХ ФОКАЛЬНОЙ ИШЕМИИ | 2005 |
|
RU2428987C2 |
| ФАРМАЦЕВТИЧЕСКАЯ НЕЙРОПРОТЕКТОРНАЯ, АНТИОКСИДАНТНАЯ, АНТИГИПОКСАНТНАЯ, АНТИАПОПТОТИЧЕСКАЯ И МЕМБРАНОПРОТЕКТОРНАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ | 2008 |
|
RU2385722C1 |
| СПОСОБ ЛЕЧЕНИЯ НЕЙРОТРАВМЫ | 2012 |
|
RU2749191C2 |
| ГИБРИДНЫЙ БЕЛОК IGF-1-LONG ДЛЯ ЛЕЧЕНИЯ ИНСУЛЬТА, НУКЛЕИНОВАЯ КИСЛОТА, ВЕКТОР, КЛЕТКА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ | 2018 |
|
RU2711111C1 |
| СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМБИНАЦИИ ДЛЯ ЛЕЧЕНИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ И ИШЕМИЧЕСКИХ БОЛЕЗНЕЙ МОЗГА | 2012 |
|
RU2569302C2 |
Предложено: применение CDP-холина (цитидин-дифосфат-холина) или его соли в качестве профилактического средства для лечения церебральной ишемии и способ такого профилактического лечения. Изобретение отличается тем, что для CDP-холина или его соли выявлен новый, неизвестный ранее механизм действия: ингибирование активации каспазной цепи, причем эффективность действия высока при профилактическом приеме. 2 н. и 4 з.п. ф-лы, 5 ил.

| US 5872108 А, 16.02.1999 | |||
| Химический источник тока | 1977 |
|
SU1122241A3 |
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| СРЕДСТВО ДЛЯ УСИЛЕНИЯ АНТИАГРЕГАЦИОННОГО ЭФФЕКТА АСПИРИНА | 1991 |
|
RU2007170C1 |
Авторы
Даты
2005-07-10—Публикация
2001-03-13—Подача