Область техники, к которой относится изобретение
Эндометриоз представляет собой одну из наиболее часто встречаемых патологий, диагностируемых у гинекологических пациенток. Например, в Соединенном Королевстве и США этой болезнью поражены между 10% и 25% женщин с симптомами гинекологических заболеваний. Клинический диагноз ставят обычно при лапароскопическом исследовании геморрагических или фибротических участков на тазовых органах. Эктопическая (имеющая несвойственную локализацию) эндометриальная ткань подвергается циклическим изменениям в ответ на гормоны яичников. Циклическое кровотечение из отложений эндометрия вносит вклад в местную воспалительную реакцию. Эндометриоз, как правило, поражает женщин детородного возраста с частотой на уровне по меньшей мере 1% (см. работу Shaw R.W., Атлас эндометриоза (An Atlas of Endometriosis), The Parthenon Publishing Group, (1993)).
Эндометриоз обычно классифицируют следующим образом: внутренний генитальный эндометриоз (аденомиоз), наружный генитальный эндометриоз и экстрагенитальный эндометриоз.
Хроническая боль в области таза может быть либо обусловленной эндометриозом, либо представлять собой самостоятельное заболевание.
Непроходимость фаллопиевых труб (НФТ) представляет собой относительно распространенное заболевание и может быть причиной до 20% случаев трубного бесплодия (см. статью Winfield A.C. и соавт., Видимая роговидная окклюзия при гистеросальпингографии и ее восстановление с помощью глюкагона (Apparent cornual occlusion in hysterosalpingography: Reversal by glucagon), AJR Am. J. Roentgenol., 139:525-527, (1982)).
Уровень техники
Sampson предположил, что менструальная регургитация и последующая имплантация эндометриальной ткани на поверхности брюшины приводит к эндометриозу [см. статью Sampson J.A, Перитонеальный эндометриоз, обусловленный менструальной диссиминацией эндометриальной ткани в полость брюшины (Peritoneal endometriosis due to menstrual dissemination of the endometrial tissue into the peritoneal cavitiy), Am. J. Obstet. Gynecol., 14:422, (1927)]. В патогенезе эндометриоза может участвовать ряд этиологических факторов: Dmowski и соавт. предположили, что к эндометриозу приводят генетические и иммунологические факторы [см. статью Dmowski W. P., Steele R.W. и Baker G.F., Клеточный иммунодефицит при эндометриозе (Deficient cellular immunity in endometriosis), Am. J. Obstet. Gynecol., 141, 377, (1981)]. Была продемонстрирована эмболизация сосудов и лимфатической сети в отдаленных участках, и она объясняет (редкие) случаи эндометриоза вне полости брюшины, например, кожного, легочного, почечного эндометриоза.
Клетки, выстилающие мюллеров проток, происходят из стволовых клеток, которые дифференцируются в перитонеальные клетки и клетки на поверхности яичников. Полагают, что данные зрелые клетки проходят обратную дедифференцировку до их стволовой природы, а затем трансформируются в эндометриальные клетки [см. статью Levander G., Образование кости путем индукции. Экспериментальное исследование (Bone formation by induction. An experimental study), Arch. Klin. Chir., 202, 497, (1941)]. Дисменорея, острая или хроническая боль в области таза, диспареуния и бесплодие представляют наиболее часто встречающиеся из описанных клинических симптомов.
НФТ представляет разнородную группу указанной патологии, в основе которой лежит внутренняя окклюзия или наружное сжатие вследствие эстрогенчувствительных нарушений, таких как эндометриоз, аденомиоз, эндосальпингиоз и миома. Кроме лапароскопии, НФТ обычно диагностируют с помощью гистеросальпингографии.
Лечение первого выбора предусматривает лапароскопическое удаление образований эндометрия. После данной процедуры может следовать лечение даназолом или агонистом LHRH (в течение шести месяцев). Во время лечения даназолом женщины могут испытывать нарушения со стороны желудочно-кишечного тракта и печени, а также тяжелые андрогенные побочные эффекты.
С теоретической точки зрения для лечения эндометриоза и миомы матки предполагалось также использовать прямую супрессию путем введения антагониста LHRH с целью снижения продолжительности лечения и ускоренного улучшения субъективных симптомов [см. статью Тh. Reissmann и соавт., Human Reproduction, т. 10, № 8, стр.1974-1981, (1995)].
Далее Hodgen в Патенте США 5658884 описывает схему терапевтического лечения состояния, зависимого от половых желез, путем снижения поступления эстрогена посредством длительного введения антагониста GnRH (гонадотропин-рилизинг-гормона) в течение 6 месяцев или более длительно в количестве, эффективно подавляющем пролиферацию эндометриальной ткани, практически не блокируя образование эндогенного эстрогена. С этой целью Hodgen представляет такую схему или дозу антагониста GnRH, при которой достигается уровень эстрадиола в сыворотке в течение 24 часов в интервале приблизительно от 25 до 50 и предпочтительно приблизительно от 35 до 45 пг/мл. Однако Hodgen не описывает уровни эстрадиола в сыворотке, колеблющиеся между 50 пг/мл и 75 пг/мл. Более того, Hodgen представляет в Патенте США 5658884 только непрерывное длительное лечение (на основе ежедневных или периодических введений, при этом последнее означает еженедельное или ежемесячное введение), но не кратковременное стимулирующее лечение в течение только 4-12 недель. Hodgen также не описывает некую комбинированную терапию с использованием антагониста GnRH при лечении эндометриоза. Лечение описано только на обезьянах и включает также проведение дорогостоящего и повторяющегося теста на стимулирующее введение прогестерона для получения среднего за 24 часа уровня эстрадиола в сыворотке 30-50 пг/мл.
Как следствие непродолжительности эффекта терапии с использованием агониста LHRH, в течение нескольких дней могло происходить обострение симптомов заболевания. После пролонгированного лечения, которое требуется, чтобы избежать повторной пролиферации ткани эндометрия, появляются симптомы отмены гормонов, а также деминерализация кости.
Следовательно, эффективная лекарственная терапия должна непосредственно уменьшать количество остаточной внематочной эндометриальной ткани, имеющейся после лапароскопической операции.
Продолжительность терапии должна составлять только 4-12 недель без появления каких-либо основных симптомов отмены гормонов или образования кисты яичника.
Антагонисты LHRH вызывают быструю супрессию гормонов и вследствие этого доброкачественные гинекологические опухоли, такие как фибромы матки, уменьшаются через короткий период времени [см. журнал Human Reproduction, 13, (1998)].
Сущность изобретения
Данное изобретение касается усовершенствования лекарственной терапии внематочной пролиферации эндометриальной ткани, т.е. введения антагонистов LHRH пациенткам с клиническими симптомами эндометриоза, при этом усовершенствование состоит из:
непосредственного уменьшения количества эктопической эндометриальной ткани,
немедленного прекращения симптомов, например, острой боли, хронической боли в области таза и дисменореи,
предупреждения какого-либо развития заболевания,
избежания симптомов отмены гормонов,
профилактики образования кисты яичника, деминерализации костей, а также нарушений со стороны желудочно-кишечного тракта и печени.
Соответствующую изобретению лекарственную терапию можно начинать в ранней до средней фолликулярной фазе, предпочтительно в первый - третий день менструального цикла. Во время лечения уровни концентрации эстрадиола в сыворотке поддерживают между 35 пг/мл и 80 пг/мл, предпочтительно между приблизительно 45-75 пг/мл, более предпочтительно между приблизительно 50-75 пг/мл. Антагонист LHRH вводят только в течение 4-12 недель (кратковременное стимулирующее лечение) путем либо ежедневного, еженедельного либо ежемесячного введения. Согласно данному изобретению после кратковременного стимулирующего лечения проводят введение противозачаточного препарата, нестероидного противоревматического агента, анальгетика, андрогена, отличного от 17-α-алкилзамещенного тестостерона, или любых их комбинаций.
При лечении внематочной эндометриальной ткани антагонистом LHRH терапию начинают в первый - третий день менструального цикла. Перед началом терапии с использованием антагониста LHRH ставят диагноз с помощью лапароскопии. В случаях сильной боли терапия с использованием антагониста LHRH должна быть начата без предварительной лапароскопии.
Лечение будет продолжаться до исчезновения клинической симптоматики и пока не будет отмечено прекращение пролиферации эндометрия. Дальнейшая пролиферация эндометрия не происходит вследствие немедленной супрессии гонадотропинов LH (лютеинизирующего гормона) и FSH (фолликулстимулирующего гормона), а также половых стероидов эстрадиола и прогестерона. Доброкачественные опухоли или другие зависимые от половых стероидов поражения, подобные эндометриозу, уменьшаются в течение четырех - двенадцати недель терапии. Вследствие того, что эффект является продолжительным, кисты яичника не развиваются.
Кроме того, отсутствуют какие-либо симптомы отмены гормонов, поскольку значения эстрадиола поддерживают в соответствующем ранней фолликулярной фазе интервале 35-80 пг/мл, предпочтительно между приблизительно 45-75 пг/мл, более предпочтительно между приблизительно 50-75 пг/мл без дальнейшего повышения или снижения. Определение титра дозы антагониста LHRH, например путем проведения дорогостоящего теста на стимулирующее введение прогестерона, не является необходимым.
Вследствие этого усовершенствование способа терапевтического лечения внематочной пролиферации эндометриальной ткани согласно изобретению охватывает:
непосредственное уменьшение количества эктопической эндометриальной ткани,
предупреждение какого-либо развития заболевания,
избежание симптомов отмены гормонов,
профилактику образования кисты яичника, деминерализации костей, а также нарушений со стороны желудочно-кишечного тракта и печени,
начало лекарственной терапии в первый - третий день цикла и поддержание уровней эстрадиола при значениях, характерных для ранней фолликулярной фазы, в течение всего периода лечения посредством введения антагониста LHRH, где антагонист предпочтительно представлен цетрореликсом, тевереликсом, ганреликсом, антидом или абареликсом. Антагонист может быть также представлен антагонистом LHRH D-63153 (Ac-D-Nal-D-pCI-Phe-D-Pal-Ser-N-Me-Tyr-D-Hci-Nle-Arg-Pro-D-Ala-NHg), как описано в Патентной заявке Германии № 19911771.3, поданной 11 марта 1999 г.
Антагонист LHRH может применяться в течение 4-12 недель при еженедельной дозе 3-10 мг/неделю или в течение 4-12 недель при ежедневной дозе от 0,25 мг до 0,5 мг/день.
Возможно также применение антагониста LHRH в течение 4-12 недель в месячной дозе 12 - 40 мг/месяц.
При повторном терапевтическом лечении антагонист LHRH применяют в течение 4-12 недель и повторяют курс лечения два или три раза в год, при этом повторный курс лечения не проводят непосредственно после кратковременного стимулирующего лечения. Как правило, период времени на протяжении недель или месяцев, в течение которого антагонист LHRH не вводят, находится между концом кратковременного стимулирующего лечения и началом повторного лечения.
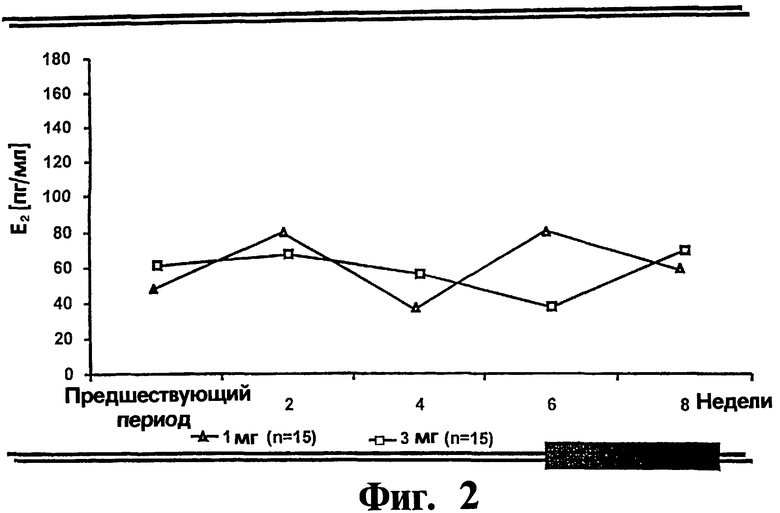
Для демонстрации возможности поддержания секреции эстрадиола на низком уровне при подобранном лечении антагонистом LHRH, обеспечивающем терапевтическую супрессию без симптомов отмены, девяти пациенткам с подтвержденным диагнозом эндометриоза подкожно вводили 3 мг цетрореликса ацетата при еженедельном введении в течение 8 недель. Поскольку пациентки хорошо переносили режим лечения при отсутствии каких-либо приливов или других симптомов отмены и без каких-либо признаков развития заболевания, подтвержденных повторным лапароскопическим исследованием, средние концентрации эстрадиола в сыворотке колебались между 37 пг/мл и 64 пг/мл, предпочтительно между 45-75 пг/мл, более предпочтительно между приблизительно 50-75 пг/мл. Гистологические биоптаты показали отсутствие пролиферации эндометрия в конце лечения. Образование кисты яичников не происходило.
Перечень фигур чертежей и иных материалов
На Фигуре 1 представлена непрерывная супрессия уровня эстрадиола до значений, соответствующих ранней фолликулярной фазе (в интервале от 35 пг/мл до 80 пг/мл, предпочтительно между 45-75 пг/мл, более предпочтительно между приблизительно 50-75 пг/мл), полученная у пациенток с эндометриозом при еженедельном введении Цетрореликса (антагониста LHRH) в дозе 3 мг в течение 8 недель. Получена незамедлительная и непрерывная супрессия уровней эстрадиола без каких-либо признаков симптомов отмены эстрадиола и без пролиферации эндометрия в конце лечения.
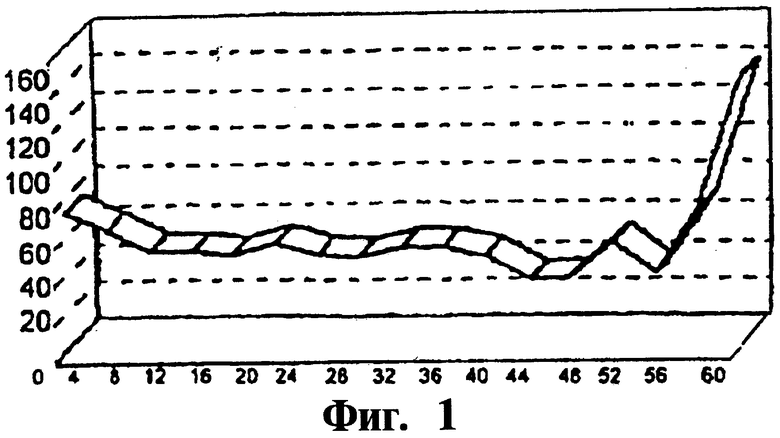
На Фигуре 2 представлены уровни эстрадиола в сыворотке после еженедельного введения цетрореликса в дозе 1 мг - 3 мг один раз/неделю. Уровни эстрадиола в сыворотке составляют между приблизительно 35-80 пг/мл, предпочтительно между приблизительно 45-75 пг/мл, более предпочтительно между приблизительно 50-75 пг/мл. Сведения, подтверждающие возможность осуществления изобретения
Пациентка с эндометриозом с характерной симптоматической болью страдает от хронического заболевания. Хирургические методы как способ лечения, а также лекарственная терапия с целью супрессии секреции половых стероидов у пациентки часто в результате приводят только к временному улучшению. Уровень рецидивов недомоганий является очень высоким и составляет приблизительно 70% в течение 5 лет после окончания лечения (см. работу Schweppe, 1999).
В то же время радикальное хирургическое вмешательство и супрессия секреции эстрогенов приводят к значительным побочным эффектам. Радикальное хирургическое вмешательство в виде гистерэктомии (экстирпации матки) с двусторонней аднексэктомией (двустронним удалением придатков) не является адекватным лечением для молодых женщин, находящихся в пременопаузе. Хронический недостаток эстрогена приводит к следующим вегетативным симптомам: приливы, потливость, сухость вагины, состояние депрессии, а также несет риск развития остеопороза. Альтернативная терапия синтетическим стероидным соединением даназолом может вызывать симптомы маскулинизации вследствие андрогенного эффекта.
Целью лекарственной терапии пациенток с эндометриозом с симптоматической болью является разработка лечения без побочных эффектов, в особенности позволяющего избежать отрицательные эффекты супрессии эстрогена, которое при этом действует в течение длительного периода после окончания лечения. Специфический фармакологический режим действия антагонистов LHRH представляет новые возможности для лечения эндометриоза.
Еженедельное введение соответствующей дозы антагониста LHRH, например подкожное введение 3 мг цетротида®/неделю в течение восьми недель приводит к контролируемой супрессии секреции эстрогена, при этом получают концентрации в сыворотке между приблизительно 35 пг/мл и приблизительно 80 пг/мл, предпочтительно между приблизительно 45-75 пг/мл, более предпочтительно между приблизительно 50-75 пг/мл. В данном диапазоне сывороточных концентраций не возникают никакие вегетативные симптомы. Можно также избежать развития остеопороза. Симптоматическую боль можно эффективно подавить на всех стадиях болезни (rAFS I-IV, где AFS - Американское травматологичесое общество). На стадиях rAFS I-II отмечена клиническая регрессия заболевания в плане снижения области имплантации (см. работу Felberbaum и соавт., 2000).
В предпочтительном варианте осуществления изобретения после данного периода от восьми до двенадцати недель пациентка могла принимать противозачаточный препарат, предпочтительно противозачаточный препарат перорального применения, предпочтительно с гестагеновыми компонентами, до появления желания забеременеть. В связи с этим следует упомянуть комбинации, содержащие 2 мг линестренола и 0,04 мг этинилэстрадиола или 2,5 мг линестренола и 0,05 мг этинилэстрадиола (например, Yermonil® Lyn-ratiopharm-Sequenz®).
Комбинированная терапия с использованием андрогенов, отличных от 17-α-алкилзамещенных тестостеронов, таких как даназол, также может применяться после режима кратковременной стимуляции антагонистом LHRH либо в виде монотерапии, либо в комбинации с нестероидными противоревматическими агентами и/или анальгетиками. Примером подходящего андрогена является галотестин™ (флуоксиместерон).
Лечение с использованием противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения, предпочтительно содержащего гестагены, следует продолжать в отдельных случаях до тех пор, пока остается ощущение боли. На данной стадии у пациентки будет относительно слабое менструальное кровотечение в результате действия гестагенового компонента данного противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения. Для того чтобы охватить также самые критические предменструальные и менструальные дни в плане ощущения боли, в данной фазе может быть предписана сопутствующая лекарственная терапия соответствующими нестероидными противоревматическими препаратами, например диклофенаком, ибупрофеном, индометацином, производными оксикама или ацетилсалициловой кислоты. Возможно также применение анальгетика, такого как флупиртинмалеат (Katadolon®).
Если в дальнейшем болевые симптомы сохраняются во время комбинированной терапии гестагеновыми противозачаточными препаратами, предпочтительно противозачаточными препаратами для перорального применения, ежедневное, еженедельное или ежемесячное лечение соответствующими дозами антагониста LHRH, как описано выше, можно повторить. Детальная информация относительно соответственных условий лечения приведена ниже. Если у пациентки абсолютно отсутствует боль, лечение может быть заменено гестагенным противозачаточным препаратом, предпочтительно противозачаточным препаратом для перорального применения, в комбинации с сопутствующей лекарственной терапией соответствующими нестероидными противоревматическими препаратами или анальгетиками.
Данный способ терапии с использованием введения антагониста LHRH с перерывами приводит к созданию нового и более рационального, не имеющего ограничений лечения при отсутствии побочного действия и в значительной мере снижает лекарственную нагрузку у пациентки.
Фармацевтические препараты, подходящие для лечения.
Фармацевтические препараты антагониста LHRH, подходящие для терапевтического лечения внематочной пролиферации эндометриальной ткани, хронической боли в области таза и непроходимости фаллопиевых труб, могут быть представлены, например:
а) ацетаты препаратов в концентрации 1 мг/1 мл или ниже, в которых порошок может быть растворен в воде для инъекций (в/и) или глюконовой кислоте (ГК);
б) ацетаты препаратов в концентрации от 1,5 мг/1 мл до 5,0 мг/1 мл, предпочтительно 2,5 мг/1 мл, в которых порошок может быть растворен в воде для инъекций (в/и) или глюконовой кислоте (ГК);
с) памоаты препаратов в концентрации от 10 мг/мл до 30 мг/мл, предпочтительно 15 мг/мл, в которых порошок лиофилизата может быть растворен в глюконовой кислоте (ГК) или воде для инъекций (в/и).
Согласно одному объекту данного изобретения предложен способ терапевтического лечения внематочной пролиферации эндометриальной ткани, хронической боли в области таза и/или непроходимости фаллопиевых труб (НФТ), усовершенствование которого состоит во введении антагониста LHRH пациентке, нуждающейся в данном лечении, в форме кратковременного стимулирующего лечения в течение приблизительно 4-12 недель с последующим прекращением введения антагониста LHRH.
Продолжительность кратковременного стимулирующего лечения составляет приблизительно от 4 до приблизительно 12 недель, что означает, что лечение может составлять между приблизительно 28 и приблизительно 84 днями или от приблизительно одного до приблизительно трех месяцев.
Согласно другому аспекту данного изобретения в вышеупомянутом способе предложено усовершенствование, в котором антагонист LHRH вводят таким образом, что уровень концентрации эстрогена в сыворотке составляет между приблизительно 35 пг/мл и приблизительно 80 пг/мл, предпочтительно между приблизительно 45-75 пг/мл, более предпочтительно между приблизительно 50-75 пг/мл.
Согласно другому аспекту данного изобретения в вышеупомянутом способе предложено усовершенствование, характеризующееся тем, что после кратковременного стимулирующего лечения антагонистом LHRH следует введение противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения.
Согласно другому аспекту данного изобретения в вышеупомянутом способе предложено усовершенствование, характеризующееся тем, что после кратковременного стимулирующего лечения антагонистом LHRH следует введение нестероидного противоревматического агента.
Согласно другому аспекту данного изобретения в вышеупомянутом способе предложено усовершенствование, характеризующееся тем, что после кратковременного стимулирующего лечения антагонистом LHRH следует введение анальгетика.
Согласно другому аспекту данного изобретения в вышеупомянутом способе предложено усовершенствование, характеризующееся тем, что после кратковременного стимулирующего лечения антагонистом LHRH следует введение андрогена, отличного от 17-α-алкилзамещенного тестостерона.
Согласно другому аспекту данного изобретения в вышеупомянутом способе предложено усовершенствование, характеризующееся тем, что после кратковременного стимулирующего лечения антагонистом LHRH следует комбинированное или раздельное введение по меньшей мере одного активного агента, выбранного из группы, состоящей из противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения, нестероидного противоревматического агента, анальгетика, андрогена, отличного от 17-α-алкилзамещенного тестостерона, или любых их комбинаций.
Согласно другому аспекту данного изобретения в вышеупомянутом способе предложено усовершенствование, характеризующееся тем, что антагонист LHRH вводят, начиная с ранней до средней фолликулярной фазы, предпочтительно в первый - третий дни цикла.
Согласно другому аспекту данного изобретения в вышеупомянутом способе предложено усовершенствование, характеризующееся тем, что антагонист LHRH выбирают из группы, состоящей из цетрореликса, тевереликса, ганиреликса, антида, абареликса и D-63153.
Согласно другому аспекту данного изобретения в вышеупомянутом способе предложено усовершенствование, характеризующееся тем, что антагонист LHRH вводят во время кратковременного стимулирующего лечения в течение 4-12 недель при еженедельной дозе 3-10 мг/неделю.
Согласно другому аспекту данного изобретения в вышеупомянутом способе предложено усовершенствование, характеризующееся тем, что антагонист LHRH вводят во время кратковременного стимулирующего лечения в течение 4-12 недель при ежедневной дозе 0,25 мг - 0,5 мг/день.
Согласно другому аспекту данного изобретения в вышеупомянутом способе предложено усовершенствование, характеризующееся тем, что антагонист LHRH вводят во время кратковременного стимулирующего лечения в течение приблизительно 4-12 недель при ежемесячной дозе приблизительно 12-40 мг/месяц.
Согласно другому аспекту данного изобретения в вышеупомянутом способе предложено усовершенствование, характеризующееся тем, что антагонист LHRH применяют для стимулирующего лечения в течение приблизительно 4-12 недель и лечение повторяют два или три раза в год.
Согласно следующему объекту данного изобретения предложена фармацевтическая композиция для лечения внематочной пролиферации эндометриальной ткани, хронической боли в области таза и/или непроходимости фаллопиевых труб (НФТ), содержащая антагонист LHRH и необязательно по меньшей мере один агент, выбранный из группы, состоящей из противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения, нестероидного противоревматического агента, анальгетика, андрогена, отличного от 17-α-алкилзамещенного тестостерона или любых их комбинаций, необязательно вместе с фармацевтически приемлемыми наполнителями, при этом антагонист LHRH вводят пациентке, нуждающейся в кратковременном стимулирующем лечении, в течение приблизительно 4-12 недель, затем введение антагониста LHRH прекращают и необязательно пациентке вводят вместе или раздельно по меньшей мере один агент, выбранный из группы, состоящей из противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения, нестероидного противоревматического агента, анальгетика, андрогена, отличного от 17-α-алкилзамещенного тестостерона, или любых их комбинаций.
Подходящие наполнители или лекарственные формы описаны, например, в монографии К.Н. Bauer, K.-H. Frömming и С. Führer, Справочник по фармацевтической технологии (Lehrbuch der Pharmazeutischen Technologie), 6 изд., Stuttgart, стр.163-186 (наполнители) и стр.227-386 (лекарственные формы), (1999), включая ссылки, приведенные в данном контексте.
Например, антагонист LHRH можно вводить подкожно (s.c.), внутримышечно (i.m.) или ингаляционно. Агенты, выбранные из группы, состоящей из противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения, нестероидного противоревматического агента, анальгетика, андрогена, отличного от 17-α-алкилзамещенного тестостерона, или любых их комбинаций могут быть введены так, как известно в области техники (см., например, Немецкую и Европейскую фармакопею или Фармакопею США), предпочтительно перорально или путем ингаляции.
Согласно другому аспекту данного изобретения представлена вышеупомянутая фармацевтическая композиция, при использовании которой антагонист LHRH вводят таким образом, что уровень концентрации эстрогена в сыворотке составляет между приблизительно 35 пг/мл и приблизительно 80 пг/мл, предпочтительно между приблизительно 45-75 пг/мл, более предпочтительно приблизительно 50-75 пг/мл.
Согласно другому аспекту данного изобретения представлена вышеупомянутая фармацевтическая композиция, при использовании которой после кратковременного стимулирующего лечения антагонистом LHRH следует введение противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения.
Согласно другому аспекту данного изобретения, представлена вышеупомянутая фармацевтическая композиция, при использовании которой после кратковременного стимулирующего лечения антагонистом LHRH следует введение нестероидного противоревматического агента.
Согласно другому аспекту данного изобретения, представлена вышеупомянутая фармацевтическая композиция, при использовании которой после кратковременного стимулирующего лечения антагонистом LHRH следует введение анальгетика.
Согласно другому аспекту данного изобретения, представлена вышеупомянутая фармацевтическая композиция, при использовании которой после кратковременного стимулирующего лечения антагонистом LHRH следует введение андрогена, отличного от 17-α-алкилзамещенного тестостерона.
Согласно другому аспекту данного изобретения представлена вышеупомянутая фармацевтическая композиция, при использовании которой после кратковременного стимулирующего лечения антагонистом LHRH следует комбинированное или раздельное введение по меньшей мере одного активного агента, выбранного из группы, состоящей из противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения, нестероидного противоревматического агента, анальгетика, андрогена, отличного от 17-α-алкилзамещенного тестостерона, или любых их комбинаций.
Согласно другому аспекту данного изобретения представлена вышеупомянутая фармацевтическая композиция, при использовании которой антагонист LHRH вводят, начиная с ранней до средней фолликулярной фазы, предпочтительно в первый - третий дни цикла.
Согласно другому аспекту данного изобретения представлена вышеупомянутая фармацевтическая композиция, при использовании которой антагонист LHRH выбран из группы, состоящей из цетрореликса, тевереликса, ганиреликса, антида, абареликса и D-63153.
Согласно другому аспекту данного изобретения представлена вышеупомянутая фармацевтическая композиция, при использовании которой антагонист LHRH вводят во время кратковременного стимулирующего лечения в течение 4-12 недель при еженедельной дозе 3-10 мг/неделю.
Согласно другому аспекту данного изобретения представлена вышеупомянутая фармацевтическая композиция, при использовании которой антагонист LHRH вводят во время кратковременного стимулирующего лечения в течение 4-12 недель при ежедневной дозе 0,25 мг - 0,5 мг/день.
Согласно другому аспекту данного изобретения представлена вышеупомянутая фармацевтическая композиция, при использовании которой антагонист LHRH вводят во время кратковременного стимулирующего лечения в течение приблизительно 4-12 недель при ежемесячной дозе приблизительно 12-40 мг/месяц.
Согласно другому аспекту данного изобретения представлена вышеупомянутая фармацевтическая композиция, в которой антагонист LHRH применяют для стимулирующего лечения в течение приблизительно 4-12 недель и лечение повторяют два или три раза в год.
Согласно другому аспекту данного изобретения представлена вышеупомянутая фармацевтическая композиция, в которой по меньшей мере один активный агент, выбранный из группы, состоящей из противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения, нестероидного противоревматического агента, анальгетика, андрогена, отличного от 17-α-алкил-замещенного тестостерона, или любых их комбинаций находятся в одной и той же или раздельных лекарственных формах.
Согласно другому объекту данного изобретения предложено применение антагониста LHRH для получения лекарственного препарата для терапевтического лечения внематочной пролиферации эндометриальной ткани, хронической боли в области таза и/или непроходимости фаллопиевых труб (НФТ), при котором антагонист LHRH вводят пациентке, нуждающейся в данном лечении, в форме кратковременного стимулирующего лечения в течение приблизительно 4-12 недель с последующим прекращением введения антагониста LHRH.
Согласно другому аспекту данного изобретения предложено применение вышеупомянутого антагониста LHRH, при котором антагонист LHRH вводят таким образом, что уровень концентрации эстрогена в сыворотке составляет между приблизительно 35 пг/мл и приблизительно 80 пг/мл, предпочтительно между приблизительно 45-75 пг/мл, более предпочтительно между приблизительно 50-75 пг/мл.
Согласно другому аспекту данного изобретения предложено применение вышеупомянутого антагониста LHRH, при котором после кратковременного стимулирующего лечения антагонистом LHRH следует введение противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения.
Согласно другому аспекту данного изобретения предложено применение вышеупомянутого антагониста LHRH, при котором после кратковременного стимулирующего лечения антагонистом LHRH следует введение нестероидного противоревматического агента.
Согласно другому аспекту данного изобретения предложено применение вышеупомянутого антагониста LHRH, при котором после кратковременного стимулирующего лечения антагонистом LHRH следует введение анальгетика.
Согласно другому аспекту данного изобретения предложено применение вышеупомянутого антагониста LHRH, при котором после кратковременного стимулирующего лечения антагонистом LHRH следует введение андрогена, отличного от 17-α-алкилзамещенного тестостерона.
Согласно другому аспекту данного изобретения предложено применение вышеупомянутого антагониста LHRH, при котором после кратковременного стимулирующего лечения антагонистом LHRH следует комбинированное или раздельное введение по меньшей мере одного активного агента, выбранного из группы, состоящей из противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения, нестероидного противоревматического агента, анальгетика, андрогена, отличного от 17-α-алкилзамещенного тестостерона, или любых их комбинаций.
Согласно другому аспекту данного изобретения предложено применение вышеупомянутого антагониста LHRH, при котором антагонист LHRH вводят, начиная с ранней до средней фолликулярной фазы, предпочтительно в первый - третий дни цикла.
Согласно другому аспекту данного изобретения предложено применение вышеупомянутого антагониста LHRH, при котором антагонист LHRH выбирают из группы, состоящей из цетрореликса, тевереликса, ганиреликса, антида, абареликса и D-63153.
Согласно другому аспекту данного изобретения предложено применение вышеупомянутого антагониста LHRH, при котором антагонист LHRH вводят в течение кратковременного стимулирующего лечения в течение приблизительно 4-12 недель при еженедельной дозе от 3 до 10 мг/неделю.
Согласно другому аспекту данного изобретения предложено применение вышеупомянутого антагониста LHRH, при котором антагонист LHRH вводят в течение кратковременного стимулирующего лечения в течение приблизительно 4-12 недель при ежедневной дозе от 0,25 мг до 0,5 мг/день.
Согласно другому аспекту данного изобретения предложено применение вышеупомянутого антагониста LHRH, при котором антагонист LHRH вводят в течение кратковременного стимулирующего лечения в течение приблизительно 4-12 недель при ежемесячной дозе от 12 до 40 мг/месяц.
Согласно другому аспекту данного изобретения предложено применение вышеупомянутого антагониста LHRH, при котором антагонист LHRH применяют для стимулирующего лечения в течение приблизительно 4-12 недель и лечение повторяют два или три раза в год.
Согласно другому аспекту данного изобретения предложено применение антагониста LHRH и по меньшей мере одного активного агента, выбранного из группы, состоящей из противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения, нестероидного противоревматического агента, анальгетика, андрогена, отличного от 17-α-алкилзамещенного тестостерона, или любых их комбинаций для приготовления лекарственного препарата для терапевтического лечения внематочной пролиферации эндометриальной ткани, хронической боли в области таза и/или непроходимости фаллопиевых труб (НФТ), при котором антагонист LHRH вводят пациентке, нуждающейся в данном лечении, в форме кратковременного стимулирующего лечения в течение приблизительно 4-12 недель, затем введение антагониста LHRH прекращают и пациентке вводят вместе или раздельно по меньшей мере один активный агент, выбранный из группы, состоящей из противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения, нестероидного противоревматического агента, анальгетика, андрогена, отличного от 17-α-алкилзамещенного тестостерона, или любых их комбинаций.
Согласно другому аспекту данного изобретения предложено применение антагониста LHRH и по меньшей мере одного вышеупомянутого активного агента, при котором антагонист LHRH вводят таким образом, что уровень концентрации эстрогена в сыворотке составляет между приблизительно 35 пг/мл и приблизительно 80 пг/мл, предпочтительно между приблизительно 45-75 пг/мл, более предпочтительно между приблизительно 50-75 пг/мл.
Согласно другому аспекту данного изобретения предложено применение антагониста LHRH и по меньшей мере одного вышеупомянутого активного агента, причем после кратковременного стимулирующего лечения антагонистом LHRH следует введение противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения.
Согласно другому аспекту данного изобретения предложено применение антагониста LHRH и по меньшей мере одного вышеупомянутого активного агента, при котором после кратковременного стимулирующего лечения антагонистом LHRH следует введение нестероидного противоревматического агента.
Согласно другому аспекту данного изобретения предложено применение антагониста LHRH и по меньшей мере одного вышеупомянутого активного агента, при котором после кратковременного стимулирующего лечения антагонистом LHRH следует введение анальгетика.
Согласно другому аспекту данного изобретения предложено применение антагониста LHRH и по меньшей мере одного вышеупомянутого активного агента, при котором после кратковременного стимулирующего лечения антагонистом LHRH следует введение андрогена, отличного от 17-α-алкилзамещенного тестостерона.
Согласно другому аспекту данного изобретения предложено применение антагониста LHRH и по меньшей мере одного вышеупомянутого активного агента, причем после кратковременного стимулирующего лечения антагонистом LHRH следует комбинированное или раздельное введение по меньшей мере одного активного агента, выбранного из группы, состоящей из противозачаточного препарата, предпочтительно противозачаточного препарата для перорального применения, нестероидного противоревматического агента, анальгетика, андрогена, отличного от 17-α-алкилзамещенного тестостерона, или любых их комбинаций.
Согласно другому аспекту данного изобретения предложено применение антагониста LHRH и по меньшей мере одного вышеупомянутого активного агента, при котором антагонист LHRH вводят, начиная с ранней до средней фолликулярной фазы, предпочтительно в первый - третий дни цикла.
Согласно другому аспекту данного изобретения предложено применение антагониста LHRH и по меньшей мере одного вышеупомянутого активного агента, при котором антагонист LHRH выбирают из группы, состоящей из цетрореликса, тевереликса, ганиреликса, антида, абареликса и D-63153.
Согласно другому аспекту данного изобретения предложено применение антагониста LHRH и по меньшей мере одного вышеупомянутого активного агента, при котором антагонист LHRH вводят в течение кратковременного стимулирующего лечения в течение 4-12 недель при еженедельной дозе от 3 до 10 мг/неделю.
Согласно другому аспекту данного изобретения предложено применение антагониста LHRH и по меньшей мере одного вышеупомянутого активного агента, при котором антагонист LHRH вводят в течение кратковременного стимулирующего лечения в течение приблизительно 4-12 недель при ежедневной дозе от 0,25 мг до 0,5 мг/день.
Согласно другому аспекту данного изобретения предложено применение антагониста LHRH и по меньшей мере одного вышеупомянутого активного агента, при котором антагонист LHRH вводят в течение кратковременного стимулирующего лечения в течение приблизительно 4-12 недель при ежемесячной дозе от 12 до 40 мг/месяц.
Согласно другому аспекту данного изобретения предложено применение антагониста LHRH и по меньшей мере одного вышеупомянутого активного агента, при котором антагонист LHRH применяют для стимулирующего лечения в течение от 4 до 12 недель и лечение повторяют два или три раза в год.
Изобретение относится к медицине, в частности к гинекологии, и касается лечения эндометриоза и состояний, с ним связанных. Для этого предлагают вводить антагонист LHRH курсами продолжительностью 4-12 недель. При этом дополнительно одновременно или последовательно вводят нестероидные противовоспалительные средства, анальгетики, противозачаточные препараты, андрогены. Изобретение обеспечивает предупреждение возврата симптоматики эндометриоза при отсутствии симптомов эстрогенной недостаточности. 4 н. и 13 з.п. ф-лы, 2 ил.
| US 5658884, 19.08.1997 | |||
| WO 9855470, 10.12.1998 | |||
| WO 9727863, 07.08.1997 | |||
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОКАЗАНИЙ К ПРОВЕДЕНИЮ ГОРМОНОТЕРАПИИ У БОЛЬНЫХ ГЕНИТАЛЬНЫМ ЭНДОМЕТРИОЗОМ | 1996 |
|
RU2108583C1 |
| СМЕТНИК В.П | |||
| и др | |||
| Неоперативная гинекология, СПб, Сотис, 1995, кн.2, с.89-93 | |||
| ЯРОЦКАЯ Е.П | |||
| Клиническая эффективность антигормонов в комбинированном лечении распространенных форм наружного генитального эндометриоза, М., 1995, с.20-33. | |||
Авторы
Даты
2005-07-10—Публикация
2000-09-20—Подача