Предлагаемое изобретение относится к биологии и медицине и может быть применено для очистки биологических жидкостей и приведения их состава к физиологическим нормам.
Известен магнитоуправляемый сорбент (МУС), выполненный из железа в виде кристаллов размерами (10-15) нм (см., например, авторское свидетельство СССР № 1589327 с приоритетом от 14.04.1988 г., МПК С 01 G 49/08).
Известный сорбент оказывает бактерицидное действие, однако он ограничен в применении, так как может использоваться только “in vitro”.
Наиболее близким аналогом-прототипом является магнитоуправляемый сорбент (МУС), с ядром в виде фракции гранулометрического состава величиной (0,1-1000) км, выполненным из железа, или из окислов железа, или из никеля, или из железоникелевого сплава и покрытым одно- или двухслойной оболочкой, выполненной или из углерода, или из оксидов алюминия, или из диоксида кремния, или из диоксида циркония, или из декстрана, например из сефадекса, или из желатина, или из альбумина, или из полисахарида, например крахмала, или из ионообменных смол, например катионов или анионов, причем наружный слой оболочки выполнен или конъюгированным с антителами, или модифицирован лекарственным препаратом, например антибиотиком, или солями фталгидразида, например солями 5-амино-2,3-дигидро-1,4-диона, или выполнен ферментированным, например уреазой (см., например, патент РФ № 2178313 с приоритетом от 29.08.2000 г., МПК А 61 М 1/16).
Этот сорбент является эффективным средством при экстракорпоральном восстановлении биологических жидкостей до физиологических норм, обеспечивая очистку, например крови, от низко-, средне- и высокомолекулярных экзо- и эндотоксинов без нарушения ее реологических свойств, коррекцию ферментного и иммунного состава биологических жидкостей, а также уничтожение патогенной микрофлоры вирусов и ретровирусов. Однако, поскольку такой сорбент является весьма дорогим препаратом, а для проведения соответствующего курса лечения требуется большое количество этого сорбента, на лечение с его применением требуются значительные финансовые затраты.
Известен способ получения магнитоуправляемого сорбента (см., например, авторское свидетельство СССР № 1589327 с приоритетом от 14.04.1988 г., МПК5 С 01 G 49/08), включающий процедуру испарения порошка железа в низкотемпературной (104·(0,5-5)К) плазме в атмосфере аргона, а полученный парообразный продукт резко охлаждают и конденсируют в газовом потоке аргона, а затем осажденный продукт в виде кристаллов переносят в дисперсионную среду, содержащую стабилизатор, например воду при рН 7-9 или масло, и, перемешивая, выдерживают там в течение (10-15) часов при температуре (50-90)° С и при остаточном давлении (1-3) мм рт. ст. до завершения газоотделения.
Известный способ обеспечивает возможность получения сорбента в виде частиц (кристаллов) железа размерами (10-15) нм, однако этот сорбент из-за малых размеров частиц обладает низкими значениями магнитной восприимчивости, в связи с чем для выведения сорбента из биологических сред требуется применение магнитных полей напряженностью (1-3) Тл, что по медико-санитарным нормам недопустимо (см., например, описание к патенту РФ № 2109522 с приоритетом от 01.08.1996 г., МПК6 А 61 М 1/36).
Наиболее близким аналогом-прототипом является способ получения магнитоуправляемого сорбента (см., например, патент РФ № 2109522 с приоритетом от 01.08.1996 г., МПК6 А 61 М 1/36), включающий фракционирование высокодисперсного порошка Ferrum reductum в потоке инертного газа со скоростью (0,02-1,00) м/с при воздействии магнитного поля напряженностью (10-103) А/м с последующей термической обработкой полученных частиц железа при температуре (1000-1500)° С в потоке инертного газа, содержащего микрочастицы угля и/или окиси кремния, и/или окиси алюминия, после которой поверхность частиц ферросорбента покрывают биологически активными соединениями - пищевыми белками или декстраном, или лекарственными препаратами, или антителами.
Такой способ обеспечивает возможность получения магнитоуправляемого сорбента определенного химического состава, эффективного при удалении “in vivo” и “in vitro” низко-, средне- и высокомолекулярных токсинов, микрофлоры и ретровирусов. Однако этот способ ограничен возможностью получения сорбента с объемными частицами, преимущественно имеющими соразмерные габариты в плане и по толщине, размером (0,5-2,5) мкм и соответствующую такой форме величину поверхности этих частиц.
Задачей данного изобретения является разработка и получение магнитоуправляемого сорбента, обладающего существенно большей поверхностью частиц без значительного увеличения массы его ядра, а также способа получения такого сорбента.
Сущность изобретения состоит в том, что в магнитоуправляемом сорбенте, включающем ядро из ферромагнетика, с одно- или двухслойной оболочкой или без оболочки, ядро выполнено в виде пластинки, габариты которой в плоскости составляют (500-5000) мкм, а толщина равна (0,1-1000) мкм.
При этом ядро выполнено или из железа, или из оксидов железа, или из никеля, или из железоникелевого сплава, или из сплава железа или никеля с титаном, или из сплава железа или никеля с танталом, или из сплава железа, никеля и титана, или из сплава железа, никеля и тантала.
Кроме того, однослойная оболочка выполнена или из углерода, или из оксидов алюминия, или из диоксида кремния, или из диоксида циркония, или из декстрана, например из сефадекса, или из желатина, или из альбумина, или из полисахарида, например крахмала, или из ионообменных смол, например катионов или анионов.
При этом в двухслойной оболочке первый по отношению к ядру (внутренний) слой выполнен или из углерода, или из оксидов алюминия, или из диоксида кремния, или из диоксида циркония, а второй - наружный слой оболочки выполнен или из декстрана, например из сефадекса, или из желатина, или из альбумина, или из полисахарида, например крахмала, или из ионообменных смол, например катионов или анионов.
Кроме того, наружный слой оболочки выполнен или конъюгированным с антителами, или модифицирован лекарственным препаратом, например антибиотиком, или солями фталгидразида, например солями 5-амино-2,3-дигидро-1,4-диона, или выполнен ферментированным, например уреазой.
Сущность изобретения заключается в том, что в способе получения магнитоуправляемого сорбента, характеризующемся тем, что порошок или железа, или/и никеля, или/и титана, или/и тантала испаряют в низкотемпературной плазме с температурой 104·(0,5-5)К, а полученный парообразный в виде соответствующих металлов или соответствующих смесей металлов продукт резко охлаждают и конденсируют в газовом потоке, например, аргона и затем осажденный продукт в виде кристаллов или, соответственно, микрослитков сплавов соответствующих металлов переносят в дисперсионную среду, содержащую стабилизатор, например воду и/или масло, и, перемешивая, выдерживают там в течение (5-15) часов при температуре (50-90)° С и при остаточном давлении (1-5) мм рт. ст. до завершения газовыделения, после чего эти кристаллы или микрослитки обрабатывают, например, прессованием, например в шаровой мельнице, до получения пластинок заданной толщины, которые затем многократно (до 10 раз) промывают в дистиллированной воде, а потом отделяют слабые части пластин, воздействуя на них, например, в воде, ультразвуком мощностью, например (200-300) Вт/см2, затем сушат полученные пластинки, например, в сухожаровом шкафу при температуре (80-110)° С, после чего высушенные пластинки фракционируют или в потоке инертного газа со скоростью (0,02-1,00) м/с при воздействии магнитного поля напряженностью 5× (10-103) А/м или с помощью, например, центрофугирования, и выделяют ядра сорбента требуемой величины, на которых послойно формируют оболочки, а полученный целевой продукт расфасовывают в светозащищенные герметично закрытые емкости и стерилизуют, например, γ -излучением, причем в качестве целевого продукта может быть выбран также сорбент, полученный сразу после фракционирования.
При этом первый (ближайший к ядру) слой оболочки формируют путем термической обработки фракционированных пластинок при температуре (1000-1500)° С в потоке инертного газа, например аргона, содержащего микрочастицы углерода, или оксида кремния, или оксида алюминия, или оксида циркония.
Кроме того, первый слой оболочки формируют путем размешивания с помощью воздействия в течение (1-10) минут ультразвуком на взвесь фракционированных пластинок в нагретом до температуры (30-80)° С водном растворе декстрана, или желатина, или альбумина, или крахмала с последующим охлаждением этой взвеси до температуры (4-10)° С, а полученный осадок заливают формалином, выдерживают в нем в течение (10-40) минут с одновременным перемешиванием, после чего тщательно высушивают при температуре (25-50)° С, размельчают и полученные капсулы сорбента (целевого продукта) фильтруют в магнитном поле.
Кроме того, первый слой оболочки формируют путем добавления в нагретую до температуры (40-60)° С взвесь фракционированных пластинок в дистиллированной воде ионнообменной смолы, например, амберлайта с последующим охлаждением этой взвеси до температуры (15-30)° С, добавлением в нее разведенной в воде азотистой кислоты (HNO2), выдерживанием в течение (10-15) минут, охлаждением до температуры (4-10)° С и выделением осадка, который промывают в физиологическом растворе, буферируют до рН 4,0± 0,5 в водном растворе смеси основания NH4ОН и соли NH4Сl.
При этом второй слой оболочки формируют путем размешивания с помощью воздействия в течение (1-10) минут ультразвуком на взвесь ферромагнетиков, покрытых оболочкой из углерода, или оксида кремния, или оксида алюминия, или оксида циркония в нагретом до температуры (30-80)° С водном растворе декстрана, или желатина, или альбумина, или крахмала с последующим охлаждением этой взвеси до температуры (4-10)° С, а полученный осадок заливают формалином, выдерживают в нем в течение (10-40) минут с одновременным перемешиванием, после чего тщательно высушивают при температуре (25-50)° С, размельчают и полученные капсулы сорбента (целевого продукта) фильтруют в магнитном поле.
Кроме того, второй слой оболочки формируют путем добавления в нагретую до температуры (40-60)° С взвесь ферромагнетиков, покрытых оболочкой из углерода, или оксида кремния, или оксида алюминия, или оксида циркония в дистиллированной воде ионнообменной смолы, например, амберлайта с последующим охлаждением этой взвеси до температуры (15-30)° С и введением с перемешиванием альбумина, например в виде сыворотки, с последующим добавлением в нее разведенной в воде азотистой кислоты (HNO2), выдерживанием в течение (10-15) минут, охлаждением до температуры (4-10)° С и выделением осадка, который активизируют, выдерживая в течение (1,5-2) часов в растворе модификатора, промывают в физиологическом растворе, буферируют до рН 4,0± 0,5 в водном растворе смеси основания NH4ОН и соли NH4Сl.
При этом в качестве модификатора используют периодат натрия (NaIO4) или глутаровый альдегид в (3-10)% растворе Na2SO4 в воде.
Кроме того, при формировании наружного слоя оболочки ее конъюгируют с антителами, путем добавления в водную суспензию магнитоуправляемого сорбента с одной или двумя оболочками, но с наружной оболочкой из сефадекса или альбумина, модифицированной, например, глутаровым альдегидом или периодатом натрия, сыворотки, например крови, содержащей антитела, специфичные к сорбируемому антигену, например антигену системной красной волчанки, в буферной жидкости с рН 6,5-10, выдерживания с перемешиванием этого состава в течение (1-3) часов при температуре (15-25)° С, последующего введения в этот состав боргидрида натрия, охлаждения до температуры (4-10)° С, повторного выдерживания с перемешиванием в течение (1-3) часов, извлечения осадка и его буферирования и высушивания.
Кроме того, при формировании наружного слоя оболочки ее модифицируют лекарственным препаратом путем нагревания до температуры (35-70)° С суспензии магнитоуправляемого сорбента с одной или двумя оболочками, но с наружной оболочкой, например, из декстрана или желатина, в физиологическом растворе, добавления туда порошка лекарственного препарата, например антибиотика, например оксациллина, выдерживания при тщательном перемешивании при вышеуказанной температуре в течение (0,5-2,5) часов, последующего охлаждения этой смеси до температуры (4-10)° С, декантирования надосадочной жидкости в магнитном поле, промывания осадка в проточной дистиллированной воде и его последующего высушивания.
Кроме того, при формировании наружного слоя оболочки ее модифицируют путем предварительного растворения кристаллов уреазы в полиэфире, например дибензо-18 краун 6, смешивания этого раствора со взвесью в дистиллированной воде магнитоуправляемого сорбента с оболочкой, например из сефадекса, выдерживания с перемешиванием при температуре (25-40)° С в течение (2-5) часов и охлаждения до температуры (4-10)° С, последующего добавления формальдегида и повторного выдерживания в течение (1-3) часов, сливания надосадочной жидкости в присутствии магнитного поля и высушивания осадка.
Кроме того, при формировании наружного слоя оболочки ее модифицируют путем нагревания водной суспензии магнитоуправляемого сорбента с оболочкой, например, из декстрана, до температуры (40-70)° С, последующего смешивания с порошком соли циркония, например соответствующей соли фталгидразида, и воздействия в течение (1-10) минут на эту смесь ультразвуком интенсивностью (50-120) Вт/см2, охлаждения образовавшейся смеси до температуры (4-10)° С, добавления формальдегида, выдерживания с перемешиванием в течение (1-3) часов, сливания надосадочной жидкости в присутствии магнитного поля и высушивания осадка.
Техническим результатом предложенного изобретения является обеспечение возможности эффективной гемоперфузии при магнитной терапии за счет подбора формы и размеров ядра магнитоуправляемого сорбента, а также способа получения такого сорбента, что позволяет обеспечить эффективную очистку биологических жидкостей, например крови, от экзо- и эндотоксинов без нарушения ее реологических свойств, обеспечить возможность коррекции ферментного и иммунного состава биологических жидкостей, а также уничтожения патогенной микрофлоры вирусов и ретровирусов при использовании существенно меньшего (в весовом отношении) предлагаемого по сравнению с ранее требуемым количеством известного аналогичного магнитоуправляемого сорбента.
Так, принимая во внимание, что очистка биологической жидкости с помощью магнитоуправляемого сорбента происходит путем взаимодействия его поверхности с корректируемой жидкостью, можно показать, что эффективная поверхность частицы известного сорбента, габариты которой по длине и ширине и толщине в среднем соизмеримы, при сохранении массы частиц существенно меньше поверхности частицы предложенного сорбента.
Возьмем для примера частицу в виде шара.
Пользуясь известными математическими формулами, получаем, что, так как величина объема шара (Vшара) равна
Vшара=4π r3/3, где r - радиус шара,
и соответственно величина поверхности шара (Sшара) равна
Sшара=4π r2,
то

Учитывая, что масса частицы пропорциональна ее объему, и предполагая, что после описанной выше процедуры получения частиц сорбента в виде пластинок, частица сорбента в виде шара будет преобразована в круглую пластинку, то, так как объем этой пластинки Vпластинки=π R2δ, а площадь поверхности Sповерхн.пласт.=π R2, где R - радиус пластинки, а δ - ее толщина, причем δ =0,1r (в соответствии с вышесказанным утверждением об уменьшении толщины частицы на порядок), то имеем, что
площадь поверхности Sповерхн.пласn.=Vпластинки/0,1 r.
Принимая во внимание, что Vпластинки=Vшара, то, так как их массы равны, получаем, что
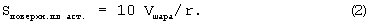
Учитывая, что таких поверхностей на пластинке две, и подставляя выражение (1) в формулу (2), имеем:
Sполной поверхн.пласт.=20 Sшара/3.
Полученные результаты подтверждают вышесказанное предположение, что в случае использования предложенного сорбента существенно увеличивается поверхность взаимодействия каждой его частицы с биологической жидкостью, а, следовательно, уменьшается и его расходование и соответственно затраты на лечение с его применением.
Магнитоуправляемый сорбент выполняют в виде ядра с одной и двумя оболочками, окружающими это ядро и без оболочки.
В качестве ядер магнитоуправляемого сорбента берут порошок из ферромагнетиков, например из железа (Fe), его оксидов (Fe2О3 или Fе3O4), никеля (Ni), железоникелевых сплавов, а также из сплава железа или никеля с титаном (Ti), или из сплава железа или никеля с танталом (Та), или из сплава железа, никеля и титана, или из сплава железа, никеля, тантала и титана и т.п. магниточувствительных материалов.
Для последующего использования выбирают фракции в виде пластинок габаритами в плоскости - (500-5000) мкм и толщиной - (0,1-1000) мкм.
Для получения ядер магнитоуправляемого сорбента, порошок с размерами частиц (102-105) нм или железа, или/и никеля, или/и титана, или/и тантала испаряют в низкотемпературной плазме с температурой 104·(0,5-5)К, а полученный парообразный в виде соответствующих металлов или соответствующих смесей металлов продукт с концентрацией (0,1-0,5) об.% резко охлаждают до температуры (50-80)° С и конденсируют в реакторе (см., например, описание к авторскому свидетельству СССР №1589327 с приоритетом от 14.04.1988 г., МПК5 С 01 G 49/08) в газовом потоке, например, аргона и затем осажденный продукт в виде кристаллов или, соответственно, микрослитков сплавов соответствующих металлов, например в количестве (0,05-10) мг, переносят в дисперсионную среду, содержащую стабилизатор, например, дистиллированную воду объемом (50-500) мл при рН 7-9 и/или минеральное, например вазелиновое, или растительное, например, оливковое или облепиховое, масло, куда предварительно вносят, например олеиновую кислоту в количестве (2-20) об.% и, перемешивая, выдерживают там в течение (5-15) часов при температуре (50-90)° С и при остаточном давлении (1-5) мм рт. ст. до завершения газовыделения.
Затем эти кристаллы или микрослитки обрабатывают, например прессованием, например, в шаровой мельнице, до получения пластинок заданной толщины, которые потом многократно (до 10 раз) промывают в дистиллированной воде, а затем отделяют слабые части пластин, воздействуя на них, например в воде, ультразвуком мощностью, например,(200-300) Вт/см2.
Полученный материал (разногабаритные пластинки и отколовшиеся кусочки) общей массой сушат, например, в сухожаровом шкафу при температуре (80-110)° С, а затем высушенный продукт (пластинки) фракционируют или в потоке инертного газа со скоростью (0,02-1,00) м/с при воздействии магнитного поля напряженностью 5× (10-103) А/м или с помощью, например, центрофугирования, и выделяют сорбент (пластинки) требуемой величины в качестве ядер, на которых послойно формируют оболочки, а полученный целевой продукт расфасовывают в светозащищенные герметично закрытые емкости и стерилизуют, например, γ -излучением, причем в качестве целевого продукта может быть выбран также сорбент, полученный сразу после фракционирования. Выход кондиционных ядер сорбента после фракционирования составляет (60-75)%.
Для получения (формирования) первого (ближайшего к ядру) слоя оболочки фракционированные пластинки подвергают термической (при температуре (1000-1500)° С) обработке в термопечи, в потоке инертного газа, например аргона, содержащего микрочастицы или углерода (С), или оксида кремния (SiO2), или оксида алюминия (Аl2О3 или Аl3O4), или оксида циркония (ZrO2). Скорость потока составляет (0,02-1,2) м/с. Качество покрытия ядер зависит от скорости пропускания потока инертного газа, а также от насыщенности этого газа микрочастицами материала оболочки и величины этих микрочастиц. В приведенных примерах толщина получаемого таким способом слоя оболочки составляет (0,2-50) мкм.
Полезный выход сорбента - (70-85)%.
При формировании первого слоя оболочки путем “обволачивания” ядер магнитоуправляемого сорбента такими веществами, как или декстран, или желатин, или альбумин, или крахмал, взвесь фракционированных пластинок в количестве (2-20) г в (10-50) мл дистиллированной воды смешивают с (50-100) мл нагретого до температуры (30-80)° С водного раствора или декстрана, или желатина, или альбумина, или крахмала, находящихся в нем в соотношении (об.%): (50-95)% - соответствующий продукт, остальное - вода, размешивают в течение (1-10) минут до получения гомогенного состава воздействием с помощью, например, ультразвукового диспергатора УЗДН-2Т (см., например, описание к авторскому свидетельству СССР № 1684616) ультразвуком с частотой колебаний (10-15) кГц и интенсивностью (50-120) Вт/см2, затем охлаждают эту взвесь, например в холодильнике, до температуры (4-10)° С, а полученный осадок заливают формалином (водный раствор НСНО), выдерживают в нем в течение (10-40) минут с одновременным перемешиванием, после чего тщательно высушивают при температуре (25-50)° С, размельчают и полученные капсулы сорбента (целевого продукта) фильтруют в магнитном поле напряженностью 5× (10-103) А/м, например, постоянного магнита, выполненного из самарий (Sm)-кобальтового (Со) сплава.
Толщина получаемого таким способом слоя оболочки составляет (0,5-3) мм.
Количественный выход сорбента составляет (85-95)% от исходного.
При формировании первого слоя оболочки путем использования ионнообменной смолы, в нагретую до температуры (40-60)° С взвесь фракционированных пластинок в количестве (2-5) г на (10-100) мл дистиллированной воды добавляют, например, (10-25) г амберлайта, затем охлаждают полученный состав до температуры (15-30)° С, добавляют разведенную в воде (в количестве (1-10) об.%) азотистую кислоту (НNO3), выдерживают в течение (10-15) минут, снова охлаждают до температуры (4-10)° С и выделяют осадок, который промывают в физиологическом растворе, буферируют до рН 4,0±0,5 в водном растворе основания NH4OH и соли NH4Cl.
Толщина получаемого таким способом слоя оболочки составляет (0,2-1) мм.
Количественный выход сорбента составляет (90-92)% от исходного.
При формировании второго слоя оболочки путем “обволачивания” магнитоуправляемого сорбента, покрытого оболочкой из углерода, или оксида кремния, или оксида алюминия, или оксида циркония такими веществами, как или декстран, или желатин, или альбумин, или крахмал, взвесь ферромагнетиков в количестве (2-20) г на (10-50) мл дистиллированной воды, покрытых оболочкой из углерода, или оксида кремния, или оксида алюминия, или оксида циркония, в течение (1-10) минут с помощью воздействия ультразвуком интенсивностью (50-120) Вт/см2 размешивают в (50-100) мл нагретого до температуры (30-80)° С (50-95)% раствора декстрана, или желатина, или альбумина, или крахмала в дистиллированной воде с последующим охлаждением этой взвеси до температуры (4-10)° С. Выделенный осадок заливают формалином, выдерживают в нем в течение (10-40) минут с одновременным перемешиванием, после чего тщательно высушивают при температуре (25-50)° С, размельчают и полученные капсулы сорбента (целевого продукта) фильтруют в магнитном поле напряженностью 5× (10-103) А/м.
Толщина получаемого таким способом этого слоя оболочки составляет (0,5-3) мм.
Количественный выход сорбента составляет (85-95)% от исходного.
При формировании второго слоя оболочки путем использования ионно-обменной смолы, взвесь в количестве (0,2-0,5) г на (10-100) мл дистиллированной воды ферромагнетиков, покрытых оболочкой из углерода, или оксида кремния, или оксида алюминия, или оксида циркония нагревают до температуры (40-60)° С, добавляют, например, (1-2) г амберлайта, затем охлаждают полученный состав до температуры (15-30)° С, добавляют разведенную в воде (в количестве (1-10) об.%) азотистую кислоту (НNО3), выдерживают в течение (10-15) минут, снова охлаждают до температуры (4-10)° С и выделяют осадок, который активизируют, выдерживая в течение (1,5-2) часов в растворе модификатора, промывают в физиологическом растворе и буферируют до рН 4,0±0,5 в водном растворе основания NF4OH и соли NH4Cl. При этом в качестве модификатора используют периодат натрия (NaIO4) или глутаровый альдегид в (3-10)% растворе Nа2SO4 в воде.
Толщина получаемого таким способом этого слоя оболочки составляет (0,2-1) мм.
Количественный выход сорбента составляет (90-95)% от исходного.
Кроме того, при формировании наружного слоя оболочки ее конъюгируют с антителами путем добавления в водную суспензию магнитоуправляемого сорбента с одной или двумя оболочками, но с наружной оболочкой из сефадекса или альбумина, модифицированной, например, глутаровым альдегидом или периодатом натрия, сыворотки, например крови (в количестве (1-50) мл сыворотки на (100-150) мл суспензии), содержащей антитела, специфичные к сорбируемому антигену, например антигену системной красной волчанки, в буферной жидкости с рН 6,5-10, выдерживания с перемешиванием этого состава в течение (1-3) часов при температуре (15-25)° С, последующего введения в этот состав боргидрида натрия, охлаждения до температуры (4-10)° С, повторного выдерживания с перемешиванием в течение (1-3) часов, извлечения осадка и его буферирования и высушивания.
Толщина соответствующего слоя оболочки увеличивается при этом на (0,2-0,5) мм.
Количественный выход сорбента составляет (92-95)% от исходного.
Кроме того, при формировании наружного слоя оболочки ее модифицируют лекарственным препаратом путем нагревания до температуры (35-70)° С водной суспензии магнитоуправляемого сорбента (на 50 мл дистиллированной воды - (10-20) г сорбента) с одной или двумя оболочками, но с наружной оболочкой, например, из декстрана или желатина, в физиологическом (0,9% растворе NaCl в дистиллированной воде) растворе, добавления туда порошка лекарственного препарата (в количестве (1-5) г на (10-50) мл суспензии), например антибиотика, например оксациллина, выдерживания при тщательном перемешивании при вышеуказанной температуре в течение (0,5-2,5) часов, последующего охлаждения этой смеси до температуры (4-10)° С, декантирования надосадочной жидкости в магнитном поле напряженностью 5× (10-103) А/м, промывания осадка в проточной дистиллированной воде и его последующего высушивания при температуре (25-40)° С.
Толщина соответствующего слоя оболочки увеличивается при этом на (0,01-0,1) мм.
Количественный выход сорбента составляет (90-95)% от исходного.
Кроме того, при формировании наружного слоя оболочки ее модифицируют путем предварительного растворения, например, (1-5) г кристаллов уреазы в (10-15) мл полиэфира, например дибензо-18 краун 6, смешивания этого раствора со взвесью в дистиллированной воде магнитоуправляемого сорбента ((10-15) г сорбента на (50-100) мл воды) с оболочкой, например из сефадекса-10, выдерживания с перемешиванием при температуре (25-40)° С в течение (2-5) часов и охлаждения до температуры (4-10)° С, последующего добавления формальдегида ((25-30) мл на 100 мл смеси) и повторного выдерживания с перемешиванием в течение (1-3) часов, сливания надосадочной жидкости в присутствии магнитного поля напряженностью 5× (10-103) А/м и высушивания осадка, например, в сушильном шкафу при температуре (50-85)° С.
Толщина соответствующего слоя оболочки увеличивается при этом на (0,5-1) мм.
Количественный выход сорбента составляет (90-95)% от исходного.
Кроме того, при формировании наружного слоя оболочки ее модифицируют путем нагревания до температуры (40-70)° С водной суспензии магнитоуправляемого сорбента с оболочкой, например, из декстрана, ((15-20) г сорбента на 75-100 мл дистиллированной воды), последующего смешивания с порошком соли циркония, например соответствующей соли фталгидразида, например 5-амино-2,3-дигидро-1,4-диона, и воздействия в течение (1-10) минут на эту смесь ультразвуком с частотой колебаний (15-25) кГц и интенсивностью (50-120) Вт/см2, охлаждения образовавшейся смеси до температуры (4-10)° С, добавления формальдегида ((25-30) мл на 100 мл смеси), выдерживания в нем с перемешиванием в течение (1-3) часов, сливания надосадочной жидкости в присутствии магнитного поля напряженностью 5× (10-103) А/м и высушивания осадка при температуре (25-45)° С.
Толщина соответствующего слоя оболочки увеличивается при этом на (0,01-0,1) мм.
Количественный выход сорбента составляет (90-95)% от исходного.
Возможность эффективного применения предложенного полученного вышеприведенными способами магнитоуправляемого сорбента (МУС), подтверждается примерами:
Пример 1. Беспородной собаке весом 12 кг ввели (per os) 4,3 г веронала. Через 45 мин количество барбитурата в крови 118 мкг/мл.
Проведена процедура экстракорпорального восстановления (коррекции) крови с помощью соответствующего устройства (УКБЖ-1). Кровь животного выводилась порциями по 10 мл, которые смешивались в равных соотношениях объемов с суспензией МУСа в физиологическом растворе, включавшей (мас.%): МУС (ядра - пластинки никеля, внутренняя оболочка - углерод, наружная - декстран) - 1,5; антикоагулянт (гепарин) - 0,015; физиологический раствор - остальное, выдерживалась в течение 2-3 секунд и вводилась животному обратно.
За сеанс пропущено около 1 литра крови.
Показания до и после сеанса коррекции:
Кроме того, за время сеанса проведено промывание желудка, внутривенно животному введено 500 мл раствора электролитов и 2% глюкозы.
После сеанса состояние средней тяжести, рефлексы живые.
В последующих примерах приведены данные сорбционной эффективности, а также селективных и функциональных свойств известных магнитоуправляемых сорбентов, приведенные, например, в описании к патенту РФ № 2178313 (см., например, патент РФ № 2178313 с приоритетом от 29.08.2000 г., МПК А 61 М 1/16) и результатов, полученных при проведении исследований с магнитоуправляемыми сорбентами, предлагаемыми в данном изобретении.
Пример 2. В пробирку со 100 мл крови беспородной собаки ввели 5 мл раствора карбофоса. Концентрация карбофоса в крови - 0,015 мкг/мл.
Полученную смесь разделили на две части и в каждую ввели по 20 мл суспензии МУСа, причем в одну - суспензию в физиологическом растворе известного МУСа (ядра - частицы железа, оболочки - оксид кремния) в количестве 1,0 г, а в другую предложенного того же состава материала, но ядра - пластинки, в количестве 0,1 г.
После перемешивания полученных составов в течение 1,5 минут надосадочная жидкость декантирована, а осадок удержан с помощью магнита.
Концентрация карбофоса в надосадочной жидкости, полученной от первого состава 0,002 мкг/мл, а в надосадочной жидкости, полученной от второго состава, 0,012 мкг/мл.
Пример 3. В пробирки, содержащие по 20 мл сыворотки крови собаки со смоделированной почечной недостаточностью (в первой - мочевина в концентрации 26,4 м моль/л, во второй - 30,2 м моль/л), внесены - в первую 200 мг известного МУСа с оболочкой из сефадекса-10, ферментированной уреазой, а во вторую - 30 мг предлагаемого МУСа с ядрами в виде титановых пластинок с оболочками, аналогичными вышеуказанным.
После выдержки (со встряхиванием) полученных составов в течение 5 секунд и удаления надосадочной жидкости в магнитном поле концентрация содержания мочевины в надосадочной жидкости в первой пробирке - 10,7 м моль/л, во второй - 12,1 м моль/л.
Пример 4. В пробирки по 20 мл с раствором натриевой соли фосфорной кислоты (NaH2PO4) в воде внесены - в первую 100 мг известного МУСа с оболочкой из ионообменной смолы, модифицированной катионами (полисахариды с СООH+ груп.), во вторую 10 мг предлагаемого МУСа с ядрами из танталовых пластинок с оболочками, аналогичными вышеуказанным.
После перемешивания (встряхиванием) полученных составов и удаления в магнитном поле надосадочной жидкости концентрация фосфатов в надосадочной жидкости, полученной из первой пробирки, уменьшилась на 57% относительно начальной, а в надосадочной жидкости, полученной из второй пробирки, соответственно уменьшилась почти наполовину (на 44,8%) от начальной концентрации фосфатов.
Пример 5. В пробирки, содержащие по 20 мл раствора солей сернистой кислоты в воде, внесены - в первую 100 мг известного МУСа с оболочкой из ионообменной смолы, модифицированной анионитами (с NН3 × - груп.), во вторую - 20 мг предлагаемого МУСа с ядрами из железоникелевых пластинок с оболочками, аналогичными вышеуказанным.
После перемешивания (встряхиванием) полученных составов и удаления в магнитном поле надосадочной жидкости, концентрация солей сернистой кислоты в надосадочной жидкости, полученной из первой и второй пробирок, практически одинаково
уменьшилась - в первой - на 72% относительно начальной концентрации, а во второй - на 73, 4%.
Пример 6. В пробирки, содержащие по 20 мл крови больного хронической почечно-печеночной недостаточностью, внесены - в первую 100 мг известного МУСа с оболочкой из декстрана, модифицированной циркониевой солью люминола, во вторую - 30 мг предлагаемого МУСа с ядрами из железотитановых пластинок с оболочками, аналогичными вышеуказанным.
После перемешивания (встряхиванием) полученных составов и удаления в магнитном поле надосадочной жидкости концентрация солей фосфорной кислоты (NaH2PO4) в надосадочной жидкости, полученной из первой пробирки, - 0,07 мг/мл, а полученной из второй пробирки, - 0,021 мг/ мл. (Начальная концентрация этой соли - 0,61 мг/мл.)
Пример 7. В пробирки, содержащие по 10 мл сыворотки крови больного хронической почечно-печеночной недостаточностью, внесены - в первую 50 мг известного МУСа (ядра - частицы из железоникелевого сплава, оболочки из сефадекса и модифицированы уреазой), во вторую - 10 мг предлагаемого МУСа (ядра - пластинки из железоникелевого сплава, с оболочками, аналогичными вышеуказанным).
После выдерживания в течение 10 секунд и декантирования надосадочной жидкости (проведения сорбции) концентрация мочевины в надосадочной жидкости, полученной из первой пробирки, на 23% меньше начальной концентрации мочевины в сыворотке крови, а концентрация мочевины в надосадочной жидкости, полученной из второй пробирки, на 35% меньше начальной концентрации мочевины.
Пример 8. В пробирки, содержащие по 20 мл крови больного сепсисом, внесены - в первую 150 мг известного МУСа с ядрами из железоникелевого сплава и оболочкой из желатина, модифицированного оксациллином, во вторую - 15 мг предлагаемого МУСа (ядра-пластинки из сплава железа, никеля, титана и тантала, с оболочками, аналогичными вышеуказанным).
После перемешивания встряхиванием содержимого пробирок в течение 2 минут надосадочная жидкость декантирована, твердая составляющая удержана магнитным полем.
Произведен посев на агар-агаре крови, взятой у больного и крови, подвергнутой воздействию МУСа - надосадочной жидкости, взятой из каждой пробирки.
В посеве от взятой крови наблюдался рост колоний стрептококка и золотистого стафилококка, в посеве от крови, взятой из пробирок, роста колоний не наблюдалось.
Пример 9. В пробирки, содержащие по 10 мл плазмы лимфы больной сепсисом, внесены - в первую 100 мг известного МУСа (ядра - железоникелевый сплав, оболочки из декстрана), во вторую 15 мг предлагаемого МУСа (ядра - пластинки из сплава железа, никеля, титана и тантала, с оболочками, аналогичными вышеуказанным).
После перемешивания (встряхиванием) полученных составов и удаления в магнитном поле надосадочной жидкости произведен посев на агар-агаре лимфы, взятой у больной, и лимфы (надосадочной жидкости), подвергнутой воздействию МУСа.
В посеве от лимфы без лимфосепарации наблюдались множественные колонии стафилококка, в посеве от надосадочных жидкостей колонии практически отсутствуют.
Пример 10. В пробирки, содержащие по 5 мл ликвора, окрашенного кровью (больной с черепно-мозговой травмой), внесены - в первую 50 мг известного МУСа (ядра - железо, оболочки из диоксида кремния), во вторую 15 мг предлагаемого МУСа (ядра - пластинки из сплава железа и тантала, с оболочками, аналогичными вышеуказанным).
После осаждения ликвор в пробирках приобрел светло-желтый цвет.
Эффективность применения разработанного препарата подтверждена в экспериментах при исследовании сорбционной способности МУСа для каждого из вышеприведенных вариантов его выполнения и, при этом, результаты, сопоставимые с результатами использования аналогичных вариантов известного МУСа, достигались при значительно меньших количествах предложенного сорбента.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ ДЛЯ ЭКСТРАКОРПОРАЛЬНОЙ ОБРАБОТКИ БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ И СПОСОБ ПОЛУЧЕНИЯ МАГНИТОУПРАВЛЯЕМОГО СОРБЕНТА ДЛЯ ЕЕ ОСУЩЕСТВЛЕНИЯ (ВАРИАНТЫ) | 2000 |
|
RU2178313C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИОННОГО МАГНИТНОГО МАТЕРИАЛА НА ОСНОВЕ ОКСИДОВ КРЕМНИЯ И ЖЕЛЕЗА | 2014 |
|
RU2575458C1 |
| СИСТЕМА КОРРЕКЦИИ БИОЛОГИЧЕСКОЙ ЖИДКОСТИ | 2003 |
|
RU2252037C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАГНИТОУПРАВЛЯЕМОГО КОМПОЗИТА ДЛЯ БИОМЕДИЦИНСКИХ ЦЕЛЕЙ | 1996 |
|
RU2109522C1 |
| МАГНИТОУПРАВЛЯЕМЫЙ СОРБЕНТ ДЛЯ УДАЛЕНИЯ БИЛИРУБИНА ИЗ БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ | 2012 |
|
RU2524620C2 |
| МЕТАЛЛИЧЕСКИЕ ПИГМЕНТЫ С АНТИКОРРОЗИЙНЫМИ ПОКРЫТИЯМИ НА ОСНОВЕ АЛЮМИНИЯ И/ИЛИ ЕГО СПЛАВОВ | 2020 |
|
RU2746989C1 |
| МАГНИТОУПРАВЛЯЕМЫЙ СОРБЕНТ, СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2008 |
|
RU2356620C1 |
| МАТРИЦА ИММУНОСОРБЕНТА | 1998 |
|
RU2140084C1 |
| ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ, ОБЛАДАЮЩИЕ ИММУНОМОДУЛИРУЮЩИМ, ПРОТИВОВОСПАЛИТЕЛЬНЫМ И ПРОТИВООПУХОЛЕВЫМ СВОЙСТВАМИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2004 |
|
RU2295338C2 |
| ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ, ОБЛАДАЮЩИЕ ИММУНОМОДУЛИРУЮЩИМ, ПРОТИВОВОСПАЛИТЕЛЬНЫМ И ПРОТИВООПУХОЛЕВЫМ СВОЙСТВАМИ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2004 |
|
RU2295335C2 |
Изобретение относится к биологии и медицине и может быть применено для очистки биологических жидкостей. Сорбент содержит ядро из ферромагнетика, с одно- или двухслойной оболочкой или без оболочки, ядро выполнено в виде пластинки, габариты которой в плоскости составляют (500-5000) мкм, а толщина равна (0,1-1000) мкм. Способ получения магнитоуправляемого сорбента характеризуется тем, что порошок или железа, или/и никеля, или/и титана, или/и тантала испаряют в низкотемпературной плазме, полученный продукт охлаждают и конденсируют в газовом потоке, затем осажденный продукт переносят в дисперсионную среду, содержащую стабилизатор, после чего кристаллы или микрослитки обрабатывают до получения пластинок заданной толщины, которые затем промывают в дистиллированной воде, отделяют слабые части пластин, воздействуя на них ультразвуком, сушат, высушенные пластинки фракционируют и выделяют ядра сорбента требуемой величины, на которых послойно формируют оболочки. Получен магнитоуправляемый сорбент, обладающий существенно большей поверхностью частиц без значительного увеличения массы его ядра, обеспечивающий эффективную очистку биологических жидкостей. 2 н. и 14 з.п. ф-лы.
| КОМПОЗИЦИЯ ДЛЯ ЭКСТРАКОРПОРАЛЬНОЙ ОБРАБОТКИ БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ И СПОСОБ ПОЛУЧЕНИЯ МАГНИТОУПРАВЛЯЕМОГО СОРБЕНТА ДЛЯ ЕЕ ОСУЩЕСТВЛЕНИЯ (ВАРИАНТЫ) | 2000 |
|
RU2178313C1 |
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| СПОСОБ ХРОМАТОГРАФИЧЕСКОГО РАЗДЕЛЕНИЯ ПАРОФАЗНОЙ СМЕСИ | 1994 |
|
RU2065606C1 |
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| СПОСОБ ПОЛУЧЕНИЯ МАГНИТОУПРАВЛЯЕМОГО КОМПОЗИТА ДЛЯ БИОМЕДИЦИНСКИХ ЦЕЛЕЙ | 1996 |
|
RU2109522C1 |
| Прибор с двумя призмами | 1917 |
|
SU27A1 |
| Способ получения магнитоуправляемого композиционного материала | 1988 |
|
SU1589327A1 |
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
| US 5980479 A | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| МАТРИЦА ИММУНОСОРБЕНТА | 1998 |
|
RU2140084C1 |
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| МАГНИТОУПРАВЛЯЕМЫЙ НОСИТЕЛЬ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 1992 |
|
RU2030918C1 |
| Прибор для промывания газов | 1922 |
|
SU20A1 |
Авторы
Даты
2005-07-10—Публикация
2003-10-14—Подача