Настоящее изобретение относится к применению 4-хлор-5-[(4,5-дигидро-1Н-имидазол-2-ил)амино]-6-метокси-2-метилпиримидина (моксонидина) и его физиологически приемлемых кислотно-аддитивных солей для лечения обусловленных инфарктом миокарда поражений сердечной мышцы и к получению лекарственных средств, предназначенных для такого лечения.
В основу изобретения была положена задача получить новые фармацевтические композиции, которые могли бы оказывать эффективное воздействие на процесс выздоровления и/или реабилитации пациентов, перенесших инфаркт миокарда, и могли бы тем самым применяться для лечения обусловленных инфарктом миокарда поражений сердечной мышцы в соответствии с предусматриваемой терапией этого заболевания, равно как и постинфарктных состояний.
Согласно изобретению для получения соответствующих фармацевтических композиций, предназначенных для лечения обусловленных инфарктом миокарда поражений сердечной мышцы, предлагается применять 4-хлор-5- [(4,5-дигидро-1Н-имидазол-2-ил)амино] -6-метокси-2-метилпиримидин формулы I
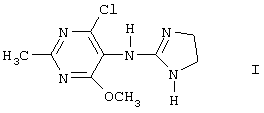
и его физиологически приемлемые кислотно-аддитивные соли.
В качестве физиологически приемлемых кислотно-аддитивных солей моксонидина пригодны соли с органическими кислотами, например галогеново-дородными кислотами, или с органическими кислотами, например низшими алифатическими моно- либо дикарбоновыми кислотами, такими как уксусная кислота, фумаровая кислота или винная кислота, или ароматическими карболовыми кислотами, такими, например, как салициловая кислота.
Применяемые согласно изобретению соединения подпадают под объем описанных в заявке DE 2849537 производных 5-[(2-имидазолин-2-ил)амино] пиримидина, которые обладают понижающими кровяное давление свойствами и которые известны из этой заявки. Содержащие моксонидин фармацевтические композиции являются коммерчески доступными продуктами под торговым наименованием Physiotens®, обладающими противогипертоническими свойствами, и в качестве таких гипотензивных средств применяются в медицине. Указанные соединения можно получать известным образом с помощью описанных в вышеназванной заявке способов либо аналогичных им.
Неожиданно было установлено, что моксонидин и его физиологически приемлемые кислотно-аддитивные соли оказывают положительное, способствующее выздоровлению и/или реабилитации, воздействие на состояние сердечной мышцы после перенесенного инфаркта и пригодны тем самым для лечения постинфарктных поражений миокарда у человека и крупных млекопитающих.
Под понятием "инфаркт миокарда" имеется в виду в основном некроз одного или нескольких участков сердечной мышцы в результате устойчивого полного прекращения кровоснабжения этого (-их) участка (-ов) или его снижения до критического уровня. При остром инфаркте миокарда, т.е. в остром периоде заболевания, наряду с такими общими терапевтическими мерами, как анальгезия, успокоение седативными средствами, введение кислорода, постельный режим и диета, применяют прежде всего тромболитическую, соответственно фибринолитическую терапию с той целью, чтобы за счет реперфузии ишемической области по возможности максимально (первично) уберечь не затронутую ишемией сердечную мышцу от полной гибели клеток (т.е. от окончательного некроза) и ограничить тем самым развитие инфаркта предельно малой зоной. Другие (дополнительные) меры могут быть направлены на улучшение состояния сердечной мышцы, прежде всего в зоне инфаркта, как в острой фазе заболевания, так и в постинфарктный период.
Применяемые согласно изобретению для лечения обусловленных инфарктом миокарда поражений сердечной мышцы соединения в основном пригодны благодаря этому для использования в рамках терапии указанного заболевания.
Они могут применяться поэтому уже в острой фазе заболевания, а также прежде всего при постинфарктном лечении пациентов как после проведения фибринолитической терапии, так и без данного лизиса. При постинфарктном лечении пациентов с лизисом применяемые согласно изобретению соединения оказывают прежде всего также профилактическое действие, предотвращая таким образом развитие сердечной недостаточности (функциональной недостаточности миокарда), обусловленное перенесенным инфарктом миокарда. Сказанное относится также к пациентам, при лечении которых использовали β-адреноблокаторы.
У перенесших инфаркт пациентов без лизиса заболевание переходит в хроническую фазу. Для таких пациентов в хронической стадии особое значение имеет тот факт, что симпатическая нервная система (СНС) играет важную роль в регуляции сердечно-сосудистой системы. Так, симпатическая стимуляция представляет собой наиболее важный механизм повышения сердечного выброса, поскольку эта стимуляция способствует как повышению интенсивности сокращения сердечной мышцы, так и повышению частоты сердечных сокращений. Острый инфаркт миокарда приводит среди прочего к активации СНС, способствующей поддержанию перфузионного давления и перфузии ткани.
Такая острая ситуация может развиться с переходом в хроническую фазу, в которой активация симпатической нервной системы способствует гипертрофии и перестройке (ремодуляции) не затронутого миокарда. Этот процесс, однако, может превысить допустимую степень, и продолжающаяся СНС-активация может привести по различным причинам к нежелательным последствиям:
1) Хроническую активацию центральной симпатической нервной системы, поскольку она усиливает сердечную недостаточность, следует рассматривать как неблагоприятный фактор. При устойчивой адренергической стимуляции на сердце в виде компенсации уменьшается количество адренорецепторов. Следствием же этого защитного механизма сердца против устойчиво повышенного уровня катехоламинов является значительное ухудшение регуляции частоты и силы сердечных сокращений через автономную нервную систему.
2) Стимуляция СНС повышает сосудистый тонус и тем самым увеличивает нагрузку на сердце.
3) Повышенный уровень циркулирующих катехоламинов индуцирует фокальный (очаговый) некроз в сердце и способствует развитию гипертрофии сердца.
4) Повышенный уровень катехоламинов в плазме способствует неблагоприятному усилению частоты сердечных сокращений и возникновению в ряде случаев аритмий сердца.
С учетом этого для предупреждения, соответственно во избежание, слишком сильной активации симпатической нервной системы целесообразной может оказаться такая стратегия лечения пациентов с инфарктом миокарда, которая включала бы прежде всего профилактику возникновения после перенесенного заболевания сердечной слабости.
Неожиданным образом было установлено, что применяемый согласно изобретению при лечении инфаркта миокарда и/или при постинфарктном лечении моксонидин дает тот неожиданный эффект, который проявляется в эффективном, способствующем процессу выздоровления и/или реабилитации воздействии на функциональное состояние сердечной мышцы и прежде всего при постинфарктном лечении в хронической стадии. Применение моксонидина при постинфарктном лечении способствует уменьшению массы сердца и снижению симпатической активации, что подтверждается данными измерения уровня норадреналина в плазме. Тем самым моксонидин может успешно применяться с целью снизить чрезмерную гипертрофию сердца, прежде всего на последующих фазах в постинфарктный период. Кроме того, моксонидин позволяет снизить уровень норадреналина в плазме крови, благодаря чему обеспечивается возможность эффективно нормализовать симпатическую активацию после перенесенного инфаркта миокарда.
При предлагаемом в изобретении лечении поражений сердечной мышцы, обусловленных инфарктом миокарда, моксонидин и его физиологически приемлемые кислотно-аддитивные соли можно включать в состав обычных фармацевтических композиций и вводить орально, внутривенно или же трансдермально. Так, в частности, моксонидин и его физиологически приемлемые кислотно-аддитивные соли могут содержаться в твердых или жидких фармацевтических композициях в эффективном, способствующем процессу лечения и/или реабилитации функционального состояния сердечной мышцы количестве совместно с обычными фармацевтическими вспомогательными веществами и/или носителями. В качестве примеров твердых препаратов, предназначенных для непосредственного либо постепенного (пролонгированного) высвобождения активного вещества, можно назвать такие назначаемые для орального введения препараты, как таблетки, драже, капсулы, порошки или грануляты, а также суппозитории и пластыри (так называемые ТТС, трансдермальные терапевтические системы). Эти твердые препараты наряду с обычно используемыми в фармацевтике вспомогательными веществами, например замасливателями, разрыхлителями таблеток и др., могут содержать в своем составе также обычно используемые в фармацевтике неорганические и/или органические носители, такие, например, как молочный сахар, тальк или крахмал. В случае использования пластырей активное вещество помещают в соответствующий "резервуар", прежде всего, например, в матрицу (в частности, в полимерную матрицу). Жидкие препараты, такие как растворы, суспензии или эмульсии активных веществ, могут содержать обычные разбавители, такие как вода, масла и/или суспендирующие агенты, например полиэтиленгликоли и т.п. Возможно дополнительное добавление и других вспомогательных веществ, таких, например, как консерванты, вкусовые добавки и т.п.
Из активных веществ совместно с фармацевтическими вспомогательными веществами и/или носителями можно по обычной технологии приготавливать смеси и композиции. Так, например, для изготовления твердых лекарственных форм активные вещества можно смешивать по обычной технологии с вспомогательными веществами и/или носителями и затем эту смесь гранулировать мокрым либо сухим методом. Гранулят или порошки можно непосредственно помещать в капсулы или обычным образом таблетировать. Равным образом можно изготавливать драже. Пластыри, соответственно трансдермальные терапевтические системы, можно изготавливать по обычной технологии с использованием, например, покрывной пленки, "резервуара" для активных веществ (самоклеящегося или с дополнительным адгезионным слоем) и удаляемой защитной пленки, при этом в таких системах для регулируемого высвобождения активных веществ можно предусмотреть матрицу или мембрану (т.е. дополнительную контрольную мембрану).
Экспериментальные исследования и их результаты
Эффективность моксонидина при лечении инфаркта миокарда и прежде всего в постинфарктный период может быть подтверждена в стандартном опыте по определению фармакологических показаний касательно воздействия субстанций на такие факторы, которые влияют на функциональное состояние сердечной мышцы после перенесенного инфаркта. Для подтверждения такого воздействия на факторы, влияющие на функциональное состояние сердечной мышцы, прежде всего в хронической стадии заболевания, проводят соответствующие эксперименты на животных, используя в этих целях, например, крыс линии Wistar с хроническим инфарктом миокарда (ИМ-крысы).
При исследованиях на ИМ-крысах было установлено, что уровень норадреналина в плазме после инфаркта резко возрастает. В прогрессирующих фазах сердечной недостаточности уровень норадреналина в плазме может и далее повышаться. Тщательные исследования на ИМ-крысах позволили установить, что даже через три недели после инфаркта, т.е. по завершении так называемого периода излечения, частота сердечных сокращений (измерения in vivo на произвольно выбранных крысах в бодрствующем состоянии), как очевидно, оставалась повышенной, тогда как уровень норадреналина в плазме все еще примерно на 50% превышал этот показатель у так называемых псевдоинфарктных крыс (т.е. крыс, подвергнутых мнимой операции без лигирования (перетяжки коронарной артерии). Кроме того, в центральной нервной системе этих животных наблюдался повышенный уровень метаболизма в паравентрикулярном гипоталамусе и в Locus coeruleus (синем пятне), в котором регулируются симпатические воздействия на периферию. Исследования поведенческой реакции инфарктных крыс показали, что животные проявляют повышенное чувство страха. Проведенные на ИМ-крысах наблюдения позволяют, таким образом, сделать вывод о том, что имело место хроническое повышение активации симпатической нервной системы.
Подопытные животные и дозировка
Описанные ниже опыты проводили на самцах крыс линии Wistar (вес 270-320 г, поставщик фирма Harlan Zeist, Нидерланды). Животных выдерживали при 12-часовом цикле свет/темнота, животные получали в каждом случае в достаточном количестве стандартный для крыс корм и воду. Одних животных (ИМ-крыс) подвергали операции с лигированием коронарной (венечной) артерии, других, псевдоинфарктных, крыс подвергали операции без наложения такой лигатуры (перетяжки). По истечении 24 ч из числа ИМ-крыс произвольно выбирали несколько особей и затем имплантировали им осмотические мининасосы (типа Modell 2001 фирмы Alzet) с целью подкожного введения моксонидина в суточной дозировке 3, соответственно 6, мг/кг или же вводили только инертный наполнитель. Лечение с использованием моксонидина проводили непрерывно до завершения экспериментов, продолжавшихся в течение 3 недель после оперативного вмешательства.
Лигирование (перетяжка) коронарной артерии
Левую переднюю нисходящую коронарную артерию лигировали при анестезии пентобарбиталом (60 мг/кг внутрибрюшинно). Краткое описание операции: После интубации трахеи над четвертым реберным промежутком проводили надрез кожи. Прилегающие мышцы раздвигали и отводили в сторону. Затем животным подключали искусственную вентиляцию легких (частота 65-70/мин, рабочий объем 3 мл) и грудную полость вскрывали за счет разделения межреберных мышц. Далее вскрывали перикард. Сердце оставляли в положении in situ и под левой коронарной (венечной) артерией вблизи места отхождения (начала) легочной артерии накладывали шов шелком 6-0. Затем шов стягивали. Псевдоинфарктных животных подвергали такой же процедуре, но без указанной выше перетяжки артерии. Ребра стягивали шелком 3-0. В завершение мышцы возвращали в первоначальное положение и кожу сшивали.
Подготовка и сбор проб крови
Через 19 дней после хирургического вмешательства с целью осуществить перетяжку коронарной артерии крыс повторно наркотизировали пентобарбиталом и через бедерную артерию вводили в абдоминальную аорту катетер (ПЭ-10, получение тепловой сваркой с ПЭ-50). Катетер постепенно перемещали подкожно к затылку животного, где его, оставив один конец выступающим наружу, закрепляли и закрывали. После двух дней отдыха животных в день отбора проб к катетеру с целью его удлинения подсоединяли обработанный гепарином и заполненный физиологическим раствором шланг и по истечении по меньшей мере 60 мин отбирали 2 пробы крови по 1 мл каждая. Затем кровь собирали в предварительно охлажденные пробирки, подготовленные с использованием 10 мкл ЭДТК (0,1М). После центрифугирования плазму собирали в предварительно охлажденные трубки, заполненные либо 1,2 мг глутатиона, либо 10 мкл апротинина (100 ME; ME = международные единицы) с целью определить содержание катехоламинов или предсердный натрийуретический фактор (ПНФ). Трубки с пробами выдерживали при -80°С. Концентрацию норадреналина, адреналина и дофамина в плазме выявляли с помощью ЖХВД, тогда как ПНФ анализировали с использованием метода РИА (радиоиммуноанализ).
Исследования коллагена сердца
Количество интерстициального коллагена определяли на 6-7 сердцах подопытных животных, произвольно выбранных из каждой экспериментальной группы. С этой целью сердца фиксировали путем перфузии с использованием формальдегида, содержавшего 3,6 мас.%-ный фосфатный буфер. Из желудочков сердец после удаления предсердий и крупных сосудов, начиная от верхушки сердца и до основания сердца, нарезали 4 кольца, которые затем по меньшей мере в течение 24 ч выдерживали в формальдегиде. После такого фиксажа кольца обезвоживали и заливали парафином. Депарафинированные образцы толщиной 5 мкм сначала в течение 5 мин инкубировали с использованием 0,2 мас./об. %-ного водного раствора фосформолибденовой кислоты, а затем в течение 45 мин - 0,1 мас. %-ного красителя Sirius Rot F3BA (фирмы Polysciencies Inc., Норгемптон, Великобритания) в насыщенной пикриновой кислоте, после чего промывали в течение 2 мин 0,01М соляной кислотой, обезвоживали и для последующих микроскопических исследований заливали энтелланом (фирма Merck, Дармштадт, Германия). Содержание интерстициального коллагена, удаленного от зоны инфаркта, определяли во внутрижелудочковой перегородке по интенсивности окраски красителем Sirius Rot при 40-кратном коэффициенте увеличения на каждое сердце.
Анализ полученных данных
Полученные данные, если не указано иное, выражали в виде группового среднего ± среднее стандартное отклонение. При этом анализировали только данные, полученные в зоне инфаркта, включая основную часть свободной стенки сердца левого желудочка, поскольку в отношении меньших зон инфаркта обычно имеет место полная гемодинамическая компенсация. Полученные данные анализировали с помощью "однофакторного дисперсионного анализа" (ANOVA), после которого проводили post-hoc-анализ согласно Бонферрони.
Результаты исследований
Исследования проводили на четырех группах крыс, включавших 2 группы инфарктных животных, которым вводили моксонидин (суточные дозы 3 и 6 мг/кг), одну группу инфарктных животных, которым не вводили моксонидин, и сравнительную группу, подвергнутую псевдооперации (псевдоинфарктные крысы). Перетяжка коронарной артерии приводила к обширному инфаркту в свободной стенке левого желудочка. Смертность подопытных животных составляла в целом порядка 29%, причем этот показатель в двух инфарктных группах был практически идентичным. Данные по 5 животным, у которых суточная доза моксонидина составляла 6 мг/кг, пришлось исключить, поскольку область инфаркта у них была слишком мала. Результаты опытов, где применяли суточную дозу 6 мг/кг и, соответственно, 3 мг/кг, представлены в таблице 1 и более подробно рассматриваются ниже. Приведенные в таблице 1 результаты включают данные по группам в количестве от 7 до 14 особей, за исключением данных о коллагене, и отдельно данные по группам в количестве 6-7 особей.
Если в начале экспериментов подопытные животные имели примерно одинаковый вес, то после лечения моксонидином вес инфарктных крыс по сравнению с весом инфарктных крыс, которым не вводили моксонидин, был несколько меньше, а по сравнению с псевдоинфарктными крысами их вес был заметно ниже. Масса сердца у инфарктных крыс, которым вводили моксонидин, была значительно меньше, чем у инфарктных крыс, не подвергнутых такому лечению. Эти эффекты, как очевидно из таблицы 1, были обусловлены различиями в дозировке, т.е. зависели от того, вводили ли суточную дозу в количестве 3 или 6 мг/кг. Полученные данные позволяют сделать вывод о том, что благодаря введению моксонидина удавалось предотвратить чрезмерную гипертрофию сердца.
У инфарктных животных, которым не вводили моксонидин, наблюдалась определенная на основании уровня норадреналина в плазме и ПНФ заметно более высокая нейрогуморальная активность. Уровень же ПНФ в плазме у животных, подвергнутых лечению моксонидином, по сравнению с этим показателем у инфарктных крыс, которым не вводили моксонидин, оставался неизменным. Благодаря применению моксонидина уровень норадреналина в плазме удавалось снизить примерно на 50% от аналогичного показателя у псевдоинфарктных крыс.
Как было установлено, уровень норадреналина в плазме у инфарктных животных, которым не вводили моксонидин, был значительно повышен и в три раза превышал этот показатель у псевдоинфарктных крыс. Благодаря применению моксонидина уровень норадреналина у инфарктных животных из группы, которой вводили суточную дозу в количестве 6 мг/кг, удавалось снизить почти на 50% от этого показателя у псевдоинфарктных крыс. У группы животных, которым вводили суточную дозу 3 мг/кг, наблюдалось значительное снижение уровня норадреналина в плазме. Эти данные подтверждают, что суточные дозы моксонидина 3, соответственно 6 мг/кг, могут обеспечить эффективное снижение активации симпатической нервной системы после инфаркта миокарда.
Результаты измерений касательно коллагена сердца у групп, которым вводили суточную дозу 3, соответственно 6 мг/кг, также представлены в таблице 1.
Частота сердечных сокращений, выявленная у инфарктных животных в состоянии бодрствования, была заметно выше по сравнению с этим показателем у псевдоинфарктных крыс. Такую тахикардию благодаря введению моксонидина не только удавалось предотвратить, но и более того: у инфарктных животных, получавших моксонидин, по сравнению с псевдоинфарктными крысами наблюдалось замедление сердечной деятельности, т.е. урежение нормального ритма (брадикардия).
Данные опытов на сравнительной группе псевдооперированных животных (ПСЕВДО), на инфарктных животных, не подвергавшихся лечению (ИНФАРКТ), и на животных, которым вводили моксонидин (ИНФ+МОКС); суточная доза 3 мг/кг и суточная доза 6 мг/кг
Принятые сокращения:
САД - среднее артериальное давление;
НА - норадреналин;
ПНФ - предсердный натрийуретический фактор;
* значительно отличается от псевдоинфарктных крыс;
# значительно отличается от не подвергавшихся лечению инфарктных крыс.
Представленные результаты экспериментов служат однозначным подтверждением того факта, что благодаря применению моксонидина при лечении инфаркта миокарда и прежде всего при лечении в постинфарктном периоде удается эффективно воздействовать на функциональное состояние сердечной мышцы. На основании данных об уровне катехоламинов в плазме можно заключить, что моксонидин обеспечивает возможность эффективно нормализовать активацию симпатической нервной системы у инфарктных животных. Этот вывод подтверждают данные о частоте сердечных сокращений (in vivo, на животных в состоянии бодрствования), поскольку частота сердечных сокращений у крыс, которым вводили моксонидин, была даже ниже, чем у псевдоинфарктных крыс. Этот фактор обусловлен предположительно действием моксонидина скорее в хронической, а не в острой стадии инфаркта, поскольку при лечении в острой стадии снижение частоты сердечных сокращений сопровождается возрастанием среднего артериального давления, которое при лечении в хронической стадии не наблюдается. При этом учитывается эффективность действия моксонидина в целом. Хотя достигаемые положительные эффекты касательно соотношения масса сердца/вес тела нельзя, по-видимому, оценить однозначно, а данные о содержании интерстициального коллагена объяснить незначительным эффектом ремодуляции (перестройки), тем не менее полученные результаты указывают на вполне очевидную тенденцию: моксонидин обладает профилактическим действием против чрезмерной гипертрофии сердца и нежелательной ремодуляции.
Таким образом, представленные выше результаты проведенных экспериментов свидетельствуют о том, что моксонидин и его кислотно-аддитивные соли оказывают эффективное, способствующее процессу выздоровления и/или реабилитации воздействие на состояние сердечной мышцы после перенесенного инфаркта миокарда и могут тем самым применяться для лечения обусловленных инфарктом поражений сердечной мышцы у человека и крупных млекопитающих, при этом такое лечение может проводиться как в острой стадии заболевания, так и в первую очередь в постинфарктном периоде. При этом моксонидин, прежде всего при постинфарктном лечении, может оказывать профилактическое действие на прогрессирующее развитие сердечной слабости после заболевания. Назначаемые дозы моксонидина или его кислотно-аддитивных солей могут подбираться в каждом случае индивидуально и варьироваться в зависимости от особенностей состояния пациента и формы применения. Как правило, при лечении инфаркта в острой стадии заболевания, соответственно в постинфарктном периоде, суточную дозу для орального введения человеку назначают в пределах от 0,05 до 5 мг, предпочтительно примерно от 0,25 до 3 мг. При этом моксонидин и его кислотно-аддитивные соли в составе соответствующих фармацевтических композиций могут предназначаться как для немедленного, так и для пролонгированного, контролируемого и/или регулируемого высвобождения активного вещества. Для специалиста при этом очевидно, что содержание действующего вещества в композициях с пролонгированным, контролируемым и/или регулируемым высвобождением последнего может быть выше по сравнению с композициями, предназначенными для его немедленного высвобождения.
Ниже на примере более подробно поясняется технология приготовления и состав одной из возможных фармацевтических композиций, содержащей моксонидин, для применения при лечении инфаркта миокарда и/или при постинфарктном лечении, при этом данный пример никоим образом не ограничивает объем изобретения.
Пример 1
Содержащие моксонидин таблетки в пленочной оболочке
Состав:
Сердцевина таблеток:
Пленочная оболочка:
Для нанесения оболочки на 10000 таблеток весом 100 мг каждая требуется 4,8 кг указанной выше суспензии
Получение сердцевины таблеток
Из моксонидина и лактозы приготавливают смесь, после чего эту смесь увлажняют раствором связующего повидон в воде, тщательно разминают при перемешивании и полученный продукт расстилают на решетчатых полках и сушат при температуре порядка 50°С до конечного содержания влаги максимум 0,5%. Высушенный продукт пропускают через сито с размером ячеек 0,75 мм (машина Фрюитта). После смешения полученного гранулята с кросповидоном и стеаратом магния осуществляют таблетирование с получением в результате сердцевины таблеток весом 100 мг каждая и содержанием 0,25 мг активного вещества соответственно.
Получение суспензии для пленочной оболочки
Гидроксипропилметилцеллюлозу и полиэтиленгликоль 6000 растворяют в одной части воды. Затем к этому раствору добавляют при перемешивании суспензию из талька, диоксида титана и оксида железа в остальном количестве воды. Полученную суспензию при легком перемешивании разбавляют 30%-ной водной дисперсией этилцеллюлозы.
Нанесение пленочной оболочки на сердцевину таблеток
Указанную выше суспензию напыляли на сердцевину таблеток с помощью аппарата для нанесения пленочного покрытия при одновременном нагреве сердцевины до температуры порядка 40°С нагретым до примерно 70°С воздухом. В завершение изготовленные таким путем таблетки с пленочным покрытием подвергали в течение 16 ч сушке при температуре порядка 45°С.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ СЕЛЕКТИВНЫЙ АГОНИСТ ИМИДАЗОЛИНОВОГО РЕЦЕПТОРА I1 И БЛОКАТОР РЕЦЕПТОРА АНГИОТЕНЗИНА II | 2004 |
|
RU2362561C2 |
| СИНЕРГЕТИЧЕСКИЕ КОМПОЗИЦИИ, КОТОРЫЕ СОДЕРЖАТ ИНГИБИТОР РЕНИНА, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ЛЕЧЕНИЯ СЕРДЕЧНО-СОСУДИСТЫХ ЗАБОЛЕВАНИЙ | 2001 |
|
RU2310443C2 |
| СИНЕРГЕТИЧЕСКИЕ КОМБИНАЦИИ, КОТОРЫЕ СОДЕРЖАТ ИНГИБИТОР РЕНИНА, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ЛЕЧЕНИЯ СЕРДЕЧНО-СОСУДИСТЫХ ЗАБОЛЕВАНИЙ | 2006 |
|
RU2346703C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ИНГИБИТОР РЕНИНА, БЛОКАТОР КАЛЬЦИЕВЫХ КАНАЛОВ И ДИУРЕТИК | 2003 |
|
RU2316318C2 |
| Трансляционная модель хронической сердечной недостаточности: способ и критерии оценки формирования | 2018 |
|
RU2744681C1 |
| ГИПОТЕНЗИВНАЯ КОМБИНАЦИЯ ВАЛСАРТАНА И БЛОКАТОРА КАЛЬЦИЕВЫХ КАНАЛОВ | 1999 |
|
RU2450813C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИИШЕМИЧЕСКОЙ И АНТИГИПОКСИЧЕСКОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2356573C1 |
| ГИПОТЕНЗИВНАЯ КОМБИНАЦИЯ ВАЛСАРТАНА И БЛОКАТОРА КАЛЬЦИЕВЫХ КАНАЛОВ | 1999 |
|
RU2243768C2 |
| ПРИМЕНЕНИЕ ИНГИБИТОРОВ ДИПЕПТИДИЛПЕПТИДАЗЫ IV | 2004 |
|
RU2385723C2 |
| ПРИМЕНЕНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ | 2005 |
|
RU2426532C2 |
Изобретение относится к медицине, в частности к производству лекарственных средств для кардиологии. Для этого предлагается использовать моксонидин в качестве активного начала при получении фармацевтических композиций, предназначенных для лечения обусловленных инфарктом поражений сердечной мышцы. Указанные композиции способствуют предотвращению прогрессирования инфаркта, а также лечению его осложнений. 2 з.п. ф-лы, 1 табл.
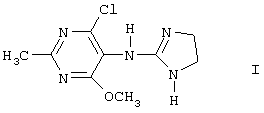
и его физиологически приемлемых кислотно-аддитивных солей в качестве активного начала при получении фармацевтических композиций, предназначенных для лечения обусловленных инфарктом миокарда поражений сердечной мышцы.
| WO 9746241, 11.12.1997 | |||
| УСТРОЙСТВО для НАГРЕВА ТЕПЛОНОСИТЕЛЕЙ | 0 |
|
SU317855A1 |
| ПРОТИВОГИПЕРГЛИКЕМИЧЕСКИ ЭФФЕКТИВНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2145857C1 |
| ГЛЕЗЕР М.Г | |||
| и др | |||
| Справочник по фармакотерапии сердечно-сосудистых заболеваний, М., 1996, с.434, 439, 441, 454-455 | |||
| LEPRAN ISTVAN et al | |||
| Effect of moxonidin on arrhythmi.s induced by coronary artery occlusion and reperfusion., J | |||
| Cardiovasc | |||
| PharmacoL, 1994, 24 s | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
Авторы
Даты
2005-09-27—Публикация
2000-01-28—Подача