ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Данное изобретение относится к новым таксанам, которые имеют исключительную применимость в качестве противоопухолевых средств.
Таксановая группа терпенов, членами которой являются баккатин III и таксол, представляет значительный интерес как биологического, так и химического рода. Сам таксол используется в качестве противоракового хемотерапевтического агента и обладает широким спектром ингибирующей опухоли активности. Таксол имеет 2'R,3'S-конфигурацию и представлен следующей структурной формулой:

где Ac представляет собой ацетил.
Colin и др. описали в патенте US 4814470, что некоторые аналоги таксола имеют значительно большую активность, чем таксол. Один из указанных аналогов, обычно называемый доцетакселем, имеет следующую структурную формулу:

Хотя таксол и доцетаксель могут использоваться в качестве хемотерапевтических агентов, существуют ограничения их эффективности, включая ограниченную эффективность против некоторых видов рака и токсичность для субъекта при введении в различных дозах. Соответственно, остается потребность в дополнительных хемотерапевтических агентах с улучшенной эффективностью и меньшей токсичностью.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Среди объектов данного изобретения, следовательно, предусмотрены таксаны, которые имеют преимущества по сравнению с таксолом и доцетакселем по эффективности в качестве противоопухолевых агентов и по токсичности. Обычно эти таксаны содержат сложноэфирный заместитель, иной чем формиат, ацетат и гетерозамещенный ацетат, в положении С-7, гидроксизаместитель в положении С-10 и ряд С-3'-заместителей.
Коротко говоря, данное изобретение, следовательно, относится к таксановой композиции, как таковой, к фармацефтическим композициям, содержащим таксан и фармацевтически приемлемый носитель, и к способам введения.
Другие объекты и признаки данного изобретения будут частично прояснены и частично отмечены ниже.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВОПЛОЩЕНИЙ
В одном из воплощений настоящего изобретения таксаны по данному изобретению соответствуют структуре (1):
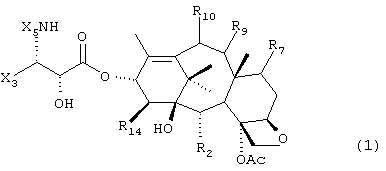
где
R2 представляет собой ацилокси;
R7 представляет собой R7aCOO-;
R7a представляет собой гидрокарбил, замещенный гидрокарбил или гетероцикло, где указанный гидрокарбил или замещенный гидрокарбил содержат атомы углерода в альфа- и бета-положениях относительно углерода, заместителем у которого является R7a;
R9 представляет собой кето, гидрокси или ацилокси;
R10 представляет собой гидрокси;
R14 представляет собой гидридо или гидрокси;
Х3 представляет собой замещенные или незамещенные алкил, алкенил, алкинил, фенил или гетероцикло;
Х5 представляет собой -СОХ10, -СООХ10 или -CONHX10;
Х10 представляет собой гидрокарбил, замещенный гидрокарбил или гетероцикло;
Ac представляет собой ацетил;
R7, R9 и R10 независимо друг от друга имеют альфа- или бета-стереохимическую конфигурацию.
В одном воплощении R2 представляет собой сложный эфир (R2aC(O)O-), карбамат (R2aR2bNC(O)O-), карбонат (R2aOC(O)O-) или тиокарбамат (R2aSC(O)O-), где R2a и R2b независимо друг от друга означают водород, гидрокарбил, замещенный гидрокарбил или гетероцикло. В предпочтительном воплощении R2 представляет собой сложный эфир (R2aC(O)O-), где R2a представляет собой арил или гетероароматическую группу. В другом предпочтительном воплощении R2 представляет собой сложный эфир (R2aC(O)O-), где R2a представляет собой замещенные или незамещенные фенил, фурил, тиенил или пиридил. В одном конкретном предпочтительном воплощении R2 представляет собой бензоилокси.
В одном воплощении R7 представляет собой R7aCOO-, где R7a представляет собой (i) замещенный или незамещенный С2-С8 алкил (прямой, разветвленный или циклический), такой как этил, пропил, бутил, пентил или гексил; (ii) замещенный или незамещенный С2-С8 алкенил (прямой, разветвленный или циклический), такой как этенил, пропенил, бутенил, пентенил или гексенил; (iii) замещенный или незамещенный С2-С8 алкинил (прямой или разветвленный), такой как этинил, пропинил, бутинил, пентинил или гексинил; (iv) замещенный или незамещенный фенил; или (v) замещенный или незамещенный гетероароматический радикал, такой как фурил, тиенил или пиридил. Заместителями могут быть гидрокарбил или любые содержащие гетероатом заместители, указанные здесь и далее для замещенного гидрокарбила. В предпочтительном воплощении R7a представляет собой этил, прямой, разветвленный или циклический пропил, прямой, разветвленный или циклический бутил, прямой, разветвленный или циклический пентил, прямой, разветвленный или циклический гексил, прямой или разветвленный пропенил, изобутенил, фурил или тиенил. В другом воплощении R7a представляет собой замещенный этил, замещенный пропил (прямой, разветвленный или циклический), замещенный пропенил (прямой или разветвленный), замещенный изобутенил, замещенный фурил или замещенный тиенил, где заместитель(и) выбран(ы) из группы, включающей гетероцикло, алкокси, алкенокси, алкинокси, арилокси, гидрокси, защищенный гидрокси, кето, ацилокси, нитро, амино, амидо, тиол, кеталь, ацеталь, сложноэфирную и простую эфирную группу, но не фосфорсодержащие группы.
Если R9 представляет собой кето в одном из воплощений данного изобретения, в других воплощениях R9 может иметь альфа- или бета-стереохимическую конфигурацию, предпочтительно бета-стереохимическую конфигурацию, и может быть, например, α- или β-гидрокси- или α- или β-ацилокси. Например, если R9 представляет собой ацилокси, это может быть сложный эфир (R9аС(О)О-), карбамат (R9aR9bNC(O)O-), карбонат (R9аОС(О)О-) или тиокарбамат (R9аSC(О)О-), где R9а и R9b независимо друг от друга означают водород, гидрокарбил, замещенный гидрокарбил или гетероцикло. Если R9 представляет собой сложный эфир (R9aC(O)O-), R9a представляет собой замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный арил или замещенный или незамещенный гетероароматический радикал. Еще более предпочтительно, R9 представляет собой сложный эфир (R9aC(O)O-), где R9a представляет собой замещенный или незамещенный фенил, замещенный или незамещенный фурил, замещенный или незамещенный тиенил или земещенный или незамещенный пиридил. В одном из воплощений R9 представляет собой (R9aC(O)O-), где R9a представляет собой метил, этил, пропил (прямой, разветвленный или циклический), бутил (прямой, разветвленный или циклический), пентил (прямой, разветвленный или циклический) или гексил (прямой, разветвленный или циклический). В другом воплощении R9 представляет собой (R9aC(O)O-), где R9а представляет собой замещенный метил, замещенный этил, замещенный пропил (прямой, разветвленный или циклический), замещенный бутил (прямой, разветвленный или циклический), замещенный пентил (прямой, разветвленный или циклический) или замещенный гексил (прямой, разветвленный или циклический), где заместитель(и) выбран(ы) из группы, включающей гетероцикло, алкокси, алкенокси, алкинокси, арилокси, гидрокси, защищенный гидрокси, кето, ацилокси, нитро, амино, амидо, тиол, кеталь, ацеталь, сложноэфирную и простую эфирную группу, но не фосфорсодержащие группы.
Примерами заместителей Х3 являются замещенные или незамещенные С2-С8 алкилы, замещенные или незамещенные С2-С8 алкенилы, замещенные или незамещенные от С2 до С8 алкинилы, замещенные или незамещенные гетероароматические радикалы, содержащие 5 или 6 кольцевых атомов, и замещенный или незамещенный фенил. Примерами предпочтительных заместителей Х3 являются замещенные или незамещенные этил, пропил, бутил, циклопропил, циклобутил, циклогексил, изобутенил, фурил, тиенил и пиридил.
Примерами заместителей Х5 являются -СОХ10, -СООХ10 или -CONHX10, где Х10 представляет собой замещенные или незамещенные алкил, алкенил, фенил или гетероароматический радикал. Примерами предпочтительных заместителей Х3 являются -СОХ10, -СООХ10 или -CONHX10, где Х10 представляет собой (i) замещенный или незамещенный C1-C8 алкил, такой как замещенные или незамещенные метил, этил, пропил (прямой, разветвленный или циклический), бутил (прямой, разветвленный или циклический), пентил (прямой, разветвленный или циклический) или гексил (прямой, разветвленный или циклический); (ii) замещенный или незамещенный С2-С8 алкенил, такой как замещенные или незамещенные этенил, пропенил (прямой, разветвленный или циклический), бутенил (прямой, разветвленный или циклический), пентенил (прямой, разветвленный или циклический) или гексенил (прямой, разветвленный или циклический); (iii) замещенный или незамещенный С2-С8 алкинил, такой как замещенные или незамещенные этинил, пропинил (прямой или разветвленный), бутинил (прямой или разветвленный), пентинил (прямой или разветвленный) или гексинил (прямой или разветвленный); (iv) замещенный или незамещенный фенил; или (v) замещенный или незамещенный гетероароматический радикал, такой как фурил, тиенил или пиридил, где заместитель(и) выбран(ы) из группы, включающей гетероцикло, алкокси, алкенокси, алкинокси, арилокси, гидрокси, защищенный гидрокси, кето, ацилокси, нитро, амино, амидо, тиол, кеталь, ацеталь, сложноэфирную и простую эфирную группу, но не фосфорсодержащие группы.
В одном из предпочтительных воплощений таксаны по данному изобретению соответствуют следующей структурной формуле (2):

где
R7 представляет собой R7aCOO-;
R10 представляет собой гидрокси;
Х3 представляет собой замещенные или незамещенные алкил, алкенил, алкинил или гетероцикло;
X5 представляет собой -СОХ10, -СООХ10 или -CONHX10;
Х10 представляет собой гидрокарбил, замещенный гидрокарбил или гетероцикло;
R7a представляет собой гидрокарбил, замещенный гидрокарбил или гетероцикло, где указанные гидрокарбил или замещенный гидрокарбил содержат атомы углерода в альфа- и бета-положениях относительно углерода, заместителем которого является Ra;
Bz представляет собой бензоил;
Ac представляет собой ацетил.
Например, в указанном предпочтительном воплощении, в котором таксан соответствует структуре (2), R7a может быть замещенными или незамещенными этилом, пропилом или бутилом, более предпочтительно замещенными или незамещенными этилом или пропилом, еще более предпочтительно замещенным или незамещенным этилом и еще более предпочтительно незамещенным этилом. Если R7a выбран среди указанных, в одном из воплощений Х3 выбран из замещенных или незамещенных алкилов, алкенилов, фенила или гетероцикло, более предпочтительно замещенных или незамещенных алкенилов, фенила или гетероцикло, еще более предпочтительно замещенных или незамещенных фенила или гетероцикло и еще более предпочтительно гетероцикло, такого как фурил, тиенил или пиридил. Если R7a и Х3 выбраны среди указанных, в одном из воплощений X5 выбран из -СОХ10, где Х10 представляет собой фенил, алкил или гетероцикло, более предпочтительно фенил. Альтернативно, если R7a и Х3 выбраны среди указанных, в одном из воплощений Х5 выбран из -СОХ10, где Х10 представляет собой фенил, алкил или гетероцикло, более предпочтительно фенил, или X5 означает -СООХ10, где Х10 представляет собой алкил, предпочтительно трет-бутил. Следовательно, среди более предпочтительных воплощений представлены таксаны, соответствующие структуре 2, в которой (i) X5 представляет собой -СООХ10, где Х10 представляет собой трет-бутил, или Х5 представляет собой -СОХ10, где Х10 представляет собой фенил, (ii) Х3 представляет собой замещенные или незамещенные циклоалкил, алкенил, фенил или гетероцикло, более предпочтительно замещенные или незамещенные изобутенил, фенил, фурил, тиенил или пиридил, еще более предпочтительно незамещенные изобутенил, фурил, тиенил или пиридил, и (iii) R7a представляет собой незамещенные этил или пропил, более предпочтительно этил.
Среди предпочтительных воплощений, следовательно, представлены таксаны, соответствующие структуре 1 или 2, где R7 представляет собой R7aCOO-, где R7a представляет собой этил. В указанном воплощении Х3 предпочтительно представляет собой циклоалкил, изобутенил, фенил, замещенный фенил, такой как пара-нитрофенил, или гетероцикло, более предпочтительно гетероцикло, еще более предпочтительно фурил, тиенил или пиридил; и X5 предпочтительно представляет собой бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил. В другой альтернативе указанного воплощения Х3 представляет собой гетероцикло; X5 представляет собой бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил, еще более предпочтительно трет-бутоксикарбонил; R2 представляет собой бензоил, R9 представляет собой кето и R14 представляет собой гидридо. В другой альтернативе указанного воплощения Х3 представляет собой гетероцикло; X5 представляет собой бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил, еще более предпочтительно трет-бутоксикарбонил; R2 представляет собой бензоил, R9 представляет собой кето и R14 представляет собой гидридо. В другой альтернативе указанного воплощения Х3 представляет собой гетероцикло; X5 представляет собой бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил, еще более предпочтительно трет-бутоксикарбонил; R2 представляет собой бензоил, R9 представляет собой кето и R14 представляет собой гидрокси. В другой альтернативе указанного воплощения Х3 представляет собой гетероцикло; X5 представляет собой бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил, еще более предпочтительно трет-бутоксикарбонил; R2 представляет собой бензоил, R9 представляет собой гидрокси и R14 представляет собой гидрокси. В другой альтернативе указанного воплощения Х3 представляет собой гетероцикло; X5 представляет собой бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил, еще более предпочтительно трет-бутоксикарбонил; R2 представляет собой бензоил, R9 представляет собой гидрокси и R14 представляет собой гидридо. В другой альтернативе указанного воплощения Х3 представляет собой гетероцикло; X5 представляет собой бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил, еще более предпочтительно, трет-бутоксикарбонил; R2 представляет собой бензоил, R9 представляет собой ацилокси и R14 представляет собой гидрокси. В другой альтернативе указанного воплощения Х3 представляет собой гетероцикло; Х5 представляет собой бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил, еще более предпочтительно трет-бутоксикарбонил; R2 представляет собой бензоил, R9 представляет собой ацилокси и R14 представляет собой гидридо. В каждой из альтернатив указанного воплощения, где таксан имеет структуру 1, каждый из R7 и R10 может иметь бета-стереохимическую конфигурацию, каждый из R7 и R10 может иметь альфа-стереохимическую конфигурацию, R7 может иметь альфа-стереохимическую конфигурацию, тогда как R10 имеет бета-стереохимическую конфигурацию, или R7 может иметь бета-стереохимическую конфигурацию, тогда как R10 имеет альфа-стереохимическую конфигурацию.
Также среди предпочтительных воплощений представлены таксаны, соответствующие структуре 1 или 2, где R7 представляет собой R7aCOO-, где R7а представляет собой пропил. В данном воплощении Х3 представляет собой предпочтительно циклоалкил, изобутенил, фенил, замещенный фенил, такой как пара-нитрофенил, или гетероцикло, более предпочтительно гетероцикло, еще более предпочтительно фурил, тиенил или пиридил; и X5 представляет собой предпочтительно бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил. В одной альтернативе указанного воплощения Х3 представляет собой гетероцикло; X5 представляет собой бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил, еще более предпочтительно трет-бутоксикарбонил; R2 представляет собой бензоил, R9 представляет собой кето и R14 представляет собой гидридо. В другой альтернативе указанного воплощения Х3 представляет собой гетероцикло; X5 представляет собой бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил, еще более предпочтительно трет-бутоксикарбонил; R2 представляет собой бензоил, R9 представляет собой кето и R14 представляет собой гидридо. В другой альтернативе указанного воплощения Х3 представляет собой гетероцикло; X5 представляет собой бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил, еще более предпочтительно трет-бутоксикарбонил; R2 представляет собой бензоил, R9 представляет собой кето и R14 представляет собой гидрокси. В другой альтернативе указанного воплощения Х3 представляет собой гетероцикло; X5 представляет собой бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил, еще более предпочтительно трет-бутоксикарбонил; R2 представляет собой бензоил, R9 представляет собой гидрокси и R14 представляет собой гидрокси. В другой альтернативе указанного воплощения Х3 представляет собой гетероцикло; X5 представляет собой бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил, еще более предпочтительно трет-бутоксикарбонил; R2 представляет собой бензоил, R9 представляет собой гидрокси и R14 представляет собой гидридо. В другой альтернативе указанного воплощения Х3 представляет собой гетероцикло; X5 представляет собой бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил, еще более предпочтительно трет-бутоксикарбонил; R2 представляет собой бензоил, R9 представляет собой ацилокси и R14 представляет собой гидрокси. В другой альтернативе указанного воплощения Х3 представляет собой гетероцикло; X5 представляет собой бензоил, алкоксикарбонил или гетероциклокарбонил, более предпочтительно бензоил, трет-бутоксикарбонил или трет-амилоксикарбонил, еще более предпочтительно трет-бутоксикарбонил; R2 представляет собой бензоил, R9 представляет собой ацилокси и R14 представляет собой гидридо. В каждой из альтернатив указанного воплощения, где таксан имеет структуру 1, каждый из R7 и R10 может иметь бета-стереохимическую конфигурацию, каждый из R7 и R10 может иметь альфа-стереохимическую конфигурацию, R7 может иметь альфа-стереохимическую конфигурацию, тогда как R10 имеет бета-стереохимическую конфигурацию, или R7 может иметь бета-стереохимическую конфигурацию, тогда как R10 имеет альфа-стереохимическую конфигурацию.
Таксаны общей формулы 1 могут быть получены обработкой β-лактама алкоголятом, имеющим тексановое тетрациклическое ядро и металлоксидный заместитель в положении С-13, с получением соединения, имеющего β-амидоэфирный заместитель в положении С-13 (как описано более полно Holton в патенте US 5466834), с последующим удалением гидроксизащитной группы.
β-Лактам имеет следующую структурную формулу (3):

где P2 представляет собой гидроксизащитную группу и Х3 и Х5 такие, как определено выше; и алкоголят имеет структурную формулу (4):

где М представляет собой металл или аммоний, Р10 представляет собой гидроксизащитную группу и R2, R9, R7 и R10 такие, как определены выше.
Алкоголят (4) может быть получен из 10-дезацетилбаккатина III (или его производного) путем селективной защиты С-10 гидроксильной группы и затем этерификацией С-7 гидроксильной группы с последующей обработкой амидом металла. В одном из воплощений данного изобретения С(10) гидроксильную группу 10-дезацетилбаккатина III селективно защищают силильной группой, используя, например, силиламид или биссилиламид в качестве силилирующего агента. Предпочтительными силилирующими агентами являются три(гидрокарбил)силил-трифторметилацетамиды и бис-три(гидрокарбил)-силилтрифторметилацетамиды (с гидрокарбилами, замещенными или незамещенными алкилом или арилом), такие как N,O-бис-(триметилсилил)трифторацетамид, N,O-бис-(триэтилсилил)-трифторацетамид, N-метил-N-триэтилсилилтрифторацетамид и N,O-бис(трет-бутилдиметилсилил)трифторацетамид. Силилирующие агенты могут быть использованы либо индивидуально, либо в сочетании с каталитическим количеством основания, такого как основание щелочного металла. В качестве катализаторов в общем предпочтительны амиды щелочных металлов, такие как амид лития, и, в частности, гексаметилдисилазид лития. Растворителем для селективной реакции силилирования предпочтительно является эфирный растворитель, такой как тетрагидрофуран. В качестве альтернативы, однако, могут быть использованы другие растворители, такие как простой эфир или диметоксиэтан. Температура, при которой проводят селективное силилирование в положении С(10), не ограничена узкими рамками. Обычно, однако, его ведут при 0°С или выше.
Селективную этерификацию С(7) гидроксильной группы защищенного в положении С(10) таксана можно осуществить с применением различных обычных ацилирующих агентов, включая, но не ограничиваясь ими, производные замещенных и незамещенных карбоновых кислот, например галогеноангидриды карбоновых кислот, ангидриды, дикарбонаты, изоцианаты и галогеноформиаты. Например, С(7) гидроксильная группа 10-защищенного 10-дезацетилбаккатина III может быть селективно алкилирована дибензилкарбонатом, диаллилдикарбонатом, 2,2,2-трихлорэтилхлорформиатом, бензилхлорформиатом или другими обычными ацилирующими агентами. Обычно ацилирование С(7) гидроксигруппы С(10) защищенного таксана более эффективно и более селективно, чем С(7) ацилирование 7,10-дигидрокситаксана, такого как 10-DAB; другими словами, если С(10) гидроксильная группа защищена, существует значительное различие в реакционной способности оставшихся С(7), С(13) и С(1) гидроксильных групп. Указанные реакции ацилирования могут быть проведены в присутствии или в отсутствие аминового основания.
Производные 10-дезацетилбаккатина III, имеющие альтернативные заместители в положении С(2), С(9) и С(14), и способы их получения известны из современного уровня техники. Производные таксана, имеющие ацилокси заместители, отличные от бензоилоксигруппы при С(2), могут быть получены, например, как описано Holton и др. в патенте US №5728725 или Kingston и др. в патенте US №6002023. Таксаны, имеющие ацилокси- или гидроксизаместители при С(9) вместо кето, могут быть получены, например, как описано Holton и др. в патенте US №6011056 или Gunawardana и др. в патенте US №5352806. Таксаны, имеющие бета-гидроксизаместители при С(14), могут быть получены из природного 14-гидрокси-10-дезацетилбаккатина III.
Способы получения и разделения исходных β-лактамов обычно хорошо известны. Например, β-лактам может быть получен, как описано Holton в патенте US №5430160, и полученные энантиомерные смеси β-лактамов могут быть разделены с помощью стереоселективного гидролиза, используя липазу или фермент, как описано, например, Patel в патенте US №5879929, Patel в патенте US №5567614, или гомогенатом печени, как описано, например, в патентной заявке РСТ №00/41204. В предпочтительном воплощении, в котором β-лактам замещен фурилом в С(4)-положении, β-лактам может быть получен, как показано на следующей схеме реакций:
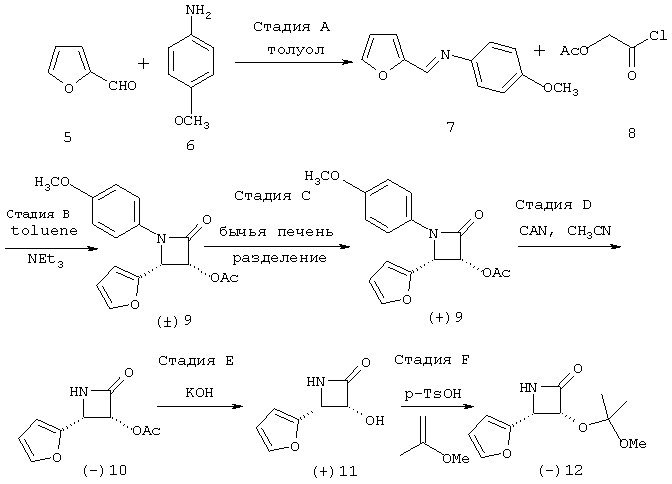
где Ac представляет собой ацетил, NEt3 представляет собой триэтиламин, CAN представляет собой церийаммонийнитрат и р-TsOH представляет собой пара-толуолсульфоновую кислоту. Растворение бычьей печени может быть произведено, например, объединением смеси энантиомерных β-лактамов с суспензией бычьей печени (полученной, например, помещением 20 г замороженной бычьей печени в смеситель и затем прибавлением буферного раствора с рН 8 до получения общего объема 1 л).
Соединения формулы 1 по данному изобретению могут использоваться для ингибирования роста опухолей у млекопитающих, в том числе у человека, и предпочтительно вводятся в виде фармацевтической композиции, содержащей эффективное противоопухолевое количество соединения по данному изобретению в сочетании с по меньшей мере одним фармацевтически или фармакологически приемлемым носителем. Носитель, известный также в технике как эксципиент, растворитель, вспомогательное соединение, добавка или разбавитель, представляет собой любое соединение, которое является фармацевтически инертным, придает подходящую консистенцию или форму композиции и не уменьшает терапевтической эффективности противоопухолевых соединений. Носитель является "фармацевтически или фармакологически приемлемым", если он не вызывает побочных, аллергических или других неблагоприятных реакций при введении млекопитающему или человеку как назначено.
Фармацевтические композиции, содержащие противоопухолевые соединения по данному изобретению, могут быть приготовлены любым удобным способом. Соответствующая готовая препаративная форма зависит от выбора пути введения. Композиции по изобретению могут быть приготовлены для любого пути введения при условии, что целевая ткань доступна указанным путем. Подходящие пути введения включают, но не ограничиваются ими, пероральное, парентеральное (например, внутривенное, внутриартериальное, подкожное, ректальное, внутримышечное, внутриглазничное, внутрикапсульное, интраспинальное, внутрибрюшинное или внутригрудинное), местное (назальное, чрезкожное, внутриглазное), внутрипузырное, подоболочечное, энтеральное, легочное, внутрилимфатическое, внутриполостное, вагинальное, трансуретральное, внутрикожное, ушное, интрамаммарное, щечное, ортотопическое, внутритрахеальное, внутриочаговое, чрезкожное, эндоскопическое, через слизистую оболочку, сублингвальное и кишечное введение.
Фармацевтически приемлемые носители для использования в композициях по данному изобретению хорошо известны обычным специалистам в данной области и выбираются с учетом ряда факторов: конкретное используемое противоопухолевое соединение и его концентрация, стабильность и предполагаемая биодоступность; заболевание, нарушение или состояние, подвергаемые действию композиции; субъект, его возраст, размеры и общее состояние и путь введения. Подходящие носители легко определяются обычными специалистами в данной области (смотри, например, J.G.Nairn, в Remington's Pharmaceutical Science (A.Gennaro, ed.), Mack Publishing Co., Easton, Pa., (1985), с.1492-1517, содержание которой включено здесь в качестве ссылки).
Композиции предпочтительно приготовлены в виде таблеток, диспергируемых порошков, пилюль, капсул, желатиновых прокладок, покрышек, гелей, липосом, гранул, растворов, суспензий, эмульсий, сиропов, эликсиров, пастилок, драже, лепешек или любых других дозированных форм, которые могут вводиться перорально. Методы и композиции для изготовления пероральных дозированных форм, которые могут использоваться в данном изобретении, описаны в следующих ссылках: 7 Modern Pharmaceutics, части 9 и 10 (Banker & Rhodes, Editors, 1979); Lieberman и др.. Pharmaceutical Dosage Forms: Tablets (1981); и Ansel, Introduction to Pharmaceutical Dosage Forms 2-е издание (1976).
Композиции по изобретению для перорального введения содержат эффективное противоопухолевое количество соединения по изобретению в фармацевтически приемлемом носителе. Подходящие носители для твердых дозированных форм включают сахара, крахмалы и другие удобные вещества, включая лактозу, тальк, сахарозу, желатин, карбоксиметилцеллюлозу, агар, маннит, сорбит, фосфат кальция, карбонат кальция, карбонат натрия, каолин, альгиновую кислоту, аравийскую камедь, кукурузный крахмал, картофельный крахмал, сахаринат натрия, карбонат магния, трагакант, микрокристаллическую целлюлозу, коллоидный диоксид кремния, кроскармелозу натрия, тальк, стеарат магния и стеариновую кислоту. Далее такие дозированные формы могут быть непокрытыми или покрытыми с помощью известных методов, например, для задержки разрушения и абсорбции.
Противоопухолевые соединения по данному изобретению также предпочтительно вводят в состав препаратов для парентерального введения, например вводят в состав препаратов для инъекций внутривенным, внутриартериальным, подкожным, ректальным, подкожным, внутримышечным, внутриглазничным, внутрикапсульным, интраспинальным, внутрибрюшинным или внутригрудинным путями. Композиции по изобретению для парентерального введения содержат эффективное противоопухолевое количество противоопухолевого вещества в фармацевтически приемлемом носителе. Дозированными формами, пригодными для парентерального введения, являются растворы, суспензии, дисперсии, эмульсии или любые другие дозированные формы, которые могут быть введены парентерально. Технология и композиции для изготовления парентеральных дозированных форм известны из современного уровня техники.
Подходящими носителями, применяемыми при изготовлении жидких дозированных форм для перорального или парентерального введения, являются неводные, фармацевтически приемлемые полярные растворители, такие как масла, спирты, амиды, сложные эфиры, простые эфиры, кетоны, углеводороды и их смеси, также как и вода, соляные растворы, растворы декстрозы (например, DW5), растворы электролитов или любые другие водные фармацевтически приемлемые жидкости.
Подходящие неводные фармацевтически приемлемые полярные растворители включают, или не ограничиваются ими, спирты (например, α-формиат глицерина, β-формиат глицерина, 1,3-бутиленгликоль, алифатические или ароматические спирты, содержащие 2-30 атомов углерода, такие как метанол, этанол, пропанол, изопропанол, бутанол, трет-бутанол, гексанол, октанол, амиленгидрат, бензиловый спирт, глицерин, гликоль, гексиленгликоль, тетрагидрофуриловый спирт, лауриловый спирт, цетиловый спирт, или стеариловый спирт, эфиры жирных кислот с жирными спиртами, такие как полиалкиленгликоли (например, полипропиленгликоль, полиэтиленгликоль), сорбит, сахароза и холестерин); амиды (например, диметилацетамид (ДМА), бензилбензоат ДМА, диметилформамид, N-(β-гидроксиэтил)-лактамид, N,N-диметил-ацетамид-амиды, 2-пирролидинон, 1-метил-2-пирролидинон или поливинилпирролидон); сложные эфиры (например, 1-метил-2-пирролидинон, 2-пирролидинон, ацетаты, такие как моноацетат глицерина, диацетат глицерина и триацетат глицерина, алифатические или ароматические сложные эфиры, такие как этилкаприлат или октаноат, алкилолеат, бензилбензоат, бензилацетат, диметилсульфоксид (ДМСО), сложные эфиры глицерина, такие как моно-, ди- или триглицерилцитраты или тартраты, этилбензоат, этилацетат, этилкарбонат, этиллактат, этилолеат, эфиры жирных кислот с сорбитом, эфиры жирных кислот с ПЭГ, моностеарат глицерина, сложные эфиры глицерина (глицериды), такие как моно-, ди- или триглицериды, эфиры жирных кислот, такие как изопропилмиристат, эфиры жирных кислот с ПЭГ, такие как гидроксиолеат ПЭГ и гидроксистеарат ПЭГ, N-метилпирролидинон, плуроник 60 (pluronic 60), полиэфир полиоксиэтиленсорбита с олеиновой кислотой, такой как поли(олеат)2-4 поли-(этоксилированного)30-60 сорбита, моноолеат поли (оксиэтилена)15-20, моно-12-гидроксистеарат поли (оксиэтилена)15-20 и монорицинолеат поли (оксиэтилена)15-20, сложные эфиры полиоксиэтилен-сорбита, такие как моноолеат полиоксиэтилен-сорбита, монопальмитат полиоксиэтилен-сорбита, монолаурат полиоксиэтилен-сорбита, моностерат полиоксиэтилен-сорбита и Polisorbate® 20, 40, 60 или 80 от ICI Americas, Wilmington, DE, поливинилпирролидон, алкиленоксимодифицированные эфиры жирных кислот, такие как полиоксил 40 гидрированное касторовое масло и полиоксиэтилированное касторовое масло (например, раствор Cremophor® EL или раствор Cremophor® RH 40), сахариды жирных кислот (то есть продукты конденсации моносахарида (например, пентозы, такой как рибоза, рибулоза, арабиноза, ксилоза, ликсоза и ксилулоза, гексозы, такой как глюкоза, фруктоза, галактоза, манноза и сорбоза, триозы, тетрозы, гептозы и октозы), дисахарида (например, сахарозы, мальтозы, лактозы и трегалозы) или олигосахарида или их смеси с С4-С22 жирной кислотой(ами) (например, насыщенными жирными кислотами, такими как каприловая кислота, каприновая кислота, лауриновая кислота, миристиновая кислота, пальмитиновая кислота и стеариновая кислота, и ненасыщенными жирными кислотами, такими как пальмитолеиновая кислота, олеиновая кислота, элаидиновая кислота, эруковая кислота и линолевая кислота)) или стероидные сложные эфиры); алкиловые, ариловые или циклические простые эфиры, содержащие 2-30 атомов углерода (например, диэтиловый эфир, тетрагидрофуран, диметилизосорбид, моноэтиловый эфир диэтиленгликоля); гликофурфурол (эфир полиэтиленгликоля и тетрагидрофурфурилового спирта); кетоны, содержащие 3-30 атомов углерода (например, ацетон, метилэтилкетон, метилизобутилкетон); алифатические, циклоалифатические или ароматические углеводороды, содержащие 4-30 атомов углерода (например, бензол, циклогексан, дихлорметан, диоксоланы, гексан, н-декан, н-додекан, н-гексан, сульфолан, тетраметиленсульфон, тетраметиленсульфоксид, толуол, диметилсульфоксид (ДМСО) или тетраметиленсульфоксид); масла минерального, растительного, животного, эфирного или синтетического происхождения (например, минеральные масла, такие как алифатические или воскообразные углеводороды, ароматические углеводороды, смешанные алифатическо-ароматические углеводороды, и очищенное парафиновое масло, растительные масла, такие как льняное, тунговое, сафлоровое, соевое, касторовое, хлопковое, арахисовое, рапсовое, кокосовое, пальмовое, оливковое, кукурузное, из зародышей кукурузы, кунжутное, персиковое и арахисовое масло и глицериды, такие как моно-, ди- или триглицериды, животные масла, такие как рыбий жир, пиронафт, спермацет, жир печени трески, haliver, сквален, сквалан и жир печени акулы, олеиновые кислоты и полиоксиэтилированное касторовое масло); алкил- или арилгалогениды, содержащие 1-30 атомов углерода и, возможно, более одного галогенного заместителя; метиленхлорид; моноэтаноламин; нефтяной бензин; trolamine; омега-3 полиненасыщенные жирные кислоты (например, альфа-линоленовая кислота, эйкозанпентаеновая кислота, докозанпентаеновая кислота или докозангексаеновая кислота); полигликолевый эфир 12-гидроксистеариновой кислоты и полиэтиленгликоля (Solutol® HS-15, от BASF, Людвигсхафен, Германия); полиоксиэтиленглицерин; лаурат натрия; олеат натрия; или моноолеат сорбитана.
Другие фармацевтически приемлемые растворители для использования в изобретении хорошо известны обычным специалистам в данной области и указаны в The Chemotherapy Sourse Book (Williams & Wilkens Publishing), The Handbook of Pharmaceutical Excipiets (American Pharmaceutical Association, Washington D.C., и The Pharmaceutical Society of Great Britain, Лондон, Англия, 1968), Modern Pharmaceutics (G.Banker и др., eds., 3-е изд.) (Marcel Dekker, Inc. Нью-Йорк, Нью-Йорк, 1995), The Pharmacological Basis of Therapeutics (Goodman & Gilman, McGraw Hill Publishing), Pharmaceutical Dosage Forms (H.Lieberman и др., eds.) (Marcel Dekker, Inc., Нью-Йорк, Нью-Йорк, 1980), Remington's Pharmaceutical Sciences (A.Gennaro, ed., 19-е изд.) (Mack Publishing, Easton, PA, 1995), The United States Pharmacopeia 24, The National Formulary 19 (National Publishing, Philadelphia, PA, 2000), A.J.Spiegel и др., и Use of Nonaqueous Solvents in Parenteral Products, JOURNAL OF PHARMACEUTICAL SCIENCES, том 52, №10, стр. 917-927 (1963).
Предпочтительными растворителями являются такие, которые, как известно, стабилизируют противоопухолевые средства, такие как масла, богатые триглицеридами, например подсолнечное масло, соевое масло или их смесь, и эфиры алкиленоксимодифицированных жирных кислот, такие как полиоксил 40 гидрированное касторовое масло и полиоксиэтилированное касторовое масло (например, раствор Cremophor® EL или раствор Cremophor® RH 40). Коммерчески доступными триглицеридами являются эмульгированное соевое масло Intralipid® (Kabi-Pharmacia Inc., Стокгольм, Швеция), эмульсия Nutralipid® (McGaw, Irvine, Калифорния), 20%-ная эмульсия Lyposyn® II (20%-ный раствор жировой эмульсии, содержащей 100 мг сафлорового масла, 100 мг соевого масла, 12 мг яичных фосфатидов и 25 мг глицерина на мл раствора; Abbot Laboratories, Чикаго, Иллинойс), 2%-ная эмульсия Liposyn® III (2%-ный раствор жировой эмульсии, содержащей 100 мг сафлорового масла, 100 мг соевого масла, 12 мг яичных фосфатидов и 25 мг глицерина на мл раствора; Abbot Laboratories, Чикаго, Иллинойс), природные или синтетические производные, глицерина, содержащие докозагексаеноильную группу на уровне между 25% и 100% по массе в расчете на общее содержание жирной кислоты (Dhasco® (из Martek Biosciences Corp., Columbia, MD), DHA Maguro® (из Daito Enterprises, Los Angeles, CA)), Soyacalr® и Travemulsion®. Этанол является предпочтительным растворителем для применения в растворении противоопухолевого вещества с получением растворов, эмульсий и подобного.
В композиции по изобретению могут быть включены дополнительные второстепенные компоненты для различных целей, хорошо известные в фармацевтической промышленности. Указанные компоненты интересны с точки зрения большинства придаваемых свойств, которые улучшают удерживание противоопухолевого вещества в месте введения, повышают стабильность соединения, контролируют рН, облегчают введение противоопухолевого вещества в готовые препаративные фармацевтические формы и подобное. Предпочтительно каждый из указанных компонентов отдельно присутствует в количестве менее чем 15 массовых % от всей композиции, более предпочтительно менее 5 массовых % и наиболее предпочтительно менее чем 0,5 массовых % от всей композиции. Некоторые компоненты, такие как наполнители и разбавители, могут составлять до 90 мас.% от всей композиции, как хорошо известно для готовых препаративных форм. Такими добавками являются агенты, защищающие от замерзания для предотвращения переосаждения таксана, поверхностно-активные, смачивающие или эмульгирующие агенты (например, летицин, полисорбат-80, Tween® 80, плуроник (pluronic) 60, полиоксиэтиленстеарат), консерванты (например, этил-пара-гидроксибензоат), противомикробные консерванты (например, бензиловый спирт, фенол, мета-крезол, хлорбутанол, сорбиновая кислота, тимеросаль (thimerosal) и парабен), агенты для поддерживания рН или буферирующие агенты (например, кислоты, основания, ацетат натрия, монолаурат сорбитана), агенты для поддерживания осмотичности (например, глицерин), загустители (например, моностеарат алюминия, стераиновая кислота, цетиловый спирт, стеариловый спирт, гуаровая смола, метилцеллюлоза, гидроксипропилцеллюлоза, тристеарин, сложные эфиры цетилового воска, полиэтиленгликоль), подкрашиватели, красители, жидкие вспомогательные средства, нелетучие силиконы (например, циклометикон), глины (например, бентониты), адгезивы, увеличивающие объем агенты, отдушки, подслащивающие вещества, адсорбенты, наполнители (например, сахара, такие как лактоза, сахароза, маннит или сорбит, целлюлоза или фосфат кальция), разбавители (например, вода, солевой раствор или раствор электролита), связующие (например, крахмалы, такие как кукурузный крахмал, пшеничный крахмал, рисовый крахмал или картофельный крахмал, желатина, смола траганта, метилцеллюлоза, гидроксипропилметилцеллюлоза, натрийкарбоксиметилцеллюлоза, поливинилпирролидон, сахара, полимеры, аравийская камедь), дезинтегрирующие агенты (например, крахмалы, такие как кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал или карбоксиметилкрахмал, поперечно сшитый поливинилпирролидон, агар, альгиновая кислота или ее соль, такая как альгинат натрия, кроскармелоза натрия или кросповидон), смазки (например, оксид кремния, тальк, стеариновая кислота или ее соли, такие как стеарат магния, или полиэтиленгликоль), агенты покрытия (например, концентрированные растворы сахара, включая гуммиарабик, тальк, поливинилпирролидон, карбопольгель, полиэтиленгликоль или диоксид титана), и антиоксиданты (например, метабисульфит натрия, бисульфит натрия, сульфит натрия, декстроза, фенолы и тиофенолы).
В предпочтительном воплощении фармацевтическая композиция изобретения содержит по меньшей мере один неводный, фармацевтически приемлемый растворитель и противоопухолевое вещество, имеющее растворимость в этаноле по меньшей мере около 100, 200, 300, 400, 500, 600, 700 или 800 мг/мл. Хотя не будучи связано с конкретной теорией, утверждают, что растворимость в спирте противоопухолевого вещества может быть непосредственно отнесена к его эффективности. Противоопухолевое вещество может также быть способным к кристаллизации из раствора. Другими словами, кристаллическое противоопухолевое вещество, такое как вещество 1393, может быть растворено в растворителе с получением раствора и затем перекристаллизовано упариванием растворителя без образования аморфного противоопухолевого вещества. Предпочтительно также, чтобы противоопухолевое вещество имело значение ID50 (то есть концентрацию лекарства, дающую 50%-ное ингибирование образования опухоли) по меньшей мере в 4, 5, 6, 7, 8, 9 или 10 раз меньшее, чем у паклитакселя, будучи измерено согласно протоколу, приведенному в рабочих примерах.
Введение дозированных форм указанными путями может быть непрерывным или периодическим, в зависимости, например, от физиологического состояния пациента, является ли цель введения терапевтической или профилактической, и от других факторов, известных практикующим специалистам.
Дозы и режим введения фармацевтических композиций изобретения могут быть легко определены как обычно используемые при лечении рака. Понятно, что дозы противоопухолевых веществ зависят от возраста, пола, здоровья и веса реципиента, вида конкурентного лечения, частоты обработки и природы ожидаемого эффекта. Для любого способа введения фактическое количество доставленного противоопухолевого вещества, также как и режим дозирования, необходимый для достижения описанного: здесь преимущественного эффекта, зависит также, в частности, от таких факторов, как биосовместимость противоопухолевого вещества, нарушения, которое излечивают, желаемой терапевтической дозы, и других факторов, которые очевидны специалистам в данной области. Дозы, введенные животному, в частности человеку, в контексте данного изобретения должны быть достаточными для достижения желаемого терапевтического ответа у животного за приемлемый период времени. Предпочтительно эффективным количеством противоопухолевого вещества, введенного перорально или другим путем, является любое количество, которое приводит к желаемому терапевтическому ответу при введении указанным путем. Предпочтительно композиции для перорального введения готовят таким образом, чтобы единичная доза одной или более пероральных готовых препаративных форм содержала по меньшей мере 20 мг противоопухолевого вещества на м2 площади поверхности тела пациента или по меньшей мере 50, 100, 150, 200, 300, 400 или 500 мг противоопухолевого вещества на м2 площади поверхности тела пациента, где средняя площадь поверхности тела человека равна 1,8 м2. Предпочтительно единичная доза композиции для перорального введения содержит от примерно 20 до примерно 600 мг противоопухолевого вещества на м2 площади поверхности тела пациента, более предпочтительно от примерно 25 до примерно 400 мг/м2, даже более предпочтительно от примерно 40 до примерно 300 мг/м2 и еще более предпочтительно от примерно 50 до примерно 200 мг/м2. Предпочтительно композиции для парентерального введения приготовлены таким образом, что единичная доза содержит по меньшей мере 20 мг противоопухолевого вещества на м2 площади поверхности тела пациента или по меньшей мере 40, 50, 100, 150, 200, 300, 400 или 500 мг противоопухолевого вещества на м2 площади поверхности тела пациента. Предпочтительно единичная доза в одном или более парентеральных препаратов содержит от примерно 20 до примерно 500 мг противоопухолевого вещества на м2 площади поверхности тела соединения, более предпочтительно от примерно 40 до примерно 400 мг/м2 и даже более предпочтительно от примерно 60 до примерно 350 мг/м2. Однако дозировка может сильно зависеть от режима дозирования, которое может быть отрегулировано, как необходимо для достижения желаемого терапевтического эффекта. Следует отметить, что пределы эффективных доз, указанные здесь, не предлагают ограничивать изобретение и представляют собой предпочтительные пределы доз. Наиболее предпочтительные дозы следует назначать индивидуальному субъекту, как это понимает и определяет обычный специалист в данной области без излишего экспериментирования.
Концентрация противоопухолевого вещества в жидкой фармацевтической композиции предпочтительно равна между примерно 0,01 мг и примерно 10 мг на мл композиции, более предпочтительно между примерно 0,1 мг и примерно 7 мг на мл, даже более предпочтительно между примерно 0,5 мг и примерно 5 мг на мл и наиболее предпочтительно между примерно 1,5 мг и примерно 4 мг на мл. Относительно низкие концентрации обычно предпочтительны, поскольку противоопухолевые вещества наиболее растворимы в растворах с низкими концентрациями. Концентрация противоопухолевого вещества в твердой фармацевтической композиции для перорального введения находится предпочтительно в пределах между примерно 5 масовыми % и примерно 50 массовыми % в расчете на общую массу композиции, более предпочтительно между примерно 8 массовыми % и примерно 40 массовыми % и наиболее предпочтительно между примерно 10 массовыми % и примерно 30 массовыми %.
В одном из воплощений растворы для перорального введения готовят растворением противоопухолевого вещества в любом фармацевтически приемлемом растворителе, способным к растворению вещества (например, этаноле или метиленхлориде) с получением раствора. Соответствующий объем носителя, который является раствором, таким как раствор Cremophor® EL, прибавляют к раствору при перемешивании с получением фармацевтически приемлемого раствора для перорального введения пациенту. При желании такие растворы могут быть образованы с содержанием минимального количества или свободными от этанола, который, как известно на современном уровне техники, вызывает вредный физиологический эффект при введении в определенных концентрациях в пероральных готовых препаративных формах.
В другом воплощении порошки или таблетки для перорального введения готовят растворением противоопухолевого вещества в любом фармацевтически приемлемом растворителе, способным к растворению вещества (например, в этаноле или метиленхлориде) с получением раствора. Растворитель может быть способен к упариванию, если раствор сушат в вакууме. Перед сушкой к раствору может быть прибавлен дополнительный носитель, такой как раствор Cremophor® EL. Полученный раствор сушат в вакууме с получением стекловидной массы. Стекловидную массу затем смешивают со связующим с образованием порошка. Порошок может быть смешан с наполнителем или подходящими таблетирующими агентами и переработан с образованием таблеток для перорального введения пациенту. Порошок также может быть добавлен к любому жидкому носителю, как описано выше, с получением раствора, эмульсии, суспензии или подобного для перорального введения.
Эмульсии для парентерального введения могут быть получены растворением противоопухолевого вещества в любом фармацевтически приемлемом растворителе, способном к растворению вещества (например, в этаноле или метиленхлориде) с получением раствора. К раствору при перемешивании прибавляют соответствующий объем носителя, который является эмульсией, такой как эмульсии Liposyn® II или Liposyn® III, с получением фармацевтически приемлемой эмульсии для парентерального введения пациенту. При желании такие эмульсии могут быть приготовлены с содержанием минимального количества или свободными от этанола или раствора Cremophor®, которые, как известно на современном уровне техники, вызывают вредный физиологический эффект при введении определенных концентраций в парентеральных готовых препаративных формах.
Растворы для парентерального введения могут быть получены растворением противоопухолевого вещества в любом фармацевтически приемлемом растворителе, способном к растворению вещества (например, в этаноле или метиленхлориде) с получением раствора. К раствору при перемешивании прибавляют соответствующий объем носителя, который является раствором, таким как раствор Cremophor®, с получением фармацевтически приемлемого раствора для парентерального введения пациенту. При желании указанные растворы могут быть приготовлены с содержанием минимального количества или свободными от этанола или раствора Cremophor®, которые, как известно на современном уровне техники, вызывают вредный физиологический эффект при введении определенных концентраций в парентеральных готовых препаративных формах.
При желании эмульсии или растворы для перорального или парентерального введения могут быть расфасованы в IV пузырьки, ампулы или другие подходящие емкости в концентрированной форме и разбавленны любой фармацевтически приемлемой жидкостью, такой как солевой раствор, с получением приемлемой концентрации таксана перед применением, как известно на современном уровне техники.
Определения
Термины "углеводород" и "гидрокарбил", как использованы здесь, описывают органические соединения или радикалы, состоящие исключительно из элементов углерода и водорода. Указанными частями являются алкильные, алкенильные, алкинильные и арильные радикалы. К данным радикалам относятся также алкильные, алкенильные, алкинильные и арильные радикалы, замещенные другими алифатическими или циклическими углеводородными группами, такие как алкарил, алкенарил и алкинарил. Если не определено иначе, эти радикалы предпочтительно содержат от 1 до 20 атомов углерода.
"Замещенными гидрокарбильными" радикалами, описанными здесь, являются гидрокарбильные радикалы, замещенные по меньшей мере одним отличающимся от углерода атомом, включая радикалы, в которых углеродный атом в цепи замещен гетероатомом, таким как азот, кислород, кремний, фосфор, бор, сера или галоген. К данным заместителям относятся галоген, гетероцикло, алкокси-, алкенокси-, алкинокси-, арилокси-, гидрокси-, замещенная гидрокси-, кетогруппа, ацил, ацилокси-, нитро-, амино-, амидо-, нитро-, цианогруппы, тиольные, кетальные, ацетальные, сложноэфирные простые эфирные группы.
Термин "гетероатом" представляет собой атомы, отличающиеся от углерода и водорода.
"Гетерозамещенные метильные" радикалы означают здесь метильные группы, в которых атом углерода ковалентно связан с по меньшей мере одним гетероатомом и, возможно, с водородом; гетероатомом является, например, атом азота, кислорода, кремния, фосфора, бора, серы или галогена. Гетероатом может быть, в свою очередь, замещен другими атомами с образованием гетероциклического радикала, алкокси-, алкенокси-, алкинокси-, арилокси-, гидрокси-, замещенной гидрокси-, окси-, ацилокси-, нитро-, амино-, амидогрупп, тиольных, кетальных ацетальных, сложноэфирных или простых эфирных радикалов.
"Гетерозамещенные ацетатные радикалы", описанные здесь, являются ацетатными группами, в которых углерод метильной группы ковалентно связан с по меньшей мере одним гетероатомом и, возможно, с водородом; гетероатомом является, например, атом азота, кислорода, кремния, фосфора, бора, серы или галогена. Гетероатом может быть, в свою очередь, замещен другими атомами с образованием гетероциклического радикала, алкокси-, алкенокси-, алкинокси-, арилокси-, гидрокси-, замещенных гидрокси-, окси-, ацилокси-, нитро-, амино-, амидогрупп, тиольных, кетальных, ацетальных, сложноэфирных или простых эфирных радикалов.
Если не определено иначе, описанные здесь алкильные группы предпочтительно являются низшими алкилами, содержащими от одного до восьми атомов углерода в основной цепи и до 20 атомов углерода. Они могут быть линейной или разветвленной цепью или циклическими, и к ним относятся метил, этил, пропил, изопропил, бутил, гексил и подобные.
Если не определено иначе, описанные здесь алкенильные группы предпочтительно являются низшими алкенилами, содержащими от двух до восьми атомов углерода в основной цепи и до 20 атомов углерода. Они могут быть линейными или разветвленными и к ним относятся этенил, пропенил, изопропенил, бутенил, изобутенил, гексенил и подобные.
Если не определено иначе, описанные здесь алкинильные группы предпочтительно являются низшими алкинилами, содержащими от двух до восьми атомов углерода в основной цепи и до 20 атомов углерода. Они могут быть прямыми или разветвленными и к ним относятся этинил, пропинил, бутинил, изобутинил, гексинил и подобные.
Термины "арил" и "ar", как использованы здесь индивидуально или в качестве части другой группы, означают необязательно замещенные гомоциклические ароматические группы, предпочтительно моноциклические или бициклические группы, содержащие от 6 до 12 углеродов в цикле, такие как фенил, бифенил, нафтил, замещенный фенил, замещенный бифенил или замещенный нафтил. Фенил и замещенный фенил являются более предпочтительными арилами.
Термины "галоген" или "галогено", как использованы здесь индивидуально или как часть другой группы, относятся к хлору, брому, фтору и иоду.
Термины "гетероцикло" или "гетероциклический", как использовано здесь индивидуально или как часть другой группы, означают необязательно замещенные, полностью насыщенные или ненасыщенные, моноцикличекие или бициклические, ароматические или неароматические группы, содержащие по меньшей мере один гетероатом в по меньшей мере одном цикле и предпочтительно 5 или 6 атомов в каждом цикле. Гетероциклическая группа предпочтительно содержит 1 или 2 атома кислорода, 1 или 2 атома серы и/или от 1 до 4 атомов азота в цикле и может быть связана с остатком молекулы через углерод или гетероатом. Примерными гетероциклами являются гетероароматические соединения, такие как фурил, тиенил, пиридил, оксазолил, пирролил, индолил, хинолинил или изохинолинил и подобные. Примерными заместителями являются одна или более из следующих групп: гидрокарбил, замещенный гидрокарбил, кето-, гидрокси-, замещенная гидроксигруппа, ацил, ацилокси-, алкокси-, алкенокси-, алкинокси-, арилоксигруппы, галоген, амидо-, амино-, нитро-, цианогруппы, тиольные, кетальные, ацетальные, сложноэфирные и простые эфирные группы.
Термин "гетероароматический", как использован здесь индивидуально или как часть другой группы, представляет собой необязательно замещенные ароматические группы, содержащие по меньшей мере один гетероатом в по меньшей мере одном цикле и предпочтительно 5 или 6 атомов в каждом цикле. Гетероароматическая группа предпочтительно содержит 1 или 2 атома кислорода, 1 или 2 атома серы и/или от 1 до 4 атомов азота в цикле и может быть связана с остатком молекулы через углерод или гетероатом. Примерными гетероароматическими группами являются фурил, тиенил, пиридил, оксазолил, пирролил, индолил, хинолинил или изохинолинил и подобные. Примерными заместителями являются одна или более из следующих групп: гидрокарбил, замещенный гидрокарбил, кето-, гидрокси-, замещенная гидроксигруппа, ацил, ацилокси-, алкокси-, алкенокси-, алкинокси-, арилоксигруппы, галоген, амидо-, амино-, нитро-, цианогруппы, тиольные, кетальные, ацетальные, сложноэфирные и простые эфирные группы.
Термин "ацил", как использован здесь индивидуально или как часть другой группы, представляет собой радикал, образованный удалением гидроксигруппы из группы -СООН органической карбоновой кислоты, например, RC(O)-, где R представляет собой R1, R1O-, R1R2N- или R1S-, R1 представляет собой гидрокарбил, гетерозамещенный гидрокарбил или гетероцикло, а R2 представляет собой водород, гидрокарбил или замещенный гидрокарбил.
Термин "ацилокси", как использован здесь индивидуально или как часть другой группы, представляет собой ацильную группу, как описано выше, связанную через кислородную связь (-O-), например, RC(O)O-, где R такой как определено в связи с термином "ацил".
Если не определено иначе, описанные здесь алкоксикарбонилоксирадикалы содержат низший углеводородный радикал или замещенный углеводородный радикал или замещенный углеводородный радикал.
Если не определено иначе, описанные здесь карбамоилоксирадикалы являются производными карбаминовой кислоты, в которой один или оба водорода у амина заменены гидрокарбилом, замещенным гидрокарбилом или гетероциклическим радикалом.
Термин "гидроксизащитная группа", как использован здесь, означает группу, способную защитить свободную гидроксильную группу ("защищенный гидроксил"), которая после реакции, для которой была предназначена защита, может быть удалена без повреждения остающейся молекулы. Варианты защитных групп для гидроксильной группы и синтезы с ними могут быть найдены в "Protective Groups in Organic Syntheses", T.W.Greene, John Wiley and Sons, 1981, или Fieser & Fieser. Примерными защитными группами для гидроксила являются метоксиметил, 1-этоксиэтил, бензилоксиметил, (бета-триметилсилилэтокси)метил, тетрагидропиранил, 2,2,2-трихлорэтоксикарбонил, трет-бутил-(дифенил)силил, триалкилсилил, трихлорметоксикарбонил и 2,2,2-трихлоэтоксиметил.
Как использовано здесь, "Ac" представляет собой ацетил; "Bz" представляет собой бензоил; "Et" представляет собой этил; "Me" представляет собой метил; "Ph" представляет собой фенил; "Pr" представляет собой пропил; "Bu" представляет собой бутил; "Am" представляет собой амил; "cpro" представляет собой циклопропил; "iPr" представляет собой изопропил; "tBu" и "t-Bu" означают трет-бутил; "R" представляет собой низший алкил, если не определено иначе; "Py" представляет собой пиридин или пиридил; "TES" представляет собой триэтилсилил; "TMS" представляет собой триметилсилил; "LAH" представляет собой алюмогидрид лития; "10-DAB" представляет собой 10-дезацетилбаккатин III; "защитная группа для аминогруппы" представляет собой, но не ограничивает, карбаматы, например 2,2,2-трихлорэтилкарбамат или трет-бутилкарбамат; "защищенная гидроксигруппа" представляет собой ОР, где Р представляет собой гидроксизащитную группу; "PhCO" представляет собой фенилкарбонил; "tBuOCO" и "Boc" означают трет-бутоксикарбонил; "tAmOCO" представляет собой трет-амилоксикарбонил; "2-FuCO" представляет собой 2-фурилкарбонил; "2-ThCO" представляет собой 2-тиенилкарбонил; "2-PyCO" представляет собой 2-пиридилкарбонил; "3-PyCO" представляет собой 3-пиридилкарбонил; "4-PyCO" представляет собой 4-пиридилкарбонил; "С4Н7СО" представляет собой бутенилкарбонил; "tC3Н5СО" представляет собой транс-пропенилкарбонил; "EtOCO" представляет собой этоксикарбонил; "ibueCO" представляет собой изобутенилкарбонил; "iBuCO" представляет собой изобутилкарбонил; "iBuOCO" представляет собой изобутоксикарбонил; "iPrOCO" представляет собой изопропилоксикарбонил; "nPrOCO" представляет собой н-пропилоксикарбонил; "nPrCO" означает н-пропилкарбонил; "ibue" представляет собой изобутенил; "THF" представляет собой тетрагидрофуран (ТГФ); "DMAP" представляет собой 4-диметиламинопиридин (ДМАП); "LHMDS" представляет собой гексаметилдисилазанид лития.
Следующие примеры иллюстрируют изобретение.
Пример 1

10-Триэтилсилил-10-дезацетилбаккатин III.
К раствору 1,0 г (1,84 ммоль) 10-дезацетилбаккатина III в 50 мл ТГФ при -10°С в атмосфере азота прибавляли 0,857 мл (2,76 ммоль, 1,5 мол эквив.) N,O-(бис)-TES-трифторацетамида за 3 мин. Затем добавляли 0,062 мл 0,89 М раствора в ТГФ бис(триметилсилил)амида лития (0,055 ммоль, 0,03 мол. экв.). Через 10 мин прибавляли 0,038 мл (0,92 ммоль, 0,5 мол. экв.) метанола и через 5 мин дополнительно прибавляли 4 мл (0,055 ммоль, 0,03 мол. экв.) уксусной кислоты. Раствор разбавляли 300 мл этилацетата и промывали два раза 100 мл насыщенного водного раствора бикарбоната натрия. Объединенные водные слои экстрагировали 100 мл этилацетата и объединенные органические слои промывали насыщенным солевым раствором, сушили над сульфатом натрия и концентрировали при уменьшенном давлении. К остатку прибавляли 100 мл гексана и твердый продукт (1,23 г, 101%) собирали фильрованием. Перекристаллизация твердого вещества растворением в кипящем этилацетате (20 мл, 17 мл/г) и охлаждение до комнатной температуры дало 1,132 г (94%) белого твердого продукта с т.пл. 242°С; [α]D 25 - 60,4 (с 0,7, CHCl3); 1H ЯМР (COCl3, 400 МГц) δ (м.д.): 8,10 (2Н, д, Jm=7,5 Гц, Bz-орто), 7,60 (1Н, т, Jm=7,5 Гц, Bz-пара), 7,47 (2Н, т, Jo=7,5 Гц, Bz-мета), 5,64 (1H, д, J3=6,9 Гц, Н2), 5,26 (1Н, с, Н10), 4,97 (1H, дд, J6β=2,2 Гц, J6α=9,9 Гц, Н5), 4,85 (1H, дд, J14α=8,9 Гц, J14β=8,9 Гц, Н13), 4,30 (1H, д, J20β=8,5 Гц, H20α), 4,23 (1H, ддд, J7OH=4,5 Гц, J6α=6,6 Гц, J6β=11,0 Гц, Н7), 4,15 (1H, д, J20α=8,5 ГЦ, Н20β), 4,00 (1H, д, J2=6,9 Гц, Н3), 2,58 (1H, ддд, J7=6,6 Гц, J5=9,9 Гц, J6β=14,5 Гц, Н6α), 2,28-2,25 (5Н, м, 4Ac, Н14α, Н14β), 2,02 (3Н, с, 18Ме), 1,97 (1H, д, J7=4,5 Гц, Н7OН), 1,78 (1H, ддд, J7=11,0 Гц, J5=2,2 Гц, J6α=14,5 Гц, Н6β), 1,68 (3Н, с, 19Ме), 1,56 (1H, с, ОН1), 1,32 (1H, д, J13=8,8 Гц, ОН13), 1,18 (3Н, с, 17Ме), 1,06 (3Н, с, 16Ме), 0,98 (9Н, т, JCH2 (TES)=7,3 Гц, СН3 (TES)), 0,65 (6Н, дкв., JCH3 (TES)=7,3 Гц, СН2(TES)).

10-Триэтилсилил-10-дезацетил-7-пропионилбаккатин III.
К раствору 1,0 г (1,517 ммоль) 10-триэтилсилил-10-дезацетилбаккатина III и 37,0 мг (0,303 ммоль) ДМАП в 20 мл дихлорметана при комнатной температуре в атмосфере азота прибавляли 0,920 мл (11,381 ммоль) пиридина и 0,329 мл (3,794 ммоль, 2,5 мол. экв.) пропионилхлорида в указанном порядке. Смесь перемешивали при комнатной температуре 6 ч, разбавляли 350 мл этилацетата и экстрагировали 50 мл 10%-ного водного раствора сульфата меди. Органический слой промывали 50 мл насыщенного водного раствора бикарбоната натрия, 50 мл насыщенного солевого раствора, сушили над сульфатом натрия и концентрировали при пониженном давлении. Сырой продукт растворяли в 75 мл этилацетата, прибавляли 100 мг Norit A, смесь фильтровали через целит и концентрировали при пониженном давлении, получая 1,13 г материала. Перекристаллизация из этилацетата/гексана (растворяли в 6,5 мл кипящего этилацетата, затем прибавляли 24 мл гексана, оставляли охлаждаться до комнатной температуры и оставляли стоять на 17 ч) дала 787 мг (72,5%) белого кристаллического твердого вещества. Вторая перекристаллизация (примерно 340 мг материала растворяли в 2 мл кипящего этилацетата, затем прибавляли 10 мл гексана, оставляли охлаждаться до комнатной температуры и оставляли стоять на 17 ч) дала 181 мг (16,7%) белого кристаллического твердого вещества. Общий выход после перекристаллизации был 89,2%, т.пл. 129°С; [α]D 25 - 47,9 (с 1,0, CHCl3); ЯМР 1H (COCl3, 300 МГц) δ (м.д.): 8,10 (2Н, д, Jm=7,4 Гц, Bz-орто), 7,60 (1H, т, Jm=7,4 Гц, Bz-пара), 7,48 (2Н, дд, Jo=7,4 Гц, Jp=7,4 Гц, Bz-мета), 5,64 (1H, д, J3=7,4 Гц, Н2), 5,47 (1H, дд, J6α=7,4 Гц, J6β=10,1 Гц, Н7), 5,28 (1H, с, Н10), 4,94 (1H, д, J6α=9,4 Гц, Н5), 4,80-4,90 (1H, м, Н13), 4,31 (1H, д, J20β=8,1 Гц, Н20α), 4,16 (1H, д, J20α=8,l Гц, Н20β), 4,06 (1H, д, J2=7,4 Гц, Н3), 2,55 (1H, ддд, J7=7,4 Гц, J5=9,4 Гц, J6β=14,8 ГЦ, Н6α), 2,28 (3Н, с, 4Ac), 2,23-2,32 (4Н, м, 7СН2, Н14α, Н14β), 2,07 (3Н, с, 18Ме), 2,02 (1H, д, J13=4,7 Гц, ОН13), 1,76-1,87 (4Н, м, 5 Н6β, 19Ме), 1,60 (1H, с, ОН1), 1,17 (3Н, с, 17Ме), 1,09 (3Н, т, J7CH2=7,4 Гц, 7СН3), 1,04 (3Н, с, 16Ме), 0,96 (9Н, т, JCH2(TES)=8,0 Гц, СН3(TES)), 0,52-0,62 (6Н, м, СН2(TES)).

2'-O-МОР-3'-дезфекил-3'-(2-фурил)-10-триэтилсилил-7-пропионилтаксотер.
К раствору 493 мг (0,690 ммоль) 10-триэтилсилил-10-дезацетил-7-пропионилбаккатина III в 4 мл безводного ТГФ в атмосфере азота при -45°С прибаляли 0,72 мл (0,72 ммоль) 1М раствора LiHMDS в ТГФ. Через 0,5 ч прибавляли раствор 263 мг (0,814 ммоль) бета-лактама (перварительно высушенного как описано выше) в 2 мл безводного ТГФ. Смесь нагревали до 0°С и через 2 ч прибавляли 0,5 мл насыщенного водного раствора бикарбоната натрия. Смесь разбавляли 50 мл этилацетата и промывали два раза 5 мл насыщенного солевого раствора. Органическую фазу сушили над сульфатом натрия и концентрировали при пониженном давлении, получая 742 мг (104%) светло-желтого твердого вещества. Твердое вещество перекристаллизовывали растворением его в 12 мл смеси 1:5 этилацетата и гексана при кипячении с обратным холодильником и последующим охлаждением до комнатной температуры, получая 627 мг (88%) белого кристаллического вещества. Упаривание маточного раствора дало 96 мг материала, который перекристаллизовывали как описано выше из 2 мл смеси 1:5 эцетилацетата и гексана, получая дополнительно 46 мг (6%) белого кристаллического твердого вещества. Общий выход после перекристаллизации был 94%. Упаривание маточного раствора дало 46 мг материала, который был очищен колоночной хроматографией на силикагеле, дав дополнительно 20 мг (3%) продукта с т.пл. 207-209°С; [α]D 25 - 30,0 (с 5,0, метанол); 1H ЯМР (COCl3, 400 МГц) δ (м.д.): 8,09-8,11 (м, 2Н), 7,58-7,61 (м, 1Н), 7,47-7,51 (м, 2Н), 7,39 (д, J=0,8 Гц, 1Н), 6,34 (дд, J=3,2, 1,6 Гц, 1Н), 6,26 (д, J=3,2 Гц), 6,14 (дд, J=8,8, 8,8 Гц, 1Н), 5,71 (д, J=6,8 Гц, 1Н), 5,47 (дд, J=10,0, 7,2 Гц, 1Н), 5,30-5,36 (м, 2Н), 5,28 (с, 1Н), 4,95 (д, J=7,6 Гц, 1Н), 4,76 (с, 1Н), 4,33 (д, J=8,0 Гц, 1Н), 4,19 (д, J=8,4 Гц, 1Н), 4,03 (д, J=6,8 Гц, 1Н), 2,83 (с, 3Н), 2,55 (ддд, J=17,2, 9,6, 7,6, 1Н), 2,50 (с, 3Н), 2,20-2,40 (м, 2Н), 2,28 (кв., J=7,6 Гц, 2Н), 1,95 (с, 3Н), 1,84 (ддд, J=14,8, 10,8, 2 Гц), 1,80 (с, 3Н), 1,67 (с, 1Н), 1,39 (с, 9Н), 1,32 (с, 3Н), 1,21 (с, 3Н), 1,20 (с, 3Н), 1,74 (с, 3Н), 1,09 (т, J=7,6 Гц, 3Н), 0,93-0,99 (м, 9Н), 0,50-0,65 (м, 6Н).

3'-Дезфенил-3'-(2-фурил)-7-пропионилтаксотер (1393)
К раствору 206 мг (0,199 ммоль) 2'-O-МОР-3'-дезфенил-3'-(2-фурил)-10-триэтилсилил-7-пропионилтаксотера в 1,7 мл пиридина и 5,4 мл ацетонитрила при 0°С прибавляли 0,80 мл (2,0 ммоль) водного раствора, содержащего 49% HF. Смесь нагревали до комнатной температуры 14 ч и затем разбавляли 20 мл этилацетата и промывали три раза 2 мл насыщенного водного бикарбоната натрия и затем 8 мл насыщенного солевого раствора. Органическую фазу сушили над сульфатом натрия и концентрировали при пониженном давлении, получая 170 мг (100%) белого твердого вещества. Сырой продукт кристаллизовали с 2 мл растворителя (СН2Cl2:гексан=1:1,7), получая 155 мг (90,5%) белых кристаллов. Концентрирование маточного раствора при пониженном давлении дало 15 мг материала, который перекристаллизовывали с применением 0,2 мл смеси 1:1,7 метиленхлорида и гексана, получая дополнительно 11 мг (7,5%) белых кристаллов. Общий выход от перекристаллизации был 98%, т.пл. 150-152°С; [α]D 25 - 27,0 (с 5,0, метанол; анализ: вычислено для C44H55NO16·0,5 H2O: С, 61,18; Н, 6,48. Найдено: С, 61,40; Н. 6,65. 1H ЯМР (CDCCl3, 500 МГц) d (м.д.): 8,11 (д, J=7,5 Гц, 2Н), 7,61 (дд, J=7,5, 7,5 Гц, 1Н), 7,50 (дд, J=8,0, 7,5 Гц, 2Н), 7,41 (д, J=1,0 Гц, 1Н), 6,38 (dd, J=3,0, 2,0 Гц, 1Н), 6,33 (д, J=3,5 Гц), 6,22 (дд, J=9,5, 9,5 Гц, 1H), 5,69 (д, J=7,0 Гц, 1 Н), 5,49 (дд, J=11,0, 7,5 Гц, 1 Н), 5,35 (д, J=9,5 Гц, 1 Н), 5,33 (д, J=1,5 Гц, 1H), 5,25 (д, J=9,5 Гц, 1H), 4,94 (д, J=8,5 Гц, 1H), 4,71 (дд, J=5,5, 2,0 Гц, 1H), 4,33 (д, J=8,5 Гц, 1H), 4,21 (д, J=8,5 Гц, 1H), 4,01 (д, J=6,5 Гц, 1Н), 3,97 (д, J=1,5 Гц, 1H), 3,30 (д, J=5,5 Гц, 1H), 2,54 (ддд, J=16,5, 9,5, 7,0, 1H), 2,41 (с, 3Н), 2,37 (дд, J=15,0, 9,0 Гц, 1H), 2,30 (дд, J=17,5, 9,5 Гц, 1H), 2,25 (кв., J=7,5 Гц, 2Н), 1,96 (с, 3Н), 1,93 (ддд, J=14,5, 11,0, 2,5 Гц), 1,85(с, 3Н), 1,64 (с, 1H), 1,36 (с, 9Н), 1,23 (с, 3Н), 1,10 (т, J=7,5 Гц, 3Н).
Пример 2
Процедуры примера 1 повторяли, но другими подходящими защищенными β-лактамами были заменены β-лактамы примера 1 для получения серии соединений, имеющих структурную формулу (13) и комбинации заместителей, приведенные в следующей таблице 1.

Пример 3
Следуя процедуре, описанной в примере 1 и в другом месте описания, могут быть получены конкретные таксаны, имеющие структурную формулу 14, где: R7 как определено ранее, в том числе R7 представляет собой R7aCOO- и R7a представляет собой (i) замещенный или незамещенный C2-C8 алкил (прямой, разветвленный или циклический), такой как этил, пропил, бутил, пентил или гексил; (ii) замещенный или незамещенный C2-C8 алкенил (прямой, разветвленный или циклический), такой как этенил, пропенил, бутенил, пентенил или гексенил; (iii) замещенный или незамещенный C2-C8 алкинил (прямой или разветвленный), таклй как этинил, пропинил, бутинил, пентинил или гексинил; (iv) замещенный или незамещенный фенил; или (v) замещенный или незамещенный гетероцикло, такой как фурил, тиенил или пиридил. Заместителями могут быть гидрокарбил или любые содержащие гетероатом заместители, выбранные из группы, состоящей из гетероцикло, алкокси-, алкенокси-, алкинокси-, арилокси-, гидрокси-, защищенной гидрокси-, кето-, асилокси-, нитро-, амино-, амидогрупп, тиольной, кетальной, ацетальной, сложноэфирной и простой эфирной групп, но не фосфорсодержащих радикалов (см. табл.2).

Пример 4
Следуя методу, описанному в примере 1 и в другом месте описания, могут быть получены конкретные таксаны, имеющие структурную формулу 15, где R10 представляет собой гидрокси и R7 в каждой из серий (то есть в каждой из серий с "А" по "К") такой, как определено ранее, в том числе R7 представляет собой R7aCOO- и R7a представляет собой (i) замещенный или незамещенный, предпочтительно незамещенный, С2-С8 алкил (прямой, разветвленный или циклический), такой как этил, пропил, бутил, пентил или гексил; (ii) замещенный или незамещенный, предпочтительно незамещенный, C2-C8 алкенил (прямой, разветвленный или циклический), такой как этенил, пропенил, бутенил, пентенил или гексенил; (iii) замещенный или незамещенный, предпочтительно незамещенный, С2-С8 алкинил (прямой или разветвленный), такой как этинил, пропинил, бутинил, пентинил или гексинил; (iv) замещенный или незамещенный, предпочтительно незамещенный, фенил; или (v) замещенный или незамещенный, предпочтительно незамещенный гетероароматический радикал, такой как фурил, тиенил или пиридил.
В соединениях серии "А" Х10 представляет собой в остальном как определено здесь. Предпочтительно гетероцикло представляет собой замещенные или незамещенные фурил, тиенил или пиридил, Х10 представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил (например, трет-бутил) и каждый из R7 и R10 имеет бета-стереохимическую конфигурацию.
В соединениях серии "В" Х10 и R2a означают в остальном как определено здесь. Предпочтительно гетероцикло представляет собой замещенные или незамещенные фурил, тиенил или пиридил, Х10 предпочтительно представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил (например, трет-бутил), R2a предпочтительно представляет собой фурил, замещенный или незамещенный тиенил, пиридил, фенил или низший алкил и каждый из R7 и R10 имеют бета-стереохимическую конфигурацию.
В соединениях серии "С" Х10 и R9а означают как определено здесь. Предпочтительно гетероцикло представляет собой замещенные или незамещенные фурил, тиенил или пиридил, Х10 предпочтительно представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил (например, трет-бутил), R9а предпочтительно представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил и каждый из R7, R9 и R10 имеют бета-стереохимическую конфигурацию.
В соединениях серий "D" и "Е" Х10 представляет собой как определено здесь. Предпочтительно гетероцикло представляет собой замещенные или незамещенные фурил, тиенил или пиридил, Х10 предпочтительно представляет собой замещенные или незамещенные фурил, тиенил пиридил, фенил или низший алкил (например, трет-бутил) и каждый из R7, R9 (только для серии D) и R10 имеют бета-стереохимическую конфигурацию.
В соединениях серии "F" Х10, R2a, и R9а означают как определено здесь. Предпочтительно гетероцикло представляет собой замещенные или незамещенные фурил, тиенил или пиридил, Х10 предпочтительно представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил (например, трет-бутил), R2a предпочтительно представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил и каждый из R7, R9 и R10 имеет бета-стереохимическую конфигурацию.
В соединениях серии "G" Х10 и R2a означают как определено здесь. Предпочтительно гетероцикло представляет собой замещенные или незамещенные фурил, тиенил или пиридил, Х10 предпочтительно представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил (например, трет-бутил), R2a предпочтительно представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил и каждый из R7, R9 и R10 имеют бета-стереохимическую конфигурацию.
В соединениях серии "Н" Х10 представляет собой как определено здесь. Предпочтительно гетероцикло представляет собой замещенные или незамещенные фурил, тиенил или пиридил, Х10 предпочтительно представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил (например, трет-бутил), R2a предпочтительно представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил и каждый из R7 и R10 имеет бета-стереохимическую конфигурацию.
В соединениях серии "I" Х10 и R2a означают как определено здесь. Предпочтительно гетероцикло представляет собой замещенные или незамещенные фурил, тиенил или пиридил, Х10 предпочтительно представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил (например, трет-бутил), R2a предпочтительно представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил и каждый из R7 и R10 имеет бета-стереохимическую конфигурацию.
В соединениях серии "J" Х10 и R2a означают как определено здесь. Предпочтительно гетероцикло представляет собой замещенные или незамещенные фурил, тиенил или пиридил, Х10 предпочтительно представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил (например, трет-бутил), R2a предпочтительно представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил и каждый из R7, R9 и R10 имеет бета-стереохимическую конфигурацию.
В соединениях серии "К" Х10, R2a и R9а означают как определено здесь. Предпочтительно гетероцикло представляет собой замещенные или незамещенные фурил, тиенил или пиридил, Х10 предпочтительно представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил (например, трет-бутил), R2a предпочтительно представляет собой замещенные или незамещенные фурил, тиенил, пиридил, фенил или низший алкил, и каждый из R7, R9 и R10 имеет бета-стереохимическую конфигурацию.
Любые заместители в каждом из Х3, Х5, R2, R7 и R9 могут быть гидрокарбилом или любым содержащим гетероатом заместителем, выбранным из группы, состоящей из гетероцикло, алкокси-, алкенокси-, алкинокси-, арилокси-, гидрокси-, защищенной гидрокси-, кето-, асилокси-, нитро-, амино-, амидогрупп, тиольной, кетальной, ацетальной, сложноэфирной и простой эфирной групп, но не фосфорсодержащих радикалов.

С2-С8 алкил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкенил
С2-С8 алкенил
С2-С8 алкенил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкенил
С2-С8 алкенил
С2-С8 алкенил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкенил
С2-С8 алкенил
С2-С8 алкенил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкенил
С2-С8 алкенил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкенил
С2-С8 алкенил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкенил
С2-С8 алкенил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкенил
С2-С8 алкенил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкенил
С2-С8 алкенил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкенил
С2-С8 алкенил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкенил
С2-С8 алкенил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкил
С2-С8 алкенил
С2-С8 алкенил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
С2-С8 алкинил
Пример 5
Цитотоксичность in vitro, измеренная пробой образования колонии клеток
Четыреста клеток (НСТ116) помещали в 60 мм чашки Петри, содержащие 2,7 мл среды (модифицированной среды McCoy's 5a, содержащей 10% зародышевой бычьей сыворотки и 100 единиц/мл пенициллина и 100 г/мл стрептомицина). Клетки инкубировали в инкубаторе с CO2 при 37°С 5 ч для осаждения на дно чашек Петри. Соединения, идентифицированные в примере 2, были свежеприготовленными в среде с десятикратной от конечной концентрации, и затем 0,3 мл указанного основного раствора прибавляли к 2,7 мл среды в чашке. Клетки затем инкубировали с лекарством 72 ч при 37°С. По окончании инкубирования содержащую лекарство среду декантировали, чашки споласкивали 4 мл солевого раствора Hank's Balance (HBSS), прибавляли 5 мл свежей среды и чашки возвращали в инкубатор для образования колонии. Колонии клеток обсчитывали с применением счетчика колоний через 7 дней инкубирования. Было подсчитано выживание клеток и для каждого соединения были определены значения ID50 (концентрация лекарства, обеспечивающая 50%-ное ингибирование образования колонии) (см. табл.4).
Пример 6
Приготовление растворов для перорального введения
Раствор 1: Противоопухолевое соединение 1393 растворяли в этаноле с получением раствора, содержащего 140 мг вещества на мл раствора. К раствору при перемешивании прибавляли равный объем раствора Cremophor® EL с получением раствора, содержащего 70 мг вещества 1393 на мл. Данный раствор разбавляли, используя 9 частей по весу физиологического раствора с получением фармацевтически приемлемого раствора для введения пациенту.
Раствор 2: Противоопухолевое соединение 1458 растворяли в этаноле с получением раствора, содержащего 310 мг вещества на мл раствора. К раствору при перемешивании прибавляли равный объем раствора Cremophor® EL с получением раствора, содержащего 155 мг вещества 1458 на мл. Данный раствор разбавляли, используя 9 частей по весу физиологического раствора с получением фармацевтически приемлемого раствора для введения пациенту.
Раствор 3: Противоопухолевое соединение 1351 растворяли в этаноле с получением раствора, содержащего 145 мг вещества на мл раствора. К раствору при перемешивании прибавляли равный объем раствора Cremophor® EL с получением раствора, содержащего 72,5 мг соединения 1351 на мл. Данный раствор разбавляли, используя 9 частей по весу физиологического раствора с получением фармацевтически приемлемого раствора для введения пациенту.
Раствор 4: Противоопухолевое соединение 4017 растворяли в этаноле с получением раствора, содержащего 214 мг вещества на мл раствора. К раствору при перемешивании прибавляли равный объем раствора Cremophor® EL с получением раствора, содержащего 107 мг соединения 4017 на мл. Данный раствор разбавляли, используя 9 частей по весу физиологического раствора с получением фармацевтически приемлемого раствора для введения пациенту.
Раствор 5: Противоопухолевое соединение 1393 растворяли в 100%-ном этаноле, затем смешивали с равным объемом раствора Cremophor® EL с получением раствора, содержащего 70 мг соединения 1393 на мл. Данный раствор разбавляли, используя 9 частей по весу D%W (водный раствор, содержащий 5% по весу на объем декстрозы) или 0,9%-ного солевого раствора с получением фармацевтически приемлемого раствора для введения пациенту.
Пример 7
Приготовление суспензии, содержащей соединение 1393, для перорального введения
Пероральную композицию противоопухолевого соединения 1393 готовили суспендированием 25 мг вещества 1393 в виде тонкого порошка в 1 мл носителя, содержащего 1% карбоксиметилцеллюлозы (CMC) в деионизированной воде.
Пример 8
Приготовление таблетки, содержащей соединение 1393, для перорального применения
Противоопухолевое соединение 1393 (100 мг) растворяли в метиленхлориде (2 мл) и прибавляли раствор Cremophor® EL (100 мг). Метиленхлорид упаривали в вакууме с получением стеклообразной массы. К стеклообразной массе прибавляли микрокристаллическую целлюлозу (600 мг) и перемешивали с получением порошка, который может быть переработан в форму таблетки.
Пример 9
Приготовление эмульсии, содержащей соединение 1393 для парентерального введения
Эмульсия 1: Противоопухолевое соединение 1393 растворяли в 100% этаноле с получением раствора, содержащего 40 мл соединения 1393 на мл раствора. Раствор затем разбавляли 19 частями по весу Liposyn® III (20%) при перемешивании с получением эмульсии, содержащей 2 мг соединения 1393 на мл, для парентерального введения.
Эмульсия 2: Противоопухолевое соединение 1393 растворяли в 100% этаноле с получением раствора, содержащего 40 мл соединения 1393 на мл раствора. Раствор затем разбавляли 19 частями по весу Liposyn® III (2%) при перемешивании с получением эмульсии, содержащей 2 мг соединения 1393 на мл, для парентерального введения.
Эмульсия 3: Противоопухолевое соединение 1393 растворяли в 100% этаноле с получением раствора, содержащего мг соединения 1393 на мл раствора. Раствор затем разбавляли 9 частями по весу Liposyn® III (2%) при перемешивании с получением эмульсии, содержащей 4 мг соединения 1393 на мл, для парентерального введения.
Пример 10
Приготовление растворов, содержащих соединение 1393, для парентерального введения
Раствор 1: Противоопухолевое соединение 1393 растворяли в 100% этаноле с получением раствора, содержащего 140 мг соединения 1393 на мл раствора. Раствор затем разбавляли при перемешивании равным объемом раствора Cremophor® EL и затем разбавляли 9 частями по весу нормального солевого раствора с получением раствора, содержащего 7 мг соединения 1393 на мл раствора для парентерального введения.
Раствор 2: Противоопухолевое соединение 1393 растворяли в 100% этаноле с получением раствора, содержащего 140 мг соединения 1393 на мл раствора. Раствор затем разбавляли при перемешивании равным объемом раствора Cremophor® EL и затем разбавляли 4 частями по весу нормального солевого раствора с получением раствора, содержащего 11,7 мг соединения 1393 на мл раствора для парентерального введения.
Раствор 3: Противоопухолевое соединение 1393 растворяли в 100% этаноле с получением раствора, содержащего 140 мг соединения 1393 на мл раствора. Раствор затем разбавляли при перемешивании равным объемом раствора Cremophor® EL и затем разбавляли 2,33 частями по весу нормального солевого раствора с получением раствора, содержащего 16,2 мг соединения 1393 на мл раствора для парентерального введения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТАКСАН, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ И СПОСОБ ИНГИБИРОВАНИЯ РОСТА ОПУХОЛИ | 2001 |
|
RU2264400C2 |
| ТАКСАНЫ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СПОСОБЫ ИНГИБИРОВАНИЯ | 2001 |
|
RU2265019C2 |
| КАТАЛИТИЧЕСКАЯ СИСТЕМА | 2003 |
|
RU2326123C2 |
| ПРОИЗВОДНЫЕ ТАКСАНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ | 1994 |
|
RU2137764C1 |
| АЗАИНДОЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА Xa | 2004 |
|
RU2330853C2 |
| ТИОЛСУЛЬФОНАМИДНЫЕ ИНГИБИТОРЫ МЕТАЛЛОПРОТЕАЗЫ | 1997 |
|
RU2202540C2 |
| ТАКСАНЫ С БОКОВОЙ ЦЕПЬЮ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, СПОСОБЫ ПОЛУЧЕНИЯ | 1993 |
|
RU2125042C1 |
| НОВЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ КАК ИНГИБИТОРЫ BRD4 | 2016 |
|
RU2721120C2 |
| ПОЛИЦИКЛИЧЕСКИЕ АГЕНТЫ ДЛЯ ЛЕЧЕНИЯ РЕСПИРАТОРНО-СИНЦИТИАЛЬНЫХ ВИРУСНЫХ ИНФЕКЦИЙ | 2007 |
|
RU2486185C2 |
| ПРОИЗВОДНЫЕ ОКСАДИАЗОЛА, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВЫМ ДЕЙСТВИЕМ, ЛЕКАРСТВЕННОЕ СРЕДСТВО, ИХ СОДЕРЖАЩЕЕ, И СПОСОБ ЛЕЧЕНИЯ | 2001 |
|
RU2275371C2 |
Изобретение относится к новым соединениям - С7 сложноэфирзамещенньм таксанам общей структурной формулы:

где R2 представляет собой бензоилокси; R7 представляет собой R7aCOO-;
R10 представляет собой гидрокси; Х3 представляет собой С1-8алкил, С2-8алкенил, С2-8алкинил или 5- или 6-членную гетероарильную группу, содержащую гетероатом, выбранный из О, N и S; X5 представляет собой -СОХ10, где Х10 представляет собой С1-8алкил, С2-8алкенил, фенил или 5- или 6-членную гетероарильную группу, содержащую гетероатом, выбранный из О, N и S; или представляет собой -СООХ10, где Х10 представляет собой С1-8алкил или С2-8алкенил; R7a представляет собой С1-20алкил или С2-20алкенил; Ас представляет собой ацетил. Эти соединения обладают противоопухолевой активностью. Изобретение также относится к способу ингибирования роста опухолей у млекопитающих и фармацевтической композиции на основе полученных соединений. Технический результат - получения новых производных таксана, обладающих более высокой противоопухолевой активностью и более низкой токсичностью по сравнению с таксолом и таксотером. 3 н. и 36 з.п. ф-лы, 4 табл.

где R2 представляет собой бензоилокси;
R7 представляет собой R7aCOO-;
R10 представляет собой гидрокси;
Х3 представляет собой C1-8алкил, С2-8алкенил, С2-8алкинил или 5- или 6-членную гетероарильную группу, содержащую гетероатом, выбранный из О, N и S;
Х5 представляет собой -СОХ10, где Х10 представляет собой С1-8алкил, С2-8алкенил, фенил или 5- или 6-членную гетероарильную группу, содержащую гетероатом, выбранный из О, N и S;
или представляет собой -СООХ10, где Х10 представляет собой С1-8алкил или С2-8алкенил;
R7a представляет собой С1-20алкил или С2-20алкенил;
Ас представляет собой ацетил.
| RU 2059631 C1, 10.05.1996 | |||
| ТАКСОИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1995 |
|
RU2144920C1 |
| WO 9744026 A1, 27.11.1997 | |||
| Приспособление для автоматического и периодического продвигания бумажной ленты в адресопечатающей машине | 1924 |
|
SU1366A1 |
| US 5415869 A, 16.05.1995. | |||
Авторы
Даты
2005-11-27—Публикация
2001-02-02—Подача