Изобретение относится к новым замещенным иминоазинам, способам их получения и их применению в качестве средств обработки растений, в особенности, в качестве гербицидов.
Известно, что определенные замещенные иминопиридины обладают гербицидными свойствами (см. заявку на Европейский патент 432600). Активность этих соединений, однако, не во всех отношениях является удовлетворительной.
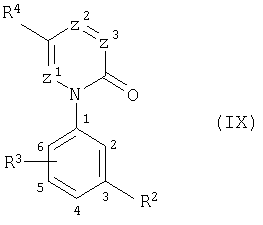
В настоящее время найдены новые замещенные иминоазины общей формулы (I):
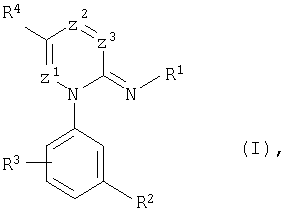
в которой
R1 означает нитрогруппу, цианогруппу или одну из группировок -R5, -CQ1Q2R5, -NH-CQ1-R5 или -SO2-R6;
R2 означает нитрогруппу, цианогруппу, SF5, атом галогена или, соответственно, незамещенный(ную) или замещенный(ную) алкил, алкоксил, алкилтиогруппу, алкилсульфинил, алкилсульфонил или алкилсульфонилоксигруппу;
R3 означает атом водорода, или атом галогена, или вместе с R2 означает незамещенную или замещенную алкилендиоксигруппу;
R4 означает атом водорода, цианогруппу, карбоксил, карбамоил, атом галогена или незамещенный, или замещенный алкил;
Q1 означает атом кислорода, атом серы или N-R5;
Q2 означает простую связь или атом кислорода, атом серы или N-R5;
R5 означает атом водорода, аминогруппу или, соответственно, незамещенный(ную) или замещенный(ную) алкил, алкоксил, алкиламиногруппу, диалкиламиногруппу, алкилиденаминогруппу, алкенил, алкенилоксигруппу, алкинил, циклоалкил, циклоалкиламиногруппу, циклоалкилалкил, арил, ариламиногруппу, арилалкил, гетероциклил или гетероциклилалкил;
R6 означает, соответственно, незамещенный или замещенный алкил, алкенил, циклоалкил, циклоалкилалкил, арил, арилалкил, гетероциклил или гетероциклилалкил;
Z1 означает атом азота или C-R4;
Z2 означает атом азота или C-R4;
Z3 означает атом азота или C-R4.
В определениях углеводородные цепи, как алкил, алкенил или алкинил, а также в сочетании с гетероатомами, как в алкиламиногруппе, соответственно, являются линейными или разветвленными. R3 предпочтительно находится в м- или п-положении в фенильном кольце.
Ниже указываются предпочтительные заместители, соответственно, предпочтительные области значений имеющихся в вышеприведенных и нижеприводимых формулах остатков:
R1 предпочтительно означает цианогруппу или одну из группировок -R5, -CQ1-Q2R5, -NH-CQ1-Q2R5 или -SO2R6;
R2 предпочтительно означает нитрогруппу, цианогруппу, SF5, атом галогена или, соответственно, незамещенный(ную) или замещенный(ную) цианогруппой, галогеном или алкоксилом с 1-4 атомами углерода алкил, алкоксил, алкилтиогруппу, алкилсульфинил, алкилсульфонил или алкилсульфонилоксигруппу, соответственно, с 1-5 атомами углерода;
R3 предпочтительно означает атом водорода, или атом галогена, или вместе с R2 означает незамещенную или замещенную галогеном алкилендиоксигруппу с 1-3 атомами углерода;
R4 предпочтительно означает атом водорода, цианогруппу, карбоксил, карбамоил, атом галогена или незамещенный или замещенный цианогруппой, галогеном или алкоксилом с 1-4 атомами углерода алкил с 1-5 атомами углерода;
Q1 предпочтительно означает атом кислорода или атом серы;
R5 предпочтительно означает атом водорода или аминогруппу; соответственно, незамещенный или замещенный цианогруппой, галогеном или алкоксилом с 1-4 атомами углерода алкил или алкоксил, соответственно, с 1-6 атомами углерода; алкиламиногруппу с 1-6 атомами углерода; диалкиламиногруппу, соответственно, с 1-6 атомами углерода в алкильных группах; алкилиденаминогруппу с количеством атомов углерода вплоть до шести; соответственно, незамещенный(ную) или замещенный(ную) цианогруппой или галогеном алкенил, алкенилоксигруппу или алкинил, соответственно, с 2-6 атомами углерода; соответственно, незамещенный(ную) или замещенный(ную) цианогруппой, галогеном или алкилом с 1-4 атомами углерода циклоалкил, циклоалкиламиногруппу или циклоалкилалкил, соответственно, с 3-6 атомами углерода в циклоалкильной группе и, при данных условиях, с 1-4 атомами углерода в алкильной части; соответственно, незамещенный(ную) или замещенный(ную) нитрогруппой, цианогруппой, фенилом, феноксигруппой, фенилтиогруппой, галогеном, алкилом с 1-4 атомами углерода, галогеналкилом с 1-4 атомами углерода, алкоксилом с 1-4 атомами углерода, галогеналкоксилом с 1-4 атомами углерода, алкилтиогруппой с 1-4 атомами углерода, галогеналкилтиогруппой с 1-4 атомами углерода, алкилсульфинилом с 1-4 атомами углерода, галогеналкилсульфинилом с 1-4 атомами углерода, алкилсульфонилом с 1-4 атомами углерода, галогеналкилсульфонилом с 1-4 атомами углерода или диалкиламино-сульфонилом с 1-4 атомами углерода в каждой алкильной части арил, ариламиногруппу или арилалкил, соответственно, с 6 или 10 атомами углерода в арильной группе и, при данных условиях, с 1-4 атомами углерода в алкильной части; или, соответственно, незамещенный или замещенный нитрогруппой, цианогруппой, фенилом, феноксигруппой, фенилтиогруппой, галогеном, алкилом с 1-4 атомами углерода, галогеналкилом с 1-4 атомами углерода, алкоксилом с 1-4 атомами углерода, галогеналкоксилом с 1-4 атомами углерода, алкилтиогруппой с 1-4 атомами углерода, галогеналкилтиогруппой с 1-4 атомами углерода, алкилсульфинилом с 1-4 атомами углерода, галогеналкилсульфинилом с 1-4 атомами углерода, алкилсульфонилом с 1-4 атомами углерода, галогеналкилсульфонилом с 1-4 атомами углерода или диалкиламиносульфонилом с 1-4 атомами углерода в каждой алкильной части моноциклический или бициклический гетероциклил или гетероциклилалкил, соответственно, с количеством атомов углерода вплоть до десяти и с количеством атомов азота вплоть до четырех и/или с одним или двумя атомами кислорода или серы в гетероциклильной группе и, при данных условиях, с 1-4 атомами углерода в алкильной части;
R6 предпочтительно означает незамещенный или замещенный галогеном алкил с 1-6 атомами углерода; незамещенный или замещенный галогеном алкенил с 2-6 атомами углерода; незамещенный или замещенный галогеном или алкилом с 1-4 атомами углерода циклоалкил или циклоалкилалкил, соответственно, с 3-6 атомами углерода в циклоалкильной группе и, при данных условиях, с 1-4 атомами углерода в алкильной части; соответственно, незамещенный или замещенный нитрогруппой, цианогруппой, галогеном, алкилом с 1-4 атомами углерода, галогеналкилом с 1-4 атомами углерода, алкоксилом с 1-4 атомами углерода, галогеналкоксилом с 1-4 атомами углерода, алкилтиогруппой с 1-4 атомами углерода, галогеналкилтиогруппой с 1-4 атомами углерода, алкилсульфинилом с 1-4 атомами углерода, галогеналкилсульфинилом с 1-4 атомами углерода, алкилсульфонилом с 1-4 атомами углерода, галогеналкилсульфонилом с 1-4 атомами углерода или диалкиламиносульфонилом с 1-4 атомами углерода в каждой алкильной части арил или арилалкил, соответственно, с 6 или 10 атомами углерода в арильной группе и, при данных условиях, с 1-4 атомами углерода в алкильной части; или, соответственно, незамещенный или замещенный нитрогруппой, цианогруппой, галогеном, алкилом с 1-4 атомами углерода, галогеналкилом с 1-4 атомами углерода, алкоксилом с 1-4 атомами углерода, галогеналкоксилом с 1-4 атомами углерода, алкилтиогруппой с 1-4 атомами углерода, галогеналкилтиогруппой с 1-4 атомами углерода, алкилсульфинилом с 1-4 атомами углерода, галогеналкилсульфинилом с 1-4 атомами углерода, алкилсульфонилом с 1-4 атомами углерода, галогеналкилсульфонилом с 1-4 атомами углерода или диалкиламиносульфонилом с 1-4 атомами углерода в каждой алкильной части моноциклический или бициклический гетероциклил или гетероциклилалкил, соответственно, с количеством атомов углерода вплоть до десяти и с количеством атомов азота вплоть до четырех и/или с одним или двумя атомами кислорода или серы в гетероциклильной группе и, при данных условиях, с 1-4 атомами углерода в алкильной части;
Z1 предпочтительно означает C-R4;
Z2 предпочтительно означает C-R4;
Z3 предпочтительно означает C-R4;
далее,
R2 особенно предпочтительно означает нитрогруппу, цианогруппу, SF5, атом фтора, хлора или брома, или, соответственно, незамещенный(ную) или замещенный(ную) цианогруппой, фтором, хлором, метоксигруппой или этоксигруппой метил, этил, н- или изопропил, метоксигруппу, этоксигруппу, н- или изопропоксигруппу, метилтиогруппу, этилтиогруппу, н- или изопропилтиогруппу, метилсульфинил, этилсульфинил, н- или изопропилсульфинил, метилсульфонил, этилсульфонил, н- или изопропилсульфонил, метилсульфонилоксигруппу, этилсульфонилоксигруппу, н- или изопропилсульфонилоксигруппу;
R3 особенно предпочтительно означает атом водорода, атом фтора, хлора или брома, или вместе с R2 означает, соответственно, незамещенную или замещенную фтором и/или хлором метилендиоксигруппу или этилендиоксигруппу;
R4 особенно предпочтительно означает атом водорода, цианогруппу, карбоксил, карбамоил, атом фтора, хлора, брома, или незамещенный или замещенный цианогруппой, фтором, хлором, метоксигруппой или этоксигруппой метил, этил, н- или изопропил;
Q1 особенно предпочтительно означает атом кислорода;
R5 особенно предпочтительно означает атом водорода или аминогруппу; соответственно, незамещенный(ную) или замещенный(ную) цианогруппой, фтором, хлором, метоксигруппой или этоксигруппой метил, этил, н- или изопропил, н-, изо-, втор- или трет-бутил, метиламиногруппу, этиламиногруппу, н- или изопропиламиногруппу, н-, изо-, втор- или трет-бутиламиногруппу; диметиламиногруппу или диэтиламиногруппу; пропилиденаминогруппу или бутилиденаминогруппу; соответственно, незамещенный или замещенный цианогруппой, фтором, хлором и/или бромом пропенил, бутенил, пропинил или бутинил; соответственно, незамещенный(ную) или замещенный(ную) цианогруппой, фтором, хлором, бромом, метилом, этилом, н- или изопропилом циклопропил, циклобутил, циклопентил, циклогексил, циклопропиламиногруппу, циклобутиламиногруппу, циклопентиламиногруппу, циклогексиламиногруппу, циклопропилметил, циклобутилметил, циклопентилметил или циклогексилметил; соответственно, незамещенный(ную) или замещенный(ную) нитрогруппой, цианогруппой, фенилом, феноксигруппой, фенилтиогруппой, фтором, хлором, бромом, метилом, этилом, н- или изопропилом, н-, изо-, втор- или трет-бутилом, дихлорметилом, дифторметилом, трихлорметилом, трифторметилом, хлордифторметилом, фтордихлорметилом, метоксигруппой, этоксигруппой, н- или изопропоксигруппой, дифторметоксигруппой, трифторметоксигруппой, метилтиогруппой, этилтиогруппой, н- или изопропилтиогруппой, дифторметилтиогруппой, трифторметилтиогруппой, метилсульфинилом, этил-сульфинилом, трифторметилсульфинилом, метилсульфонилом, этилсульфонилом, трифторметилсульфонилом или диметиламиносульфонилом фенил, нафтил, фениламиногруппу, бензил или фенилэтил; или, соответственно, незамещенный или замещенный цианогруппой, фенилом, феноксигруппой, фенилтиогруппой, фтором, хлором, бромом, метилом, этилом, н- или изопропилом, н-, изо-, втор- или трет-бутилом, дихлорметилом, дифторметилом, трихлорметилом, трифторметилом, хлордифторметилом, фтордихлорметилом, метоксигруппой, этоксигруппой, н- или изопропоксигруппой, дифторметоксигруппой, трифторметоксигруппой, метилтиогруплой, этилтиогруппой, н- или изопропилтиогруппой, дифторметилтиогруппой, трифторметилтиогруппой, метилсульфинилом, этилсульфинилом, трифторметилсульфинилом, метилсульфонилом, этилсульфонилом, трифторметилсульфонилом или диметиламиносульфонилом гетероциклил или гетероциклилалкил из ряда: фурил, тетрагидрофурил, бензофурил, тиенил, бензотиенил, пирролил, бензопирролил, пиразолил, бензопиразолил, оксазолил, бензоксазолил, изоксазолил, тиазолил, бензтиазолил, оксадиазолил, тиадиазолил, пиридинил, хинолинил, пиримидинил, фурилметил, тиенилметил, пирролилметил, пиразолилметил, оксазолилметил, тиазолилметил, пиридинилметил, пиримидинилметил;
R6 особенно предпочтительно означает, соответственно, незамещенный или замещенный фтором и/или хлором метил, этил, н- или изопропил, н-, изо-, втор- или трет-бутил; соответственно, незамещенный или замещенный фтором, хлором и/или бромом пропенил или бутенил; соответственно, незамещенный или замещенный фтором, хлором, бромом, метилом, этилом, н- или изопропилом циклопропил, циклобутил, циклопентил, циклогексил, циклопропилметил, циклобутилметил, циклопентилметил или циклогексилметил; соответственно, незамещенный или замещенный нитрогруппой, цианогруппой, фтором, хлором, бромом, метилом, этилом, н- или изопропилом, н-, изо-, втор- или трет-бутилом, дихлорметилом, дифторметилом, трихлорметилом, трифторметилом, хлордифторметилом, фтордихлорметилом, метоксигруппой, этоксигруппой, н- или изопропоксигруппой, дифторметоксигруппой, трифторметоксигруппой, метилтиогруппой, этилтиогруппой, н- или изопропилтиогруппой, дифторметилтиогруппой, трифторметилтиогруппой, метилсульфинилом, этилсульфинилом, трифторметилсульфинилом, метилсульфонилом, этилсульфонилом, трифторметилсульфонилом или диметиламиносульфонилом фенил или нафтил; или, соответственно, незамещенный или замещенный цианогруппой, фтором, хлором, бромом, метилом, этилом, н- или изопропилом, н-, изо-, втор- или трет-бутилом, дихлорметилом, дифторметилом, трихлорметилом, трифторметилом, хлордифторметилом, фтордихлорметилом, метоксигруппой, этоксигруппой, н- или изопропоксигруппой, дифторметоксигруппой, трифторметоксигруппой, метилтиогруппой, этилтиогруппой, н- или изопропилтиогруппой, дифторметилтиогруппой, трифторметилтиогруппой, метилсульфинилом, этилсульфинилом, трифторметилсульфинилом, метилсульфонилом, этилсульфонилом, трифторметилсульфонилом или диметиламиносульфонилом гетероциклил или гетероциклилалкил из ряда: фурил, бензофурил, тиенил, бензотиенил, пирролил, бензопирролил, пиразолил, бензопиразолил, оксазолил, бензоксазолил, изоксазолил, тиазолил, бензтиазолил, пиридинил, хинолинил, пиримидинил, фурилметил, тиенилметил, пирролилметил, пиразолилметил, оксазолилметил, тиазолилметил, пиридинилметил, пиримидинилметил;
Z1 особенно предпочтительно означает метиновую группу;
Z2 особенно предпочтительно означает метиновую группу;
Z3 особенно предпочтительно означает метиновую группу;
далее,
R2 в высшей степени предпочтительно означает цианогруппу, атом фтора, хлора или брома, или, соответственно, незамещенный(ную) или замещенный(ную) фтором, хлором, метоксигруппой или этоксигруппой метил, этил, метоксигруппу, этоксигруппу, метилтиогруппу, этилтиогруппу, метилсульфинил, этилсульфинил, метилсульфонил, этилсульфонил, метилсульфонилоксигруппу или этилсульфонилоксигруппу;
R4 в высшей степени предпочтительно означает атом водорода, цианогруппу, атом фтора, хлора, брома, или незамещенный или замещенный фтором, хлором, метоксигруппой или этоксигруппой метил или этил;
R5 в высшей степени предпочтительно означает атом водорода или аминогруппу; соответственно, незамещенный(ную) или замещенный(ную) цианогруппой, фтором, хлором, метоксигруппой или этоксигруппой метил, этил, н- или изопропил, метиламиногруппу, этиламиногруппу, н- или изопропиламиногруппу; диметиламиногруппу; соответственно, незамещенный или замещенный фтором, хлором и/или бромом пропенил, бутенил, пропинил или бутинил; соответственно, незамещенный(ную) или замещенный(ную) фтором, хлором, бромом, метилом или этилом циклопропил, циклопентил, циклогексил, циклопропиламиногруппу, циклопентиламиногруппу, циклогексиламиногруппу, циклопропилметил, циклопентилметил или циклогексилметил; или, соответственно, незамещенный(ную) или замещенный(ную) нитрогруппой, цианогруппой, фтором, хлором, бромом, метилом, этилом, н- или изопропилом, н-, изо-, втор- или трет-бутилом, трифторметилом, метоксигруппой, этоксигруппой, н- или изопропоксигруппой, дифторметоксигруппой, трифторметоксигруппой, метилтиогруппой, этилтиогруппой, н- или изопропилтиогруппой, дифторметилтиогруппой, трифторметилтиогруппой, метилсульфинилом, этилсульфинилом, трифторметилсульфинилом, метилсульфонилом, этилсульфонилом, трифторметилсульфонилом или диметиламиносульфонилом фенил, фениламиногруппу, бензил или фенилэтил;
R6 в высшей степени предпочтительно означает, соответственно, незамещенный или замещенный фтором и/или хлором метил, этил, н- или изопропил, н-, изо-, втор- или трет-бутил; соответственно, незамещенный или замещенный фтором, хлором, бромом, метилом или этилом циклопропил, циклопентил или циклогексил; или незамещенный, или замещенный нитрогруппой, цианогруппой, фтором, хлором, бромом, метилом, этилом, н- или изопропилом, н-, изо-, втор- или трет-бутилом, трифторметилом, метоксигруппой, этоксигруппой, н- или изопропоксигруппой, дифторметоксигруппой, трифторметоксигруппой, метилтиогруппой, этилтиогруппой, н- или изопропилтиогруппой, дифторметилтиогруппой, трифторметилтиогруппой, метилсульфинилом, этилсульфинилом, трифторметилсульфинилом, метилсульфонилом, этилсульфонилом, трифторметилсульфонилом или диметиламиносульфонилом фенил;
причем
R2 чаще всего предпочтительно означает трифторметил;
R4 чаще всего предпочтительно означает метил.
В высшей степени предпочтительную группу представляют собой те соединения формулы (I), в которой
R1 означает цианогруппу или одну из группировок -CQ1-Q2-R5 или -SO2-R6;
R2 означает трифторметил, дифторметоксигруппу или трифторметоксигруппу;
R3 означает атом водорода, фтора или хлора, или вместе с радикалом R2- в ортоположении - означает дифторметилендиоксигруппу или тетрафторэтилендиоксигруппу;
R4 означает атом водорода, фтора, хлора, брома или метил;
Q1 означает атом кислорода или атом серы;
Q2 означает простую связь или атом кислорода, атом серы или N-R5;
R5 означает атом водорода; соответственно, незамещенный или замещенный цианогруппой, фтором, хлором, метоксигруппой или этоксигруппой метил, этил, н- или изопропил; соответственно, незамещенный или замещенный фтором, хлором и/или бромом пропенил, бутенил, пропинил или бутинил; соответственно, незамещенный или замещенный фтором, хлором или метилом циклопропил, циклопентил, циклогексил, циклопропилметил, циклопентилметил или циклогексилметил; или, соответственно, незамещенный или замещенный нитрогруппой, цианогруппой, фтором, хлором, бромом, метилом, этилом, н- или изопропилом, н-, изо-, втор- или трет-бутилом, трифторметилом, метоксигруппой, этоксигруппой, н- или изопропоксигруппой, дифторметоксигруппой, трифторметоксигруппой, метилтиогруппой, этилтиогруппой, н- или изопропилтиогруппой, дифторметилтиогруппой, трифторметилтиогруппой, метилсульфинилом, этилсульфинилом, трифторметилсульфинилом, метилсульфонилом, этилсульфонилом, трифторметилсульфонилом или диметиламиносульфонилом фенил или бензил;
R6, соответственно, означает незамещенный или замещенный фтором и/или хлором метил, этил, н- или изопропил, н-, изо-, втор- или трет-бутил; соответственно, незамещенный или замещенный фтором, хлором или метилом циклопропил, циклопентил или циклогексил; или незамещенный или замещенный нитрогруппой, цианогруппой, фтором, хлором, бромом, метилом, этилом, н- или изопропилом, н-, изо-, втор- или трет-бутилом, трифторметилом, метоксигруппой, этоксигруппой, н- или изопропоксигруппой, дифторметоксигруппой, трифторметоксигруппой, метилтиогруппой, этилтиогруппой, н- или изопропилтиогруппой, дифторметилтиогруппой, трифторметилтиогруппой, метилсульфинилом, этилсульфинилом, трифторметилсульфинилом, метилсульфонилом, этилсульфонилом, трифторметилсульфонилом или диметиламиносульфонилом фенил;
Z1 означает метиновую группу;
Z2 означает метиновую группу; и
Z3 означает метиновую группу,
Согласно изобретению предпочтительными являются те соединения формулы (I), в которых имеется комбинация указанных выше как предпочтительные значений остатков.
Согласно изобретению особенно предпочтительными являются те соединения формулы (I), в которых имеется комбинация указанных выше как особенно предпочтительные значений остатков.
Согласно изобретению в высшей степени предпочтительными являются те соединения формулы (I), в которых имеется комбинация указанных выше как в высшей степени предпочтительные значений остатков.
Вышеуказанные общие или указанные в предпочтительных областях значения остатков относятся как к конечным продуктам формулы (I), так и также, соответственно, к необходимым в каждом случае для их получения исходным или промежуточным продуктам.
Эти значения остатков можно любым образом комбинировать друг с другом, следовательно, также между указанными предпочтительными областями.
Новые замещенные иминоазины общей формулы (I) обладают представляющими интерес биологическими свойствами. Они отличаются в особенности сильной гербицидной активностью.
Новые замещенные иминоазины общей формулы (I) получают тем, что
(а) иминоазины общей формулы (II):
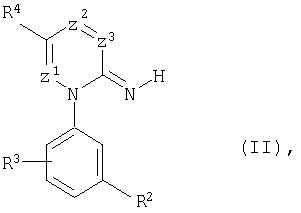
в которой
R2, R3, R4, Z1, Z2 и Z3 имеют вышеуказанные значения,
- или аддукты с кислотой иминоазинов общей формулы (II), как, например, гидрохлориды, -
вводят во взаимодействие с соединениями общей формулы (III):

в которой
R1 имеет вышеуказанное значение;
X1 означает атом галогена -SO2СН3, -O-CO-R5 или -O-SO2-R6; и
R5 и R6 имеют вышеуказанные значения;
или с изо(тио)цианатами общей формулы (IV):

в которой
Q1 и R5 имеют вышеуказанные значения,
в случае необходимости, в присутствии вспомогательного для реакции средства и, в случае необходимости, в присутствии разбавителя;
или тем, что
(б) азинтионы общей формулы (V):
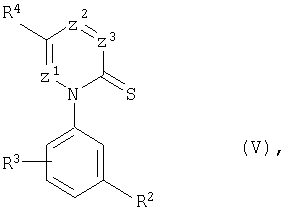
в которой
R2, R3, R4, Z1 Z2 и Z3 имеют вышеуказанные значения,
вводят во взаимодействие с соединениями общей формулы (VI):

в которой
R6 имеет вышеуказанное значение и
М означает эквивалент металла,
в случае необходимости, в присутствии одного или нескольких разбавителей;
или тем, что
(в) хлоразиниевые соединения общей формулы (VII):

в которой
R2, R3, R4, Z1, Z2 и Z3 имеют вышеуказанные значения, и
Y означает атом хлора, PCl4, POCl4 или PCl6,
вводят во взаимодействие с аминосоединениями общей формулы (VIII):

в которой
R1 имеет вышеуказанное значение,
в случае необходимости, в присутствии вспомогательного для реакции средства и, в случае необходимости, в присутствии разбавителя;
или тем, что
(г) иминоазины общей формулы (II):

в которой
R2, R3, R4, Z1, Z2 и Z3 имеют вышеуказанные значения,
- или аддукты с кислотой иминоазинов общей формулы (II), как, например, гидрохлориды,-
вводят во взаимодействие с азотной кислотой, в случае необходимости, в присутствии вспомогательного для реакции средства и/или разбавителя.
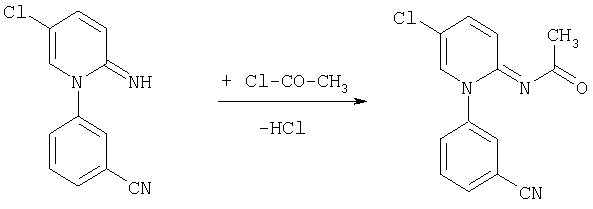
Если используют, например, 5-хлор-1-(3-цианофенил)-2(1Н)-пиридиний и ацетилхлорид в качестве исходных веществ, то протекание реакции в случае предлагаемого согласно изобретению способа (а) можно представить в виде следующей реакционной схемы:
Если используют, например, 1-(3-хлорфенил)-5-этил-2(1Н)-пиридинтион и натриевую соль амида N-хлорбензолсульфокислоты в качестве исходных веществ, то протекание реакции в случае предлагаемого согласно изобретению способа (б) можно представить в виде следующей реакционной схемы:

Если используют, например, 1-(3-бромфенил)-2-хлор-5-трифторметилпиридинийхлорид и диметилгидразин в качестве исходных веществ, то протекание реакции в случае предлагаемого согласно изобретению способа (в) можно представить в виде следующей реакционной схемы:

Если используют, например, 5-бром-1-(3-хлордифторметилфенил)-2(1Н)-пиридиний и азотную кислоту в качестве исходных веществ, то протекание реакции в случае предлагаемого согласно изобретению способа (г) можно представить в виде следующей реакционной схемы:

Используемые в случае предлагаемых согласно изобретению способов (а) и (г) для получения соединений общей формулы (I) в качестве исходных веществ иминоазины, в общем, отвечают формуле (II). В общей формуле (II) R2, R3, R4, Z1 Z2 и Z3 предпочтительно имеют те значения, которые уже были указаны выше в связи с описанием предлагаемых согласно изобретению соединений общей формулы (I) как предпочтительные, особенно предпочтительные или в высшей степени предпочтительные для R2, R3, R4, Z1, Z2 и Z3.
Исходные вещества общей формулы (II) еще неизвестны из литературы; в качестве новых веществ они являются также объектом настоящей заявки.
Новые иминоазины общей формулы (II) получают тем, что
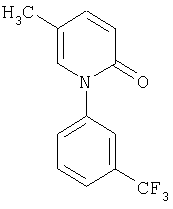
(α) азиноны общей формулы (IX):

в которой
R2, R3, R4, Z1, Z2 и Z3 имеют вышеуказанные значения,
на первой стадии вводят во взаимодействие с хлорирующими средствами, как, например, фосген, дифосген, оксалилхлорид, тионилхлорид, трихлорид фосфора, фосфорилхлорид или пентахлорид фосфора, в случае необходимости, в присутствии вспомогательных для реакции средств, как, например, N,N-диметилформамид, и, в случае необходимости, в присутствии разбавителей, как, например, 1,2-дихлорэтан, при температурах от 0 до 150°С (см. примеры получения),
и получаемые при этом хлоразиниевые соединения общей формулы (VII):
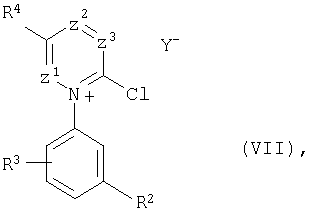
в которой
R2, R3, R4, Z1 Z2 и Z3 имеют вышеуказанные значения, и
Y означает атом хлора, PCl4, POCl4 или PCl6;
на второй стадии вводят во взаимодействие с аммиаком, в случае необходимости, в присутствии разбавителя, как, например, метанол, и, в случае необходимости, в присутствии акцептора кислоты, как, например, метила натрия, при температурах от 0 до 80°С (см. примеры получения);
или тем, что
(β) замещенные иминоазины общей формулы (Ia):
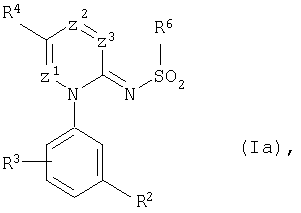
в которой
R2, R3, R4, Z1, Z2 и Z3 имеют вышеуказанные значения,
вводят во взаимодействие с сильной кислотой, как, например, серная кислота, которая, в случае необходимости, разбавлена водой, при температурах от 0 до 100°С (см. примеры получения).
Исходные вещества общей формулы (IX) отчасти известны и/или их можно получать само по себе известными способами (см. Chem. Pharm. Bull., 45. 719-721 (1997); заявки на патенты ФРГ 1900947, 2362958, 2555411; см. также примеры получения).
Исходные вещества общей формулы (IXa):

в которой
R2, R3 и R4 имеют вышеуказанные значения,
являются новыми соединениями согласно настоящему изобретению для получения соединений общей формулы (II).
В общей формуле (IXa) радикалы R2, R3 и R4 предпочтительно имеют те значения, которые уже были указаны выше в связи с описанием предлагаемых согласно изобретению соединений общей формулы (I) как предпочтительные, особенно предпочтительные или в высшей степени предпочтительные для R2, R3 и R4.
Исходные вещества общей формулы (IXa) еще неизвестны из литературы; в качестве новых веществ они являются также объектом настоящей заявки.
Новые соединения общей формулы (IXa) можно получать само по себе известными способами (см. Chem. Pharm. Bull., 45, 719-721 (1997); заявки на патенты ФРГ 1900947, 2362958,2555411; см. также примеры получения).
Соединения общей формулы (IX) также, как и соединения общей формулы (IXa), обладают представляющими интерес биологическими свойствами. В особенности они обладают сильным гербицидным действием.
Замещенные иминоазины общей формулы (Ia) представляют собой предлагаемые согласно изобретению новые соединения; их предпочтительно получат согласно предлагаемому в изобретении способу (б).
Используемые, далее, в случае предлагаемого согласно изобретению способа (а) в качестве исходных веществ для получения соединений общей формулы (I) соединения, в общем, отвечают формулам (III), соответственно, (IV). В общих формулах (III) и (IV) радикал R1 предпочтительно имеет то значение, которое уже было указано выше в связи с описанием предлагаемых согласно изобретению соединений общей формулы (I) как предпочтительное, особенно предпочтительное или в высшей степени предпочтительное для радикала R1; X1 означает предпочтительно атом фтора, хлора, брома или группировку -O-CO-R1, в особенности атом хлора или брома; Q1 предпочтительно означает атом кислорода или атом серы.
Исходные вещества общих формул (III) и (IV) являются известными органическими химическими реагентами для синтеза.
Используемые в случае предлагаемого согласно изобретению способа (б) в качестве исходных веществ для получения соединений общей формулы (I) азинтионы, в общем, отвечают формуле (V). В общей формуле (V) радикалы R2, R3, R4, Z1, Z2 и Z3 предпочтительно имеют те значения, которые уже указаны выше в связи с описанием предлагаемых согласно изобретению соединений общей формулы (I) как предпочтительные, особенно предпочтительные или в высшей степени предпочтительные для R2, R3, R4, Z1, Z2 и Z3.
Исходные вещества общей формулы (V) еще неизвестны из литературы; в качестве новых веществ они являются также объектом настоящей заявки.
Новые азинтионы общей формулы (V) получают тем, что азиноны общей формулы (IX):

в которой
R2, R3, R4, Z1, Z2 и Z3 имеют вышеуказанные значения,
вводят во взаимодействие с реагентом для введения серы, как, например, пентасульфид фосфора (Р2S5, соответственно, P4S10), в случае необходимости, в присутствии вспомогательного для реакции средства, как, например, пиридин, при температурах от 10 до 150°С (см. примеры получения).
Исходные вещества общей формулы (IX) известны и/или их можно получать само по себе известными способами (см. Chem. Pharm. Bull., 45, 719-721 (1997); заявки на патенты ФРГ 1900947, 2362958, 2555411; см. также примеры получения).
Азиноны общей формулы (IX) получают тем, что азиноны общей формулы (X):

в которой
R4, Z1, Z2 и Z3 имеют вышеуказанные значения, вводят во взаимодействие с галогенаренами общей формулы (XI):

в которой
R2 и R3 имеют вышеуказанные значения и
X2 означает атом фтора, хлора, брома или иода,
в случае необходимости, в присутствии катализатора, как, например, иодид одновалентной меди, в случае необходимости, в присутствии акцептора кислоты, как, например, карбонат калия, и, в случае необходимости, в присутствии разбавителя, как, например, N,N-диметилформамид, при температурах от 20 до 200°С (см. примеры получения).
Используемые в случае предлагаемого согласно изобретению способа (в) в качестве исходных веществ для получения соединений общей формулы (I) хлоразиниевые соединения, в общем, отвечают формуле (VII). В общей формуле (VII) радикалы R2, R3, R4, Z1, Z2 и Z3 предпочтительно имеют те значения, которые уже указаны выше в связи с описанием предлагаемых согласно изобретению соединений общей формулы (I) как предпочтительные, особенно предпочтительные или в высшей степени предпочтительные для R2, R3, R4, Z1, Z2 и Z3.
Исходные вещества общей формулы (VII) еще неизвестны из литературы; в качестве новых веществ они являются также объектом настоящей заявки.
Новые хлоразиниевые соединения общей формулы (VII) получают тем, что азиноны общей формулы (IX):

в которой
R2, R3, R4, Z1, Z2 и Z3 имеют вышеуказанные значения,
вводят во взаимодействие с хлорирующими средствами, как, например, фосген, дифосген, оксалилхлорид, тионилхлорид, трихлорид фосфора, фосфорилхлорид или пентахлорид фосфора, в случае необходимости, в присутствии вспомогательных для реакции средств, как, например, N,N-диметилформамид, и, в случае необходимости, в присутствии разбавителей, как, например, 1,2-дихлорэтан, при температурах от 0 до 150°С (см. примеры получения).
Используемые, далее, в случае предлагаемого согласно изобретению способа (в) в качестве исходных веществ для получения соединений общей формулы (I) аминосоединения, в общем, отвечают формуле (VIII). В общей формуле (VIII) радикал R1 предпочтительно имеет то значение, которое уже указано выше в связи с описанием предлагаемых согласно изобретению соединений общей формулы (I) как предпочтительное, особенно предпочтительное или в высшей степени предпочтительное для радикала R1.
Исходные вещества общей формулы (VIII) являются известными химическими реагентами для синтеза.
В качестве вспомогательных для реакции средств в случае предлагаемых согласно изобретению способов (а) и (в) используют, в общем, обычные неорганические или органические основания или акцепторы кислоты. К ним предпочтительно относятся ацетата, амиды, карбонаты, гидрокарбонаты, гидриды, гидроксиды или алкоголяты щелочных или щелочноземельных металлов, как, например, ацетат натрия, калия или кальция; амид лития, натрия, калия или кальция; карбонат натрия, калия или кальция; гидрокарбонат натрия, калия или кальция; гидрид лития, натрия, калия или кальция; гидроксид лития, натрия, калия или кальция; метилат, этилат, н- или изопропилат, н-, изо-, втор- или трет-бутилат натрия или калия; далее, также основные органические азотсодержащие соединения, как, например, триметиламин, триэтиламин, трипропиламин, трибутиламин, этилдиизопропиламин, N,N-диметилциклогексиламин, дициклогексиламин, этилдициклогексиламин, N,N-диметиланилин, N,N-диметилбензиламин, пиридин, 2-метилпиридин, 3-метилпиридин, 4-метилпиридин, 2,4-диметилпиридин, 2,6-диметилпиридин, 3,4-диметилпиридин и 3,5-диметилпиридин, 5-этил-2-метилпиридин, 4-диметиламинопиридин, N-метилпиперидин, 1,4-диазабицикло[2,0,0]октан, 1,5-диазабицикло[4,0,0]нон-5-ен или 1,8-диазабицикло[5,0,0]ундец-7-ен.
В качестве других вспомогательных для реакции средств в случае предлагаемых согласно изобретению способов (а) и (в) используют также межфазные катализаторы. В качестве примеров таких катализаторов следует назвать:
тетрабутиламмонийбромид, тетрабутиламмонийхлорид, тетраоктиламмонийхлорид, тетрабутиламмонийгидросульфат, метилтриоктиламмонийхлорид, гексадецилтриметиламмонийхлорид, гексадецилтриметиламмонийбромид, бензилтриметиламмонийхлорид, бензилтриэтиламмонийхлорид, бензилтриметиламмонийгидроксид, бензилтриэтиламмонийгидроксид, бензилтрибутиламмонийхлорид, бензилтрибутиламмонийбромид, тетрабутилфосфонийбромид, тетрабутилфосфонийхлорид, трибутилгексадецилфосфонийбромид, бутилтрифенилфосфонийхлорид, этилтриоктилфосфонийбромид, тетрафенилфосфонийбромид.
В качестве вспомогательных для реакции средств и/или разбавителей в случае предлагаемого согласно изобретению способа (г) используют, в общем, применяемые при реакциях нитрования вещества. К ним предпочтительно относятся серная кислота, уксусная кислота и уксусный ангидрид.
Предлагаемые согласно изобретению способы (а), (б) и (в) получения соединений общей формулы (I) предпочтительно осуществляют при использовании одного или нескольких разбавителей. В качестве разбавителей для осуществления предлагаемых согласно изобретению способов (а), (б) и (в) используют, наряду с водой, прежде всего инертные органические растворители. К ним в особенности относятся алифатические, алициклические или ароматические, в случае необходимости, галогенированные углеводороды, как, например, бензин, бензол, толуол, ксилол, хлорбензол, дихлорбензол, петролейный эфир, гексан, циклогексан, дихлорметан, хлороформ, тетрахлоруглерод; простые эфиры, как диэтиловый эфир, диизопропиловый эфир, диоксан, тетрагидрофуран или этиленгликольдиметиловый или диэтиловый эфир; кетоны, как ацетон, бутанон или метилизобутилкетон; нитрилы, как ацетонитрил, пропионитрил или бутиронитрил; амиды, как N,N-диметилформамид, N,N-диметилацетамид, N-метилформанилид, N-метилпирролидон или триамид гексаметилфосфорной кислоты; сложные эфиры, как метилацетат или этилацетат; сульфоксиды, как диметилсульфоксид; спирты, как метанол, этанол, н- или изопропанол, этиленгликольмонометиловый эфир, этиленгликольмоноэтиловый эфир, диэтиленгликольмонометиловый эфир, диэтиленгликольмоноэтиловый эфир, их смеси с водой или чистая вода.
При осуществлении предлагаемых согласно изобретению способов (а), (б), (в) и (г) температуры реакции могут изменяться в широких пределах. В общем, работают при температурах от -30 до 150°С, предпочтительно от -10 до 120°С.
Предлагаемые согласно изобретению способы осуществляют, в общем, при нормальном давлении. Однако, предлагаемые согласно изобретению способы также можно осуществлять при повышенном или пониженном давлении, в общем, от 0,1 до 10 бар.
Для осуществления предлагаемых согласно изобретению способов исходные вещества используют, в общем, приблизительно в эквимолярных количествах. Однако, компоненты также можно использовать в большем избытке. Взаимодействие осуществляют, в общем, в пригодном разбавителе, в случае необходимости, в присутствии вспомогательного для реакции средства и реакционную смесь перемешивают, в общем, в течение нескольких часов при необходимой температуре. Обработку осуществляют обычными способами (см. примеры получения).
Предлагаемые согласно изобретению биологически активные вещества можно применять в качестве дефолиантов, десикантов, средств для предуборочного уничтожения ботвы и в особенности в качестве средств уничтожения сорняков. Под сорняком в самом широком смысле нужно понимать все растения, которые вырастают в местах, где они нежелательны. Действуют ли предлагаемые согласно изобретению вещества в качестве гербицидов общего действия или селективных гербицидов, зависит по существу от используемого количества.
Предлагаемые согласно изобретению биологически активные вещества можно применять, например, в случае следующих растений:
Двудольные сорняки семейств: Abutilon, Amaranthus, Ambrosia, Anoda, Anthemis, Aphanes, Atriplex, Bellis, Bidens, Capsella, Carduus, Cassia, Centaurea, Chenopodium, Cirsium, Convolvulus, Datura, Desmodium. Emex, Erysimum, Euphorbia, Galeopsis, Galinsoga, Galium, Hibiscus, Ipomoea, Kochia, Lamium, Lepidium, Lindernia, Matricaria, Mentha, Mercurialis, Mullugo, Myosotis, Papaver, Phaibitis, Plantago, Polygonum, Portulaca, Ranunculus, Raphamis. Rorippa, Rotala, Rumex, Salsola, Senecio, Sesbania, Sida, Sinapis, Solanum, Sonchus, Sphenoclea, Stellaria, Taraxacum, Thlaspi, Trifolium, Urtica, Veronica, Viola, Xanthium.
Двудольные культуры семейств: Arachis, Beta, Brassica, Cucumis, Cucurbita, Helianthus, Daucus, Glycine, Gossypium, Ipomoea, Lactuca, Linum, Lycopersicon, Nicotiana, Phaseolus, Pisum, Solanum, Vicia.
Однодольные сорняки семейств: Aegilops, Agropyron, Agrostis, Alopecurus, Apera, Avena, Brachiaria, Bromus, Cenchrus, Commelma, Cynodon, Cyperus, Dactyloctenium, Digitaria, Echinochloa, Eleocharis, Eleusine, Eragrostis, Eriochloa, Festuca, Fimbristylis, Heteranthera, Imperata, Ischaemum, Leptochloa, Lolium, Monochoria, Panicum, Paspalum, Phalaris, Phleum, Poa, Rottboellia, Sagittaria, Scirpus, Setaria, Sorghum.
Однодольные культуры семейств: Allium, Ananas, Asparagus, Avena, Hordeum, Oryza, Panicum, Saccharum, Secale, Sorghum, Triticale, Triticum, Zea.
Применение биологически активных веществ согласно изобретению, однако, никоим образом не ограничивается этими семействами, а равным образом распространяется также на другие растения.
В зависимости от концентрации биологически активные вещества согласно изобретению пригодны для общей борьбы с сорняками, например, на промышленных сооружениях, на рельсовых путях, на дорогах и на площадях, заросших и не заросших деревьями. Биологически активные вещества согласно изобретению также могут быть использованы для борьбы с сорняками в многолетних культурах, например, в лесах, в насаждениях декоративных древесных пород, плодово-ягодных насаждениях, виноградниках, насаждениях цитрусовых культур, орехов, бананов, на кофейных плантациях, чайных плантациях, насаждениях каучуковых деревьев, масличных пальм, деревьев-какао, ягодных насаждениях и хмельниках, на декоративных газонах и спортивных площадках, сенокосно-пастбищных угодьях, а также для селективной борьбы с сорняками в однолетних культурах.
Предлагаемые согласно изобретению соединения формулы (I), а также соединения формул (IX) и (IXa) обладают сильной гербицидной активностью и широким спектром действия в случае применения в почве и на надземных частях растений. В известной мере они пригодны также для селективной борьбы с однодольными и двудольными сорняками в однодольных и двудольных культурах как по довсходовому способу, так и также по послевсходовому способу.
Предлагаемые согласно изобретению биологически активные вещества в определенных концентрациях, соответственно, определенных нормах расхода можно применять также для борьбы с вредными животными и грибковыми или бактериальными болезнями растений. В случае необходимости их также можно использовать в качестве промежуточных продуктов или форпродуктов для синтеза других биологически активных веществ.
Согласно изобретению можно обрабатывать все растения или части растений. Под растениями при этом понимают все растения и популяции растений как желательные и нежелательные дикорастущие растения или культурные растения (включая, естественно, имеющиеся культурные растения). Культурными растениями могут быть растения, которые можно получать обычными методами культивирования и оптимизации, или биотехнологическими и генно-инженерными методами, или комбинациями этих методов, включая трансгенные растения и включая сорта растений, защищаемые или незащищаемые законом об охране новых сортов растений. Под частями растений нужно понимать все надземные и подземные части и органы растений, как побег, лист, цветок и корень, причем нужно назвать, например, листья, иглы, стебли, стволы, цветы, плодовые тела, плоды и семена, а также корни, клубни и ризомы. К частям растений относятся также собранный урожай, а также вегетативный и генеративный материал для размножения, например черенки, клубни, ризомы, отводки и семена.
Предлагаемую согласно изобретению обработку растений и частей растений с помощью биологически активных веществ осуществляют непосредственно или путем воздействия на среду их произрастания или закрытое хранилище согласно обычным методам обработки, например, путем погружения, мелкокапельного опрыскивания, испарения, создания искусственного тумана, разбрасывания, намазывания, и, далее, в случае материала для размножения, в особенности в случае семян, путем однослойного или многослойного покрытия.
Биологически активные вещества можно переводить в обычные препаративные формы, как растворы, эмульсии, смачивающиеся порошки, суспензии, дусты, пылевидные препараты, пасты, растворимые порошки, грануляты, суспензионно-эмульсионные концентраты, импрегнированные биологически активными веществами природные и синтетические вещества, а также сверхтонкие капсулирования в полимерных веществах.
Эти препаративные формы получают известным образом, например, путем смешения биологически активных веществ с нейтральными наполнителями, следовательно, с жидкими растворителями и/или твердыми носителями, в случае необходимости, при использовании поверхностно-активных веществ, следовательно, эмульгаторов, и/или диспергаторов, и/или пенообразующих веществ.
В случае использования воды в качестве нейтрального наполнителя можно применять также, например, органические растворители в качестве вспомогательных растворителей. В качестве жидких растворителей по существу используют ароматические углеводороды, как ксилол, толуол или алкилнафталины, хлорированные ароматические углеводороды и хлорированные алифатические углеводороды, как хлорбензолы, хлорэтилены или дихлорметан, алифатические углеводороды, как циклогексан или парафины, например, нефтяные фракции, минеральные и растительные масла, спирты, как бутанол или гликоль, а также их простые и сложные эфиры, кетоны, как ацетон, метилэтилкетон, метилизобутилкетон или циклогексанон, сильно полярные растворители, как диметилформамид и диметилсульфоксид, а также воду.
В качестве твердых носителей используют, например, аммониевые соли и природную каменную муку, как каолины, глины, тальк, мел, кварц, аттапульгит, монтмориллонит или диатомовые земли, и синтетическую каменную муку, как высокодисперсная кремневая кислота, оксид алюминия и силикаты; в качестве твердых носителей для гранулятов используют, например, измельченные и фракционированные горные породы, как кальцит, мрамор, пемза, сепиолит, доломит, а также синтетические грануляты из неорганической и органической муки, а также грануляты из органического материала, как опилки, скорлупа кокосовых орехов, кукурузные початки и стебли табачных растений; в качестве эмульгаторов и/или пенообразующих веществ используют, например, неионные и анионные эмульгаторы, как полиоксиэтиленовые эфиры жирных кислот, простые полиоксиэтиленовые эфиры жирных спиртов, например, алкиларилполигликолевые эфиры, алкилсульфонаты, алкилсульфаты, арилсульфонаты, а также белковые гидролизаты; в качестве диспергаторов используют, например, лигнинсульфитные щелоки и метилцеллюлозу.
В препаративных формах можно использовать улучшающие адгезию средства, как карбоксиметилцеллюлоза, природные и синтетические порошкообразные, гранулированные или латексообразные полимеры, как гуммиарабик, поливиниловый спирт, поливинилацетат, а также природные фосфолипиды, как кефалины и лецитины, и синтетические фосфолипиды. Другими добавками могут быть минеральные и растительные масла.
Можно использовать красители, как неорганические пигменты, например, оксид железа, диоксид титана, ферроциановый синий, и органические красители, как ализариновые, азо- и металлфталоцианиновые красители, и микроэлементы, как соли железа, марганца, бора, меди, кобальта, молибдена и цинка.
Препаративные формы содержат, в общем, 0,1-95 масс.%, предпочтительно 0,5-90 масс.%, биологически активного вещества.
Предлагаемые согласно изобретению биологически активные вещества могут найти применение в качестве таковых или в их препаративных формах также в смеси с известными гербицидами и/или с веществами, которые повышают совместимость с культурными растениями ("антидоты"), для борьбы с сорняками, причем возможны готовые препаративные формы или резервуарные смеси. Следовательно, также возможны смеси со средствами борьбы с сорняками, которые содержат один или несколько известных гербицидов и антидот.
Для смесей используют известные гербициды, например, следующие:
ацетохлор, ацифлуорфен(-натрий), аклонифен, алахлор, аллоксидим(-натрий), аметрин, амикарбазон, амидохлор, амидосульфурон, анилофос, асулам, атразин, азафенидин, азимсульфурон, бефлубетамид, беназолин(-этил), бенфурезат, бенсульфурон(-метил), бентазон, бензфендизон, бензобициклон, бензофенап, бензоилпроп(-этил), биалафос, бифенокс, биспирибак(-натрий), бромобутид, бромофеноксим, бромоксинил, бутахлор, бутафенацил(-аллил), бутроксидим, бутилат, кафенстрол, калоксидим, карбетамид, карфентразон(-этил), хлометоксифен, хлорамбен, хлоридазон, хлоримурон(-этил), хлорнитрофен, хлорсульфурон, хлортолурон, цинидон(-этил), цинметилин, циносульфурон, клефоксидим, клетодим, клодинафоп(-пропаргил), кломазон, кломепроп, клопиралид, клопирасульфурон(-метил), клорансулам(-метил), кумилурон, цианазин, цибутрин, циклоат, циклосульфамурон, циклоксидим, цигалофоп(-бутил), 2,4-D, 2,4-DB, десмедифам, диаллат, дикамба, дихлорпроп(-Р), диклофоп(-метил), диклосулам, диэтатил(-этил), дифензокват, дифлуфеникан, дифлуфензопир, димефурон, димепиперат, диметахлор, диметаметрин, диметенамид, димексифлам, динитрамин, дифенамид, дикват, дитиопир, диурон, димрон, эпроподан, ЕРТС, эспрокарб, эталфлуралин, этаметсульфурон(-метил), этофумезат, этоксифен, этоксисульфурон, этобензанид, феноксапроп(-Р-этил), фентразамид, флампроп(-изопропил,-изопропил-L,-метил), флазасульфурон, флорасулам, флуазифоп(-Р-бутил), флуазолат, флукарбазон(-натрий), флуфенацет, флуметсулам, флумиклорак(-пентил), флумиоксазин, флумипропин, флуметсулам, флуометурон, флуорохлоридон, флуорогликофен(-этил), флупоксам, флупропацил, флупирсульфурон(-метил,-натрий), флуренол(-бутил), флуридон, флуроксипир(-бутоксипропил,-метил), флурпримидол, флуртамон, флутиацет(-метил), флутиамид, фомесафен, форамсульфурон, глуфозинат(-аммоний), глифозат(-изопропиламмоний), галосафен, галоксифоп(-этоксиэтил,-Р-метил), гексазинон, имазаметабенз(-метил), имазаметапир, имазамокс, имазапик, имазапир, имазаквин, имазетапир, имазосульфурон, иодосульфурон(-метил,-натрий), иоксинил, изопропалин, изопротурон, изоурон, изоксабен, изоксахлортол, изоксафлутол, изоксапирифоп, лактофен, ленацил, линурон, МСРА, мекопроп, мефенацет, мезотрион, метамитрон, метазахлор, метабензтиазурон, метобензурон, метобромурон, (альфа-)метолахлор, метосулам, метоксурон, метрибузин, метсульфурон(-метил), молинат, монолинурон, напроанилид, напропамид, небурон, никосульфурон, норфлуразон, орбенкарб, оризалин, оксадиаргил, оксадиазон, оксасульфурон, оксацикломефон, оксифлуорфен, паракват, пеларгоновая кислота, пендиметалин, пендралин, пентоксазон, фенмедифам, пиколинафен, пиперофос, претилахлор, примисульфурон(-метил), профлуразол, прометрин, пропахлор, пропанил, пропаквизафоп, пропизохлор, пропоксикарбазон(-натрий), пропизамид, просульфокарб, просульфурон, пирафлуфен(-этил), пиразогил, пиразолат, пиразосульфурон(-этил), пиразоксифен, пирибензоксим, пирибутикарб, пиридат, пиридатол, пирифталид, пириминобак(-метил), пиритиобак(-натрий), квинхлорак, квинмерак, квинокламин, квизалофоп(-Р-этил,-Р-тефурил), римсульфурон, сетоксидим, симазин, симетрин, сулькотрион, сульфентразон, сульфометурон(-метил), сульфозат, сульфосульфурон, тебутам, тебутиурон, тепралоксидим, тербутилазин, тербутрин, тенилхлор, тиафлуамид, тиазопир, тидиазимин, тифенсульфурон(-метил), тиобенкарб, тиокарбазил, тралкоксидим, триаллат, триасульфурон, трибенурон(-метил), триклопир, тридифан, трифлуралин, трифлоксисульфурон, трифлусульфурон(-метил), тритосульфурон.
Также возможна смесь с другими известными биологически активными веществами, как фунгициды, инсектициды, акарициды, нематициды, вещества для защиты от выклевывания птицами, вещества для питания растений и средства для улучшения структуры почвы.
Биологически активные вещества можно применять индивидуально, в виде их препаративных форм или приготовленных из них путем дальнейшего разбавления форм применения как готовые к употреблению растворы, суспензии, эмульсии, порошки, пасты и грануляты. Применение осуществляют обычным образом, например путем поливки, опрыскивания, мелкокапельного опрыскивания, разбрасывания.
Предлагаемые согласно изобретению биологически активные вещества можно наносить как до, так и также после появления всходов растений. Их можно также вносить перед посевом в почву.
Используемое количество биологически активного вещества может колебаться в широких пределах. Оно зависит по существу от рода желательного эффекта. В общем, нормы расхода составляют от 1 г до 10 кг, предпочтительно от 5 г до 5 кг, биологически активного вещества на гектар поверхности почвы.
Получение и применение предлагаемых согласно изобретению биологически активных веществ следует из нижеприводимых примеров.
Примеры получения
Пример 1

Смесь из 2,3 г (10 ммоль) 5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридиния, 2,1 г (10 ммоль) ангидрида трифторуксусной кислоты, 1,0 г (10 ммоль) триэтиламина и 50 мл этилацетата перемешивают в течение 60 минут при комнатной температуре (примерно 20°С). Затем реакционную смесь промывают водой, сушат над сульфатом натрия и фильтруют. Фильтрат концентрируют в вакууме водоструйного насоса, остаток настаивают с диизопропиловым эфиром и выпавший в осадок кристаллический продукт выделяют путем отфильтровывания под вакуумом.
Получают 0,5 г (14% от теоретически рассчитанного количества) 2,2,2-трихлор-N-[5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридинилиден]ацетамида с температурой плавления 115°С.
Пример 2
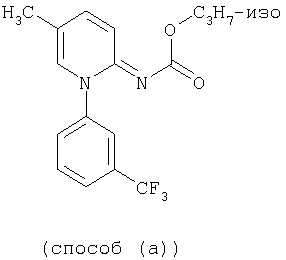
Смесь из 1,1 г (4 ммоль) 5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридиния, 5 мл (5 ммоль) изопропилового эфира хлормуравьиной кислоты, 0,5 г (5 ммоль) триэтиламина и 50 мл этилацетата перемешивают в течение 60 минут при комнатной температуре (примерно 20°С). Затем реакционную смесь промывают водой, водную фазу дополнительно экстрагируют дихлорметаном, объединенные органические фазы сушат над сульфатом натрия и фильтруют. Из фильтрата тщательно отгоняют растворители при пониженном давлении.
Получают 0,6 г (46% от теоретически рассчитанного количества) эфира N-[5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридинилиден]-O-метилкарбаминовой кислоты в виде аморфного остатка.
log P=1,59 (в отношении определения значений log P см. с.57).
Пример 3

Смесь из 1,1 г (4 ммоль) 5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридиния, 0,6 г (5 ммоль) бромциана, 0,5 г (5 ммоль) триэтиламина и 50 мл этилацетата перемешивают в течение 30 минут при комнатной температуре (примерно 20°С). Затем реакционную смесь промывают водой, водную фазу дополнительно экстрагируют дихлорметаном, объединенные органические фазы сушат над сульфатом натрия и фильтруют. Из фильтрата тщательно отгоняют растворители при пониженном давлении.
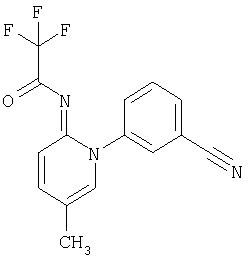
Получают 0,35 г (32% от теоретически рассчитанного количества) 5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридинилиденцианамида с температурой плавления 165°С.
Пример 4

Смесь из 2,6 г (10 ммоль) 5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридиния, 0,6 г (10 ммоль) метилизоцианата и 100 мл ацетонитрила выдерживают в течение двух часов при комнатной температуре (примерно 20°С). Затем концентрируют в вакууме водоструйного насоса, остаток настаивают с диизопропиловым эфиром и выпавший в осадок кристаллический продукт выделяют путем отфильтровывания под вакуумом.
Получают 2,1 г (68% от теоретически рассчитанного количества) N-метил-N'-[5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридинилиден]мочевины с температурой плавления 114°С.
Пример 5
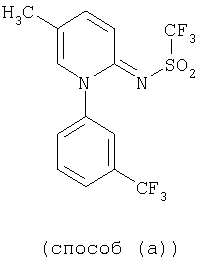
2,9 г (10 ммоль) 5-Метил-1-(3-трифторметилфенил)-2(1Н)-пиридинийгидрохлорида, 3,1 г (30 ммоль) триэтиламина и 100 мл ацетонитрила, при комнатной температуре (примерно 20°С) и при перемешивании, по каплям смешивают с 2,9 г (10 ммоль) ангидрида трифторметансульфокислоты. Реакционную смесь перемешивают в течение 60 минут при комнатной температуре и затем концентрируют в вакууме водоструйного насоса. Полученный в виде остатка сырой продукт очищают путем колоночной хроматографии (силикагель; смесь этилацетата и гексана в соотношении 9:1).
Получают 0,40 г (10% от теоретически рассчитанного количества) амида N-[5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридинилиден]трифторметансульфокислоты с температурой плавления 206°С.
Пример 6
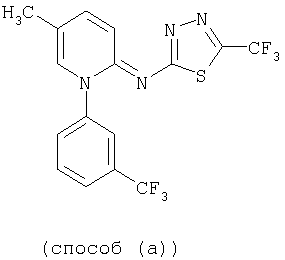
Смесь из 2,9 г (10 ммоль) 5-Метил-1-(3-трифторметилфенил)-2(1Н)-пиридиний-гидрохлорида, 2,3 г (10 ммоль) 2-метилсульфонил-5-трифторметил-1,3,4-тиадиазола, 4,2 г (30 ммоль) карбоната калия и 30 мл диметилсульфоксида перемешивают в течение 60 минут при температуре 100°С и после охлаждения выливают примерно в равный объем дихлорметана. После промывки водой и насыщенным водным раствором хлорида натрия органическую фазу сушат над сульфатом натрия и фильтруют. Фильтрат концентрируют в вакууме водоструйного насоса, остаток настаивают с диэтиловым эфиром и выпавший в осадок кристаллический продукт выделяют путем отфильтровывания под вакуумом.
Получают 2,3 г (57% от теоретически рассчитанного количества) N-(5-трифторметил-1,3,4-тиадиазол-2-ил)-5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридиния с температурой плавления 179°С.
Пример 7

2,7 г (10 ммоль) 5-Метил-1-(3-трифторметилфенил)-2(1Н)-пиридинтиона вводят в 50 мл хлороформа и, при комнатной температуре (примерно 20°С) и при перемешивании, по каплям смешивают с раствором 2,9 г (10 ммоль) гидрата натриевой соли амида N-хлор-п-толуолсульфокислоты (хлорамин-Т-гадрат) в 50 мл этанола. Реакционную смесь перемешивают в течение 15 часов при комнатной температуре, затем концентрируют в вакууме водоструйного насоса, остаток обрабатывают хлороформом, полученный раствор промывают водой и затем насыщенным водным раствором гидрокарбоната натрия, сушат над сульфатом натрия и фильтруют. Фильтрат концентрируют в вакууме водоструйного насоса и остаток выдерживают в течение 15 минут в высоком вакууме при температуре 180°С. После охлаждения и настаивания с диизопропиловым эфиром выпавший в осадок кристаллический продукт выделяют путем отфильтровывания под вакуумом.
Получают 1,8 г (49% от теоретически рассчитанного количества) 4-метил-N-[5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридинилиден] бензолсульфонамида с температурой плавления 174°С.
Пример 8
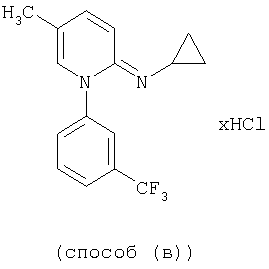
Смесь из 1,6 г (5 ммоль) 2-хлор-5-метил-1-(3-трифторметилфенил)пиридинийхлорида, 0,9 г (15 ммоль) циклопропиламина и 50 мл метанола выдерживают в течение 15 часов при комнатной температуре (примерно 20°С) и затем концентрируют в вакууме водоструйного насоса. Остаток обрабатывают дихлорметаном, полученный раствор промывают водой, сушат над сульфатом натрия и фильтруют. Фильтрат концентрируют в вакууме водоструйного насоса, остаток обрабатывают метанолом и соляной кислотой и летучие компоненты тщательно отгоняют при пониженном давлении. Полученный в виде остатка сырой продукт очищают путем колоночной хроматографии (силикагель; смесь этилацетата и гексана в соотношении 5:1).
Получают 1,5 г (91% от теоретически рассчитанного количества) 5-циклопропил-5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридиния в виде маслянистого продукта.
log P=1,51 (в отношении определения значений log P см. с.57).
Аналогично методикам примеров 1-8, а также соответственно общему описанию предлагаемых согласно изобретению способов получения можно также получать, например, указанные в нижеприводимой таблице 1 соединения общей формулы (I).


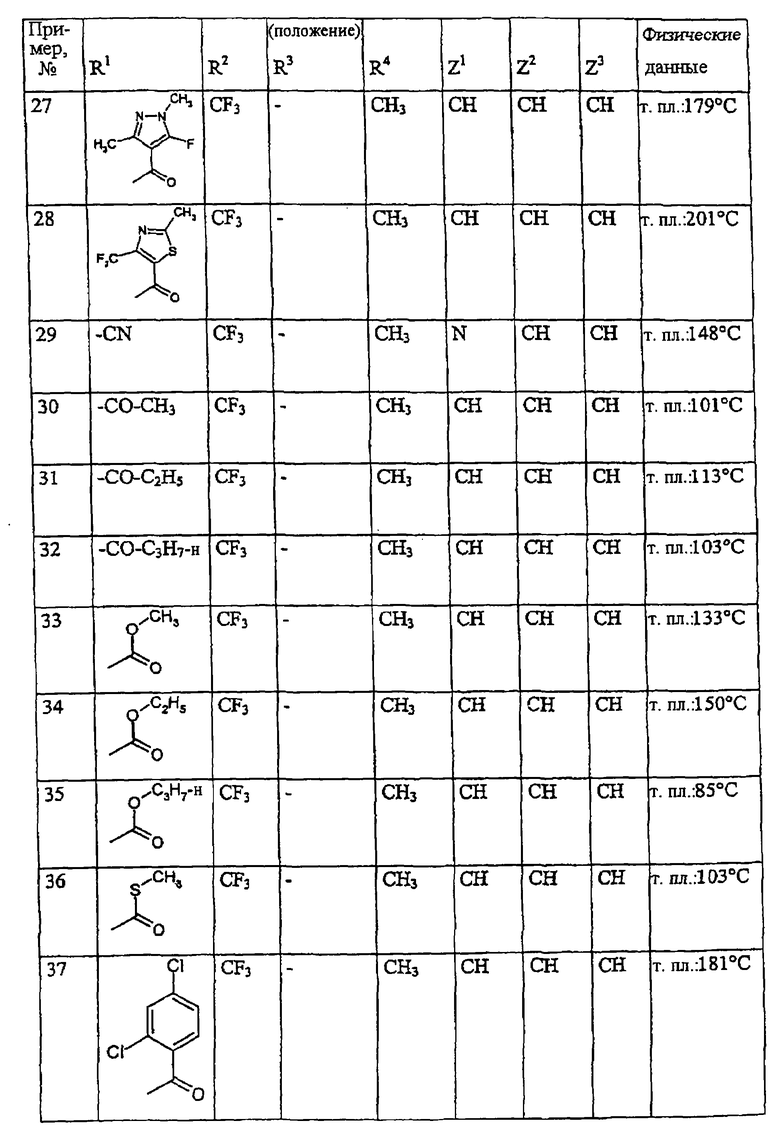


Определение указанных в таблице 1 значений log P осуществляют согласно Директиве EEC 79/831, Приложение V.A8, путем ВЭЖХ (высокоэффективная жидкостная хроматография) при использовании колонки с обращенной фазой (С 18). Температура: 43°С.
(а) Элюенты для определения в кислой области значений рН: 0,1%-ная водная фосфорная кислота, ацетонитрил; линейный градиент от 10% ацетонитрила до 90% ацетонитрила; соответствующие результаты измерения в таблице 1 обозначены индексома).
(б) Элюенты для определения в нейтральной области значений рН: 0,01 М водный раствор фосфатного буфера, ацетонитрил; линейный градиент от 10% ацетонитрила до 90% ацетонитрила; соответствующие результаты измерения в таблице 1 обозначены индексом б).
Калибрование осуществляют с помощью неразветвленных алкан-2-онов (с 3-16 атомами углерода), значения log P которых известны (определение значений log P осуществляют на основании времен удерживания путем линейной интерполяции между двумя последовательными алканонами).
Значения λmax определяют с помощью УФ-спектров при длинах волн от 200 до 400 нм для максимальных величин хроматографических пиков.
Исходные вещества формулы (II)
Пример (II-1)
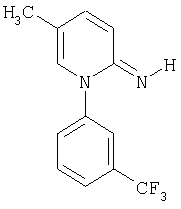
(способ (α))
Стадия 1
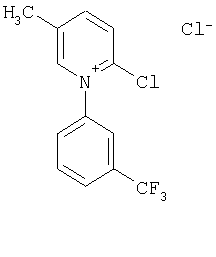
Смесь из 2,5 г (10 ммоль) 5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридона, 3,9 г (30 ммоль) оксалилхлорида, 40 мл 1,2-дихлорэтана и двух капель N,N-диметилформамида кипятят с обратным холодильником вплоть до прекращения выделения газа. После охлаждения до комнатной температуры выпавший в осадок кристаллический продукт выделяют путем отфильтровывания под вакуумом.
Получают 2,1 г (65% от теоретически рассчитанного количества) 2-хлор-5-метил-1-(3-трифторметилфенил)пиридинийхлорида с температурой плавления 194°С.
Стадия 2

3,1 г (10 ммоль) 2-Хлор-5-метил-1-(3-трифторметилфенил)пиридинийхлорида вводят в 40 мл метанола и при температуре от 20 до 30°С в эту смесь пропускают аммиак вплоть до насыщения раствора. Затем к этому раствору добавляют 3,6 г (20 ммоль) метилата натрия в виде 30%-ного метанольного раствора и после этого смесь концентрируют в вакууме водоструйного насоса.
Таким образом полученный продукт (5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридиний) без дальнейшей очистки можно вводить во взаимодействие согласно предлагаемому в изобретении способу (а).
Пример (II-1)

(способ (β))
Смесь из 10 г (24 ммоль) 4-метил-N-[5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридинилиден]бензолсульфонамида и 50 г 80%-ной серной кислоты перемешивают в течение 15 часов при температуре 50°С и затем по каплям добавляют к 1 М водному раствору карбоната натрия. Затем экстрагируют этилацетатом, органическую фазу сушат над сульфатом натрия и фильтруют. Из фильтрата тщательно отгоняют растворитель при пониженном давлении.
Получают 2,3 г (38% от теоретически рассчитанного количества) 5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридиния, который без дальнейшей очистки можно вводить во взаимодействие согласно предлагаемому в изобретении способу (а).
Аналогично методикам примера (II-1) можно также, например, получать указанные в нижеприводимой таблице 2 соединения общей формулы (II).
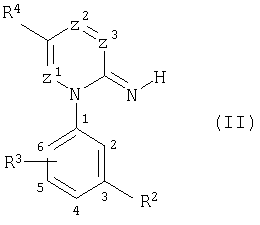
Примеры соединений формулы (II) (причем при этом речь идет, соответственно, о гидрохлоридах)
Пример (II-26): 5-метил-1-(2,3-дифторметилендиоксифенил)-2(1Н)-пиридиний;
Пример (II-27): 5-метил-1-(3,4-дифторметилендиоксифенил)-2(1Н)-пиридиний;
Пример (II-28): 5-метил-1-(2,3-тетрафторэтилендиоксифенил)-2(1H)-пиридиний;
Пример (II-29): 5-метил-1-(3,4-тетрафторэтилендиоксифенил)-2(1Н)-пиридиний;
Пример (II-30): 5-метил-1-(2,3-хлортрифторэтилендиоксифенил)-2(1Н)-пиридиний;
Пример (II-31): 5-метил-1-(3,4-хлортрифторэтилендиоксифенил)-2(1Н)-пиридиний.
Исходные вещества формулы (V)
Пример (V-1)

Смесь из 18,7 г (74 ммоль) 5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридинона, 16,4 г (74 ммоль) пентасульфида фосфора и 75 мл пиридина кипятят с обратным холодильником в течение двух часов и после охлаждения выливают в 300 мл воды. После перемешивания в течение ночи выпавший в осадок кристаллический продукт выделяют путем отфильтровывания под вакуумом.
Получают 12,8 г (64% от теоретически рассчитанного количества) 5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридинтиона с температурой плавления 96°С.
Аналогично методике примера (V-1) можно также, например, получать указанные в нижеприводимой таблице 3 соединения общей формулы (V).

Примеры соединений формулы (V)
Пример (V-26): 5-метил-1-(2,3-дифторметилендиоксифенил)-2(1Н)-пиридинтион;
Пример (V-27): 5-метил-1-(3,4-дифторметилендиоксифенил)-2(1Н)-пиридинтион;
Пример (V-28): 5-метил-1-(2,3-тетрафторэтилендиоксифенил)-2(1Н)-пиридинтион;
Пример (V-29): 5-метил-1-(3,4-тетрафторэтилендиоксифенил)-2(1Н)-пиридинтион;
Пример (V-30): 5-метил-1-(2,3-хлортрифторэтилендиоксифенил)-2(1Н)-пиридинтион;
Пример (V-31): 5-метил-1-(3,4-хлортрифторэтилендиоксифенил)-2(1Н)-пиридинтион.
Форпродукты формулы (VII)
Пример (VII-1)

Смесь из 2,5 г (10 ммоль) 5-метил-1-(3-трифторметилфенил)-2(1Н)-пиридона, 3,9 г (30 ммоль) оксалилхлорида, 40 мл 1,2-дихлорэтана и двух капель N,N-диметилформамида кипятят с обратным холодильником вплоть до прекращения выделения газа. После охлаждения до комнатной температуры выпавший в осадок кристаллический продукт выделяют путем отфильтровывания под вакуумом.
Получают 2,1 г (65% от теоретически рассчитанного выхода) 2-хлор-5-метил-1-(3-трифторметилфенил)пиридинийхлорида с температурой плавления 194°С.
Аналогично методике примера (VII-1) можно также, например, получать указанные в нижеприводимой таблице 4 соединения общей формулы (VII).
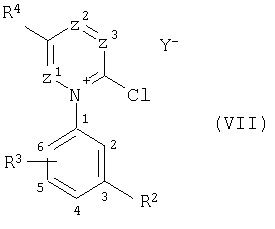
Примеры соединений формулы (VII) (Y при этом означает, соответственно, хлор)
Пример (VII-26): 2-хлор-5-метил-1-(2,3-дифторметилендиоксифенил)пиридинийхлорид;
Пример (VII-27): 2-хлор-5-метил-1-(3,4-дифторметилендиоксифенил)пиридинийхлорид;
Пример (VII-28): 2-хлор-5-метил-1-(2,3-тетрафторэтилендиоксифенил)пиридинийхлорид;
Пример (VII-29): 2-хлор-5-метил-1-(3,4-тетрафторэтилендиоксифенил)пиридинийхлорид;
Пример (VII-30): 2-хлор-5-метил-1-(2,3-хлортрифторэтилендиоксифенил)пиридиний-хлорид;
Пример (VII-31): 2-хлор-5-метил-1-(3,4-хлортрифторэтилендиоксифенил)пиридиний-хлорид.
Исходные вещества формулы (IX)
Пример (IX-1)
Смесь из 21,8 г (0,20 моль) 5-метил-2-пиридона, 54 г (0,24 моль) 3-бромбензо-трифторида, 27,7 г (0,20 моль) карбоната калия, 2 г (10 ммоль) иодида одновалентной меди и 300 мл N,N-диметилформамида перемешивают в течение 15 часов при температуре 100°С и следующие 6 часов при температуре 140°С. После охлаждения до комнатной температуры смешивают с 300 мл этилацетата и затем разбавляют водой примерно вдвое. Органическую фазу отделяют, а водную фазу дополнительно экстрагируют этилацетатом. Объединенные органические фазы промывают водой, сушат над сульфатом натрия и фильтруют. Из фильтрата тщательно отгоняют растворитель при пониженном давлении.
Получают 20,7 г (41% от теоретически рассчитанного количества) 5-метил-1-(3-три-фторметилфенил)-2(1Н)-пиридинона с температурой плавления 95°С.
Аналогично методике примера (IX-1) можно также, например, получать указанные в нижеприводимой таблице 5 соединения общей формулы (IX).
Примеры соединений формулы (IX)
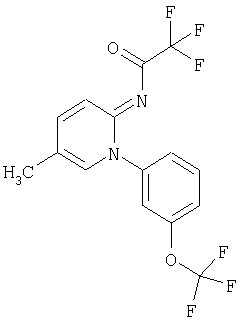
Пример (IX-28): 5-метил-1-(2,3-дифторметилендиоксифенил)-2(1Н)-пиридинон (log P=3,95а));
Пример (IX-29): 5-метил-1-(3,4-дифторметилендиоксифенил)-2(1Н)-пиридинон;
Пример (IX-30): 5-метил-1-(2,3-тетрафторэтилендиоксифенил)-2(1Н)-пиридинон;
Пример (IX-31): 5-метил-1-(3,4-тетрафторэтилендиоксифенил)-2(1Н)-пиридинон;
Пример (IX-32): 5-метил-1-(2,3-хлортрифторэтилендиоксифенил)-2(1Н)-пиридинон;
Пример (IX-33): 5-метил-1-(3,4-хлортрифторэтилендиоксифенил)-2(1Н)-пиридинон;
Пример (IX-34): 3-метил-1-(3-трифторметилфенил)-2(1Н)-пиридинон (т.пл.: 122°С);
Пример (IX-35): 5-трифторметил-1-(3-трифторметилфенил)-2(1Н)-пиридинон (log P=2,78а)).
(в отношении определения значений log P см. с.57).
Примеры применения
Пример А
Довсходовой тест
Растворитель: 5 масс. частей ацетона
Эмульгатор: 1 масс. часть простого алкиларилполигликолевого эфира
Для получения целевой композиции с биологически активным веществом 1 масс. часть биологически активного вещества смешивают с указанным количеством растворителя, добавляют указанное количество эмульгатора и концентрат разбавляют водой до желательной концентрации.
Семена тестируемых растений высевают в обычную почву. Спустя 24 часа почву обрызгивают композицией с биологически активным веществом таким образом, что наносят, соответственно, желательное количество биологически активного вещества на единицу площади. Концентрацию биологически активного вещества в рабочем растворе выбирают таким образом, что в 1000 л воды на гектар наносят, соответственно, желательное количество биологически активного вещества.
Спустя три недели оценивают степень повреждения растений в процентах повреждения по сравнению с развитием необработанных контрольных растений.
При этом:
0% означает, что нет никакого действия (как и необработанные контрольные растения);
100% означает полное уничтожение.
В этом тесте, например, соединения согласно примеру получения 1, 2, 3, IX-1, IX-3, IX-11 и IX-16 при отчасти хорошей совместимости по отношению к культурным растениям, как, например, рис, оказывают сильное действие против сорняков.
Пример Б
Послевсходовой тест
Растворитель: 5 масс. частей ацетона
Эмульгатор: 1 масс. часть простого алкиларилполигликолевого эфира
Для получения целевой композиции с биологически активным веществом 1 масс. часть биологически активного вещества смешивают с указанным количеством растворителя, добавляют указанное количество эмульгатора и концентрат разбавляют водой до желательной концентрации.
С помощью композиции с биологически активным веществом опрыскивают тестируемые растения, которые имеют высоту 5-15 см, таким образом, что наносят, соответственно, желательные количества биологически активного вещества на единицу площади. Концентрацию рабочего раствора выбирают таким образом, что в 1000 л воды на гектар наносят, соответственно, желательные количества биологически активного вещества.
Спустя три недели оценивают степень повреждения растений в процентах повреждения по сравнению с развитием необработанных контрольных растений.
При этом:
0% означает, что нет никакого действия (как и необработанные контрольные растения);
100% означает полное уничтожение.
В этом тесте, например, соединения согласно примеру получения 1, 3, IX-1 и IX-16 оказывают сильное действие против сорняков.



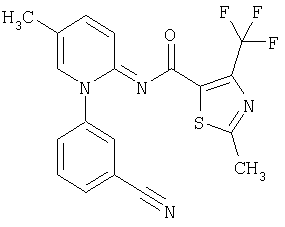

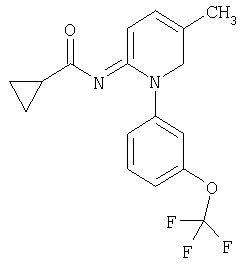

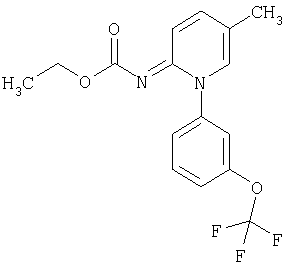

Примеры соединений формулы (II)
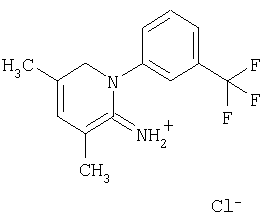




Примеры соединений формулы (VII)

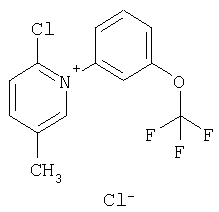
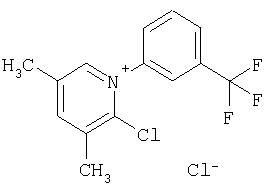
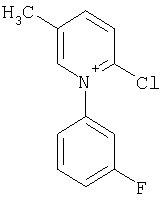
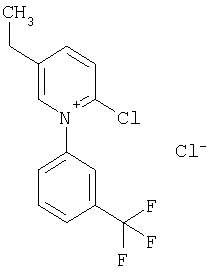






(Довсходовой тест согласно примеру А)


(Послевсходовой тест согласно примеру Б)

| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ТЕТРАЦИКЛИЧЕСКИЕ АНАЛОГИ КАМПТОТЕЦИНОВ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1998 |
|
RU2220144C2 |
| СРЕДСТВО, УСИЛИВАЮЩЕЕ ПРОТИВООПУХОЛЕВОЕ ДЕЙСТВИЕ С ПРИМЕНЕНИЕМ СОЕДИНЕНИЯ ПИРАЗОЛО[3,4-d]ПИРИМИДИНА | 2018 |
|
RU2799006C2 |
| НОВОЕ ПИРАЗОЛО[3, 4-D]ПИРИМИДИНОВОЕ СОЕДИНЕНИЕ ИЛИ ЕГО СОЛЬ | 2016 |
|
RU2705579C2 |
| ТЕТРАГИДРОПИРИДИН- ИЛИ 4-ГИДРОКСИПИПЕРИДИН-АЛКИЛАЗОЛЫ ИЛИ ИХ ФИЗИОЛОГИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1995 |
|
RU2168507C2 |
| СОЕДИНЕНИЯ ПИРИДАЗИНОНА И ГЕРБИЦИД, СОДЕРЖАЩИЙ ДАННОЕ СОЕДИНЕНИЕ | 2008 |
|
RU2463296C2 |
| ЗАМЕЩЕННЫЕ ТИЕНИЛ(АМИНО)СУЛЬФОНИЛМОЧЕВИНЫ И ГЕРБИЦИДНОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 2000 |
|
RU2252223C2 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТАГОНИСТИЧЕСКОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ АНГИОТЕНЗИНА, НА ИХ ОСНОВЕ | 1992 |
|
RU2053229C1 |
| ПРОИЗВОДНЫЕ ЦИКЛОАЛКАНО-ПИРИДИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 1997 |
|
RU2194698C2 |
| КОНДЕНСИРОВАННЫЕ 5-ЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ ИЛИ ИХ СОЛИ, ПРОЯВЛЯЮЩИЕ АКТИВНОСТЬ ПО ТОРМОЖЕНИЮ АГРЕГАЦИИ | 1992 |
|
RU2041211C1 |
| ЦИКЛИЧЕСКИЕ АЗОТСОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ, СМЕСЬ ИХ ИЗОМЕРОВ, ОТДЕЛЬНЫЕ ИЗОМЕРЫ ИЛИ ИХ СОЛИ | 1994 |
|
RU2126002C1 |
Описываются в п.п.1-6 замещенные иминоазины формулы (I), в которой R1 означает цианогруппу или одну из группировок -CQ1-Q2R5, -NH-CQ1-Q2-R5 или -SO2-R6; R2 означает цианогруппу, атом галогена, замещенный алкил или алкоксил; R3 означает атом водорода или атом галогена; R4 означает атом водорода или незамещенный алкил; Q1 означает атом кислорода; Q2 означает простую связь или атом кислорода, атом серы или N-R5; R5 означает атом водорода или, соответственно, незамещенный или замещенный алкил, алкенил, алкенилоксигруппу, циклоалкил, фенил, фенилалкил, тиадиазолил, пиримидинил, пиразолил, тиазолил; R6 означает, соответственно, замещенный или незамещенный алкил, циклоалкил, фенил; Z1 означает атом азота или C-R4; Z2 означает С-R4; Z3 означает C-R4. Описываются также в п.7 иминоазины общей формулы (II), в п.8 хлоразиниевые соединения формулы (VII), в п.9 соединения пиридинона формулы (IXa), значения заместителей у которых указаны выше, в п.10 гербицидное средство, содержащее эти соединения. Технический результат - представленные соединения обладают высокой гербицидной активностью против широкого спектра сорняков. 5 н. и 5 з.п. ф-лы, 8 табл.
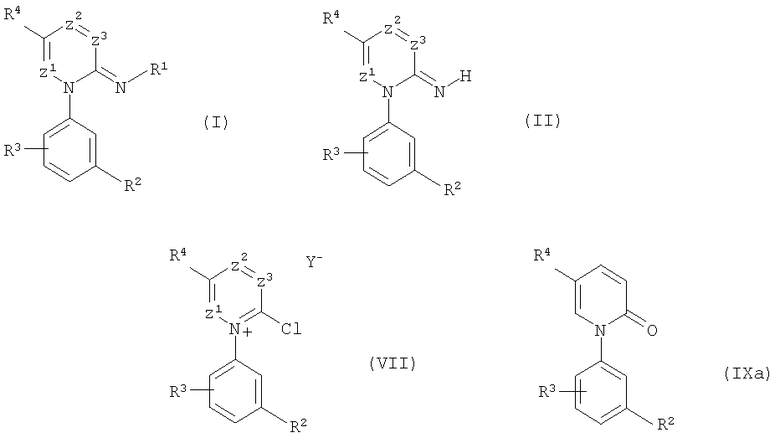
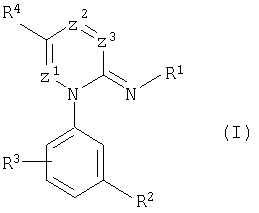
в которой R1 означает цианогруппу или одну из группировок -CQ1-Q2-R5, -NH-CQl-Q2-R5 или -SO2-R6;
R2 означает цианогруппу, атом галогена, замещенный алкил или алкоксил;
R3 означает атом водорода или атом галогена;
R4 означает атом водорода или незамещенный алкил;
Q1 означает атом кислорода,
Q2 означает простую связь или атом кислорода, атом серы или N-R5;
R5 означает атом водорода или, соответственно, незамещенный(ную) или замещенный(ную) алкил, алкенил, алкенилоксигруппу, циклоалкил, фенил, фенилалкил, тиадиазолил, пиримидинил, пиразолил, тиазолил;
R6 означает, соответственно, незамещенный или замещенный алкил, циклоалкил, фенил;
Z1 означает атом азота или C-R4;
Z2 означает C-R4;
Z3 означает C-R4.
R2 означает цианогруппу, атом галогена, замещенный галогеном алкил или алкоксил;
R3 означает атом водорода или атом галогена;
R4 означает атом водорода или незамещенный алкил с 1-5 атомами углерода;
Q1 означает атом кислорода;
R5 означает атом водорода, соответственно, незамещенный или замещенный алкил с 1-6 атомами углерода; замещенный(ную) галогеном алкенил, алкенилоксигруппу с 2-6 атомами углерода, незамещенный циклоалкил с 3-6 атомами углерода в циклоалкильной группе, фенил, замещенный галогеном, незамещенный фенилалкил, тиадиазолил, пиримидинил, пиразолил, тиазолил, замещенные алкилом с 1-4 атомами углерода, галогеналкилом с 1-4 атомами углерода, алкоксилом с 1-4 атомами углерода;
R6 означает, соответственно, замещенный галогеном алкил, незамещенный циклоалкил, замещенный алкилом с 1-4 атомами углерода фенил;
Z1 означает C-R4;
Z2 означает C-R4;
Z3 означает C-R4.
R6 означает, соответственно, замещенный фтором метил, незамещенный циклопропил или замещенный метилом фенил.
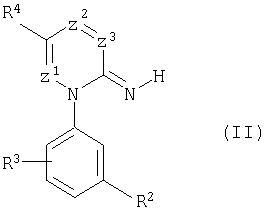
в которой R2 означает трифторметил, цианогруппу, трифторметоксигруппу, фтор;
R3 означает атом водорода или фтора;
R4 означает атом водорода, или незамещенный метил, или этил;
Z1 означает атом азота или метиновую группу;
Z2 означает метиновую группу;
Z3 означает метиновую группу, C-CONH2, С-СН3, или их аддукты с кислотой.
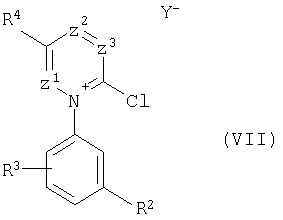
в которой R2 означает трифторметил, цианогруппу, трифторметоксигруппу, фтор;
R3 означает атом водорода или фтора;
R4 означает атом водорода, незамещенный метил или этил;
Z1 означает атом азота или метиновую группу;
Z2 означает метиновую группу;
Z3 означает метиновую группу или С-СН3 и
Y означает хлор.

в которой R2 означает трифторметил, цианогруппу, трифторметоксигруппу, фтор;
R3 означает атом водорода или фтора, или вместе с остатком R2 в ортоположении означает дифтор, метилендиокси;
R4 означает незамещенный метил или этил.
| ГЕНЕРАТОР ЦИЛИНДРИЧЕСКИХ Л\ЛГНИТНЫХДОМЕНОВ | 1973 |
|
SU432600A1 |
| US 3697522, 10.10.1972 | |||
| ПРОИЗВОДНЫЕ 3(2Н) - ПИРИДАЗИНОНА | 1992 |
|
RU2054422C1 |
Авторы
Даты
2005-12-10—Публикация
2001-05-08—Подача