Изобретение относится к новым химическим веществам, обладающим ценными свойствами, в частности к циклическим азотсодержащим производным общей формулы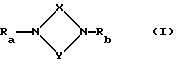
где X - карбиминогруппа, незамещенная или замещенная у атома азота алкилом, арилом, гетероарилом или цианогруппой, карбонил, тиокарбонил, сульфонил, 1-нитроэтен-2,2-диил или 1,1-дициано-этен-2,2-диил,
Y - незамещенный или замещенный Rc или Rd, или Rc и Rd, неразветвленный алкилен или алкенилен с 2 - 4 атомами углерода, который дополнительно может быть замещен одним или двумя алкильными группами, и в котором одна или две метиленовые группы могут быть заменены карбонилом, 1,2-циклоалкилен с 5 - 7 атомами углерода, незамещенный или замещенный Rc или Rd, или Rc и Rd, 1,2- циклоалкенилен с 5 - 7 атомами углерода, незамещенный или замещенный Rc или Rd или Rc и Rd, 1,2-арилен, 1,2-фенилен, в котором одна или две метиновые группы заменены атомом азота или одна или две группы -CH=CH- заменены группой -CO-NH- или одна метиновая группа заменена атомом азота и одна группа -CH= CH- заменена группой -CO-NH-, причем вышеназванные гетероциклические группы могут быть замещены одной или двумя алкильными группами, группа -CO-NH-, -NH-CO-, -CH=N- или -N=CH-, незамещенная или замещенная Rc или Rd,
первый из остатков Ra - Rd означает группу A-B-, в которой A - группа формул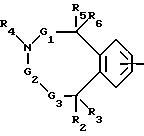

или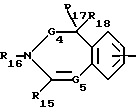
где бензоостаток может быть монозамещен остатком R25, моно- или дизамещен остатком R26 или монозамещен остатком R25 и дополнительно монозамещен остатком R26, причем заместители R25 и R26, которые могут быть одинаковыми или различными, имеют нижеуказанные значения, при этом в одном из бензоостатков 1 - 3 метиновые группы могут быть заменены атомом азота или одна группа -CH= CH- может быть заменена группой -CO-NR1- или одна метиновая группа может быть заменена атомом азота и одна группа -CH=CH- может быть заменена группой -CO-NR1-, где R1, означает атом водорода или алкил,
G1 и G4 - связь или метилен, который может быть моно- или дизамещен алкилом, арилом или гетероарилом, причем заместители могут быть одинаковыми или различными,
G2 - связь или метилен, замещенный остатками R7 и R8,
G3 - связь, метилен, замещенный остатками R9 и R10, или же карбонил, если G2 не означает связь,
G5 - атом азота или метин, незамещенный или замещенный алкилом, арилом или гетероарилом,
R2 - атом водорода, алкил, арил или гетероарил или же гидроксил или алкоксил, если по крайней мере одна из групп G2 и G3 не означает связь,
R3 - атом водорода, алкил, арил или гетероарил или же R3 вместе с R2 образуют атом кислорода, если по крайней мере одна из групп G2 и G3 не означает связь,
R4 и R14 - атом водорода, циклоалкил с 3 - 7 атомами углерода, циклоалкилалкил с 3 - 7 атомами углерода в циклоалкильной части, алкил с 1 - 8 атомами углерода, алкенил с 3 - 8 атомами углерода, который не может быть связан с атомом азота через винильную группу, гидроксиалкил, алкоксиалкил, аминоалкил, алкиламиноалкил, диалкиламиноалкил, цианоалкил, карбоксиалкил, алкоксикарбонилалкил, аминокарбонилалкил, N-алкиламинокарбонилалкил, N,N-диалкиламинокарбонилалкил, арилалкил, гетероарилалкил, алкоксикарбонил, арилметилоксикарбонил, формил, ацетил, трифторацетил, аллилоксикарбонил, амидино или группа R11CO-0-(R12CR13)-O-CO-, где R11 - алкил с 1 - 8 атомами углерода, циклоалкил с 5 - 7 атомами углерода, арил или арилалкил, R12 - атом водорода, алкил, циклоалкил с 5 - 7 атомами углерода или арил и R13 - атом водорода или алкил, или R4 вместе с R3 означают неразветвленный алкилен с 2 - 4 атомами углерода или же метилен, если G2 не означает связь,
R5 - атом водорода, алкил, арил или гетероарил или же гидроксил или алкоксил, если G1 не означает связь, или же R4 вместе с R5 означают дополнительную связь, если G1 означает связь,
R6 - атом водорода, алкил, арил или гетероарил или же атом хлора, гидроксил, метоксил, амино, алкиламино или диалкиламино, если G1 означает связь и R4 вместе с R5 означают дополнительную связь, или же R6 вместе с R5 означают атом кислорода, если G1 не означает связь,
R7 - атом водорода, алкил, арил или гетероарил,
R8 - атом водорода, алкил, арил или гетероарил или R8 вместе с R4 означают неразветвленный алкилен с 2 - 5 атомами углерода,
R9 - атом водорода, алкил, арил или гетероарил или же гидроксил или алкоксил, если G2 не означает связь,
R10 - атом водорода, алкил, арил или гетероарил или R10 вместе с R4 означают неразветвленный алкилен с 2 - 4 атомами углерода,
R15 - атом водорода или хлора, алкил, арил, гетероарил, гидроксил, метоксил, амино, алкиламино или диалкиламино,
R16 - атом водорода, циклоалкил с 3 - 7 атомами углерода, циклоалкилалкил с 3 - 7 атомами углерода в циклоалкильной части, алкил с 1 - 8 атомами углерода, алкенил с 3 - 8 атомами углерода, который не может быть связан с атомом азота через винильную группу, гидроксиалкил, алкоксиалкил, аминоалкил, алкиламиноалкил, диалкиламиноалкил, цианалкил, карбоксиалкил, алкоксикарбонилалкил, аминокарбонилалкил, N-алкиламинокарбонилалкил, N,N-диалкиламинокарбонилалкил или арилалкил,
R17 - атом водорода или алкил или же R16 вместе с R17 означают дополнительную связь, если G4 означает связь,
R18 - атом водорода, алкил или же атом фтора, хлора или брома, гидроксил, метоксил, амино, алкиламино или диалкиламино, если G4 означает связь и R16 и R17 вместе означают дополнительную связь,
n - число 1 или 2,
В - связь, алкилен, алкенилен, арилен, пиридинилен, пиримидинилен, пиразинилен или пиридазинилен, в которых одна или две группы -CH=N- могут быть заменены группой -CO-NH- и один из атомов азота может быть связан с остатком A вместо связи с атомом водорода, причем указанные гетероциклические группы дополнительно могут быть замещены одной или двумя алкильными группами, циклоалкилен с 4 - 7 атомами углерода, незамещенный или замещенный одной или двумя алкильными группами, незамещенный или замещенный одной или двумя алкильными группами циклоалкилен с 5 - 7 атомами углерода, в котором одна группа 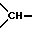 заменена атомом азота, причем, кроме того, в указанных 5- до 7-членных кольцах одна смежная с атомом азота метиленовая группа может быть заменена карбонилом, второй из остатков Ra - Rd означает группу формулы
заменена атомом азота, причем, кроме того, в указанных 5- до 7-членных кольцах одна смежная с атомом азота метиленовая группа может быть заменена карбонилом, второй из остатков Ra - Rd означает группу формулы
F - E - D-,
где D - алкилен с 1 - 6 атомами углерода, в котором одна метиленовая группа может быть заменена атомом кислорода или серы, сульфинилом, сульфонилом или группой -NR19-, где R19 означает атом водорода, алкил, алкилкарбонил, алкилсульфонил, арилкарбонил или арилсульфонил, или в котором одна этиленовая группа может быть заменена группой -CO-NR20- или -NR20-CO-, где R20 означает атом водорода или алкил, алкенилен с 2 - 6 атомами углерода, арилен, пиридинилен, пиримидинилен, пиразинилен или пиридазинилен, в которых одна или две группы -CH=N- могут быть заменены группой -CO-NH- и один из атомов азота вместе с атомом водорода может также быть связан с остатком E, если последний не означает связь или не связан через гетероатом или карбонил с остатком D, причем указанные гетероциклические группы дополнительно могут быть замещены одной или двумя алкильными группами, инданилен, нафтилен, 1,2,3,4-тетрагидронафтилен или бензосуберанилен, в которых одно из колец связано с остатком E, а другое - с циклическим остатком общей формулы (I), причем насыщенные кольца могут быть замещены одной или двумя алкильными группами, а ароматические кольца могут быть замещены атомом фтора, хлора, брома или йода, алкилом, трифторметилом, гидроксилом, алкоксилом, алкилсульфенилом, алкилсульфинилом, алкилсульфонилом или цианогруппой, циклоалкилен с 4 - 7 атомами углерода, незамещенный или замещенный одной или двумя алкильными группами, незамещенный или замещенный одной или двумя алкильными группами циклоалкилен с 5 - 7 атомами углерода, в котором одна группа 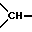 заменена атомом азота, причем, кроме того, в указанных 5- до 7-членных кольцах одна смежная с атомом азота метиленовая группа может быть заменена карбонилом, незамещенный или замещенный одной или двумя алкильными группами пиперазинилен, в котором одна смежная с атомом азота метиленовая группа может быть заменена карбонилом, или алкиленкарбонил с общим числом атомов углерода 2-6, если E - циклическая иминогруппа, причем карбонил связан с атомом азота циклической иминогруппы группы E, или же связь, если E не означает связь,
заменена атомом азота, причем, кроме того, в указанных 5- до 7-членных кольцах одна смежная с атомом азота метиленовая группа может быть заменена карбонилом, незамещенный или замещенный одной или двумя алкильными группами пиперазинилен, в котором одна смежная с атомом азота метиленовая группа может быть заменена карбонилом, или алкиленкарбонил с общим числом атомов углерода 2-6, если E - циклическая иминогруппа, причем карбонил связан с атомом азота циклической иминогруппы группы E, или же связь, если E не означает связь,
E - связь, алкилен с 1 - 6 атомами углерода, который может быть замещен одной или двумя алкильными группами с 1 - 8 атомами углерода, алкенилом или алкинилом с 2 - 4 атомами углерода, гидроксилом, аминогруппой, арилом, гетероарилом, алкоксилом или алкиламиногруппой с 1 - 8 атомами углерода, диалкиламиногруппой с общим числом атомов углерода 2 - 10, группой HNR21- или N-алкил-NR21-, где R21 означает алкилкарбонил или алкилсульфонил с 1 - 8 атомами углерода в алкильной части, алкилоксикарбонил с общим числом атомов углерода 2 - 5, циклоалкилкарбонил или циклоалкилсульфонил с 5 - 7 атомами углерода в циклоалкильной части, арилалкилкарбонил, арилалкилсульфонил, арилалкоксикарбонил, арилкарбонил или арилсульфонил, алкенилен с 2 - 6 атомами углерода, арилен, пиридинилен, пиримидинилен, пиразинилен или пиридазинилен, незамещенный или замещенный одной или двумя алкильными группами, незамещенный или замещенный одной или двумя алкильными группами циклоалкилен с 5 - 7 атомами углерода, в котором одна группа 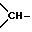 заменена атомом азота, связанным с атомом углерода остатка D, циклоалкилен с 4 - 7 атомами углерода в циклоалкиленовой части, незамещенный или замещенный одной или двумя алкильными группами с 1 - 8 атомами углерода, алкенилом или алкинилом с 2 - 4 атомами углерода, гидроксилом, аминогруппой, арилом, гетероарилом, алкоксилом или алкиламиногруппой с 1 - 8 атомами углерода, диалкиламиногруппой с общим числом атомов углерода 2 - 10, группой HNR21- или N-алкил-NR21-, где R21 имеет вышеуказанное значение, или же связанный с остатком D через остаток W алкилен, в котором W означает атом кислорода или серы, сульфинил, сульфонил, группу -NR19-, -NR20-CO- или -CO-NR20-, где R19 и R20 имеют вышеуказанные значения, при этом алкилен может быть дополнительно замещен одной или двумя алкильными группами с 1 - 8 атомами углерода, алкенилом или алкинилом с 2 - 4 атомами углерода, гидроксилом, аминогруппой, арилом, гетероарилом, алкоксилом или алкиламиногруппой с 1 - 8 атомами углерода, диалкиламиногруппой с общим числом атомов углерода 2 - 10, группой -HNR21- или N-алкил-NR21, где R21 имеет вышеуказанное значение, причем гетероатом дополнительного заместителя отделен от гетероатома остатка W по крайней мере двумя атомами углерода, если D не означает связь,
заменена атомом азота, связанным с атомом углерода остатка D, циклоалкилен с 4 - 7 атомами углерода в циклоалкиленовой части, незамещенный или замещенный одной или двумя алкильными группами с 1 - 8 атомами углерода, алкенилом или алкинилом с 2 - 4 атомами углерода, гидроксилом, аминогруппой, арилом, гетероарилом, алкоксилом или алкиламиногруппой с 1 - 8 атомами углерода, диалкиламиногруппой с общим числом атомов углерода 2 - 10, группой HNR21- или N-алкил-NR21-, где R21 имеет вышеуказанное значение, или же связанный с остатком D через остаток W алкилен, в котором W означает атом кислорода или серы, сульфинил, сульфонил, группу -NR19-, -NR20-CO- или -CO-NR20-, где R19 и R20 имеют вышеуказанные значения, при этом алкилен может быть дополнительно замещен одной или двумя алкильными группами с 1 - 8 атомами углерода, алкенилом или алкинилом с 2 - 4 атомами углерода, гидроксилом, аминогруппой, арилом, гетероарилом, алкоксилом или алкиламиногруппой с 1 - 8 атомами углерода, диалкиламиногруппой с общим числом атомов углерода 2 - 10, группой -HNR21- или N-алкил-NR21, где R21 имеет вышеуказанное значение, причем гетероатом дополнительного заместителя отделен от гетероатома остатка W по крайней мере двумя атомами углерода, если D не означает связь,
F - карбонил, замещенный гидроксилом, алкоксилом с 1 - 8 атомами углерода, арилалкоксигруппой или группой R22O-, где R22 означает циклоалкил с 4 - 8 атомами углерода и циклоалкилалкил с 3 - 8 атомами углерода в циклоалкильной части, в которых циклоалкильная часть может быть замещена алкилом, алкоксилом или диалкиламиногруппой, или алкилом и 1 - 3 метильными группами, при этом одна метиленовая группа в 4- до 8-членной циклоалкильной части может быть заменена атомом кислорода или алкилиминогруппой, бензоциклоалкил с 9 - 12 атомами углерода, арил, сульфо-, фосфоно-, O-алкилфосфоно-, O,O'-диалкилфосфоногруппа, тетразол-5-ил- или группа R23CO-O-CHR24-O-CO-, где R23 означает алкил или алкоксил с 1 - 8 атомами углерода, циклоалкил с 5 - 7 атомами углерода, циклоалкоксил с 5 - 7 атомами углерода в циклоалкильной части, арил, арилокси, арилалкил или арилалкокси и R24 - атом водорода или алкил,
кратчайшее расстояние между остатком F и расположенным на максимальном расстоянии от остатка F атомом азота группы A-B- составляет по крайней мере 11 связей,
третий из остатков Ra - Rd означает атом водорода, алкил, перфторалкил, алкоксил, алкилсульфенил, алкилсульфинил, алкилсульфонил, амино, алкиламино, диалкиламино, арил, гетероарил или арилалкил,
четвертый из остатков Ra - Rd означает атом водорода, алкил или арил, причем, если ничего другого не упомянуто,
под вышеуказанным термином "арил" следует понимать фенил, который может быть монозамещен остатком R25, моно-, ди- или тризамещен остатком R26 или монозамещен остатком R25 и дополнительно моно- или дизамещен остатком R26, причем заместители могут быть одинаковыми или различными, при этом R25 означает циано, карбоксил, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, алкоксикарбонил, алкилкарбонил, алкилсульфенил, алкилсульфинил, алкилсульфонил, алкилсульфонилокси, перфторалкил, перфторалкокси, нитро, амино, алкиламино, диалкиламино, алкилкарбониламино, фенилалкилкарбониламино, фенилкарбониламино, алкилсульфониламино, фенилалкилсульфониламино, фенилсульфониламино, N-алкил-алкилкарбониламино, N-алкил-фенилалкилкарбониламино, N-алкил-фенилкарбониламино, N-алкил-алкилсульфониламино, N-алкил-фенилалкилсульфониламино, N-алкил-фенилсульфониламино, аминосульфонил, алкиламиносульфонил или диалкиламиносульфонил, R26 - алкил, гидроксил или алкоксил, атом фтора, хлора, брома или йода, причем два остатка R26, если они связаны со смежными атомами углерода, могут также представлять собой алкилен с 3 - 6 атомами углерода, 1,3-бутадиен-1,4-диилен или метилендиокси-группу,
под вышеуказанным термином "арилен" следует понимать фенилен, который может быть монозамещен остатком R25, моно- или дизамещен остатком R26 или монозамещен остатком R25 и дополнительно монозамещен остатком R26, причем заместители могут быть одинаковыми или различными и имеют вышеуказанные значения,
под вышеуказанным термином "гетероарил" следует понимать 5-членное гетероароматическое кольцо, содержащее один атом кислорода, серы или азота, один атом азота и один атом кислорода, серы или азота или же два атома азота и один атом кислорода, серы или азота, или же содержащее 1, 2 или 3 атома азота 6-членное гетероароматическое кольцо, в котором одна или две группы -CH= N- могут быть заменены группой -CO-NR20, где R20 имеет вышеуказанное значение, при этом указанные гетероароматические кольца могут быть замещены одной или двумя алкильными группами или же атомом фтора, хлора, брома или йода, гидроксилом или алкоксилом на углеродном скелете,
а также, если ничего другого не упомянуто, вышеуказанные алкильные, алкиленовые или алкоксильные группы могут содержать 1 - 4 атома углерода и каждый из атомов углерода в вышеуказанных алкиленовых и циклоалкиленовых группах связан, как максимум, с одним гетероатомом,
смесям их изомеров или отдельным изомерам или их солям.
Предпочитаемыми соединениями вышеуказанной общей формулы (I), однако являются те, у которых
X - карбиминогруппа, незамещенная или замещенная у атома азота алкилом или цианогруппой, карбонил, тиокарбонил или сульфонил,
Y - незамещенный или замещенный Rc или Rd или Rc и Rd неразветвленный алкилен с 2 или 3 атомами углерода, который дополнительно может быть замещен одной или двумя алкильными группами и в котором одна метиленовая группа может быть заменена карбонилом, незамещенный или замещенный Rc или Rd или Rc и Rd неразветвленный алкенилен с 2 или 3 атомами углерода, в котором одна возможно имеющаяся метиленовая группа может быть заменена карбонилом, незамещенный или замещенный Rc или Rd или Rc и Rd 1,2-циклоалкилен с 5 - 7 атомами углерода, 1,2-циклоалкенилен с 5 - 7 атомами углерода, 1,2-арилен, 1,2-фенилен, в котором одна или две метиновые группы заменены атомом азота, причем вышеназванные гетероциклические группы могут быть замещены одной или двумя алкильными группами, группа -CO-NH-, -NH-CO-, -CH=N- или -N=CH-, незамещенные или замещенные Rc или Rd,
первый из остатков Ra - Rd означает группу A-B-, в которой
A - группа формул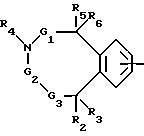
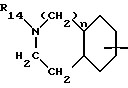
или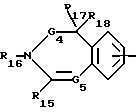
где бензоостаток может быть монозамещен остатком R25, моно- или дизамещен остатком R26 или монозамещен остатком R25 и дополнительно монозамещен остатком R26, причем заместители R25 и R26, которые могут быть одинаковыми или различными, имеют нижеуказанные значения, при этом в одном из бензоостатков 1 - 3 метиновые группы могут быть заменены атомом азота или одна группа -CH= CH- может быть заменена группой -CO-NR1- или одна метиновая группа может быть заменена атомом азота и одна группа -CH=CH- может быть заменена группой -CO-NR1-, где R1 означает атом водорода или алкил,
G1 и G4 - связь или метилен, который может быть моно- или дизамещен алкилом или арилом, причем заместители могут быть одинаковыми или различными,
G2 - связь или метилен, замещенный остатками R7 и R8,
G3 - связь или метилен, замещенный остатками R9 и R10,
G5 - атом азота или метин, незамещенный или замещенный алкилом или арилом,
R2 - атом водорода, алкил или арил или же гидроксил или алкоксил, если по крайней мере одна из групп G2 и G3 не означает связь,
R3 - атом водорода, алкил или арил,
R4 и R14 - атом водорода, циклоалкил с 3 - 7 атомами углерода, циклоалкилалкил с 3 - 7 атомами углерода в циклоалкильной части, алкил с 1 - 6 атомами углерода, алкенил с 3 - 6 атомами углерода, который не может быть связан с атомом азота через винильную группу, гидроксиалкил, алкоксиалкил, карбоксиалкил, алкоксикарбонилалкил, аминокарбонилалкил, N-алкиламинокарбонилалкил, N,N-диалкиламинокарбонилалкил, арилалкил, алкоксикарбонил, арилметилоксикарбонил, формил, ацетил, трифторацетил, аллилоксикарбонил, амидино или группа R11CO-O-(R12CR13)-O-CO-, где R11 - алкил с 1 - 8 атомами углерода, циклоалкил с 5 - 7 атомами углерода, арил или арилалкил, R12 - атом водорода, алкил, циклоалкил с 5 - 7 атомами углерода или арил и R13 - атом водорода, или R4 вместе с R3 означают неразветвленный алкилен с 2 - 4 атомами углерода или же метилен, если G2 не означает связь,
R5 - атом водорода, алкил или арил или же гидроксил или алкоксил, если G1 не означает связь, или же R4 вместе с R5 означают дополнительную связь, если G1 означает связь,
R6 - атом водорода, алкил или арил или же атом хлора, гидроксил, метоксил, амино, алкиламино или диалкиламино, если G1 означает связь и R4 вместе с R5 означают дополнительную связь,
R7 - атом водорода, алкил или арил,
R8 - атом водорода, алкил или арил или R8 вместе с R4 означают неразветвленный алкилен с 2 - 5 атомами углерода,
R9 - атом водорода, алкил или арил или же гидроксил или алкоксил, если G2 не означает связь,
R10 - атом водорода, алкил или арил или R10 вместе с R4 означают неразветвленный алкилен с 2 - 4 атомами углерода,
R15 - атом водорода или хлора, алкил, арил, гидроксил, метоксил, амино, алкиламино или диалкиламино,
R16 - атом водорода, циклоалкил с 3 - 7 атомами углерода, циклоалкилалкил с 3-7 атомами углерода в циклоалкильной части, алкил с 1 - 6 атомами углерода, алкенил с 3 - 6 атомами углерода, который не может быть связан с атомом азота через винильную группу, гидроксиалкил, алкоксиалкил, карбоксиалкил, алкоксикарбонилалкил, аминокарбонилалкил, N-алкиламинокарбонилалкил, N,N-диалкиламинокарбонилалкил или арилалкил,
R17 - атом водорода или алкил или же R16 вместе с R17 означают дополнительную связь, если G4 означает связь,
R18 - атом водорода, алкил или же атом фтора, хлора или брома, гидроксил, метоксил, амино, алкиламино или диалкиламино, если G4 означает связь и R16 и R17 вместе означают дополнительную связь,
n - число 1 или 2,
В - связь, алкилен с 1 - 6 атомами углерода, арилен, пиридинилен, пиримидинилен, пиразинилен или пиридазинилен, в которых одна или две группы -CH= N- могут быть заменены группой -CO-NH-, причем указанные гетероциклические группы дополнительно могут быть замещены одной или двумя алкильными группами, циклоалкилен с 4 - 7 атомами углерода, незамещенный или замещенный одной или двумя алкильными группами, незамещенный или замещенный одной или двумя алкильными группами циклоалкилен с 5 - 7 атомами углерода, в котором одна группа 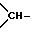 заменена атомом азота, причем, кроме того, в указанных 5- до 7-членных кольцах одна смежная с атомом азота метиленовая группа может быть заменена карбонилом,
заменена атомом азота, причем, кроме того, в указанных 5- до 7-членных кольцах одна смежная с атомом азота метиленовая группа может быть заменена карбонилом,
второй из остатков Ra - Rd означает группу формулы
F - E - D -,
где алкилен с 1 - 6 атомами углерода, в котором одна метиленовая группа может быть заменена атомом кислорода или серы, сульфинилом, сульфонилом или группой -NR19-, где R19 означает атом водорода, алкил, алкилкарбонил, алкилсульфонил, арилкарбонил или арилсульфонил, или в котором одна этиленовая группа может быть заменена группой -CO-NR20- или -NR20-CO-, где R20 означает атом водорода или алкил, алкенилен с 2 - 6 атомами углерода, арилен, пиридинилен, пиримидинилен, пиразинилен или пиридазинилен, в которых одна или две группы -CH=N- могут быть заменены группой -CO-NH-, причем указанные гетероциклические группы дополнительно могут быть замещены одной или двумя алкильными группами, инданилен, нафтилен, 1,2,3,4-тетрагидронафтилен или бензосуберанилен, в которых одно из колец связано с остатком E, а другое - с циклическим остатком общей формулы (I), причем насыщенные кольца могут быть замещены одной или двумя алкильными группами, а ароматические кольца могут быть замещены атомом фтора, хлора, брома или йода, алкилом, трифторметилом, гидроксилом, алкоксилом, алкилсульфенилом, алкилсульфинилом, алкилсульфонилом или цианогруппой, циклоалкилен с 4 - 7 атомами углерода, незамещенный или замещенный одной или двумя алкильными группами, незамещенный или замещенный одной или двумя алкильными группами циклоалкилен с 5 - 7 атомами углерода, в котором одна группа  заменена атомом азота, причем, кроме того, в указанных 5- до 7-членных кольцах одна смежная с атомом азота метиленовая группа может быть заменена карбонилом, незамещенный или замещенный одной или двумя алкильными группами пиперазинилен, в котором одна смежная с атомом азота метиленовая группа может быть заменена карбонилом, или алкиленкарбонил с общим числом атомов углерода 2 - 6, если E - циклическая иминогруппа, причем карбонил связан с атомом азота циклической иминогруппы группы E, или же связь, если E не означает связь,
заменена атомом азота, причем, кроме того, в указанных 5- до 7-членных кольцах одна смежная с атомом азота метиленовая группа может быть заменена карбонилом, незамещенный или замещенный одной или двумя алкильными группами пиперазинилен, в котором одна смежная с атомом азота метиленовая группа может быть заменена карбонилом, или алкиленкарбонил с общим числом атомов углерода 2 - 6, если E - циклическая иминогруппа, причем карбонил связан с атомом азота циклической иминогруппы группы E, или же связь, если E не означает связь,
E - связь, алкилен с 1 - 6 атомами углерода, который может быть замещен одной или двумя алкильными группами с 1 - 6 атомами углерода, гидроксилом, аминогруппой или арилом, алкоксилом или алкиламиногруппой с 1 - 6 атомами углерода, диалкиламиногруппой с общим числом атомов углерода 2 - 8, группой HNR21- или N-алкил-NR21-, где R21 означает алкилкарбонил или алкилсульфонил с 1 - 6 атомами углерода в алкильной части, алкилоксикарбонил с общим числом атомов углерода 2 - 5, циклоалкилкарбонил или циклоалкилсульфонил с 5 - 7 атомами углерода в циклоалкильной части, арилалкилкарбонил, арилалкилсульфонил, арилалкоксикарбонил, арилкарбонил или арилсульфонил, алкенилен с 2 - 6 атомами углерода, арилен, пиридинилен, пиримидинилен, пиразинилен или пиридазинилен, незамещенный или замещенный одной или двумя алкильными группами, незамещенный или замещенный одной или двумя алкильными группами циклоалкилен с 5 - 7 атомами углерода, в котором одна группа 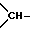 заменена атомом азота, связанным с атомом углерода остатка D, циклоалкилен с 4 - 7 атомами углерода, незамещенный или замещенный одной или двумя алкильными группами с 1 - 6 атомами углерода, гидроксилом, аминогруппой, арилом, алкоксилом или алкиламиногруппой с 1 - 6 атомами углерода, диалкиламиногруппой с общим числом атомов углерода 2 - 8, группой HNR21- или N-алкил-NR21-, где R21 имеет вышеуказанное значение, или же связанный с остатком D через остаток W алкилен, в котором W означает атом кислорода или серы, сульфинил, сульфонил, группу -NR19, -NR20-CO- или -CO-NR20-, где R19 и R20 имеют вышеуказанные значения, при этом алкилен может быть дополнительно замещен одной или двумя алкильными группами с 1 - 6 атомами углерода, гидроксилом, аминогруппой, арилом, алкоксилом или алкиламиногруппой с 1 - 6 атомами углерода, диалкиламиногруппой с общим числом атомов углерода 2 - 8, группой -HNR21- или N-алкил-NR21-, где R21 имеет вышеуказанное значение, причем гетероатом дополнительного заместителя отделен от гетероатома остатка W по крайней мере двумя атомами углерода, если D не означает связь,
заменена атомом азота, связанным с атомом углерода остатка D, циклоалкилен с 4 - 7 атомами углерода, незамещенный или замещенный одной или двумя алкильными группами с 1 - 6 атомами углерода, гидроксилом, аминогруппой, арилом, алкоксилом или алкиламиногруппой с 1 - 6 атомами углерода, диалкиламиногруппой с общим числом атомов углерода 2 - 8, группой HNR21- или N-алкил-NR21-, где R21 имеет вышеуказанное значение, или же связанный с остатком D через остаток W алкилен, в котором W означает атом кислорода или серы, сульфинил, сульфонил, группу -NR19, -NR20-CO- или -CO-NR20-, где R19 и R20 имеют вышеуказанные значения, при этом алкилен может быть дополнительно замещен одной или двумя алкильными группами с 1 - 6 атомами углерода, гидроксилом, аминогруппой, арилом, алкоксилом или алкиламиногруппой с 1 - 6 атомами углерода, диалкиламиногруппой с общим числом атомов углерода 2 - 8, группой -HNR21- или N-алкил-NR21-, где R21 имеет вышеуказанное значение, причем гетероатом дополнительного заместителя отделен от гетероатома остатка W по крайней мере двумя атомами углерода, если D не означает связь,
F - карбонил, замещенный гидроксилом, алкоксилом с 1 - 6 атомами углерода, арилалкоксигруппой или группой R22O-, где R22 означает циклоалкил с 4 - 7 атомами углерода и циклоалкилалкил с 3 - 7 атомами углерода в циклоалкильной части, в которых циклоалкильная часть может быть замещена алкилом, алкоксилом или диалкиламиногруппой, алкилом и 1 - 3 метильными группами, при этом одна метиленовая группа в 5- до 7-членной циклоалкильной части может быть заменена атомом кислорода или алкилиминогруппой, бензоциклоалкил с 9 - 11 атомами углерода, фосфоно-, O-алкилфосфоногруппа, O,O'-диалкилфосфоногруппа, тетразол-5-ил или группа R23CO-O-CHR24-O-CO-, где R23 означает алкил или алкоксил с 1 - 8 атомами углерода, циклоалкил с 5 - 7 атомами углерода, циклоалкоксил с 5 - 7 атомами углерода в циклоалкильной части, арил, арилокси, арилалкил или арилалкокси и R24 - атом водорода или алкил,
кратчайшее расстояние между остатком F и расположенным на максимальном расстоянии от остатка F атомом азота группы A-B- составляет по крайней мере 11 связей,
третий из остатков Ra - Rd означает атом водорода, алкоксил, который не может быть связан с атомом азота, алкил, трифторметил, арил, арилалкил, тиенил, тиазолил, пиридил, пиримидил, пиразинил или пиридазинил и
четвертый из остатков Ra - Rd означает атом водорода или алкил,
причем, если ничего другого не упомянуто,
под вышеуказанным термином "арил" следует понимать фенил, который может быть монозамещен остатком R25, моно-, ди- или тризамещен остатком R26 или монозамещен остатком R25 и дополнительно моно- или дизамещен остатком R26, причем заместители могут быть одинаковыми или различными, при этом R25 означает цианогруппу, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, алкилкарбонил, алкилсульфенил, алкилсульфинил, алкилсульфонил или трифторметил, R26 - алкил, гидроксил или алкоксил, атом фтора, хлора или брома, причем два остатка R26, если они связаны со смежными атомами углерода, могут также представлять собой алкилен с 3 - 6 атомами углерода, 1,3-бутадиен-1,4-диилен или метилендиокси-группу,
под вышеуказанным термином "арилен" следует понимать фенилен, который может быть монозамещен остатком R25, моно- или дизамещен остатком R26 или монозамещен остатком R25 и дополнительно монозамещен остатком R26, причем заместители могут быть одинаковыми или различными и имеют вышеуказанные значения,
а также, если ничего другого не упомянуто, вышеуказанные алкильные, алкиленовые или алкоксильные группы могут содержать 1 - 4 атома углерода и каждый из атомов углерода в вышеуказанных алкиленовых и циклоалкиленовых группах связан, как максимум, с одним гетероатомом,
смесь их изомеров или отдельные изомеры или их соли,
в частности соединения общей формулы (I), у которых
X - карбиминогруппа, незамещенная или замещенная у атома азота цианогруппой, карбонил или сульфонил,
Y - незамещенная или замещенная Rс или Rc и Rd группа -CH2CH2-, -CH2CH2CH2-, -CH=CH-, -CH2CO- или -COCH2-, незамещенная или замещенная Rc или Rd группа -CO-NH-, -NH-CO-, -CH=N- или -N=CH-,
первый из остатков Ra - Rd означает группу A-B-, в которой
A - группа формул
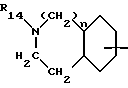
или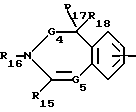
где бензоостаток может быть заменен атомом фтора, хлора или брома, алкилом, цианогруппой, трифторметилом, гидроксилом или алкоксилом или 1 - 3 метиновые группы могут быть заменены атомом азота,
G1 - связь или метилен, который может быть моно- или дизамещен алкилом, причем заместители могут быть одинаковыми или различными,
G2 - связь или метилен, замещенный остатками R7 и R8,
G3 - метилен, замещенный остатками R9 и R10,
G4 - связь,
G5 - атом азота или метин, незамещенный или замещенный алкилом,
R2 - атом водорода или алкил,
R3 - атом водорода или алкил,
R4 - атом водорода, циклоалкил с 3 - 7 атомами углерода, циклоалкилалкил с 3 - 7 атомами углерода в циклоалкильной части, алкил с 1 - 6 атомами углерода, алкенил с 3 - 6 атомами углерода, который не может быть связан с атомом азота через винильную группу, гидроксиалкил, алкоксиалкил, карбоксиалкил, алкоксикарбонилалкил, аминокарбонилалкил, N-алкиламинокарбонилалкил, N, N-диалкиламинокарбонилалкил, арилалкил, алкоксикарбонил, арилметилоксикарбонил, формил, ацетил, трифторацетил или группа R11CO-O-(R12CR13)-O-CO-, где R11 - алкил, R12 - атом водорода или алкил и R13 - атом водорода, или R4 вместе с R3 означают неразветвленный алкилен с 2 или 3 атомами углерода,
R5 - атом водорода или алкил или же R4 вместе с R5 означают дополнительную связь, если G1 означает связь,
R6 - атом водорода или алкил или амино, если G1 означает связь и R4 вместе с R5 означают дополнительную связь,
R7 - атом водорода или алкил,
R8 - атом водорода или алкил или R8 вместе с R4 означают неразветвленный алкилен с 3 или 4 атомами углерода,
R9 - атом водорода или алкил,
R10 - атом водорода или алкил или R10 вместе с R4 означают неразветвленный алкилен с 3 или 4 атомами углерода,
R14 - атом водорода или алкил,
R15 - атом водорода или алкил,
R16 - атом водорода или алкил,
R17 - атом водорода или алкил или R16 вместе с R17 означают дополнительную связь,
R18 - атом водорода, алкил или же атом хлора или амино, если R16 и R17 вместе означают дополнительную связь,
n - число 1 или 2,
В - связь, алкилен с 1 - 6 атомами углерода, арилен, замещенный одной или двумя алкильными группами пиридинилен, пиримидинилен, пиразинилен или пиридазинилен, незамещенный или замещенный одной или двумя алкильными группами циклогексилен, незамещенный или замещенный одной или двумя алкильными группами пиперидинилен, в котором одна смежная с атомом азота метиленовая группа может быть заменена карбонилом,
второй из остатков Ra - Rd означает группу формулы
F - E - D -,
где алкилен, арилен, замещенный одной или двумя алкильными группами пиридинилен, пиримидинилен, пиразинилен или пиридазинилен, инданилен, нафтилен, 1,2,3,4-тетрагидронафтилен или бензосуберанилен, в которых одно из колец связано с остатком E, а другое - с циклическим остатком общей формулы (I), незамещенный или замещенный одной или двумя алкильными группами циклоалкилен с 4 - 7 атомами углерода, циклоалкилен с 5 - 7 атомами углерода, незамещенный или замещенный одной или двумя алкильными группами, в котором одна группа 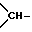 заменена атомом азота, причем, кроме того, в указанных 5- до 7-членных кольцах одна смежная с атомом азота метиленовая группа может быть заменена карбонилом, или алкиленкарбонил, если E - циклическая иминогруппа, причем карбонил связан с атомом азота циклической иминогруппы группы E, или же связь, если E не означает связь,
заменена атомом азота, причем, кроме того, в указанных 5- до 7-членных кольцах одна смежная с атомом азота метиленовая группа может быть заменена карбонилом, или алкиленкарбонил, если E - циклическая иминогруппа, причем карбонил связан с атомом азота циклической иминогруппы группы E, или же связь, если E не означает связь,
E - связь, алкилен, который может быть замещен алкильной группой с 1 - 6 атомами углерода, аминогруппой, арилом, алкиламиногруппой, диалкиламиногруппой, группой HNR21- или N-алкил-NR21-, где R21 означает алкилкарбонил или алкилсульфонил с 1 - 6 атомами углерода в алкильной части, алкилоксикарбонил с общим числом атомов углерода 2 - 5, циклоалкилкарбонил или циклоалкилсульфонил с 5 - 7 атомами углерода в циклоалкильной части, арилалкилкарбонил, арилалкилсульфонил, арилалкоксикарбонил, арилкарбонил или арилсульфонил, алкенилен с 2 - 4 атомами углерода, арилен, незамещенный или замещенный одной или двумя алкильными группами пиридинилен, пиримидинилен, пиразинилен или пиридазинилен, незамещенный или замещенный одной или двумя алкильными группами циклоалкилен с 5 - 7 атомами углерода, в котором одна группа 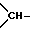 заменена атомом азота, связанным с атомом углерода остатка D, циклоалкилен с 4 - 7 атомами углерода, незамещенный или замещенный одной или двумя алкильными группами, связанный с остатком D через остаток W алкилен, в котором W означает атом кислорода или серы, сульфинил, сульфонил, группу -NR20-CO- или -CO-NR20-, где R20 означает атом водорода или алкил, при этом алкилен может быть дополнительно замещен алкильной группой с 1 - 6 атомами углерода, аминогруппой, арилом, алкиламиногруппой, диалкиламиногруппой, группой -HNR21- или N-алкил-NR21, где R21 имеет вышеуказанное значение, причем гетероатом дополнительного заместителя отделен от гетероатома остатка W по крайней мере двумя атомами углерода, если D не означает связь,
заменена атомом азота, связанным с атомом углерода остатка D, циклоалкилен с 4 - 7 атомами углерода, незамещенный или замещенный одной или двумя алкильными группами, связанный с остатком D через остаток W алкилен, в котором W означает атом кислорода или серы, сульфинил, сульфонил, группу -NR20-CO- или -CO-NR20-, где R20 означает атом водорода или алкил, при этом алкилен может быть дополнительно замещен алкильной группой с 1 - 6 атомами углерода, аминогруппой, арилом, алкиламиногруппой, диалкиламиногруппой, группой -HNR21- или N-алкил-NR21, где R21 имеет вышеуказанное значение, причем гетероатом дополнительного заместителя отделен от гетероатома остатка W по крайней мере двумя атомами углерода, если D не означает связь,
F - карбонил, замещенный гидроксилом, алкоксилом, арилалкоксигруппой или группой R22O-, где R22 означает циклоалкил с 5 - 7 атомами углерода или циклоалкилалкил с 5 - 7 атомами углерода в циклоалкильной части, группа R23CO-O-CHR24-O-CO-, где R23 означает алкил, алкоксил, циклоалкил с 5 - 7 атомами углерода, циклоалкоксил с 5 - 7 атомами углерода в циклоалкильной части и R24 - атом водорода или алкил, фосфоно или O-алкилфосфоно,
кратчайшее расстояние между остатком F и расположенным на максимальном расстоянии от остатка F атомом азота группы A-B- составляет по крайней мере 11 связей,
третий из остатков Ra - Rd означает атом водорода, алкоксил, который не может быть связан с атомом азота, алкил, трифторметил или арил, и
четвертый из остатков Ra - Rd означает атом водорода или алкил,
причем, если ничего другого не упомянуто,
под вышеуказанным термином "арил" следует понимать фенил, который может быть монозамещен остатком R25, моно-, ди- или тризамещен остатком R26 или монозамещен остатком R25 и дополнительно моно- или дизамещен остатком R26, причем заместители могут быть одинаковыми или различными, при этом R25 означает циано, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, алкилкарбонил, алкилсульфенил, алкилсульфинил, алкилсульфонил или трифторметил, R26 - алкил, гидроксил или алкоксил, атом фтора, хлора или брома, причем два остатка R26, если они связаны со смежными атомами углерода, могут также представлять собой неразветвленный алкилен с 3 или 4 атомами углерода, 1,3-бутадиен-1,4-диилен или метилендиокси-группу,
под вышеуказанным термином "арилен" следует понимать фенилен, который может быть монозамещен остатком R25, моно- или дизамещен остатком R26 или монозамещен остатком R25 и дополнительно монозамещен остатком R26, причем заместители могут быть одинаковыми или различными и имеют вышеуказанные значения,
а также, если ничего другого не упомянуто, вышеуказанные алкильные, алкиленовые или алкоксильные группы могут содержать 1 - 4 атома углерода и каждый из атомов углерода в вышеуказанных алкиленовых и циклоалкиленовых группах связан, как максимум, с одним гетероатомом,
смеси их изомеров или отдельные изомеры или их соли.
Особо предпочитаемыми соединениями обшей формулы (I) являются те, у которых
X - карбонил или сульфонил,
Y - группа -CH2CH2-, -CH2CH2CH2-, -CH=CH-, -CH2CO- или -COCH2-, незамещенная или замещенная одной или двумя метиленовыми группами, незамещенная или замещенная Rc группа -CO-NH-, -CH=N- или -N=CH-,
первый из остатков Ra - Rc означает группу A-B-, в которой
A - группа формул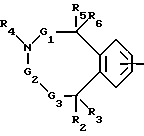

или
где в бензоостатке одна или две метиновые группы могут быть заменены атомом азота,
G1 - связь или метилен,
G2 - связь,
G3 - метилен,
G4 - связь,
G5 - атом азота или метин,
R2 - атом водорода,
R3 - атом водорода,
R4 - атом водорода, циклопропил или циклопропилметил, алкил с 1 - 6 атомами углерода, аллил, гидроксиалкил, карбоксиалкил, алкоксикарбонилалкил или бензил,
R5 - атом водорода,
R6 - атом водорода,
R14 - атом водорода или алкил,
R15 - атом водорода или алкил,
R16 - атом водорода или алкил,
R17 - атом водорода или R16 вместе с R17 означают дополнительную связь,
R18 - атом водорода или же амино, если R16 и R17 вместе означают дополнительную связь,
n - число 1 или 2,
В - связь или фенилен,
второй из остатков Ra - Rc означает группу формулы
F - E - D-,
где D - алкилен, фенилен, циклогексилен или пиперидинилен, где кольцевой атом азота связан с незамещенным или замещенным неразветвленным алкиленом остатка E, или связь,
E - неразветвленный алкилен, который может быть замещен алкилом или фенилом, алкенилен с 2 - 4 атомами углерода, фенилен, или же неразветвленный O-алкилен, связанный с остатком D через атом кислорода, если D не означает связь,
F - карбонил, замещенный гидроксилом или алкоксилом,
кратчайшее расстояние между остатком F и расположенным на максимальном расстоянии от остатка F атомом азота группы A-B- составляет по крайней мере 11 связей,
третий из остатков Ra - Rc означает атом водорода, алкоксил, который не может быть связан с атомом азота, алкил или фенил,
причем, если ничего другого не упомянуто, вышеуказанные алкильные, алкиленовые или алкоксильные группы могут содержать 1 - 4 атома углерода и каждый из атомов углерода в вышеуказанных алкиленовых и циклоалкиленовых группах связан, как максимум, с одним гетероатомом,
смеси их изомеров или отдельные изомеры или их соли.
Особо предпочитаемыми соединениями общей формулы (I) являются те, у которых
X - карбонил,
Y - группа -CH2CH2-, -CH2CH2CH2-, -CH=CH-, -CH2CO- или -COCH2- или незамещенная или замещенная метилом группа -N=CH-,
остаток Ra означает группу A-B-, в которой
A - группа формул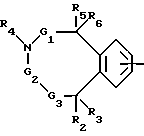
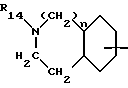
или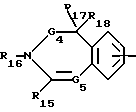
где в бензоостатке одна или две метиновые группы могут быть заменены атомом азота,
G1 - связь или метилен,
G2 - связь,
G3 - метилен,
G4 - связь,
G5 - метин,
R2 - атом водорода,
R3 - атом водорода,
R4 - атом водорода, алкил с 1 - 4 атомами углерода, аллил или бензил,
R5 - атом водорода,
R6 - атом водорода,
R14 - атом водорода или метил,
R15 - атом водорода,
R16 вместе с R17 - связь,
R18 - атом водорода или амино,
n - число 1,
B - связь,
остаток Rb означает группу формулы
F - E - D-,
где D - группа -CH2CH2-, 1,4-фенилен или 1,4-циклогексилен,
E - незамещенная или замещенная метилом группа -CH2CH2-, группа -CH=CH-, 1,4-фенилен или группа -O-CH2, где атом кислорода группы -O-CH2- связан с остатком D,
F - карбонил, замещенный гидроксилом или алкоксилом с 1 - 4 атомами углерода,
кратчайшее расстояние между остатком F и расположенным на максимальном расстоянии от остатка F атомом азота группы A-B- составляет по крайней мере 11 связей,
смеси их изомеров или отдельные изомеры или их соли.
В качестве особо предпочитаемых соединений можно назвать, например, следующие:
(а) 1-[4-[2-(метоксикарбонил)этил] фенил] -3-(1,2,3,4- тетрагидроизохинолин-6-ил)-имидазолидин-2-он,
(б) 1-[4-(2-карбоксиэтил)фенил] -3-(1,2,3,4- тетрагидроизохинолин-6-ил)-имидазолидин-2-он,
(в) 1-[4-(2-карбоксиэтил)фенил] -3-(2-метил-1,2,3,4- тетрагидроизохинолин-6-ил)-имидазолидин-2-он,
(г) 1-[4-(2-изобутилоксикарбонил)этил]фенил]-3-(1,2,3,4- тетрагидроизохинолин-6-ил)-имидазолидин-2-он,
(д) 1-[4-(2-карбоксиэтил)фенил] -3-(2,3,4,5-тетрагидро-1Н-3- бензацепин-7-ил)-имидазолидин-2-он,
(е) 1-[4-(2-метоксикарбонил)этил]фенил]-3-(2,3,4,5-тетрагидро- 1Н-3-бензацепин-7-ил)-имидазолидин-2-он,
(ж) 1-[4-(2-изопропилоксикарбонил)этил] фенил]-3- (2,3,4,5-гетрагидро-1H-3-бензацепин-7-ил)-имидазолидин-2-он,
(з) 1-[4-(2-карбоксиэтил)фенил] -3-(3-метил-2,3,4,5-тетрагидро- 1Н-3-бензацепин-7-ил)-имидазолидин-2-он,
(и) 4-[4-(2-карбоксиэтил)фенил] -5-метил-2-(2,3,4,5-тетрагидро- 1Н-3-бензацепин-7-ил)-4Н-1,2,4-триазол-3-он,
(й) 1-[транс-4-(2-карбоксиэтил)циклогексил]-3- (2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-имидазолидин-2-он,
(к) 1-[4-(2-метоксикарбонил)этил] фенил] -3-(3-метил- 2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-имидазолидин-2-он,
(л) 1-[4-[2-(этоксикарбонил)этил] фенил] -3-(3-метил- 2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-имидазолидин-2-он,
(м) 1-[4-[2-(изопропилоксикарбонил)этил]фенил]-3-(3-метил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-он,
(н) 1-[транс-4-(2-карбоксиэтил)циклогексил] -3-(3-метил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-он,
(о) 1-[транс-4-[2-(изопропилоксикарбонил)этил] циклогексил] -3-(3- метил-2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-имидазолидин-2-он,
(п) 1-[транс-4-[2-(этоксикарбонил)этил] циклогексил] -3-(3-метил- 2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-имидазолидин-2-он,
(р) 1-[транс-4-(2-(метоксикарбонил)этил] циклогексил] -3-(3-метил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-он,
(с) 1-[транс-4-[(карбоксиметил)окси] циклогексил]-3-(3-метил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-он,
(т) 3-[транс-4-(2-карбоксиэтил)циклогексил] -1-(3-метил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-гидантоин
(у) 1-[транс-4-(2-карбоксиэтил)циклогексил]-3-(3-этил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-он,
их таутомеры и их соли.
Новые соединения общей формулы (I) можно получать, например, по нижеследующим способам:
а) Для получения соединений общей формулы (I), в которой F означает карбоксил,
соединение обшей формулы (II)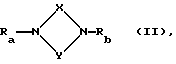
в которой Ra, Rb, X и Y имеют вышеуказанные значения при условии, что один из остатков Ra - Rd означает группу F'-E-D-, где E и D имеют вышеуказанные значения и F' означает группу, переводимую в карбоксильную группу путем гидролиза, обработки кислотами, термолиза или гидрогенолиза,
переводят в соединение общей формулы (I), в которой F означает карбоксильную группу.
Функциональные производные карбоксильной группы, например, ее незамещенные или замещенные амиды, сложные эфиры, сложные тиоэфиры, сложные триметилсилиловые эфиры, сложные ортоэфиры, сложные иминоэфиры, амидины или ангидриды, или нитрил можно переводить в карбоксильную группу путем гидролиза, сложные эфиры с третичными спиртами, например, трет.бутиловый эфир можно переводить в карбоксильную группу путем обработки кислотой или путем термолиза, и сложные эфиры с аралканолами, например, сложный бензиловый эфир можно переводить в карбоксильную группу путем гидрогенолиза.
Гидролиз целесообразно осуществляют или в присутствии кислоты, такой как, например, соляная кислота, серная кислота, фосфорная кислота, уксусная кислота, трихлоруксусная кислота, трифторуксусная кислота или их смесей, или в присутствии основания, такого, как, например, гидроокись лития, гидроокись натрия или гидроокись калия в среде пригодного растворителя, такого, как, например, вода, смесь воды и метанола, смесь воды и этанола, смесь воды и изопропанола, метанол, этанол, смесь воды и тетрагидрофурана или смесь воды и диоксана при температурах между -10 и 120oC, например при температурах между комнатной температурой и температурой кипения реакционной смеси.
В указанных условиях реакции возможно имеющиеся N-ациламино- или N-ациламиногруппы, например N-трифторацетилиминогруппу, можно переводить в соответствующие амино- или иминогруппы. Кроме того, при обработке органической кислотой, такой, как, например, трихлоруксусная кислота или трифторуксусная кислота, возможно имеющиеся спиртовые гидроксильные группы можно одновременно переводить в соответствующую ацилоксигруппу как, например, трифторацетоксигруппу.
В том случае, если в соединении формулы (II) F' означает цианогруппу или аминокарбонил, то данные группы можно переводить в карбоксильную группу нитритом, например, нитритом натрия, в присутствии кислоты, такой, как, например, серная кислота, причем целесообразно данную кислоту одновременно используют в качестве растворителя, при этом реакцию осуществляют при температурах между 0 и 50oC.
В том случае, если в соединении формулы (II) F' означает, например, трет. бутилоксикарбонил, то трет.бутил можно снимать путем обработки кислотой, такой, как, например, трифторуксусная кислота, муравьиная кислота, п-толуолсульфокислота, серная кислота, соляная кислота, фосфорная кислота или полифосфорная кислота, в случае необходимости в среде инертного растворителя, такого, как, например, метиленхлорид, хлороформ, бензол, толуол, диэтиловый эфир, тетрагидрофуран или диоксан, предпочтительно при температурах между -10 и 120oC, например при температурах между 0 и 60oC, или же путем термообработки, в случае необходимости, в среде инертного растворителя, такого, как, например, метиленхлорид, хлороформ, бензол, толуол, тетрагидрофуран или диоксан, и предпочтительно в присутствии каталитического количества кислоты, такой, как, например, п-толуолсульфокислота, серная кислота, фосфорная кислота или полифосфорная кислота, предпочтительно при температуре кипения используемого растворителя, например, при температурах между 40 и 120oC. В указанных условиях реакции возможно имеющиеся N-трет.бутилоксикарбониламино- или N-трет. бутилоксикарбонилиминогруппы можно переводить в соответствующие амино- или иминогруппы.
В том случае, если в соединении формулы (II) F' означает, например, бензилоксикарбонил, то бензил можно отщеплять и путем гидрогенолиза в присутствии катализатора гидрирования, например, палладия на угле, в среде пригодного растворителя, такого, как, например, метанол, этанол, смесь этанола и воды, ледяная уксусная кислота, сложный этиловый эфир уксусной кислоты, диоксан или диметилформамид, предпочтительно при температурах между 0 и 50oC, например при комнатной температуре, и при давлении водорода 1 - 5 бар. При гидрогенолизе можно одновременно переводить другие остатки, например, нитрогруппу в аминогруппу, бензилоксигруппу в гидроксильную группу и N-бензиламино-, N-бензилимино-, N-бензилоксикарбониламино- или N-бензилоксикарбонилиминогруппы в соответствующую амино- или иминогруппу.
б) Для получения соединений общей формулы (I), где R16 и R17 вместе означают дополнительную связь, G4 - связь и по крайней мере один из остатков R15 или R18 - гидроксил, метоксил, аминогруппу, алкиламиногруппу или диалкиламиногруппу с 1 - 4 атомами углерода в алкильной части:
Соединение общей формулы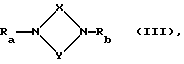
где Ra, Rb X и Y имеют вышеуказанные значения при условии, что один из остатков Ra - Rd означает группу A-B-, где B имеет вышеуказанное значение и A означает группу формулы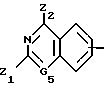
где бензоостаток и G5 имеют вышеуказанные значения, Z1 и Z2, которые могут быть одинаковыми или различными, означают нуклеофильную удаляемую группу, такую, как, например, атом галогена, например атом хлора или брома, при этом, однако остаток Z1 может иметь вышеуказанные для R15 или остаток Z2 указанные для R18 значения,
подвергают взаимодействию с соединением общей формулы
H - R27 (IV)
где R27 означает гидроксил, метоксил, аминогруппу, формиламиногруппу, ацетиламиногруппу, алкиламиногруппу или диалкиламиногруппу с 1 - 4 атомами углерода в алкильной части.
Взаимодействие целесообразно осуществляют в среде растворителя, такого, как, например, вода, ацетон, этанол, тетрагидрофуран, диоксан, диметилформамид или диметилсульфоксид, в случае необходимости, однако в избытке применяемого соединения общей формулы (IV) в качестве растворителя и, в случае необходимости, в присутствии основания, такого, как, например, гидроокись натрия, гидроокись калия, карбонат калия, амид натрия или гидрид натрия, при температурах между 0 и 250oC, предпочтительно, однако при температурах между 50 и 225oC.
в) Для получения соединений общей формулы (I), где R16 и R17 вместе означают дополнительную связь, G4 - связь и R18 - атом хлора или брома:
Взаимодействие соединения общей формулы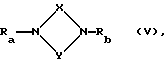
где Ra, Rb, X и Y имеют вышеуказанные значения при условии, что один из остатков Ra - Rd означает группу A-B-, где B имеет вышеуказанное значение и A означает группу формулы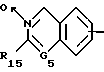
где бензоостаток и G5 имеют вышеуказанные значения и R15, означает атом водорода или вышеуказанные для R15 алкильные или арильные группы, галоидангидридом кислоты.
В качестве галоидангидрида кислоты применяют, например, фосфороксихлорид или фосфороксибромид, и реакцию можно осуществлять в присутствии растворителя, такого, как, например, бензол, дихлорбензол, нитробензол, четыреххлористый углерод и, в случае необходимости, в присутствии соли соответствующей галогенводородной кислоты, такой, как, например, хлорид натрия или бромид натрия, при повышенных температурах, например, при температурах между 50 и 250oC, предпочтительно, однако, при температуре кипения реакционной смеси.
г) Для получения соединений общей формулы (I), где X означает замещенную цианогруппой карбиминогруппу, карбонил или сульфонил и Y - незамещенный или замещенный Rc или Rd или Rc и Rd неразветвленный алкилен с 2 - 4 атомами углерода:
Циклизация соединения общей формулы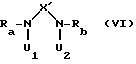
где Ra и Rb имеют вышеуказанные значения, X' означает замещенную цианогруппой карбиминогруппу, карбонил или сульфонил, один из остатков U1 или U2 - атом водорода и другой из остатков U1 или U2 незамещенный или замещенный Rс или Rd или Rс и Rd неразветвленный алкилен с 2 - 4 атомами углерода, который в конце дополнительно связан с нуклеофильной удаляемой группой, такой, как атом галогена, например, атом хлора, брома или йода, гидроксил или сложный эфир сульфокислоты, например, метансульфонилокси или п-толуолсульфонилокси.
Взаимодействие предпочтительно осуществляют в среде растворителя, такого, как, например, метиленхлорид, ацетонитрил, тетрагидрофуран, толуол, диметилформамид или диметилсульфоксид, в случае необходимости в присутствии основания, такого, как, например, гидрид натрия, карбонат калия, трет.бутилат калия или N-этилдиизопропиламин или, в случае необходимости, в присутствии обезвоживающего агента, такого как смеси трифенилфосфина и сложного диэтилового эфира азодикарбоновой кислоты при температурах между -20 и 100oC, предпочтительно при температурах между 0 и 60oC.
д) Для получения соединений общей формулы (I), где X означает карбонил, a Y одну из вышеуказанных алкиленовых или алкениленовых групп.
Взаимодействие соединения общей формулы
R28 - NH - T (VII)
с изоцианатом обшей формулы
O = C = N - R29 (VII)
где один из остатков R28 или R29 имеет указанные для Ra значения и другой из остатков R28 или R29 имеет вышеуказанные для Rb значения и Т означает незамещенную или замещенную в алкилиденовой части Rc или Rd или Rc и Rd группу формулы
-(CH2)m-HC(OR30)2,
где m означает число 1, 2 или 3 и R30 - алкил с 1 - 4 атомами углерода,
с последующим, в случае необходимости, гидрированием.
Взаимодействие можно осуществлять в среде инертного растворителя как диоксана или толуола при температурах между 20 и 200oC, предпочтительно при температурах между 20 и 160oC.
Мочевина с открытой цепью, возможно полученная в качестве промежуточного продукта в результате взаимодействия соединения общей формулы (VII) с изоцианатом общей формулы (VIII), переводят потом в желаемое соединение, в случае необходимости в присутствии кислоты, такой, как, например, уксусная кислота, трифторуксусная кислота, п-толуолсульфоновая кислота или соляная кислота, в случае необходимости в среде растворителя, такого, как, например, метанол, этанол, тетрагидрофуран или метиленхлорид, при температурах между 0oC и температурой кипения реакционной смеси.
Последующее, в случае необходимости, гидрирование предпочтительно осуществляют водородом в присутствии катализатора, такого, как, например, палладия на угле или платина, в среде растворителя, такого, как, например, метанол, этанол, сложный этиловый эфир уксусной кислоты или ледяная уксусная кислота, в случае необходимости с добавкой кислоты, такой как соляной, при температурах между 0 и 100oC, предпочтительно, однако при температурах между комнатной температурой и 50oC и давлении водорода 1 - 7 бар, предпочтительно, однако 3 - 5 бар.
е) Для получения соединений общей формулы (I), в которой G1 и G2 означают связь, G3 - метилен, незамещенный или замещенный алкилом с 1 - 4 атомами углерода, R2, R4 и R5 атом водорода, R3 и R6, которые могут быть одинаковыми или различными, - атом водорода или алкил с 1 - 4 атомами углерода:
Гидрирование соединения общей формулы
где Ra, Rb, X и Y имеют вышеуказанные значения при условии, что один из остатков Ra - Rd означает группу A-B-, где B имеет вышеуказанное значение и A означает группу формулы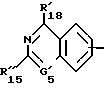
где бензоостаток имеет вышеуказанное значение, 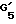 означает метин, незамещенный или замещенный алкилом с 1 - 4 атомами углерода,
означает метин, незамещенный или замещенный алкилом с 1 - 4 атомами углерода, 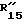 и
и  которые могут быть одинаковыми или различными, означают атом водорода или алкил с 1 - 4 атомами углерода.
которые могут быть одинаковыми или различными, означают атом водорода или алкил с 1 - 4 атомами углерода.
Гидрирование предпочтительно осуществляют в среде подходящего растворителя, такого, как, например, метанол, смесь метанола и воды, уксусная кислота, этилацетат, этанол, диэтиловый эфир, тетрагидрофуран, диоксан или диметилформамид с водородом в присутствии катализатора гидрирования, такого, как, например, никель Ренея, платина, двуокись платины, родия или палладия на угле, в случае необходимости с добавкой кислоты, такой как соляной, при температурах между 0 и 100oC, предпочтительно при температурах между 20 и 80oC. При этом имеющиеся, в случае необходимости, в соединении общей формулы (IX) незамещенные или замещенные алкениленовые группы можно переводить в незамещенные или замещенные алкиленовые группы.
(ж) Для получения соединений общей формулы (I), где F означает алкоксил с 1 - 6 атомами углерода, арилалкоксил с 1 - 4 атомами углерода в алкоксильной части, при этом арильная часть имеет вышеуказанное значение, или карбонил, замещенный группой R22O-.
Взаимодействие соединения общей формулы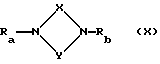
где Ra, Rb, X и Y имеют вышеуказанные значения при условии, что один из остатков Ra - Rd означает группу F''-E-D-, где E и D имеют вышеуказанные значения и F'' означает карбоксил или алкоксикарбонил,
со спиртом общей формулы
HO - R31, (XI)
где R31 имеет вышеуказанные для R22 значения, а также означает алкил с 1 - 6 атомами углерода или арилалкил, в котором арильная часть имеет вышеуказанное значение и алкильная часть может содержать 1 - 4 атома углерода.
Взаимодействие карбоксильного соединения со спиртом осуществляют, в случае необходимости, в среде растворителя или смеси растворителей, такого, как, например, метиленхлорид, диметилформамид, бензол, толуол, хлорбензол, тетрагидрофуран, смесь бензола и тетрагидрофурана или диоксан или, особо предпочтительно, в соответствующем спирте общей формулы (XI), в случае необходимости в присутствии кислоты как соляной кислоты или в присутствии обезвоживающего агента, такого, как, например, сложный изобутиловый эфир хлормуравьиной кислоты, сложный тетраэтиловый эфир ортоугольной кислоты, сложный триметиловый эфир ортоуксусной кислоты, 2,2-диметоксипропан, тетраметоксисилан, тионилхлорид, триметилхлорсилан, серная кислота, метансульфокислота, п-толуолсульфокислота, трихлорид фосфора, фосфорный ангидрид, N,N'-дициклогексилкарбодиимид, смесь N,N'-дициклогексилкарбодиимида и N-тидроксисукцинимида, смесь N,N'-дициклогексилкарбодиимида и 1-гидрокси-бензтриазола, N, N'-карбонилдиимидазол или смесь трифенилфосфина и четыреххлористого углерода, и, в случае необходимости, с добавкой основания, такого, как, например, пиридин, 4-диметиламинопиридин или триэтиламин, целесообразно при температурах между 0 и 150oC, предпочтительно при температурах между 0 и 100oC.
Взаимодействие соответствующего алкоксикарбонильного соединения со спиртом общей формулы (XI) предпочтительно осуществляют в среде соответствующего спирта в качестве растворителя, в случае необходимости в присутствии дополнительного растворителя, такого, как, например, метиленхлорид или диэтиловый эфир, предпочтительно в присутствии кислоты, такой как соляной, при температурах между 0 и 150oC, предпочтительно при температурах между 50 и 100oC.
(з) Для получения соединений общей формулы (I), где один из остатков R4, R14 или R16 означает незамещенные или замещенные алкил, алкенил, циклоалкил, циклоалкилалкил или аралкил.
Взаимодействие соединения общей формулы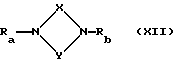
где Ra, Rb, X и Y имеют вышеуказанные значения при условии, что один из остатков Ra - Rd означает группу A-B-, где A и B имеют вышеуказанные значения при условии, что R4, R14 и R16 означают атом водорода,
с соединением общей формулы
Z3 - R32 (XIII)
где R32 означает алкил с 1 - 8 атомами углерода, циклоалкил или циклоалкилалкил, в которых циклоалкильная часть может содержать 3 - 7 атомов углерода, а алкильная часть - 1 - 4 атома углерода, алкениловая группа с 3 - 8 атомами углерода, арилалкил, гидроксиалкил, алкоксиалкил, цианоалкил, карбоксиалкил, алкоксикарбонилалкил, аминокарбонилалкил, N-алкиламинокарбонилалкил или N, N-диaлкилaминoкapбонил, в которых арильная часть и алкильные части имеют вышеуказанные значения, и Z3 означает нуклеофильную удаляемую группу как атом галогена, например, атом хлора, брома или йода, или сложный эфир сульфокислоты, такую, как, например, метансульфонилоксигруппа или п-толуолсульфонилоксигруппа, или Z3 вместе со смежным атомом водорода остатка R32 означают атом кислорода.
Алкилирование соединением формулы (XIII), где Z3 означает нуклеофильную удаляемую группу, целесообразно осуществляют в среде растворителя, такого, как, например, метиленхлорид, тетрагидрофуран, диоксан, диметилсульфоксид или диметилформамид, в случае необходимости в присутствии основания, такого, как, например, карбонат натрия, карбонат калия или натровый щелок или в присутствии третичного органического основания, такого, как, например, N-этил-диизопропиламин или N-метил-морфолин, которые могут одновременно служить в качестве растворителя, при температурах между -30 и 150oC, предпочтительно, однако при температурах между 20 и 120oC.
Восстановительное алкилирование карбонильным соединением обшей формулы (XIII) осуществляют в присутствии комплексного гидрида металла, такого, как, например, боргидрид натрия, боргидрид лития или циановый боргидрид натрия, целесообразно при значении pH 6 - 7 и комнатной температуре или в присутствии катализатора гидрирования, например водорода в присутствии палладия на угле, при давлении водорода 1 - 5 бар. Метилирование, однако, предпочтительно осуществляют в присутствии муравьиной кислоты в качестве восстановителя при повышенных температурах, например при температурах между 60 и 120oC.
(и) Для получения соединений общей формулы (I), в которой X означает карбиминогруппу, замещенную у атома азота цианогруппой, карбонил или сульфонил:
Взаимодействие соединения общей формулы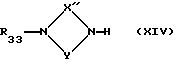
с соединением общей формулы
Z4 - R34 (XV)
где Y имеет вышеуказанное значение, X'' означает карбиминогруппу, замещенную у атома азота цианогруппой, карбонил или сульфонил, один из остатков R33 или R34 имеет вышеуказанные для Ra значения и другой из остатков R33 или R34 имеет вышеуказанные для Rb значения, a Z4 означает нуклеофильную удаляемую группу как атом галогена, гидроксил или сложный эфир сульфокислоты, например, атом фтора, хлора, брома или йода, метансульфонилоксигруппу или п-толуолсульфонилоксигруппу.
Взаимодействие предпочтительно осуществляют в среде растворителя, такого, как, например, метиленхлорид, ацетонитрил, тетрагидрофуран, толуол, пиримидин, диметилформамид, диметилсульфоксид или N-метил-пирролидон, в случае необходимости в присутствии одного или нескольких оснований, таких, как, например, гидрид натрия, карбонат калия, трет.бутилат калия, N-этил-диизопропиламин, трис-[2-(2-метоксиэтокси)этил] амин или N,N,N',N'-тетраметилэтилендиамин и, в случае необходимости, в присутствии обезвоживающего агента как смеси трифенилфосфина и сложного диэтилового эфира азодикарбоновой кислоты и, в случае необходимости, в присутствии порошковой меди или одной или нескольких солей меди как йодида меди (I) в качестве ускорителя реакции при температурах между -20 и 250oC, предпочтительно, однако при температурах между 0 и 60oC, если Z4 связан с алифатическим атомом углерода, или при температурах между 60 и 180oC, если Z4 связан с ароматическим атомом углерода, причем в данном случае Z4 может означать лишь атом галогена.
(й) Для получения соединений общей формулы (I), в которой R4 или R14 означают алкоксикарбонил, арилметилоксикарбонил, формил, ацетил, трифторацетил, аллилоксикарбонил или группу R11CO-O-(R12CR13)-O-CO-, в которой R11 - R13 и арильная часть имеют вышеуказанные значения и алкоксильная часть может содержать 1 - 4 атома углерода:
Взаимодействие соединения общей формулы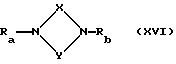
где Ra, Rb, X и Y имеют вышеуказанные значения при условии, что R4 или R14 означает атом водорода,
с соединением общей формулы
Z5 - R35 (XVII)
где R35 означает алкоксикарбонил с общим числом атомов углерода 2-5, арилметилоксикарбонил, в котором арильная часть имеет вышеуказанное значение, формил, ацетил, аллилоксикарбонил, группу R11CO-O-(R12CR13)-O-CO-, где R11 - R13 имеют вышеуказанные значения, или трифторацетил, и Z5 означает нуклеофильную удаляемую группу как атом галогена, арилоксил, арилтио, алкоксил, алкоксикарбонилоксил, аралкоксикарбонилоксил или N-имидазолил, например атом хлора или брома или 4-нитро-феноксигруппу.
Ацилирование целесообразно осуществляют в среде растворителя, такого, как, например, тетрагидрофуран, метиленхлорид, хлороформ, диметилформамид, вода или смеси данных растворителей, в случае необходимости в присутствии основания, такого, как, например, карбонат натрия, карбонат калия или натровый щелок или в присутствии третичного органического основания, такого, как, например, триэтиламин, N-этил-диизопропиламин, N-метил-морфолин или пиридин, которые одновременно могут служить в качестве растворителя, при температурах между -30 и 100oC, предпочтительно, однако при температурах между -10 и 60oC.
(к) Для получения соединений общей формулы (I), в которой F означает карбонил, замещенный алкоксильной группой с 1 - 6 атомами углерода, арилалкоксильной группой, где арильная часть имеет вышеуказанное значение и алкоксильная часть может содержать 1 - 4 атома углерода, группой R22O- или R23CO-O-CHR24-O-, при этом R22 - R24 имеют вышеуказанные значения:
Взаимодействие соединения общей формулы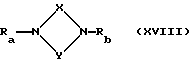
где Ra, Rb, X и Y имеют вышеуказанные значения при условии, что один из остатков Ra - Rd означает группу F'''-E-D-, в которой E и D имеют вышеуказанные значения и F''' означает карбоксил,
с соединением общей формулы
Z6 - R36, (XIX)
где R36 означает алкил с 1 - 6 атомами углерода, арилалкил, в котором арильная часть имеет вышеуказанное значение и алкильная часть может содержать 1 - 4 атома углерода, группу R22- или R23CO-O-CHR24-, где R22 - R24 имеют вышеуказанные значения, и Z6 означает нуклеофильную удаляемую группу как атом галогена или сложный эфир сульфокислоты, такой, как, например, атом хлора или брома, метансульфонилоксигруппа или п-толуолсульфонилоксигруппа.
Взаимодействие предпочтительно осуществляют в среде растворителя, такого, как, например, метиленхлорид, тетрагидрофуран, диоксан, диметилсульфоксид или диметилформамид, в случае необходимости в присутствии ускорителя реакции как йодида натрия или калия и предпочтительно в присутствии основания, такого, как, например, карбонат натрия, карбонат калия или натровый щелок или в присутствии третичного органического основания, такого, как, например, N-этил-диизопропиламин или N-метил-морфолин, которые одновременно могут также служить в качестве растворителя, или, в случае необходимости, в присутствии карбоната серебра или окиси серебра при температурах между -30 и 100oC, предпочтительно, однако при температурах между -10 и 80oC.
(л) Для получения соединений общей формулы (I), в которой X означает карбонил и Y - незамещенный или замещенный Rc или Rd или Rc и Rd неразветвленный алкилен с 2-4 атомами углерода, в котором метиленовая группа в конце заменена карбонилом:
Циклизация образовавшегося при необходимости в реакционной смеси соединения общей формулы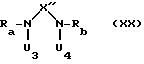
где Ra и Rb имеют вышеуказанные значения, X'' означает карбонил, один из остатков U3 или U4 - атом водорода, а другой из остатков U3 или U4 означает незамещенный или замещенный Rc или Rd или Rc и Rd неразветвленный алкилен с 2-4 атомами углерода, в котором метиленовая группа в конце заменена группой Z7-CO-, в которой Z7 означает нуклеофильную удаляемую группу как атом галогена, гидроксил, алкоксил, арилоксил или арилалкоксил, например атом хлора или брома, гидроксил, метокси, этокси, фенокси или бензилокси.
Взаимодействие предпочтительно осуществляют в среде растворителя, такого, как, например, метиленхлорид, ацетонитрил, тетрагидрофуран, толуол, диметилформамид или диметилсульфоксид, в случае необходимости в присутствии основания, такого, как, например, гидрид натрия, карбонат калия, трет.бутилат калия или N-этил-диизопропиламин или, в случае необходимости, в присутствии обезвоживающего агента, такого, как, например, смесь трифенилфосфина и сложного диэтилового эфира азодикарбоновой кислоты или N,N'-карбонилдиимидазола при температурах между -20 и 200oC, предпочтительно при температурах между 0 и 160oC.
Если согласно изобретению получают соединение общей формулы (I), содержащее ненасыщенную углерод-углеродную связь, то его можно переводить в соответствующее насыщенное соединение общей формулы (I) путем каталитического гидрирования.
Каталитическое гидрирование предпочтительно осуществляют водородом в присутствии катализатора как палладия на угле в среде растворителя, такого, как, например, метанол, этанол, сложный этиловый эфир уксусной кислоты или ледяная уксусная кислота, в случае необходимости с добавкой кислоты как соляной кислоты при температурах между 0 и 100oC, предпочтительно, однако при температурах между 20 и 60oC, при давлении водорода 1 - 7 бар, предпочтительно, однако, при 3 - 5 бар.
При вышеуказанных реакциях возможно имеющиеся реакционноспособные группы как гидроксил, карбоксил, фосфоно-, O-алкил-фосфоно-, амино-, алкиламино-, имино- или амидиногруппы во время реакции можно защищать обычными защитными группами, которые снимаются по завершении реакции.
В качестве защитного остатка для гидроксильной группы можно применять, например, триметилсилил, ацетил, бензоил, трет.бутил, тритил, бензил или тетрагидропиранил,
в качестве защитного остатка для карбоксильной группы - триметилсилил, метил, этил, трет.бутил, бензил или тетрагидропиранил,
в качестве защитного остатка для фосфоногруппы - алкил, такой, как, например, метил, этил, изопропил или н-бутил, фенил или бензил,
в качестве защитного остатка для амидиногруппы, незамещенной или замещенной алкилом, - бензилоксикарбонил, и
в качестве защитного остатка для амино-, алкиламино- или иминогруппы - формил, ацетил, трифторацетил, этоксикарбонил, трет.бутоксикарбонил, бензилоксикарбонил, бензил, метоксибензил или 2,4-диметоксибензил, для иминогруппы - дополнительно метил, а для аминогруппы - фталил.
Возможное последующее снятие использованного защитного остатка осуществляют, например, путем гидролиза в среде водного растворителя, такого, как, например, вода, смесь изопропанола и воды, смесь уксусной кислоты и воды, смесь тетрагидрофурана и воды или смеси диоксана и воды, в присутствии кислоты, такой, как, например, трифторуксусная кислота, соляная кислота или серная кислота, или в присутствии щелочного основания, такого, как, например, гидроокись натрия или калия, или путем расщепления простого эфира, например в присутствии триметилсилана йода, при температурах между 0 и 120oC, предпочтительно при температурах между 10 и 100oC.
Снятие бензилового, метоксибензилового или бензилоксикарбонилового остатка осуществляют, однако, например путем гидрогенолиза, например водородом в присутствии катализатора как палладия на угле в среде растворителя, такого, как, например, метанол, этанол, сложный этиловый эфир уксусной кислоты или ледяная уксусная кислота, в случае необходимости с добавкой кислоты как соляной кислоты при температурах между 0 и 100oC, предпочтительно, однако при температурах между 20 и 60oC, при давлении водорода 1 - 7 бар, предпочтительно, однако 3 - 5 бар. Снятие 2,4-диметоксибензилового остатка осуществляют, однако предпочтительно в среде трифторуксусной кислоты в присутствии анизола.
Снятие трет. бутилового или трет.бутилоксикарбонилового остатка осуществляют предпочтительно путем обработки кислотой, такой, как, например, трифторуксусная кислота или соляная кислота, или путем обработки триметилсиланом йода, в случае необходимости при использовании растворителя, такого, как, например, метилен-хлорид, диоксан, метанол или простой эфир.
Снятие трифторацетилового остатка предпочтительно осуществляют путем обработки кислотой, такой как соляной, в случае необходимости в присутствии растворителя, такого как, например, уксусная кислота или метанол, при температурах между 50 и 120oC или путем обработки натровым щелоком, в случае необходимости в присутствии растворителя, такого как, например, тетрагидрофуран или метанол, при температурах между 0 и 50oC.
Снятие метиловой группы с метилиминогруппы предпочтительно осуществляют в присутствии сложных 1-хлоралкильных эфиров хлормуравьиной кислоты как сложного 1-хлорэтилового эфира хлормуравьиной кислоты, предпочтительно в присутствии основания, такого как 1,8-бис-(диметиламино)-нафталина, в присутствии растворителя, такого как, например, метиленхлорид, 1,2-дихлорэтан, толуол или диоксан, при температурах между 0 и 150oC, предпочтительно при температурах между 20oC и температурой кипения реакционной смеси, и последующей обработки спиртом, таким как метанол, при температурах между 20oC и температурой кипения употребляемого спирта.
Снятие фталилового остатка предпочтительно осуществляют в присутствии гидразина или первичного амина, такого, как, например, метиламин, этиламин или н-бутиламин, в среде растворителя, такого, как, например, метанол, этанол, изопропанол, смесь толуола и воды или диоксан, при температурах между 20 и 50oC.
Снятие лишь одного алкильного остатка с O,O'-диалкилфосфоногруппы осуществляют, например, йодидом натрия в среде растворителя, такого как, например, ацетон, этилметилкетон, ацетонитрил или диметилформамид, при температурах между 40 и 150oC, предпочтительно, однако при температурах между 60 и 100oC.
Снятие обоих алкильных остатков с O,O'-диалкилфосфоногруппы осуществляют, например, йодистым триметилсиланом, бромистым триметилсиланом или смесью хлористого триметилсилана и йодида натрия в среде растворителя, такого как, например, метиленхлорид, хлороформ или ацетонитрил, при температурах между 0oC и температурой кипения реакционной смеси, предпочтительно, однако при температурах между 20 и 60oC.
Кроме того, полученные соединения общей формулы (I) можно разделять на их энантиомеры и/или диастереомеры. Так, например, смеси цис-/транс-изомеров можно разделять на отдельные цис- и транс-изомеры, а соединения по крайней мере с одним оптически активным атомом углерода - на отдельные энантиомеры.
Так, например, полученные смеси цис-/транс-изомеров можно разделять путем хроматографии на отдельные цис- и транс-изомеры, полученные соединения общей формулы (I), имеющиеся в виде рацематов, по общеизвестным методам (см. Аллингер Н. Л. и Элиел Е.Л. в "Topics in Stereochemistry", том 6, Вайли Интерсайенс, 1971) - на оптические антиподы, а соединения общей формулы (I) по крайней мере с двумя асимметричными атомами углерода на основе своих физико-химических различий по общеизвестным методам, например, путем хроматографии и/или фракционной кристаллизации - на диастереомеры, которые, если они имеются в виде рацематов, могут потом, как вышеуказано, разделять на энантиомеры.
Разделение энантиомеров предпочтительно осуществляют путем колоночной хроматографии на хиральных фазах или путем перекристаллизации из оптически активного растворителя, или путем взаимодействия с образующим с рацемическим соединением соли или производные как, например, сложные эфиры или амиды, оптически активным веществом, в частности кислотой и их активированными производными или спиртами, и путем разделения получаемой таким образом диастереомерной смеси солей или производного, например на основе различной растворимости, причем из чистых диастереомерных солей или производных можно освобождать свободные антиподы путем воздействия подходящих средств. Особо применяемыми оптически активными кислотами являются, например, D- и L-формы винной кислоты или дибензоилвинной кислоты, ди-о-толилвинная кислота, яблочная кислота, миндальная кислота, камфарная сульфокислота, глутаминовая кислота, аспарагиновая кислота или хинная кислота. В качестве оптически активного спирта можно назвать, например, (+)- или (-)-ментол, а в качестве оптически активного ацилового остатка в амидах - например (+)- или (-)-ментилоксикарбонил.
Кроме того, получаемые соединения формулы (I) могут переводить в их соли, в частности для фармацевтического применения в их физиологически переносимые соли с неорганическими или органическими кислотами. В качестве кислот можно применять такие, как, например, соляная кислота, бромистоводородная кислота, серная кислота, фосфорная кислота, фумаровая кислота, янтарная кислота, молочная кислота, лимонная кислота, винная кислота или малеиновая кислота.
Кроме того, получаемые таким образом новые соединения формулы (I), если последние содержат карбоксил, сульфо- фосфоно- O-алкил-фосфоно- или тетразол-5-ил-группу, при желании затем переводят в их соли с неорганическими или органическими основаниями, в частности для фармацевтического применения в их физиологически переносимые соли. В качестве оснований можно применять, например, гидроокись натрия, гидроокись калия, аргинин, циклогексиламин, этаноламин, диэтнол- амин и триэтаноламин.
Применяемые в качестве исходных веществ соединения отчасти известны из литературы или их можно получать по общеизвестным из литературы методам (см. примеры I-XVI).
Так, например, соответствующее циклическое производное мочевины получают путем циклизации соответственно замещенной мочевины, которую получают в результате взаимодействия соответствующего амина со соответствующим изоцианатом, или в результате взаимодействия соответственно замещенного диамина с производным угольной кислоты, например фосгеном, или соответствующее производное триазолона - путем циклизации соответствующего семикарбазида, получаемого в результате взаимодействия соответствующего изоцианата со соответствующим гидразидом.
В получаемых таким образом производных циклической мочевины можно потом, в случае необходимости, переводить карбонил в соответствующую тиокарбонильную или карбимино-группу по известным методам.
В получаемых таким образом циклических исходных соединениях или уже в необходимых для их получения исходных соединениях возможно имеющийся сложный эфир можно переводить в карбоксил путем гидролиза или возможно имеющийся карбоксил - в сложный эфир.
Как уже выше упомянуто, новые циклические азотсодержащие производные общей формулы (I) и их соли, в частности их физиологически переносимые соли с неорганическими или органическими кислотами или основаниями, обладают ценными свойствами. Так, например, кроме противовоспалительного действия и тормозящего разложение костей действия они, в частности, обладают антитромботическим, антиагрегаторным, противоопухолевым и противометастазным действиями.
Биологическое действие соединений общей формулы (I) исследовали, например, нижеописанным образом.
1. Торможение связывания 3H-BIBU 52 с тромбоцитами человека
В суспензию тромбоцитов человека в плазме добавляют 3H-BIBU 52 [= (3S, 5S)-5-[(4'-амидино-4-бифенилил)оксиметил] - 3-[(карбоксил)метил]-2-пирролидинон[3-3H-4-бифенилил] ] , заменяющий известный из литературы лиганд 125J-фибриноген, и инкубируют с разными концентрациями исследуемых соединений. Свободный и связанный лиганды разделяют путем центрифугирования, и их количество определяют путем сцинтилляции. На основе результатов опыта определяют торможение связывания 3H-BIBU 52 исследуемым соединением.
Для осуществления опыта путем прокола антикубитальной вены извлекают кровь, которую для задержки свертывания обрабатывают тринатрийцитратом (конечная концентрация: 13 ммоль). Кровь подвергают центрифугированию при 170 х g в течение 10 минут. Богатую тромбоцитами плазму удаляют, и остаточную кровь для получения плазмы еще раз подвергают центрифугированию. Богатую тромбоцитами плазму разбавляют аутогенной плазмой в соотношении 1 : 10. 750 мкл полученной жидкости вместе с 50 мкл физиологического раствора поваренной соли, 100 мкл раствора исследуемого соединения, 50 мкл 14C-сахарозы (3700 Бк) и 50 мкл 3H-BIBU 52 (конечная концентрация: 5 нмоль) инкубируют при комнатной температуре в течение 20 минут. Для определения неспецифического связывания вместо исследуемого соединения используют 5 мкл BIBU 52 (конечная концентрация: 30 мкмоль). Пробы подвергают центрифугированию при 10000 х g в течение 20 сек, надосадочную жидкость удаляют. 100 мкл данной жидкости подвергают измерению для определения свободного лиганда. Продукт центрифугирования растворяют в 500 мкл 0,2 н. гидроокиси натрия, к 450 мкл получаемого раствора добавляют 2 мл сцинтиляционной жидкости и 25 мкл 5 н. соляной кислоты и измеряют. Еще имеющуюся в продукте центрифугирования плазму определяют исходя из содержания 14C, а связанный лиганд - исходя 3H. После вычитания неспецифического связывания сравнивают активность центрифугата с концентрацией исследуемого соединения и определяют ту концентрацию, при которой исследуемое соединение задерживает связывание 3H BIBU 52 на 50% (концентрацию торможения КТ50).
2. Антитромботическое действие
Методика
Агрегацию тромбоцитов определяют по методу Борн и Кросс (J. Physiol, 170, стр. 397, 1964 г.) на богатой тромбоцитами плазме здоровых людей. Для задержки свертывания к крови добавляют 3,14%-ный цитрат натрия в объемном соотношении 1:10.
Индуцированная коллагеном агрегация
Снижение оптической плотности суспензии тромбоцитов измеряют фотометрически и регистрируют после добавления вызывающего агрегацию вещества. Скорость агрегации определяют на основе угла наклона кривой плотности. Точка кривой, показывающая наибольшую светопроницаемость, служит для расчета оптической плотности.
Количество коллагена выбирают как можно более маленьким, но достаточным для получения необратимой кривой реакции. Используют имеющийся в торговле коллаген фирмы Гормонхеми, г. Мюнхен/DE. Перед добавлением коллагена плазму вместе с исследуемым соединением инкубируют при температуре 37oC в течение 10 минут.
На основе кривых по концентрациям и действию определяют эффективную дозу ЭД50 в нмоль, т.е., дозу, при которой достигается 50%-ное торможение изменения оптической плотности.
Результаты опыта приведены в следующей таблице.
Кроме того, соединения примеров 7 и 19, например, тормозят индуцированную коллагеном агрегацию тромбоцитов ex vivo на макаке-резусе после оральной дачи 1 мг/кг в течение более 5 и 8 часов соответственно.
Новые соединения обладают хорошей переносимостью организмом, так как, например, после внутривенной дачи трем мышам 30 мг на кг соединения согласно примерам 8 (1) или 19 ни одно из животных не умерло.
Благодаря тормозящему действию на взаимодействие между клетками или между клетками и матрицами новые гетероциклы общей формулы (I) и их физиологически переносимые аддитивные соли пригодны для лечения и профилактики болезней, при которых возникают агрегации клеток разного размера, или при которых некоторую роль играет взаимодействие между клетками и матрицами, например, для борьбы и профилактики венозных и артериальных тромбозов, церебрососудистых болезней, эмболии легочной артерии или ее ветвей, инфаркта миокарда, артериосклероза, остеопороза и метастазирования опухолей или лечения генетически обусловленных или приобретенных нарушений взаимодействия между клетками или между клетками и твердыми структурами. Кроме того, данные соединения пригодны для сопутствующего лечения при тромболизе при использовании фибринолитических лекарств или при вмешательстве в сосуды, например, при чрескожной баллонной ангиопластики коронарных артерий, а также для лечения в случае состояния шока, псориаза, диабета и воспалений.
Для лечения и профилактики вышеуказанных болезней новые соединения применяют в дозах между 0,1 мкг и 30 мг на кг веса тела, предпочтительно 1 мкг - 15 мг на кг веса тела, при 1 - 4 дозах в день. Для этого новые соединения общей формулы (I) можно переводить в известные препараты, например, таблетки, драже, капсули, порошки, суспензии, растворы, аэрозоли или суппозитории, в случае необходимости, в сочетании с другими активными веществами, например, антагонистами рецептора тромбоксана или задерживающими синтез тромбоксана веществами или их смесью, антагонистами серотонина, антагонистами α- рецепторов, алкилнитратами, например, тринитратом глицерина, веществами, задерживающими фосфодиэстеразу, простациклином и их аналогами, фибринолитическими лекарствами, например, активатором плазминогена ткани, проурокиназой, стрептокиназой, или тормозящими свертывание лекарствами, например, гепарином, сульфатом дерматана, активированным белком C, антагонистами витамина K, гирудином, ингибиторами тромбина или других активированных факторов свертывания, вместе с одним или некоторыми известными инертными носителями и/или разбавителями, например, кукурузным крахмалом, лактозой, сахарозой, микрокристаллической целлюлозой, стеаратом магния, поливинилпирролидоном, лимонной кислотой, винной кислотой, водой, смесью воды и этанола, смесью воды и глицерина, смесью воды и сорбита, смесью воды и полиэтиленгликоля, пропиленгликолем, стеариловым спиртом, карбоксиметилцеллюлозой или содержащими жир веществами, например, отвержденным жиром, или их пригодными смесями.
Нижеследующие примеры поясняют получение исходных соединений.
Пример I
1-(изохинолин-N-оксид-6-ил)-3-[4-[2-(метоксикарбонил)этил]фенил]- имидазолидин-2-он
2,6 г 1-(изохинолин-6-ил)-3-[4-[2-(метоксикарбоил)этил]фенил]- имидазолидин-2-она при нагревании растворяют в 175 мл метиленхлорида. Охлаждают на ледяной бане и смешивают с 1,46 г 90%-ной 3-хлорпероксибензойной кислоты. После перемешивания в течение суток при 0oC разбавляют метиленхлоридом и два раза экстрагируют раствором бикарбоната натрия и раствором тиосульфата натрия, а затем водой. Органическую фазу отделяют, сушат и упаривают в ротационном испарителе.
Выход: 2,4 г (88% теории)
Значение Rf: 0,15 (силикагель; смесь метиленхлорида, метанола и этилацетата в соотношении 20 : 1 : 1)
Пример II
N-(2-гидроксиэтил)N'-(изохинолин-6-ил)-N-[4-[2-(метокси- карбонил)этил] фенил]-мочевина
К 7,2 г имидазола и 10,1 г N,N'-карбонилдиимидазола в 100 мл диметилформамида при температуре 0 - 10oC прикапывают 9,0 г 6-аминоизохинолина в 70 мл диметилформамида. После перемешивания в течение 2 часов при комнатной температуре прикапывают 15,3 г N-(2-гидpoкcиэтил)-4-[2-(мeтoкcикapбoнил)этил] -aнилинa в 20 мл диметилформамида и перемешивают 2,5 суток при комнатной температуре. Растворяют 750 мл этилацетата и дважды экстрагируют водой и насыщенным раствором поваренной соли. Органическую фазу отделяют, сушат и сгущают. Остаток очищают путем колоночной хроматографии на силикагеле с применением в качестве элюента смеси этилацетата, метиленхлорида и метанола в соотношении 70 : 30 : 10.
Выход: 4,8 г (19% теории)
Значение Rf: 0,48 (силикагель; смесь метиленхлорида, метанола и этилацетата в соотношении 20 : 1: 1)
Аналогичным образом получают следующие соединения:
(1) N-2,2-диэтоксиэтил)-N'-(изохинолин-6-ил)-N-[4-[2- (метоксикарбонил)этил] фенил]-мочевина
Значение Rf: 0,50 (силикагель; смесь метиленхлорида и метанола в соотношении 20:1)
(2) N-(3-этил-2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-N'-(2,2- диэтоксиэтил)-N'-[транс-4-[2-(метоксикарбонил)этил]циклогексил]- мочевина
Точка плавления: 101 - 104oC
Значение Rf: 0,63 (силикагель; смесь метиленхлорида, метанола и конц. водного аммиака в соотношении 90 : 10 : 2)
(3) N-(7-этил-6,7,8,9-тетрагидро-5Н-пиразино[2,3-d] ацепин-2-ил)- N'-2,2-диэтоксиэтил)-N'-[транс-4-[2-(метоксикарбонил)этил]- циклогексил]-мочевина
Реакцию осуществляют в присутствии 1,1'-карбонил-ди-(1,2,4-триазола)
Точка плавления: 100 - 102oC
Значение Rf: 0,41 (силикагель; смесь метиленхлорида и метанола в соотношении 9:1)
Рассчитано: C 62,40; H 8,73; N 13,48.
Найдено: C 62,19; H 8,79; N 13,62.
(4) N-(7-бензил-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-d]ацепин-2- ил)-N'-диэтоксиэтил)-N'-[транс-4-[2-(метоксикарбонил)этил]- циклогексил]-мочевина
Реакцию осуществляют в присутствии 1,1'-карбонил-ди-(1,2,4-триазола)
Значение Rf: 0,23 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Пример III
N-(3-трет. бутилоксикарбонил-2,3,4,5-тетрагидро-1Н-3-бензацепин- 7-ил)-N-(2-гидроксиэтил)-N'-[4-[2-(метоксикарбонил)этил]фенил- мочевина
4,5 г 3-(трет.бутилоксикарбонил)-7-[(2-гидроксиэтил)амино]- 2,3,4,5-тетрагидро-1Н-3-бензацепина и 3,7 г 4-[2-(метоксикарбонил)этил]-фенилизоцианата (полученного из соответствующего амина путем взаимодействия с фосгеном) перемешивают в 35 мл диоксана 3,5 часов при комнатной температуре. Реакционную смесь сгущают, остаток растирают вместе с трет.бутил-метиловым эфиром и отсасывают. Продукт промывают трет.бутил-метиловым эфиром и сушат.
Выход: 6,3 г (76% теории)
Точка плавления: 115 - 117oC
Значение Rf: 0,30 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
Аналогичным образом получают следующие соединения:
(1) 1-ацетил-4-[4-[2-(метоксикарбонил)этил]фенил]-семикарбацид
(Взаимодействие ацетилгидразина с 4-[2-(метоксикарбонил)этил]-фенилизоцианатом)
Точка плавления: 159 - 165oC
Значение Rf: 0,37 (силикагель; смесь метиленхлорида и метанола в соотношении 9:1)
(2) N-(2-гидроксиэтил)-N-[тpaнс-4-[2-(метоксикарбонил)этил] - циклогексил]-N'-(3-трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин- 7-ил)-мочевина
Точка плавления: 150 - 152oC
Значение Rf: 0,31 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
(3) N-(2,2-диэтoкcиэтил)-N-(3-тpифтopaцeтил-2,3,4,5-тeтpaгидpo- 1H-3-бeнзaцeпин-7-ил)-N'-[транс-4-[2-(метоксикарбонил)этил] - циклогексил]-мочевина
Применяемый [транс-4-[2-(метоксикар бонил)этил] циклогексил]-изоцианат получают из соответствующего амина в виде гидрохлорида в результате взаимодействия с фосгеном. Применяемый 7-[(2,2-диэтоксиэтил)амино]-3-трифторацетил-2,3,4,5-тетрагидро-1H-3- бензацепин [значение Rf: 0,76 (силикагель; смесь циклогексана и этилацетата в соотношении 3 : 2)] получают путем взаимодействия 7-амино-3-трифторацетил- 2,3,4,5-тетрагидро-1Н-3-бензацепина с диэтилацеталем бромацетальдегида в присутствии N-этил-диизопропиламина.
Значение Rf: 0,26 (силикагель; смесь циклогексана и этилацетата в соотношении 3 : 2)
(4) N-[транс-[[метоксикарбонил)метил]окси]циклогексил]-N'- (2,2-диэтоксиэтил)-N'(3-трифторацетил-2,3,4,5-тетрагидро-1Н-3- бензацепин-7-ил)-мочевина
Применяемый [транс-4-[(метоксикарбоинл)метил]окси]циклогексил]- изоцианат получают из соответствующего амина в виде гидрохлорида в результате взаимодействия с фосгеном.
Значение Rf: 0,20 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
(5) N-(2-гидроксиэтил)-N-[4-[транс-2-(метоксикарбонил)этенил]- фенил]-N'-(3-трифторацетил-2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)- мочевина
Применяемый (3-трифторацетил-2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил-изоцианат получают из соответствующего амина в результате взаимодействия с фосгеном.
Точка плавления: начиная с 118oC
Значение Rf: 0,18 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
(6) N-[4-(2-этоксикарбонил)-1-пропил] фенил-N'-(2,2-диэтоксиэтил)-N'-(3-трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-мочевина
Применяемый [4-[2-(этоксикарбонил)-1-пропил]фенил]-изоцианат получают в результате взаимодействия соответствующего амина с фосгеном.
Значение Rf: 0,35 (силикагель; смесь циклогексана и этилацетата в соотношении 2 : 1)
(7) N-[тpaнc-4-[2-(мeтoкcикapбoнил)этил]циклoгeкcил]-N'- [(бeнзилoкcикapбoнил)метил]-N'-(3-трифторацетил-2,3,4,5-тетрагидро- 1H-3-бензацепин-7-ил)-мочевина
Применяемый 7-[[(бензилоксикарбонил)метил] амино] -3- трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин [значение Rf: 0,24 (силикагель; смесь циклогексана и этилацетата в соотношении 4 : 1] получают в результате взаимодействия 7-амино-3-трифторацетил- 2,3,4,5-тетрагидро-1H-3-бензацепина со сложным бензиловым эфиром бромуксусной кислоты в присутствии N-этил-диизопропиламина.
Значение Rf: 0,51 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
(8) N-(3-гидpoкcипpoпил)-N-[тpaнc-4-[2-мeтoкcикaрбoнил)этил]- циклoгeкcил]-N'-(3-трифторацетил-2,3,4,5-тетрагидро-1H-3-бензацепин- 7-ил)мочевина
Точка плавления: 129 - 130oC
(9) l-aцeтил-4-[трaнc-4-[2-(мeтoксикарбонил)этил] -циклoгeкcил] - ceмикaрбазид
Точка плавления: 176 - 179oC
Значение Rf: 0,24 (силикагель; смесь метиленхлорида и метанола в соотношении 95:5)
(10) 1-формил-4-[транс-4-[2-(метоксикарбонил)этил] циклогексил] - семикарбазид
Точка плавления: 169 - 171oC
(11) N-[4-[2-этоксикарбонил)-1-фенил-этил] фенил] -N'-(2,2- диэтоксиэтил)-N'-(3-трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин- 7-ил)-мочевина
Применяемый [4-[2-(этоксикарбонил)-1-фенил-этил]фенил]-изоцианат получают из соответствующего амина путем взаимодействия с фосгеном. Сырой продукт непосредственно применяют для получения соединения примера 5(6).
(12) 1-формил-4-(3-трифторацетил-2,3,4,5-тетрагидро-1Н-3- бензацепин-7-ил)-семикарбазид
Значение Rf: 0,41 (силикагель; смесь метиленхлорида и метанола в соотношении 9:1)
Пример IV
3-(трет. бутилоксикарбонил)-7-[(2-гидроксиэтил)амино] -2,3,4,5- тетрагидро-1H-3-бензацепин
7,2 г 7-амино-3-(трет.бутилоксикарбонил)-2,3,4,5-тетрагидро-1H- 3-бензацепина (полученного из 7-нитро-2,3,4,5-тетрагидро-1Н-3- бензацепина путем взаимодействия со сложным ди-трет.бутиловым эфиром пироугольной кислоты и последующего гидрирования в присутствии палладия на активированном угле) в 130 мл метанола при перемешивании смешивают с 1,53 мл ледяной уксусной кислоты и 1,8 г димерного гликол-альдегида. Потом добавляют 1,9 г цианборгидрида натрия и перемешивают в течение часа при комнатной температуре. Реакционную смесь упаривают, остаток распределяют между этилацетатом и водой. Органическую фазу отделяют, дважды промывают водой, сушат и упаривают в ротационном испарителе. Остаток очищают путем колоночной хроматографии на силикагеле с применением в качестве элюента смеси циклогексана и этилацетата в соотношении 4 : 6.
Выход: 5,4 г (64% теории)
Точка плавления: 86 - 89oC
Значение Rf: 0,39 (силикагель; смесь циклогексана и этилацетата в соотношении 4 : 6)
Аналогичным образом получают следующее соединение:
Сложный метиловый эфир транс-4-[(2-гидроксиэтил)амино]-коричной кислоты
Точка плавления: 117 - 118oC
Значение Rf: 0,25 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
Пример V
(4aRS, 6RS, 8aRS)-6-[(2,2-димeтoкcиэтил)aминo] -2-мeтил- 1,2,3,4,4а, 5,6,7,8,8a-декагидроизохинолин
К раствору 9,0 г (4аRS,8аRS)-2-метил-6-оксо- 1,2,3,4,4а,5,6,7,8,8a-декагидроизохинолина и 6,8 г диметилацеталя амино-ацетальдегида в 90 мл ацетонитрила добавляют 31 мл 3 н. соляной кислоты и перемешивают 30 минут при комнатной температуре. Затем охлаждают на ледяной бане и порциями добавляют 4,4 г цианборгидрида натрия. После 30-минутного перемешивания при комнатной температуре и стояния в течение ночи сгущают, разбавляют ледяной водой и доводят до значения pH 10 - 11. Три раза экстрагируют этилацетатом. Объединенные экстракты этилацетата дважды промывают насыщенным раствором поваренной соли, сушат и сгущают. Остаток очищают путем колоночной хроматографии на основной окиси алюминия.
Выход: 7,35 г (53% теории)
Значение Rf: 0,25 (окись алюминия; этилацетат)
В качестве побочного продукта примера (V) выделяют (4aRS,6SR,8aRS)-6-[(2,2-ди-метоксиэтил)амино] -2-метил- 1,2,3,4,4а,5,6,7,8,8a-декагидроизохинолин.
Значение Rf: 0,56 (окись алюминия; этилацетат)
Пример VI
7-йод-3-трифторацетил-2,3,4,5-тетрагидро-1H-3-бензацепин
2,6 г 7-амино-3-трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепина при перемешивании кратковременно нагревают с 50 мл 10%-ной соляной кислоты, затем охлаждают до 0oC и при дальнейшем охлаждении при 0oC каплями добавляют 695 мг нитрита натрия в 14 мл воды. Потом при 0oC прикапывают раствор 1,7 г йодида калия и 1,3 г йода в 10 мл воды и перемешивают в течение ночи при комнатной температуре. Затем декантируют и полученный остаток растворяют в метиленхлориде. Органическую фазу промывают раствором дисульфита натрия и водой, отделяют, сушат, фильтруют и упаривают в ротационном испарителе. Сырой продукт очищают колоночной хроматографией на силикагеле с применением в качестве элюента смеси циклогексана и этилацетата в соотношении 4:1.
Выход: 2,4 г (65% теории)
Точка плавления: 80 - 82oC
Значение Rf: 0,61 (силикагель; смесь циклогексана и этилацетата в соотношении 4 : 1)
Пример VII
7-амино-3-трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин
17,3 г 7-нитро-3-трифторацетил-2,3,4,5-тетрагидро-1H-3- бензацепина гидрируют при давлении водорода 3,52 кг/см2 и комнатной температуре в течение часа в 200 мл этилацетата на 3 г 10%-ного палладия на активном угле. Катализатор отсасывают и фильтрат упаривают. Остаток нагревают вместе с трет. бутилметиловым эфиром и охлаждают. Осадок отсасывают, промывают трет. бутилметиловым эфиром и сушат.
Выход: 12,2 г (79% теории)
Точка плавления: 102 - 104oC
Значение Rf: 0,31 (силикагель; смесь циклогексана и этилацетата в соотношении 2 : 1)
Аналогичным образом получают следующие соединения:
(1) 7-амино-3-трет.бутилоксикарбонил-2,3,4,5-тетрагидро-1Н-3- бензацепин
Применяемый в качестве исходного соединения 3-трет. бутилоксикарбонил-7-нитро-2,3,4,5-тетрагидро-1Н-3-бензацепин (точка плавления: 100 - 102oC) получают в результате взаимодействия гидрохлорида 7-нитро-2,3,4,5-тетрагидро-1H-3-бензацепина со сложным ди-трет.бутиловым эфиром пироугольной кислоты в присутствии натрового щелока.
Значение Rf: 0,40 (силикагель; смесь циклогексана и этилацетата в соотношении 7 : 3)
(2) 7-амино-3-этил-2,3,4,5-тетрагидро-1H-3-бензацепин
Взаимодействие на никеле Ренея в среде метанола.
Значение Rf: 0,58 (силикагель; смесь толуола, диоксана, метанола и конц. водного аммиака в соотношении 20 : 50 : 20 : 3)
(3) Гидрохлорид сложного этилового эфира 3-(4-аминофенил)-3-фенил-пропионовой кислоты
Осуществление реакции в среде этанола в присутствии этанольной соляной кислоты. Исходное соединение, сложный этиловый эфир 3-(4-нитрофенил)-3-фенилакриловой кислоты (значение Rf: 0,36 (силикагель; смесь циклогексана и метиленхлорида в соотношении 1 : 1), получают в результате взаимодействия 4-нитробензофенона со сложным триэтиловым эфиром фосфоноуксусной кислоты.
Значение Rf: 0,40 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного раствора поваренной соли в соотношении 6 : 4)
Пример VIII
7-нитро-3-трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин
К раствору 23,3 г 3-трифторацетил-2,3,4,5-тетрагидро-1Н-3- бензацепина [значение Rf: 0,76 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1), полученный путем взаимодействия 2,3,4,5-тетрагидро-1Н-3-бензацепина с ангидридом трифторуксусной кислоты в присутствии N-этил-диизопропиламина] в 60 мл конц. серной кислоты при 0 - 8oC прикапывают в течение 1,5 часов смесь 9,7 г нитрата калия и 50 мл конц. серной кислоты. Нагревают до комнатной температуры, подают на 1 л льда и экстрагируют этилацетатом. Объединенные этилацетатные фазы промывают водой и насыщенным раствором поваренной соли, сушат и упаривают. Остаток нагревают вместе с трет.бутил-метиловым эфиром. Затем охлаждают, продукт отсасывают и промывают трет.бутил-метиловым эфиром.
Выход: 16,2 г (59% теории)
Точка плавления: 116 - 119oC
Значение Rf: 0,57 (силикагель; смесь циклогексана и этилацетата в соотношении 2 : 1)
Аналогичным образом можно получать следующее соединение:
Гидрохлорид 7-нитро-2,3,4,5-тетрагидро-1Н-3-бензацепина
Получение с использованием смеси серной кислоты и нитрата калия и изолирование в качестве гидрохлорида
Точка плавления: 235 - 238oC (разл.)
Рассчитано: C 52,52; H 5,74; N 12,25; Cl 15,50.
Найдено: C 52,44; H 5,80; N 12,07; Cl 15,36.
Пример IX
4-[4-[2-(метоксикарбонил)этил]фенил]-5-метил-4Н-1,2,4-триазол-3-он
8,1 г 1-ацетил-4-[4-[2-(метоксикарбонил)этил]фенил]- семикарбазида вместе с 60 мл 1 н. натрового щелока нагревают на паровой бане в течение 1,5 часов. Затем немного охлаждают, фильтруют и фильтрат слабо подкисляют лимонной кислотой. Фильтруют и фильтрат смешивают с концентрированной соляной кислотой. Осадок фильтруют, промывают водой и сушат. Промежуточный продукт перемешивают в течение ночи в метаноле с небольшим количеством метанольной соляной кислоты. Реакционную смесь сгущают и остаток растирают вместе с трет. бутил-метиловым эфиром, отсасывают и сушат.
Выход: 4,98 г (65% теории)
Значение Rf: 0,40 (силикагель; смесь толуола, диоксана, этанола и этилацетата в соотношении 90:10:10:6)
Рассчитано: С 59,76; H 5,79; N 16,08.
Найдено: C 59,54; H 5,86; N 16,05.
Аналогичным образом получают следующие соединения:
(1) 4-[транс-4-[2-(метоксикарбонил)этил] циклогексил] -5-метил-4Н- 1,2,4-триазол-3-он
Точка плавления: 179 - 181oC
(2) 4-[транс-4-[2-(метоксикарбонил)этил] циклогексил] -4Н-1,2,4- триазол-3-он
Точка плавления: 142 - 144oC
(3) 4-(3-трет.бутилоксикарбонил-2,3,4,5-тетрагидро-1Н-3- бензацепин-7-ил)-4Н-1,2,4-триазол-3-он
Исходное соединение: соединение примера III (12)
Промежуточный продукт подвергают взаимодействию со сложным ди-трет.бутиловым эфиром пироугольной кислотой (вместе с метанольной соляной кислотой). Точка плавления: 185 - 186oC
Значение Rf: 0,25 (силикагель; смесь циклогексана и этилацетата в соотношении 2 : 3)
Пример X
N-[транс-4-[2-(метоксикарбонил)этил]циклогексил]-этаноламин
5,0 г N-бензил-N-[транс-4-[2-(метоксикарбонил)этил]циклогексил]- этаноламина гидрируют в 150 мл метанола в течение 105 минут при температуре 50oC и давлении водорода 3,52 кг/см2 на 1,0 г 10%-ного палладия на активном угле. Фильтруют и упаривают.
Выход: 3,3 г (92% теории)
Значение Rf: 0,20 (силикагель; смесь метиленхлорида, метанола и конц. водного аммиака в соотношении 9 : 1 : 0,4)
Аналогичным образом получают следующие соединения:
(1) Сложный трет.бутиловый эфир (транс-4-аминоциклогексил)оксиуксусной кислоты
Исходное соединение, сложный трет.бутиловый эфир [транс-(4- дибензиламино)циклогексил] оксиуксусной кислоты [значение Rf: 0,51 (силикагель; смесь циклогексана и этилацетата в соотношении 4 : 1)], получают в результате взаимодействия транс-4- (дибензиламино)циклогексанола со сложным трет.бутиловым эфиром бромуксусной кислоты в смеси толуола и 50%-ного натрового щелока в присутствии гидрогенсульфата тетрабутиламмония.
Значение Rf: 0,56 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
(2) N-(3-гидроксипропил)-N-[транс-4-[2-(метоксикарбонил)этил]- циклогексил]-амин
Значение Rf: 0,10 (силикагель; смесь метиленхлорида и метанола в соотношении 9:1)
(3) Гидрохлорид сложного метилового эфира [[транс-4-[2- (метоксикарбонил)этил]циклогексил]амино]-уксусной кислоты
Точка плавления: 166 - 168oC
Гидрирование в присутствии метанольной кислоты.
Значение Rf: 0,69 (силикагель; смесь метиленхлорида, метанола и конц. водного аммиака в соотношении 95 : 5 : 1)
Пример XI
N-бензил-N-[транс-4-[2-(метоксикарбонил)этил]циклогексил]- этаноламин
6,2 г гидрохлорида N-[транс-4-[2-(метоксикарбонил)этил]- циклогексил] бензиламина, 12,8 г N-этил-диизопропиламина и 5,0 г 2-бромэтанола перемешивают 22 часа при 100oC и затем охлаждают. Распределяют между этилацетатом и водой, водную фазу экстрагируют этилацетатом и объединенные этилацетатные фазы промывают насыщенным раствором поваренной соли. Этилацетатные фазы упаривают и остаток очищают путем колоночной хроматографии на силикагеле с применением в качестве элюента смеси метиленхлорида и метанола в соотношении 9 : 1.
Выход: 5,1 г (80% теории)
Значение Rf: 0,67 (силикагель; смесь метиленхлорида и метанола в соотношении 9:1)
Аналогичным образом получают следующие соединения:
(1) N-(3-гидроксипропил)-N-[транс-4-[2-(метоксикарбонил)этил] - циклогексил]-бензиламин
Значение Rf: 0,70 (силикагель; смесь метиленхлорида и метанола в соотношении 9:1)
(2) Сложный метиловый эфир N-бензил-[[транс-4-[(2- метоксикарбонил)этил] циклогексил]амино]-уксусной кислоты
Значение Rf: 0,86 (силикагель; смесь циклогексана и этилацетата в соотношении 3 : 7)
(3) 3-этил-7-нитро-2,3,4,5-гетрагидро-1H-3-бензацепин
Значение Rf: 0,32 (силикагель; смесь метиленхлорида и метанола в соотношении 95:5)
Пример XII
Гидрохлорид N-[транс-4-[2-(метоксикарбонил)этил] циклогексил]- бензиламина
8,0 г гидрохлорида сложного метилового эфира 3-(транс-4-аминоциклогексил)пропионовой кислоты) 4,3 г бензальдегида и 5,0 мл триэтиламина в 150 мл метанола гидрируют в течение 4 часов при давлении водорода 3,52 кг/см2 на 1,0 г никеля Ренея при температуре 50oC. После охлаждения отсасывают и фильтрат упаривают. Остаток распределяют между этилацетатом и водой, водную фазу добавкой натрового щелока доводят до pH 8 - 9 и экстрагируют этилацетатом. Объединенные этилацетатные фазы промывают насыщенным раствором поваренной соли, сушат и упаривают в ротационном испарителе. Остаток суспендируют в диэтиловом эфире и смешивают с метанольной соляной кислотой. Осадок отсасывают, промывают простым диэтиловым эфиром и сушат.
Выход: 7,4 г (66% теории)
Точка плавления: 170 - 172oC
Рассчитано: С 65,47; H 8,40; N 4,49; Cl 11,37.
Найдено: C 65,38; H 8,44; N 4,46; Cl 11,40.
Пример XIII
Гидрохлорид сложного метилового эфира (транс-4-аминоциклогексил)оксиуксусной кислоты
Над охлажденным на ледяной бане раствором 59,4 г сложного трет.бутилового эфира (транс-4-аминоциклогексил)оксиуксусной кислоты в 500 мл метанола пропускают хлористый водород в течение часа и потом перемешивают в течение ночи при комнатной температуре. Сгущают досуха, остаток растирают вместе с ацетоном, а твердое вещество отсасывают и сушат.
Выход: 34,3 г (59% теории)
Точка плавления: 157 - 160oC
Пример XIV
2-(3-трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)- 3,4-дигидро-2Н,5Н-1,2,5-тиадиазол-1,1-диоксид
а) Диамид N-(2-хлорэтил)-N'-(3-трифторацетил-2,3,4,5-тетрагидро- 1Н-3-бензацепин-7-ил)-серной кислоты
К смеси 7,6 г 7-амино-3-трифторацетил-2,3,4,5-тетрагидро-1Н-3- бензацепина и 7,7 мл N-этил-диизопропиламина в 70 мл метиленхлорида прикапывают 4,8 г [(2-хлорэтил)амино]сульфонилхлорида в 30 мл метиленхлорида при температуре -5oC. Перемешивают в течение часа при 0oC и в течение ночи при комнатной температуре. Реакционную смесь разбавляют метиленхлоридом и промывают водой, 1 н. соляной кислотой и еще раз водой. Органическую фазу сушат, сгущают и остаток очищают колоночной хроматографией на силикагеле с применением в качестве элюента смеси циклогексана и этилацетата в соотношении 1 : 1.
Выход: 7,8 г (72% теории)
Точка плавления: 128 - 130oC
Значение Rf: 0,64 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
б) 2-(3-трифторацетил-2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)- 3,4-дигидро-2Н,5Н-1,2,5-тиадиазол-1,1-диоксид
7,8 г соединения примера XIVa) растворяют в 20 мл диметилформамида и смешивают с 2,5 г трет.бутилата калия. После перемешивания при комнатной температуре в течение 3 часов подают на 300 мл 15%-ного водного раствора лимонной кислоты и экстрагируют три раза этилацетатом. Объединенные органические фазы сушат, сгущают и остаток очищают колоночной хроматографией на силикагеле с применением в качестве элюента смеси циклогексана и этилацетата в соотношении 1 : 1.
Выход: 2,1 г (30% теории)
Точка плавления: 165 - 167oC
Значение Rf: 0,30 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
Пример XV
(3-метил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-борная кислота
К 7,1 г 7-йод-3-метил-2,3,4,5-тетрагидро-1Н-3-бензацепина [значение Rf: 0,85 (силикагель; смесь толуола, диоксана, метанола и конц. водного аммиака в соотношении 20 : 50 : 20 : 5), полученного из соединения примера VI в результате взаимодействия смеси натрового щелока и метанола и последующего взаимодействия со смесью формалина и муравьиной кислоты] в 50 мл диэтилового эфира прикапывают 1,6 мл н-бутиллития в гексане при температурах между -70 и -75oC. После 30-минутного перемешивания при -70oC прикапывают 5,7 мл триизопропилбората в 30 мл диэтилового эфира. Перемешивают в течение часа при -75oC, затем нагревают до -50oC и добавляют 70 мл воды. Перемешивают в течение часа при нагревании до комнатной температуры, потом отделяют водную фазу, которую добавкой ледяной уксусной кислоты доводят до pH 8-8,5. Продукт отсасывают, промывают небольшим количеством холодной воды и сушат при 60oC.
Выход: 3,7 г (73% теории)
Точка плавленая: 153 - 155oC (спекание с 148oC)
Значение Rf: 0,80 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Пример XVI
1-[2-(этоксикарбонил)этил]-3-[4-(трифторметилсульфонилокси)- фенил]-имидазолидин-2-он
а) N-(2,2-диэтоксиэтил-4-бензилокси-анилин
Полученный из 4-бензилоксианилина в результате взаимодействия с бромацетальдегид-диэтилацеталом в присутствии N-этил-диизопропиламина.
Значение Rf: 0,42 (силикагель; смесь циклогексана и этилацетата в соотношении 85:15)
б) N-(4-бензилоксифенил)-N-(2,2-диэтоксиэтил)-N'-[2-(этокси- карбонил)этил)-мочевина
Полученный из N-(2,2-диэтоксиэтил)-4-бензилокси-анилина в результате взаимодействия с [2-(этоксикарбонил)этил]-изоцианатом.
Значение Rf: 0,45 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
в) 1-(4-бензилоксифенил)-3-[2-(этоксикарбонил)этил]-3Н-имидазол-2-он
Полученный в результате обработки N-(4-бензилоксифенил)-N- (2,2-диэтоксиэтил)-N'-[2-(этоксикарбонил)этил] -мочевины трифторуксусной кислотой в метиленхлориде.
Точка плавления: 66 - 68oC
Значение Rf: 0,41 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
г) 1-(4-гидроксифенил)-3-[2-(этоксикарбонил)этил]- имидазолидин-2-он
Полученный из 1-(4-бензилоксифенил)-3-[2-(этоксикарбонил)этил]-3Н-имидазол-2-она путем каталитического гидрирования в присутствии палладия на угле в этаноле при 40oC и давлении водорода 3,52 кг/см2.
Значение Rf: 0,20 (силикагель; смесь метиленхлорида и метанола в соотношении 100:2)
д) 1-[2-(этoкcикapбoнил)этил] -3-[4-(тpифтopметилcульфoнилoкcи)- фенилl-имидазолидин-2-он
Полученный из 1-(4-гидроксифенил)-3-[2-(этоксикарбонил)этил]- имидазолидин-2-она в результате взаимодействия с ангидридом трифторметансульфокислоты в пиридине при 0oC.
Точка плавления: 81 - 83oC
Значение Rf: 0,66 (силикагель; смесь метиленхлорида и метанола в соотношении 100:1)
Рассчитано: C 43,90; H 4,18; N 6,83; S 7,81.
Найдено: C 43,92; H 4,20; N 6,98; S 7,91.
Нижеследующие примеры поясняют получение циклических азотсодержащих производных формулы (I).
Пример 1
1-(1-аминоизохинолин-6-ил)-3-[4-(2-карбоксиэтил)фенил] - имидазолидин-2-он х 1 H2O x 1,2 CH3•COOH
300 мг 3-[4-2-карбоксиэтил)фенил]-1-(1-хлоризохинолин-6-ил)- имидазолидин-2-она, 895 мг ацетамида и 524 мг карбоната калия тщательно перемешивают в ступке и затем при перемешивании нагревают до 200oC в течение 3 часов в атмосфере азота. После охлаждения смешивают с 20 мл воды и добавкой 1 н. соляной кислоты доводят до pH 8-9. Осадок отсасывают и несколько раз промывают водой. После высушивания осадок суспендируют в 50 мл смеси метиленхлорида и метанола в соотношении 4 : 1 и обрабатывают в ультразвуковой бане в течение 30 минут. Осадок отсасывают и два раза повторяют обработку смесью метиленхлорида и метанола в ультразвуковой бане. Остаток на фильтре смешивают при слабом нагревании в смеси 30 мл метанола и 10 мл ледяной уксусной кислоты. Фильтруют от нерастворившихся компонентов и маточный раствор сгущают досуха. Остаток еще раз смешивают с толуолом и сгущают. Потом сушат в вакууме при температуре 60oC.
Выход: 70 мг (20% теории)
Точка плавления: > 250oC
Значение Rf: 0,78 (обратнофазная колоночная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 8 : 4)
Рассчитано: C 60,25; H 5,79; N 12,01.
Найдено: C 60,20; H 5,43; N 11,54.
Масс-спектр М+ = 376
Пример 2
3-[4-(2-карбоксиэтил)фенил]-1-(1-хлоризохинолин-6-ил)- имидазолидин-2-он
1 г 1-(1-хлоризохинолин-6-ил)-3-[4-[2-(метоксикарбонил)этил]- фенил]-имидазолидин-2-она, 100 мл диоксана, 80 мл воды и 8,5 мл 1 н. натрового щелока перемешивают 3 часа при комнатной температуре. Добавляют 9 мл 1 н. соляной кислоты, смесь сгущают и осадок отсасывают. Продукт промывают водой и сушат при 50oC.
Выход: 0,78 г (80% теории)
Точка плавления: 236 - 240oC (разл.)
Значение Rf: 0,36 (силикагель; смесь метиленхлорида, метанола и этилацетата в соотношении 20:1:1)
Аналогичным образом получают следующие соединения:
(1) 1-[4-(2-карбоксиэтил)фенил]-3-(изохинолин-6-ил)-3Н-имидазол- 2-он
Точка плавления: 305 - 310oC
Значение Rf: 0,49 (силикагель; смесь метиленхлорида и метанола в соотношении 9:1)
Рассчитано: C 70,18; H 4,77; N 11,69.
Найдено: C 69,95; H 4,93; N 11,64.
(2) 1-[4-(2-карбоксиэтил)фенил] -3-(1,2,3,4-тетрагидроизохинолин- 6-ил)-имидазолидин-2-он
Значение Rf: 0,44 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 67,54; H 6,21; N 11,25.
Найдено: C 67,58; H 6,42; N 11,23.
(3) 2-[транс-4-[2-(метоксикарбонил)этил] циклогексил] -5- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-3,4-дигидро-2Н,5Н-1,2,5- тиадизол-1,1-диоксид
Получение в смеси метанола и натрового щелока; исходное соединение: соединение примера 18.
Значение Rf: 0,36 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Пример 3
1-(1-хлоризохинолин-6-ил)-3-[4-[2-(метоксикарбонил)этил] фенил] - имидазолидин-2-он
2,2 г 1-(изохинолин-N-оксид-6-ил)-3-[4-[2-(метоксикарбонил)- этил]фенил] -имидазолидин-2-она и 25 мл оксихлорида фосфора 2 часа кипятят с обратным холодильником. Оксихлорид фосфора затем отгоняют и остаток подают на лед. Значение pH смеси добавкой насыщенного раствора бикарбоната натрия доводят до 8-9. Несколько раз экстрагируют метиленхлоридом, органические фазы сушат, сгущают и остаток очищают колоночной хроматографией на силикагеле с применением в качестве элюента смеси метиленхлорида и метанола в соотношении 20 : 1.
Выход: 1,0 г (43% теории)
Значение Rf: 0,66 (силикагель; смесь метиленхлорида и метанола в соотношении 20:1)
Пример 4
1-(изохинолин-6-ил)-3-[4-[2-(метоксикарбонил)этил] фенил] - имидазолидин-2-он
К раствору 3,0 г N-(2-гидроксиэтил)-N'-(изохинолин-6-ил)-N-[4- [2-(метоксикарбонил)этил] фенил-мочевины и 2,0 г трифенилфосфина в 105 мл ацетонитрила добавляют 1,31 мл сложного диэтилового эфира азодикарбоновой кислоты в 36 мл ацетонитрила при внутренней температуре 42-52oC. После перемешивания в течение 2 часов при 45oC охлаждают до -5oC и продолжают перемешивать еще 2 часа. Осадок отсасывают и промывают небольшим количеством холодного ацетонитрила.
Выход: 2,6 г (90% теории)
Точка плавления: 213 - 215oC
Значение Rf: 0,60 (силикагель; смесь метиленхлорида и метанола в соотношении 20:1)
Аналогичным образом получают следующие соединения:
(1) 1-(3-трет.бутилоксикарбонил-2,3,4,5-тетрагидро-1Н-3- бензацепин-7-ил)-3-[4-[2-(метоксикарбонил)этил]фенил]-имидазолидин-2-он
Точка плавления: 165 - 167oC
Значение Rf: 0,77 (силикагель; смесь метиленхлорида и этилацетата в соотношении 9:1)
(2) 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил]-3-(3- трифторацетил-2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-имидазолидин- 2-он
Точка плавления: 250 - 255oC (разл.)
Значение Rf: 0,45 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
(3) 1-[4-[транс-2-(метоксикарбонил)этенил] фенил]-3-(3- трифторацетил-2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-имидазолидин-2-он
Точка плавления: 216 - 220oC
Значение Rf: 0,38 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
(4) 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил]-3-(3- трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)- 3,4,5,6-тетрагидро-1Н-пиримидин-2-он
Точка плавления: 125 - 127oC
Значение Rf: 0,54 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 2)
Пример 5
1-(изохинолин-6-ил)-3-[4-[2-(метоксикарбонил)этил] фенил]-3Н- имидазол-2-он
7,3 г N-(2,2-диэтоксиэтил)-N'-(изохинолин-6-ил)-N-[4-[2- (метоксикарбонил)этил] фенил]-мочевины перемешивают 2 часа в 35 мл трифторуксусной кислоты при комнатной температуре. Затем частично сгущают и смешивают с ледяной водой. При перемешивании и охлаждении подщелачивают натровым щелоком, осадок отсасывают и промывают небольшим количеством метанола. Получаемый продукт перекристаллизовывают из метанола.
Выход: 4,45 г (76% теории)
Точка плавления: 158 - 161oC
Значение Rf: 0,29 (силикагель; смесь метиленхлорида и метанола в соотношении 95:5)
Рассчитано: C 70,76; H 5,13; N 11,25.
Найдено: C 70,52; H 5,08; N 11,35.
Аналогичным образом получают следующие соединения:
(1) 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил)-3-(3- трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-3Н-имидазол- 2-он
Получение путем сухого нагревания до 160 - 170oC.
Точка плавления: 121 - 124oC
Значение Rf: 0,35 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
(2) 1-[транс-4-[[(метоксикарбонил)метил]окси]циклогексил]-3-(3- трифторацетил-2,3,4,5-гетрагидро-1H-3-бензацепин-7-ил)-3Н-имидазол-2- он
Точка плавления: 148 - 149oC
Значение Rf: 0,28 (силикагель; смесь этилацетата и циклогексана в соотношении 2 : 1)
(3) 1-[4-[2-{ этоксикарбонил)-1-пропил] фенил)-3-(3-трифторацетил- 2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-3Н-имидазол-2-он
Значение Rf: 0,32 (силикагель; смесь циклогексана и этилацетата в соотношении 2 : 1)
(4) 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил] -3-(3-этил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-3H-имидазол-2-он
Значение Rf: 0,30 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
(5) 1-(транс-4-[2-(метоксикарбонил)этил] циклогексил)-3-(7-этил- 6,7,8,9-тетрагидро-5Н-пиразино[2,3-d]ацепин-2-ил)-3Н-имидазол-2-он
Точка плавления: 135 - 136oC
Рассчитано: C 64,61; H 7,78; N 16,38.
Найдено: C 64,82; H 7,84; N 16,27.
(6) 1-[4-[2-(этоксикарбонил)-1-фенил-этил] фенил]-3-(3- трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-3Н-имидазол- 2-он
Значение Rf: 0,24 (силикагель; смесь циклогексана и этилацетата в соотношении 7 : 3)
(7) 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил] -3-(7-бензил- 6,7,8,9-тетрагидро-5Н-пиримидо[4-5-d]ацепин-2-ил) -3Н-имидазол-2-он
Точка плавления: 131 - 134oC
Значение Rf: 0,38 (силикагель; смесь метиленхлорида и метанола в соотношении 20 : 1)
Пример 6
Ацетат 1-[4-[2-(метоксикарбонил)этил]фенил]-3-(1,2,3,4-тетрагидро- изохинолин-6-ил)-имидазолидин-2-она
2,0 г 1-(изохинолин-6-ил)-3-[4-[2-(метоксикарбонил)этил]фенил]- 3Н-имидазол-2-она в 50 мл ледяной уксусной кислоты гидрируют при давлении 3,52 кг/см на 0,5 г окиси платины при комнатной температуре в течение 40 минут. Фильтруют от катализатора, сгущают и остаток подвергают перекристаллизации из метанола.
Выход: 1,7 г (72% теории)
Точка плавления: 170 - 173oC (разл.)
Рассчитано: C 65,59; H 6,65; N 9,56.
Найдено: C 65,90; H 6,78; N 9,69.
Значение Rf: 0,30 (силикагель; смесь толуола, диоксана, метанола и конц. водного аммиака в соотношении 20 : 50 : 20 : 5)
Масс-спектр: М+ = 379
Аналогичным образом получают следующие соединения:
(1) 1-[транс-4-(2-карбоксиэтил] циклогексил] -3-(3-метил- 2,3,4,5,5а, 6,7,8,9,9а-декагидро-1Н-3-бензацепин-7-ил)-имидазолидин- 2-он x 1,35 HCl x 1,9 H2O
Получение в смеси диоксана и воды с применением платиново-родиевого катализатора.
В качестве исходного соединения применяют соединение примера 19.
Масс-спектр: М+ = 405
Рассчитано: С 56,49; H 9,10; N 8,59; Cl 9,79.
Найдено: C 56,63; H 8,81; N 8,60; Cl 9,92.
(2) 1-[транс-4-(2-карбоксиэтил]циклогексил]-3- (2,3,4,5,5а,6,7,8,9,9а-декагидро-1Н-3-бензацепин-7-ил)-имидазолидин- 2-он x 1,05 HCl x 0,9 H2O
Получение в смеси диоксана и воды с применением платиново-родиевого катализатора.
В качестве исходного соединения применяют соединение примера 14 (1).
Масс-спектр: М+ = 391
Рассчитано: C 59,43; H 9,03; N 9,45; Cl 8,05.
Найдено: C 59,49; H 8,83; N 9,35; Cl 8,30.
Пример 7
Гидрохлорид 1-[4-(2-(изобутилоксикарбонил)этил] фенил]-3- (1,2,3,4-тетрагидроизохинолин-6-ил)-имидазолидин-2-она x 1H2O
Над суспензией 150 мг 1-[4-(2-карбоксиэтил)фенил]-3-1,2,3,4-тетрагидроизохинолин-6-ил)- имидазолидин-2-она в 4,6 мл изобутанола при перемешивании в течение 30 минут пропускают соляную кислоту. Перемешивают в течение ночи при комнатной температуре, смешивают с ацетоном и отсасывают осадок. Продукт суспендируют в ацетоне, отсасывают, промывают ацетоном и диэтиловым эфиром и сушат.
Выход: 140 мг (77% теории)
Рассчитано: C 65,56; H 7,04; N 9,18; Cl 7,74.
Найдено: C 65,38; H 7,03; N 9,47; Cl 7,92.
Значение Rf: 0,19 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного раствора поваренной соли в соотношении 6 : 4)
Масс-спектр: М+ = 421
Аналогичным образом получают следующие соединения:
(1) Гидрохлорид 1-[4-[2-(изопропилоксикарбонил)этил]фенил]-3- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-она
Рассчитано: C 63,08; H 7,20; N 8,83; Cl 7,45.
Найдено: C 62,79; H 7,14; N 8,83; Cl 7,80.
Значение Rf: 0,21 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного раствора поваренной соли в соотношении 6 : 4)
Масс-спектр: М+ = 421
(2) Гидрохлорид 1-[4-[2-(метоксикарбонил)этил] фенил] -3-(3-метил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-она x 0,75H2O
Точка плавления: 248 - 250oC
Рассчитано: C 63,01;H 6,94,; N 9,19; Cl 7,75.
Найдено: C 63,09; H 6,98; N 9,22; Cl 7,88.
Значение Rf: 0,28 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного раствора поваренной соли в соотношении 6 : 4)
(3) Гидрохлорид 1-[4-[2-(этоксикарбонил)этил] фенил] -3-(3-метил- 2,3,4,5-гетрагидро-3H-3-бензацепин-7-ил)-имидазолидин-2-она
Значение Rf: 0,22 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного раствора поваренной соли в соотношении 6 : 4)
(4) Гидрохлорид 1-[4-[2-(изопропилоксикарбонил)этил]фенил]-3-(3-метил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-она
Значение Rf: 0,19 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного раствора поваренной соли в соотношении 6 : 4)
(5) Гидрохлорид 1-[транс-4-[2-(изопропилоксикарбонил)этил] циклогексил] -3-(3-метил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)- имидазолидин-2-она
Использование тионилхлорида и хлористого водорода.
Точка плавления: > 250oC
Значение Rf: 0,17 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 65,32; H 8,43; N 8,79; Cl 7,42.
Найдено: С 65,10; H 8,41; N 8,91; Cl 7,66.
(6) Гидрохлорид 1-[транс-4-[2-(этоксикарбонил)этил]циклогексил]- 3-(3-метил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин- 2-она
Использование тионилхлорида и хлористого водорода.
Точка плавления: > 250oC
Значение Rf: 0,24 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 64,71; H 8,25; N 9,09; Cl 7,64.
Найдено: C 64,09; H 8,22; N 9,08; Cl 7,72.
(7) Гидрохлорид 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил]- 3-(3-метил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-она
Использование тионилхлорида и хлористого водорода.
Точка плавления: > 250oC
Значение Rf: 0,29 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 64,05; H 8,04; N 9,34; Cl 7,88.
Найдено: C 64,10; H 7,97; N 9,52; Cl 8,11.
(8) Гидрохлорид 1-[транс-4-[2-(изопропилоксикарбонил)этил] циклогексил] -3-(2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин- 2-она
Использование тионилхлорида и хлористого водорода.
Значение Rf: 0,20 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного раствора поваренной соли в соотношении 6 : 4)
(9) Гидрохлорид 1-[транс-4-[2-(этоксикарбонил)этил] циклогексил] - 3-(2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-она
Использование тионилхлорида и хлористого водорода.
Значение Rf: 0,23 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 64,05; H 8,06; N 9,34; Cl 7,88.
Найдено: C 63,77; H 8,23 N 9,07; Cl 7,91.
(10) Гидрохлорид 1-[транс-4-[2-(метоксикарбонил)этил]циклогексил]- 3-(2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-имидазолидин-2-она
Использование тионилхлорида и хлористого водорода.
Значение Rf: 0,26 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 63,36; H 7,86; N 9,64; Cl 8,13.
Найдено: C 63,34; H 7,88; N 9,73; Cl 8,11.
Пример 8
1-[4-(2-карбоксиэтил)фенил] -3-(2-метил- 1,2,3,4-тетрагидроизохинолин-6-ил)-имидазолидин-2-он x 0,2H2O
350 мг ацетата 1-[4-[2-(метоксикарбонил)этил]фенил]-3- (1,2,3,4-тетрагидроизохинолин-6-ил)-имидазолидин-2-она, 0,7 мл воды, 0,15 мл муравьиной кислоты и 0,7 мл 37%-ного водного раствора формальдегида перемешивают в течение часа при 65oC. Добавляют толуол и сгущают. Смешивают с толуолом и еще раз упаривают. Остаток смешивают с 2 мл тетрагидрофурана, 1 мл воды и 0,8 мл 4 н. натрового щелока при комнатной температуре в течение 2,5 суток. Добавляют 220 мг хлористого аммония в 1 мл воды и перемешивают 2 часа. Реакционную смесь отчасти упаривают в ротационном испарителе, охлаждают льдом, твердый продукт отсасывают, после чего промывают его водой, ацетоном и диэтиловым эфиром, а затем сушат.
Выход: 220 мл (72% теории)
Точка плавления: 245 - 248oC
Рассчитано: C 68,98; H 6,68; N 10,97.
Найдено: C 68,91; H 6,69; N 10,92.
Значение Rf: 0,41 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного раствора поваренной соли в соотношении 6 : 4)
Масс-спектр: М+ = 379
Аналогичным образом получают следующее соединение:
Гидрохлорид 1-[4-(2-(карбоксиэтил)фенил] -3-(3-метил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-она x 1,5 воды
Последующее расщепление сложного эфира осуществляют смесью ледяной уксусной кислоты и соляной кислоты (вместо натровым щелоком).
Рассчитано: С 60,45; H 6,84; N 9,20; Cl 7,76.
Найдено: C 60,45; H 6,86; N 9,18; Cl 8,09.
Значение Rf: 0,31 (силикагель; смесь метиленхлорида, метанола и конц. водного аммиака в соотношении 4 : 1 : 0,2)
Масс-спектр: М+ = 393
Пример 9
1-[4-(2-(карбоксиэтил)фенил] -3- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-он
800 мг гидрохлорида 1-[4-[2-(метоксикарбонил)этил]фенил]-3- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-она смешивают с 10 мл полуконцентрированной соляной кислоты и 10 мл ледяной уксусной кислоты. По истечении 2 часов добавляют еще 5 мл полуконцентрированной соляной кислоты и 5 мл ледяной уксусной кислоты и перемешивают при комнатной температуре в течение ночи. Реакционную смесь упаривают и остаток суспендируют в 10 мл воды. Добавкой 2 н. натрового щелока pH доводят до 6, твердый продукт отсасывают, промывают ледяной водой и затем сушат.
Выход: 560 мг (79% теории)
Значение Rf: 0,40 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Масс-спектр: М+ = 379
Аналогичным образом получают следующие соединения:
(1) Гидрохлорид 1-[4-(2-(карбоксиэтил)фенил] -3-(4аRS, 6RS, 8аRS)-1,2,3,4,4а,5,6,7,8,8а- декагидроизохинолин-6-ил)-имидазолидин-2-она
Выделение в качестве гидрохлорида
Значение Rf: 0,41 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Масс-спектр: М+ = 371
(2) Гидрохлорид 1-[4-(2-карбоксиэтил)фенил] -3-(3-этил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-она
Значение Rf: 0,36 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Масс-спектр: М+ = 407
(3) Гидрохлорид 3-[транс-4-(2-(карбоксиэтил)циклогексил]-1- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-гидантоина
Точка плавления: > 250oC
Значение Rf: 0,36 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 60,61; H 6,94; N 9,64; Cl 8,13.
Найдено: C 60,45; H 6,90; N 9,61; Cl 8,28.
(4) 1-[транс-4-(2-(карбоксиэтил)циклогексил] -3-(7-этил- 6,7,8,9-тетрагидро-5Н-пиридазино[2,3-d]ацепин-2-ил)-имидазолидин-2-он x 2HCl x 0,9H2O
Точка плавления: 283 - 286oC
Значение Rf: 0,46 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 52,36; H 7,35; N 13,88; Cl 14,05.
Найдено: C 52,70; H 7,44; N 13,86; Cl 14,01.
(5) Гидрохлорид 1-[транс-4-(2-(карбоксиэтил)циклогексил] -3-(3-этил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-3Н-имидазол-2-она x 0,5 H2О
Значение Rf: 0,38 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 63,08; H 7,22; N 9,19; Cl 7,76.
Найдено: C 63,26; H 7,69; N 9,28; Cl 7,64.
(6) Гидрохлорид 1-[транс-4-(2-(карбоксиэтил)циклогексил]-3- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-гидантоина
Значение Rf: 0,16 (силикагель; смесь метиленхлорида, метанола и конц. водного аммиака в соотношении 80 : 20 : 2)
Рассчитано: C 60,61; H 6,94; N 9,64; Cl 8,13.
Найдено: C 60,34; H 6,94; N 9,58; Cl 8,27.
(7) 1-[транс-4-(2-карбоксиэтил)циклогексил]-3- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-3,4,5,6-тетрагидро-1Н- пиримидин-2-он x 1,65HCl x 0,7H2О
Точка плавления: 230 - 235oC
Значение Rf: 0,40 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 58,27; H 7,71; N 8,86; Cl 12,33.
Найдено: C 58,04; H 7,70; N 8,82; Cl 12,43.
(8) Гидрохлорид 1-(2-карбоксиэтил)-3-[4-(3-метил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил) фенил]-имидазолидин-2-она
Точка плавления: > 250oC
Значение Rf: 0,20 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
(9) Гидрохлорид 1-[транс-4-(2-карбоксиэтил)циклогексил]-3-(6,7,8,9-тетрагидро-5Н- пиримидо[4,5-d]ацепин-2-ил)-имидазолидин-2-она
Значение Rf: 0,60 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
(10) Гидрохлорид 1-[транс-4-(2-карбоксиэтил)циклогексил] -3-(3- этил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-она
Точка плавления: > 270oC
Значение Rf: 0,35 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
(11) 1-[транс-4-(2-карбоксиэтил)циклогексил]-3-(3-пропил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-он x 1,07HCl x 1H2О
Точка плавления: > 250oC
Значение Rf: 0,32 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 61,96; H 8,33; N 8,67; Cl 7,83.
Найдено: C 62,10; H 8,14; N 8,77; Cl 7,94.
(12) 1-[транс-4-(2-карбоксиэтил)циклогексил] -3-(3-аллил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-он x 1,1 HCl x 1,5H2O
Точка плавления: > 250oC
Значение Rf: 0,30 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4) \
Рассчитано: C 60,94; H 8,00; N 8,53; Cl 7,91.
Найдено: C 61,32; H 7,63; N 8,47; Cl 7,82.
(13) Гидрохлорид 1-[транс-4-(2-карбоксиэтил)циклогексил]-3-[3- (2-гидроксиэтил)-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил]- имидазолидин-2-она
Точка плавления: 257 - 260oC
Значение Rf: 0,46 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
(14) Гидрохлорид 1-[транс-4-(2-карбоксиэтил)циклогексил]-3-[3- (карбоксиметил)-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил]-имидазолидин- 2-она
Точка плавления: > 280oC
Значение Rf: 0,39 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
(15) Гидрохлорид 1-[транс-4-(2-карбоксиэтил)циклогексил]-3-(3- бензил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил]-имидазолидин-2-она
Точка плавления: > 250oC
Значение Rf: 0,21 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
(16) Гидрохлорид 1-[транс-4-(2-карбоксиэтил)циклогексил]-3-[3- (циклопропилметил)-2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил] - имидазолидин-2-она
Точка плавления: > 280oC
Значение Rf: 0,31 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Пример 10
Гидрохлорид 1-[4-[2-(метоксикарбонил)этил] фенил]-3- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил]-имидазолидин-2-она
2,3 г 1-(3-трет.бутилоксикарбонил-2,3,4,5-тетрагадро-1Н-3- бензацепин-7-ил)-3-[4-[2-(метоксикарбонил)этил] фенил]-имидазолидин- 2-она перемешивают в 30 мл метанольной соляной кислоты в течение 2 часов при комнатной температуре. Реакционную смесь упаривают, остаток смешивают с ледяной водой, отсасывают, промывают небольшим количеством метанола и трет.бутилметиловым эфиром, а затем сушат.
Выход: 1,8 г (90% теории)
Рассчитано: C 64,25; H 6,56; N 9,77; Cl 8,25.
Найдено: C 64,08; H 6,60; N 9,92; Cl 8,51.
Значение Rf: 0,26 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Масс-спектр: М+ = 393
Пример 11
Гидрохлорид 1-[(4aRS, 6RS, 8aRS)- 1,2,3,4,4a,5,6,7,8,8a-декагидроизохинолин-6-ил]-3-[4-[2- (метоксикарбонил)этил]фенил]-имидазолидин-2-она
К 216 мг 1-[4-[2-(метоксикарбонил)этил]фенил]-3-[(4аRS,6RS,8аRS)- 2-метил-1,2,3,4,4а, 5,6,7,8,8а-декагидроизохинолин-6-ил]-имидазолидин- 2-она и 185 мг 1,8-бис-(диметиламино)-нафталина в 5 мл 1,2-дихлорэтана добавляют 0,09 мл сложного 1-хлорэтилового эфира хлормуравьиной кислоты, перемешивают 20 минут при комнатной температуре и потом нагревают 2,5 часа с обратным холодильником. Реакционную смесь сгущают, остаток смешивают с 10 мл метанола и нагревают 3 часа с обратным холодильником. Реакционную смесь подкисляют метанольной соляной кислотой, сгущают и очищают путем колоночной хроматографии на силикагеле с применением в качестве элюента смеси метиленхлорида и метанола в соотношении 92:8.
Выход: 200 мг (87% теории)
Значение Rf: 0,35 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Пример 12
1-(4-[2-(метоксикарбонил)этил] фенил] -3-[(4аRS, 6RS, 8аRS)- 2-метил-1,2,3,4,4а,5,6,7,8,8а-декагидроизохинолин-6-ил]-имидазолидин- 2-он
950 мг 1-[4-[2-(метоксикарбонил)этил] фенил] -3-[(4аRS,6RS,8аRS)-2-метил-1,2,3,4,4а, 5,6,7,8,8а-декагидроизохинолин-6-ил]-3Н-имидазол- 2-она в 50 мл этилацетата гидрируют при давлении водорода 3,52 кг/см2 в присутствии палладия на активном угле в течение 5 часов при комнатной температуре, а затем в течение 5 часов при 50oC. Катализатор фильтруют и фильтрат сгущают. Остаток кратковременно нагревают в присутствии трет.бутил-метилового эфира, потом при перемешивании охлаждают. Твердый продукт отсасывают, промывают трет.бутил-метиловым эфиром и сушат.
Выход: 300 мг (31% теории)
Точка плавления: 155 - 157oC
Значение Rf: 0,29 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Аналогичным образом получают следующие соединения:
(1) 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил]-3-(3- трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил]-имидазолидин- 2-он
Точка плавления: 165 - 168oC
Значение Rf: 0,44 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
(2) 1-[транс-4-[[(метоксикарбонил)метил]окси]циклогексил]-3-(3- трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил]-имидазолидин- 2-он
Точка плавления: 146 - 147oC
Значение Rf: 0,62 (силикагель; смесь этилацетата и циклогексана в соотношении 3 : 1)
(3) 1-[4-[2-(этоксикарбонил)-1-пропил] фенил] -3-(3-трифторацетил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил]-3Н-имидазолидин-2-он
Значение Rf: 0,32 (силикагель; смесь циклогексана и этилацетата в соотношении 2 : 1)
(4) 1-[2-[4-(метоксикарбонил)фенил]этил]-3-(3-трифторацетил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил]-имидазолидин-2-он
Точка плавления: 143 - 144oC
Значение Rf: 0,46 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
(5) Гидрохлорид 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил] -3-(3-этил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил]-имидазолидин-2-она
Точка плавления: начиная с 230oC (разл.)
Значение Rf: 0,22 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
(6) 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил] -3-(7-этил- 6,7,8,9-тетрагидро-5Н-пиразино[2,3-d]ацепин-2-ил]-имидазолидин-2-он
Точка плавления: 136 - 138oC
Значение Rf: 0,33 (силикагель; смесь метиленхлорида и метанола в соотношении 9:1)
(7) 1-[4-[2-(этоксикарбонил)-1-фенил-этил] фенил]-3-(3- трифторацетил-2,3,4,5-тетрагидро-1H-бензацепин-7-ил]-имидазолидин-2-он
Значение Rf: 0,22 (силикагель; смесь циклогексана и этилацетата в соотношении 7 : 3)
Пример 13
1-[4-[2-(метоксикарбонил)этил] фенил] -3-[(4аRS, 6RS, 8аRS)-2-метил- 1,2,3,4,4а,5,6,7,8,8а-декагидроизохинолин-6-ил]-3Н-имидазол-2-она
К 6,9 г (4аRS,6RS,8аRS)-6-[(2,2-диметоксиэтил)амино]-2-метил- 1,2,3,4,4а, 5,6,7,8,8а-декагидроизохинолина в 30 мл диоксана добавляют 6,4 г 4-[2-(метоксикарбонил)этил] -фенилизоцианата и перемешивают 2 часа при комнатной температуре. Реакционную смесь сгущают, подают в 100 мл метанола, смешивают с метанольной соляной кислотой и нагревают 20 минут с обратным холодильником. Реакционную смесь сгущают и остаток перемешивают с 200 мл водой. Отсасывают от осадка и фильтрат экстрагируют этилацетатом. Органическую фазу удаляют. Водную фазу подщелачивают раствором карбоната калия и несколько раз экстрагируют этилацетатом. Объединенные экстракты этилацетата промывают насыщенным раствором поваренной соли, сушат и сгущают. Сырой продукт очищают путем колоночной хроматографии на основной окиси алюминия с применением в качестве элюента этилацетата и последующим растиранием вместе с трет.бутил-метиловым эфиром.
Выход: 1,03 г (9% теории)
Значение Rf: 0,55 (силикагель; смесь толуола, диоксана, метанола и конц. водного аммиака в соотношении 20 : 50 : 20 : 5)
Аналогичным образом получают следующие соединения:
(1) 1-[4-[2-(метоксикарбонил)этил] фенил]-3-[(4аRS,6RS,8аRS)-2- метил-1,2,3,4,4а,5,6,7,8,8а-декагидроизохинолин-6-ил]-3Н-имидазол-2-он x 0,3H20
Точка плавления: 140 - 145oC
Рассчитано: C 68,56; H 7,91; N 10,43.
Найдено: C 68,49; H 7,97; N 10,51.
(2) 1-[2-[4-(метоксикарбонил)фенил] этил]-3-(3-трифторацетил- 2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил]-3Н-имидазол-2-он
Амин и изоцианат перемешивают в диоксане сначала при комнатной температуре, затем на паровой бане. В отличие от примера 13 реакционную смесь не обрабатывают метанольной соляной кислотой. Исходный [2-[4-(метоксикарбонил)фенил] этил]-изоцианат получают в результате взаимодействия соответствующего амина в виде гидрохлорида с фосгеном.
Точка плавления: 165 - 167oC
Значение Rf: 0,31 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
Пример 14
Гидрат гидрохлорида 4-[4-[2-(карбоксиэтил)фенил]-5-метил-2- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-4Н-1,2,4-триазол-3-она
410 мг 4-[4-[2-(метоксикарбонил)этил]фенил]-5-метил]-2-(3- трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-4Н-1,2,4- триазол-3-она смешивают с 10 мл ледяной уксусной кислоты и 10 мл полуконцентрированной соляной кислоты в течение 7 часов при 90oC. После охлаждения упаривают, остаток перемешивают с водой, отсасывают и промывают водой и ацетоном.
Выход: 240 мг (57% теории)
Точка плавления: > 250oC
Значение Rf: 0,43 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 59,12; H 6,09; N 12,53; C l7,93.
Найдено: C 58,96; H 6,13; N 12,31; Cl 7,74.
Аналогичным образом получают следующие соединения:
(1) Гидрохлорид 1-[транс-4-(2-карбоксиэтил)циклогексил]-3- (2,3,4,5-тетрагидро-1Н-3-бензацеgин-7-ил]-имидазолидин-2-она
Точка плавления: > 250oC
Значение Rf: 0,46 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 62,62; H 7,64; N 9,98; Cl 8,40.
Найдено: C 62,24; H 7,67; N 10,01;Cl 8,86.
(2) 2-[транс-4-(2-карбоксиэтил)циклогексил]-5- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил]-3,4-дигидро-2Н,5Н- 1,2,5-тиадиазол-1,1-диоксид
Значение Rf: 0,50 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
(3) Гидрохлорид 1-[транс-4-[(карбоксиметил)окси] циклогексил] -3- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил]-имидазолидин-2-она
Точка плавления: 316 - 317oC (разл.)
Значение Rf: 0,66 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 59,50; H 7,13; N 9,91; Cl 8,36.
Найдено: C 59,26; H 7,13; N 9,94; Cl 8,44.
(4) Гидрохлорид 1-[4-(транс-2-карбоксиэтенил]фенил]-3- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил]-имидазолидин-2-она
Значение Rf: 0,64 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Масс-спектр: М+ = 377
(5) Гидрохлорид 1-[4-(2-карбокси-1-пропил)фенил]-3- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил]-имидазолидин-2-она x H2O
Значение Rf: 0,34 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 61,66; H 6,71; N 9,38; Cl 7,91.
Найдено: С 61,56; H 6,75; N 9,30; Сl 8,14.
(6) Гидрохлорид 2-[транс-4-(2-карбоксиэтил)циклогексил]-4- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-4Н-1,2,4-триазол-3-она
Получение с использованием 2 н. соляной кислоты
Исходное соединение: соединение примера 18 (1)
Точка плавления: > 220oC
Значение Rf: 0,50 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 59,92; H 6,94; N 13,31; Cl 8,42.
Найдено: C 60,03; H 6,99; N 13,32; Cl 8,46.
(7) Гидрохлорид 4-[транс-4-(2-карбоксиэтил)циклогексил] -2- (2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-4Н-1,2,4-триазол-3-она
Точка плавления: > 240oC
Значение Rf: 0,64 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
(8) Гидрохлорид 4-[транс-4-(2-карбоксиэтил)циклогексил] -2- (2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-5-метил-4Н-1,2,4-триазол- 3-она
Значение Rf: 0,48 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 60,75; H 7,18; N 12,88; Cl 8,15.
Найдено: C 60,54; H 7,26; N 12,68; Cl 8,54.
(9) Гидрохлорид 1-[4-(2-карбокси-1-фенил-этил)фенил] -3- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-она
Значение Rf: 0,31 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
(10) Гидрохлорид 1-[2-(4-карбоксифенил)этил)-3- (2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-имидазолидин-2-она x H2О
Значение Rf: 0,40 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Масс-спектр: М+ = 379
Рассчитано: C 60,89; H 6,50; N 9,68; Cl 8,17.
Найдено: C 60,57; H 6,62; N 9,77; Cl 8,22.
Пример 15
4-[4-[2-(метоксикарбонил)этил] фенил] -5-метил-2-(3-трифторацетил- 2,3,4,5-гетрагидро-1Н-3-бензацепин-7-ил)-4Н-1,2,4-триазол-3-он
1,6 г 7-йод-3-трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепина, 1,1 г 4-[4-[2-(метоксикарбонил)этил] фенил] -5-метил-4Н-1,2,4-триазол- 3-она, 0,19 мл трис-[2-(2-метоксиэтокси)этил] -амина, 130 мг хлорида меди (I), 130 мг йодида меди (I) и 1,1 г карбоната калия нагревают с обратным холодильником в 30 мл диметилформамида в течение 2 часов. После охлаждения упаривают и остаток распределяют между водой и хлористым метиленом. Твердый продукт отсасывают, органическую фазу отделяют, промывают водой, сушат, фильтруют и упаривают в ротационном испарителе. Остаток очищают путем колоночной хроматографии на силикагеле с применением в качестве элюента смеси циклогексана и этилацетата в соотношении 1 : 1.
Выход: 340 мг (16% теории)
Точка плавления: 160 - 162oC
Значение Rf: 0,51 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
Аналогичным образом получают следующие соединения:
(1) 4-[транс-4-[2-(метоксикарбонил)этил]циклогексил)-2-(3- трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-5-метил-4Н- 1,2,4-триазол-3-он
Точка плавления: 175 - 177oC
Значение Rf: 0,50 (силикагель; смесь метиленхлорида и этилацетата в соотношении 90:10)
(2) 4-[транс-4-[2-(метоксикарбонил)этил]циклогексил]-2-(3- трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-4Н- 1,2,4-триазол-3-он
Значение Rf: 0,40 (силикагель; смесь метиленхлорида и метанола в соотношении 100:1)
Пример 16
1-[транс-4-[2-(метоксикарбонил)этил] циклогексил] -3-(3- трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-гидантоин
К 4,1 г (3-трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7- ил)-изоцианата и 3,7 г гидрохлорида сложного метилового эфира [[транс-4-[2-(метоксикарбонил)-этил] циклогексил] амино-уксусной кислоты в 50 мл ацетонитрила добавляют 3,2 мл N-этил-диизопропиламина и перемешивают 2,5 суток при комнатной температуре. Реакционную смесь сгущают, остаток подают в этилацетат и промывают водой и раствором поваренной соли. Органическую фазу сушат, сгущают и остаток кристаллизуют небольшим количеством метанола на ледяной бане. Продукт отсасывают, промывают холодным метанолом и сушат.
Выход: 4,1 г (56% теории)
Точка плавления: 118 - 120oC
Значение Rf: 0,85 (силикагель; этилацетат)
Пример 17
Гидрохлорид 1-[транс-4-[2-(изопропоксикарбонил)этил] циклогексил] - 3-(3-пропил-2,3,4,5-гетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин- 2-она
230 мг гидрохлорида 1-[транс-4-[2-(изопропоксикарбонил)этил] циклогексил]-3-(3-аллил-2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)- имидазолидин-2-она гидрируют в 10 мл изопропанола при давлении водорода 3,52 кг/см2 на 50 мг 10%-ного палладия на активном угле при температуре 30oC в течение 6 часов. Катализатор отсасывают и фильтрат упаривают.
Выход: 240 мг
Значение Rf: 0,55 (силикагель; смесь метиленхлорида, метанола и конц. водного аммиака в соотношении 95 : 5 : 1)
Пример 18
2-[транс-4-[2-(метоксикарбонил)этил] циклогексил] -5-(3- трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-3,4-дигидро- 2Н, 5Н-1,2,5-тиадиазол-1,1-диоксид
К 1,25 г 2-(3-трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин- 7-ил)-3,4-дигидро-2Н, 5Н-1,2,5-тиадиазол-1,1-диоксида, 0,64 г сложного метилового эфира 3-(цис-4-гидроксициклогексил)пропионовой кислоты [значение Rf: 0,58 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1), выделившегося из смеси цис- и транс- изомеров путем колоночной хроматографии на силикагеле с применением в качестве элюента смеси циклогексана и этилацетата в соотношении 1 : 1)] и 0,90 г трифенилфосфина в 2 мл ацетонитрила прикапывают 0,54 мл сложного диэтилового эфира азодикарбоновой кислоты. Добавляют еще 1,5 г сложного метилового эфира 3-(цис- 4-гидроксициклогексил)пропионовой кислоты, а также смесь 0,90 г трифенилфосфина и 0,54 мл сложного диэтилового эфира азодикарбоновой кислоты в 2 мл ацетонитрила. После 30-минутного перемешивания при комнатной температуре добавляют еще раз смесь 0,90 г трифенилфосфина и 0,54 мл сложного диэтилового эфира азодикарбоновой кислоты. После перемешивания при комнатной температуре в течение ночи упаривают в ротационном испарителе и остаток очищают путем колоночной хроматографии на силикагеле с применением в качестве элюента смеси циклогексана, этилацетата и метиленхлорида в соотношении 1 : 1 : 1.
Выход: 700 мг (38% теории)
Точка плавления: 169 - 173oC
Значение Rf: 0,61 (силикагель; смесь циклогексана, этилацетата и метиленхлорида в соотношении 1 : 1 : 1)
Аналогичным образом получают следующие соединения:
(1) 2-[транс-4-[2-(метоксикарбонил)этил] циклогексил] -4-(3- трет.бутилоксикарбонил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-4Н- 1,2,4-триазол-3-он
Точка плавления: 162 - 164oC
Значение Rf: 0,43 (силикагель; смесь циклогексана, этилацетата и метиленхлорида в соотношении 1 : 1 : 1)
Пример 19
Гидрохлорид 1-[транс-4-(2-карбоксиэтил)циклогексил] -3-(3-метил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-она
К смеси 5,0 г гидрохлорида 1-[транс-4-(2-карбоксиэтил) циклогексил]-3-(2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин- 2-она, 4,5 мл муравьиной кислоты, 3,6 мл 37%-ного водного формальдегида и 20 мл воды добавляют при охлаждении льдом 2,0 г бикарбоната натрия и нагревают до 65oC. После 8 часов охлаждают, перемешивают в течение ночи и смесь упаривают на ротационном испарителе. Остаток перемешивают с водой и еще раз упаривают. Затем остаток опять перемешивают с водой и добавкой соляной кислоты доводят до pH 1. Упаривают на ротационном испарителе, остаток смешивают с небольшим количеством воды и отсасывают. Фильтровальный осадок смешивают с ацетоном, продукт отсасывают, промывают ацетоном и сушат в вакууме.
Выход: 3,7 г (71% теории)
Точка плавления: 292 - 295oC (разл.)
Значение Rf: 0,38 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Аналогичным образом получают следующие соединения:
(1) Гидрохлорид 1-[транс-4-[(карбоксиметил)окси]циклогексил]- 3-(3-метил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-она x NaCl x 0,5H2O
Значение Rf: 0,62 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4).
Рассчитано: C 52,28; H 6,58; N 8,31; Cl 13,49.
Найдено: C 52,28; H 6,68; N 8,33; Cl 14,03.
(2) Гидрохлорид 1-[4-(2-карбокси-1-пропил)фенил]-3-(3-метил- 2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-имидазолидин-2-она x 0,5 H2O
Значение Rf: 0,29 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: С 63,63; H 6,90; N 9,28; Cl 7,83.
Найдено: C 63,32; H 6,99; N 9,32; Cl 7,81.
(3) Гидрохлорид 3-[транс-4-(2-карбоксиэтил)циклогексил] -1-(3- метил-2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-гидантоина
Точка плавления: > 250oC
Значение Rf: 0,32 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4).
Рассчитано: C 61,39; H 7,17; N 9,34; Cl 7,88.
Найдено: C 61,39; H 7,25; N 9,37; Cl 7,92.
(4) Гидрохлорид 1-[транс-4-(2-карбоксиэтил)циклогексил] -3-(3- метил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-гидантоина
Значение Rf: 0,37 (силикагель; смесь метиленхлорида, метанола и конц. водного аммиака в соотношении 80 : 20 : 2).
Рассчитано: C 61,39; H 7,17; N 9,34; Cl 7,88.
Найдено: C 61,11; H 7,26; N 9,36; Cl 7,86.
(5) Гидрохлорид 2-[транс-4-(2-карбоксиэтил)циклогексил] -4-(3- метил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-4Н-1,2,4-триазол-3-она x 1,1H2O
Точка плавления: > 220oC
Значение Rf: 0,48 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4).
Рассчитано: C 58,10; H 7,36; N 12,32; Cl 7,80.
Найдено: C 58,07; H 7,36; N 12,28; Cl 7,83.
(6) Гидрохлорид 1-[транс-4-(2-карбоксиэтил)циклогексил] -3- (7-метил-6,7,8,9-тетрагидро-5Н-пиримидо-[4,5-d]ацепин-2-ил)- имидазолидин-2-она
Значение Rf: 0,56 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4).
Масс-спектр: М+ = 401
(7) 4-[транс-4-(2-карбоксиэтил)циклогексил] -2-(3-метил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-5-метил-4Н-1,2,4-триазол-3-он x 1,1HCl x 0,2H2O
Точка плавления: 238 - 240oC
Значение Rf: 0,37 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4).
Рассчитано: C 60,55; H 7,40; N 12,28; Cl 8,55.
Найдено: C 60,68, H 7,53; N 12,31; Cl 8,36.
(8) 1-[транс-4-(2-карбоксиэтил)циклогексил] -3-(3-метил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-3,4,5,6-тетрагидро-1Н- пиримидин-2-он x 1,05 HCl x 0,3H2O
Точка плавления: 237 - 240oC
Значение Rf: 0,37 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4).
Рассчитано: C 63,04; H 8,07; N 9,18; Cl 8,14.
Найдено: C 62,97; H 8,05; N 9,15; Cl 8,16.
Пример 20
1-(3-этил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-3-[4-[2- (метоксикарбонил)этил]фенил-имидазолидин-2-он
600 мг гидрохлорида 1-[4-[2-(метоксикарбонил)этил]фенил]-3- (2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-имидазолидин-2-она и 128 мг гидрида натрия (55%-ного в парафиновом масле) в 15 мл диметилформамида обрабатывают в ультразвуковой бане в течение 2,5 часов. Добавляют 125 мкл этилйодида и продолжают обработку в течение дополнительных 2,5 часов. Реакционную смесь смешивают с 50 мл воды, осадок отсасывают, промывают водой и сушат. Сырой продукт очищают путем колоночной хроматографии на силикагеле с применением в качестве элюента смеси метиленхлорида, метанола и конц. водного аммиака в соотношении 9 : 1 : 0,1.
Выход: 260 мг (44% теории)
Точка плавления: 168 - 170oC
Значение Rf: 0,45 (силикагель; смесь метиленхлорида, метанола и конц. водного аммиака в соотношении 4 : 1 : 0,2)
Аналогичным образом получают следующие соединения:
(1) 1-(3-бутил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-3-[4- [2-(метоксикарбонил)этил]фенил]-имидазолидин-2-он
Значение Rf: 0,64 (силикагель; смесь метиленхлорида, метанола и конц. водного аммиака в соотношении 4 : 1 : 0,2)
(2) Гидрохлорид 1-[транс-4-[2-(изопропоксикарбонил)этил] циклогексил]-3-(3-аллил-2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)- имидазолидин-2-она
Получение с применением смеси аллилбромида и N-этил-диизопропиламина в ацетонитриле
Значение Rf: 0,63 (силикагель; смесь метиленхлорида, метанола и конц. водного аммиака в соотношении 95 : 5 : 1)
(3) Гидрохлорид 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил]- 3-(3-бензил-2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-имидазолидин- 2-она
Значение Rf: 0,30 (силикагель; смесь метиленхлорида и метанола в соотношении 95 : 5)
(4) Гидройодид 1-(транс-4-[2-(метоксикарбонил)этил]циклогексил]- 3-[3-(циклопропилметил)-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)- имидазолидин-2-она
Получение в ацетонитриле с применением циклопропилметилбромида в присутствии йодида натрия и N-этил-диизопропиламина
Точка плавления: 225 - 230oC (разл.)
Значение Rf: 0,72 (силикагель; смесь метиленхлорида, метанола и конц. водного аммиака в соотношении 90 : 10 : 2)
(5) Гидройодид 1-[транс-4-[2-(метоксикарбонил)этил]циклогексил]- 3-[3-(2-гидроксиэтил)-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)- имидазолидин-2-она
Получение в ацетонитриле с применением 2-бромэтанола в присутствии йодида натрия и N-этил-диизопропиламина
Точка плавления: > 200oC
Значение Rf: 0,55 (силикагель; смесь метиленхлорида, метанола и конц. водного аммиака в соотношении 90 : 10 : 2)
(6) 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил]-3-[3- метоксикарбонилметил)-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)- имидазолидин-2-он
Получение в ацетонитриле с применением сложного метилового эфира 2-бромуксусной кислоты в присутствии йодида натрия и N-этил-диизопропиламина. Выделение свободного основания.
Точка плавления: 127 - 129oC
Значение Rf: 0,28 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Пример 21
Гидрохлорид 3-[транс-4-[2-(метоксикарбонил)этил] циклогексил] - 1-(2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-гидантоина
Над 920 мг 3-[транс-4-[2-(метоксикарбонил)этил] циклогексил] -1- (3-трифторацетил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-гидантоина в 50 мл метанола пропускают хлористый водород в течение 10 минут и потом нагревают с обратным холодильником в течение 5 часов. Охлаждают, продукт отсасывают, промывают метанолом и диэтиловым эфиром и сушат при 80oC. Выход: 770 мг (95% теории)
Точка плавления: > 250oC
Значение Rf: 0,23 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Аналогичным образом получают следующие соединения:
(1) Гидрохлорид 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил]- 3-(2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-гидантоина
Точка плавления: > 250oC
Значение Rf: 0,43 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 61,39; H 7,17; N 9,34; Cl 7,88.
Найдено: C 61,10; H 7,21; N 9,29; Cl 8,03.
(2) Гидрохлорид 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил]- 3-(2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-3,4,5,6-тетрагидро-1Н- пиримидин-2-она
Значение Rf: 0,31 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Пример 22
3-[транс-4-[2-(метоксикарбонил)этил] циклогексил] -1-(3- трифторацетил- 2,3,4,5-тетрагидро-1H-3-бензацепин-7-ил)-гидантоина
К 2,1 г N-[транс-4-[2-(метоксикарбонил)этил]циклогексил)-N'-[( бензилоксикарбонил)метил] -N'-(3-трифторацетил-2,3,4,5-тетрагидро-1Н- 3-бензацепин-7-ил)-мочевины в 25 мл кипящего толуола добавляют 40 мг трет.бутилата калия и нагревают с обратным холодильником в течение 30 минут. Реакционную смесь охлаждают, смешивают с несколькими каплями ледяной уксусной кислоты, сгущают и очищают путем колоночной хроматографии на силикагеле с применением в качестве элюента смеси циклогексана и этилацетата в соотношении от 8 : 2 до 7 : 3, а также путем кристаллизации из метанола.
Выход: 0,95 г (55% теории)
Точка плавления: 132 - 134oC
Значение Rf: 0,59 (силикагель; смесь циклогексана и этилацетата в соотношении 1 : 1)
Аналогичным образом получают следующие соединения:
(1) Гидрохлорид 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил]- 3-(2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-гидантоина
Точка плавления: > 250oC
Значение Rf: 0,43 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Рассчитано: C 61,39; H 7,17; N 9,34; Cl 7,88.
Найдено: C 61,10; H 7,21; N 9,29; Cl 8,03.
(2) Гидрохлорид 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил]- 3-(2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-3,4,5,6-тетрагидро-1Н- пиримидин-2-она
Значение Rf: 0,31 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Пример 23
1-[транс-4-[2-(метоксикарбонил)этил] циклогексил] -3-(6,7,8,9- тетрагидро-5Н-пиримидо[4,5-d]ацепин-2-ил)-имидазолидин-2-он
1,0 г 1-[транс-4-[2-(метоксикарбонил)этил] циклогексил]-3-(7- бензил-6,7,8,9-тетрагидро-5Н-пиримидо[4,5-d] ацепин-2-ил)-3Н-имидазол- 2-она гидрируют в 15 мл метанола при давлении водорода 3,52 кг/см2 в присутствии 500 мг палладия на активном угле (10% палладия) в течение 17 часов при комнатной температуре. Фильтруют от катализатора и фильтрат упаривают. Остаток непосредственно применяют для получения соединения примера 9 (16).
Значение Rf: 0,44 (обратнофазная хроматография на силикагеле; смесь метанола и 5%-ного водного раствора поваренной соли в соотношении 6 : 4)
Пример 24
1-[2-(этоксикарбонил)этил] -3-[4-(3-метил- 2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-фенил]-имидазолидин-2-он
3,1 г (3-метил-2,3,4,5-тетрагидро-1Н-3-бензацепин-7-ил)-борной кислоты, 4,1 г 1-[2-(этоксикарбонил)этил]-3-[4- (трифторметилсульфонилокси)фенил]-имидазолидин-2-она, 3,5 г тетракис-(трифенилфосфин)-палладия и 6,5 мл триэтиламина перемешивают в 25 мл диметилформамида в атмосфере азота в течение 4 часов при 100oC. Реакционную смесь охлаждают, сгущают в вакууме и остаток подают в хлористый метилен. Смесь фильтруют на кизельгуре, фильтрат сгущают и остаток очищают путем колоночной хроматографии на силикагеле с применением в качестве элюента смеси метиленхлорида и метанола в соотношении 100 : 7.
Выход: 2,7 г (63% теории)
Значение Rf: 0,31 (силикагель; смесь метиленхлорида и метанола в соотношении 100 : 7).
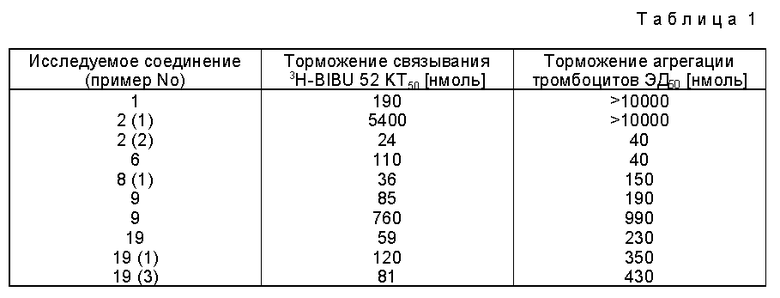
Новые гетероциклы формулы I, где Х - карбиминогруппа, замещенная у атома азота цианогруппой, карбонил, сульфонил, У - незамещенная или замещенная остатком Rc, Rd или Rc и Rd группа формулы - CH2-CH2-, -CH2-CH2-CH2-, -СН=СН-, CH2CO- или -СОСН2-, незамещенная радикалом Rc или Rd группа формулы -CO-NH-, -NH-CO-, -CH=N-, или -N=CH-, один из остатков Ra-Rd означает группу А-В-, в которой А - группа формул а-в (значения других радикалов см. в п.1 формулы изобретения). Соединения I, кроме противовоспалительного действия и тормозящего разложение костей действия обладают антитромботическим, антиагрегаторным, противоопухолевым и противометастазным действиями. 3 c. и 3 з. п.ф-лы, 2 табл.

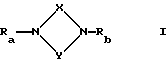
где X - карбиминогруппа, замещенная у атома азота цианогруппой, карбонил, сульфонил;
Y - незамещенная или замещенная остатком RcRd или Rc и Rd группа формулы -CH2-CH2-, -CH2-CH2-CH2-, -CH= CH-, -CH2CO- или -COCH2-, незамещенная или замещенная радикалом Rc или Rd группа формулы -CO-NH-, -NH-CO-, -CH=N- или -N=CH-,
один из остатков Ra - Rd означает группу A-B-, в которой A - группа формул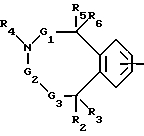
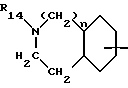
или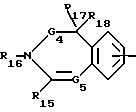
где бензоостаток указанных групп может быть замещен атомом фтора, хлора или брома, алкилом, алкоксилом, гидроксилом, трифторметилом или цианогруппой или 1 - 3 метиновые группы могут быть заменены атомом азота;
G1 - связь или метилен, который может быть моно- или дизамещен алкилом, причем заместители могут быть одинаковыми или различными;
G2 - связь или метилен, замещенный остатками R7 и R8;
G3 - метилен, замещенный остатками R9 и R10;
G4 - связь;
G5 - атом азота или метин, незамещенный или замещенный алкилом;
R2 - атом водорода или алкил;
R3 - атом водорода или алкил;
R4 - атом водорода, циклоалкил с 3 - 7 атомами углерода, циклоалкилалкил с 3 - 7 атомами углерода в циклоалкильной части, алкил с 1 - 6 атомами углерода, алкенил с 3 - 6 атомами углерода, который не может быть связан с атомом азота через винильную группу, гидроксиалкил, алкоксиалкил, карбоксиалкил, алкоксикарбонилалкил, аминокарбонилалкил, N-алкиламинокарбонилалкил, N, N-диалкиламинокарбонилалкил, арилалкил, алкоксикарбонил, арилметилоксикарбонил, формил, ацетил, трифторацетил или группа R11CO-O-(R12CR13)-O-CO-, где R11 - алкил с 1 - 4 атомами углерода, R12 - атом водорода или алкил, R13 - атом водорода, или R4 вместе с R3 означают неразветвленный алкилен с 2 или 3 атомами углерода;
R5 - атом водорода или алкил, или R4 вместе с R5 означают дополнительную связь, если G1 означает связь;
R6 - атом водорода, или алкил, или аминогруппа, если G1 означает связь и R4 вместе с R5 означают дополнительную связь;
R7 - атом водорода или алкил;
R8 - атом водорода или алкил, или R8 вместе с R4 означают неразветвленный алкилен с 3 или 4 атомами углерода;
R9 - атом водорода или алкил;
R10 - атом водорода или алкил, или R10 вместе с R4 означают неразветвленный алкилен с 3 или 4 атомами углерода;
R14 - атом водорода или алкил;
R15 - атом водорода или алкил;
R16 - атом водорода или алкил;
R17 - атом водорода или алкил, или R16 вместе с R17 означают дополнительную связь;
R18 - атом водорода, или алкил, или атом фтора, или амино, если R16 и R17 вместе означают дополнительную связь;
n = 1 или 2;
B - связь, алкилен, арилен, пиридинилен, пиримидинилен, пиразинилен или пиридазинилен, незамещенные или замещенные одной или двумя алкильными группами, циклогексилен, незамещенный или замещенный одной или двумя алкильными группами, незамещенный или замещенный одной или двумя алкильными группами пиперидинилен, в котором смежная с атомом азота метиленовая группа может быть заменена карбонилом,
второй из остатков Ra - Rd означает группу формулы
F-E-D-,
где D - алкилен с 1 - 4 атомами углерода, арилен, незамещенные или замещенные одной или двумя алкильными группами пиридинилен, пиримидинилен, пиразинилен и пиридазинилен, инданилен, нафтилен, 1,2,3,4-третрагидронафтилен или бензосуберанилен, в которых одно из колец связано с остатком E, а другое - с циклическим остатком общей формулы I, циклоалкилен с 4 - 7 атомами углерода, незамещенный или замещенный одной или двумя алкильными группами, незамещенный или замещенный одной или двумя алкильными группами циклоалкилен с 5 - 7 атомами углерода, в котором одна группа  заменена атомом азота, причем, кроме того, в указанных 5- до 7-членных кольцах смежная с атомом азота метиленовая группа может быть заменена карбонилом, или алкиленкарбонил с общим числом атомов углерода 2 - 6, если E означает циклическую иминогруппу, причем карбонил связан с атомом азота циклической иминогруппы группы остатка E, или же связь, если E не означает связь;
заменена атомом азота, причем, кроме того, в указанных 5- до 7-членных кольцах смежная с атомом азота метиленовая группа может быть заменена карбонилом, или алкиленкарбонил с общим числом атомов углерода 2 - 6, если E означает циклическую иминогруппу, причем карбонил связан с атомом азота циклической иминогруппы группы остатка E, или же связь, если E не означает связь;
E - связь, алкилен с 1 - 4 атомами углерода, который может быть замещен алкилом с 1 - 6 атомами углерода, аминогруппой, арилом, алкиламиногруппой с 1 - 4 атомами углерода, диалкиламиногруппой с общим числом атомов углерода 2 - 8, группой HNR21- или N-алкил- NR21-, где R21 означает алкилкарбонил или алкилсульфонил с 1 - 6 атомами углерода в алкильной части, алкилоксикарбонил с общим числом атомов углерода 2 - 5, циклоалкилкарбонил или циклоалкилсульфонил с 5 - 7 атомами углерода в циклоалкильной части, арилалкилкарбонил арилалкилсульфонил, арилалкоксикарбонил, арилкарбонил или арилсульфонил, алкенилен с 2 - 4 атомами углерода, арилен, незамещенные или замещенные одной или двумя алкильными группами пиридинилен, пиримидинилен, пиразинилен и пиридазинилен, незамещенный или замещенный одной или двумя алкильными группами циклоалкилен с 5 - 7 атомами углерода, в котором одна группа  заменена атомом азота, связанным с атомом углерода остатка D, циклоалкилен с 4 - 7 атомами углерода в циклоалкиленовой части, незамещенный или замещенный одной или двумя алкильными группами с 1 - 4 атомами углерода, или же, если D не означает связь, то связанный с остатком D через остаток W алкилен, в котором W означает атом кислорода или серы, сульфинил, сульфонил, группу -NR20-CO- или -CO- NR20-, где R20 означают атом водорода или алкил, при этом алкилен может быть дополнительно замещен алкилом с 1 - 6 атомами углерода, аминогруппой, арилом, алкиламиногруппой с 1 - 4 атомами углерода, диалкиламиногруппой с общим числом атомов углерода 2 - 8, группой -HNR21- или N-алкил- NR21-, где R21 имеет указанное значение, причем гетероатом дополнительного заместителя отделен от гетероатома остатка W по крайней мере двумя атомами углерода;
заменена атомом азота, связанным с атомом углерода остатка D, циклоалкилен с 4 - 7 атомами углерода в циклоалкиленовой части, незамещенный или замещенный одной или двумя алкильными группами с 1 - 4 атомами углерода, или же, если D не означает связь, то связанный с остатком D через остаток W алкилен, в котором W означает атом кислорода или серы, сульфинил, сульфонил, группу -NR20-CO- или -CO- NR20-, где R20 означают атом водорода или алкил, при этом алкилен может быть дополнительно замещен алкилом с 1 - 6 атомами углерода, аминогруппой, арилом, алкиламиногруппой с 1 - 4 атомами углерода, диалкиламиногруппой с общим числом атомов углерода 2 - 8, группой -HNR21- или N-алкил- NR21-, где R21 имеет указанное значение, причем гетероатом дополнительного заместителя отделен от гетероатома остатка W по крайней мере двумя атомами углерода;
F - карбонил, замещенный гидроксилом, алкоксилом с 1 - 4 атомами углерода, арилалкоксигруппой или группой R22O-, где R22 означает циклоалкил с 5 - 7 атомами углерода и циклоалкилалкил с 5 - 7 атомами углерода в циклоалкильной части, фосфоно, O-алкилфосфоно, группа R23CO-O-CHR24-O-CO-, где R23 означает алкил или алкоксил с 1 - 4 атомами углерода, циклоалкил с 5 - 7 атомами углерода, циклоалкоксил с 5 - 7 атомами углерода в циклоалкильной части и R24 - атом водорода или алкил, при этом кратчайшее расстояние между остатком F и расположенным на максимальном расстоянии от остатка F атомом азота группы A-B- составляет по крайней мере 11 связей;
третий из остатков Ra - Rd означает атом водорода, алкил с 1 - 4 атомами углерода, трифторметил, арил, или же алкоксил с 1 - 4 атомами углерода, который не может быть связан с атомом азота;
четвертый из остатков Ra - Rd означает атом водорода или алкил с 1 - 4 атомами углерода, причем если нечего другого не упомянуто, под указанным термином "арил" следует понимать фенил, который может быть монозамещен остатком R25, представляющим собой циано, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, алкилкарбонил, алкилсульфенил, алкилсульфинил, алкилсульфонил или трифторметил, моно-, ди- или тризамещен остатком R26, представляющим собой алкил, гидроксил, алкоксил, атом фтора, хлора или брома, причем два остатка R26, если они связаны со смежными атомами углерода, могут также представлять собой неразветвленный алкилен с 3 или 4 атомами углерода, 1,3-бутадиен-1,4-диилен или метилендиоксигруппу, или монозамещен упомянутым остатком R25 и дополнительно моно- или дизамещен упомянутым остатком R26, причем указанные заместители могут быть одинаковыми или различными, под указанным термином "арилен" следует понимать фенилен, который может быть монозамещен указанным остатком R25, моно- или дизамещен указанным остатком R26 или монозамещен указанным остатком R25 и дополнительно монозамещен указанным остатком R26, причем заместители могут быть одинаковыми или различными и имеют указанные значения, а также, если ничего другого не упомянуто, указанные алкильные, алкиленовые или алкоксильные группы содержат 1 - 4 атома углерода и каждый из атомов углерода в указанных алкиленовых и циклоалкиленовых группах связан, как максимум, с одним гетероатомом,
смеси их изомеров, или отдельные изомеры, или их соли.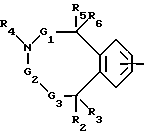
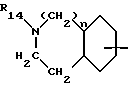
или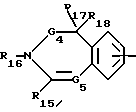
где одна или две метиновые группы в бензоостатке указанных групп могут быть заменены атомом азота;
G1 - связь или метилен;
G2 - связь;
G3 - метилен;
G4 - связь;
G5 - атом азота или метин;
R2 - атом водорода;
R3 - атом водорода;
R4 - атом водорода, циклоалкил, циклопропилметил, алкил с 1 - 6 атомами углерода, аллил, гидроксиалкил, карбоксиалкил с 1 - 4 атомами углерода в алкильной части, алкоксикарбонилалкил с 1 - 4 атомами углерода в алкоксильной и алкильной частях или бензил;
R5 - атом водорода;
R6 - атом водорода;
R14 - атом водорода или алкил с 1- 4 атомами углерода;
R15 - атом водорода или алкил с 1 - 4 атомами углерода;
R16 - атом водорода или алкил с 1 - 4 атомами углерода;
R17 - атом водорода или же R16 вместе с R17 означают дополнительную связь;
R18 - атом водорода, или же амино, если R16 и R17 вместе означают дополнительную связь;
n - число 1 или 2;
B - связь или фенилен,
второй из остатков Ra - Rc означает группу формулы
F-E-D-,
где D - связь, алкилен с 1 - 4 атомами углерода, фенилен, циклогексилен или пиридинилен, при этом кольцевой атом азота связан с незамещенным или замещенным алкиленом остатка E;
E - неразветвленный алкилен с 1 - 4 атомами углерода, который может быть замещен одной алкильной группой с 1 - 4 атомами углерода или фенилом, алкенилен с 2 - 4 атомами углерода, фенилен или же неразветвленный О-алкилен, связанный через атом азота с остатком D, если D не означает связь;
F - карбонил, замещенный гидроксилом или алкоксилом с 1 - 4 атомами углерода, при этом кратчайшее расстояние между остатком F и расположенным на максимальном расстоянии от остатка F атомом азота группы A-B - составляет по крайней мере 11 связей;
третий из остатков Ra - Rc означает атом водорода, алкоксил с 1 - 4 атомами углерода, который не может быть связан с атомом азота, алкил с 1 - 4 атомами углерода или фенил, причем, если ничего другого не упомянуто, каждый из атомов углерода в указанных алкиленовых и циклоалкиленовых группах связан, как максимум, с одним гетероатомом,
смесь их изомеров, или отдельные изомеры, или их соли.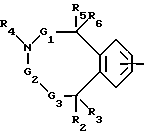
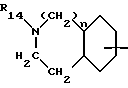
или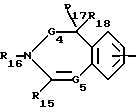
где 1 или 2 метиновые группы в бензоостатке указанных групп могут быть заменены атомом азота;
G1 - связь или метилен;
G2 - связь;
G3 - метилен;
G4 - связь;
G5 - метин;
R2 - атом водорода;
R3 - атом водорода;
R4 - атом водорода, алкил с 1 - 4 атомами углерода, аллил или бензил;
R5 - атом водорода;
R6 - атом водорода;
R14 - атом водорода или метил;
R15 - атом водорода;
R16 - вместе с R17 означают связь;
R18 - атом водорода или амино;
n - число 1;
B - связь;
остаток Rb означает группу формулы
F-E-D,
где D - группа -CH2-CH2-, 1,4-фенилен или 1,4-циклогексилен;
E - группа CH2-CH2-, незамещенная или замещенная метилом, группа -CH= CH-, 1,4-фенилен или группа -O-CH2-, где атом кислорода связан с остатком D;
F - карбонил, замещенный гидроксилом или алкоксилом с 1 - 4 атомами углерода, при этом кратчайшее расстояние между остатком F и расположенным на максимальном расстоянии от остатка F атомом азота группы A-B - составляет по крайней мере 11 связей,
смесь их изомеров, или отдельные изомеры, или их соли.
(а) 1-[4-[2-(метоксикарбонил)этил] фенил]-3-(1,2,3,4-тетрагидроизохинолин-6-ил)-имидазолидин-2-он,
(б) 1-[4-(2-карбоксиэтил)фенил]-3-(1,2,3,4-тетрагидроизохинолин-6-ил)-имидазолидин-2-он,
(в) 1-[4-(2-карбоксиэтил)фенил] -3-(2-метил-1,2,3,4-тетрагидроизохинолин-6-ил)-имидазолидин-2-он,
(г) 1-[4-(2-изобутилоксикарбонил)этил)фенил] -3-(1,2,3,4-тетрагидроизохинолин-6-ил)-имидазолидин-2-он,
(д) 1-[4-(2-карбоксиэтил)фенил]-3-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-имидазолидин-2-он,
(е) 1-[4-(2-метоксикарбонил)этил)фенил] -3-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-имидазолидин-2-он,
(ж) 1-[4-(2-изопропилоксикарбонил)этил)фенил] -3-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-имидазолидин-2-он,
(з) 1-[4-(2-карбоксиэтил)фенил] -3-(3-метил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-имидазолидин-2-он,
(и) 4-[4-(2-карбоксиэтил)фенил] -5-метил-2-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-4H-1,2,4-триазол-3-он,
(й) 1-[транс-4-(2-карбоксиэтил)циклогексил] -3-(2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-имидазолидин-2-он,
(к) 1-[4-[2-(метоксикарбонил)этил] фенил] -3-(3-метил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-имидазолидин-2-он,
(л) 1-[4-[2-(этоксикарбонил)этил]фенил]-3-(3-метил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-имидазолидин-2-он,
(м) 1-[4-[2-(изопропилоксикарбонил)этил] фенил]-3-(3-метил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-имидазолидин-2-он,
(н) 1-[транс-4-(2-карбоксиэтил)циклогексил] -3-(3-метил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-имидазолидин-2-он,
(о) 1-[транс-4-(2-изопропилоксикарбонил)этил] циклогексил]-3-(3-метил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-имидазолидин-2-он,
(п) 1-[транс-4-(2-этоксикарбонил)этил]циклогексил]-3-(3-метил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-имидазолидин-2-он,
(р) 1-[транс-4-(2-метоксикарбонил)этил] циклогексил] -3-(3-метил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-имидазолидин-2-он,
(с) 1-[транс-4-[(карбоксиметил)окси] циклогексил] -3-(3-метил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-имидазолидин-2-он,
(т) 3-[транс-4-[(карбоксиэтил)циклогексил] -1-(3-метил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-гидантоин и
(у) 1-[транс-4-(2-карбоксиэтил)циклогексил] -3-(3-этил-2,3,4,5-тетрагидро-1H-3-бензазепин-7-ил)-имидазолидин-2-он,
их таутомеры или их соли.
| Способ получения 2-гетерилзамещенных бензимидазола | 1975 |
|
SU541846A1 |
Авторы
Даты
1999-02-10—Публикация
1994-02-21—Подача