Изобретение относится к новым 4-арил-тетра-гидропиридинам и 4-арил-пиперидинолам, соединенным с алкил-азолами и имеющим общую формулу (I):
и их физиологически приемлемым солям, к способам их получения, к использованию их в качестве лекарственных средств, а также к фармацевтическим композициям на их основе.
Соединения, составляющие предметы изобретения, также могут быть использованы в фармацевтической промышленности в качестве промежуточных продуктов синтеза и для получения лекарственных средств.
Эти соединения обладают сильным сродством к рецепторам сигма- и/или 5HTIA-типа и, следовательно, потенциально пригодны для лечения некоторых психических и неврологических расстройств у людей и млекопитающих животных.
Существуют случаи, при которых воздействуют на сигма-рецепторы для лечения психоза. Многочисленные нетипичные, относящиеся к лечению психоза средства, такие как римказол (Schwarcz G. и др. Drug Dev. Res., 1985, 5, 387), ремоксиприд (Wadworth A. N. и др. Drugs, 1990, 40, 863), тиоспирон (Jain А. К. и др. Int. Clin. Psychopharmacol., 1987, 2, 129), показывают значительное сродство к сигма-рецепторам.
С другой стороны, исследования в отношении биологии и функции рецепторов сигма-типа показывают, что координационные соединения с рецептором сигма-типа могут быть эффективны при лечении некоторых моторных расстройств, в особенности хореи Гентингтона, дистонии и синдрома Туретта. Присутствие рецепторов сигма-типа в черном веществе (мозга) позволяет их использовать при лечении болезни Паркинсона (Walker J.M. и сотр., Pharmacological Reviews, 1990, 42, 355).
Некоторые координационные соединения с рецептором сигма-типа связаны с модуляцией эффектов, вызываемых медиацией NMDA-рецептора, и действуют как антиишемические агенты в тестах ин виво (Rao T.S. и др. Molecular Pharmacology, 1990, 37, 978) с возможностью использования в качестве нейрозащитных средств и при лечении эпилепсии и конвульсии (Kaiser С., Neurotransmissions VII, 1991).
Известно, что координационные соединения с рецептором сигма-типа оказывают антиамнезическое воздействие на животных, используемых в качестве моделей (Early и др. Brain Research, 1991, 546, 281).
Координационные соединения рецепторов сигма-типа влияют на уровнях ацетилхолина у животных, используемых в качестве моделей (Matsuno и др. Brain Research, 1992, 575, 315) и, следовательно, могут быть использованы для лечения старческого слабоумия, например, типа болезни Альцгеймера.
Координационные соединения рецепторов 5HTIA-типа, в особенности агонисты или частичные агонисты 5HTIA, проявляют обнаруживаемую анксиолитическую и антидепрессивную активность (Glitz D.A., Drugs, 1991, 41, 11).
Следовательно, агенты, обладающие сильным сродством к рецепторам сигма- и/или 5HTIA-типа, могут быть использованы в случае одного или нескольких указанных заболеваний.
В литературе описаны примеры 4-арил-1,2,3,6-тетрагидро пиридинов и 4-арил-4-гидроксипиперидинов, однако, там отсутствует описание соединений, в которых эти подструктуры соединены с азотом азольного ядра с помощью алкильной незамещенной цепи:
Davis L. Temple и др., патент США 4320131: 16 марта 1982 г.; Richard A. Glennon и др., J. Med. Chem. 1991, 34, 3360-65; Jean-Luc Malleron и др., J. Med. Chem. 1991, 34, 8, 2477-83; Henning Botcher и др., J. Med. Chem., 1992, 35, 4020-26; Zhuihua Sui и др. Synthesis, 1993, 803-8;
David L. Schuster и др. , J. Med. Chem. 1993, 36, 3923-28; David J. Wustrow и др., BioMed. Chem. Lett., 1993, 3, 277-280; Shimazaki Norihiko и др. Can. Pat. App., CA 2053475 AA.
Заявителем ранее был описан ряд N-алкилазолов, соединенных с азотом различных гетероциклов, используемых в качестве небензодиазепиновых агентов для лечения беспокойств (европейские патенты NN 382637, 497659 и 502786) и для лечения других нарушений поведения (европейские патенты NN 429360 и 497658). В вышеуказанных патентах описаны соединения общей формулы (I), в которой А обозначает атом азота, следовательно, в них речь идет о пиперазиновом ядре.
В настоящем изобретении пиперазиновое ядро заменяют пиперидиновым или тетрагидропиридиновым.
Соединения, составляющие объекты изобретения, отвечают общей формуле (I):
в которой R1, R2 и R3, одинаковые или разные, обозначают каждый атом водорода, атом галогена, линейный или разветвленный алкильный радикал, пергалогеноалкильный радикал, арильный или замещенный арильный радикал или алкоксильный радикал; более того, два смежных радикала могут образовывать ароматический или насыщенный цикл;
А обозначает атом углерода, а пунктирная линия обозначает дополнительную связь, или А обозначает атом углерода, соединенный с гидроксильной группой (C-OH), а пунктирная линия обозначает отсутствие дополнительной связи;
"n" может иметь значения от 2 до 6, предпочтительно обозначает 4;
Z1 обозначает атом азота или замещенный атом углерода, который может быть обозначен как C-R4;
Z2 обозначает атом азота или замещенный атом углерода, который может быть обозначен как C-R5;
Z4 обозначает атом азота или замещенный атом углерода, который может быть обозначен как C-R7;
R4, R5, R6 и R7, одинаковые или разные, обозначают атом водорода, атом галогена, линейный или разветвленный алкильный радикал, гидроксильный радикал, алкоксильный радикал, карбоксильный радикал, карбоксамидный радикал, алкилкарбоксилатный радикал, арильный или замещенный арильный радикал, или два смежных радикала могут составлять часть другого цикла, ароматического или неароматического.
Изобретение также относится к физиологически приемлемым солям соединений общей формулы (I), в особенности солям соляной, бромоводородной, серной, фосфорной, уксусной, молочной, малоновой, янтарной, глутаровой, фумаровой, яблочной, винной, лимонной, аскорбиновой, малеиновой, бензойной, фенилуксусной, коричной, салициловой кислот и алкил-, циклоалкил- или арил-сульфокислот.
Радикал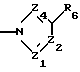
обозначает азол, за исключением тетразолов, в которых Z1, Z2 и Z4 обозначают одновременно атом азота.
Когда R4, R5, R6 и R7 не составляют часть другого, ароматического или неароматического, цикла, то речь идет предпочтительно об азоле, в котором один из Z1, Z2 или Z4 обозначает атом азота, в частности, о пиразоле (Z1 или Z4 = N) или имидазоле (Z2 = N).
Когда R4, R5, R6 или R7 составляют часть другого, ароматического или нет, цикла, то "азольная" составляющая вышеуказанного радикала остается главной, т. е. он не охватывает радикалы, такие как β- или γ-карболины, пирролоазепины, и радикалы, содержащие карбонильные функции, такие как пиразолоны, имидазолоны, бензимидазолоны и вообще гетероциклы, включающие карбонильную функцию.
Когда R4, R5, R6 или R7 составляют часть другого, ароматического или нет, цикла, то вышеуказанный радикал предпочтительно обозначает бициклический радикал, в частности, индольный, индазольный, бензимидазольный или бензотриазольный радикал.
Под линейным или разветвленным алкилом предпочтительно понимают низший алкил с 1-6 C-атомами, в частности метил, этил или пропил, причем это определение применяется также к алкильным остаткам алкоксильных и алкилкарбоксилатных радикалов.
Под арилом или замещенным арилом понимают предпочтительно фенил, в случае необходимости замещенный одним или несколькими радикалами, выбираемыми среди галогенов и линейных или разветвленных алкильных радикалов.
Под галогеном понимают фтор, хлор или бром, предпочтительно хлор.
Наконец, под пергалогеналкилом понимают линейный или разветвленный алкильный радикал, у которого все атомы водорода заменены на атомы галогенов. Предпочтительно речь идет о перфторалкильном радикале, в частности о трифторметильном радикале.
Новые производные общей формулы (I) можно получать следующими способами:
СПОСОБ А
Путем взаимодействия спиранового производного общей формулы (II):
в которой R1, R2, R3 и А имеют вышеуказанное значение, "m" может иметь значения 0 - 4 и X обозначает удаляемую группу, как хлор, бром, мезилокси-группа или тозилокси-группа;
с азотсодержащим гетероциклом общей формулы (III):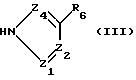
в которой Z1, Z2, Z4 и R6 имеют вышеуказанное значение.
Реакцию осуществляют в растворе диметилсульфоксида; диметилформамида, спирта, такого как этанол, ароматического углеводорода, такого как толуол, или алифатического углеводорода, такого как гексан, или простого эфира, как диоксан. Эту реакцию проводят предпочтительно в присутствии основания, как карбонат калия или триэтиламин.
Температура реакции изменяется от комнатной до температуры кипения используемого растворителя.
Время реакции составляет 1-24 часа;
СПОСОБ Б
Путем одновременного "в одну стадию" взаимодействия между производным общей формулы (IV), алкилирующим агентом общей формулы (V) и азотсодержащим гетероциклом общей формулы (III):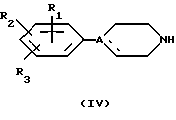
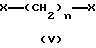
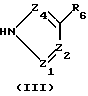
где R1, R2, R3, A, X, "n", Z1, Z2, Z4 и R6 имеют вышеуказанное значение.
Реакцию проводят в растворе диметилсульфоксида, диметил формамида, спирта, такого как этанол, ароматического углеводорода, такого как толуол, или алифатического углеводорода, такого как гексан, или простого эфира, как диоксан. Эту реакцию проводят предпочтительно в присутствии основания, например карбоната калия или триэтиламина.
Температура реакции изменяется в пределах от комнатной до температуры кипения используемого растворителя.
Время реакции составляет от 1 до 24-х часов;
СПОСОБ В
Получение соединений общей формулы (I) можно осуществлять путем взаимодействия в условиях алкилирования аминов общей формулы (IV):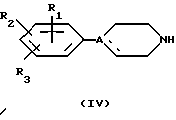
в которой R1, R2, R3 и A имеют вышеуказанное значение, с соединениями общей формулы (VI):
в которой X, "n", Z1, Z2, Z4 и R6 имеют вышеуказанное значение.
Реакцию проводят в растворе диметилсульфоксида, диметилформамида, спирта, такого как этанол, ароматического углеводорода, такого как толуол, или алифатического углеводорода, такого как гексан, или простого эфира, такого как диоксан. Эту реакцию осуществляют предпочтительно в присутствии основания, как карбонат калия или триэтиламин.
Температура реакции изменяется в пределах от комнатной до температуры кипения используемого растворителя.
Время реакции составляет от 1 до 24-х часов;
СПОСОБ Г
Соединения общей формулы (I) можно получать путем взаимодействия, в условиях алкилирования, соединения общей формулы (VII):
в которой R1, R2, R3, "n" и A имеют вышеуказанное значение, с азотсодержащим гетероциклом общей формулы (III):
в которой Z1, Z2, Z4 и R6 имеют вышеуказанное значение.
Реакцию проводят в растворе диметилсульфоксида, диметилформамида, спирта, такого как этанол, ароматического углеводорода, такого как толуол, или алифатического углеводорода, такого как гексан, или простого эфира, такого как диоксан. Эту реакцию проводят предпочтительно в присутствии основания, например карбоната калия или триэтиламина.
Температура реакции изменяется в пределах от комнатной до температуры кипения используемого растворителя.
Время реакции составляет от 1 до 24-х часов;
СПОСОБ Д
Путем дегидратации соединений общей формулы (I)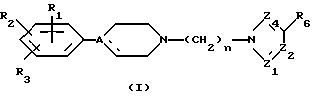
в которой R1, R2, R3, "n", Z1, Z2, Z4 и R6 имеют вышеуказанное значение; А обозначает атом углерода, связанный с гидроксильной группой (C-OH), а пунктирная линия обозначает отсутствие какой-либо дополнительной связи.
Реакцию проводят в кислой среде, как, например, соляная кислота, трифторуксусная кислота, серная кислота или фосфорная кислота, или путем обработки тионилхлоридом в бензоле.
Температура реакции изменяется в пределах от комнатной до 180oС.
Время реакции изменяется от 1 до 14 часов;
СПОСОБ Е
Путем присоединения металлоорганических реагентов, например фениллития или фенилмагнийбромида, к соединениям общей формулы (VIII):
в которой "n", Z1, Z2, Z4 и R6 имеют вышеуказанное значение.
Реакцию проводят в растворе инертного растворителя, обычно простого эфира, как, например, диметоксиэтан, тетрагидрофуран или диэтиловый эфир.
Температура реакции изменяется в пределах от комнатной до температуры кипения с обратным холодильником используемого растворителя.
Время реакции составляет от 5 минут до 24-х часов;
СПОСОБ Ж
Путем восстановления карбонила амидной группы соединений общей формулы (IX):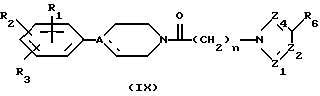
в которой R1, R2, R3, A, "n", Z1, Z2, Z4 и R6 имеют вышеуказанное значение.
Реакцию проводят предпочтительно в инертном органическом растворителе, например в диэтиловом эфире или тетрагидрофуране, с помощью восстановителей, как LiAlH4, AlH3 или диборан.
Температура реакции изменяется в пределах от комнатной до температуры кипения используемого растворителя.
Время реакции составляет от 5 минут до 24-х часов;
СПОСОБ 3
Путем взаимодействия соединения общей формулы (I) с неорганической или органической нетоксичной кислотой в соответствующем растворителе, которым может быть, например, спирт, как метанол, этанол или любой из пропанолов или бутанолов; сложный эфир, как этилацетат, или нитрил, как ацетонитрил; и используя обычные методы осаждения, кристаллизации и т.д., получают соответствующую соль.
Неорганическую кислоту выбирают среди соляной, бромоводородной, серной или фосфорной кислот, а органическую кислоту выбирают среди моно-, ди- или трикарбоновых кислот, как, например, уксусная, молочная, малоновая, янтарная, глутаровая, фумаровая, яблочная, винная, лимонная, аскорбиновая, малеиновая, бензойная, фенилуксусная, коричная, салициловая кислоты и алкил-, циклоалкил- или арилсульфокислоты.
Можно получать моно- или дисоли кислоты и эти соли могут быть в безводной или гидратированной форме.
Изобретение иллюстрируется нижеследующими примерами, которые не ограничивают ни специфические условия способа, ни объем охраны изобретения.
СПОСОБ А
ПРИМЕР 1
Получение 4-хлор-1-[4-(4-гидрокси-4-фенил-1-пиперидинил) бутил]-1H-пиразола
Смесь из 15.0 г (48 ммоль) 8-гидрокси-8-фенил-5-азоний- спиро-[4,5]-декана, 5.4 г (53 ммоль) 4-хлор-пиразола и 13.2 г карбоната калия в 200 мл диметилформамида кипятят с обратным холодильником в течение 20 часов. Затем выпаривают досуха при пониженном давлении, снова растворяют в хлороформе и промывают несколько раз водой. Органическую фазу сушат над безводным сульфатом натрия и выпаривают при пониженном давлении с получением сырого продукта, который суспендируют в диэтиловом эфире, отфильтровывают на холоде и промывают диэтиловым эфиром. Получают 12.4 г (37.1 ммоль) 4-хлор-1-[4-(4-гидрокси-4-фенил-1-пиперидинил) бутил]-1H-пиразола.
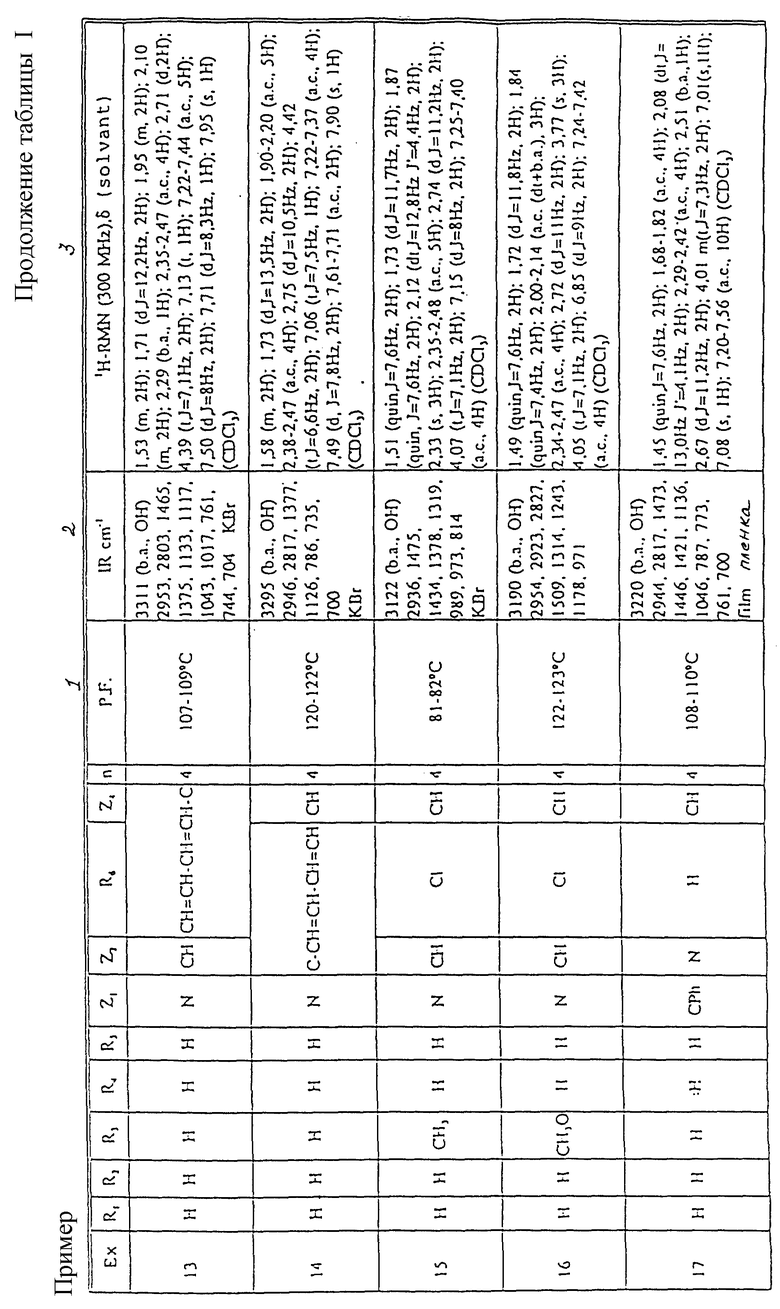
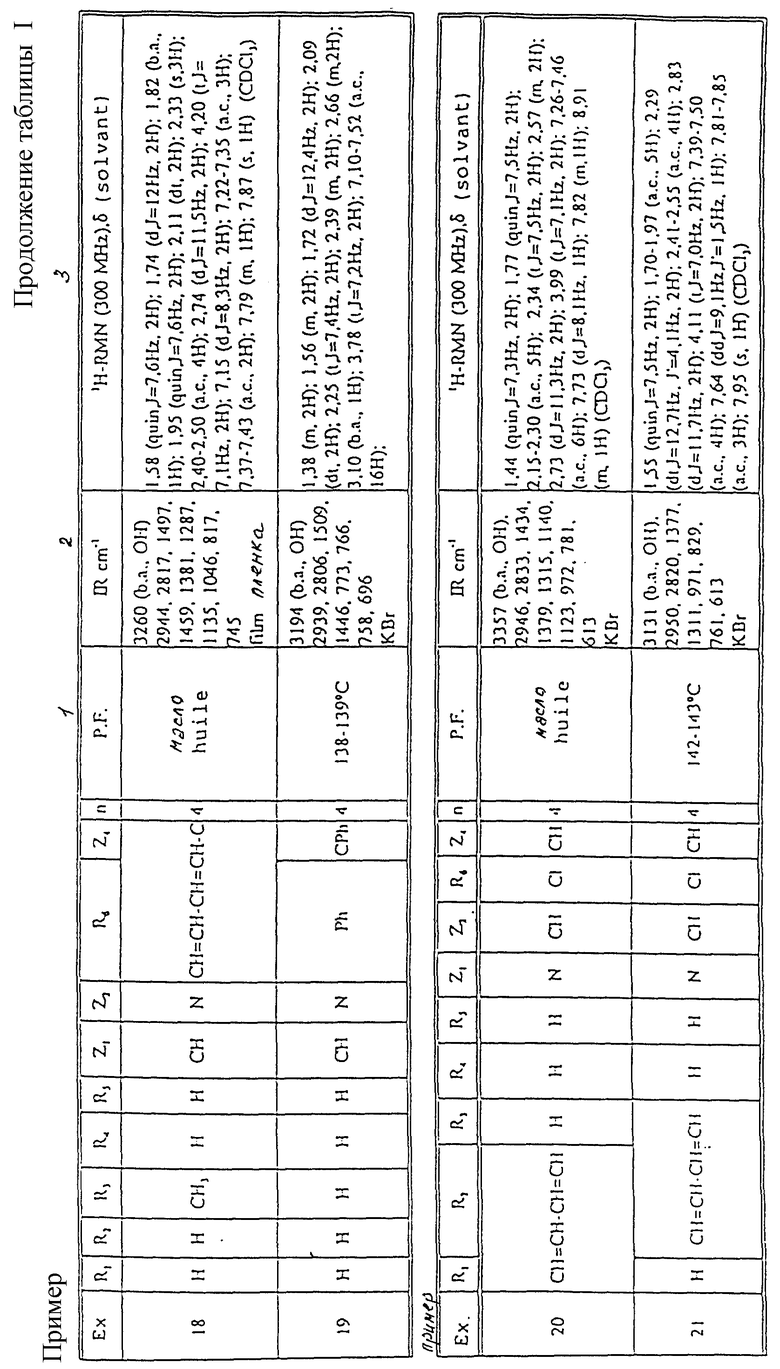
Температура плавления и спектроскопические данные для идентификации этого продукта представлены в Таблице 1.
СПОСОБ Б
ПРИМЕР 7
Получение 4-хлор-1-[4-[4-гидрокси-4-(3-фторметилфенил)-1- пиперидинил] бутил]-1H-пиразола
Смесь из 8.6 г (35 ммоль) 4-гидрокси-4-(3-трифторметил- фенил)-1-пиперидина, 7.68 г 1,4-дибром-бутана и 13.8 г карбоната калия в 100 мл диметилформамида кипятят с обратным холодильником в течение 4-х часов. Затем добавляют 3.59 г (35 ммоль) 4-хлор-пиразола и кипятят с обратным холодильником в течение 14 часов. После этого выпаривают досуха при пониженном давлении, снова растворяют в хлороформе и промывают несколько раз водой. Органическую фазу сушат над безводным сульфатом натрия и выпаривают при пониженном давлении с получением сырого продукта, который очищают путем хроматографии на силикагеле. Получают 9.7 г (24.2 ммоль) 4-хлор-1-[4-[4-гидрокси-4-(3-трифторметилфенил)-1- пиперидинил] бутил]-1H-пиразола.
Спектроскопические данные для идентификации этого продукта представлены в Таблице 1.
СПОСОБ В
ПРИМЕР 14а
Получение 1-[4-[4-фенил-1-(1,2,3,6-тетрагидро-пиридинил)]бутил] индола
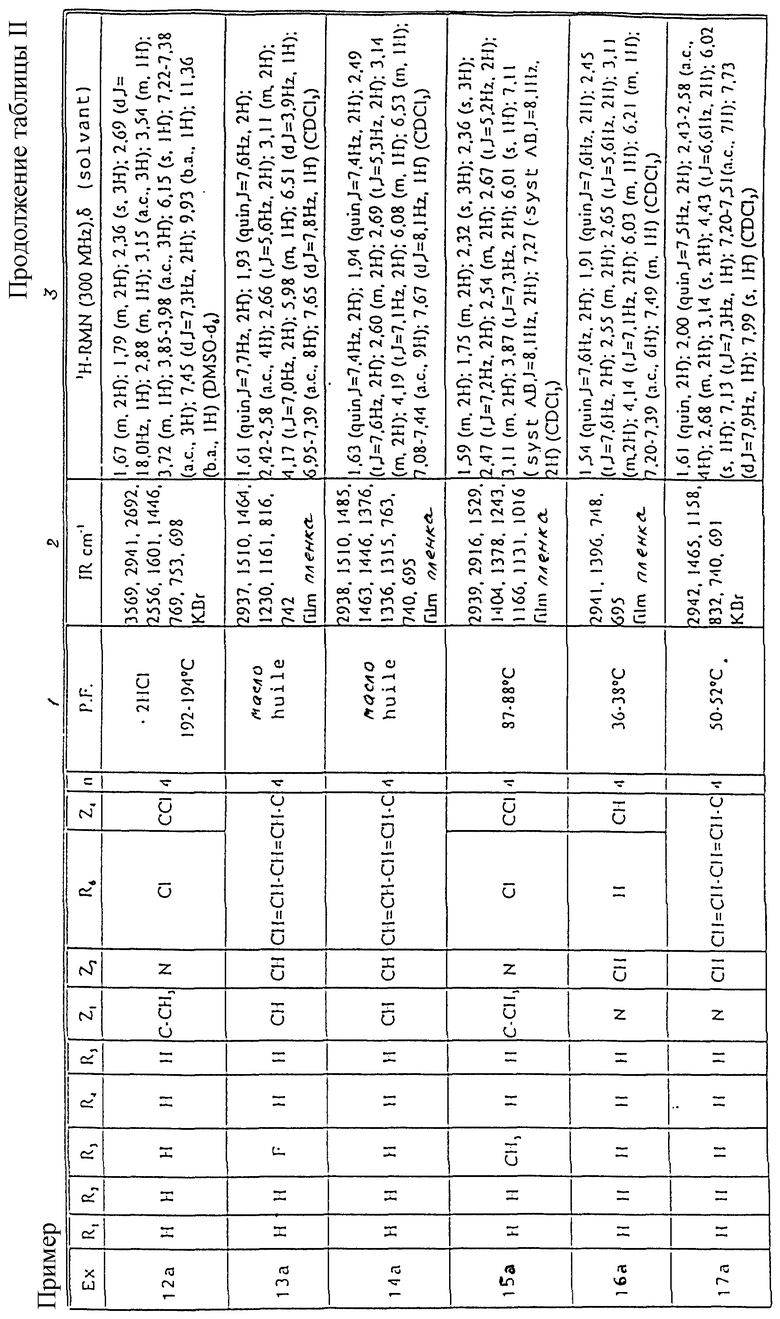
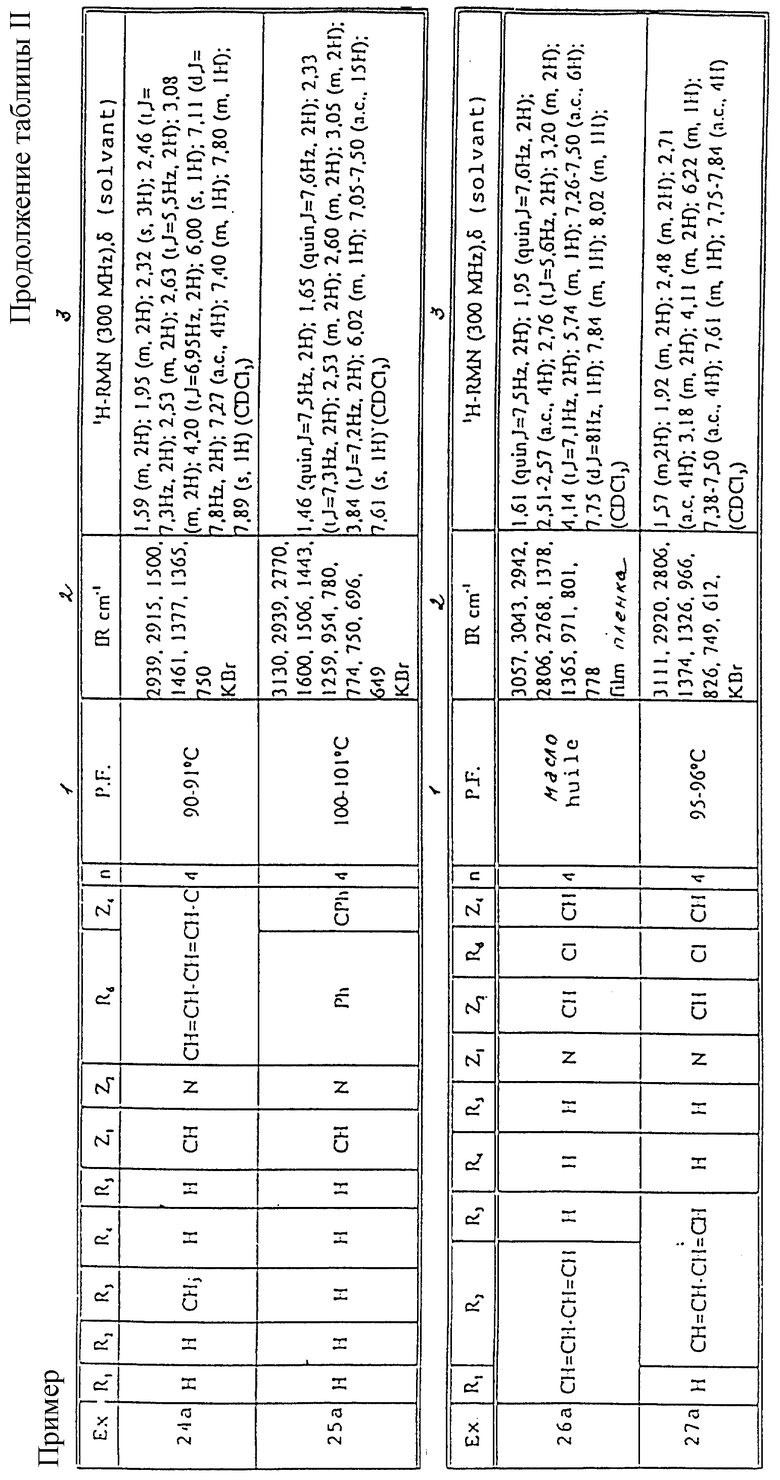
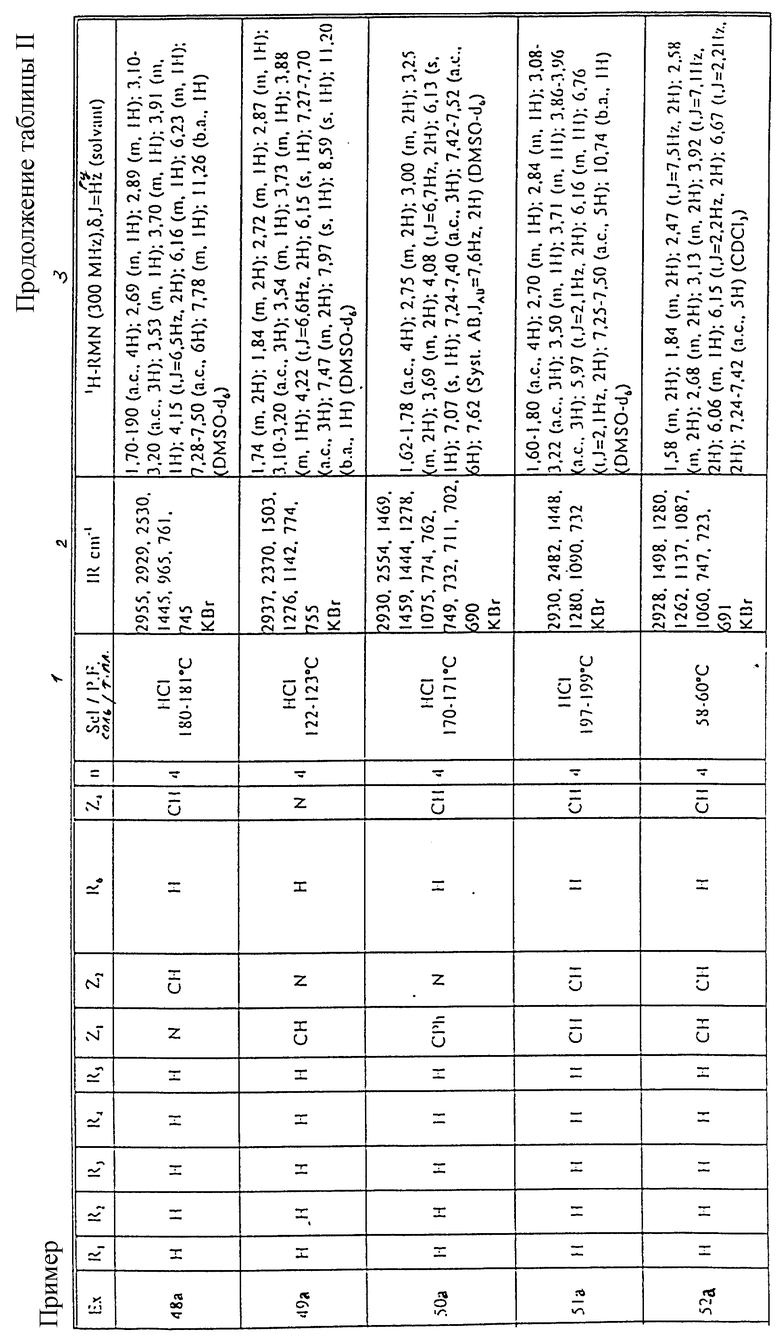
Смесь из 4.8 г (30 ммоль) 4-фенил~1,2,3,6-тетрагидропиридина, 6.22 г 1-(4-хлорбутил) индола, 8.3 г карбоната калия в 100 мл диметилформамида нагревают при 90oC в течение 3-х часов. Затем выпаривают досуха при пониженном давлении, снова растворяют в хлороформе и промывают несколько раз водой. Органическую фазу сушат над безводным сульфатом натрия и выпаривают при пониженном давлении с получением сырого продукта, который очищают путем хроматографии на силикагеле. Получают 5.7 г (17.3 ммоль) 1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)] бутил]индола. Спектроскопические характеристики для идентификации этого продукта представлены в Таблице II.
СПОСОБ Г
ПРИМЕР 21а
Получение 4-хлор-1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)] пропил] -1H-пиразола
К суспензии 1.0 г NaH в диметилформамиде прикапывают раствор из 2.05 г (20 ммоль) 4-хлор-пиразола в диметилформамиде. Суспензию белого цвета нагревают в течение 30 минут при 100oC. Охлаждают и добавляют 4.7 г (20 ммоль) 1-(3-хлор-пропил)-4-фенил-1,2,3,6-тетрагидропиридина, растворенные в диметилформамиде. Кипятят с обратным холодильником в течение 2-х часов, после чего выпаривают досуха, остаток экстрагируют хлороформом, раствор промывают водой и сушат над сульфатом натрия. Сырой полученный продукт очищают путем хроматографии на силикагеле. Получают 5.2 г (17.2 ммоль) 4- хлор-1-[4-[4-фенил-1-(1,2,3,6- тетрагидропиридинил)]пропил]-1H-пиразола.
Спектроскопические характеристики (данные) для идентификации этого продукта представлены в Таблице II.
СПОСОБ Д
ПРИМЕР 2а
Получение 1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)] -бутил] -1H-бензимидазола
Раствор из 13.4 г (38.2 ммоль) 1-[4-(4-гидрокси-4-фенил-1-пиперидинил) бутил] -1H-бензимидазола, 150 мл концентрированной НС1 и 75 мл этанола кипятят с обратным холодильником в течение 6 часов. Органическую фазу сушат над безводным сульфатом натрия и выпаривают при пониженном давлении, получая сырой продукт, который очищают путем хроматографии на силикагеле. Получают 9.1 г (27.5 ммоль) 1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1H- бензимидазола.
Температура плавления и спектроскопические характеристики для идентификации этого продукта представлены в Таблице II.
СПОСОБ Е
ПРИМЕР 11
Получение 4,5-дихлор-1-[4-[4-гидрокси-4-(4-метил-фенил)-1-пиперидинил] бутил]-2-метил-1Н-имидазола
К суспензии из 1.08 г (11.4 ммоль) MgCl2 в 15 мл безводного тетрагидрофурана при -40oC и в атмосфере азота, добавляют раствор 1.0 г (3.3 ммоль) 4,5-дихлор-2-метил-1-[4-(4-оксо-1-пиперидинил)бутил] -1H-имидазола в 10 мл безводного ТГФ. Смесь перемешивают в течение 5 минут, затем при -40oC добавляют 6.8 мл 1.0 М раствора 4-метилфенилмагнийбромида. Полученную суспензию перемешивают в течение 15 минут при -40oC и в течение 3-х часов при комнатной температуре. После этого добавляют водный раствор хлорида аммония и тетрагидрофуран выпаривают. Полученную водную фазу экстрагируют хлороформом. Xлороформную фазу промывают водой, сушат над безводным сульфатом натрия и выпаривают досуха, получая сырой продукт, который очищают путем хроматографии на силикагеле с получением 1.02 г (2.6 ммоль) 4,5-дихлор-1-[4-[4-гидрокси-4-(4-метилфенил)-1-пиперидинил]бутил]-2-метил-1Н-имидазола.
Спектроскопические характеристики для идентификации этого продукта представлены в Таблице 1.
СПОСОБ Ж
ПРИМЕР 16а
Получение 1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)] бутил]-1H-пиразола
К раствору 3.3 г (10 моль) 1-[4-[4-фенил-1-(1,2,3,6- тетрагидропиридинил)] -3-оксо-бутил] -1H-пиразола в 25 мл ТГФ добавляют 2.0 г LiAlH4. Полученную смесь кипятят с обратным холодильником в течение 2-х часов. Избыток LiAlH4 разлагают путем добавления концентрированного раствора NaOH и воды. Неорганические соли отфильтровывают и ТГФ выпаривают в вакууме, получая 2.6 г (8.2 моль) 1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)] бутил]-1H-пиразола.
Температура плавления и спектроскопические характеристики для идентификации этого продукта представлены в Таблице 11.
СПОСОБ 3
ПРИМЕР 11а
Получение 4,5-дихлор-2-метил-1-[4-[4-фенил-1-(1,2,3,6- тетрагидропиридинил)]бутил]-1H-имидазол-хлоргидрата
К раствору из 7.4 г (20.3 ммоль) 4,5-дихлор-2-метил-1-[4- [4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1H-имидазола в 15 мл абсолютного этанола, охлажденному на ледяной бане, добавляют 2.5 мл 8.4 н. раствора хлороводорода в этаноле. Спустя несколько минут появляется осадок, который отфильтровывают, промывают холодным этанолом и сушат, получая 7.7 г (19.2 ммоль) 4,5-дихлор-2-метил-1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)] бутил]-1H-имидазол-хлоргидрата.
Температура плавления и спектроскопические данные (характеристики) для идентификации этого продукта представлены в Таблице II.
Используемые в таблицах сокращения;
s. = синглет (с.)
d. = дублет (д.)
t. = триплет (т.)
m. = мультиплет (м.)
quin. = квинтет
Hz = Герц (Гц)
syst. = система
DMSO = ДМСО (диметилсульфоксид)
b.a. = абсорбционная полоса (а.п.)
a.c. = центрированная абсорбционная полоса (ц.п.)
БИОЛОГИЧЕСКИЕ ИСПЫТАНИЯ
Связывание с рецептором серотонина (5HT1A)
Используют гомогенизат гиппокампа крысы согласно модификации способа S. J. Peroutka, J. of Neurochem., 47 (2), 529- 540 (1986). В качестве радиокоординационного соединения используют [3H]8-OH-DPAT и для измерения неспецифической связи используют серотонин. Время инкубации составляет 15 минут при температуре 37oC. Радиокоординационное соединение, связанное с протеином, отделяют путем отфильтровывания через фильтры из стекловолокна и определяют радиоактивность, удержанную на фильтре, путем жидкостной сцинтилляции. Константы ингибирования (Ki, нМ) рассчитывают путем анализа нелинейной регрессии, используя программу EBDA/LIGAND (Munson и Rodbard, Analytical Biochemistry, 107, 220 (1980)).
Связывание с рецептором сигма-типа
Используют гомогенизат головного мозга (без мозжечка) морской свинки согласно модификации способа L. Radesca и др., J. Med. Chem., 34, 3058-3065 (1991). В качестве радиокоординационного соединения используют [3H] (+)-3-РРР и для измерения неспецифической связи используют галоперидол. Время инкубации составляет 120 минут при температуре 25oC. Радиокоординационное соединение, связанное с протеином, отделяют путем отфильтровывания через фильтры из стекловолокна и определяют радиоактивность, удержанную на фильтре, путем жидкостной сцинтилляции. Константы ингибирования (Ki, нМ) рассчитывают путем анализа нелинейной регрессии, используя программу EBDA/LIGAND (Munson и Rodbard, Analytical Biochemistry, 107, 220 (1980)).
Ежедневная доза для человека составляет 1 - 500 мг соединения 1, которая может быть введена за один или несколько приемов. Готовят композиции в виде таких препаративных форм, которые приемлемы для используемого метода введения, как, например, в виде таблеток, драже, капсул, свечей, растворов или суспензий. Эти композиции готовят известными способами, и они содержат 1 - 60 мас.% действующего начала (соединения общей формулы (I)) и 40 - 99 мас.% соответствующего фармацевтического эксципиента, совместимого с действующим началом и физической формой используемой композиции. В качестве примера приводится формула таблетки, которая содержит продукт согласно изобретению:
Пример формулы для таблетки
соединение примера 11а - 5 мг
лактоза - 60 мг
кристаллическая целлюлоза - 25 мг
повидон К 90 - 5 мг
предварительно желатинированный крахмал - 3 мг
коллоидальный диоксид кремния - 1 мг
стеарат магния - 1 мг
общая масса - 100 мги















Изобретение относится к новым тетрагидропиридин- или 4-гидроксипиперидин-алкилазолам формулы I, где R1, R2, R3 и R6 обозначают водород, галоген, С1-С6-алкил, С1-С6-перфторалкил, С1-С6-алкоксил или два смежных радикала могут образовывать приконденсированное бензольное кольцо, А обозначает атом углерода, а пунктирная линия обозначает дополнительную связь, или А обозначает атом углерода, связанный с гидроксильной группой (C-OH), а пунктирная линия обозначает отсутствие дополнительной связи, n = 2 - 6, Z1, Z2 и Z3 обозначают атом азота или замещенный атом углерода, или их физиологически премлемым солям, которые обладают антипсихотической или анксиолитической активностью. 8 с. и 2 з.п. ф-лы, 3 табл. 
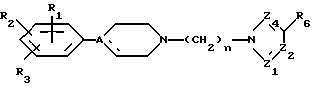
в которой R1, R2 и R3, одинаковые или разные, обозначают каждый атом водорода, атом галогена, линейный или разветвленный алкильный радикал С1-C6, перфторалкильный радикал С1-C6, алкоксильный радикал С1-C6 или два смежных радикала могут образовывать приконденсированное бензольное кольцо;
А обозначает атом углерода, а пунктирная линия обозначает дополнительную связь, или А обозначает атом углерода, связанный с гидроксильной группой (С-ОН), а пунктирная линия обозначает отсутствие дополнительной связи;
n может иметь значения 2-6, предпочтительно обозначает 4;
Z1 обозначает атом азота или замешенный атом углерода, который может быть представлен как С-R4,
Z2 обозначает атом азота или замещенный атом углерода, который может быть представлен как C-R5,
Z4 обозначает атом азота или замещенный атом углерода, который может быть представлен как С-R7;
R4, R5, R6 и R7, одинаковые или разные, обозначают атом водорода, атом галогена, линейный или разветвленный алкильный радикал С1-C6, гидроксильный радикал, алкоксильный радикал С1-C6, фенильный или галогенфенильный радикал, или два смежных радикала, выбранных из R4, R5, R6 и R7, могут образовывать приконденсированное бензольное кольцо с получением бициклического радикала,
или их физиологически приемлемые соли, за исключением 1-[3-(1Н-бензимидазол-1-ил)пропил]-4-(4-хлорфенил)-4-пиперидинола.
1) 4-хлор-1-[4-(4-гидрокси-4-фенил-1-пиперидинил)бутил)-1Н-пиразол,
2) 4,5-дихлор-1-[4-(4-гидрокси-4-фенил-1-пиперидинил)-бутил)-2-метил-1Н-имидазол,
3) 1-[4-(4-гидрокси-4-фенил-1-пиперидинил)бутил]-1H-бензимидазол,
4) 1-[4-гидрокси-4-фенил-1-пиперидинил)бутил]-1Н-1,2,4-триазол,
5) 4-хлор-1-[4-[4-(4-хлорфенил)-4-гидрокси-1-пиперидинил]бутил]-1H-пиразол,
6) 4,5-дихлор-1-[4-[4-гидрокси-4-(4-хлорфенил)-1-пиперидинил]бутил]-2-метил-1Н-имидазол,
7) 4-хлор-1-[4-[4-гидрокси-4-(3-трифторметилфенил)-1-пиперидинил]бутил] -1Н-пиразол,
8) 4,5-дихлор-1-[4-[4-гидрокси-4-(3-трифторметилфенил)-1-пиперидинил)бутил]-2-метил-1Н-имидазол,
9) 4,5-дихлор-1-[4-[4-(4-фторфенил)-4-гидрокси-1-пиперидинил]бутил]-2-метил-1Н-имидазол,
10) 1-[4-(4-гидрокси-4-фенил-1-пиперидинил)бутил]индол,
11) 4,5-дихлор-1-[4-[4-гидрокси-4-(4-метилфенил)-1-пиперидинил]бутил]-2-метил-1Н-имидазол,
12) 1-[4-(4-гидрокси-4-фенил-1-пиперидинил)бутил]-1H-пиразол,
13) 1-[4-(4-гидрокси-4-фенил-1-пиперидинил)бутил]-1H-индазол,
14) 2-[4-(4-гидрокси-4-фенил-1-пиперидинил)бутил]-2Н-индазол,
15) 4-хлор-1-[4-[4-гидрокси-4-(4-метилфенил)-1-пиперидинил] бутил]-1Н-пиразол,
16) 4-хлор-1-[4-[4-гидрокси-4-(4-метоксифенил)-1-пиперидинил)бутил] -1Н-пиразол,
17) 1-[4-(4-гидрокси-4-фенил-1-пиперидинил)бутил]-2-фенил-1Н-имидазол,
18) 1-[4-(4-гидрокси-4-(4-метилфенил)-1-пиперидинил] -бутил] -1Н-бензимидазол,
19) 4,5-дифенил-1-[4-(4-гидрокси-4-фенил-1-пиперидинил)бутил]-1Н-имидазол,
20) 4-хлор-1-[4-[4-гидрокси-4-(1-нафтил)-1-пиперидинил] бутил]-1Н-пиразол,
21) 4-хлор-1-[4-[4-гидрокси-4-(2-нафтил)-1-пиперидинил] бутил]-1Н-пиразол,
22) 4-хлор-1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-пиразол,
23) 1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)] бутил)-1Н-бензимидазол,
24) 1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-1,2,4-триазол,
25) 4-хлор-1-[4-[4-(4-хлорфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил] -1Н-пиразол,
26) 4,5-дихлор-1-[4-[4-(4-хлорфенил)-1-(1,2,3,6-тетрагидропиридинил)] бутил]-2-метил-1Н-имидазол,
27) 4-хлор-1-[4-[4-(3-трифторметилфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-пиразол,
28) 4,5-дихлор-2-метил-1-[4-[4-(3-трифторметилфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-имидазол,
29) 4-хлор-1-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил] -1H-пиразол,
30) 4,5-дихлор-1-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)] бутил]-2-метил-1Н-имидазол,
31) 4,5-дихлор-1-[4-[4-(фенил-1-(1,2,3,6-тетрагидропиридинил)] бутил]-2-метил-1Н-имидазол,
32) 4,5-дихлор-1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-2-метил-1Н-имидазол-хлоргидрат,
33) 4,5-дихлор-1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-2-метил-1Н-имидазол-дихлоргидрат,
34) 1-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил]индол,
35) 1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]индол,
36) 4,5-дихлор-2-метил-1-[4-[4-(4-метилфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-имидазол,
37) 1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-пиразол,
38) 1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-инидазол,
39) 2-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-2Н-инидазол,
40) 4-хлор-1-[4-[4-(4-метилфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил] -1Н-пиразол,
41) 4-хлор-1-[4-[4-(4-метоксифенил)-1-(1,2,3,6-тетрагидропиридинил)] бутил]-1Н-пиразол,
42) 4-хлор-1-[4-[4-фенил-1-(1,2,3,6-тетрагидропирндинил)]пропил]-1H-пиразол,
43) 4,5-дихлор-1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)] пропил]-2-метил-1H-имидазол,
44) 2-фенил-1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил)-1H-имидазол,
45) 1-[4-[4-(4-метилфенил)-1-(1,2,3,6-тетрагидропиридинил)] бутил]-1Н-бензимидазол,
46) 4,5-дифенил-1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)] бутил]-1Н-имидазол (R4, R5, R6 и R7 не составляют часть другого, возможно, ароматического цикла),
47) 4-хлор-1-[4-[4-(1-нафтил)-1-(1,2,3,6-тетрагидропиридинил)] бутил]-1Н-пиразол,
48) 4-хлор-1-[4-[4-(2-нафтил)-1-(1,2,3,6-тетрагидропиридинил)] бутил]-1Н-пиразол,
49) 1-[2-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)] этил] -1Н-бензимидазол,
50) 1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-бензимидазол-хлоргидрат,
51) 1-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-бензимидазол,
52) 1-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-бензимидазол-хлоргидрат,
53) 4,5-дихлор-2-метил-1-[4-[4-(3-трифторметилфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-имидазол-хлоргидрат,
54) 4-хлор-1-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил] -1Н-пиразол-хлоргидрат,
55) 1-[4-[4-(4-фенил)-1-(1,2,3,6-тетрагидропиридинил)] бутил] -1Н-индазол-хлоргидрат,
56) 4,5-дихлор-1-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)] бутил]-2-метил-1Н-имидазол-хлоргидрат,
57) 4-(4-хлорфенил)-1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил] -1Н-пиразол-хлоргидрат,
58) 4-(4-хлорфенил)-2-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил] -1Н-пиразол,
59) 1-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)] бутил] -1Н-триазол-хлоргидрат,
60) 1-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)] бутил] -1Н-триазол,
61) 1-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)] бутил]-2-метил-1Н-бензимидазол,
62) 1-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-индазол,
63) 2-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил]-2Н-индазол,
64) 2-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил]-2Н-бензотриазол-хлоргидрат,
65) 2-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил]-2Н-бензотриазол,
66) 1-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-бензотриазол-хлоргидрат,
67) 1-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-бензотриазол,
68) 4-хлор-1-[4-[4-(4-фторфенил)-1-(1,2,3,6-тетрагидропиридинил)]бутил] -1Н-пиразол-хлоргидрат,
69) 1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-пиразол-хлоргидрат,
70) 1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-триазол-хлоргидрат,
71) 2-фенил-1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)] бутил]-1Н-имидазол-хлоргидрат,
72) 1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-пиррол-хлоргидрат,
73) 1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-пиррол,
74) 4-(4-хлорфенил)-1-[4-(4-гидрокси-4-фенил-1-пиперидинил)бутил] -1Н-пиразол,
75) 1-[4-[4-(4-фторфенил)-4-гидрокси-1-пиперидинил]-бутил]-1Н-бензимидазол,
76) 4-хлор-1-[4-[4-гидрокси-4-(3-трифторметилфенил)-1-пиперидинил]бутил] -1H-пиразол,
77) 1-[4-[ 4-(4-фторфенил)-4-гидрокси-1-пиперидинил]-бутил]-1H-индазол,
78) 2-[4-[4-(4-фторфенил)-4-гидрокси-1-пиперидинил]-бутил]-2Н-индазол,
79) 2-[4-[4-(4-фторфенил)-4-гидрокси-1-пиперидинил] -бутил] -2Н-бензотриазол,
80) 1-[4-[4-(4-фторфенил)-4-гидрокси-1-пиперидинил] -бутил] -2Н-бензотриазол,
81) 3-хлор-1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1Н-индазол,
82) 3-хлор-1-[4-[4-фенил-1-(1,2,3,6-тетрагидропиридинил)]бутил]-1H-индазол-хлоргидрат.
в которой R1, R2, R3 и А имеют значения, указанные в п.1;
m может иметь значение 0-4;
Х обозначает удаляемую группу, как хлор, бром, мезилокси- или тозилоксигруппа,
с азотсодержащим гетероциклическим соединением формулы III
в которой Z1, Z2, Z4 и R6 имеют вышеуказанные значения.


где R1, R2, R3, A, X, "n", Z1, Z2, Z4 и R6 имеют вышеуказанные значения,
5. Способ получения соединений формулы I по любому из пп.1 и 2, отличающийся тем, что осуществляют взаимодействие в условиях алкилирования аминов формулы IV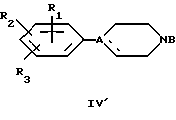
в которой R1, R2, R3 и А имеют вышеуказанное значение, B означает Н или группу -(СН2)n-Х, с производными общей формулы VI
в которой Z1, Z2, Z4, R6 имеют указанное выше значение;
B' имеет значения В, при условии, что когда А означает атом углерода, соединенный с гидроксильной группой, то В означает группу -(СН2)n-Х, а В' означает Н.
в которой R1, R2, R3, n, Z1, Z2, Z4 и R6 имеют вышеуказанное значение;
А обозначает атом углерода, связанный с гидроксильной группой (С-ОН), а пунктирная линия обозначает отсутствие дополнительной связи.
в которой n, Z1, Z2, Z4 и R6 имеют вышеуказанное значение.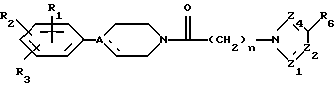
в которой R1, R2, R3, А, "n", Z1, Z2, Z4 и R6 имеют вышеуказанное значение.
| ТРИЦИКЛИЧЕСКИЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ИНГИБИТОРЫ JAK | 2012 |
|
RU2632870C2 |
| Электролизер для получения магния | 1973 |
|
SU441349A1 |
| US 4754038 A, 28.06.88 | |||
| US 4539407 A, 03.09.85 | |||
| Способ получения производных пиперазина или пиперидина или их солей | 1977 |
|
SU683621A3 |
Авторы
Даты
2001-06-10—Публикация
1995-07-26—Подача