Настоящее изобретение относится к гербицидным сульфонамидам, способам их получения и препаративным формам на их основе.
В патентах ЕР №323040 и WO №91/10653 раскрываются гербицидные сульфонамиды, родственные соединениям настоящего изобретения.
Одним из объектов настоящего изобретения являются новые сульфонамиды формулы:
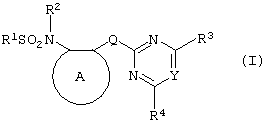
и их соли, где
А представляет собой замещенное или незамещенное бензольное кольцо, или 5-членное замещенное или незамещенное гетероароматическое кольцо;
-Q- представляет собой -O-, -S- или группу -CXX'-,
X и X', которые могут быть одинаковыми или различными, представляют собой атом водорода, атом галогена, циано-, возможно замещенную алкильную группу, или группу -ORa, -SRa или -CORb; или один из Х или X' представляет собой гидроксильную группу, а другой принимает определенные выше значения; или X и X' вместе образуют группу =O или =S;
Ra представляет собой возможно замещенную алкильную, арильную или ацильную группу;
Rb представляет собой возможно замещенную алкильную или арильную группу, или принимает значение -ORc или -NRcRd;
Rc и Rd, которые могут бить одинаковыми или различными, представляют собой атом водорода, возможно замещенную алкильную или арильную группу;
Y представляет собой атом азота или группу CR9;
R1 представляет собой возможно замещенную алкильную, алкенильную, алкинильную, циклоалкильную, арильную группу, гетероциклическую, бензогетероциклическую или аминогруппу;
R2 представляет собой атом водорода, возможно замещенную алкильную или карбоксильную ацильную группу; или группу -SO2R1;
R3 и R4, которые могут быть одинаковыми или различными, представляют собой атом водорода, атом галогена, возможно, замещенную алкильную, алкоксильную, циклоалкильную или аминогруппу или возможно замещенную гетероциклическую группу; и
R9 представляет собой атом водорода или, возможно, замещенную алкильную группу;
при условии, что когда Q принимает значение -O- или -S-, кольцо A представляет собой 5-членное замещенное или незамещенное гетероароматическое кольцо; и
при условии, что когда заместитель R1 представляет собой замещенный алкил, он не является группой формулы:
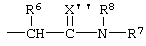
где заместитель Х'' представляет собой атом кислорода или серы, а каждый из заместителей R6, R7 и R8 представляет собой атом водорода или, возможно, замещенную алкильную группу.
Когда A является 5-членным гетероциклическим кольцом, то он предпочтительно проставляет собой замещенное или незамещенное тиофеновое, фурановое, пиррольное, тиазольное, изотиазольное, пиразольное, имидазольное, оксазольное или изоксазольное кольцо.
В кольце A любой из заместителей у атома углерода предпочтительно представляет собой атом галогена, цианогруппы, группу -COOR10 (где заместитель R10 представляет собой атом водорода или, возможно, замещенную алкильную группу), или, возможно, замещенную алкильную, алкоксильную, арилокси-, гетероциклилокси- или аминогруппу. Предпочтительно такими замещающими группами являются атомы фтора и хлора.
Любой из заместителей у атома азота кольца A предпочтительно представляет собой замещенную или незамещенную алкильную, алкоксильную, амино- или арильную группу, особенно метильную группу.
Любая из присутствующих алкильных групп в молекуле предпочтительно имеет от 1 до 8 атомов углерода, более предпочтительно от 1 до 6 атомов углерода, особенно от 1 до 4 атомов углерода. Конкретные предпочтительные незамещенные алкильные или алкилсодержащие группы включают метил, этил, н-пропил, изопропил, н-бутил, трет.-бутил, метокси, этокси и н-пропокси.
Если любая из алкильных групп в молекуле замещена, то заместителями могут быть, например, один или более атомов галогена (например, фтора, хлора или брома), алкокси- или алкилтиогрупп, содержащих от 1 до 4 атомов углерода (например, метокси- или этокси-), гидрокси-, нитро-, меркапто-, амино-, замещенные аминогруппы, карбамоильные, замещенные карбамоильные, тиокарбамоильные, замещенные тиокарбамоильные, циано-, ацильные, арильные или гетероарильные группы. Особенно предпочтительными замещенными алкилсодержащими группами являются хлорметильная, бромметильная, дихлорметильная, трифторметильная, дифторметокси, цианометильная, метоксиэтильная или этоксиэтильная.
Любая из присутствующих алкенильных или алкинильных групп в молекуле предпочтительно имеет от 2 до 6 атомов углерода, например винильная, аллильная или пропаргильная. Любая такая алкенильная или алкинильная группа предпочтительно является незамещенной, хотя, если это необходимо, она может быть замещена, например, галогеном.
Любая из присутствующих циклоалкильных групп в молекуле предпочтительно имеет от 3 до 7 атомов углерода,особенно предпочтительны циклопентильная или циклогексильная группа. Они предпочтительно являются незамещенными.
Любая из присутствующих арильных групп в молекуле предпочтительно представляет собой фенильную, которая желательно замещена одной или более алкильными, алкокси-, алкоксикарбонильными или алкилтиогруппами, содержащими от 1 до 4 атомов углерода (и которые в свою очередь сами могут быть замещенными), атомами галогена, циано-, аминосульфонильными или нитрогруппами; особенно предпочтительно, чтобы фенильная группа была замещена одним или более атомов хлора, брома или фтора, и/или одной или более метильными, метокси-, трифторметильными, метилтио-, метоксикарбонильными, этоксикарбонильными или нитрогруппами.
Любая из гетероциклильных групп в молекуле, не являющаяся кольцом А, предпочтительно представляет собой фурил, тиенил или азотсодержащий гетероцикл, например 5- или 6-членное гетероциклическое кольцо, например пирролил, оксазолил, изоксазолил, изотиазолил, пиримидинил, триазолил или имидазолил. Заместитель R1 также может предпочтительно представлять собой пиридил, фурил, тиенил или бициклическую гетероциклильную группу, например триазолотриазолил, триазолопиримидинил или пиразолопиримидинил.
Любая из бензогетероциклильных групп в молекуле предпочтительно представляет собой бензотиофеновую, бензодиоксолановую, хинолиновую, хиназолиновую, бензотиазольную или дигидробензофурановую группу.
Любой из атомов галогена в молекуле предпочтительно представляет собой атом фтора, хлора или брома.
Любая из замещенных аминогрупп в молекуле может быть моно- или дизамещенной, например, алкилами, содержащими от 1 до 4 атомов углерода, алкенилами, содержащими от 2 до 4 атомов углерода, карбамоильными или ацильными карбоксильными, алкоксикарбонильными, алкилкарбамоильными или диалкилкарбамоильными группами, в которых алкильная группа содержит от 1 до 4 атомов углерода.
Используемое здесь понятие "ацил" подразумевает остаток карбоновой, сульфоновой или фосфорсодержащей кислот, например, группы алканоил, алкеноил, алкиноил, циклоалканоил, аралканоил, ароил, карбамоил, тиокарбамоил, алкоксикарбонил, сульфонил, сульфамоил и фосфонил, в которых любые алкильные, алкенильные, алкинильные или арильные группы могут быть замещенными или незамещенными.
Особенно предпочтительны группы, в которых R1 может представлять собой метил, хлорметил, бромметил, цианометил, трифторметил или 2,2,2-трифторэтил.
Заместитель R2 предпочтительно представляет собой атом водорода.
Каждый из R3 и R4 предпочтительно представляет собой атом водорода, метил, метоксигруппу или атом хлора.
Особенно предпочтительно, если заместители R3 и R4 одинаковы и наиболее предпочтительно, когда оба из них представляют собой метоксигруппу.
Кольцо A предпочтительно представляет собой бензольное (возможно, замещенное атомами фтора, хлора, брома, метильной, метокси- или этоксигруппами) или пиразольное (возможно, замещенное одной или более метильными группами).
Заместитель Q предпочтительно представляет собой -CH2-, -CH(CH3)-, -S- или -O-.
Предпочтительными солями соединений формулы I являются соли, образованные сильными основаниями, такими как соли щелочных металлов (например, калия или натрия), соли аминов (например, трифтиламина, диизопропиламина, циклогексиламина или пиперидина).
Наиболее предпочтительными соединениями настоящего изобретения являются соединения, которые приведены ниже в Примерах.
Другим объектом настоящего изобретения является способ получения сульфонамида формулы I, заключающийся во взаимодействии амина формулы:
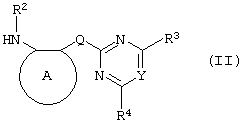
где заместители А, Q, Y и R2-R4 принимают описанные выше значения, с подходящим сульфоновым ангидридом формулы (R1SO2)2O или сульфонилгалогенидом формулы R1SO2Hal, где Hal является атомом галогена, а заместитель R1 принимает описанные выше значения, с образованием требуемого соединения.
Реакция достаточно легко протекает в присутствии основания, например органического основания, такого как пиридин.
В свою очередь соединения формулы II могут быть получены реакцией замещенного амина формулы:
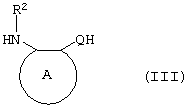
где A, Q и R2 принимают описанные выше значения, в присутствии основания с соединением формулы:
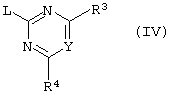
где заместители Y, R3 и R4 принимают описанные выше значения, а заместитель L является уходящей группой, с образованием требуемого соединения.
Уходящая группа L может быть любой подходящей для этого группой, однако предпочтительно она представляет собой атом галогена, особенно атом хлора, или метилсульфонильную группу.
В качестве основания предпочтительно использовать алкиллитий, например трет.-бутиллитий, и реакцию желательно проводить в среде растворителя, например тетрагидрофурана.
Соединения формулы II, в которых заместитель R2 представляет собой атом водорода, альтернативно могут быть получены восстановлением соответствующих нитросоединений формулы:
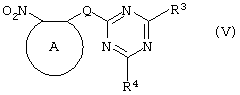
где заместители А, Q, Y, R3 и R4 принимают описанные выше значения.
Восстановление удобно осуществлять с помощью хлорида олова(II); альтернативный метод заключается в обработке железом в кислой среде, особенно предпочтительно в трифторуксусной кислоте и/или ее ангидриде, по методикам, которые сами по себе известны. По последней методике первоначально происходит превращение нитрогруппы в группу -NHCOCF3, которая затем превращается в аминогруппу действием основания, например карбоната калия.
При необходимости соединения формулы II могут быть превращены в другие соединения формулы II известными методами. Например, соединения формулы II, в которых заместитель Х или X' представляет собой алкильную группу, могут быть получены из соответствующих соединений формулы II, в которых Q представляет собой -CH2-, а R2 - атом водорода, первоначально защитой аминогруппы, например, реакцией соединения с ди-трет.-бутилдикарбонатом, обработкой защищенного соединения алкилирующим агентом, например метилиодидом, в присутствии сильного основания, с последующим снятием защиты аминогруппы, например, трифторуксусной кислотой.
В свою очередь соединения формулы V могут быть получены взаимодействием соединения формулы:
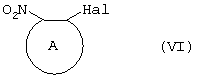
где заместитель А принимает описанные выше значения, а Hal является атомом галогена, в присутствии основания с соединением, соответствующим формуле IV, в котором заместители R3 и R4 принимают описанные выше значения, а заместитель L представляет собой группу -OH, где заместитель Q принимает описанные выше значения.
Альтернативно соединения формулы V могут быть получены реакцией нитросоединения формулы:
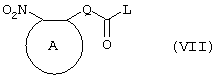
где заместители A и Q принимают описанные выше значения, а заместитель L представляет собой уходящую группу (предпочтительно атом хлора или имидазол-I-ил), в присутствии основания с соединением формулы R3C(=NH)YHC(=NH)R4, где заместители Y, R3 и R4 принимают описанные выше значения.
Предпочтительным основанием является диизопропилэтиламии.
Соединения формулы II, где заместитель А представляет собой N-метилпиразольное кольцо, а заместитель R3 - атом водорода, альтернативно могут быть получены реакцией диметиламиноакрилонитрила формулы:
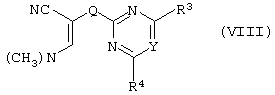
где заместители Q, Y, R3 и R4 принимают описанные выше значения, с метилгидразином в уксусной кислоте с образованием целевого соединения.
Исходные вещества в описанных выше процессах, в частности особенно соединения формул III, IV, VI, VII и VIII, являются либо известными соединениями, либо могут быть получены известными методами из родственных соединений, которые хорошо известны квалифицированным в этой области специалистам.
Соли соединений формулы I могут быть получены известными методами обработкой соответствующих свободных соединений подходящим основанием в подходящем растворителе (например, в эфире).
Соединения формулы I, в которых заместитель R2 отличен от атома водорода, альтернативно могут быть получены из солей соединений формулы I реакцией с подходящим алкилирующим или ацилирующим агентом, содержащим требуемую группу R2, методами, аналогичными известным.
Соединения формулы I обладают гербицидной активностью в отношении широкого спектра широколиственных и злаковых сорняков, но являются относительно безопасными для некоторых культур. Следовательно, они могут быть использованы в качестве селективных сербицидов, в частности, для уничтожения большого числа сорняков в посевах зерновых, сахарной свеклы или других культур, например пшеницы, ячменя, кукурузы, сои, масляничного рапса, хлопчатника или риса.
Таким образом, еще одним объектом настоящего изобретения является способ уничтожения сорной растительности на участках, засоренных сорняками или на участках, на которых предполагается их появление, который заключается в обработке вышеуказанных участков эффективным количеством одного или более соединений формулы I.
Желательными дозами применения соединений формулы I или их солей являются дозы в интервале от 0.001 до 2 кг/га, предпочтительно от 0.005 до 1 кг/га, более предпочтительно от 0.01 до 0.5 кг/га.
Другим объектом настоящего изобретения являются препаративные формы, которые содержат одно или более соединений настоящего изобретения в смеси с приемлемым носителем и/или поверхностно-активным веществом.
Препаративные формы обычно содержат 0.01 до 99 мас.% соединений настоящего изобретения и обычно первоначально готовятся в виде концентратов, содержащих от 0.5 до 99%, предпочтительно от 0.5 до 85% и более предпочтительно от 10 до 50 мас.% этих соединений. Такие концентраты разбавляются, если необходимо, перед обработкой участков так, чтобы содержание активного ингредиента в используемой рецептуре составляло от 0.01 до 5 мас.%.
В качестве носителя может быть использована вода, в которой в некоторых случаях может содержаться органический растворитель, хотя обычно он не используется. Текучий суспензионный концентрат может быть получен путем измельчения соединения с водой, смачивателем и суспендирующим агентом, например с ксантановой смолой.
В качестве носителя может быть использован несмешивающийся с водой органический растворитель, например углеводород, кипящий в интервале 130-270°C, например ксилол, в котором растворяется или суспендируется соединение настоящего изобретения. Также может быть получен эмульгирующийся концентрат, содержащий не смешивающийся с водой растворитель и поверхностно-активное вещество так, что концентрат действует как самоэмульгирующееся масло при смешении его с водой.
В качестве носителя может быть использован и твердый продукт, который подвергается тонкому измельчению или гранулированию. Примерами приемлемых твердых носителей являются известняк, глины, песок, слюда, мел, аттапульгит, диатомит, перлит, сепиолит, кремнеземы, силикаты, лигносульфонаты и твердые удобрения. Носитель может быть природным или синтетическим материалом, или модифицированным природным продуктом.
Смачивающиеся порошки, растворимые или диспергирующиеся в воде, также могут быть получены путем смешения соединения настоящего изобретения в форме частиц с носителем в форме частиц или при разбрызгивании расплавленного соединения на носитель в форме частиц, смешанный со смачивающим агентом и диспергирующим агентом и с последующим измельчением всей порошкообразной смеси.
Аэрозольная препаративная форма может быть приготовлена путем смешения соединения настоящего изобретения с пропиллентом, например с полигалогенированными алканами, таким как дихлорфторметан, а также, при необходимости, с растворителем.
Понятие "поверхностно-активное вещество" в широком смысле включает материалы, называемые эмульгирующими агентами, диспергирующими агентами и смачивающими агентами. Такие агенты хорошо известны в данной области.
Используемые поверхностно-активные вещества могут быть анионными, например, такими как моно- или диэфиры фосфорной кислоты и этоксилированных жирных спиртов, или соли таких эфиров, сульфаты жирных спиртов, такой как додецилсульфат натрия, этоксилированные сульфаты жирных спиртов, этоксилированные сульфаты алкилфенола, лигнинсульфаты, нефтяные сульфонаты, алкиларилсульфонаты, такие как алкилбензолсульфонаты или низшие алкилнафталинсульфонаты, соли сульфированных продуктов конденсации нафталина с формальдегидом, или более сложные сульфонаты, такие как сульфонаты амидов, например сульфированный продукт конденсации олеиновой кислоты и N-метилтаурина или диалкилсульфосукцинаты, например натриевая соль сульфированного диоктилсукцината.
Поверхностно-активные вещества могут также представлять собой неионные агенты, например продукты конденсации либо эфиров жирных кислот, жирных спиртов, амидов жирных кислот, либо алкилзамещенных фенолов с этиленоксидом, эфиры жирных кислот с простыми эфирами многоатомных спиртов, например сорбитановые эфиры жирных кислот, продукты конденсации таких эфиров с этиленоксидом, например полиоксиэтиленсорбитановые эфиры жирных кислот, блок-сополимеры этиленоксида и пропиленоксида, ацетиленовые гликоли, такие как 2,4,7,9-тетраметил-5-децин-4,7-диол, или этоксилированные ацетиленовые гликоли.
Поверхностно-активные вещества также могут быть катионными агентами, например алкил- и/или арилзамещенными четвертичными аммониевыми соединениями, такими как цетилтриметиламмонийбромид, и этоксилированными жирными третичными аминами.
Предпочтительными поверхностно-активными веществами являются этоксилированные сульфаты жирных спиртов, лигнинсульфонаты, алкиларилсульфонаты, соли сульфированных продуктов конденсации нафталина с формальдегидом, олеил-N-метилтаурид натрия, диалкилсульфосукцинаты, этоксилированные алкилфенолы и жирные алкилэтоксилаты.
Активные соединения настоящего изобретения, особенно те, которые представлены в приведенных ниже Примерах, могут быть смешаны с другими пестицидами, например с другим гербицидом, фунгицидом или инсектицидом или с регулятором роста растений. Особенно предпочтительно использование другого гербицида. Приемлемыми дополнительными гербицидами являются триэтазин, линурон, МСРА, дихлорпроп, изоксабен, дифлувеникан, метолахлорн, фторметурон, оксифлуорфен, фомесафен, бентазон, прометрин, норфлуразон, хломазон, ЭПТК, имазаквин, более предпочтительно изопротурон, ментибензтиазурон, трифлуралин, иоксинил, бромоксинил, беназолин, мекопроп, флуроксипир, алахлор, ацифлуорфен, лактофен, метрибузин и пендиметалин, и наиболее предпочтительно этофумесат и фенмедифам.
Соединения настоящего изобретения могут быть использованы для обработки растений, почвы, наземных и водных площадей и особенно участков, на которых растут культуры или на которых они должны будут выращиваться. Данные соединения обладают как довсходовой, так и послевсходовой активностью.
Изобретение иллюстрируется следующими примерами.
ПРИМЕР А
ПРИМЕР А1
1,1,1-Трифтор-2'-(4,6-диметоксипиримидин-2-илметил)метансульфонанилид
(а) 2-(4,6-Диметоксипиримидин-2-илметил)анилин
Метод 1
К раствору о-толуидина (5.35 г) в сухом тетрагидрофуране (100 мл) при перемешивании и температуре -70°С в атмосфере азота добавляют по каплям н-бутиллитий (21 мл 2.5 М раствора в гексане). Полученной суспензии дают нагреться до 5°С, получая светло-желтый раствор. В реационную смесь барботируют сухой диоксид углерода в течение приблизительно 6 мин. Растворитель упаривают при перемешивании в высоком вакууме при комнатной температуре. Полученное белое твердое вещество суспендируют в сухом тетрагидрофуране и охлаждают до 70°С в атмосфере азота и по каплям в течение 15 мин добавляют трет.-бутиллитий (70 мл 1.6 М раствора в пентане). Смеси дают нагреться до -15°C и перемешивают при этой температуре в течение 75 мин. Смесь охлаждают до -70°C и добавляют по каплям раствор 4,6-диметокси-2-метилсульфонилпиримидина (10.9 г) в тетрагидрофуране. Смесь перемешивают при -75°C в течение 60 мин и оставляют на ночь при комнатной температуре. Растворитель упаривают в вакууме, к остатку в атмосфере азота при охлаждении водой со льдом добавляют 2 н. соляную кислоту. Затем добавляют 250 мл воды, полученный мутный раствор подщелачивают насыщенным раствором бикарбоната натрия и экстрагируют эфиром (2×400 мл). Объединенные экстракты промывают насыщенным раствором бикарбоната натрия, сушат и упаривают. Полученное оранжевое масло очищают хроматографированием, получают 2 г продукта в виде твердого вещества желтого цвета, т.пл. 82-84°C.
Метод 2
(I) 4,6-Диметокси-2-(2-нитробензил)пиримидин
К суспензии дихлоргидрата малонимидата (73.2 г) в метиленхлориде (400 мл) при -40°С в атмосфере азота при перемешивании добавляют по каплям диизопропилэтиламин (240 мл), перемешивают в течение 25 мин, получают суспензию A. К суспензии карбонилдиимидазола (53.3 г) в метиленхлориде (400 мл) при перемешивании при комнатной температуре порциями добавляют 2-нитрофенилуксусную кислоту (65.16 г). Полученный раствор перемешивают в течение 10 мин и в течение 30 мин при -40°C при перемешивании добавляют по каплям к суспензии А. Смесь перемешивают при -40°С в течение 45 мин и при комнатной температуре в течение ночи. Раствор промывают водой (400 мл), 2 н. HCl (400 мл) и насыщенным раствором бикарбоната натрия (400 мл), сушат и упаривают. Полученное твердое вещество оранжевого цвета перемешивают с 2-пропанолом (60 мл) в течение 10 мин и фильтруют. Фильтрат промывают 50 мл 2-пропанола и сушат, получают 32.6 г требуемого продукта в виде желтого твердого вещества, т.пл. 92-93°C.
(II) 2-(4,6-Диметоксипиримидин-2-илметил)анилин
К суспензии дигидрата хлорида олова(II) (133 г) в этаноле (300 мл) при перемешивании добавляют продукт со стадии (I). Смесь кипятят в течение 2 ч, выливают в воду со льдом (2500 мл) и экстрагируют этилацетатом (3×500 мл). Объединенные экстракты промывают насыщенным раствором хлорида натрия, сушат и упаривают, получают 24.3 г требуемого продукта в виде коричневого твердого вещества, т.пл. 82-84°С.
(б) 1,1,1-Трифтор-2'-(4,6-диметоксипиримидин-2-илметил)-метансульфонанилид
К раствору 2-(4,6-диметоксипиримидин-2-илметил)анилина (0.98 г) и пиридина (0.31 г) в сухом метиленхлориде (15 мл) при -70°C в атмосфере азота порциями добавляют трифторметансульфоновый ангидрид (1.12 г). Полученный оранжевый раствор перемешивают в течение 2 ч при -75°C и дают нагреться до комнатной температуры в течение 1 ч. Смесь промывают водой, сушат, получают красное масло, которое очищают хроматографированием и перекристаллизацией из петролейного эфира 60-80°, получают 0.4 г продукта в виде белого твердого вещества, т.пл. 99-100°C.
ПРИМЕР А2
1,1,1-Трифтор-2'-[1-(4,6-диметоксипиримидин-2-ил)этил]метансульфонанилид
(а) трет.-Бутил-[2-(4,6-диметоксипиримидин-2-илметил)фенил]карбамат
Раствор продукта со стадии (а) Примера А1 (24.1 г) и ди-трет.-бутилдикарбоната (24 г) кипятят в сухом тетрагидрофуране (250 мл) в атмосфере азота в течение 4 ч. Растворитель упаривают, полученное коричневое масло кристаллизуют из гексана (200 мл), получают 28 г требуемого соединения в виде коричневого твердого вещества, т.пл. 98-100°C.
(б) трет.-Бутил-[2-[1-(4,6-диметоксипиримидин-2-ил)этил]-фенил]карбамат
Продукт с вышеописанной стадии (а) (1 г) растворяют в сухом тетрагидрофуране (20 мл) и в атмосфере азота добавляют тетраметилэтилендиамин (1.1 мл). Раствор охлаждают до -70°C и по каплям добавляют 1.7 М раствор трет.-бутиллития в пентане (4.3 мл). Затем смесь перемешивают при -20°C в течение 1 ч, охлаждают до -70°C и добавляют метилиодид (0.45 г). Реакционной смеси дают нагреться до 0°С и добавляют насыщенный раствор хлорида аммония (25 мл). Смесь экстрагируют тетрагидрофураном (3×50 мл), объединенные экстракты сушат и упаривают, полученное палево-коричневое твердое вещество растирают с гексаном, получают 0.73 г требуемого продукта, т.пл. 119-121°С.
(в) 2-[1-(4,6-Диметоксипиримидин-2-ил)этил]анилин
Продукт с вышеописанной стадии (б) (5.0 г) добавляют к трифторуксусной кислоте (25 мл) и полученный раствор перемешивают при комнатной температуре в течение 3 ч. Раствор упаривают, остаток растирают с диизопропиловым эфиром и охлаждают смесью сухой лед-ацетон. Твердое вещество отфильтровывают, промывают диизопропиловым эфиром, получают 3.5 г требуемого продукта, т.пл. 136-139°C.
(г) 1,1,1-Трифтор-2'-[1-(4,6-диметоксипиримидин-2-ил)этил]-метансульфонанилид
Названное соединение получают по методике, аналогичной описанной на стадии (б) Примера А1, используя в качестве исходного продукт с вышеописанной стадии (в), т.пл. 132-133°C.
ПРИМЕР A3
1,1,1-Трифтор-2'-(4,6-диметокси-1,3,5-триазин-2-илметил)метансульфонанилид
(а) 2,4-Диметокси-6-(2-нитробензил)-1,3,5-триазин
К суспензии 2-нитрофенилуксусной кислоты (3.4 г) в метиленхлориде (30 мл) при перемешивании порциями добавляют карбонилдиимидазол (3.34 г) и перемешивают смесь при комнатной температуре в течение 30 мин. Полученный раствор красного цвета при перемешивании добавляют по каплям к суспензии цинковой соли диметилимидодикарбонимидата (3.0 г) в метиленхлориде (25 мл) при -35°C. Реакционную смесь перемешивают при комнатной температуре в течение ночи и выливают в воду (100 мл). Смесь экстрагируют метиленхлоридом (3×50 мл), объединенные экстракты сушат и упаривают. Полученное масло красного цвета растирают с эфиром, получают 1.41 г требуемого продукта в виде твердого вещества палево-коричневого цвета, т.пл. 91.6-92.3°C.
(б) 1,1,1-Трифтор-2'-(4,6-диметокси-1,3,5-триазин-2-ил-метил)метансульфонанилид
Названное соединение получают по методикам, аналогичным описанным в Примере А1(а), Метод 2(II) и А1(б), используя в качестве исходного продукт с вышеописанной стадии (А), т.пл. 101-108°C.
ПРИМЕР А4
N-[3-(4,6-диметоксипиримидин-2-илметил)-2-пиридил]-1,1,1-трифторметансульфонамид
(а) трет.-Бутил-(3-метил-2-пиридил)карбамат
Раствор 2-амино-3-метилпиридина (20 г) и ди-трет.-бутилдикарбоната (46.8 мл) в сухом тетрагидрофуране кипятят в течение 3 ч и упаривают. Полученное темно-коричневое масло растворяют в этилацетате (400 мл), промывают 1 н. лимонной кислотой (3×200 мл) и насыщенным раствором хлорида натрия, сушат и упаривают. Полученный палево-желтый твердый остаток кристаллизуют из смеси гексан-диизопропиловый эфир (1:2), получают 6.5 г требуемого продукта в виде палево-желтого твердого вещества, т.пл. 135-137°С.
(б) трет.-Бутил-[3-(4,6-диметоксипиримидин-2-илметил)-2-пиридил]-карбамат
Продукт с вышеописанной стадии (а) (5 г) растворяют в сухом тетрагидрофуране (100 мл) и в атмосфере азота при -70°C добавляют по каплям трет.-бутиллитий (19.2 мл 2.5 М раствора в гептане). Смесь перемешивают при -70°C в течение 20 мин, затем при 5°C в течение 3 ч. Смесь охлаждают до -70°С, добавляют 4,6-диметокси-2-метилсульфонилпиримидин (5.42 г) и перемешивают при -70°С в течение 1 ч и при комнатной температуре в течение ночи. К смеси добавляют насыщенный раствор хлорида аммония (500 мл) и экстрагируют этилацетатом (2×100 мл). Объединенные экстракты промывают насыщенным раствором хлорида натрия (50 мл), сушат и упаривают. Полученное оранжевое масло растирают с гексаном, получают 5.35 г требуемого продукта в виде твердого вещества палево-желтого цвета, т.пл. 89-92°С.
(в) N-[3-(4,6-диметоксипиримидин-2-илметил)-2-пиридил]-1,1,1-трифторметансульфонамид
Названное соединение получают по методике, аналогичной описанной на стадии (б) Примера А1, используя в качестве исходного продукт с вышеописанной стадии (б), т. пл. 124-126°C.
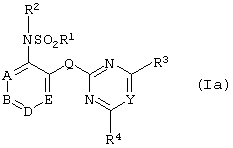
ПРИМЕРЫ А5-А17
Методами, аналогичными описанным выше в Примере А1, могут быть получены следующие соединения формулы Ia, где А представляет собой =CR5; заместитель Q представляет собой -CH2-; заместитель R2 представляет собой Н; В, D и Е принимают значение =CH-; а каждый из заместителей R3 и R4 представляет собой метоксигруппу:
ПРИМЕРЫ А18-А20
Методами, аналогичными описанным выше в Примере А1, могут быть получены следующие соединения формулы Ia, где А представляет собой атом азота; заместитель Q представляет собой -CH2-; заместитель R2 представляет собой Н; В, D и Е принимают значение =CH-; а каждый из заместителей R3 и R4 представляет собой метоксигруппу:
ПРИМЕРЫ А21-А68
Описанными выше методами могут быть получены следующие соединения формулы 1а, где заместитель R2 представляет собой атом водорода; каждый из заместителей R3 и R4 представляет собой метоксигруппу, а заместитель представляет собой -CH-:
ПРИМЕРЫ А69-А125
Описанными выше методами могут быть получены следующие соединения формулы Ia, где заместитель R2 представляет собой Н; каждый из заместителей R3 и R4 представляет собой метоксигруппу; А представляет собой =CR5; а заместитель Q представляет собой -CH2-:
ПРИМЕРЫ А126-А127
Описанными выше методами могут быть получены следующие соединения формулы Ia, где заместитель R2 представляет собой Н; каждый из заместителей R3 и R4 представляет собой метоксигруппу; А представляет собой =CR5; а заместитель Q представляет собой -CHMe-:
ПРИМЕР Б
ПРИМЕР Б1
N-[3-(4,6-Диметоксипиримидин-2-илтио)-1,5-диметил-1Н-пиразол-4-ил]-1,1,1-трифторметансульфонамид и N-[5-(4,6-диметоксипиримидин-2-илтио)-1,3-диметил-1Н-пиразол-4-ил]-1,1,1-трифторметансульфонамид
(а) 5-(4,6-диметоксипиримидин-2-илтио)-3-метил-4-нитро-1H-пиразол
К раствору 4,6-диметокси-2-меркаптопиримидина (4.65 г) в водном растворе гидроксида калия (1,7 г в 75 мл воды) по каплям добавляют раствор 1,4-динитро-3-метилпиразола (4.65 г), растворенного в минимальном количестве этанола. Реакция протекает экзотермично и по ее окончании смесь перемешивают в течение 45 мин. Выпавший осадок отфильтровывают, промывают свежей водой, сушат, получают 6.3 г требуемого продукта, т.пл. 175-176°С.
(б) 5-(4,6-Диметоксипиримидин-2-илтио)-1,3-диметил-4-нитро-1H-пиразол и 3-(4,6-диметоксипиримидин-2-илтио)-1,5-диметил-4-нитро-1Н-пиразол
К смеси 60%-ной суспензии гидрида натрия (0.47 г) и сухого диметилформамида (20 мл) при перемешивании и охлаждении на ледяной бане порциями добавляют продукт с вышеописанной стадии (а) (3.15 г). По окончании добавления смесь перемешивают в течение 10 мин при комнатной температуре и добавляют по каплям метилиодид (1.7 г). Смесь перемешивают при комнатной температуре в течение 2.5 ч, выливают воду со льдом (50 мл), экстрагируют этилацетатом (3×50 мл), объединенные экстракты промывают водой и сушат сульфатом магния. Фильтрацией и последующим упариванием выделяют сырой продукт в виде масла.
Сырой продукт подвергают быстрой хроматографии на силикагеле (элюент этилацетат-петролейный эфир 40-60°, 1:1) и выделяют два новых продукта. Упариванием фракций, содержащих чистые вещества, выделяют два различных твердых продукта.
По результатам тонкослойной хроматографии (ТСХ) на силикагелевых пластинках (элюент этилацетат-петролейный эфир 40-60°, 1:1) один продукт имеет Rf около 0,75 (по-видимому, 5-(4,6-диметоксипиримидин-2-илтио)-1,3-диметил-4-нитро-1Н-пиразол), а другой - Rf около 0,3 (по-видимому, 3-(4,6-диметоксипиримидин-2-илтио)-1,5-диметил-4-нитро-1Н-пиразол). Выход продукта с Rf 0,75 составляет 1.3 г, т.пл. 124-125°C. Выход продукта с Rf 0,3 составляет 0.82 г, т.пл. 155-156°C.
(в) 3-(4,6-Диметоксипиримидин-2-илтио)-1,5-диметил-1H-пиразол-4-амин и 5-(4,6-диметоксипиримидин-2-илтио)-1,3-диметил-1H-пиразол-4-амин
Смесь продукта со стадии (б) (Rf 0,3) (2,4 г) и дигидрата хлорида олова(II) (8,7 г) в этаноле (100 мл) перемешивают при кипячении в течение 4 ч. Этанол упаривают в вакууме, остаток перемешивают с водой (100 мл) и подщелачивают твердым бикарбонатом натрия. Добавляют этилацетат (100 мл), полученную эмульсию фильтруют через кизельгуровую прокладку и органический слой отделяют. Осадок промывают этилацетатом (общим количеством 75 мл), а водный слой экстрагируют этилацетатом (2×50 мл). Объединенные органические слои промывают водой (50 мл), отделяют и сушат сульфатом магния. После упаривания этилацетата остается масло, которое кристаллизуется. Сырой продукт очищают быстрой хроматографией на силикагеле (элюент этилацетат), выделяют новый продукт с Rf 0.3 (ТСХ на силикагеле, элюент этилацетат). Упариванием фракций, содержащих чистый новый продукт, получают 1.33 г твердого вещества с т.пл. 104-105°C.
Аналогичным методом получают другой изомер, выход 2.6 г, т.пл. 74-75°C.
(г) N-[3-(4,6-Диметоксипиридин-2-илтио)-1,5-диметил-1H-пиразол-4-ил]-1,1,1-трифторметансульфонамид (Б1а) и N-[5-(4,6-диметоксипиримидин-2-илтио)-1,3-диметил-1Н-пиразол-4-ил]1,1,1-трифторметансульфонамид (Б1б)
К раствору аминопиразола с вышеописанной стадии (в) (Rf 0.3, 1.2 г) в сухом метиленхлориде (30 мл) при перемешивании и при -60°С (охлаждение на бане сухой лед-ацетон) добавляют по каплям раствор трифторметансульфонового ангидрида (1.2 г) в сухом метиленхлориде (10 мл). По окончании добавления температуру смеси медленно доводят до комнатной и перемешивают в течение ночи. Полученный темно-красный раствор разбавляют 100 мл свежего метиленхлорида, промывают водой (25 мл), 1 М HCl (25 мл) и водой (25 мл). Слои разделяют, органический слой сушат сульфатом магния, фильтруют, упаривают, получают полутвердое темно-красное вещество. Быстрой хроматографией на силикагеле (элюент этилацетат-петролейный эфир 40-60°, 1:1) выделяют новый продукт с Rf 0.5 (ТСХ на силикагелевых пластинках, элюент этилацетат-петролейный эфир 40-60°, 1:1). Фракции, содержащие чистый новый продукт, упаривают, получают требуемый продукт (Б1а) в виде белого твердого вещества. Выход 0.83 г, т.пл. 203-204°C.
Аналогичным методом получают другой изомер (Б1б), выход 1.8 г, т.пл. 145-146°C.
ПРИМЕР Б2
1-Циано-N-[3-(4,6-диметоксипиримидин-2-илтио)-1,5-диметил-1Н-пиразол-4-ил]-1,1,1-трифторметансульфонамид (Б2а) и 1-циано-N-[5-(4,6-диметоксипиримидин-2-илтио)-1,3-диметил-1H-пиразол-4-ил]-1,1,1-трифторметансульфонамид (Б2б)
Аминопиразол со стадии (с) Примера Б1 (Rf 0,3, 0,8 г) растворяют в сухом метиленхлориде (10 мл) и при перемешивании добавляют сухой пиридин (0.23 г). Смесь охлаждают до -78°C (на бане сухой лед-ацетон) и порциями добавляют цианометансульфонилхлорид (0,4 г, 0,00285 моля). Смеси дают медленно нагреться до комнатной температуры и перемешивают в течение 2 дней. Затем смесь разбавляют этилацетатом до 100 мл и промывают водой, 1 М HCl, снова водой и разделяют слои. Органический слой фильтруют, сушат сульфатом магния, фильтруют и упаривают. Остаток подвергают быстрой хроматографии на силикагеле (элюент диэтиловый эфир), получают новый продукт с Rf 0,4 (приблизительно) (ТСХ на силикагеле, элюент диэтиловый эфир).
Фракции с чистым продуктом объединяют, упаривают, получают требуемый продукт (Б2а) в виде твердого вещества желтого цвета (700 мг), т.пл. 166-167°С.
Аналогичным методом получают другой изомер (Б2б) в виде твердого вещества, выход 1,6 г.
ПРИМЕР Б3
1-Циано-N-[4-(4,6-диметоксипиримидин-2-илтио)-1-метил-1H-пиразол-5-ил]метансульфонамид (Б3а) и 1-циано-N-[4-(4,6-диметоксипиримидин-2-илтио)-1-метил-1H-пиразол-3-ил]метансульфонамид (Б3б)
(а) 2-(4,6-Диметоксипиримидин-2-илтио)-3-(диметиламино)-акрилонитрил
Смесь диметилацеталя диметилформамида (5.8 г) и 2-(4,6-диметоксипиримидин-2-илтио)ацетонитрила (5.1 г) перемешивают при 100°С на масляной бане в течение 5 ч и оставляют на ночь при комнатной температуре. Сырой твердый продукт растирают с диизопропиловым эфиром, получают требуемый продукт в виде твердого вещества желтого цвета с выходом 5.4 г.
(б) 4-(4,6-Диметоксипиримидин-2-илтио)-1-метилпиразол-3-амин и 4-(4,6-диметоксипиримидин-2-илтио)-1-метилпиразол-5-амин
К смеси продукта с вышеописанной стадии (а) (2,6 г) и ледяной уксусной кислоты (10 мл) добавляют по каплям метилгидразин (1,0 г), нагревают на масляной бане до 100°C и выдерживают в течение 3 часов. Смеси дают охладиться и выливают в воду (100 мл). Затем смесь нейтрализуют твердым бикарбонатом натрия и экстрагируют этилацетатом (3×75 мл). Объединенные органические слои промывают водой (30 мл), отделяют, сушат сульфатом магния, фильтруют и упаривают. Полученное масло подвергают быстрой хроматографии на силикагеле (элюент - чистый этилацетат), получают главным образом один продукт (Rf 0.3, ТСХ на силикагеле, элюент этилацетат). Фракции с чистым продуктом объединяют, упаривают, получают не совсем белый продукт с выходом 2.2 г. Спектр 1Н ЯМР указывает, что он представляет собой 50/50 смесь двух возможных изомерных продуктов. Полученные изомеры были разделены с помощью препаративной жидкостной хроматографией высокого давления. Упариванием фракций, содержащих отдельные чистые изомеры, получают оба продукта в виде бесцветных кристаллов.
Один из полученных продуктов (А) выделен с выходом 480 мг, т.пл. 110-111°C (по видимому, 4-(4,6-диметоксипиримидин-2-илтио)-1-метилпиразол-5-амин). Другой продукт (Б) (по-видимому, 4-(4,6-диметоксипиримидин-2-илтио)-1-метилпиразол-3-амин), выделен с выходом 800 мг, т.пл. 160-161°C.
(в) 1-Циано-N-[4-(4,6-диметоксипиримидин-2-илтио)-1-метил-1H-пиразол-5-ил]метансульфонамид и 1-циано-N-[4-(4,6-диметоксипиримидин-2-илтио)-1-метил-1Н-пиразол-3-ил] метансульфонамид
Раствор пиразола (А) с вышеописанной стадии (б) (475 мг) в метиленхлориде (10 мл) охлаждают до -78°C (на бане сухой лед-ацетон) и при перемешивании добавляют пиридин (0,15 мл). С помощью шприца добавляют по каплям раствор цианометансульфохлорида (250 мл) в метиленхлориде (1 мл), затем дают медленно нагреться до комнатной температуры и перемешивают в течение ночи. Смесь разбавляют этилацетатом до 100 мл, промывают водой (30 мл), разбавленной соляной кислотой (2×30 мл) и насыщенным раствором хлорида натрия (30 мл). Органический слой отделяют, сушат сульфатом магния, фильтруют, упаривают, получают не совсем белый твердый продукт (по-видимому, 1-циано-N-[4-(4,6-диметоксипиримидин-2-илтио)-1-метил-1Н-пиразол-5-ил]метансульфонамид) (Б3а). После перекристаллизации из этанола выделяют 350 мг продукта, т.пл. 206-207°C. Другой изомер (Б3б) получают аналогичным методом, используя в качестве исходного пиразол (Б) с вышеописанной стадии (б), выход 650 мг, т.пл. 147-148°C.
ПРИМЕР Б4
N-[3-(4,6-Диметокси-1,3,5-триазин-2-ил)-1,5-диметил-1Н-пиразол-4-ил]-1,1,1-трифторметансульфонамид
(а) Диэтил-(5-метил-4-нитропиразол-3-ил)малонат
К смеси 60%-ной суспензии гидрида натрия (2.3 г) в сухом тетрагидрофуране (100 мл) при перемешивании и охлаждении на ледяной бане добавляют по каплям диэтилмалонат (9.4 г), перемешивают в течение 10 мин, после чего небольшими порциями в течение 10 мин добавляют 1,5-динитро-3-метилпиразол (5.0 г), поддерживая температуру 10-12°C. Смесь перемешивают при комнатной температуре в течение 30 мин и в течение приблизительно 5 мин добавляют по каплям ледяную уксусную кислоту (3 мл). Смесь разбавляют этилацетатом (400 мл), промывают водой (2×30 мл), органический слой отделяют, сушат сульфатом магния, фильтруют и упаривают. Остаток представляет собой масло, которое кристаллизуется при растирании с перролейным эфиром 60-80°С. Получают 7,5 г требуемого продукта в виде палево-желтого твердого вещества, т.пл. 100-102°С.
(б) (5-Метил-4-нитропиразол-3-ил)уксусная кислота
Смесь гидроксида калия (5.9 г), продукта предыдущей стадии (7.5 г) и 50%-ного водного этанола (100 мл) кипятят при перемешивании в течение 1.5 часа, дают охладиться, упаривают почти досуха, разбавляют водой (100 мл) и подкисляют концентрированной соляной кислотой. Полученную смесь нагревают до приблизительно 80°C в течение 0,5 часа, охлаждают и упаривают досуха. Остаток обрабатывают этилацетатом (100 мл), промывают водой (2×20 мл), органический слой отделяют, сушат сульфатом магния, фильтруют и упаривают. Получают 3.85 г требуемого продукта в виде твердого вещества желтого цвета.
(в) Метил-(5-метил-4-нитропиразол-3-ил)ацетат
Продукт с предыдущей стадии (3.85 г) растворяют в метаноле (75 мл), содержащем несколько капель концентрированной серной кислоты. Полученную смесь кипятят при перемешивании в течение 2 ч и дают охладиться. Метанол упаривают в вакууме, остаток растворяют в этилацетате, промывают водой, органический слой отделяют, сушат сульфатом магния, фильтруют и упаривают. Получают 4.0 г требуемого продукта в виде твердого вещества кремового цвета, т.пл. 132-133°C.
(г) Метил (1,5-диметил-4-нитро-1Н-пиразол-3-ил)ацетат и метил (1,3-диметил-4-нитро-1Н-пиразол-5-ил)ацетат
К смеси карбоната калия (2.5 г) и диметилформамида (30 мл) при перемешивании добавляют продукт с предыдущей стадии (3.3 г), в одну порцию добавляют метилиодид (2.6 г), при этом наблюдается умеренно экзотермическая реакция. Смесь перемешивают в течение ночи при комнатной температуре, разбавляют 100 мл воды и экстрагируют диэтиловым эфиром (4×50 мл). Объединенные экстракты промывают водой (30 мл), отделяют, сушат сульфатом магния, фильтруют и упаривают. Получают 3.2 г требуемой изомерной смеси продуктов в виде маслянистого твердого вещества.
(д) (1,5-Диметил-4-нитро-1H-пиразол-3-ил)уксусная кислота и (1,3-диметил-4-нитро-1Н-пиразол-5-ил)уксусная кислота
К раствору продукта с предыдущей стадии (3.2 г) в этаноле (25 мл) при перемешивании добавляют раствор гидроксида калия (1.7 г) в воде (25 мл) и кипятят при перемешивании в течение 3 ч. Смесь упаривают почти досуха, разбавляют 50 мл воды, подкисляют концентрированной соляной кислотой и упаривают. Остаток растворяют в этилацетате, промывают водой, сушат сульфатом магния, фильтруют и упаривают. Получают 3.2 г требуемой изомерной смеси продуктов в виде твердого вещества оранжевого цвета.
(е) 2-(1,3-Диметил-4-нитро-1H-пиразол-5-илметил)-4,6-диметокси-1,3,5-триазин и 2-(1,5-диметил-4-нитро-1Н-пиразол-3-илметил)-4,6-диметокси-1,3,5-триазин
Продукт с предыдущей стадии (2.56 г) растворяют в метиленхлориде (50 мл) в атмосфере азота, которую поддерживают в течение всех последующих операций. К смеси добавляют карбонилдиимидазол (2.0 г) и перемешивают в течение 30 мин. Полученную смесь при перемешивании добавляют по каплям к суспензии цинковой соли диметилимидодикарбонимидата (2.1 г) в метиленхлориде (25 мл) при -35°C. Реакционной смеси дают нагреться до комнатной температуры и перемешивают в течение ночи. К смеси добавляют воду (50 мл) и метиленхлорид (50 мл), фильтруют через кизельгур, слои разделяют, водный слой экстрагируют метиленхлоридом (3×30 мл). Объединенные органические слои промывают водой, сушат сульфатом магния, упаривают, получают 3,8 г сырого продукта. Быстрой хроматографией на силикагеле (элюент этилацетат) получают два новых продукта, имеющих Rf 0,6 и приблизительно 0,4. Фракции, содержащие продукты, упаривают и получают:
Rf 0.6: 1.0 г 2-(1,3-диметил-4-нитро-1Н-пиразол-5-илметил)-4,6-диметокси-1,3,5-триазин в виде кристаллического твердого вещества и
Rf 0.4: 1.0 г 2-(1,5-диметил-4-нитро-1Н-пиразол-3-илметил)-4,6-диметокси-1,3,5-триазин, т.пл. 145°C.
(ж) 2-(4-Амино-1,5-диметил-4-нитро-1H-пиразол-3-илметил)-4,6-диметокси-1,3,5-триазин
К суспензии 10%-ного палладия на угле (приблизительно 10 мг) в воде (5 мл) добавляют раствор боргидрида натрия (0.13 мл) в воде (5 мл). Через смесь пропускают азот и в течение 5 мин по каплям добавляют раствор продукта с предыдущей стадии с Rf 0.4 (0.5 г) в метаноле (30 мл). Смесь выдерживают при комнатной температуре в течение 30 мин, после чего добавляют уксусную кислоту (1 мл). Смесь фильтруют через кизельгур, промывают метанолом и упаривают почти досуха. Остаток разбавляют 15 мл воды, нейтрализуют твердым бикарбонатом натрия, экстрагируют этилацетатом (3×30 мл), сушат сульфатом магния, фильтруют и упаривают. Получают 400 мг требуемого продукта в виде вязкого оранжевого масла.
(з) N-[3-(4,6-Диметокси-1,3,5-триазин-2-ил)-1,5-диметил-1Н-пиразол-4-ил]-1,1,1-трифторметансульфонамид
К раствору продукта с предыдущей стадии (0.4 г) и пиридина (0.13 мл) в метиленхлориде (15 мл) при перемешивании при -60°С медленно по каплям добавляют раствор трифторметансульфонового ангидрида (0.43 г) в метиленхлориде (5 мл). Смеси дают медленно нагреться до комнатной температуры и перемешивают еще 24 ч. Затем смесь промывают водой (10 мл), отделяют, сушат сульфатом магния, фильтруют и упаривают. Получают 100 мг требуемого продукта в виде палево-желтого вязкого масла.
ПРИМЕР Б5
1-Циано-N-[5-(4,6-диметоксипиримидин-2-илтио)-1,2-диметил-1Н-имидазол-4-ил]металсульфонамид
(а) 1,2-Диметил-4-бром-5-нитро-1Н-имидазол и 1,2-диметил-5-бром-4-нитро-1H-имидазол
2-Метил-4-бром-5-нитроимидазол (35 г) растворяют в водном растворе гидроксида натрия (7 г). При комнатной температуре по каплям добавляют диметилсульфат (21.3 г) и реакционную смесь перемешивают в течение 2 ч. Выпавший осадок отфильтровывают, промывают водой, сушат, получают 33 г смеси изомеров, которые разделяют хроматографированием (элюент петролейный эфир 60-80° - этилацетат, 8:2). Выделяют 9.4 г 1,2-диметил-4-бром-5-нитро-1Н-имидазола, т.пл. 98-99°C и 19.3 г 1,2-диметил-5-бром-4-нитро-1Н-имидазола, т.пл. 160-162°C.
(б) 5-(4,6-Диметоксипиримидин-2-илтио)-1,2-диметил-4-нитро-1H-имидазол
К раствору 4,6-диметокси-2-меркаптопиримидина (3.0 г) в водном растворе гидроксида натрия (0.7 г в 100 мл воды) по каплям добавляют раствор 1,2-диметил-5-бром-4-нитро-1H-имидазола (3.9 г) в этаноле (50 мл) и смесь перемешивают при комнатной температуре в течение 6 ч. Выделившийся осадок отфильтровывают, промывают водой, сушат и перекристаллизовывают из ацетонитрила. Получают 3.1 г требуемого продукта, т.пл. 228-230°C.
(в) 2,2,2-Трифтор-N-[5-(4,6-диметоксипиримидин-2-илтио)-1,2-диметил-1Н-имидазол-4-ил]ацетамид
Смесь продукта с предыдущей стадии (7.0 г), трифторуксусной кислоты (130 мл), трифторуксусного ангидрида (18 мл) и железного порошка (5.0 г) нагревают при перемешивании до 70°C и выдерживают при этой температуре в течение 8 ч. Смесь фильтруют, фильтрат выливают на воду со льдом, подщелачивают 5 н. раствором гидроксида натрия и экстрагируют этилацетатом. Объединенные экстракты сушат сульфатом магния, растворитель упаривают, остаток очищают хроматографированием (элюент петролейный эфир 60-80° - этилацетат, 8:2), получают 5.0 г требуемого продукта, т.пл. 160-162°C.
(г) 5-(4,6-диметоксипиримидин-2-илтио)-1,2-диметил-1Н-имидазол-4-амин
К раствору продукта с предыдущей стадии (5.4 г) в метаноле (200 мл) добавляют карбонат калия (1.5 г) и реакционную смесь кипятят в течение 6 ч. Смесь фильтруют, фильтрат упаривают, остаток перекристаллизовывают из ацетонитрила, получают 2.6 г требуемого продукта.
(д) 1-Циано-N-[5-(4,6-диметоксипиримидин-2-илтио)-1,2-диметил-1Н-имидазол-4-ил]метансульфонамид
К раствору продукта с предыдущей стадии (1.0 г) в метиленхлориде (10 мл) добавляют пиридин (0.3 г), охлаждают до -45°C и в одну порцию добавляют цианометилсульфонилхлорид (0.5 г). Смесь перемешивают при -45°C в течение 30 мин, дают нагреться до комнатной температуры и перемешивают в течение ночи при комнатной температуре. Затем смесь выливают в воду, экстрагируют этилацетатом и очищают хроматографированием (элюент петролейный эфир 60-80° - этилацетат, 8:2), получают 0.7 г требуемого продукта, т.пл. 223-225°C.
ПРИМЕР Б6
1-Циано-N-[2-(4,6-димитоксипиримидин-2-илтио)-3-тиенил]-метансульфонамид
(а) 4,6-Диметокси-2-(3-нитро-2-тиенилтио)пиримидин
К раствору гидроксида натрия (1.2 г) в воде (50 мл) добавляют 4,6-диметокси-2-меркаптопиримидин (5.3 г) и смесь перемешивают при комнатной температуре в течение 15 мин. К смеси добавляют раствор 2-хлор-3-нитротиофена (5.0 г) в этаноле (50 мл), перемешивают при комнатной температуре в течение 6 часов, выпавший осадок отфильтровывают, промывают водой, сушат, получают 7.6 г требуемого продукта, т.пл. 199-201°C.
(б) N-[2-(4,6-Диметоксипиримидин-2-илтио)-3-тиенил]-2,2,2-трифторацетамид
Смесь продукта с предыдущей стадии (2.0 г), трифторуксусной кислоты (50 мл), трифторуксусного ангидрида (5.0 мл) и железного порошка (1.8 г) нагревают при перемешивании до 70°C и выдерживают при этой температуре в течение 8 ч. Смесь фильтруют, фильтрат выливают в воду со льдом, подщелачивают 5 н. раствором гидроксида натрия, экстрагируют этилацетатом, сушат сульфатом магния и упаривают до небольшого объема. Продукт кристаллизуется, давая 1.2 г требуемого продукта, т.пл. 88-90°C.
(в) 2-(4,6-Диметоксипиримидин-2-илтио)тиофен-3-амин
К раствору продукта с предыдущей стадии (2.2 г) в метаноле (30 мл) добавляют карбонат калия (1.0 г), реакционную смесь нагревают при перемешивании до 40°С и выдерживают при этой температуре в течение 6 ч. Смесь охлаждают, фильтруют, фильтрат упаривают, остаток очищают хроматографированием (элюент петролейный эфир 60-80° - этилацетат, 8:2), получают 1.0 г требуемого продукта в виде оранжевого масла.
(г) 1-Циано-N-[2-(4,6-диметоксипиримидин-2-илтио)-3-тиенил]метансульфонамид
Раствор продукта с предыдущей стадии (1.2 г) и пиридина (1.0 мл) в метиленхлориде (10 мл) охлаждают до -78°C и при перемешивании по каплям добавляют раствор цианометилсульфонилхлорида (0.6 г) в метиленхлориде (5 мл), поддерживая температуру в интервале от -78 до -60°С. Смесь перемешивают при -78°С в течение 15 мин, дают нагреться до комнатной температуры и перемешивают в течение 16 ч. Затем смесь выливают в воду и экстрагируют метиленхлоридом. Объединенные экстракты сушат сульфатом магния, растворитель упаривают. Твердый остаток очищают хроматографированием (элюент петролейный эфир 60 - 80° - этилацетат, 8:2), получают 0.4 г требуемого продукта, т.пл. 118-120°C.
ПРИМЕР Б7
N-[2-(4,6-Диметоксипиримидин-2-илтио)-3-тиенил]-1,1,1-трифторметансульфонамид
Раствор продукта со стадии (в) Примера Б6 (1.0 г) и пиридина (0.6 мл) в метиленхлориде (25 мл) охлаждают до -78°C и при перемешивании по каплям добавляют раствор трифторметансульфонового ангидрида (1.1 г) в метиленхлориде (5 мл), поддерживая температуру в интервале от -78 до -60°C. Смесь перемешивают при -78°С в течение 15 мин, дают нагреться до комнатной температуры и перемешивают в течение ночи при комнатной температуре. Затем смесь выливают в воду, экстрагируют метиленхлоридом. Объединенные экстракты сушат сульфатом магния, растворитель упаривают. Твердый остаток очищают хроматографированием (элюент петролейный эфир 60-80° - этилацетат, 8:2), получают требуемый продукт (Б7а), т.пл. 103-104°C, а также соответствующее соединение, где заместитель R2 представляет собой -SO2CF3 (R7б), т.пл. 136-138°С.
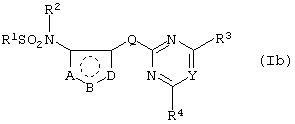
ПРИМЕР Б8
Описанными выше методами могут быть получены следующие соединения формулы 16, где заместитель R2 представляет собой атом водорода; каждый из заместителей R3 и R4 представляет собой метоксигруппу, а заместитель Q представляет собой -CH2-:
ПРИМЕР гербицидной активности А (довсходовой)
Семена испытуемых видов, которые перечислены ниже, высевают в чашки площадью 8.5 см2, наполненные стерильным суглинком до уровня 2 см от верха, и покрывают слоем суглинка в 2-5 мм. Чашки поливают и затем обрабатывают путем нанесения на поверхность почвы указанных ниже соединений Примеров, составленных в виде раствор/суспензия в смеси ацетона и раствора полиоксиэтилированного (20 молями) монолаурата (смачиватель, 10 г/л) в объемном отношении 3:1. Концентрацию каждого испытываемого соединения и объем применения рассчитывают так, чтобы получить желаемую норму расхода соединения в 200 л/га.
После 3-4 недель выращивания в теплице (минимальная температура 16°C для видов, приспособленных к умеренному климату, 21°C для видов, неприспособленных к умеренному климату, при продолжительности фотопериода 16 ч) растения оценивают визуально для выявления любого гербицидного эффекта. Все различия по сравнению с необработанным контролем оценивают по балльной шкале, в соответствии с которой:
0=нет эффекта,
1=1-24% эффекта,
2=25-69% эффекта,
3=70-89% эффекта и
4=90-100% эффекта.
Для обозначения видов растений в приведенной ниже таблице используются следующие буквенные обозначения:
а - Triticum aestivum (пшеница)
б - Hordeum vulgare (ячмень)
в - Beta vulgaris (сахарная свекла)
г - Brassica napus (рапс)
д - Alopecurus myosuroides (лисохвост мышехвостиковидный)
е - Avena fatua (овсюг)
ж - Elymus repens (пырей)
з - Bromus sterilis (костер бесплодный)
и - Viola arvensis (фиалка полевая)
к - Stellaria media (звездчатка)
л - Galium aparine (подмаренник цепкий)
м - Matricaria inodora (ромашка непахучая)
н - Polygonum lapathifolium (горец бледный)
о - Veronica persicae (вероника персидская)
Полученные результаты представлены ниже:
ПРИМЕР гербицидной активности А (послевсходовой)
Перечисленные ниже растения выращивают в теплице (минимальная температура 16°С для видов, приспособленных к умеренному климату, 21°С для видов, неприспособленных к умеренному климату, при продолжительности фотопериода 16 ч) в чашках площадью 8,5 см2, содержащих стерильный суглинок, а затем обрабатывают в камере для опрыскивания на стадии 3-4 листьев соединениями перечисленных ниже Примеров, сформированных в виде раствор/суспензия в смеси ацетона и раствора полиоксиэтилированного, (20 молями) монолаурата (смачиватель, 10 г/л) в объемном отношении 3:1. Концентрацию каждого испытываемого соединения и объем применения рассчитывают так, чтобы получить желаемую норму расхода соединения в 200 л/га.
После 3-4 недель выращивания в теплице растения оценивают визуально для выявления любого гербицидного эффекта. Все различия по сравнению с необработанным контролем оценивают по балльной шкале, в соответствии с которой:
0=нет эффекта,
1=1-24% эффекта,
2=25-69% эффекта,
3=70-89% эффекта и
4=90-100% эффекта.
Для обозначения видов растений в приведенной ниже таблице используются те же обозначения, что и в Примере гербицидной активности А.
Полученные результаты представлены ниже:
ДОПОЛНИТЕЛЬНЫЕ ЭКСПЕРИМЕНТАЛЬНЫЕ ДАННЫЕ
Было обнаружено, что помимо соединений, описанных в настоящей заявке, соединения, представленные в таблицах 1 и 4 ниже, также применимы в качестве гербицидов. Они входят в объем формулы изобретения и, таким образом, дополнительно подтверждают заявленный объем изобретения.
Тест 1
Соединения 1-А, 1-В, 1-С и 1-D, представленные в таблице 1 ниже, испытывают на гербицидное действие в отношении сорняков при довсходовом и послевсходовом применении в соответствии с ГЕРБИЦИДНЫМИ ПРИМЕРАМИ А и В описания. Результаты испытаний приведены в таблицах 2 и 3 ниже. Результаты доказывают, что соединения обладают ценным гербицидным действием при довсходовом и/или послевсходовом применении.
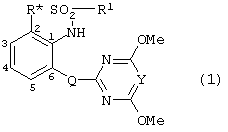
Аббревиатуры, используемые в таблицах 2 и 3:
АИ=активный ингредиент
ЕС=Echinochloa grus-galli
SE=Setaria lutescens
PH=Pharbitis purpurea
SI=Sinapis alba
CP=Chrysanthemum segetum
GA=Gallium aparine
MA=Matricaria inodora
ST=Stellaria media - = не испытывался
Все отличия от необработанного контроля оценивают в соответствии с показателем, где 0 - отсутствие эффекта, 1=1-24%, 2=25-69%, 3=70-89% и 4=90-100% действие.
Все соединения, представленные в таблице 4 выше, получают в соответствии со способами, описанными в данном изобретении. Данные соединения также испытывают на гербицидное действие при довсходовом и послевсходовом применении.
Испытанные соединения проявляют гербицидную активность с оценкой от "хорошо" до "отлично" (от 70 до 100% по сравнению с контролем) в отношении важных видов сорных растений, таких как:
Sinapis alba,
Matricaria inodora,
Chrysanthemum segetum,
Avena sativa,
Stellaria media,
Echinochloa crus-galli,
Lolium multiflorum,
Setaria spp,
Abutilon theophrasti,
Amaranthus retroflexus and
Panicum miliaceum
при довсходовом применении в дозе 0,5 кг и менее активного ингредиента на гектар.
Кроме того, испытанные соединения обладают гербицидной активностью с оценкой от "хорошо" до "отлично" в отношении важных видов сорных растений, таких как:
Sinapis alba,
Echinochloa crus-galli,
Lolium rnultrflorum,
Matricaria inodora,
Chrysanthemum segetum,
Setaria spp.,
Abutilon theophrasti,
Amaranthus retroflexus,
Panicum miliaceum and
Avena sativa
при послевсходовом применении в дозе 0,5 кг и менее активного ингредиента на гектар.
Из представленных выше дополнительных данных видно, что заявленный объем притязаний для соединений формулы (I) является достаточно обоснованным и полностью подтвержденным, и что арильные группы могут быть замещены различными заместителями без потери полезного гербицидного действия. Кроме того, заместители Х на мостике СХХ'' могут быть модифицированы в объеме пункта 1 для включения Х или X', которые представляют собой фенилтио, алкилтио, алкокси, галоген, гидрокси и т.п. их производные (или предшественники), такие как фенокси.
ДОПОЛНИТЕЛЬНЫЕ ЭКСПЕРИМЕНТАЛЬНЫЕ ДАННЫЕ
Исследовались гербициды формулы (I')

где
Соединения, представленные в таблице, получены способом, представленным в заявке.
Соединения были проверены в полевых условиях на гербицидную активность против сорняков, типичных для рисовых полей.
Условия проверки и полученные результаты.
Семена сорняков были высеяны в грунт под слоем воды толщиной 3 см. Испытуемые соединения использовали в форме стандартных композиций на водной основе. После обработки растений их содержали 28 дней в тепличных условиях. После этого сорняки были оценены путем сравнения с контролем (необработанные растения). Результаты представлены ниже.
Соединение (граммов ДВ/га)
Обозначения
EC=Echinochloa oryzicola
МО=Monoochoria vaginalis
SC=Scirpus juncoides
Эффективность соединений выражена при помощи оценочной шкалы:
0=отсутствие эффекта - 9% эффект;
1=10-29%;
2=30-49%
3=50-69%
4=70-89%;
5=90-100% эффект.
Под эффектом понимается величина разности количества сорняков при обработке и в контроле по отношению к контролю.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ПИРИМИДИНА, СПОСОБ БОРЬБЫ С СОРНЯКАМИ И ГЕРБИЦИДНЫЙ СОСТАВ | 1990 |
|
RU2041214C1 |
| СПОСОБ ПОДАВЛЕНИЯ РОСТА НЕЖЕЛАТЕЛЬНОЙ РАСТИТЕЛЬНОСТИ, ЗАМЕЩЕННЫЕ ГЕТЕРОЦИКЛАМИ ПИРИДИНЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2140739C1 |
| СОЕДИНЕНИЯ ОКСАЗОЛИДИНДИГАЛОАЦЕТАМИДА И СПОСОБ УМЕНЬШЕНИЯ ФИТОТОКСИЧЕСКОГО ДЕЙСТВИЯ ГЕРБИЦИДОВ | 1988 |
|
RU2093029C1 |
| ЭФИРЫ ТРИСКАРБАМИНОВОЙ КИСЛОТЫ, СПОСОБ УМЕНЬШЕНИЯ АБСОРБЦИИ ХОЛЕСТЕРИНА И ФАРМКОМПОЗИЦИЯ ДЛЯ ПОНИЖЕНИЯ АБСОРБЦИИ ХОЛЕСТЕРИНА | 1994 |
|
RU2130928C1 |
| ТРИЦИКЛИЧЕСКИЕ ДИАЗЕПИНОВЫЕ АНТАГОНИСТЫ ВАЗОПРЕССИНА И АНТАГОНИСТЫ ОКСИТОЦИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ | 1994 |
|
RU2126006C1 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ПИРАЗОЛА, ПРОМЕЖУТОЧНЫЕ ДЛЯ ИХ ПОЛУЧЕНИЯ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С СОРНЯКАМИ | 1993 |
|
RU2137771C1 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛА, СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ | 1991 |
|
RU2137761C1 |
| ПРОИЗВОДНЫЕ ПИРИМИДИН- И ТРИАЗИНКАРБОНОВЫХ КИСЛОТ ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 1995 |
|
RU2163808C2 |
| Способ получения сульфоанилидов или их солей с основаниями | 1989 |
|
SU1750428A3 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛА И СОДЕРЖАЩИЕ ИХ ГЕРБИЦИДЫ | 1994 |
|
RU2154063C2 |
Изобретение относится к новым сульфонамидам формулы:
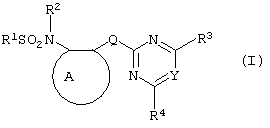
и их соли, где А представляет собой замещенное или незамещенное бензольное кольцо или 5-членное или 6-членное замещенное или незамещенное гетероароматическое кольцо, выбранное из группы, включающей тиенил, пиразолил, имидазолил, пиридил, где необязательные заместители выбраны из группы, состоящей из галогена, незамещенного или замещенного С1-С4алкила, незамещенного или замещенного С1-С4алкокси, нитро, фенила, фенокси, бензоила и С1-С4алкилкарбоксилата, когда любой алкильный фрагмент в последних указанных заместителях замещен одним или несколькими атомами галогена, С1-С4алкоксигруппами, циано, и фенилом; Q представляет собой -О-, -S- или группу формулы -СХХ'; Х и X', которые могут быть одинаковыми или разными, представляют собой каждый водород, галоген, циано, алкил, содержащий 1-8 атомов углерода, или группу -ORa, -SRa или один из Х и X' представляет собой гидрокси, а другой принимает значения, определенные выше; Ra означает С1-С8алкил; фенил; Rb означает С1-С8алкил, фенил; Y означает азот или группу CR9; R1 означает С1-С8алкил, незамещенный или замещенный галогеном, цианогруппой, фенилом или С1-С4алкоксикарбониламиногруппой, или представляет собой фенил; R2 означает Н, С1-С4алкил; R3 и R4, которые могут быть одинаковыми или разными, представляют собой каждый С1-С4алкил, С1-С4алкоксигруппу, галоген; R9 означает Н; при условии, что когда Q представляет собой О или -S-, кольцо А представляет собой 5-членное замещенное или незамещенное гетероароматическое кольцо, как определено выше. Соединения формулы I обладают гербицидной активностью, что позволяет использовать их для уничтожения сорняков. Описан способ получения соединения I. 4 н. и 5 з.п. ф-лы, 4 табл.
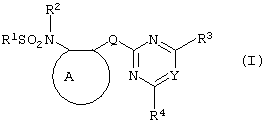
и их соли, где
А представляет собой замещенное или незамещенное бензольное кольцо или 5-членное или 6-членное замещенное или незамещенное гетероароматическое кольцо, выбранное из группы, включающей тиенил, пиразолил, имидазолил, пиридил, где необязательные заместители выбраны из группы, состоящей из галогена, незамещенного или замещенного алкила, содержащего 1-4 атомов углерода, незамещенного или замещенного алкокси, содержащего 1-4 атомов углерода, нитро, фенила, фенокси, бензоила и алкилкарбоксилата, содержащего 1-4 атомов углерода в алкильном фрагменте, когда любой алкильный фрагмент в последних указанных заместителях замещен одним или несколькими атомами галогена, алкоксигруппами, содержащими 1-4 атомов углерода, циано и фенилом;
Q представляет собой -О-, -S- или группу формулы -СХХ';
Х и X', которые могут быть одинаковыми или разными, представляют собой каждый водород, галоген, циано, алкил, содержащий 1-8 атомов углерода, или группу -ORa, -SRa или один из Х и X' представляет собой гидрокси, а другой принимает значения, определенные выше;
Ra представляет собой алкил, содержащий 1-8 атомов углерода, или фенил;
Rb представляет собой алкил, содержащий 1-8 атомов углерода, или фенил;
Y представляет собой азот или группу CR9;
R1 представляет собой алкил, содержащий 1-8 атомов углерода, незамещенный или замещенный галогеном, цианогруппой, фенилом или алкоксикарбониламиногруппой, содержащей 1-4 атомов углерода в алкильном фрагменте, или представляет собой фенил;
R2 представляет собой водород или алкил, содержащий 1-4 атомов углерода;
R3 и R4, которые могут быть одинаковыми или разными, представляют собой каждый алкил, содержащий 1-4 атомов углерода, алкоксигруппу, содержащую 1-4 атомов углерода, или галоген;
R9 представляет собой водород,
при условии, что когда Q представляет собой О или -S-, кольцо А представляет собой 5-членное замещенное или незамещенное гетероароматическое кольцо, как определено выше.
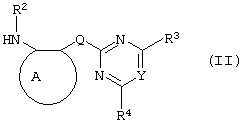
где значения A, R1, R2, Q, n, R3, R4, Y приведены выше, с сульфоновым ангидридом формулы (R1SO2)2O или сульфонилгалогенидом формулы R1SO2Hal, где Hal представляет галоген.
| Огнетушитель | 0 |
|
SU91A1 |
| иСеОСНЭЗНАЯ ;:-и^:;Т>&:о-Т1:ХШ1'1ЕСКДВ;:;:;'i&/.;''^-' ' tii't''^ | 0 |
|
SU363040A1 |
| Способ получения триазолсульфонамидов | 1987 |
|
SU1644719A3 |
Авторы
Даты
2005-12-27—Публикация
1992-11-02—Подача