Изобретение относится к области медицины, в частности к фармакологии, а именно к фармацевтическим композициям для лечения рассеянного склероза, других нейродегенеративных заболеваний, а также синдрома хронической усталости.
Рассеянный склероз - демиелинизирующее заболевание центральной нервной системы неизвестной этиологии. Рассеянный склероз характеризуется диссеминированной демиелинизацией аксонов мозга в перивентрикулярных областях и в corpus callosum. В патогенезе рассеянного склероза ведущую роль играет аутоиммунное воспаление, проявляющееся в деструкции миелина по типу гиперчувствительности замедленного типа, механизм которой опосредован Th1 лимфоцитами.
Появление очагов демиелинизации в стволовых структурах головного мозга и вертебро-базилярная недостаточность являются причиной вестибулярных нарушений при рассеянном склерозе, возникающих в результате ухудшения реологических свойств крови, спазма сосудов мелкого и среднего калибра. Нарушения вестибулярной функции в виде перманентных или пароксизмальных расстройств являются почти обязательными для рассеянного склероза. Вестибулярная дисфункция проявляется обычно симптомами раздражения - ощущение головокружения, спонтанный нистагм, нарушение вестибуло-спинальных рефлексов, спинальных функций и других.
Изменения психической сферы имеют различные клинические проявления: астенический синдром, истероформные реакции, обсессивные нарушения, состояния депрессии и эйфории, своеобразное органическое слабоумие. Депрессия встречается у 20-30% больных, причем у 2-3% возникают суицидальные попытки. Риск самоубийств у больных рассеянным склерозом достоверно выше, чем в популяции в целом.
Этиотропной терапии рассеянного склероза в настоящее время не существует. Комплексная симптоматическая терапия заболевания направлена на предупреждение деструкции мозговой ткани и подавление аутоиммунного воспаления. Терапия включает кортикостероиды, адренокортикотропный гормон (АКТГ), интерфероны, глатирамера ацетат, в острой стадии заболевания назначают иммуносупрессивную терапию цитостатиками.
Однако существующая схема комплексной терапии рассеянного склероза имеет существенные недостатки. Применяемые медикаментозные и физические методы терапии не позволяют существенно уменьшить выраженность неврологических проявлений, скорость их нарастания или существенно увеличить длительность ремиссий. С помощью указанных препаратов невозможно достигнуть репарации дефектов, связанных с деструкцией миелина в оболочках аксонов, и, следовательно, выздоровления больного.
Во-вторых, не удается также улучшить состояние больных и остановить утрату памяти, внимания и адекватного мышления, также как купировать пирамидную симптоматику: головокружения, потерю зрения и другие нарушения. Кроме того, используемые препараты не устраняют аутоиммунный компонент в патогенезе рассеянного склероза и, таким образом, не способны разорвать порочный круг прогрессирования болезни.
Вместе с тем, кортикостероидная терапия в возрастающих дозах дает целый ряд побочных эффектов, проявляющихся в развитии синдрома Иценко-Кушинга, гипертонии, обострении язвенной болезни, гипертрихозе и других эффектах, а иммуносупрессивная терапия существенно повышает риск развития инфекционных заболеваний.
Известно, что синдром хронической усталости, который в настоящее время рассматривается как самостоятельное заболевание, часто встречается при рассеянном склерозе. Обычно это синдром проявляется в виде неспособности к длительному или повторному выполнению обычных, повседневных для больного, действий и потребностью в частом отдыхе. Усталость затрагивает не только физическую, но и умственную работоспособность. Хроническая усталость существенно влияет на качество жизни больных и даже на ранних стадиях заболевания ограничивает их способность к профессиональной деятельности. Считается, что в развитии этого синдрома принимает участие и иммунная система, что проявляется, в частности, в повышении содержания провоспалительных цитокинов в сыворотке крови больных.
Специфического лечения синдрома хронической усталости не существует. Вместе с тем предлагается достаточное количество средств и методов лечения, включающих применение голодания, специальных диет, витаминотерапии, фитотерапии, нутрицевтиков и биологически активных добавок (БАД), адаптогенов, антидепрессантов, некоторых транквилизаторов, ноотропных средств, энтеросорбентов и других средств.
Однако все указанные методы и средства лечения синдрома хронической усталости являются симптоматическими и не учитывают в полной мере патогенетические особенности развития и течения заболевания.
Известно применение лекарственных средств на основе производных бензимидазола для повышения психической и физической работоспособности лиц, в профессиональной деятельности связанных с повышенными физическими нагрузками, при астенических состояниях; в комплексной терапии черепно-мозговых травм, при нарушениях мозгового кровообращения.
Известно применение 2-этил-меркаптобензимидазола бромида в качестве психотропного средства, обладающего актопротекторным психоэнергизирующим и антигипоксическим действием (RU, 1251374, A1).
Известно также применение в фармацевтических композициях производных 2-этилтиобензимидазола гидробромида и гидрохлорида, проявляющих слабую транквилизирующую активность (RU, 2061686, С1).
Известно лекарственное средство, относящееся к группе актопротекторов, оказывающих умеренное психостимулирующее действие, в котором активным ингредиентом является 2-этил-меркаптобензимидазола гидробромид, применяемое для лечения системной красной волчанки (RU, 2157684, С2). Это соединение, обладающее антигипоксической активностью, используют при пограничных психиатрических расстройствах, когда показана стимуляция психических и физических функций.
Известно применение 2-этил-меркаптобензимидазола бромида при лечении больных первичным биллиарным циррозом в качестве иммуномодулирующего средства, действующего на клеточное звено иммунитета и способствующего повышению эффективности других, применяемых в комплексной терапии циррозов, препаратов направленного действия (RU, 2188012, С2).
Известно применение актопротекторов, содержащих в качестве активного ингредиента производное 2-этилтиобензимидазола гидробромида моногидрата, для лечения миодистрофии Дюшенна - Беккера (RU, 2173144, С2). При этом отмечено, что указанное производное вследствие структурного сходства с пуриновыми основаниями аденином и гуанином усиливает синтез митохондриальных ферментов, повышая энергетический потенциал мышечной ткани и стимулируя окислительно-восстановительные процессы. Увеличение энергетического потенциала мышечной ткани способствует активации синтеза белков и ферментов, что приводит к снижению проницаемости мембран миоцитов, способствует регенерации мышц, замедлению миодистрофического процесса.
Известно применение лекарственного средства, содержащего 2-этилтиобензимидазола гидробромид моногидрат, в качестве средства, повышающего устойчивость организма к гипоксии и восстанавливающего работоспособность при выполнении тяжелых физических нагрузок и при воздействии неблагоприятных факторов, а также для устранения полипрагмазии, для профилактики профессиональной тугоухости (RU, 2017483, С1), профилактики острых приступов глаукомы при геомагнитных бурях (RU, 2019161, C1).
Известно применение 2-этилтиобензимидазола гидробромида для лечения гипоталамо-гипофизарной недостаточности у женщин (RU, 2138263, C1) с использованием эффекта повышения устойчивости мозга к асфиксии и циркуляторной гипоксии, что проявляется выраженным увеличением мозгового кровообращения, улучшением кислородного снабжения мозга, а также эффектом торможения деградации энергетических функций митохондрий нейроглиальных клеток.
Усиление образования митохондриальных ферментов и структурных белков митохондрий обеспечивает увеличение энергопродукции и поддержание высокой степени сопряженности окисления с фосфорилированием.
Поддержание высокого уровня синтеза АТФ при дефиците кислорода способствует выраженной антигипоксической и противоишемической активности производных бензимидазола, при этом фармацевтические композиции на основе этих соединений усиливают синтез антиоксидантных ферментов и обладают выраженным антиоксидантным действием.
Цель изобретения состоит в разработке лекарственного средства и способа лечения рассеянного склероза, других нейродегенеративных заболеваний и синдрома хронической усталости.
При создании изобретения ставилась задача поиска лекарственного средства, способного оказывать сочетанное психотропное и иммунотропное действие и тем самым существенно снижать патологические эффекты, связанные с нейродегенеративными последствиями деструкции миелина при рассеянном склерозе, патологические эффекты при других нейродегенеративных заболеваниях и синдроме хронической усталости.
Анализ вышеуказанных данных выявил общие признаки в эффективности действия на центральную нервную и иммунную системы лекарственных средств на основе производных бензимидазола.
Поставленная задача была решена разработкой фармацевтической композиции, содержащей в качестве активного ингредиента производные бензимидазола, которые оказывают выраженное психостимулирующее и иммуномодулирующее действие, а также разработкой способов лечения указанных заболеваний.
Исследования биологической активности производных бензимидазола, подтверждающие эффективность препарата для лечения рассеянного склероза, других нейродегенеративных заболеваний и синдрома хронической усталости, были выполнены с применением 2-этилтиобензимидазола гидробромида на приведенных далее экспериментальных моделях.
Пример 1. Влияние производных бензимидазола на нейрохимические показатели нейродегенерации у крыс, вызванной нейротоксином МФТП (1-метил-4-фенил-1,2,3,6-тетрагидропиридин).
В качестве экспериментальной модели нейродегенеративной патологии, вызывающей стойкие нарушения специфических нейронов, активацию перекисного окисления липидов мембран, блокаду мембранного транспорта и внутриклеточного метаболизма нейромедиаторов использовали нейротоксин МФТП (Schneider&Kovelowski, 1990). Эксперименты проводили на взрослых самцах крыс линии Вистар.
Данный токсин вводили крысам внутрибрюшинно дважды в сутки в дозе 20 мг/кг, затем животных декапитировали, извлекали из мозга стриатум и изучали секреторную способность этой мозговой структуры, обеспечивающую когнитивную и двигательную деятельность, в условиях ex vivo перфузии фрагментов мозга по известной методике (Kereczen et al., 1984; Будыгин и соавт., 1996). Группе подопытных животных с моделированной нейродегенеративной патологией также вводили 2-этилтиобензимидазола гидробромид (далее ЭБИГ) в дозе 50 мг/кг внутрибюшинно.
В качестве исследуемых параметров были использованы количественное содержание нейромедиатора дофамина и его метаболита - диоксифенилуксусной кислоты (далее ДОФУК) в изолированных фрагментах полосатого тела мозга крыс. Результаты испытаний представлены в табл. 1.
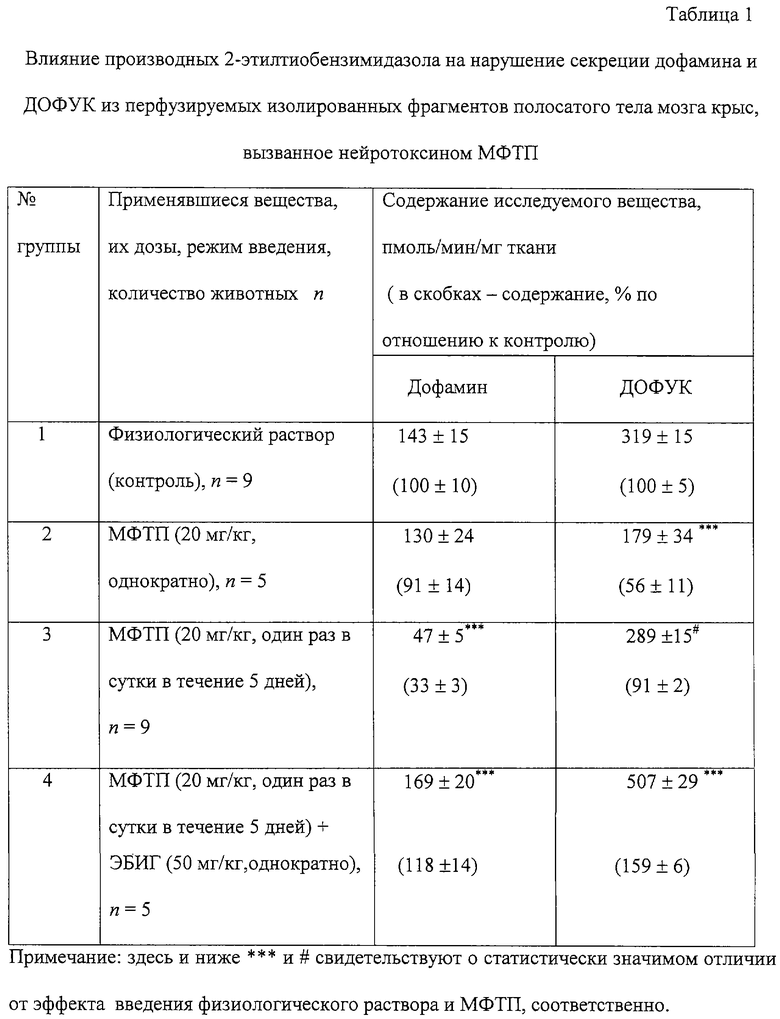
Из результатов, приведенных в табл.1, видно, что однократная инъекция нейротоксина МФТП (группа 2) подавляет метаболизм нейромедиатора дофамина, что сопровождается уменьшением концентрации ДОФУК на 44% по сравнению с контролем. Введение нейротоксина МФТП в течение 5 дней (группа 3) вызывало снижение секреции нейромедиатора дофамина до 33% по сравнению с контролем. Введение 2-этилтиобензимидазола гидробромида в дозе 50 мг/кг (группа 4) восстанавливает исходную секрецию дофамина до 118%, что свидетельствует о его способности компенсировать указанные последствия нейротоксического повреждения мозга.
Пример 2. Влияние производных бензимидазола на поведенческие симптомы нейродегенерации, вызванной у крыс нейротоксином МФТП.
Известно, что деструктивное влияние нейротоксина МФТП на секреторные процессы стриатума мозга на уровне целостного организма проявляется в виде симптомов олигокинезии, тремора и мышечной ригидности. Изменение этих показателей изучали в экспериментах на крысах линии Вистар, которым вводили нейротоксин МФТП (20 мг/кг) или нейротоксин МФТП (20 мг/кг) в сочетании с 2-этилтиобензимидазола гидробромидом (50 мг/кг), как это описано в примере 1.
В качестве исследуемых параметров были приняты выраженность олигокинезии, которая оценивалась по уровню их двигательной активности в тесте открытого поля и ригидности мышц, которую оценивали в условных единицах по известной методике (Воронина и соавт., 2000). Результаты исследований представлены в табл. 2.
(через 1 ч)
(через 3 ч)
Как можно видеть из табл. 2, введение в течение 5 дней токсина приводит к уменьшению двигательной активности животных в 10 раз и увеличению мышечной ригидности в 3 раза. Однократная инъекция 2-этилтиобензимидазола гидробромида в дозе 50 мг/кг уже через 1 час обеспечивает частичное восстановление подвижности и полное исчезновение мышечной ригидности, что свидетельствует о его способности компенсировать поведенческие симптомы нейротоксического повреждения мозга.
Пример 3. Влияние производных бензимидазола на симптомы нарушения внимания и ориентации в пространстве у мышей, вызванные возбуждающей аминокислотой l-глутаматом в нейротоксической концентрации.
В качестве экспериментальной модели нарушений внимания и ориентации в пространстве, являющихся следствием нейродегенеративных процессов, использовали тест исследовательского поведения животных в крестообразном лабиринте (метод описан Салимов, 1988; Салимов и соавт., 1995; Salimov et al., 1995). Исследования были проведены на взрослых самцах мышей линии C57BL.
В качестве повреждающего фактора использовали билатеральную аппликацию на фронтальную кору мышей (координаты: F - 2.0, L - 1.4, Н - 0.6) 5 μl 1,0 mM раствора l-глутамата. Известно, что в этой концентрации l-глутамат обладает нейротоксическим действием (Finkbeiner, Stevens, 1988; Crabbe, Dorsa, 1989; Meldrum, Garthwaite, 1990) и в течение 1-2 часов вызывает локальную гибель около 95% глутамат-чувствительных нейронов в области аппликации, восстановление которых не происходит, по крайней мере, в течение последующего месяца. Тестирование проводили через неделю после аппликации. 2-этилтиобензимидазола гидробромид вводили внутрибрюшинно в дозе 50 мг/кг за 30 минут до тестирования. Результаты испытаний приведены в табл.3.
Из табл. 3 видно, что нейротоксическая аппликация l-глутамата вызывала выраженные нарушения внимания и ориентации в пространстве, что проявлялось в виде увеличения числа переходов до первого полного обхода лабиринта. Аппликация l-глутамата вызывала также замедление исследовательской активности мышей, что проявлялось в виде увеличения продолжительности обследования лабиринта до критерия 12 переходов. Однократная инъекция 2-этилтиобензимидазола гидробромида в дозе 50 мг/кг полностью устраняла указанные поведенческие проявления нейротоксического действия l-глутамата.
Пример 4. Влияние производных бензимидазола на симптомы хронической усталости у мышей, вызванные субхроническим введением нейролептика галоперидола.
В качестве экспериментальной модели синдрома хронической усталости использовали оценку времени сложной сенсомоторной (исследовательской) активности у мышей, получавших субхронический курс нейролептика галоперидола.
Как показывают измерения связывания меченых агонистов дофаминовых рецепторов, ежедневное введение галоперидола в течение 2-3 недель в дозах выше 0,5 мг/кг приводит к увеличению числа D2 рецепторов дофамина в стриатуме (Joseph et al., 1983; Fleminger et al., 1983; Hitri et al., 1978) и в прилежащем ядре (Seeger et al., 1982; Wolffgramm et al., 1990; Hitri et al., 1978), наблюдаемому в течение не менее 7 дней после отмены галоперидола. При этом наблюдаются хронические затруднения сложной сенсомоторной (исследовательской) активности (Salimov et al., 2000).
Исследования были проведены на взрослых самцах мышей линии C57BL. Галоперидол в дозе 1 мг/кг вводили внутрибрюшинно один раз в сутки в течение 12 дней. Исследовали сенсомоторную активность мышей в крестообразном лабиринте по известному методу (Салимов, 1988; Салимов и соавт., 1995; Salimov et al., 1995) через сутки после окончания субхронического введения нейролептика галоперидола. 2-этилтиобензимидазола гидробромид (ЭБИГ) вводили внутрибрюшинно в дозе 50 мг/кг за 30 мин до теста. Результаты испытаний приведены в табл.4.
Из таблицы 4 видно, что введение нейролептика галоперидола вызывает хроническое затруднение (замедление) исследовательской активности, что проявлялось в виде увеличения времени, которое требовалось животным, чтобы совершить 12 переходов из рукава в рукав лабиринта. Однократное введение 2-этилтиобензимидазола гидробромида, выполненное через сутки после последней инъекции галоперидола, полностью устраняло указанные симптомы затруднения исследовательской активности.
Фармацевтическая композиция согласно изобретению, содержащая в качестве биологически активного ингредиента производное бензимидазола, была применена в клинических условиях при лечении 10 больных с рассеянным склерозом и 10 больных, страдающих синдромом хронической усталости.
Пример 5. Использование 2-этилтиобензимидазола гидробромида для лечения рассеянного склероза.
Фармацевтическая композиция согласно изобретению, содержащая в качестве биологически активного ингредиента производное бензимидазола, например 2-этилтиобензимидазола гидробромид, может быть применена, согласно изобретению, для профилактики и лечения рассеянного склероза и других нейродегенеративных заболеваний в суточной дозе 500-1500 мг курсом продолжительностью 20-25 дней с возможностью повторения курса лечения через двухнедельный интервал.
Предложенный способ лечения использовался в терапии рассеянного склероза у 10 больных с различными клиническими формами заболевания. В качестве примера эффективности и безопасности терапии рассеянного склероза 2-этилтиобензимидазолом гидробромидом приводим выписку из истории болезни.
Больная П. 47 лет (история болезни №201/46). Диагноз: Рассеянный склероз, цереброспинальная форма, рецидивирующе-реммитирующая форма. 2 степень тяжести.
Заболела в 1990 году, когда появилась резкая слабость в ногах, онемение ухудшение зрения. Через три месяца функции полностью восстановились. В 1997 году после физической нагрузки появилась слабость в руках, нарушилась координация движений, ухудшилось зрение. Лечилась пирацетамом, пентоксифиллином, поливитаминами, симптоматика медленно регрессировала. Последняя экзацербация с мая 2003.
При исследовании нервной системы: коленные и ахилловы рефлексы выше справа, гиперстезия с уровня D9 по проводниковому типу, нарушена глубокая чувствительность нижних конечностей, симптом Барре с обеих нижних конечностей, брюшные рефлексы отсутствуют, инкоординация при выполнении ПНП, неустойчивость в позе Ромберга, положительный симптом Нери, ограничение объема активных движений в шейном и поясничном отделах позвоночника, преимущественно ротационных и латерофлексионных.
При поступлении: анализ крови - Hb - 126 г/л, Эр 4,4 1012 л-1, цветной показатель - 0,87; L - 7,5·10 л, из них: эозинофилы - 1%, базофилы - нет, юные формы - нет, палочкоядерные - 2%, сегментоядерные - 74%, лимфоциты - 16%, моноциты - 7%, СОЭ - 9,0 мм/час. Уровень глюкозы - 5,17 ммоль/л, креатинин - 71,5 ммоль/л, креатин - 20,5 мкмоль/л.
Исследование мочи: цвет - желтый; прозрачность - неполная; реакция - кислая; белок - нет; глюкоза - нет; цилиндры и эпителий почек - отсутствуют; эритроциты - нет; лейкоциты 0-1 в поле зрения; плоский эпителий - 0-1 в поле зрения; бактерии в большом количестве.
ЭКГ: ЧСС - 70 в мин, синусовый ритм, блокада левой передней ветви пучка Гиса, признаки гипертрофии левого желудочка.
ЭхоКГ: умеренно выраженный склероз аорты, полости сердца не расширены.
МРТ головного мозга: патологические изменения отсутствуют.
Лечение: пирацетам, пентоксифиллин, витамины группы В, массаж. 2-этилтиобензимидазола гидробромид больная получала три раза в день по 250 мг внутрь. Прием препарата продолжался в течение трех недель.
На фоне проводимой терапии была достигнута клиническая и МР-томографическая ремиссия. У больной нормализовались клинические и иммунологические показатели. Объективно улучшилось психическое и физическое состояние, что характеризовалось снижением выраженности патологической симптоматики рассеянного склероза, нарастанием мышечной силы нижних конечностей, увеличением объемов физической нагрузки, улучшением координации движений. Существенно улучшилась память и скорость мыслительных процессов. Улучшилось настроение и сон. Больная выписана под наблюдение участкового невролога с рекомендацией продолжать курс лечения этилтиобензимидазолом амбулаторно.
В связи с вышеописанным механизмом действия производных бензимидазола, например 2-этилтиобензимидазола гидробромида, на центральную нервную систему и иммунную систему больных рассеянным склерозом фармацевтическая композиция согласно изобретению может применяется и для лечения других нейродегенеративных заболеваний, таких как болезнь Паркинсона, болезнь Альцгеймера, в суточной дозе 750-1500 мг курсом продолжительностью 20 дней с возможностью повторения курса лечения через двухнедельный интервал.
Пример 6. Использование 2-этилтиобензимидазола гидробромида для лечения синдрома хронической усталости.
Фармацевтическая композиция согласно изобретению, содержащая в качестве биологически активного вещества производные бензимидазола, например 2-этилтиобензимидазол, могут быть применены, согласно изобретению, для лечения синдрома хронической усталости в суточной дозе 500-1000 мг курсом в течение 15-20 дней с возможностью повторения курса лечения через двухнедельный интервал.
Клинические исследования эффективности применения фармацевтической композиции согласно изобретению, например, содержащей в качестве активного ингредиента 2-этилтиобензимидазола гидробромид, для лечения синдрома хронической усталости (СХУ) проводили в группе из 10 больных. В качестве примера эффективности лечения СХУ способом согласно изобретению приводим выписку из истории болезни.
Больная Ч. 29 лет (№2995/180) Диагноз: Синдром хронической усталости. Неврастения с синкопальными приступами.
Больна с 1993 года после психотравмирующей ситуации в жизни. Предъявляет жалобы на постоянную головную боль, общую слабость, слабость в нижних конечностях, шум в голове, быструю утомляемость, раздражительность, плаксивость, обморочные состояния.
При исследовании нервной системы установлено: глубокие рефлексы повышены, D=S, оживлены по функциональному типу, тремор пальцев верхних конечностей, инкоординация при выполнении динамических координаторных проб с двух сторон (функциональная).
При поступлении анализ крови: Hb - 130 г/л; Эр - 4,5 10 л; цветной показатель - 0,86; Rt - 8%; L - 4,4 10 л, из них Э - 6%, Б - нет, М - нет, Ю - нет, П - 6%, С - 47%, Л - 37%, М - 4%; Тр - 270. СОЭ - 7 мм/час. Свертываемость крови - 10 мин.
Глюкоза - 5,06 ммоль/л, мочевина - 6,6 ммоль/л, билирубин - 16,5 мкмоль/л, белок - 59 г/л, холестерин - 5,64 ммоль/л, ПТИ - 87%.
Анализ мочи: цвет - соломенно-желтый, прозрачность - неполная, плотность - 1010 г/л, реакция - кислая, белок - нет, глюкоза - нет, цилиндры, эпителий почек - не обнаружены. Эр - нет, Л - единичные в поле зрения.
ЭКГ - ЧСС - 77 в мин, положение электрической оси сердца нормальное, ритм синусовый.
ЭЭГ - легкие диффузные изменения биоэлектрической активности мозга.
Лечение: кавинтон, АТФ, витамины, сибазон, мезапам, 2-этилтиобензимидазола гидробромид больная получала ежедневно по 750 мг внутрь в течение 15 дней.
В результате проведенной терапии было достигнуто значительное улучшение общего состояния больной. Глубокие рефлексы нормализовались, значительно улучшилась координация, исчез тремор верхних конечностей. Частота и интенсивноть головных болей значительно снизилась. Улучшилось настроение, аппетит, жалобы на слабость не предъявляются. Пациентка выписана с рекомендацией провести повторный курс терапии 2-этилтиобензимидазолом гидробромидом через месяц амбулаторно.
Таким образом, из приведенных результатов испытаний фармацевтической композиции согласно изобретению, в частности биологической активности ее аквтивного ингредиента - производных бензимидазола, в частности 2-этилтиобензимидазола гидробромида, в отношении нарушений, вызванных рассеянным склерозом, другими нейродегенеративными заболеваниями и синдромом хронической усталости можно сделать следующее заключение.
Фармацевтическая композиция согласно изобретению является эффективным лекарственным средством для лечения рассеянного склероза, других нейродегенеративных заболеваний и синдрома хронической усталости при использовании способов лечения этих заболеваний согласно изобретению.
Применение производных бензимидазола или их фармакологически приемлемых солей в качестве активных ингредиентов фармацевтической композиции позволяет создавать фармацевтические композиции широкого спектра, в частности для неврологии и иммунопатологии. Производные бензимидазола оказывают воздействие на центральную нервную и иммунную систему теплокровных, которое в зависимости от количества активного ингредиента в лекарственном препарате, величины дозы, условий и режима дозирования может быть выбрано оптимальным.
Фармацевтическая композиция согласно изобретению может в качестве активного ингредиента содержать композицию из нескольких активных соединений, например бензимидазол и никотиновая кислота, которые хорошо совместимы и в зависимости от биологической активности могут, например, увеличивать эффективность действия лекарственного препарата в организме.
При этом фармацевтическая композиция согласно изобретению может представлять собой раствор активного ингредиента в фармацевтически приемлемом жидком носителе или растворителе, например в воде, физиологическом растворе, буферных растворах.
Кроме того, фармацевтическая композиция согласно изобретению может представлять собой тонкодисперсный порошок активного ингредиента, пригодный для применения в растворах для инъекций, аппликациях, в приготовлении других лекарственных форм.
Производные бензимидазола согласно изобретению хорошо растворимы в воде или в спирте, физиологическом растворе, буферных растворах или совместимы с ингредиентами, увеличивающими их растворимость.
Оральное введение представляет обычно предпочтительный путь для введения лекарственных средств в организм, так как этот способ является наиболее удобным и приемлемым для пациента. Фармацевтические композиции согласно изобретению могут быть выполнены в виде средств для орального введения, например таблеток, гранул, шариков, порошков, капсул, суспензий, эмульсий. При этом фармацевтическая композиция может дополнительно содержать средства повышения биодоступности, например микрокристаллическую целлюлозу, или, например, биологически активные добавки, что позволяет уменьшить содержание биологически активного ингредиента в разовой дозе лекарственного средства. Или, кроме того, может быть выполнена в виде спонтанно диспергируемого концентрата, который при смешивании с дистиллированной водой или спиртовым раствором создает водные микроэмульсии, фазовостабильные, с повышенной способностью проникновения и распространения.
Быстрое поглощение активного ингредиента фармацевтической композиции, согласно изобретению, может быть достигнуто парентеральной инъекцией, что для клинических условий является традиционным, но менее приемлемым при самолечении. В этом случае эффективным является доставка лекарственного средства в организм ректальным введением, с помощью суппозиториев, клизм, мягких желатиновых капсул, свечей, например в виде твердых дозированных форм с пригодной конфигурацией, которые либо плавятся при температуре тела, либо растворяются или диспергируются в полости, покрытой слизистой оболочкой.
Специалистам в области медицины известно, что для улучшения адсорбции биологически активных веществ, имеющих плохую растворимость в воде или в каких-либо избирательных средах, активный ингредиент фармацевтической композиции в форме высоконасыщенного раствора в твердой форме может быть инкапсулирован в одной или более пластинчатой мембране, содержащей липиды, например в липосомах, позволяющих доставлять активный ингредиент в специфическую область.
Согласно изобретению, в фармацевтической композиции производные бензимидазола и их соли могут содержаться в липосомальной форме, например в многофазной липосомной системе доставки лекарств, которая является стабильной и может быть легко разбавлена водой, в состоянии фармацевтической композиции от состояния разбавленной жидкости до состояния геля, что является важным для производных соединений, плохо растворимых в кислой среде желудочно-кишечного тракта, а также расширяет возможности применения более высоких доз активного ингредиента при введении орально.
Кроме того, в фармацевтической композиции согласно изобретению фармацевтически приемлемый носитель может представлять собой композицию, содержащую фармакологически активные добавки.
При этом, согласно изобретению, фармакологически активные добавки могут быть выбраны из группы, включающей стабилизаторы, диспергаторы, ароматизаторы, эмульгаторы, проводники, средства повышения биодоступности, одним из которых может быть средство для повышения растворимости труднорастворимых соединений, например растворитель диметилсульфоксид (ДМСО).
При многих заболеваниях целесообразно использовать различные способы местного воздействия на патологический процесс, особенно при наличии противопоказаний к системной терапии, например при нарушении функции печени или почек, а также других жизненно важных органов. Одним из способов местного воздействия является применение наружных лекарственных средств, содержащих анальгезирующие, противовоспалительные, иммуномодулирующие или антисептические лекарственные средства.
Известно, что, исходя из чувствительности кожи, вероятности ее раздражения и трансдермальной абсорбционной способности (гигрокопичности кожи), рН фармацевтического препарата для наружного применения желательно поддерживать в интервале 4-8, более предпочтительно в интервале 5-7. Когда рН слишком мала (3,0 и менее), высокая кислотность вызывает сильное раздражение кожи. Когда рН слишком велика (9,0 и более), трансдермальное всасывание активного ингредиента снижается, раздражение кожи усиливается, и лекарственный препарат окрашивается в желтый цвет. Наиболее оптимальные значения рН для трансдермальной абсорбции от 4 до 8.
Для усиления трансдермального поглощения (всасывания) активного ингредиента в фармацевтической композиции, согласно изобретению, может содержаться в эффективных количествах и так называемый усилитель поглощения, например органические основания, например триэтаноламин, кротамитон, сложные эфиры жирных кислот со средней длиной цепи, 1-ментол, бензиловый спирт и им подобные вещества. Органическое основание облегчает высвобождение активного ингредиента из основы, поскольку делает его более водорастворимым благодаря образованию солей. Органическое основание действует как регулятор рН лекарственного препарата.
Для регулирования рН лекарственного средства также могут быть использованы щелочные соединения (гидроокись калия и натрия, триэтаноламин, диизопропаноламин, моноэтаноламит и другие).
Растворы гидрохлоридов, ацетатов, фосфатов, гидробромидов, нитратов, сульфатов и других органических солей производных бензимидазола имеют рН 4-7, что создает хорошие перспективы создания лекарственных средств для наружного применения.
Фармацевтическая композиция для наружного применения может представлять собой гель-эмульсию, содержащую в качестве активного ингредиента производное, например, 2-этилтиобензимидазола гидробромида, согласно изобретению, гидрофильный полимер, маслянистое вещество, неионный поверхностно-активный агент, щелочное соединений или органическое основание в качестве регулятора рН среды и воду. При этом производные 2-этилтиобензимидазола гидробромида, согласно изобретению, химически совместимы с этими ингредиентами, не вызывают аллергических реакций и хорошо переносятся пациентами.
Литература
Воронина Т.А., Вальдман Е.А., Неробкова Л.Н. Методические указания по изучению антипаркинсонической активности фармакологических веществ. В. кн.: Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ, Москва, ЗАО "Ремедиум", 2000, 398 с.
Салимов P.M. Оценка упорядоченности пути в процессе исследовательского поведения у мышей. Журнал Высшей Нервной Деятельности им. И.П.Павлова, 1988, т.38, №3, с.569-571.
Салимов P.M., Полетаева И.И., Ковалев Г.И., Салимова Н.Б., Гайнетдинов P.P. Межлинейные различия в способности к экстраполяции и в освоении крестообразного лабиринта коррелируют с разными показателями обмена моноаминов мозга. Журнал Высшей Нервной Деятельности им. И.П. Павлова, 1995, т.45, с.914-924.
Crabbe J.C.; Dorsa D.M. Neonatal monosodium glutamate lesions alter neurosensivity to ethanol in adult mice. Pharmacology, Biochemistry and Behavior, 1986, v.24, p.1343-1351.
Finkbeiner S., Stevens C.F. Application of quantitative measurements for assessing glutamate neurotoxicity. Proceedings of the National Academy of Sciences of the United States of America, 1988, v.85, p.4071-4074.
Fleminger S., Rupniak N.M., Hall M.D., Jenner P., Marsden C.D. Changes in apomorphine-induced stereotypy as a result of subacute neuroleptic treatment correlates with increased D-2 receptors, but not with increases in D-1 receptors. Biochemical Pharmacology, 1983, v.32, p.2921-2927.
Hitri A., Weiner W.J, Borison R.L., Diamond B.I, Nausieda P.A., Klawans H.L. Dopamine binding following prolonged haloperidol pretreatment. Annals of Neurology, 1978, v.3, p.134-140.
Joseph J.A., Bartus R.T., Clody D., Morgan D., Finch C., Beer В., Sesack S. Psychomotor performance in the senescent rodent: reduction of deficits via striatal dopamine receptor up-regulation. Neurobiology of Aging, 1983, v.4, p.313-319.
Meldrum В., Garthwaite J. Excitatory amino acid neurotoxicity and neurodegenerative disease. Trends in Pharmacological Sciences, 1990, v.11, p.379-387.
Salimov R.; Salimova N.; Shvets L.; Shvets N. Effect of chronic piracetam on age-related changes of cross-maze exploration in mice. Pharmacology Biochemistry and Behavior, 52: 637-640; 1995.
Salimov R.M.; Salimova N.B.; Shvets L.N.; Maisky A.I. Haloperidol administered subchronically reduces the alcohol-deprivation effect in mice. Alcohol 20: 61-68; 2000.
Seeger T.F., Thai L., Gardner E.L. Behavioral and biochemical aspects of neuroleptic-induced dopaminergic supersensitivity: studies with chronic clozapine and haloperidol. Psychopharmacology, 1982, v.76, p.182-187.
Wolffgramm J., Rommelspacher H., Buck E. Ethanol reduces tolerance, sensitization, and up-regulation of D2-receptors after subchronic haloperidol. Pharmacology, Biochemistry and Behavior, 1990, v.36, p.907-914.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ АСТЕНИИ И/ИЛИ СИНДРОМА ХРОНИЧЕСКОЙ УСТАЛОСТИ | 2014 |
|
RU2578412C1 |
| ИНЪЕКЦИОННАЯ ЛЕКАРСТВЕННАЯ ФОРМА ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА, СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ И ПРИМЕНЕНИЕ | 2011 |
|
RU2520758C2 |
| НОВЫЕ КОМБИНАЦИИ НЕРАМЕКСАНА ДЛЯ ЛЕЧЕНИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ РАССТРОЙСТВ | 2008 |
|
RU2432161C1 |
| Адамантильные производные бензимидазола, обладающие антипаркинсонической активностью | 2023 |
|
RU2820315C1 |
| ИНГИБИТОРЫ GSK-3 | 2006 |
|
RU2449998C2 |
| НОВЫЕ 1,4-ДИАЗА-БИЦИКЛО[3.2.2]НОНИЛ-ОКСАДИАЗОЛИЛЬНЫЕ ПРОИЗВОДНЫЕ И ИХ МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2007 |
|
RU2427581C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ, ОКАЗЫВАЮЩАЯ ВЛИЯНИЕ НА ФУНКЦИОНИРОВАНИЕ ЦНС, СПОСОБ КОРРЕКЦИИ СОСТОЯНИЙ, СВЯЗАННЫХ С НАРУШЕНИЯМИ ФУНКЦИОНИРОВАНИЯ ЦНС; ФАРМАЦЕВТИЧЕСКИЙ НАБОР; СРЕДСТВО, СПОСОБСТВУЮЩЕЕ ПРОНИКНОВЕНИЮ ЧЕРЕЗ ГЕМАТОЭНЦЕФАЛИЧЕСКИЙ БАРЬЕР ЛЕКАРСТВЕННЫХ СУБСТАНЦИЙ И МЕТАБОЛИТОВ; ФАРМАЦЕВТИЧЕСКОЕ СРЕДСТВО ДЛЯ ЭНДОНАЗАЛЬНОГО ПРИМЕНЕНИЯ | 2004 |
|
RU2253461C1 |
| МЕТИЛТИОНИНИЙ, ПРЕДНАЗНАЧЕННЫЙ ДЛЯ ЛЕЧЕНИЯ СИНАПТОПАТИЙ | 2020 |
|
RU2835868C2 |
| ОДНОВРЕМЕННОЕ, РАЗДЕЛЬНОЕ ИЛИ РАЗНЕСЕННОЕ ВО ВРЕМЕНИ ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ, ПО МЕНЬШЕЙ МЕРЕ, ОДНОГО БОТУЛИЧЕСКОГО НЕЙРОТОКСИНА И, ПО МЕНЬШЕЙ МЕРЕ, ОДНОГО ОПИАТНОГО ПРОИЗВОДНОГО | 2007 |
|
RU2434637C2 |
| Пептид, обладающий нейропротекторной активностью на модели МФТП-индуцированного паркинсонизма и фармацевтическая композиция на его основе | 2017 |
|
RU2662429C1 |
Фармацевтическая композиция для лечения синдрома хронической усталости содержит в качестве биологически активного ингредиента 2-этилтиобензимидазол гидробромид в эффективном количестве и фармацевтически приемлемый жидкий носитель. Способ профилактики и лечения синдрома хронической усталости осуществляется путем введения указанной фармацевтической композиции в суточной дозе 250-1500 мг в течение 5-20 дней с возможностью повторения курса лечения после перерыва продолжительностью 5 или более дней. При лечении синдрома хронической усталости дополнительно применяют кавинтон, аденозинтрифосфат, витамины, сибазон, мезапам. Технический результат, который достигается при осуществлении настоящего изобретения, заключается в реализации указанного назначения. 2 н. и 2 з.п. ф-лы, 4 табл.
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| М.: ООО "Новая Волна", 2001, т.1, с.122 | |||
| Способ профилактики укачивания | 1982 |
|
SU1091931A1 |
| Средство для повышения иммунологической реактивности организма | 1983 |
|
SU1673118A1 |
Авторы
Даты
2006-01-10—Публикация
2003-07-15—Подача