Настоящее изобретение относится к О-арилглюкозидам, которые являются ингибиторами натрий-зависимых переносчиков глюкозы, обнаруженных в кишечнике и почках (SGLT2) и к способу лечения диабета, в частности, диабета типа II, а также гипергликемии, гиперинсулинемии, ожирения, гипертриглицеридемии, Синдрома X, осложнений при диабете, атеросклероза и родственных заболеваний с применением таких О-арилглюкозидов самостоятельно или в сочетании с одним, двумя или более антидиабетическими агентами другого типа и/или терапевтическими агентами другого типа, например гиполипидемическими агентами.
Примерно 100 миллионов человек во всем мире болеют диабетом типа II (NIDDM), который характеризуется гипергликемией вследствие избыточного продуцирования глюкозы печенью и периферической резистентности к инсулину, причины которых до сих пор не известны. Полагают, что гипергликемия является главным фактором риска для развития диабетических осложнений и непосредственно влияет на недостаточную секрецию инсулина, наблюдаемую при прогрессирующем NIDDM. Полагают, что нормализация содержания глюкозы в плазме больных NIDDM повысит эффективность действия инсулина и нейтрализует появление осложнений при диабете. Считают, что ингибитор натрий-зависимого переносчика глюкозы будет способствовать нормализации уровней глюкозы в крови и, возможно, нормализации веса тела за счет повышения экскреции глюкозы. Желательно также создать новые, безопасные и активные при пероральном применении антидиабетические агенты для пополнения существующих лекарственных средств, включающих сульфонилмочевины, тиазолидиндионы, метформин и инсулин, и избежать возможных побочных эффектов, обусловленных применением этих других агентов.
Гипергликемия является признаком диабета типа II (NIDDM); постоянный контроль уровня глюкозы в плазме при диабете может предупредить появление диабетических осложнений и бета-клеточную недостаточность, наблюдаемую при прогрессировании заболевания. Глюкоза плазмы в нормальном состоянии фильтруется в почечных клубочках и активно реабсорбируется в проксимальных канальцах. По-видимому, SGLT2 являются основньми переносчиками, ответственными за повторное всасывание глюкозы в этом месте. Специфический ингибитор SGLT флоризин или его близкие аналоги ингибируют этот процесс повторного всасывания у больных диабетом грызунов и собак, что приводит к нормализации уровня глюкозы в плазме вследствие промотирования выделения глюкозы без гипогликемических побочных эффектов. Сообщалось, что продолжительное лечение больных диабетом крыс Цукера с помощью ингибитора SGLT2 повышает реакцию инсулина на гликемию, увеличивает чувствительность инсулина и задерживает проявление нефропатии и невропатии у этих животных, при этом не наблюдается заметной патологии в почках и отсутствует дисбаланс электролитов в плазме. Полагают, что селективное ингибирование SGLT2 у больных диабетом нормализует содержание глюкозы в плазме за счет повышения выделения глюкозы с мочой, тем самым повышается чувствительность инсулина и замедляется развитие диабетических осложнений.
Девяносто процентов случаев повторного всасывания глюкозы в почках осуществляется в эпителиальных клетках в раннем S1 сегменте проксимального канальца коркового вещества почки и, по-видимому, SGLT2 является основным переносчиком, ответственным за это повторное всасывание. SGLT2 представляет собой белок, состоящий из 672 аминокислот, содержащий 14 мембраносвязывающих сегментов, который преимущественно экспрессирует в раннем S1 сегменте почечных проксимальных канальцев. Специфичность субстрата, зависимость от натрия и локализация SGLT2 согласуются со свойствами натрий-зависимого переносчика глюкозы с высоким потенциалом, низким сродством, ранее описанного в проксимальных канальцах коркового вещества почки. Кроме этого, исследования гибридного истощения показывают, что SGLT2 является основным котранспортером Na+/глюкозы в S1 сегменте проксимального канальца, так как практически вся Na-зависимая активность транспорта глюкозы, кодируемая мРНК коркового вещества почки, ингибируется антисмысловым олигонуклеотидом, специфичным в отношении SGLT2 крыс. SGLT2 является возможньм геном некоторых форм семейной глюкозурии, генетической аномалии, при которой повторная абсорбция глюкозы в почках в той или иной степени нарушена. Ни один из этих синдромов, исследованных до настоящего времени, не картирован до локуса SGLT2 на хромосоме 16. Однако исследования высокогомологичных SGLT грызунов четко указывают на SGLT2 как на главный натрий-зависимый переносчик глюкозы в почках и наводят на мысль, что локус глюкозурии, который был картирован, кодирует SGLT2 регулятор. Ингибирование SGLT2 следует прогнозировать для того, чтобы понизить уровень глюкозы в плазме путем повышения выделения глюкозы у больных диабетом.
SGLT1, другой натрий-зависимый котранспортер глюкозы, который на 60% идентичен SGLT2 на аминокислотном уровне, экспрессирует в тонкой кишке и в более дистальном сегменте S3 почечного проксимального канальца. Несмотря на сходство их последовательностей, SGLT1 человека и SGLT2 биохимически различаются. В случае SGLT1 молярное соотношение Na+ и транспортируемой глюкозы составляет 2:1, тогда как в случае в случае SGLT2 это соотношение составляет 1:1. Кm Na+ составляет 32 и 250 - 300 мМ для SGLT1 и SGLT2 соответственно. Значения Km поглощения глюкозы и неметаболизированного аналога глюкозы, α-метил-D-глюкопиранозида (AMG), сходны для SGLT1 и SGLT2, и составляют 0,8 и 1,6 мМ (глюкоза) и 0,4 и 1,6 мМ (AMG) для переносчиков SGLT1 и SGLT2 соответственно. Однако, эти два переносчика различаются по специфичности к субстрату относительно Сахаров, таких как галактоза, которая является субстратом только для SGLT1.
Применение флоризина, специфического ингибитора SGLT активности, подтвердило концепцию in vivo, так как оно стимулирует выделение глюкозы, снижает содержание глюкозы в плазме до и после еды и активизирует утилизацию глюкозы, не вызывая гипогликемических побочных эффектов при испытании на больных диабетом животных: нескольких моделях грызунов и одной модели собак. После применения флоризина в течение двух недель не наблюдалось никаких побочных эффектов ни в отношении ионного баланса в плазме, ни в отношении функции и морфологии почек. Кроме этого, никаких гипогликемических или других побочных эффектов не наблюдается, когда флоризин вводят нормальным животным, несмотря на наличие глюкозурии. Сообщалось, что введение ингибитора почечных SGLT в течение 6 месяцев (Tanabe Seiyaku) улучшает содержание глюкозы в плазме до и после еды, улучшает секрецию и утилизацию инсулина у подопытных страдающих ожирением крыс с NIDDM и нейтрализуют развитие нефропатии и невропатии при отсутствии гипогликемических или почечных побочных эффектов.
Сам флоризин представляет собой не очень хорошее пероральное лекарственное средство, так как он является неспецифическим ингибитором SGLT1/SGLT2, который гидролизуется в кишечнике до своего агликона флоретина, мощного ингибитора более легкого транспорта глюкозы. Конкурентное ингибирование активных транспортеров глюкозы (GLUT) нежелательно, так как полагают, что оно усиливает устойчивость к инсулину, атакже промотирует гипогликемию в ЦНС (CNS). Ингибирование SGLT1 может также вызывать серьезные побочные явления, как это иллюстрируется на примере наследственного синдрома малабсорбции глюкозы/галактозы (GGM), при котором мутации в котранспортере SGLT1 приводят к нарушению всасывания глюкозы в кишечнике и к смертельно опасной диарее и обезвоживанию. Биохимические различия между SGLT2 и SGLT1, а также степень дивергенции их последовательностей позволяют идентифицировать селективные ингибиторы SGLT2.
Синдром семейной глюкозурии является состоянием, при котором транспорт глюкозы в кишечнике и транспорт других ионов и аминокислот в почках нормальны. Больные семейной глюкозурией, по-видимому, нормально развиваются, у них нормальное содержание глюкозы в плазме, и, по-видимому, они не испытывают трудностей со здоровьем из-за этого нарушения, несмотря на временами высокие (110-114 г/день) уровни выделяемой глюкозы. Основные симптомы, наблюдаемые у этих больных, включают полифагию, полиурию и полидипсию, а почки, по-видимому, имеют нормальное строение и функцию. Таким образом, известные до настоящего времени факты говорят о том, что нарушение повторного поглощения глюкозы в почках, по-видимому, вызывает очень кратковременные негативные последствия у нормальных в других отношениях индивидуумов.
В следующих ссылках описаны О-арилглюкозидные ингибиторы SGLT2 для лечения диабета.
ЕР 598359 А1 (также японский патент 035988) (Tanabe Seiyaku) охватывает соединения следующей структуры А

ЕР 0850948 А1 охватывает структуры следующего типа В

В японской заявке 09188625 А структура В расширена за счет включения примеров соединений В, в которых R3 обозначает Н, а 5-членный цикл является насыщенным так же, как у аналогов бензотиофенов (О=S) и инденов (О=СН2)

Японская заявка 09124685 А расширяет структуру В с R3=Н за счет включения производных моноацилированного С6 гидроксила, в которых ацильная группа представляет собой бензойную или пиридинкарбоновую кислоту или уретан, образованный из соответствующего фенола.

Японский патент 09124684 раскрывает производные структуры В

В Европейской заявке 773226 А1 раскрываются производные структуры В
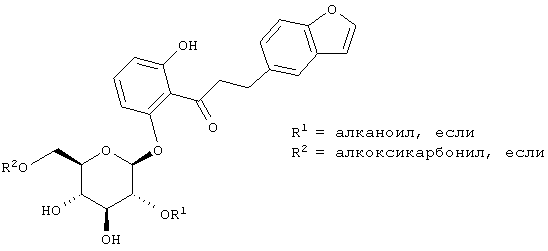
Японская заявка 08027006 А охватывает производные структуры А, в которых ацилированы различные комбинации гидроксильных групп глюкозы и, по-видимому, аналогична ЕР 598359 А1.
ЕР 684254 А1, по-видимому, охватывает производные структуры В, описанные в японской заявке 09188625 А.
Другие заявочные описания изобретения и публикации, охватывающие ингибиторы SGLT2, следующие:
К.Tsujihara, et al., Chem. Pharm. Bull.44, 1174-1180 (1996).
M.Hongu et al., Chem. Pharm. Bull.46, 22-33 (1998).
M.Hongu et al., Chem. Pharm. Bull.46, 1545-1555 (1998).
A.Oku et al., Diabetes, 48, 1794-1800 (1999).
Японский патент 10245391 (Dainippon) описывает 500 структур в качестве гипогликемических агентов для лечения диабета. Они представляют собой О-глюкозиды гидроксилированных кумаринов.
Другие ссылочные материалы, описывающие структуры О-арилглюкозидов, изображенные ниже, родственные представленным в данном описании, следующие:
1) G.К.Jain et al., Indian J. Chem., 26B, 163-166 (1989).
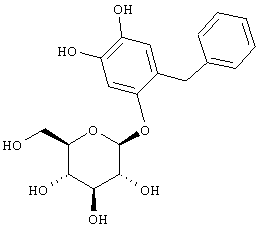
2) A.Levai et al., Acta Chim. Acad. Sci. Hung., 84, 99-107 (1975)
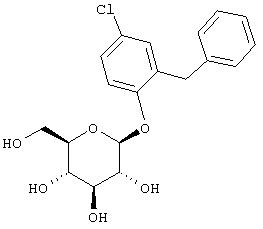
3) Н.Kaemmerer et al., Macromol. Chem., 182, 1351-1361 (1981)

Описание изобретения
Согласно данному изобретению предлагаются О-арилглюкозидные соединения формулы I

где когда Y обозначает
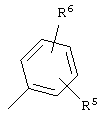
или гетероарил:
R1, R2, R3 и R4 одинаковы или различны и независимо выбираются из водорода, ОН, OR7, низшего алкила или галогена, или два из R1, R2, R3 и R4 вместе со связанными с ними атомами углерода могут образовывать аннелированный пяти-, шести- или семичленный карбоцикл или гетероцикл, который может содержать в цикле 1-4 гетероатома, этими гетероатомами могут являться N, О, S, SO и/или SO2;
R5 и R6 одинаковы или различны и независимо выбираются из водорода, ОН, OR7a, -ОАрила, ОСН2Арила, низшего алкила, циклоалкила, арила, арилалкила, CF3, арилалкенила, -OCHF2, - OCF3, галогена, -CN, -CO2R7b, -CO2H, COR8f, CHOHR8g, CH(OR7h)R8h, -CONR8R8a, -NHCOR7c, -NHSO2R7d, COR8f, -NHSO2Арил, -SR7e, -SO2R7g, -SO2Арил, -OCH2CO2R7i, -OCH2СО2Н, -OCH2CONR8bR8c, -OCH2CH2NR8dR8e или пяти-, шести или семичленного гетероцикла, который может содержать в цикле 1-4 гетероатома, представляющие собой N, О, S, SO и/или SO2, или R5 и R6 вместе с прилегающими к ним атомами углерода образуют аннелированный пяти-, шести или семичленный карбоцикл или гетероцикл, содержащий в цикле 1-4 гетероатома, которые представляют собой N, О, S, SO и/или SO2;
R7, R7a, R7b, R7c, R7d, R7d, R7e, R7f, R7g, R7h и R7i независимо обозначают низший алкил;
R8, R8a, R8b, R8c, R8d, R8e, R8f, R8g и R8h одинаковы или различны и независимо выбираются из водорода, алкила, арила, арилалкила, циклоалкила, или вместе с прилегающим к ним атомом азота образуют аннелированный пяти-, шести или семичленный гетероцикл, который может содержать в цикле 1-4 гетероатома, представляющие собой N, О, S, SO и/или SO2;
А обозначает O(CH2)m, S, NH(CH2)m или (СН2)n, где n обозначает 0-3, a m обозначает 0-2, и их фармацевтически приемлемые соли, все их стереоизомеры и все их пролекарственные сложные эфиры.
Соединения формулы I по изобретению, по определению выше, также отвечают следующим условиям:
если А обозначает СН2 и Y обозначает

и когда
1) R1 обозначает ОН и R3 обозначает алкил, по меньшей мере, один из R1, R4, R5 и R6 не обозначает водород и, предпочтительно, 4-R6 имеет значение, отличное от водорода;
2) R2 и R3 обозначают ОН, по меньшей мере, один из R1, R4, R5 и R6 не обозначает водород и, предпочтительно, 4-R6 имеет значение, отличное от водорода;
3) R2 обозначает метил, R5 обозначает ОН и R6 обозначает алкил, по меньшей мере, один из R1, R3 и R4 не обозначает водород; и
4) R2 обозначает хлор, по меньшей мере, один из R1, R3, R4, R5, R6 не обозначает водород и, предпочтительно, 4-R6 не является водородом.
В соединениях формулы I, где А обозначает O(СН2)m или NH(СН2)m, гетероатом О или N связан с арильным циклом, непосредственно связанным с глюкозидным фрагментом.
Соединения формулы I по изобретению обладает активностью как ингибиторы натрий-зависимых переносчиков глюкозы, обнаруживаемых в кишечнике и в почках млекопитающих, и применимы при лечении диабета и микро- и макрососудистых осложнений диабета, таких как ретинопатия, невропатия, нефропатия и при заживлении ран.
Настоящее изобретение предлагает соединения формулы I, фармацевтические композиции, содержащие такие соединения, и способы применения таких соединений.
Кроме того, в соответствии с данным изобретением предлагается способ лечения диабета, в частности диабета типа II и родственных заболеваний, включая осложнения при диабете, охватывающие ретинопатию, невропатию, нефропатию и заживление ран, и родственные заболевания, такие как устойчивость к инсулину, гипергликемия, гиперглицеринемия, Синдром X, повышенное содержание жирных кислот или глицерина в крови, ожирение, гипертриглицеридемия, атеросклероз и гипертензия, и способ повышения уровня липопротеинов высокой плотности, при этом терапевтически эффективное количество соединения структуры I вводят нуждающемуся в лечении больному.
Кроме того, согласно данному изобретению предлагается способ лечения диабета и родственных заболеваний по определению, приведенному выше и приводимому ниже в данном описании, при этом терапевтически эффективное количество соединения структуры I по изобретению и один, два или более антидиабетических агентов другого типа и/или один, два или более терапевтических агентов другого типа вводят нуждающемуся в лечении больному человеку.
Состояния, заболевания и болезни, в целом называемые "Синдром X" (также известный как метаболический синдром), подробно описаны в Johannsson J. Clin. Endocrinol. Metab., 727-34 (1997).
Термин "терапевтические агенты другого типа", применяемый в данном описании, относится к одному или более антидиабетическому агенту (других, нежели ингибиторы SGLT2 формулы I), одному или более агенту против ожирения и/или одному или более агенту, понижающему содержание липидов (включая агенты против склероза).
По вышеописанному способу по изобретению соединения структуры I применяются в примерном весовом соотношении с антидиабетическим (и) агентом (ами) и/или гиполипидимическим (и) агентом (ами) в зависимости от способа его применения около 0,01:1-300:1, предпочтительно, около 0,1:1-100:1, и более предпочтительно, около 0,1:1-10:1.
Предпочтительными являются соединения формулы IA

где А обозначает СН2 или О или S.
Более предпочтительными являются соединения формулы IA, где А обозначает СН2;
R1 обозначает Н, галоген или алкил;
R2 и R3, каждый, обозначает Н;
R5 обозначает Н.
Наиболее предпочтительными являются соединения формулы I структуры IB
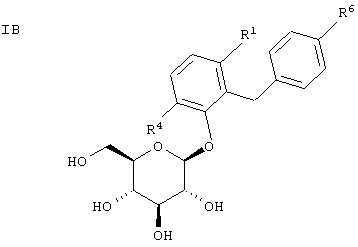
где R1 обозначает водород, галоген или алкил, или R1 и R4 независимо обозначают Н или алкил;
R6 обозначает водород, алкил, R7aO, CHF2O, CF3О или R7eS.
Примеры предпочтительных соединений формулы I по изобретению включают соединения, имеющие структуру
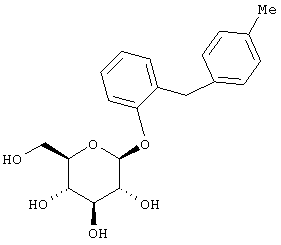 ,
,  ,
,

*R6=H, если не указано иначе
Настоящее изобретение охватывает соединения формулы I, фармацевтические композиции, содержащие такие соединения, и способы применения таких соединений.
Соединения формулы I по изобретению можно получать, как это изображено на следующих реакционных схемах и изложено в их описании, при этом температура выражается в градусах Цельсия.
Соединения формулы I по изобретению можно получать из соединений формулы II

обработкой II основанием, таким как LiOH или NaOH в растворителе, таком как МеОН/Н2О 3:1 или МеОН/ТГФ/Н2O 3:2:1.
Соединения формулы II можно получать реакцией промышленного 2,3,4,6-тетра-O-ацетил-α-D-глюкопиранозилбромида III
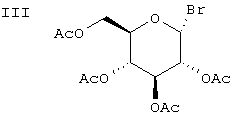
с соединениями формулы IV

в присутствии Ag2O в растворителе, таком как лутидин или хинолин, или в присутствии трифлата серебра в растворителе, таком как CH2Cl2, в присутствии основания, такого как 2,6-дитрет.-бутил-4-метилпиридин.
Схема 1

Соединения формулы IV, где А обозначает (СН2)n при n=1-3 можно получать из соединений формулы V

пропуская Н2 в растворителе, таком как МеОН или EtOH в присутствии катализатора, такого как Pd/C.
Соединения формулы V либо выпускаются промышленностью, либо легко получаются ацилированием соединений формулы VI

с соединениями формулы VII

различными методами, известными специалистам в данной области техники.
Соединения формулы IV, где А обозначает (СН2)2, можно получать из выпускаемых промышленностью соединений формулы VIII
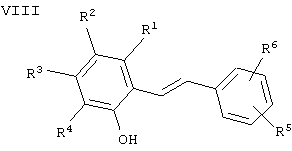
обработкой VIII Н2 в растворителе, таком как МеОН или EtOH в присутствии катализатора, такого как Pd/C.
Соединения формулы IV, где А обозначает СН2, можно получать алкилированием соединений формулы VI выпускаемыми промышленностью соединениями формулы IX
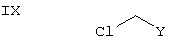
используя такой растворитель, как толуол, и основание, такое как NaH, при условии, что арильный или гетероарильный цикл ссоединения IX не является электрон-дефицитным, т.е. общая константа Гаммета σ для заместителей R5 и R6 менее ˜+0,3.
Соединения формулы IV, где А обозначает СН2, можно также получать из соединений формулы Х

восстановлением X водородом в растворителе, таком как МеОН или ETOH, в присутствии катализатора, такого как Pd/C, или силаном, например, Et3SiH в растворителе, таком как MeCN, в присутствии кислоты Льюиса, такой как ТФК или BF3·Et2O.
Соединения формулы Х легко получаются реакцией выпускаемых промышленностью соединений формулы XI

с металлоорганическими соединениями Mg+2 или Li+, получаемыми из арил или гетероарилбромидов или хлоридов формулы XII

известными специалистам в данной области техники методами.
Как показано на схеме 2, соединения IV, где А обозначает О, можно также получать реакцией соединений формулы XIII

с Н2 в растворителе, таком как МеОН или EtOH, с катализатором, таким как Pd/C. Соединения формулы XIII можно получать реакцией соединений формулы XIV
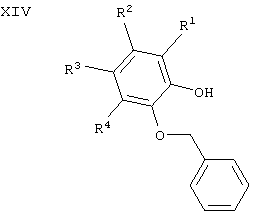
в растворителе, таком как пиридин, в присутствии Et3N, молекулярных сит и Cu(ОАс)2 с соединениями формулы XV

Соединения формулы XIV либо выпускаются промышленно, либо их можно получать из соответствующего катехола XVI

алкилированием его одним эквивалентом бензилбромида или бензилбромида методами, хорошо известными специалистам в данной области техники.
Соединения формулы XV получаются промышленно или их можно получать по реакции XVII с BCl3 при -75°С в растворителе, таком как CH2Cl2.

Соединения формулы XVII можно получать нагреванием соединений формулы XII

в растворителе, таком как ДМСО, в присутствии катализатора, такого как PdCl2·dppf, и основания, такого как КОАс, с соединением XVIII.

Схема 2

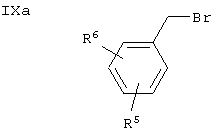
Соединения формулы IV, где А обозначает ОСН2, а именно,

можно получать реакцией соединений XVI с бензилгалогенидами формулы IXa в полярном растворителе, таком как ДМФА или ацетон, в присутствии основания, такого как Na2СО3, и катализатора, такого как NaI.
Соединения формулы IV, где А обозначает O(СН2)2, можно получать реакцией соединений XIX
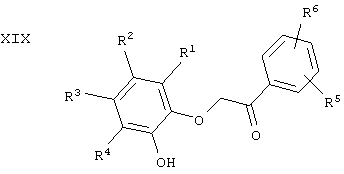
с Н2 в растворителе, таком как МеОН или EtOH, в присутствии катализатора, такого как Pd/C. Соединения формулы XIX выпускаются промышленностью, либо их можно получать алкилированием соединений формулы XVI в растворителе, таком как ацетон, в присутствии основания, такого как К2СО3, с промышленным фенацетилхлоридом или фенацетилбромидом формулы XX.
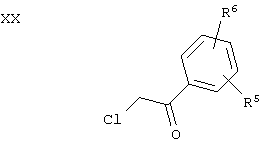
Соединения формулы IV, где А обозначает S, можно получать обработкой соединений формулы XXI
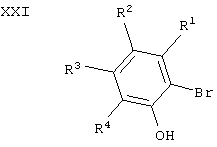
двумя эквивалентами трет.-BuLi при -78° в растворителе, таком как ТГФ, с последующим прибавлением соединений формулы XXII

Как показано на Схеме 3, соединения формулы II, где А обозначает NH, можно получать взаимодействием соединений формулы XXIII

с соединениями формулы XV в растворителе, таком как Et3N, содержащем Cu(ОАс)2 и молекулярные сита.
Соединения формулы XXIII можно получать реакцией соединений формулы XXIV
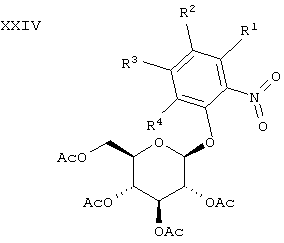
с Н2 в присутствии катализатора, такого как Pd/C, в растворителе, таком как МеОН или EtOH.
Соединения формулы XXIV можно получать конденсацией соединений формулы III с соединениями формулы XXV

в растворителе, таком как лутидин или хинолин, в присутствии Ag2O.

Соединения формулы II, где А обозначает NHCH2, можно получать конденсацией соединений формулы XXIII с соединениями формулы XXVI

при перемешивании в растворителе, таком как НОАс, с восстановителем, таким как NaCNBH3.
Соединения формулы II, где А обозначает NHCH2CH2, можно получать конденсацией соединений формулы XXIII с соединениями формулы XXVII

при перемешивании в растворителе, таком как НОАс, с восстановителем, таким как NaCNBH3.
Ниже приведен список пояснений различных терминов, применяемых для описания соединений по данному изобретению. Эти определения относятся к терминам, применяемым по всему описанию (если не указано иначе в конкретных примерах) либо самостоятельно, либо как часть более объемной группы.
В данном описании применяются следующие сокращения:
Ph = фенил
Bn = бензил
t-Bu = третичный бутил
Me = метил
Et = этил
TMS = триметилсилил
TMSN3 = триметилсилиазид
TBS = трет.-бутилдиметилсилил
ТГФ = тетрагидрофуран
Et2O = диэтиловый эфир
EtOAc = этилацетат
ДМФА = диметилформамид
МеОН = метанол
EtOH = этанол
i-PrOH = изопропанол
НОАс или АсОН = уксусная кислота
i-Pr2NEt = диизопропилэтиламин
Et3N = триэтиламин
DMAP = 4-диметиламинопиридин
NaBH4 = натрийборгидрид
LiAlH4 = алюмогидрид лития (литийалюминийгидрид)
n-BuLi = н-бутиллитий
Pd/C = палладий на угле
КОН = гидроксид (гидроокись) калия
NaOH = гидроксид (гидроокись) натрия
LiOH = гидроксид (гидроокись) лития
К2СО3 = карбонат калия
NaHCO3 = бикарбонат натрия
EDC (или EDC.HCl) или EDCI (или EDCI.HCl) или EDAC=3-этил-3'-(диметиламино)пропилкарбодиимида гидрохлорид (или 1-3-диметиламинопропил)-3-этилкарбодиимида гидрохлорид)
НОВТ или HOBT.H2O = 1-гидроксибензотриазол(а) гидрат
НОАТ = 1-гидрокси-7-азабензотриазол
Ph3Р = трифенилфосфин
Pd(OAc)2 = ацетат палладия
(Ph3Р)4Pd0 = тетракистрифенилфосфинпалладий
Ar = аргон
N2 = азот
мин = минута(ы)
h или hr = час
л = литр
мл = миллилитр
мкл = микролитр
г = грамм(ы)
мг = миллиграмм(ы)
мол = моли
ммол = ммоли
мэкв = миллиэквиваленты
RT = комнатная температура
нас. = насыщенный
aq. = водный
ТСХ = тонкослойная хроматография
ВЭЖХ = высокоэфективная жидкостная хроматография
LC/MS = высокоэффективная жидкостная хроматография/масс-спектрометрия
ЯМР = ядерный магнитный резонанс
т.пл = температура плавления
dppf = дифенилфосфинферроцен
DCE (ДХЭ) = дихлорэтан
Если не указано иначе, термин "низший алкил", "алкил" или "алк", применяемый в данном описании самостоятельно или как часть другой группы, охватывает углеводороды как с линейной, так и с разветвленной цепью, содержащие 1-20 атомов углерода, предпочтительно, 1-10 атомов углерода, более предпочтительно, 1-8 атомов углерода в нормальной цепи, такие как метил, этил, пропил, изопропил, бутил, трет.-бутил, изобутил, пентил, гексил, изогексил, гептил, 4,4-диметилпентил, октил, 2,2,4-триметилпентил, нонил, децил, ундецил, додецил, их различные разветвленные изомеры и т.п., а также такие группы, содержащие 1-4 заместителя, таких как галоид, например, F, Br, Cl или I или CF3, алкил, алкокси, арил, арилокси, арил(арил) или диарил, арилалкил, арилалкилокси, алкенил, алкинил, циклоалкил, циклоалкенил, циклоалкилалкил, циклоалкилалкилокси, при необходимости, имеющие в качестве заместителя аминогруппу, гидроксил, гидроксиалкил, ацил, оксогруппу, гетероарил, гетероарилокси, циклогетероалкил, арилгетероарил, арилоксикарбонил, гетероарилалкил, гетероарилалкокси, арилоксиалкил, арилоксиарил, алкиламидо, алканоиламино, арилкарбониламино, нитро, циано, тиол, галоидалкил, тригалоидалкил и/или алкилтио.
Если не указано иначе, термин "циклоалкил", применяемый в данном описании самостоятельно или как часть другой группы, включает насыщенные или частично ненасыщенные (содержащие 1 или 2 двойные связи) циклические углеводородные группы, содержащие 1-3 цикла, имеющие в своем составе в целом 3-20 атомов углерода, образующих циклы, предпочтительно, 3-10 атомов углерода, образующих цикл, который может быть конденсирован с 1 или 2 ароматическими циклами по определению для арила, которые включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклодецил и циклододецил, циклогексенил,



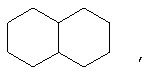

любая из этих групп может, при необходимости, иметь 1 -4 заместителя, таких как галоген, алкил, алкокси, гидрокси, арил, арилокси, арилалкил, циклоалкил, алкиламидо, алканоиламино, оксо, ацил, арилкарбониламино, амино, нитро, циано, тиол и/или алкилтио и/или любой из алкильных заместителей.
Термин "циклоалкенил", применяемый в данном описании самостоятельно или как часть другой группы, относится к циклическим углеводородам, содержащим 3-12 атомов углерода, предпочтительно, 5-10 атомов углерода, и 1 или 2 двойные связи. Примеры циклоалкенильных групп включают циклопентенил, циклогексенил, циклооктенил, циклогексадиенил и циклогептадиенил, которые могут иметь заместители, определение которых дано в разделе "циклоалкил".
Термин "алканоил", применяемый в данном описании самостоятельно или как часть других групп, относится к алкилу, связанному с карбонильной группой.
Если не указано иначе, термин "низший алкенил" или "алкенил", применяемый в данном описании самостоятельно или как часть другой группы, относится к радикалам с линейной или разветвленной цепью, содержащим 2-20 атомов углерода, предпочтительно, 2-20 атомов углерода, еще более предпочтительно, 1 -8 атомов углерода в нормальной цепи, которые имеют от одной до шести двойных связей в нормальной цепи, таким как винил, 2-пропенил, 3-бутенил, 2-бутенил, 4-пентенил, 3-пентенил, 2-гексенил, 3-гексенил, 2-гептенил,3-гептенил, 4-гептенил, 3-ноненил, 4-деценил, 3-ундеценил, 4-додеценил, 4,8,12-тетрадекатриенил и т.п., и которые, при необходимости, иметь 1-4 заместителя, а именно, галоген, галоидалкил, алкил, алкокси, алкенил, алкинил, арил, арилалкил, циклоалкил, амино, гидрокси, гетероарил, циклогетероалкил, алканоиламино, алкиламидо, арилкарбониламино, нитро, циано, тиол, алкилтио и/или любой из алкильных заместителей, представленных в данном описании.
Если не указано иначе, термин "низший алкинил", употребляемый в данном описании самостоятельно или как часть другой группы, относится к радикалам с линейной или разветвленной цепью, содержащим 2-20 атомов углерода, предпочтительно, 2-20 атомов углерода, и более предпочтительно, 2-8 атомов углерода в нормальной цепи, которые имеют одну тройную связь в нормальной цепи, таким как 2-пропинил, 3-бутинил, 2-бутинил, 4-пентинил, 3-пентинил, 2-гексинил, 3-гексинил, 2-гептинил, 3-гептинил, 4-гептинил, 3-октинил, 3-нонинил, 4-децинил, 3-ундецинил, 4-додецинил и т.п., и которые могут, при необходимости, иметь 1-4 заместителя, а именно, галоген, галоидалкил, алкил, алкокси, алкокси, алкенил, алкинил, арил, арилалкил, циклоалкил, амино, гетероарил, циклогетероалкил, гидрокси, алканоиламино, алкиламидо, арилкарбониламино, нитро, циано, тиол и/или алкилтио, и/или любой из алкильных заместителей, представленных в данном описании.
Термины "арилалкил", "арилалкенил" и "арилалкинил", применяемые самостоятельно или как часть другой группы, относятся к описанным выше алкильной, алкенильной и алкинильной группам, имеющим арильный заместитель.
Если алкильные группы по определению выше связываются с другими группами простыми связями у двух различных атомов углерода, они называются "алкиленовые" группы и могут, при необходимости, иметь заместители по определению для термина "алкил".
Если алкенильные группы по определению выше и алкинильные группы по определению выше, соответственно, связываются простыми связями у двух различных атомов углерода, они называются "алкениленовые группы" и "алкиниленовые группы", соответственно, и могут, при необходимости, иметь заместители по определению для "алкенила" и "алкинила".
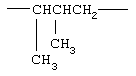
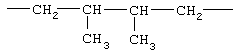
Соответствующие алкиленовые, алкениленовые или алкиниленовые группы (СН2)m, (СН2)n, или (СН2)p (где р может обозначать 1-8, предпочтительно, 1-5), которые включают алкиленовые, алкениленовые или алкиниленовые группы по определению в данном описании, могут, при необходимости, содержать 1, 2 или 3 заместителя, которые включают алкил, алкенил, галоген, циано, гидрокси, алкокси, амино, тиоалкил, кето, С3-С6-циклоалкил, алкилкарбониламино или алкилкарбонилокси.
Примеры (СН2)m, (СН2)n или (СН2)p алкиленов, алкениленов и алкиниленов включают -СН2-, -СН2СН2-,
 ,
,  ,
,  ,
, 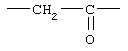 ,
,
 ,
,  ,
, 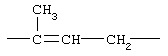 ,
,
 ,
, 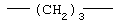 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
, 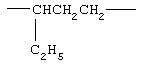 ,
,
 ,
,  ,
,  ,
, 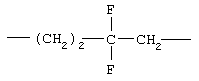 ,
,
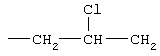 ,
,  ,
,  ,
,
 ,
, 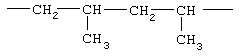 ,
, 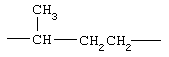 ,
,
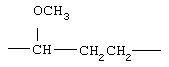 ,
, 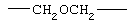 ,
, 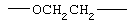 ,
, 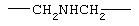 ,
,
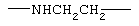 ,
,  ,
,  or
or  .
.
Термин "галоген" или "гало(ид)", применяемый в данном описании самостоятельно или как часть другой группы, относится к хлору, брому, фтору или йоду, причем предпочтительными являются хлор или фтор.
Термин "ион металла" относится к ионам щелочных металлов, таким как натрий, калий или литий, и к ионам щелочно-земельных металлов, таких как магний и кальций, а также к ионам цинка и алюминия.
Если не указано иначе, термин "арил" или "Арил", применяемый в данном описании самостоятельно или как часть другой группы, относится к моноциклическим или бициклическим ароматическим группам, содержащим 6-10 атомов углерода в цикле (таким как фенил или нафтил, включая 1-нафтил и 2-нафтил), и может, при необходимости, включать от одного до трех дополнительных циклов, конденсированных с карбоциклическим или гетероциклическим кольцом, таким как арильный, циклоалкильный, гетероарильный или циклогетероалкильный циклы, например,

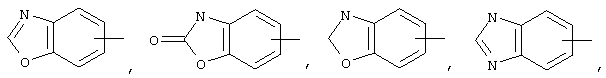
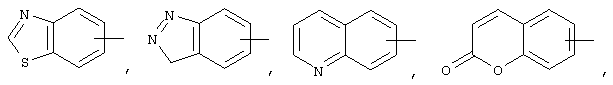
и могут, при необходимости, иметь в качестве заместителей у соответствующего атома углерода 1, 2 или 3 группы, выбираемых из водорода, галоида, галоидалкила, алкила, алкокси, галоидалкокси, алкенила, трифторметила, трифторметокси, алкинила, циклоалкилалкила, циклогетероалкила, циклогетероалкилалкила, арила, гетероарила, арилалкила, арилкарбонила, арилалкенила, аминокарбониларила, арилтио, арилсульфинила, арилазо, гетероарилалкила, гетероарилалкенила, гетероарилгетероарила, гетероарилокси, гидрокси, нитро, циано, амино, замещенного амино, причем аминогруппа содержит 1 или 2 заместителя (которые представляют собой алкил, арил или любое другое из упомянутых в определениях арильных соединений), тиола, алкилтио, гетероарилтио, арилтиоалкила, алкоксиарилтио, алкилкарбонила, арилкарбонила, алкиламинокарбонила, ариламинокарбонила, алкоксикарбонила, аминокарбонила, алкилкарбонилокси, арилкарбонилокси, алкилкарбониламино, арилкарбониламино, арилкарбониламино, арилсульфинила, арилсульфинилалкила, арилсульфониламино или арилсульфонаминокарбонила и/или любого из алкильных заместителей, представленных в данном описании.
Если не указано иначе, термин "низший алкокси", "алкокси", арилокси" или "аралкокси", применяемый в данном описании самостоятельно или как часть другой группы, включает любую из вышеуказанных алкильных, аралкильных или арильных групп, связанную с атомом кислорода.
Если не указано иначе, термин "замещенный амино", применяемый в данном описании самостоятельно или как часть другой группы, относится к замещенным аминогруппам, имеющим один или два заместителя, которые могут быть одинаковыми или различными, такие как алкил, арил, арилалкил, гетероарил, гетероарилалкил, циклогетероалкил, циклогетероалкилалкил, циклоалкил, циклоалкилалкил, галоидалкил, гидроксиалкил, алкоксиалкил или тиоалкил. Эти заместители могут дополнительно иметь в качестве заместителя карбоксильную группу и/или любой из перечисленных выше алкильных заместителей. Кроме этого, заместители в аминогруппе вместе с атомом азота, с которым они связаны, могут образовывать гетероциклические фрагменты-1-азепинил, 4-морфолинил, 4-тиаморфолинил, 1-пиперазинил, 4-алкил-1-пиперазинил, 4-арилалкил-1-пиперазинил, 4-диарилалкил-1-пиперазинил, 1-пирролидинил, 1-пиперидинил или 1-азепинил, при необходимости, имеющие в качестве заместителя алкил, алкокси, алкилтио, галоид, трифторметил или гидрокси.
Если не указано иначе, термин "низший алкилтио", "алкилтио", "арилтио" или "аралкилтио", применяемый в данном описании самостоятельно или как часть другой группы, включает любую из вышеприведенных алкильных, аралкильных или арильных групп, связанную с атомом серы.
Если не указано иначе, термин "низший алкиламино", "алкиламино", "ариламино" или "арилалкиламино", применяемый по данному описанию самостоятельно или как часть другой группы, включает любую из приведенных выше алкильных, арильных или арилалкильных групп, связанных с атомом азота.
Если не указано иначе, термин "ацил", применяемый в данном описании самостоятельно или как часть другой группы по определению в данном описании, относится к органическому радикалу, связанному с карбонильной группой; примеры ацильных групп включают любой из алкильных заместителей, связанных с карбонилом, например алканоил, алкеноил, ароил, аралканоил, гетероароил, циклоалканоил, циклогетероалканоил и т.п.
Если не указано иначе, термин "циклогетероалкил", применяемый в данном описании самостоятельно или в составе другой группы, относится к 5-, 6- или 7-членному насыщенному или частично ненасыщенному циклу, который содержит 1-2 гетероатома, таких как азот, кислород и/или серу, связанный через атом углерода или гетероатом, где это возможно, при необходимости, через линкер (СН2)p (где р обозначает 1, 2 или 3), например,
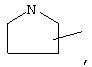

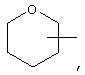



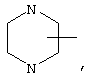

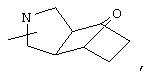



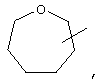
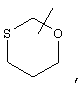
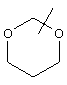
и т.п. Вышеуказанные группы могут включать 1-4 заместителя, таких как алкил, галоид, оксо и/или любой из представленных в данном описании алкильных заместителей. Кроме того, каждый из циклогетероалкильных фрагментов может быть конденсирован с циклоалкильным, арильным, гетероарильным или циклогетероалкильным кольцом.
Если не указано иначе, термин "гетероарил", применяемый в данном описании самостоятельно или в составе другой группы, относится к 5- или 6-членному ароматическому циклу, который содержит 1, 2, 3 или 4 гетероатома, таких как азот, кислород или сера, и такой цикл конденсирован с арильным, циклоалкильным, гетероарильным или циклогетероалкильным кольцом (например, бензотиофенил, индолил) и включают возможные N-оксиды. Гетероарильная группа может, при необходимости, иметь 1-4 заместителя, таких как любой из представленных выше алкильных заместителей. Примеры гетероарильных групп включают следующие:

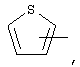
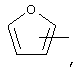





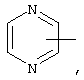


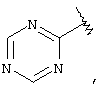



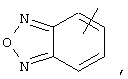



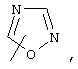
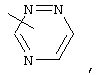
и т.п.
Термин "циклогетероалкилалкил", применяемый в данном описании самостоятельно или в составе другой группы, относится к циклогетероалкильным группам по определению выше, связанным через атом С или гетероатом с цепью (СН2)p.
Термин "гетероалкил" или "гетероалкилалкенил", применяемый в данном описании самостоятельно или в составе другой группы, относится к гетероарильной группе по определению выше, связанной через атом С или гетероатом с -(СН2)p- цепью, алкиленом или алкениленом по определению выше.
Термин "пяти, шести или семичленный карбоцикл или гетероцикл", применяемый в данном описании, относится к циклоалкильным или циклоалкенильным группам по определению выше или гетероарильньм группам или циклогетероарильным группам по определению выше, таким как тиадиазол, тетразол, имидазол или оксазол.
Термин "полигалоидалкил", применяемый в данном описании, относится к "алкильной" группе по определению выше, которая содержит 2-9, предпочтительно 2-5 галоидных заместителей, таких как F или Cl, предпочтительно F, например CF3СН2, CF3 или CF3CF2СН2.
Термин "полигалоидалкилокси", применяемый в данном описании, относится к "алкокси" или "алкилокси" группе по определению выше, которая содержит 2-9, предпочтительно, 2-5 галоидных заместителей, таких как F или Cl, предпочтительно, F, например, CF3СН2O, CF3О или CF3CF2CH2O.
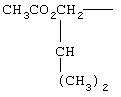
Термин "пролекарственные сложные эфиры", "пролекарственные эфиры", применяемый в данном описании, включает сложные эфиры и карбонаты, образующиеся при реакциях одной или более гидроксильных групп соединений формулы I, причем эти реакции проводятся по методикам, известным специалистам в данной области техники, с алкил-, алкокси- или арилзамещенными ацилирующими агентами с образованием ацетатов, пивалатов, метилкарбонатов, бензоатов и т.п.,. Кроме того, пролекарственные сложные эфиры карбоновых и фосфорных кислот, которые известны в технике, например, метиловый, этиловый, бензиловый и т.п.
Примеры таких пролекарственных сложных эфиров включают
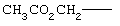 ,
,  ,
, 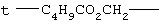 ,
,
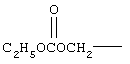 .
.
Другие примеры пригодных пролекарственных сложных эфиров включают
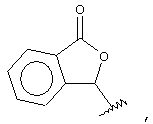

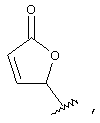


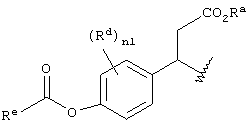
где Ra может обозначать Н, алкил (например, метил или трет.-бутил), арилалкил (например, бензил) или арил (например, фенил); Rd обозначает Н, алкил, галоген или алкокси, Re обозначает алкил, арил, арилалкил или алкоксил и n1 обозначает 0, 1 или 2.
Если соединения структуры I находятся в форме кислоты, они могут образовывать фармацевтически приемлемые соли, например соли щелочных металлов, таких как литий, натрий или калий, щелочно-земельных металлов, таких как кальций или магний, а также соли цинка или алюминия и других катионов, таких как аммоний, холин, диэтаноламин, лизин (D или L), этилендиамин, трет.-бутиламин, трет.-октиламин, трис-(гидроксиметил)аминометан (TRIS), N-метилглюкозамин (NMG), триэтаноламин и дегидроабиетиламин.
Охватываются все изомеры соединений по данному изобретению, либо в виде смеси, либо в чистом или практически чистом виде. Соединения по данному изобретению могут иметь асимметрические центры при любом атоме углерода, включая любой из заместителей R. Соответственно, соединения формулы I могут существовать в энантиомерной или диастереомерной формах или в виде их смесей. В процессе получения в качестве исходных можно применять рацематы, энантиомеры или диастереомеры. Когда получают диастереомерные или энантиомерные продукты, их можно разделять обычными методами, например хроматографией или фракционной кристаллизацией.
Если нужно, соединения структуры I можно применять в комбинации с одним или более антидиабетических агентов других типов и/или с одним или более терапевтических агентов других типов, которые можно принимать перорально в той же самой лекарственной форме или в виде отдельной пероральной лекарственной формы, или в виде инъекции.
Антидиабетический агент другого типа, который, при необходимости, можно применять в комбинации с ингибитором SGLT2 формулы I, может представлять собой 1, 2, 3 или более антидиабетических агентов или антигипергликемических агентов, включая средства, усиливающие секрецию инсулина или сенсибилизаторы инсулина, или другие антидиабетические агенты, предпочтительно имеющие механизм действия, отличный от ингибирования SGLT2, и может включать бигуаниды, сульфонилмочевины, ингибиторы глюкозидазы, PPAR γ агонисты, такие как тиазолидиндионы, ингибиторы аР2, PPAR α/γ двойные агонисты, ингибиторы дипептидилпептидазы IV (DP4) и/или меглитиниды, а также инсулин и/или глюкагоноподобный пептид-1 (GLP-1).
Полагают, что применение соединений структуры I в комбинации с 1, 2, 3 или более другими антидиабетическими агентами дает более высокий антигипергликемический результат, чем можно было бы ожидать в случае их самостоятельного применения, и больше, чем мог бы быть общий аддитивный эффект, вызываемый этими препаратами.
Другим антидиабетическим агентом может быть пероральный антигипергликемический агент, предпочтительно бигуанид, такой как метформин или фенформин или их соли, предпочтительно метформин HCl.
Если другим антидиабетическим является бигуанид, соединения структуры I применяют в весовом соотношении с бигуанидом около 0,1:1-5:1.
Другим антидиабетическим агентом, предпочтительно, может также являться сульфонилмочевина, например глибурид (также известный как глибенкламид), глимепирид (описанный в Патенте США 4379785), глипизид, гликлазид или хлорпропамид, другие известные сульфонилмочевины или другие антигипергликемические агенты, которые действуют на АТФ-зависимый канал β-клеток, причем предпочтительными являются глибурид и глипизид, которые можно принимать в виде той же самой или в виде отдельной пероральной лекарственной формы.
Соединения структуры I применяют в примерном весовом отношении к сульфонилмочевине около 0,01:1-100:1, предпочтительно около 0,2:1-10:1.
Пероральный диабетический агент может также являться ингибитором глюкозидазы, таким как акарбоза (описанная в Патенте США 4904769) или миглитол (раскрываемый в Патенте США 4639436), которую можно вводить в виде той же самой или в виде отдельной пероральной лекарственной формы.
Соединения структуры I можно применять в примерном весовом отношении к ингибитору глюкозидазы около 0,01:1-100:1, предпочтительно около 0,5:1-50:1.
Соединения структуры I можно применять в комбинации с PPAR γ агонистом, таким как тиазолидиндионовый пероральный антидиабетический агент, или другим сенсибилизатором инсулина (который повышает у больных NIDDM чувствительность к инсулину), таким как троглитазон (Rezulin® фирмы Warner-Lambert, описанный в Патенте США 4572912), розиглитазон (SKB), пиоглитазон (Takeda), MCC фирмы Mitsubishi (описан в Патенте США 5594016), GL-262570 фирмы Glaxo-Welcome, эглитазон (СР-68722, Pfizer) или дарглитазон (СР-86325, Pfizer), изаглитазон (MIT/JandJ), JTT-501 (JPNT/PandU), L-895645 (Merk), R-119702 (Sankyo/WL), NN-2344 (Dr. Reddy/NN) или YM-440 (Yamanouchi), предпочтительно розиглитазон и пиоглитазон.
Соединения структуры I применяют в примерном весовом отношении к тиазолидиндиону около 0,01:1-100:1, предпочтительно около 0,2:1-10:1.
Сульфонилмочевину и тиазолидиндион в количествах менее 150 мг перорального антидиабетического агента можно применять в виде одной таблетки вместе с соединениями структуры I.
Соединения структуры I можно также применять в комбинации с антигипергликемическим агентом, таким как инсулин, или с глюкагоноподобным пептидом -1 (GLP-1), таким как GLP-1(1-36) амид, GLP-1 (7-36) амид, GLP-1 (7-37) (как показано в Патенте США 5614492, выданном Habener, который вводится в данное описание в качестве ссылки), а также АС2993 (Amylen) и LY-315902 (Lilly), которые можно вводить в виде инъекции, назально или с помощью трансдермальных или защечных устройств.
Метформин, сульфонилмочевины, такие как глибурид, глимепирид, глипирид, глипизид, хлорпропамид и гликлазид, и ингибиторы глюкозидазы акарбоза или миглитол или инсулин (инъекции, легочно, трансбуккально или перорально), при их наличии, могут применяться в рецептурах, как описано выше, и в количествах и дозировках, указанных в Настольном врачебном справочнике (PDR).
Метформин или его соль, если они присутствуют, могут применяться в количествах, примерно, 500-2000 мг в день, которые можно вводить в виде однократной или разделенных доз один - четыре раза в день.
Антидиабетический агент ряда тиазолидиндиона, при его наличии, может применяться в количествах около 0,01-2000 мг/день, которые можно вводить в виде однократной (разовой) или разделенных доз один - четыре раза в день.
Инсулин, при его наличии, можно применять в рецептурах, количествах и дозировках, указанных в Настольном врачебном справочнике.
Пептиды GLP-1, при их наличии, можно вводить в виде трансбуккальных (внутриротовых) рецептур, назально или парентерально, как описано в Патентах США 5346701 (TheraTech), 5614492 и 5631224, которые вводятся в данное описание в качестве ссылки.
Другой антидиабетический агент может также представлять собой PPAR α/γ двойной агонист, такой как AR-НО39242 (Astra/Zeneca), GW-409544 (Glaxo-Wellcome), KRP297 (Kyorin Merck), а также антидиабетические агенты, описанные Murakami et al., "A Novel Insulin Sensitizer Acts As a Coligand for Peroxisome Proliferation - Activated Receptor Alpha (PPAR alpha) and PPAR gamma. Effect on PPAR alpha Activation on Abnormal Lipid Metabolism in Liver of Zucker Fatty Rats", Diabetes 47, 1841-1847 (1998), и в предварительной заявке на Патент США 60/155400, поданной 22 сентября 1999 года (№ дела у поверенного LA29), которые вводятся в данное описание во всей полноте в качестве ссылки, применяемые в указанных там дозах, при этом соединения, признанные в этих ссылках предпочтительными, являются предпочтительными для применения по данному описанию.
Другим антидиабетическим агентом может являться ингибитор аР2, такой как описанный в заявке на Патент США 09/391053, поданной 7 сентября 1999 года, и в предварительной заявке на Патент США 60/127745, поданной 5 апреля 1999 года (№ дела у поверенного LA27*), с применением доз, указанных в данном описании. Предпочтительными являются соединения, указанные как предпочтительные в вышеперечисленных заявках.
Другим антидиабетическим агентом может являться ингибитор DP4, такой как описанные в Международных Заявках 99/38501, 99/46272, 99/67279 (PROBIODRUG), 99/46272, 99/67279 (PROBIODRUG), 99/38278 (PROBIODRUG), 99/61431 (PROBIODRUG), NVP-DPP728A (1-[[[2-[(5-цианопиридин-2-ил)амино]этил]амино]ацетил]-2-циано-(S-пирролидин) (Novartis) (предпочтительно), описанный Hughes et al., Biochemistry, 38(36), 11597-11603, 1999, TSL-225 (триптофил-1,2,3,4-тетрагидроизохинолин-3-карбоновая кислота (описанная Yamada et al., Bioorg. and Med. Chem. Lett. 8 (1998) 1537-1540), 2-цианопирролидиды и 4-цианопирролидиды, описанные Ashworth et al., Bioorg. And Med. Chem. Lett., Vol.6, №22, pp. 1163-1166 и 2745-2748 (1996), с применением доз, указанных в вышеприведенных ссылках.
Меглитинид, который, при необходимости, может применяться в комбинации с соединением формулы I по изобретению, может представлять собой репаглинид, натеглинид (Novartis) или KAD1229 (PF/Kissei), при этом предпочтительным является репаглинид.
Ингибитор SGLT2 формулы I применяется в примерном весовом отношении к меглитиниду, PPAR α/γ двойному агонисту, ингибитору аР2 или ингибитору DP4 около 0,2:1-10:1.
Гиполипидемический агент или понижающий уровень липида агент, который, при необходимости, можно применять в комбинации с соединениями формулы I по изобретению, может включать 1, 2, 3 или более ингибиторов МТР, ингибиторы HMG СоА редуктазы, ингибиторы сквален-синтетазы, производные фибриновой кислоты, ингибиторы АСАТ, ингибиторы липоксигеназы, ингибиторы всасывания (абсорбции) холестерина, ингибиторы котранспортера Na+/желчных кислот в подвздошной кишке, положительные регуляторы LDL - рецепторной активности, вещества, усиливающие секрецию желчных кислот и/или никотиновую кислоту и ее производные.
Ингибиторы МТР, применяемые по данному описанию, охватывают ингибиторы МТР, раскрываемые в Патентах США 5595872, 5739135, 5712279, 5760246, 5827875, 5885983 и заявке на Патент США 09/175180, поданной 20 октября 1998 года, в настоящее время Патент США 5962440. Предпочтительными является каждый предпочтительный ингибитор МТР, раскрываемый в каждой из вышеуказанных патентов и заявок.
Все вышеуказанные Патенты и заявки на Патенты США вводятся в данное описание в качестве ссылки.
Наиболее предпочтительные ингибиторы МТР для применения в соответствии с настоящим изобретением включают предпочтительные ингибиторы МТР, подробно описанные в Патентах США 5739135, 5712279 и 5760246.
Наиболее предпочтительным ингибитором МТР является 9-[4-[4-[[2-(2,2,2-трифторэтокси)бензоил]амино]-1-пиперидинил]бутил]-N-(2,2,2-трифторэтил)-9Н-флуорен-9-карбоксамид.
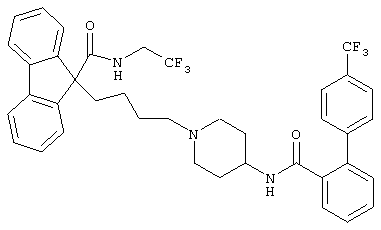
Гиполипидемический агент может являться ингибитором HMG СоА редуктазы, который включает, без ограничения, мевастатин и родственные соединения, раскрываемые в Патенте США 3983140, ловастатин (мевинолин) и родственные соединения, раскрываемые в Патенте США 4231938, правастатин и родственные соединения, например, такие которые раскрываются в Патенте США 4346227, симвастатин и родственные соединения. Раскрываемые в Патентах США 4448784 и 4450171. Другие ингибиторы HMG СоА редуктазы, которые можно применять по данному описанию, включают, но без ограничения, флувастатин, раскрываемый в Патенте США 5354772, церивастатин, описанный в Патентах США 5006530 и 5177080, аторвастатин, описанный в Патентах США 4681893, 5273995, 5385929 и 5686104, атавастатин (нисвастатин фирмы Nissan/Sankyo (NK-104)), описанный в Патенте США 5011930, визастатин (visastatin) Shionogi-Astra/Zeneca (ZD-4522), раскрываемый в Патенте США 5260440, и родственные статиновые соединения, раскрываемые в Патенте США 5753675, пиразольные аналоги производных мевалонолактона, описанные в Патенте США 4613610, инденовые аналоги производных мевалонолактона, раскрываемые в заявке РСТ WO 86/03488, 6-[2-(замещенный-пиррол-1-ил)-алкил)пиран-2-оны и их производные, раскрываемые в Патенте США 4647576, дихлорацетат SC-45355 фирмы Searle (производное 3-замещенной пентандиовой кислоты, имидазольные аналоги мевалонолактона, раскрываемые в заявке РСТ WO 86/07054, производные 3-карбокси-2-гидроксипропанфосфоновой кислоты, раскрываемые во французском патенте 2596393, производные 2,3,-дизамещенного пиррола, фурана и тиофена, раскрываемые в Европейской Патентной Заявке 0221025, нафтильные аналоги мевалонолактона, раскрываемые в Патенте США 4686237, октагидронафталины, такие как раскрываемые в Патенте США 4499289, кетоаналоги мевинолина (ловастатина), раскрываемые в Европейской Патентной Заявке 0142146 А2, и производные хинолина и пиридина, раскрываемые в Патентах США 5509219 и 5691322.
Далее, фосфиновые кислоты, применимые для ингибирования HMG СоА редуктазы, раскрываемые в английском патенте 2205837, пригодны для применения по данному описанию.
Ингибиторы сквален-синтетазы, пригодные для применения по данному описанию, включают, но без ограничения, α-фосфонсульфонаты, раскрываемые в Патенте США 5712396, α-фосфонсульфонаты, описанные Biller et al., J. Med.Chem., 1988. Vol.31, №10, pp 1869-1871, включая изопреноидные (фосфинилметил)фосфонаты, а также другие известные ингибиторы сквален-синтетазы, например, описываемые в Патентах США 4871721 и 4924024 и в Biller, S.A., Neuenschwander, К., Ponpipom, M.M., and Poulter, C.D., Current Pharmaceutical Design, 2, 1-40 (1996).
Далее, другие ингибиторы сквален-синтетазы, пригодные для применения по данному описанию, охватывают терпеноидные пирофосфаты, описанные Р.Ortiz de Montellano et al., J. Med. Chem. 1977, 20, 243-249, аналог А фарнезилдифосфата и аналоги прескваленпирофосфата (PSQ-PP), описанные Corey and Volante, J. Am. Chem. Soc., 1976, 98, 1291-1293, фосфинилфосфонаты, о которых сообщает McClard, R.W. et al., J.А.С.S., 1987, 109, 5544, и циклопропаны, описанные Capson, T.L., PhD dissertation, June, 1987, Dept. Med. Chem. U of Utah, Abstract, Table of Contents, pp 16, 17, 40-43, 48-51, Summary.
Другие гиполипидемические агенты, пригодные для применения по данному описанию, включают, но без ограничения, производные фибриновой кислоты, такие как фенофибрат, гемфиброзил, клофибрат, безафибрат, ципрофибрат, клинофибрат и т.п., пробукол и родственные соединения, раскрываемые в Патенте США 3674836, при этом предпочтительными являются пробукол и гемфиброзил, вещества, усиливающие секрецию желчных кислот, такие как холестирамин, колестипол и DEAE-Sephadex (Secholex®, Policexide®), а также липостабил (Rhone-Poulenc), Eisai E-5050 (производное N-замещенного этаноламина), иманиксил (НОЕ-402), тетрагидролипстатин (THL), истигмастанилфосфорилхолин (SPC, Roche), аминоциклодекстрин (Tanabe Seioku), Ajimoto AJ-814 (производные азулена), мелинамид (Sumimoto), Sandoz 58-035, CL-277082 и CL-283546 фирмы American Cyanamid (производные дизамещенной мочевины), никотиновую кислоту, аципимокс, ацифран, неомицин, п-аминосалициловую кислоту, аспирин, производные поли(диаллилметиламина), такие как описанные в Патенте США 4759923, соль четвертичного аммониевого основания поли(диаллилдиметиламмонийхлорид) и иононы, такие как раскрываемые в Патенте США 4027009, и другие известные агенты, понижающие содержание холестерина в сыворотке.
Другой гиполипидемический агент может представлять собой ингибитор АСАТ, такой как описанный в Drugs in Future 24, 9-15 (1999),(Avasimibe); "The АСАТ inhibitor, C1-1011 is effective in the prevention and regression of aortic fatty streak area in hamsters", Nicolosi et al., Atherosclerosis (Shannon, Irel). (1998), 137(1), 77-85; The pharmacological prophile of FCE 27677: a novel АСАТ inhibitor with potent hypolipidemic activity mediated by selective suppression of hepatic secretion of ApoB100 - containing lipoprotein", Ghiselli, Giancarlo, Cardiovasc. Drug Rev. (1998), 16(1), 16-30; "RP 73163: a bioavailable alkylsulfinyl-diphenylimidazole АСАТ inhibitor", Smith, C., et al., Bioorg. Med. Chem. Lett. (1996), 6(1), 47-50; "АСАТ inhibitors: physiologic mechanisms for hypolipidemic and anti-atherosclerotic activities in experimental animals", Krause et al., Editor(s): Ruffolo, Robert., Jr; Hollinger, Mannfred A., Inflammation: Mediators Pathways (1995), 173-98, Publisher: CRC, Boca Raton, Fla.; "АСАТ inhibitors: potential anti-atherosclerotic agents", Sliskovic et al., Curr. Med. Chem. (1994), 1(3), 204-25; "Inhibitors of acyl-CoA: cholesterol О-acyl transferase (АСАТ) as hypocholesterolemic agents. 6. The first water-soluble АСАТ inhibitor with lipid-regulating activity. Inhibitors of acyl-CoA: cholesterol acyltransferase (АСАТ). 7. Development of a series substituted N-phenyl-N'-[(1-phenylcyclopentyl)methyl]ureas with enhanced hypocholesterolemic activity". Stout et al., Chemtracts: Org. Chem. (1995), 8(6), 359-62, или TS-962 (Taisho Pharmaceutical Co. Ltd.)
Гиполипидемический агент может быть позитивным регулятором LD2 рецепторной активности, таким как MD-700 (Taisho Pharmaceutical Co Ltd.) и LY295427 (Eli Lilly). Гиполипидемический агент может быть ингибитором всасывания холестерина, предпочтительно, SCH48461 фирмы Schering-Plough, а также таким ингибитором всасывания холестерина, как раскрываемые в Atherosclerosis 115, 45-63 (1995) и J. Med. Chem. 41, 973 (1998).
Гиполипидемический агент может представлять собой ингибитор котранспортера Na+/желчных кислот, таким как описанные в Drugs in Future, 24, 425-430 (1999).
Предпочтительными гиполипидемическим агентами являются правастатин, ловастатин, симвастатин, аторвастатин, флувастатин, церивастатин и ZD-4522.
Вышеуказанные патенты США вводятся в данное описание в качестве ссылок. Применяются количества и дозы, указанные в Настольном врачебном справочнике и/или в приведенных выше патентах.
Соединения формулы I по изобретению применяются в весовом отношении к гиполипидемическому агенту (если он присутствует), примерно, 500:1-1:500, предпочтительно, около 100:1-1:100.
Применяемую дозу следует тщательно корректировать в соответствии с возрастом, весом и состоянием больного, а также со способом применения, лекарственной формой и схемой приема и ожидаемым результатом.
Патенты США вводятся в данное описание в качестве ссылок. Применяются количества и дозы, указанные в Настольном врачебном справочнике и/или в приведенных выше патентах.
Соединения формулы I по изобретению применяются в весовом отношении к гиполипидемическому агенту (если он присутствует), примерно, 500:1-1:500, предпочтительно, около 100:1-1:100.
Применяемую дозу следует тщательно корректировать в соответствии с возрастом, весом и состоянием больного, а также со способом применения, лекарственной формой и схемой приема и ожидаемым результатом.
Применяют дозы и рецептуры гиполипидемического агента, описываемые в различных патентах и заявках, обсуждаемых выше.
Дозы и препараты другого применяемого гиполипидемического агента, в случае его применения, берут из последнего издания Настольного врачебного справочника.
В случае перорального применения удовлетворительных результатов можно достичь, применяя ингибитор МТР в количествах около 0,01 мг/кг - 500 мг, предпочтительно, около 0,1 мг - 100 мг один - четыре раза в день.
Предпочтительная пероральная лекарственная форма, такая как таблетки или капсулы, содержит ингибитор МТР в количестве около 1-500 мг, предпочтительно, около 2-400 мг и, наиболее предпочтительно, около 5-250 мг один - четыре раза в день.
При пероральном приеме удовлетворительные результаты достигаются при применении ингибитора HMG СоА редуктазы, например правастатина, ловастатина, симвастатина, аторвастатина, флувастатина или церивастатина в дозах, предписываемых Настольным врачебньм справочником, например, в количествах около 1-2000 мг, и предпочтительно, около 4-200 мг.
Ингибитор сквален-синтетазы можно применять в дозах, примерно, 10-2000 мг, и предпочтительно, около 25-200 мг.
Предпочтительная пероральная лекарственная форма, такая как таблетки или капсулы, содержит ингибитор HMG СоА редуктазы в количестве около 0,1-100 мг, предпочтительно, около 5-80 мг, и более предпочтительно, около 10-40 мг.
Предпочтительная пероральная лекарственная форма, такая как таблетки или капсулы, содержит ингибитор сквален-синтетазы в количестве около 10-500 мг, предпочтительно, около 25-200 мг.
Другой гиполипидемический агент может также быть ингибитором липоксигеназы, включая ингибитор 15-липоксигеназы (15-LO), такой как производные бензимидазола, описываемые в Международной заявке WO 97/12615, ингибиторы 15-LO, описываемые WO 97/12613, изотиазолоны, подобные раскрываемым в WO 96/38144, и ингибиторы 15-LO, описываемые Sendobry et al., "Attenuation of diet-induced atherosclerosis in rabbits with a highly selective 15-lipoxygenase inhibitor lacking significant antioxidant properties", Brit. J. Pharmacology (1997) 120, 1199-12066, и Cornicelli et al., "15-Lipoxygenase and its Inhibition: A Novel Therapeutic Target for Vascular Disease", Current Pharmaceutical Design, 1999, 5, 11-20.
Соединения формулы I и гиполипидемический агент могут применяться вместе в виде одной и той же лекарственной формы или в виде раздельных лекарственных форм, принимаемых одновременно.
Вышеописанные композиции можно принимать в представленных выше лекарственных формах в виде однократной или разделенных доз один - четыре раза в день. Желательно больному начинать с комбинации низких доз и постепенно доходить до комбинации высоких доз.
Предпочтительным гиполипидемическим агентом является правастатин, симвастатин, ловастатин, аторвастатин, флувастатин или церивастатин.
Другим типом терапевтического агента, который, при необходимости, можно применять с ингибитором SGLT2 формулы I, могут являться 1, 2, 3 или более агентов против ожирения, включая бета 3 адренергический агонист, ингибитор липазы, ингибитор повторного поглощения серотонина (и дофамина), препарат тироидного рецептора бета, и/или средство, снижающее аппетит.
Бета 3 адренергический агонист, который можно, при необходимости, применять в комбинации с соединением формулы I, может представлять собой AJ9677 (Takeda/Dainippon), L750355 (Merck) или СР331648 (Pfizer) или другие известные бета 3 агонисты, описанные в Патентах США 5541204, 5770615, 5491134, 5776983 и 5488064, при это предпочтительными являются AJ 9677, L750355 и СР331648.
Ингибитор липазы, который можно, при необходимости, применять в комбинации с соединением формулы I, может представлять собой орлистат или ATL-962 (Alizyme), при этом предпочтительным является орлистат.
Ингибитор повторного поглощения серотонина (и дофамина), который, при необходимости, может применяться в комбинации с соединением формулы I, может представлять собой сибутрамин, топирамат (Johnson and Johnson) или аксокин (Regeneron), при этом предпочтительными являются сибутрамин и топирамат.
Тироидный рецептор бета, который, при необходимости, можно применять в комбинации с соединением формулы I, может представлять собой лиганд тироидного рецептора, описанный в WO 97/21993 (U.Cal SF), WO 99/00353 (KaroBio) и в английском патенте GB 98/284425 (KaroBio), при этом предпочтительными являются соединения заявителей KaroBio.
Веществом, снижающим аппетит, который, при необходимости, можно применять в комбинации с соединением формулы I, может быть дексамфетамин, фентермин, фенилпропаноламин или мазиндол, причем предпочтительным является дексамфетамин. Различные вышеописанные вещества против ожирения могут применяться в одной лекарственной форме с соединением формулы I или в различных лекарственных формах, дозы и схемы приема обычно известны из уровня техники или из PDR.
При осуществлении способа лечения диабета и родственных заболеваний по изобретению используют фармацевтическую композицию соединения формулы I с другим(и) антидиабетическим(и) агентом (ами), и/или антигипергликемическим(и) агентом (ами), и/или терапевтическими агентами другого типа, или без них в сочетании с фармацевтическим носителем или разбавителем. Можно приготовить фармацевтическую композицию, содержащую обычные твердые или жидкие наполнители или разбавители и фармацевтические добавки, соответствующие заданному способу применения, например, фармацевтически приемлемые носители, эксципиенты, связующие и т.п. Соединения можно вводить различным видам млекопитающих, включая человека, обезьян, собак и т.д. перорально, например в форме таблеток, капсул, гранул или порошков, или их можно вводить назально или в виде трансдермальных пластырей. Типичные твердые рецептуры содержат около 10-500 мг соединения формулы I. Доза для взрослых составляет, предпочтительно, 10-2000 мг в день, и ее можно принимать в виде однократной дозы или в виде отдельных доз 1 - 4 раза в день.
Типичный препарат для инъекций готовят в асептических условиях, помещая 250 мг соединения структуры I в ампулу (пробирку), лиофилизируют в асептических условиях и плотно закрывают (запаивают). С целью применения содержимое ампулы (пробирки) смешивают с 2 мл физиологического раствора, получают препарат для инъекций.
SGLТ2-ингибирующую активность соединений по изобретению можно определить с помощью аналитической системы, представленной ниже.
Анализ SGLT2 активности
Последовательность мРНК человека (GenBank № M95549) клонируют с применением обратной транскрипции и амплификации мРНК почки человека обычными методами молекулярной биологии. Последовательность кДНК стабильно трансфицируют в СНО клетки и клоны анализируют на SGLT2 активность практически так, как описано в Ryan et al. (1994). Оценку ингибирования SGLT2 активности клонально отобранной клеточной линии осуществляют, в основном, по Ryan et al., с приведенными ниже модификациями. Клетки выращивают в 96-луночных планшетах 2-4 дня до 75000 или 30000 клеток на лунку в питательной смеси F-12 (F-12 Хэма (Ham)), дополненной 10% фетальной телячьей сывороткой, 300 мкг/мл генетицина и пенициллином-стрептомицином. По достижении монослоя клетки отмывают дважды раствором 10 мМ Hepes/Tris, pH 7,4, 137 мМ N-метил-D-глюкамина, 5,4 мМ KCl, 2,8 мМ CaCl2, 1,2 мМ MgSO4. Затем клетки инкубируют с 10 мкМ [14C]AMG и 10 мкМ ингибитора (конечная концентрация раствора в ДМСО=0,5%) в 10 мМ Hepes/Tris, pH 7,4, 137 мМ NaCl, 5,4 мМ KCl, 2,8 мМ CaCl2, 1,2 мМ MgSO4 при 37°С в течение 1,5 час. Пробы для анализа поглощения разбавляют охлаждаемым льдом 1X PBS, содержащим 0,5 мМ флоризина, затем клетки лизируют 0,1% NaOH. После добавления сцинтилляционной жидкости MicroScint клетки встряхивают 1 час, а затем количественно определяют [14C]AMG с помощью сцинтилляционного счетчика TopCount. Контроль осуществляют с или без NaCl. Для определения значений IC50 используют 10 концентраций ингибитора через 2 log интервала в соответствующей области чувствительности (ответа), и во всех планшетах каждый результат проверяют трижды.
Ryan MJ, Johnson G, Kirk J, Fuerstenberg SM, Zager RA and Torok-Storb B. 1994. HK-2: an immortalized proximal tubule epithelial cell line from normal adult human kidney. Kidney International 45: 48-57.
Следующие примеры представляют собой предпочтительные варианты изобретения. Все значения температур выражены в градусах Цельсия, если не указано иначе.
Пример 1

А. 4-Метил-2'-гидроксибензгидрол
В круглодонную колбу на 500 мл, содержащую 100 мл ТГФ, под аргоном добавляют готовый реактив 1 М п-метилфенилмагнийбромид/Et2О (100 мл, 100 ммол). Затем по каплям четырьмя равными порциями за 2 час прибавляют салициловый альдегид. Через 20 мин, когда анализ ВЭЖХ показывает отсутствие альдегида, к реакционной смеси по каплям добавляют 26 мл нас. NH4Cl/H2O, при этом образуется белая суспензия. К этой суспензии добавляют 200 мл PhMe и достаточное для перемешивания количество Н2О. Органический слой декантируют, а белую пасту второй раз растирают с ТГФ/PhMe 1:1. После декантации объединенные органические вытяжки упаривают на роторном испарителе, при этом получают 9,7 г сырого 4-метил-2'-гидроксибензгидрола.
В. 2-(4'-Метилбензил)фенол
К раствору сырого 4-метил-2'-гидроксибензгидрола из раздела А (9,7 г, содержащих не более 40 ммол) в 175 мл МеОН добавляют 0,59 г 10% Pd/C и 1,75 мл ТФК. Суспензию перемешивают 40 часов при давлении Н2 1 атм, фильтруют через целит и упаривают, получают 8,6 г сырого 2-(4'-метилбензил)фенола в виде масла.

Смесь 2-(п-метилбензил)фенола (8,6 г, содержат не более 37 ммол) из раздела В, 2,6-дитрет.-бутил-4-метилпиридина (19,6 г, 52 ммол), 2.3,4.6-тетра-O-ацетил-α-D-глюкопиранозилбромида (17,5 г, 43 ммол) в 270 мл СН2Cl2 перемешивают до гомогенного состояния, а затем охлаждают до 0°С. После прибавления к охлажденному раствору AgOTf (12,2 г, 47 ммол) реакционную смесь перемешивают 1 час и прибавляют дополнительное количество 2,3,4,6-тетра-O-ацетил-α-D-глюкопиранозилбромида (7,6 г, 18 ммол) и AgTOf (6,5 г, 25 ммол). Для перемешивания суспензии требуется еще 100 мл СН2Cl2. Через 30 мин суспензию наносят непосредственно на колонку с силикагелем, которую элюируют сначала 25% EtOAc/гексаном. Нежелательный минорный α-аномерный продукт элюируют первым, затем 25-35% EtOAc/гексаном вымывают заданный заглавный тетраацетат β-O-глюкозида. После упаривания сырой продукт растворяют в минимальном количестве EtOAc и вызывают кристаллизацию, добавляя гексан. Всего получают 8,25 г чистого заданного заглавного бета-изомера плюс ˜3 г вещества, содержащего примеси.
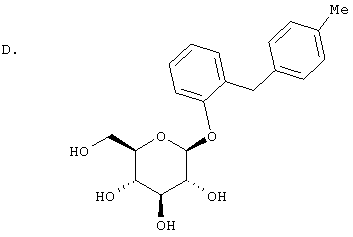
К раствору соединения из раздела С (8,25 г, 15 ммол) в 35 мл СН2Cl2 прибавляют МеОН (200 мл), а затем 0,7 мл NaOH в Н2О. Через 2 час по окончании реакции (ВЭЖХ) летучие отгоняют на роторном испарителе. Остаток, растворенный в смеси H2O/CH2Cl2/MeOH (1:10:10, 42 мл) разбавляют CH2Cl2 (400 мл), а затем наносят на колонку с силикагелем. Искомый продукт (5,68 г), после элюции 5-7% MeOH/CH2Cl2 и удаления летучих, выделяют в виде белого твердого вещества.
1Н ЯМР (400 мГц, CD3OD) δ 7,15-7,08 (м, 4Н), 7,05 (м, 3Н), 6,91 (м, 1Н), 4,93 (д, 1Н, неявный), 4,04 (д, 1Н, J=14 Гц), 3,95 (д, 1Н, J=14 Гц), 3,88 (д, 1Н, J=12 Гц), 3,68 (дд, 1Н, J=12, 3 Гц), 3,52-3,36 (м, 4Н), 2,27 (с, 3Н).
ВЭЖХ, время удерживания: 6,88 мин, Zorbax C-18 4,6×75 мм, 2,5 мл/мин, обнаружение при 220 нм, 8-мин градиент 0-100% В, 3 мин выдерживают при 100% В. Растворитель В: 90% МеОН/Н2О+0,2% Н3PO4.
Анал. Вычислено для С20Н24O6 LC-MS (M+Na) 383.
Пример 2

А. 2-(4'-Этилбензил)фенол
К раствору фенола (284 мг, 3 ммол) в PhMe (15 мл) при перемешивании под аргоном по каплям прибавляют 60% суспензию NaH в минеральном масле (144 мг, 3,6 ммол). Через 10 мин прибавляют раствор п-этилбензилхлорида (1,23 г, 5,3 ммол) в PhMe (2 мл), а затем реакционную смесь греют 6 час при 80°. По охлаждении летучие упаривают на роторном испарителе и остаток растворяют в 15 мл МеОН. Метанольный раствор экстрагируют 4х гексаном, а затем упаривают. Остаток растворяют в смеси EtOAc/Н2О (100 мл), доводят рН до 5 и разделяют два слоя. После сушки над Na2SO4 и удаления EtOAc получают 390 мг сырого заглавного 2-(4'-этилбензил)фенола. Преп. ВЭЖХ получают 275 мг чистого 2-(4'-этилбензил)фенола.

Суспензию 2-(4'-этилбензил)фенола (212 мг, 1 ммол), 2,3,4,6-тетра-O-ацетил-α-D-глюкопиранозилбромида (822 мг, 2 ммол) и Ag2O (232 мг, 2 ммол) в 4 мл лутидина перемешивают 14 час при 20°С. По достижении 80% конверсии (ВЭЖХ) снова добавляют 2,3,4,6-тетра-O-ацетил-α-D-глюкопиранозилбромид (411 мг, 1 ммол) и Ag2O (116 мг, 1 ммол) и перемешивают еще 24 час. Прибавляют Н2О (5 мл) и 1N водн. NaOH (2 мл) и перемешивают суспензию 16 час. Реакционную смесь дважды экстрагируют EtOAc. EtOAc вытяжки сушат Na2SO4 и упаривают. Остаток очищают преп.ВЭЖХ, получают 8,7 г конечного продукта.
1H ЯМР (400 мГц, CD3OD) δ 7,15 (м, 4Н), 7,08-7,01 (м, 3Н), 6,91 (м, 1Н), 4,91 (д, 1Н, неявный), 4,08 (д, 1Н, J=14 Гц), 3,95 (д, 1Н, J=14 Гц), 3,88 (д, 1Н, J=12 Гц), 3,68 (дд, 1Н, J=12 Гц, 3 Гц), 3,53-3,37 (м, 4Н), 2,57 (кв, 2Н, J=7 Гц), 1,18 (т, 3Н, J=7 Гц).
ВЭЖХ, время удерживания: 7,32 мин, Zorbax С-18 4,6×75 мм, 2,5 мл/мин, обнаружение при 220 нм, 8 мин градиент 0-100%В, 3 мин выдерживают при 100%В. Растворитель А: 10% МеОН/Н2О+0,2% Н3PO4. Растворитель В: 90% МеОН/Н2O+Н3PO4.
Анал. Вычислено для C21H26O6 LC-MS (M+Na) 397
Пример 3
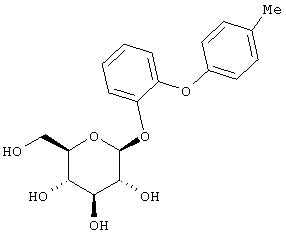
А. 2-Бензилокси-4'-метилдифениловый эфир.
Смесь 2-бензилоксифенола (5 г, 2,49 ммол), Cu(ОАс)2 (452 мг, 2,49 ммол), п-метилфенилборной кислоты (339 мг, 2,49 ммол), активированных молекулярных сит 4Å (10 г) в CH2Cl2 (8 мл) перемешивают несколько минут, прибавляют Et3N (1,26 г, 12,5 ммол), а затем пиридин (0,99 г, 12,5 ммол). Перемешивают 20 час, реакционную смесь фильтруют через целит, который промывают СН2Cl2. Фильтрат упаривают, остаток хроматографируют на силикагеле, элюент 4% EtOAc/гексан, получают 280 мг (39%) искомого заглавного 2-бензилокси-4'-метилдифенилового эфира.
В. 2-Гидрокси-4'-метилдифениловый эфир.
Раствор соединения из раздела А (280 мг, 0,96 ммол) в МеОН (50 мл) и Pd/C (30 мг) перемешивают в течение ночи при давлении Н2 1 атмосфера. Реакционную смесь фильтруют через целит, который последовательно промывают МеОН и CH2Cl2. После удаления растворителей получают 190 мг 2-гидрокси-4'-метилдифенилового эфира.
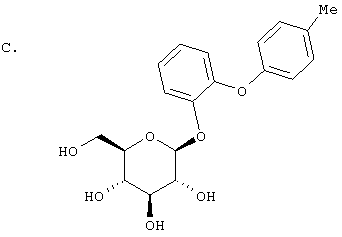
Суспензию, содержащую соединение из раздела В (94 мг, 0,47 ммол), 2,3,4,6-тетра-O-ацетил-α-D-глюкопиранозилбромид (185 мг, 0,45 ммол) и Ag2O (62 мг, 0,27 ммол) в 1 мл лутидина перемешивают 19 час при 65°. Так как реакция прошла на 50%, добавляют еще 2,3,4,6-тетра-O-ацетил-α-D-глюкопиранозилбромид (185 мг, 0,45 ммол) и Ag2O (62 мг, 0,27 ммол) и перемешивают 3 часа. По охлаждении добавляют 1N HCl (25 мл) и трижды экстрагируют EtOAc (общий объем 75 мл). Объединенные органические вытяжки промывают Н2О, водн. NaHCO3 и рассолом, сушат MgSO4. Растворитель удаляют в вакууме, получают 50 мл сырого продукта. Не очищая, его перемешивают в течение ночи в Н2О/ТГФ/МеОН (1:2:3,1 мл) вместе с LiOH (4,7 мг, 0,17 ммол). Летучие отгоняют, а остаток очищают преп. ВЭЖХ. Элюцией в 10 мин градиенте (от 30% до 90% МеОН/Н2О) с колонки с обращенной фазой YMC S5 С 18 получают после лиофилизации 26 мг конечного O-глюкозида.
1Н ЯМР (400 мГц, CD3OD) δ 2,29 (с, 3Н), 3,34-3,42 (м, 4Н), 3,67 (дд, 1Н, J=4,8 Гц, 11,3 Гц), 3,85 (дд, 1Н, J=2,2 Гц, 11,9 Гц), 4,95 (д, 1Н, J=7 Гц), 6,82-7,29 (м, 8Н).
ВЭЖХ, время удерживания: 6,47 мин, 93% чистота, Zorbax C-18 4,6х75 мм, 2,5 мл/мин, обнаружение при 220 нм, 8 мин градиент 100% В 3 мин при 100% В. Растворитель А: 10% МеОН/Н2О+0,2% Н3PO4. Растворитель В: 90% МеОН/Н2О+0,2% Н3PO4.
Анал. Вычислено для С19H22O7 MS низкого разрешения [M+Na]=385, [M+NH4]=380, [2M+NH4]=742, [M-H]=361, [2М-Н]=723.
Пример 4


Суспензию 2-нитрофенола (1,67 г, 12 ммол), 2,3,4,6-тетра-O-ацетил-α-D-глюкопиранозилбромида (4,5 г, 10,9 ммол) и Ag2O (1,6 г, 7,1 ммол) в 20 мл лутидина перемешивают 19 час при 20°. К реакционной смеси прибавляют 250 мл СН2Cl2 и фильтруют через целит. После промывания целита дополнительным количеством CH2Cl2 объединенные органические фракции упаривают, получают желтый осадок. Затирание (4Х) с МеОН, растворяющим большинство примесей, дает 4,15 г искомого заглавного 2-нитрофенил-О-глюкозида.

Неочищенное соединение из раздела А (2 г), частично растворенное в 35 мл смеси ТГФ/DCE/MeOH (2:2:3), содержащей 0,2 г 10%Pd/C, перемешивают 5 час при давлении Н2 1 атм и фильтруют через целит. Фильтрат, включая МеОН, которым промывают целит, упаривают, получают 1,8 г заглавного о-анилин-O-глюкозида.
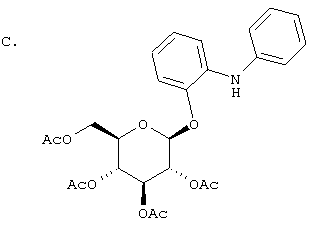
Смесь соединения из раздела В (100 мг, 0,23 ммол), Pd(OAc)2 (2,5 мг, 0,01 ммол), BINAP (0,8 мг, 0,0014 ммол) и фенилтрифлата (51 мг, 0,23 ммол) перемешивают 5 мин в PhMe (1 мл), содержащем 1 каплю Et3N, и добавляют CsCO3 (103 мг, 0,32 ммол). При нагревании до 102° светло-желтый раствор краснеет. Через 15 час на хроматограмме (ВЭЖХ) имеется новый пик плюс остаточные пики исходных. Попытки повысить конверсию путем добавления других компонентов реакции были безуспешны. Реакционную смесь по охлаждении до 20° разбавляют EtOAc и фильтруют через целит, фильтрат упаривают, а остаток хроматографируют на силикагеле, используя в качестве элюента EtOAc/гексан (3:7). Получают 10 мг искомого заглавного продукта.

Тетраацетат из раздела С (10 мг, 0,019 ммол) перемешивают в течение ночи в смеси Н2О/ТГФ/МеОН (1:2:3, 0,6 мл) с LiOH (1 мг, 0,023 ммол). Летучие удаляют после нейтрализации 1N HCl. Остаток очищают преп. ВЭЖХ на колонке YMC S5 С18 с обращенной фазой элюцией в 10 мин градиенте (от 30% до 90% MeOH/H2O), после лиофилизации получают 3 мг конечного глюкозида.
1H ЯМР (500 мГц, CD3OD) δ 3,37-3,52 (м, 4Н), 3,72 (дд, 1H, J=5 Гц), 3,89 (дд, 1Н, J=2 Гц), 4,74 (д, 1Н, J=8 Гц), 6,77-7,28 (м, 9Н).
ВЭЖХ, время удерживания: 6,2 мин, 100% чистота, Zorbax C-18 4,6х75 мм, 2,5 мл/мин, детектирование при 220 нм, 8 мин градиент 0-100 В 3 мин при 100% В. Растворитель А: 90% МеОН/Н2О+0,2% Н3PO4. Растворитель В: 90% МеОН/Н2О+0,2% Н3PO4.
Анал. Вычислено для C18H21NO6 Низк. Разр. MS [M+H]=348
Пример 5

А. 2-Гидрокси-4'-дифенилсульфид
60% NaH в минеральном масле (260 мг, 6,5 ммол) дважды промывают пентаном и суспендируют при перемешивании под аргоном в ТГФ (10 мл) при 0°, прибавляя к нему чистый о-бромфенол (500 мкл, 746 мг, 4,3 ммол). После перемешивания в течение 1 час при 20° раствор охлаждают до -78° и прибавляют 1,28 М трет.-BuLi/гексан (3,7 мл, 4,7 ммол). Через 10 мин добавляют 3 мл раствора п-толилдисульфида (1,06 г, 4,3 ммол) в ТГФ. Перемешивают 10 мин, доводят температуру до 0° и выдерживают при этой температуре 1 час. К реакционной смеси добавляют 2 мл нас. водн. NH4Cl, а затем 150 мл EtOAc. EtOAc фазу промывают нас. водн. NH4Cl, сушат MgSO4 и упаривают, получают желтое масло (910 мг). Хроматографией на силикагеле (элюент гексан/EtOAc 5:1) получают 2-гидрокси-4'-дифенилсульфид (555 мг) в виде прозрачного масла.
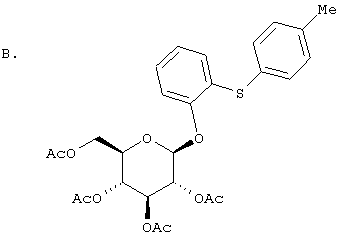
Соединение из раздела А (300 мг, 1,39 ммол), 2,6-дитрет.-бутил-4-метилпиридин (387 мг, 1,88 ммол), 2,3,4,6-тетра-O-ацетил-α-D-глюкопиранозилбромид (661 мг, 1,61 ммол) в 9 мл CH2Cl2 перемешивают до гомогенного состояния и охлаждают до 0°. К холодному раствору прибавляют AgOTf (456 мг, 1,88 ммол), перемешивают 2,5 час и прибавляют дополнительное количество 2,3,4,6-тетра-O-ацетил-α-D-глюкопиранозилбромида (274 мг, 0,66 ммол) и AgOTf (157 мг, 0,66 ммол). Через 2 час суспензию наносят на колонку с силикагелем, которую элюируют сначала смесью EtOAc/гексан. Первым элюируется минорный нежелательный α-аномер (99 мг), а затем искомый заглавный тетраацетокси-β-O-глюкозид (660 мг).

Тетраацетат из раздела В (525 мг, 0,96 ммол) перемешивают 6 час в смеси Н2O/ТГФ/МеОН (1:2:3, 9,6 мл)с LiOH (40 мг, 1 ммол). Нейтрализуют 1N HCl и удаляют летучие. 20% остатка очищают преп. ВЭЖХ на колонке YMC S5 С18 с обращенной фазой 10 мин градиентной элюцией (от 50% до 90% МеОН/Н2О), после лиофилизации получают 24 мг конечного глюкозида.
1Н ЯМР (400 мГц, CD3OD) δ 7,29 (м, 2Н), 7,18 (м, 4Н), 6,88 (м, 2Н), 4,98 (д, 1Н, J=7,0 Гц), 3,88 (м, 1Н), 3,70 (дд, 1Н, J=4,8 Гц, 11,8 Гц), 3,43 (м, 4Н), 2,34 (с, 3Н).
ВЭЖХ: время удерживания 6,85 мин; HI=100%; колонка YMC S3 ODS 4,6×50 мм; 2,5 мл/мин, детектирование при 220 нм, 0-100%В за 8 мин, выдерживают 5 мин (при 100%В). Растворитель А: 10% МеОН/Н2O+0,2% Н3PO4. Растворитель В: 90% МеОН/Н2O+0,2% Н3PO4.
Анал. Вычислено для C19H22O6S LC-MS: [М+Н] 379, [M+Na] 401, [2M+Na] 779.
Примеры 6-99
По методикам, аналогичным приведенным в Примерах 1-5, получают соединения по изобретению, приведенные в нижеследующей таблице.

*(R6=Н, если не указано иначе)




*(R6=Н, если не указано иначе)

| название | год | авторы | номер документа |
|---|---|---|---|
| С-АРИЛГЛЮКОЗИДНЫЕ ИНГИБИТОРЫ SGLT2 | 2000 |
|
RU2262507C2 |
| С-АРИЛ ГЛЮКОЗИДНЫЕ SGLT2 ИНГИБИТОРЫ И СПОСОБ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2800510C1 |
| С-АРИЛ ГЛЮКОЗИДНЫЕ SGLT2 ИНГИБИТОРЫ И СПОСОБ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2746132C1 |
| СПОСОБЫ ПОЛУЧЕНИЯ И ИСПОЛЬЗОВАНИЯ ИНГИБИТОРА SGLT2 | 2013 |
|
RU2643764C2 |
| C-АРИЛ ГЛЮКОЗИДНЫЕ SGLT2 ИНГИБИТОРЫ И СПОСОБ ИХ ПРИМЕНЕНИЯ | 2003 |
|
RU2337916C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ, СОДЕРЖАЩАЯ ИНГИБИТОР SGLT2 | 2008 |
|
RU2489151C2 |
| ИНГИБИТОРЫ ДИПЕПТИДИЛПЕПТИДАЗЫ IV НА ОСНОВЕ КОНДЕНСИРОВАННЫХ ЦИКЛОПРОПИЛПИРРОЛИДИНОВ И СПОСОБ ИХ ПРИМЕНЕНИЯ | 2001 |
|
RU2286986C2 |
| ЛИГАНДЫ ТИРОИДНОГО РЕЦЕПТОРА - ПРОИЗВОДНЫЕ АНИЛИНА | 2001 |
|
RU2260586C2 |
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ИНГИБИТОРЫ КОТРАНСПОРТЕРОВ НАТРИЯ-ГЛЮКОЗЫ 1 И 2, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2669921C2 |
| PPAR-ПОДДЕРЖИВАЮЩИЕ СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ МЕТАБОЛИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2014 |
|
RU2687490C2 |
Изобретение относится к О-арилглюкозидным ингибиторам SGLT2 формулы I

где Y обозначает
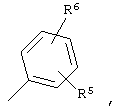


А обозначает -O(CH2)m, S, NH(СН2)m или (СН2)n, где n обозначает 0-3, a m обозначает 0-2; R1-R6 определены выше, а также к фармацевтической композиции на их основе и способам лечения диабета типа II и микро- и макрососудистых диабетических осложнений. 4 н. и 11 з.п. ф-лы, 1 табл.
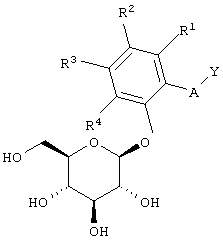
 ,
,  ,
, 
где Y обозначает R1, R2, R3 и R4 одинаковы или различны и независимо выбираются из водорода, ОН, OR7, низшего алкила или галогена, или два из R1, R2, R3 и R4 вместе со связанными с ними атомами углерода могут образовывать аннелированный шестичленный гетероцикл, который содержит один атом N;
R5 и R6 одинаковы или различны и независимо выбираются из водорода, ОН, OR7, -ОСН2-фенила, низшего алкила, фенила, CF3, стиренила, -OCF3, галогена, -SR7, -SO2R7, -OCH2CO2R7, -OCH2CO2H, -OCH2CONR8R8, -OCH2CH2NR8R8 или R5 и R6 вместе со связанными с ними атомами углерода образуют аннелированный шестичленный карбоцикл
R7 обозначает низший алкил;
R8 обозначает алкил;
А обозначает O(CH2)m, S, NH(CH2)m или (СН2)n, где n обозначает 0-3, а m обозначает 0-2, или его фармацевтически приемлемые соли или его стереоизомеры,
при следующих условиях: когда А обозначает CH2 и Y обозначает
 и
и
1) когда R1 обозначает ОН и R3 обозначает низший алкил, по меньшей мере, один из R1, R4, R5 и R6 не обозначает водород;
2) когда R2 и R3 обозначают ОН, по меньшей мере, один из R1, R4, R5 и R6 не обозначает водород;
3) когда R2 обозначает метил, R5 обозначает ОН и R6 обозначает низший алкил, по меньшей мере, один из R1, R3 и R4 не обозначает водород; и
4) когда R2 обозначает хлор, по меньшей мере, один из R1, R3, R4, R5 и R6 не обозначает водород и
когда А обозначает связь, по меньшей мере, один из R1, R3, R4, R5 и R6 не является водородом.
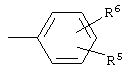 .
.
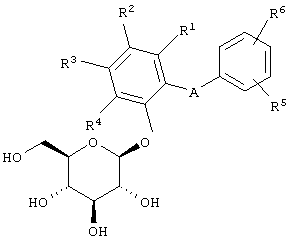
где А обозначает СН2 или О или S.

где R1 обозначает водород, галоген или низший алкил, или R1 и R4 независимо обозначают Н или алкил;
R6 обозначает водород, низший алкил, -OR7, CHF2O, -OCF3 или -SR7.



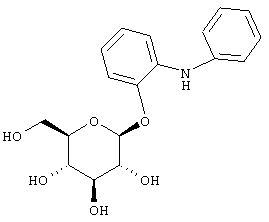


*R6 обозначает Н, если не указано иначе
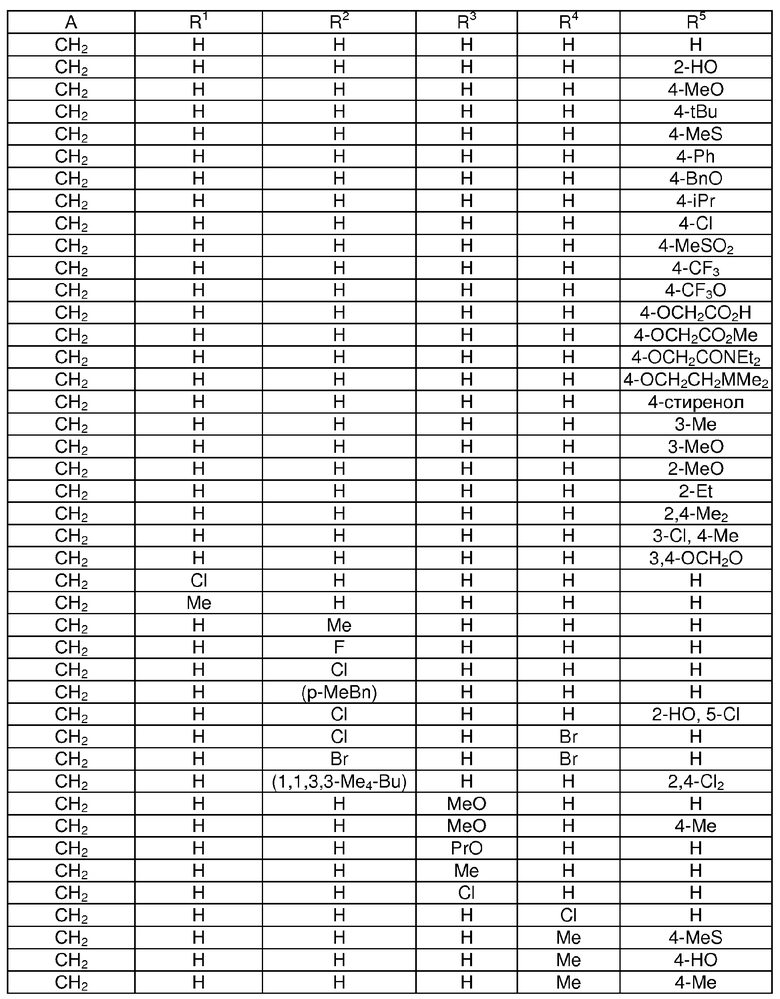





*R6 обозначает H, если не указано иначе

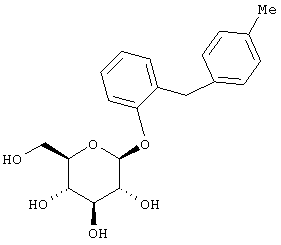


*R6 обозначает H, если не указано иначе.




*R6 обозначает Н, если не указано иначе

| T.H.Bembry, G.Powell | |||
| The Synthesis of phenolic glycosides | |||
| J | |||
| Am | |||
| Chem | |||
| Soc | |||
| Водопроводный кран | 1925 |
|
SU1942A1 |
| EP 0598359, A1, 25.05.1994 | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| ПРОИЗВОДНЫЕ ЦИКЛОГЕКСАНА ИЛИ ТЕТРАГИДРОПИРАНА, ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ИЛИ ГИДРАТЫ, ИЛИ СОЛЬВАТЫ ЭТИХ СОЕДИНЕНИЙ, ИЛИ ИХ СОЛЕЙ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ И ФУНГИЦИДНОЕ СРЕДСТВО | 1992 |
|
RU2084439C1 |
Авторы
Даты
2006-02-10—Публикация
2001-03-29—Подача