Настоящее изобретение относится к неизвестному ранее классу соединений, включающих в себя новые ингибиторы матриксной металлопротеиназы, которые представляют собой 1,3,2-осазафосфациклоалкансодержащие гидроксамовые кислоты, карбоновые кислоты, фосфоновые кислоты или тиолы, к фармацевтическим композициям, содержащим указанные соединения, способам лечения пациентов указанными соединениями и к использованию подобных соединений для получения лекарственного средства. В частности, данные соединения являются ингибиторами матриксных металлопротеиназ, принимающих участие в распаде ткани. Некоторые из соединений данного изобретения являются также ингибиторами высвобождения из клеток фактора-α опухолевого некроза (TNF-α).
Матриксные металлопротеиназы (MMP) представляют собой семейство цинковых эндопептидаз, проявляющих протеолитическую активность по отношению к большинству, если не ко всем, составляющим внеклеточного матрикса, таким, как интерстициальный и основной мембранный коллагены, фибронектин и ламинин. Они играют ключевую роль как в физиологическом, так и патологическом распаде ткани.
Было охарактеризовано, по меньшей мере, 17 различных и тем не менее высокогомологичных MMP-видов. Они разделяют каталитический домен с VAAHEXGHXXGXXH мотивом, отвечающим за лигирование цинка, который важен для каталитической функции. Члены ММР семейства отличаются друг от друга структурно за счет наличия или отсутствия дополнительных доменов, которые вносят вклад в активности, такие, как субстратная специфичность, ингибиторное связывание, матриксное связывание и клеточно-поверхностная локализация. [H.Birkedal-Hansen, W.G.Moore, M.K.Bodden, C.J.Windsor, B.Birkedal-Hansen, A.DeCarlo: Crit. Rev. Oral Biol. Med. (1993), 4, 197-250, и A.F.Chambers, L.M.Matristan: J. Natl. Cancer Inst. (1997) 89 (17), 1260-1270]. Существует три основных группы ММР, идентифицируемых по их субстратным предпочтениям: коллагеназы деградируют фибриллярный коллаген, стромелизины предпочитают в качестве субстратов протеогликаны и гликопротеины, а желатиназы особенно эффективны при деградации нефибриллярных и денатурированых коллагенов (желатина).
Кроме того, считается, что ММР важны при процессинге, или секреции, биологически важных клеточных медиаторов, таких, как TNF-α, и посттрансляционном протеолитическом процессинге, или выделении, биологически важных белков мембраны, таких, как обладающий низким сродством IgE рецептор CD 23 (для более полного списка смотри N.M.Hooper et al.: Biochem. J. (1997), 321, 265-279).
Потенциальные терапевтически признаки ММР ингибиторов обсуждались в литературе [например, T.H.Vu, Z.Werb. (1998) (в: Matrix Metalloproteinases. 1998. Edited by W.C.Parks and R.P.Mecham. Pp.115-148. Academic Press. ISBN 0-12-545090-7); D.E.Mullins et al.: Biochem. Biophys. Acta (1983), 695, 117-214; B.Henderson et al.: Drugs of the Future (1990), 15, 495-508; R.Reich et al.: Cancer Res. (1988), 48, 3307-3312]. Считается, что соединения, обладающие свойством ингибировать матриксные металлопротеиназы, потенциально полезны, но не ограничены, лечением или профилактикой состояний, включающих распад и воспаление ткани, например, ревматоидный артрит, остеоартрит, нарушения остеогенеза, такие, как остеопороз, периодонтит, гингивит, изъязвление эпидермиса роговицы или желудка, старение кожи и опухолевые метастазы, опухолевая инвазия и рост опухоли. Кроме того, ММР ингибиторы имеют потенциальную ценность для лечения нейровоспалительных расстройств, включая расстройства, при которых происходит распад миелина, например рассеянный склероз, а также при терапии зависящих от ангиогенеза заболеваний, которые включают в себя артритные состояния и рост солидных опухолей, а также псориаз, пролиферативную ретинопатию, реваскулярную глаукому, глазные опухоли, ангиофибромы и гемангиомы. Однако сравнительные вклады индивидуальных ММР в любое из приведенных выше болезненных состояний понятны еще не до конца.
TNF-α представляет собой цитокин, который производится в виде 28-kDa предшественника и высвобождается в активной 17-kDa форме. Эта активная форма может служить посредником в большом количестве вредных воздействий in vivo, включая воспаление, лихорадку, сердечно-сосудистые воздействия, кровоизлияния, коагуляцию и ревматические реакции, похожие на наблюдаемые при острых инфекциях и шоковых состояниях. Хроническое введение TNF-α может вызвать кахексию и потерю аппетита; накопление избытка TNF-α может привести к смерти. Поэтому считается, что соединения, ингибирующие производство или действие TNF-α, потенциально полезны для лечения или профилактики многих воспалительных, инфекционных, иммунологических и злокачественных заболеваний. Такие заболевания включают в себя, но не ограничиваются ими, септический шок, гемодинамический шок, септический синдром, постишемическую реперфузионную травму, болезнь Крона, микобактериальную инфекцию, менингит, псориаз, застойную сердечную недостаточность, рак, ревматоидный артрит и рассеянный склероз.
TNF-α конвертаза представляет собой металлопротеиназу, принимающую участие в биосинтезе TNF-α. Поскольку избыточное производство TNF-α было отмечено в нескольких болезненных состояниях, характеризуемых ММР-опосредованным распадом ткани, включая рассеянный склероз, артрит и рак, соединения, которые ингибируют как ММР, так и производство TNF-α, могут обладать особыми преимуществами при лечении или профилактике заболеваний или состояний, в которых задействованы оба механизма.
Многие из известных ММР ингибиторов являются производными пептидов, основанными на природных аминокислотах, и представляют собой аналоги участков расщепления в природных субстратах MMPs. Прочие известные ММР ингибиторы являются менее пептидными по структуре и могут быть рассмотрены как псевдопептиды или пептидомиметики, например сульфонамиды. Обычно такие соединения содержат группу, связывающую цинк, которая наиболее часто представляет собой гидроксамовую кислоту, обращенную гидроксамовую кислоту, карбоновую кислоту, сульфогидрил, и окисленные фосфорные группы (например, фосфиновую кислоту и фосфонамиды, включая аминофосфоновую кислоту).
Несмотря на то, что известно множество ММР ингибиторов с потенциальной активностью in vitro, многие из них оказались непригодными для дальнейшей разработки в качестве лекарственных средств, поскольку у них не доставало какой-либо полезной активности при пероральном введении в фармацевтически приемлемых дозах. Хотя известно, что на пероральную биодоступность влияет ряд факторов, разработка ферментных ингибиторов с высокой пероральной биодоступностью далека от направленной. Нахождение ряда соединений, допускающих хороший баланс между действительным уровнем активности, растворимостью в воде, пероральной абсорбцией и благоприятными фармакокинетическими свойствами, представляет собой постоянную проблему в данной области, так как эти свойства могут изменяться непредсказуемым путем в зависимости от структуры. Идентификация ММР ингибиторов, обладающих подобными свойствами, остается задачей, требующей решения.
В предшествующей области исследовали простые пептидные соединения, а также линейные и циклические сульфонамидные соединения, например, EP-A-0489577, WO 96/16931, WO 96/33991, WO 97/44315 и WO 00/09485. В патентной публикации предшествующей области существует только один пример, в котором описаны простые линейные фосфинамидные соединения [WO 98/08853]. Эти соединения структурно отличаются от циклических соединений общей формулы (I). В предшествующей области описаны лишь 1,3,2-оксазафосфороциклоалканы с простым фенильным и алкильным заместителями, однако, они не содержали необходимой гидроксамовой кислоты или других групп, связывающих цинк (например, PL 149593, FR 2567129, Izv. Akad. Nauk., Ser. Khim (1995) (11), 2241-9). В настоящее время неожиданно было найдено, что новые соединения на основе 1,3,2-оксазафосфациклоалканов общей формулы (I) настоящего изобретения являются эффективными ММР ингибиторами. Предпочтительные соединения настоящего изобретения проявляют от наномолярной до микромолярной эффективности при ингибировании ММР, таких, как ММР-13, ММР-9 и ММР-3.
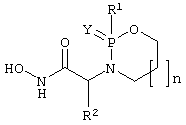
Настоящее изобретение относится к новому классу соединений общей формулы I
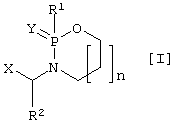
в которой Y представляет О или S;
n равно 1, 2, 3 или 4;
Х представляет гидроксамовую кислоту, карбоновую кислоту, фосфоновую кислоту, ацетилтиометильную группу или меркаптометильную группу;
R1 представляет
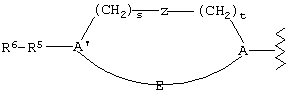
в которой Е при наличии представляет связь или необязательно замещенный метилен или этилен;
s и t независимо равны 0, 1, 2 или 3;
А и А' независимо представляют связь или насыщенный или ненасыщенный, необязательно замещенный циклический или гетероциклический углеводородный би- или трирадикал;
Z представляет связь, O, S, C(O), C(O)NR7, NR7C(O) или NR7, где R7 представляет водород, гидрокси, разветвленный или линейный, насыщенный или ненасыщенный, необязательно замещенный углеводородный радикал;
R5 представляет связь, алкановый или алкеновый бирадикал, один или более эфирных радикалов (R-O-R') или аминные бирадикалы (R-N-R'), где R и R' независимо представляют алкановые или алкеновые бирадикалы с содержанием С от 0 до 3;
R6 представляет водород, гидрокси, галоген, циано, нитро, разветвленный или линейный, насыщенный или ненасыщенный, необязательно замещенный углеводородный радикал, ненасыщенный, необязательно замещенный, циклический или гетероциклический углеводородный радикал, NR8R9, C(O)NR8R9, C(O)R8, CO(O)R8, S(O)2R9, где каждый из R8 и R9 независимо представляет водород, галоген, разветвленный или линейный, насыщенный или ненасыщенный, необязательно замещенный углеводородный радикал;
R2 представляет водород, (С1-8)алкил, (С2-6)алкенил, (С3-8)циклоалкил, арил(С0-6)алкил или гетероарил(С0-6)алкил;
при условии, что если все А, А', Z и R5 представляют связи, а s и t оба равны 0 (ноль), то R6 не является водородом;
или к их солям, гидратам или сольватам.
Как использовано в данном описании, если не определено наоборот, следующие термины имеют указанные значения.
«Алкил» относится к линейной или разветвленной алкильной группе, состоящей только из углерода и водорода, не содержащей ненасыщенности и имеющей указанное число атомов углерода, включая, например, метил, н-пропил, изобутил, трет-бутил, гексил и додецил.
«(С2-С6)алкенил» относится к линейной или разветвленной алкенильной группе, содержащей от 2 до 6 атомов углерода, содержащей, по меньшей мере, одну двойную связь либо Е, либо Z стереохимии, где это применимо. Данный термин включал бы в себя, например, винил, аллил, 1- и 2-бутенил и 2-метил-2-пропенил.
Подразумевается, что термин «алкокси» обозначает радикал формулы OR, в которой R представляет определенный выше алкил, например метокси, этокси, пропокси, бутокси и т.д.
Подразумевается, что термин «алкоксикарбонил» обозначает радикал формулы -COOR, в котором R представляет определенный выше алкил, например метоксикарбонил, этоксикарбонил, н-пропоксикарбонил, изопропоксикарбонил и т.д.
Подразумевается, что термин «насыщенный циклический углеводород» обозначает циклические соединения, необязательно конденсированные бициклические кольца, содержащие водород и углерод, которые являются насыщенными, такие, как циклопропан, циклобутан, циклопентан, циклогексан, циклогептан, циклооктан, гидроиндан и декалин.
Подразумевается, что термин «ненасыщенный циклический углеводород» обозначает циклические соединения, необязательно конденсированные бициклические кольца, содержащие водород и углерод, в которых одна или более связей углерод-углерод является ненасыщенной, такие, как циклопентен, циклогексен, циклогексадиен, циклогептен, бензол, нафтен и 1,4-дигидронафтен, индан и инден.
Подразумевается, что термин «гетероциклический углеводород» обозначает насыщенные или ненасыщенные циклические соединения, состоящие из водорода, углерода и одного или более гетероатомов, выбранных из O, S, N и Р, такие, как пиррол, фуран, тиофен, имидазол, оксазол, тиазол, пиразол, пирролидин, пиридин, пиримидин, тетрагидротиофен, тетрагидрофуран, пиперидин, пиперазин, фосфалан, фосфоринан и фосфорепан.
«Арил» относится к фенилу или нафтилу.
«Циклоалкил» обозначает насыщенную циклическую группу, содержащую от 3-8 атомов углерода, и включает в себя, например, циклопропил, циклопентил, циклогексил и циклооктил.
«Гетероарил» относится к пиридилу, индолилу, тиенилу или имидазолилу.
Если в контексте, в котором это имеет место, не указано иначе, то термин «замещенный», используемый здесь к любой из указанных групп, означает замещение заместителями вплоть до четырех, каждый из которых независимо может представлять (С1-6)алкокси, (С1-6)алкил, фенил, гидрокси, тио, (С1-6)алкилтио, амино, галоген (включая фтор, хлор, бром и йод), циано, цианометил, трифторметил, нитро, карбокси, -CONH2, галогеналкил, алкиламино, гидроксиалкил, алкилкарбонил, -CONHR12 или -CONR12R12, где R12 представляет (С1-6)алкильную группу, или остаток природной α-аминокислоты.
Соли соединений данного изобретения можно получить при действии оснований. Такие соли включают в себя соли, полученные с неорганическими или органическими основаниями, например соли металлов, такие, как соли натрия или калия, соли щелочноземельных металлов, такие, как соли магния или кальция, и соли органических аминов, такие, как соли морфолина, пиперидина, диметиламина или диэтиламина.
В том случае, когда соединения согласно изобретению содержат основные группы, соли можно получить также с фармацевтически приемлемыми неорганическими или органическими кислотами, такими, как хлористоводородная, бромистоводородная и йодистоводородная кислота, фосфорная кислота, серная кислота, азотная кислота, п-толуолсульфокислота, метансульфокислота, муравьиная кислота, уксусная кислота, пропионовая кислота, лимонная кислота, винная кислота, янтарная кислота, бензойная кислота, малеиновая кислота, причем данные примеры рассматриваются как не ограничивающие изобретение.
В соединениях в соответствии с изобретением имеются хиральные центры вследствие наличия асимметрического атома углерода и асимметрического атома фосфора. Наличие нескольких хиральных центров приводит к появлению ряда диастереоизомеров с R или S стереохимией каждого из хиральных центров. Таким же образом, существование углерод-углеродных двойных связей и циклических систем приводит к наличию геометрических и стереоизомерных форм. Необходимо понимать, что общая формула (I) и (если не указано иначе) все остальные формулы в данном описании включают в себя все подобные изомеры, в чистом виде или в виде их смесей.
В соединениях изобретения предпочтительной стереохимией, в общем виде, является следующая: С атом, содержащий R2 группу -(R), но рассматриваются также смеси, в которых преобладают указанные выше конфигурации. Без ограничения общности упомянутого выше.
Предпочтительными соединениями формулы (I) являются соединения, в которых Х представляет CONHOH. Более предпочтительными соединениями формулы (I) являются соединения, в которых Х представляет CONHOH, n=1 или 2, а Y представляет кислород.
В предпочтительном способе воплощения R1 выбирают из группы, состоящей из алкоксифенила, феноксифенила, необязательно замещенного галогеном, галогензамещенного углеводородного радикала, или циано, фенилалкила или нафтилалкила, оба из которых необязательно замещены галогеном, фенила, необязательно замещенного галогеном или нитро, углеводородного радикала, бифенила, необязательно замещенного галогеном, бензилфеноксила, фенил-(NH)-C(O)фенила, необязательно замещенного галогеном, или циано и метокси.
Примеры конкретных групп R1 включают в себя 4-метоксифенил, 4-(4-хлорфенокси)фенил, 4-(4-бромфенокси)фенил, 4-(4-трифторметилфенокси)фенил, 4'-бром-4-бифенилил, N-(4-хлорбензоил)-4-аминофенил, 4-нитрофенил, N-бензоил-4-аминофенил, 4-феноксифенил.
В предпочтительном способе воплощения R2 выбирают из группы, состоящей из водорода, (С1-8)алкила, (С2-6)алкенила и арил(С0-6)алкила.
Примеры конкретных R2 групп включают в себя водород, изопропил, аллил, изобутил, н-бутил, н-октил и бензил.
Примерами соединений изобретения являются следующие.
(±)-2-(4-Хлорфенокси)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-(4-Хлорфенокси)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-2-[(4-Бромфенил)метил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-[(4-Бифенилил)метил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-(4-Бифенилил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-(4-Бифенилил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-2-Гептил-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-Гептил-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-2-Оксо-2-[4-(фениламино)фенил]-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-Оксо-2-фенил-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-Оксо-2-фенил-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-2-Оксо-2-фенил-1,3,2-оксазафосфоронан-3-ацетогидроксамовая кислота.
(±)-α-Бутил-2-оксо-2-фенил-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-α-Бутил-2-оксо-2-фенил-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-2-(4-Метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-(4-Метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-2-(4-Метоксифенил)-2-оксо-1,3,2-оксазафосфоронан-3-ацетогидроксамовая кислота.
(αR)-2-(4-Метоксифенил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1).
(αR)-2-(4-Метоксифенил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2).
(±)-α-Бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 1).
(±)-α-Бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 2).
(±)-α-Бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1).
(±)-α-Бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2).
(±)-α-Бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота (диастереомеры 1).
(±)-α-Бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота (диастереомеры 2).
(±)-α-Аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 1).
(±)-α-Аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 2).
(±)-α-Аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1).
(±)-α-Аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2).
(αR)-2-(4-Метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1, соединение 130).
(αR)-2-(4-Метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2).
(αS)-2-(4-Метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1).
(αS)-2-(4-Метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2).
(±)-2-(4-Метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1).
(±)-2-(4-Метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2).
(±)-2-(4-Метоксифенил)-α-пропил-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 1).
(±)-2-(4-Метоксифенил)-α-пропил-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 2).
(±)-2-(4-Метоксифенил)-α-октил-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1).
(±)-2-(4-Метоксифенил)-α-октил-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2).
(αR)-2-(4-Метоксифенил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1).
(αS)-2-(4-Метоксифенил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1).
(αS)-2-(4-Метоксифенил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2).
(±)-2-Оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-Оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-2-Оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота.
(±)-α-Аллил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 1).
(±)-α-Аллил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 2).
(αR)-α-(2-Метилпропил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1).
(αR)-α-(2-Метилпропил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2).
(αR)-α-(2-Метилэтил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1).
(αR)-α-(2-Метилэтил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2).
(±)-α-Бутил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1).
(±)-α-Бутил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2).
(±)-α-Октил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1).
(±)-α-Октил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2).
(±)-2-Оксо-2-(2-фенилэтил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-(4-Метоксифенил)-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота.
(±)-2-Оксо-2-фенил-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота.
(±)-2-Гептил-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота (соединение 159).
(αR)-2-(4-Бифенилил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2).
(±)-2-[4-(4-Хлорфенилокси)фенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-2-[4-(4-Хлорфенилокси)фенил]-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота.
(αR)-2-[4-(4-Хлорфенилокси)фенил]-α-(2-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-(4'-Бром-4-бифенилил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-(4'-Бром-4-бифенилил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-2-(4'-Бром-4-бифенилил)-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота.
(±)-2-[2-(1-Нафтил)этил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-Фенил-2-тиоксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-Фенил-2-тиоксо-1,3,2-оксазафосфорепан-3-ацетамид.
(±)-2-Фенил-2-тиоксо-1,3,2-оксазафосфорокан-3-ацетамид.
(±)-2-[4-(4-Хлорфенилокси)фенил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-(4-Бромфенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-(4-Бромфенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-2-Оксо-2-(4-фенилметоксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-Оксо-2-(4-фенилметоксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-2-Оксо-2-(4-фенилметоксифенил)-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота.
(±)-2-[2-(4-Хлорфенокси)фенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-2-Оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-Оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(αR)-α-(2-Метилэтил)-2-оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1).
(αR)-α-(2-Метилэтил)-2-оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2).
(±)-2-[4-(4-Бромфенокси)фенил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота.
(±)-2-[4-(4-Бромфенокси)фенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-2-(4-Нитрофенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-2-(N-(4-хлорбензоил)-4-аминофенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота.
(±)-2-(N-Бензоил-4-аминофенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота
и соответствующие карбоновые кислоты.
Соединения настоящего изобретения можно получить рядом способов, которые хорошо известны специалистам в области органического синтеза. Соединения настоящего изобретения можно синтезировать с использованием методов, указанных ниже, а также способами, известными в области синтетической органической химии, или с помощью их вариантов, понятных специалистам в данной области. Предпочтительные способы включают в себя способы, описанные далее, но не ограничиваются ими.
Новые соединения формулы (I) можно получить согласно реакциям и методикам, описанным в данном разделе. Реакции проводят в растворителях, соответствующих используемым реагентам и веществам, и подходящих для осуществляемых превращений. Кроме того, необходимо понимать, что в описанных ниже синтетических способах все предложенные условия реакций, включая выбор растворителя, атмосферу реакции, температуру реакции, продолжительность эксперимента и методики обработки, выбраны таким образом, чтобы обеспечить стандартные условия для данной реакции, что должно быть без труда понятно специалисту в данной области. Специалисту в области органического синтеза понятно, что функциональные группы, имеющиеся в различных частях выделяемой молекулы, должны быть совместимы с предложенными реагентами и реакциями. Не все из соединений формулы (I), попадающих в данный класс, могут оказаться совместимыми с некоторыми условиями реакций, которые необходимы в некоторых из описанных способов. Такие ограничения в отношении заместителей, совместимых с условиями реакций, будут очевидны для специалиста в данной области, и можно использовать другие способы.
Соединения в соответствии с настоящим изобретением, в которых Х представляет группу гидроксамовой кислоты -CONHOH, можно получить из соединений изобретения, в которых Х представляет группу карбоновой кислоты -СООН. Этот способ включает в себя введение во взаимодействие кислоты общей формулы (II) (в данных и последующих формулах R1, R2, Y и n имеют приведенные выше значения, если конкретно не указано иначе; R13 представляет алкил; R14 представляет алкил или силил)
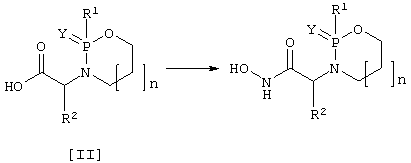
с гидроксиламином, О-защищенным гидроксиламином, N,O-дизащищенным гидроксиламином. Остальные заместители кислоты (II) могут сами быть защищены от подобной реакции, после чего снимают любые защитные группы с группы конечной гидроксамовой кислоты и с любых защищенных заместителей в R1 и R2.
Конденсацию проводят с использованием любого из множества способов образования амидных связей, известных специалисту в области органического синтеза, например способом смешанного ангидрида угольной кислоты (изобутилхлорформиат).
Соединения в соответствии с настоящим изобретением, в которых Х представляет группу гидроксамовой кислоты -CONHOH, можно также получить из сложных эфиров общей формулы (III). Такой способ включает в себя введение во взаимодействие сложного эфира общей формулы (III) с гидроксиламином или О-защищенным гидроксиламином в присутствии основания.
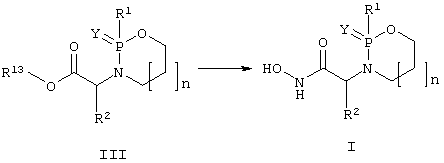
Соединения в соответствии с настоящим изобретением, в которых Х представляет группу карбоновой кислоты -СООН, можно получить из сложных эфиров общей формулы (III) при помощи основного гидролиза.
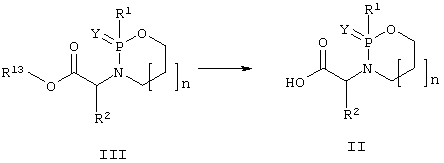
Сложные эфиры формулы (III) можно получить из фосфонилдихлоридов (IV) и аминоспиртов (V) в присутствии основания.
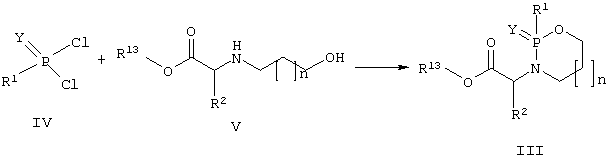
Сложные эфиры формулы (III) можно также получить из фосфонилдихлоридов (IV) и аминоспиртов (V) в присутствии основания и с последующим алкилированием промежуточного оксазафосфациклоалкана (VII) галогенэфирами (VIII) в присутствии основания.
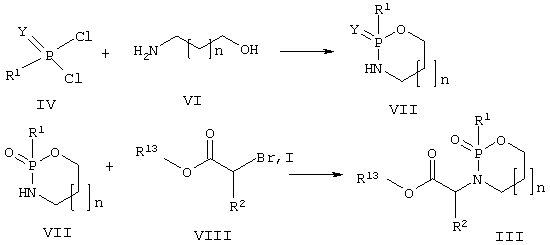
Исходные вещества (IV), (V), (VI) и (VIII) являются либо известными соединениями, либо получены известными стандартными синтетическими способами.
Соединения, содержащие фосфоновую кислоту в качестве цинксвязывающей группы (Х), можно получить алкилированием оксазафосфациклоалканов (VII) галогензамещенными алкил- или силилфосфонатами (IX) в присутствии основания с последующим снятием защиты. Снятие защиты с алкилфосфонатов осуществляют обработкой TMSI. Силилфосфонаты легко превращаются в фосфоновые кислоты при обработке водой.
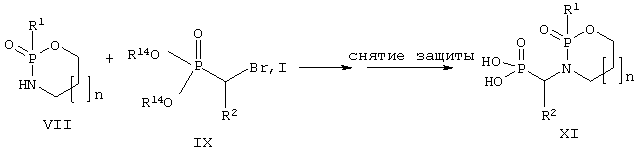
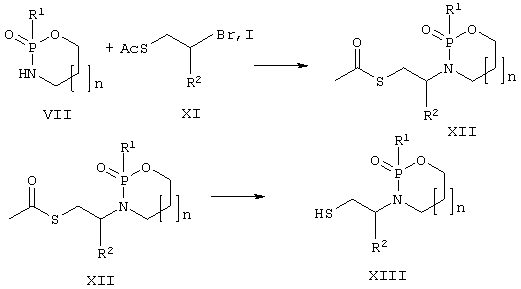
Соединения, содержащие ацетилтиометильную группу (XII) в качестве цинксвязывающей группы, можно получить алкилированием оксазафосфациклоалканов (VII) ацетилтиоэтилгалогенидом (XI) в присутствии основания. Соединения с меркаптометильной цинксвязывающей группой (XIII) можно получить при удалении ацетильной группы из соединения (XII) под действием водного основания.
Настоящие соединения предназначены для использования в фармацевтических композициях, которые полезны при лечении упомянутых выше заболеваний.
Необходимое для терапевтического эффекта количество соединения формулы I (в дальнейшем называемого активным ингредиентом), конечно, будет изменяться как для конкретного соединения, способа введения, так и для подлежащего лечению млекопитающего. Подходящая доза соединения формулы I для систематического лечения составляет от 0,1 до 200 мг/кг массы тела, при этом наиболее предпочтительная дозировка составляет от 0,2 до 50 мг/кг массы тела, при введении один или более раз в день.
Хотя активный ингредиент, такой, как соединение в соответствии с настоящим изобретением, можно вводить сам по себе в виде сырого химического соединения, предпочтительно вводить соединение данного изобретения в виде фармацевтического состава. Обычно активный ингредиент составляет от 0,1 до 100% от массы состава. Обычно разовые дозы состава содержат от 0,07 мг до 1 г активного ингредиента, предпочтительно от около 0,5 до около 500 мг активного ингредиента, более предпочтительно около 50 мг, например, для перорального введения. Для местного введения активный ингредиент предпочтительно составляет от 1 до 20% от массы состава, но активный ингредиент может составлять вплоть до 50% масса/масса. Составы, подходящие для назального или буккального введения, могут содержать от 0,1 до 20% масса/масса, например около 2% масса/масса активного ингредиента.
Под термином «разовая доза» подразумевают единичную, то есть однократную дозу, которую можно ввести пациенту и с которой легко обращаться и упаковывать, остающаяся в виде физически и химически устойчивой разовой дозы, содержащей либо активное вещество как таковое, либо его смесь с твердыми или жидкими фармацевтическими разбавителями или носителями.
Поэтому составы для медицинского использования как для ветеринарии, так и для человека, содержат активный ингредиент в сочетании с фармацевтически приемлемым носителем и необязательно с другим терапевтическим ингредиентом(и). Носитель(ли) должен быть «приемлемым» в смысле совместимости с другими ингредиентами состава и не причинять вреда его реципиенту. Составы содержат носители в форме, подходящей для перорального, глазного, ректального, парентерального (включая подкожное, внутримышечное и внутривенное), чрескожного, внутрисуставного, местного, назального или буккального введения.
Составы удобно представлять в виде разовой лекарственной формы и можно получать их любым способом, хорошо известным в области фармации. Все способы включают в себя стадию соединения активного ингредиента с носителем, который состоит из одного или более вспомогательных ингредиентов. Как правило, составы готовят путем однородного и тонкого смешивания активного ингредиента с жидким носителем, или мелко измельченным твердым носителем, или обоими, а затем при необходимости формирования продукта в желательный состав. Составы настоящего изобретения, подходящие для перорального введения, могут иметь форму отдельных единиц, таких, как капсулы, саше, таблетки или лепешки, каждая из которых содержит заранее определенное количество активного ингредиента; в форме порошка или гранул; в форме раствора или суспензии в водной жидкости или неводной жидкости или в форме эмульсии масло-в-воде или эмульсии вода-в-масле. Активный ингредиент можно также вводить в виде болюса, электуария или пасты.
Составы для ректального введения могут быть в виде суппозитория, включающего активный ингредиент и носитель, такой, как масло какао, или в виде клизмы.
Составы, подходящие для парентерального введения, обычно содержат стерильный препарат активного ингредиента в масле или воде, предпочтительно изотоничный с кровью реципиента.
Составы, подходящие для внутрисуставного введения, могут находиться в форме стерильного водного препарата активного ингредиента, который может быть в микрокристаллическом виде, например в виде водной микрокристаллической суспензии.
Для представления активного ингредиента как для внутрисуставного, так и для глазного введения, можно также использовать липосомные составы или биоразлагаемые полимерные системы.
Составы, подходящие для местного введения, включая обработку глаза, включают в себя жидкие или полужидкие препараты, такие, как жидкие мази, примочки, гели, аппликации, эмульсии масло-в-воде или вода-в-масле, такие, как кремы, мази или пасты; или растворы или суспензии, такие, как капли.
Составы, пригодные для введения в нос или буккальную полость, включают в себя порошок, самораспыляющиеся составы и спреи, такие, как аэрозоли и пульверизаторы. Помимо упомянутых выше ингредиентов, составы данного изобретения могут включать в себя один или более дополнительных ингредиентов.
Кроме того, композиции могут содержать другие терапевтически активные соединения, обычно применяемые при лечении.
Далее изобретение иллюстрировано следующими общими методиками, получениями и примерами.
Общие методики, получения и примеры
Представленные в качестве примера соединения перечислены в таблице 4, представленные в качестве примера соединения общей формулы (II) - в таблице 3, промежуточные соединения общей формулы (III) - в таблице 2, а промежуточные соединения общей формулы (VII) - в таблице 1.
Все температуры плавления не уточнялись. В спектрах ядерного магнитного резонанса (ЯМР) 1Н (300 МГц) и 13С (75,6 МГц) величины химических сдвигов (δ) (в м.д.) приведены, если не указано иначе, для растворов в дейтерохлороформе относительно стандарта тетраметилсилана (δ=0) или хлороформа (δ=7,25), или дейтерохлороформа (δ=76,81 для ЯМР 13С). Значение для мультиплета, либо разрешенного (дублет (д), триплет (т), квадруплет (кв)), либо нет (м) указано для соответствующей средней точки, если не приведен интервал, ш.с означает широкий синглет. Масс-спектры регистрировали на QUATTRO II (Micromass). Использовали безводные органические растворители. Хроматографию проводили на силикагеле.
Везде использовали следующие сокращения:
MS - масс-спектрометрия
NMM - N-метилморфолин
ЯМР - ядерный магнитный резонанс
к.т. - комнатная температура
ТГФ - тетрагидрофуран
TMSI - триметилйодсилан
Dba - трис(дибензилиденацетон)дипалладий (0)
Ph - фенил
Таблица 1
Некоторые соединения общей формулы (VII)
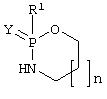
Таблица 2
Некоторые соединения общей формулы (III)
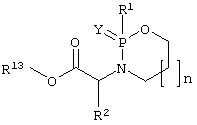
(изомер 1)
(изомер 2)
(изомеры 1)
(изомеры 2)
(изомеры 1)
(изомеры 2)
(изомеры 1)
(изомеры 2)
(изомеры 1)
(изомеры 2)
(изомер 1)
(изомер 2)
(изомеры 1)
(изомеры 2)
(изомер 1)
(изомер 2)
(изомеры 1)
(изомеры)
(изомер 1)
(изомер 2)
(изомер 1)
(изомер 2)
(изомеры 1)
(изомеры 2)
(изомеры 1)
(изомеры 2)
(изомер 1)
(изомер 2)
(изомеры 1)
(изомеры 2)
(изомер 1)
(изомер 1)
(изомер 2)
(изомер 1)
Продолжение таблицы
(изомер 2)
(изомер 1)
(изомер 2)
Продолжение таблицы
(изомер 1)
(изомеры 1)
(изомеры 2)
Таблица 3
Некоторые соединения общей формулы (II)
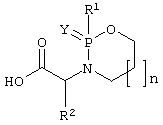
(изомер 1)
(изомер 2)
(изомеры 1)
(изомеры 2)
(изомеры 1)
Продолжение таблицы
(изомеры 2)
(изомеры 1)
(изомеры 2)
(изомеры 1)
(изомеры 2)
(изомер 1)
(изомер 2)
(изомеры 1)
(изомеры 2)
(изомер 1)
(изомер 2)
(изомеры 1)
(изомеры 2)
(изомер 1)
(изомер 2)
(изомеры 1)
(изомеры 2)
(изомеры 1)
(изомеры 2)
(изомеры 1)
(изомеры 2)
Продолжение таблицы
(изомеры 1)
(изомеры 2)
(изомер 1)
(изомер 2)
(изомеры 1)
(изомеры 2)
(изомер 1)
(изомер 2)
(изомер 1)
(изомер 2)
(изомер 1)
(изомер 2)
Таблица 4
Примеры соединений (I)
№
(изомер 1)
(изомер 2)
(изомеры 1)
(изомеры 2)
(изомеры 1)
Продолжение таблицы
(изомеры 2)
(изомеры 1)
(изомеры 2)
(изомеры 1)
(изомеры 2)
(изомеры 1)
(изомеры 2)
(изомер 1)
(изомер 2)
(изомер 1)
(изомер 2)
(изомеры 1)
(изомеры 2)
(изомеры 1)
(изомеры 2)
(изомеры 1)
(изомеры 2)
(изомер 1)
(изомер 1)
(изомер 2)
Продолжение таблицы
(изомеры 1)
(изомеры 2)
(изомер 1)
(изомер 2)
(изомер 1)
(изомер 2)
(изомеры 1)
(изомеры 2)
(изомеры 1)
(изомеры 2)
(изомер 1)
Продолжение таблицы
(изомер 1)
(изомер 2)
Общая методика 1: получение гидроксамовых кислот общей формулы (I) из соответствующих карбоновых кислот общей формулы (II).
Раствор карбоновой кислоты общей формулы (II) (2,9 ммоль) в ТГФ (45 мл) охлаждали до -10°С в атмосфере аргона. После этого прибавляли при перемешивании NMM (0,3 мл, 3,0 ммоль) и изобутилхлорформиат (0,4 мл, 3,0 ммоль). После перемешивания в течение ночи при -10°С добавляли О-триметилсилилгидроксиламин (0,4 мл, 3,2 ммоль) и оставляли смесь при -10°С на 5 ч. Затем смесь подкисляли 4 М уксусной кислотой, экстрагировали EtOAc/H2O. Водный слой вновь экстрагировали EtOAc и промывали объединенные органические слои насыщенным раствором соли, сушили (MgSO4) и концентрировали. Остаток очищали хроматографией (хлороформ/метанол/NH3 (25%) 90:10:1) или кристаллизацией, получая гидроксамовую кислоту общей формулы (I).
Общая методика 2: получение гидроксамовых кислот общей формулы (I) из соответствующих сложных эфиров общей формулы (III).
К раствору сложного эфира общей формулы (III) (0,20 ммоль) в сухом метаноле (2 мл) прибавляли О-триметилсилилгидроксиламин (72 мкл, 0,60 ммоль) и метилат натрия (1,4 М, 214 мкл, 0,30 ммоль). После перемешивания при к.т. в течение 1 часа раствор подкисляли 4 М АсОН до рН 4, концентрировали при пониженном давлении и экстрагировали EtOAc/H2O. Водный слой вновь экстрагировали EtOAc, а объединенные органические слои промывали насыщенным раствором соли, сушили (MgSO4) и концентрировали при пониженном давлении. Остаток очищали хроматографией (хлороформ/метанол/NH3 (водн. 25%) 90:10:1) или кристаллизацией, получая гидроксамовую кислоту общей формулы (I).
Общая методика 3: получение карбоновых кислот общей формулы (II) из соответствующих оксазафосфациклоалкановых эфиров общей формулы (III).
Раствор сложного эфира общей формулы (III) (0,26 ммоль) в метаноле (2 мл) и водном гидроксиде натрия (2 М, 2 мл) перемешивали в течение ночи при к.т., подкисляли 4 М АсОН и экстрагировали EtOAc/H2O. Водный слой вновь экстрагировали EtOAc, а объединенные органические слои промывали насыщенным раствором соли, сушили (MgSO4) и концентрировали при пониженном давлении. Остаток очищали хроматографией (хлороформ/метанол/уксусная кислота 80:20:1) или кристаллизацией, получая карбоновую кислоту общей формулы (II).
Общая методика 4: получение оксазафосфациклоалкановых эфиров общей формулы (III) циклизацией фосфонилдихлоридов общей формулы (IV) с аминоспиртами общей формулы (V).
Раствор аминоспирта общей формулы (V) (0,42 ммоль) и NMM (0,85 ммоль) в сухом CH2Cl2 (20 мл) охлаждали до -40°С в атмосфере аргона и прибавляли раствор фосфонилдихлорида общей формулы (IV) (0,42 ммоль) в сухом CH2Cl2 (10 мл). Смесь перемешивали при -40°С в течение 1 часа, затем при к.т. в течение ночи. После гашения водой водную фазу экстрагировали EtOAc. Объединенные органические слои промывали насыщенным раствором соли, сушили (MgSO4) и концентрировали при пониженном давлении. Остаток очищали хроматографией (хлороформ/метанол), получая оксазафосфациклоалкановый эфир общей формулы (III).
Общая методика 5: получение оксазафосфациклоалканов общей формулы (VII) циклизацией фосфонилдихлоридов общей формулы (IV) с аминоспиртами общей формулы (VI).
Раствор аминоспирта общей формулы (VI) (9,57 ммоль) и N-этилморфолина (19,1 ммоль) в сухом CH2Cl2 и раствор фосфонилдихлорида общей формулы (IV) в сухом CH2Cl2 (каждый с общим объемом 9 мл) одновременно прибавляли к 22 мл сухого CH2Cl2 при 0°С при перемешивании в течение 2 часов. По завершении прибавления суспензию перемешивали в течение ночи при к.т. и экстрагировали EtOAc/Н2О. Водную фазу вновь тщательно экстрагировали EtOAc, а объединенные органические экстракты сушили (MgSO4) и концентрировали при пониженном давлении. Остаток очищали кристаллизацией, получая оксазафосфациклоалкан общей формулы (VII).
Общая методика 6: получение оксазафосфациклоалкановых эфиров общей формулы (III) алкилированием оксазафосфациклоалканов общей формулы (VII) сложными эфирами бромуксусной кислоты общей формулы (VIII).
Раствор оксазафосфациклоалкана общей формулы (VII) (0,76 ммоль) в сухом ТГФ (4 мл) охлаждали до -70°С и прибавляли по каплям н-бутиллитий (0,76 ммоль), после чего прибавляли раствор сложного эфира бром- или йодуксусной кислоты общей формулы (VIII) (0,76 ммоль) в сухом ТГФ (1,5 мл). Смесь вынимали из охлаждающей бани и перемешивали при к.т. в течение 4 часов, гасили водой и экстрагировали EtOAc/H2O. Водную фазу вновь экстрагировали EtOAc, а объединенные органические слои промывали водой и насыщенным раствором соли, сушили (MgSO4) и концентрировали при пониженном давлении. Остаток очищали хроматографией, получая оксазафосфациклоалкановый эфир общей формулы (III).
Получение 1: (±)-2-оксо-2-фенил-1,3,2-оксазафосфоринан (соединение 201)
Общая методика 5.
Исходные вещества: 3-амино-1-пропанол и фенилфосфонилдихлорид.
1Н ЯМР (CDCl3) δ 7,87-7,75 (м, 2H), 7,56-7,40 (м, 3H), 4,45 (м, 1H), 4,12 (м, 1H), 3,74 (ш.с, 1H), 3,43 (м, 1H), 3,20 (м, 1H), 2,06 (м, 1H), 1,73 (м, 1H).
Получение 2: (±)-2-оксо-2-фенил-1,3,2-оксазафосфорепан (соединение 202)
Общая методика 5.
Исходные вещества: 4-амино-1-бутанол и фенилфосфонилдихлорид.
13С ЯМР (CDCl3) δ 131,5, 131,4, 130,9, 128,3, 65,4, 41,2, 31,9, 29,9.
Получение 3: (±)-2-оксо-2-фенил-1,3,2-оксазафосфорокан (соединение 203)
Общая методика 5.
Исходные вещества: 5-амино-1-пентанол и фенилфосфонилдихлорид.
13С ЯМР (CDCl3) δ 131,5, 131,4, 130,9, 128,3, 66,0, 41,3, 29,7, 29,2, 24,2.
Получение 4: (±)-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан (соединение 204)
Общая методика 5.
Исходные вещества: 3-амино-1-пропанол и 4-метоксифенилфосфонилдихлорид.
1Н ЯМР (CDCl3) δ 7,75 (м, 2H), 6,96 (м, 2H), 4,45 (м, 1H), 4,12 (м, 1H), 3,85 (с, 3H), 3,43 (м, 2H), 3,21 (м, 1H), 2,04 (м, 1H), 1,76 (м, 1H).
Получение 5: (±)-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан (соединение 205)
Общая методика 5.
Исходные вещества: 4-амино-1-бутанол и 4-метоксифенилфосфонилдихлорид.
13С ЯМР (CDCl3) δ 162,2, 132,8, 122,8, 113,9, 65,2, 55,3, 41,2, 32,0, 30,0.
Получение 6: (±)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан (соединение 206)
Общая методика 5.
Исходные вещества: 4-амино-1-бутанол и фенилфосфонилдихлорид.
13С ЯМР (CDCl3) δ 160,6, 156,0, 132,9, 129,9, 125,2, 124,2, 119,8, 117,8, 65,4, 41,2, 32,0, 30,0.
Получение 7: (±)-2-оксо-2-(2-фенилэтил)-1,3,2-оксазафосфоринан (соединение 207)
Общая методика 5.
Исходные вещества: 3-амино-1-пропанол и 2-фенилэтилфосфонилдихлорид.
1Н ЯМР (CDCl3) δ 7,30 (м, 2H), 7,22 (м, 3H), 4,41 (м, 1H), 4,16 (м, 1H), 3,33 (м, 1H), 3,15 (м, 1H), 2,69 (м, 3H), 2,12 (м, 2H), 1,98 (м, 1H), 1,76 (м, 1H).
Получение 8: (±)-2-гептил-2-оксо-1,3,2-оксазафосфоринан (соединение 208)
Общая методика 5.
Исходные вещества: 3-амино-1-пропанол и н-гептилфосфонилдихлорид.
1Н ЯМР (CDCl3) δ 4,41 (м, 1H), 4,17 (м, 1H), 3,35 (м, 1H), 3,19 (м, 1H), 2,91 (ш.с, 1H), 1,98 (м, 1H), 1,77 (м, 2H), 1,62 (м, 2H), 1,48-1,20 (м, 9H), 0,88 (т, 3H).
Получение 9: (±)-2-(4-бифенилил)-2-оксо-1,3,2-оксазафосфоринан (соединение 209)
Общая методика 5.
Исходные вещества: 3-амино-1-пропанол и 4-бифенилилфосфонилдихлорид.
1Н ЯМР (CDCl3) δ 7,88 (м, 2H), 7,68 (м, 2H), 7,60 (м, 2H), 7,43 (м, 3H), 4,50 (м, 1H), 4,18 (м, 1H), 3,46 (м, 2H), 3,27 (м, 1H), 2,08 (м, 1H), 1,79 (м, 1H).
Получение 10: (±)-этил-2-(4-хлорфенокси)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (соединение 210)
Общая методика 4.
Исходные вещества: 4-хлорфенилфосфорилдихлорид и этиловый эфир N-(3-гидроксипропил)глицина.
13С ЯМР (CDCl3) δ 169,7, 149,6, 129,9, 129,7, 121,4, 70,0, 61,2, 49,8, 48,0, 25,9, 14,2.
Получение 11: (±)-метил-2-(4-хлорфенокси)-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (соединение 211)
Общая методика 4.
Исходные вещества: 4-хлорфенилфосфорилдихлорид и метиловый эфир N-(4-гидроксибутил)глицина.
13С ЯМР (CDCl3) δ 171,1, 149,6, 130,1, 129,5, 122,1, 67,1, 52,1, 49,9, 48,2, 29,6, 26,3.
Получение 12: (±)-этил-2-[(4-бромфенил)метил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (соединение 212)
Общая методика 4.
Исходные вещества: 4-бромфенилфосфонилдихлорид и этиловый эфир N-(3-гидроксипропил)глицина.
1Н ЯМР (CDCl3) δ (д, 2H), 7,27 (дд, 2H), 4,32 (м, 1H), 4,24-3,98 (м, 2H), 4,19 (кв, 2H), 3,57 (дд, 1H), 3,23 (м, 3H), 2,97 (м, 1H), 1,88 (м, 1H), 1,33 (м, 1H), 1,28 (т, 3H).
Получение 13: (±)-этил-2-[(4-бифенилил)метил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (соединение 213)
Методика: смесь соединения 210 (0,21 ммоль) и Pd(PPh3)4 (0,0105 ммоль) в толуоле (1,5 мл) перемешивали в течение 30 минут в атмосфере аргона, после чего прибавляли фенилбороновую кислоту (0,42 ммоль) и Na2CO3 (0,46 ммоль в 230 мкл Н2О) и перемешивали смесь при 110оС в течение ночи. Смесь разбавляли эфиром, фильтровали через целит, концентрировали при пониженном давлении и очищали флэш-хроматографией, получая соединение 211.
1Н ЯМР (CDCl3) δ 7,58 (м, 4H), 7,43 (м, 4H), 7,33 (м, 1H), 4,34 (м, 1H), 4,25-4,00 (м, 2H), 4,20 (кв, 2H), 3,63 (дд, 1H), 3,45-3,18 (м, 3H), 2,99 (м, 1H), 1,87 (м, 1H), 1,36 (м, 1H), 1,28 (т, 3H).
Получение 14: (±)-этил-2-(4-бифенилил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (соединение 214)
Общая методика 6.
Исходные вещества: соединение 209 и этилбромацетат.
1Н ЯМР (CDCl3) δ 7,95 (м, 2H), 7,68 (м, 2H), 7,61 (м, 2H), 7,46 (м, 2H), 7,40 (м, 1H), 4,53 (м, 1H), 4,25 (м, 1H), 4,20-4,00 (м, 3H), 3,75 (дд, 1H), 3,47 (м, 1H), 3,31 (м, 1H), 2,14 (м, 1H), 2,05 (м, 1H), 1,23 (т, 3H).
Получение 15: (±)-метил-2-(4-бифенилил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (соединение 215)
Общая методика 4.
Исходные вещества: 4-бифенилилфосфонилдихлорид и метиловый эфир N-(4-гидроксибутил)глицина.
13С ЯМР (CDCl3) δ 171,9, 144,4, 140,3, 131,8, 129,2, 128,9, 127,9, 127,3, 127,0, 65,3, 51,9, 48,5, 47,5, 29,5, 26,6.
Получение 16: (±)-этил-2-гептил-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (соединение 216)
Общая методика 4.
Исходные вещества: н-гептилфосфонилдихлорид и этиловый эфир N-(3-гидроксипропил)глицина.
1Н ЯМР (CDCl3) δ 4,39 (м, 1H), 4,18 (кв, 2H), 4,17 (м, 2H), 3,60 (дд, 1H), 3,43 (м, 1H), 3,05 (м, 1H), 2,10 (м, 1H), (м, 3H), 1,61 (м, 2H), 1,46-1,20 (м, 8H), 1,27 (т, 3H), 0,88 (т, 3H).
Получение 17: (±)-метил-2-гептил-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (соединение 217)
Общая методика 4.
Исходные вещества: н-гептилфосфонилдихлорид и метиловый эфир N-(4-гидроксибутил)глицина.
13С ЯМР (CDCl3) δ 172,2, 64,4, 51,9, 48,5, 47,6, 31,7, 30,9, 29,4, 28,9, 26,9, 26,5, 22,6, 22,5, 14,1.
Получение 18: (±)-этил-2-оксо-2-[4-(фениламино)фенил]-1,3,2-оксазафосфоринан-3-ацетат (соединение 218)
Методика: смесь анилина (0,25 ммоль), соединения 244 (0,27 ммоль), Pd2(dba)3 (0,006 ммоль), 2,2'-бис(дифенилфосфино)-1,1'-бинафтила (BINAP, 0,02 ммоль) и Cs2CO3 (0,35 ммоль) в диоксане (1 мл) в атмосфере аргона нагревали при 100°С в течение ночи. Затем суспензию разбавляли эфиром, фильтровали, концентрировали при пониженном давлении и очищали флэш-хроматографией, получая соединение 216.
1Н ЯМР (CDCl3) δ 7,73 (м, 2H), 7,32 (м, 2H), 7,15 (м, 2H), 7,04 (м, 3H), 6,10 (ш.с, 1H), 4,48 (м, 1H), 4,30-4,05 (м, 3H), 3,98 (дд, 1H), 3,65 (дд, 1H), 3,5-3,2 (м, 2H), 2,05 (м, 2H), 1,23 (т, 3H).
Получение 19: (±)-этил-2-оксо-2-фенил-1,3,2-оксазафосфоринан-3-ацетат (соединение 219)
Общая методика 6.
Исходные вещества: соединение 201 и этилбромацетат.
1Н ЯМР (CDCl3) δ 7,88 (м, 2H), 7,47 (м, 3H), 4,51 (м, 1H), 4,3-4,1 (м, 1H), 4,13 (кв, 2H), 4,03 (дд, 1H), 3,73 (дд, 1H), 3,44 (м, 1H), 3,28 (м, 1H), 2,14 (м, 1H), 2,00 (м, 1H), 1,35-1,17 (т, 3H).
Получение 20: (±)-этил-2-оксо-2-фенил-1,3,2-оксазафосфорепан-3-ацетат (соединение 220)
Общая методика 4.
Исходные вещества: фенилфосфонилдихлорид и метиловый эфир N-(4-гидроксибутил)глицина.
13С ЯМР (CDCl3) δ 171,3, 131,6, 131,3, 130,6, 128,3, 65,3, 61,0, 48,6, 47,4, 29,5, 26,5, 14,2.
Получение 21: (±)-этил-α-бутил-2-оксо-2-фенил-1,3,2-оксазафосфорепан-3-ацетат (диастереомеры 1, соединение 221)
Общая методика 6.
Исходные вещества: соединение 202 и этил-2-йодгексаноат.
13С ЯМР (CDCl3) δ 172,5, 131,5, 131,4, 136,0, 128,0, 65,4, 60,4, 59,2, 43,9, 30,7, 29,8, 29,4, 28,6, 22,5, 14,0, 13,8.
Получение 22: (±)-этил-α-бутил-2-оксо-2-фенил-1,3,2-оксазафосфорепан-3-ацетат (диастереомеры 2, соединение 222)
Общая методика 6.
Исходные вещества: соединение 202 и этил-2-йодгексаноат.
13С ЯМР (CDCl3) δ 173,3, 131,5, 131,4, 131,2, 128,2, 65,3, 60,9, 57,8, 41,7, 29,6, 29,0, 28,5, 27,7, 22,3, 14,2, 13,8.
Получение 23: (±)-этил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (соединение 223)
Общая методика 6.
Исходные вещества: соединение 204 и этилбромацетат.
1Н ЯМР (CDCl3) δ 7,83 (м, 2H), 6,96 (м, 2H), 4,49 (м, 1H), 4,30-4,05 (м, 3H), 3,98 (дд, 1H), 3,84 (с, 3H), 3,65 (дд, 1H), 3,41 (м, 1H), 3,28 (м, 1H), 2,07 (м, 2H), 1,23 (т, 3H).
Получение 24: (±)-метил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (соединение 224)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и метиловый эфир N-(4-гидроксибутил)глицина.
13С ЯМР (CDCl3) δ 171,9, 162,3, 133,2, 122,0, 113,8, 65,2, 55,3, 51,9, 48,4, 47,4, 29,5, 26,5.
Получение 25: (±)-этил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоронан-3-ацетат (соединение 225)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и метиловый эфир N-(5-гидроксипентил)глицина.
13С ЯМР (CDCl3) δ 171,2, 162,3, 133,8, 121,7, 113,8, 60,9, 60,5, 55,3, 45,9, 42,3, 27,7, 24,3, 19,1, 18,5, 14,2.
Получение 26: (αR)-метил-2-(4-метоксифенил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 1, соединение 226)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-валина.
1Н ЯМР (CDCl3) δ 7,64 (м, 2H), 6,94 (м, 2H), 4,44 (м, 1H), 4,20 (м, 1H), 3,85 (т, 1H), 3,84 (с, 3H), 3,45 (с, 3H), 3,43 (м, 2H), 2,16 (м, 2H), 1,96 (м, 1H), 1,14 (д, 3H), 0,90 (д, 3H).
Получение 27: (αR)-метил-2-(4-метоксифенил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 2, соединение 227)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-валина.
1Н ЯМР (CDCl3) δ 7,78 (м, 2H), 6,95 (м, 2H), 4,49 (м, 1H), 4,24 (м, 1H), 3,85 (с, 3H), 3,76 (с, 3H), 3,68 (м, 1H), 3,46 (дд, 1H), 3,22 (м, 1H), 2,08 (м, 3H), 0,80 (д, 3H), 0,70 (д, 3H).
Получение 28: (±)-этил-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (диастереомеры 1, соединение 228)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и этиловый эфир N-(4-гидроксибутил)-(±)-норлейцина.
13С ЯМР (CDCl3) δ 172,7, 162,2, 133,4, 122,5, 113,5, 65,3, 60,4, 59,2, 55,3, 43,9, 30,8, 29,8, 29,5, 28,6, 22,5, 14,0, 13,9.
Получение 29: (±)-этил-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (диастереомеры 2, соединение 229)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и этиловый эфир N-(4-гидроксибутил)-(±)-норлейцина.
13С ЯМР (CDCl3) δ 173,4, 162,2, 133,3, 122,7, 113,7, 65,2, 60,9, 57,8, 52,3, 41,6, 29,6, 29,0, 28,5, 27,7, 22,3, 14,2, 13,8.
Получение 30: (±)-этил-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорокан-3-ацетат (диастереомеры 1, соединение 230)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и этиловый эфир N-(5-гидроксипентил)-(±)-норлейцина.
13С ЯМР (CDCl3) δ 172,4, 162,1, 133,3, 122,3, 113,5, 65,2, 60,4, 59,1, 55,3, 44,0, 31,6, 29,3, 29,1, 28,9, 24,4, 22,6, 14,0.
Получение 31: (±)-этил-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (диастереомеры 2, соединение 231)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и этиловый эфир N-(5-гидроксипентил)-(±)-норлейцина.
MS. Вычислено для С20Н32NO5P: 397,20; найдено [M+H]+=398; [M+Na]+=420.
Получение 32: (±)-метил-α-аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (диастереомеры 1, соединение 232)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-(±)-аллилглицина.
13С ЯМР (CDCl3) δ 172,3, 162,5, 134,1, 133,8, 121,8, 117,9, 113,9, 66,7, 57,0, 55,3, 51,7, 41,3, 34,4, 26,7.
Получение 33: (±)-метил-α-аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (диастереомеры 2, соединение 233)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-(±)-аллилглицина.
13С ЯМР (CDCl3) δ 172,7, 162,5, 134,1, 134,0, 122,0, 117,9, 113,8, 66,2, 57,3, 55,3, 52,1, 40,8, 34,3, 26,3.
Получение 34: (±)-этил-α-аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (диастереомеры 1, соединение 234)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и метиловый эфир N-(4-гидроксибутил)-(±)-аллилглицина.
13С ЯМР (CDCl3) δ 172,0, 162,2, 134,8, 133,4, 122,4, 117,9, 113,5, 65,3, 60,6, 58,9, 55,3, 43,9, 35,2, 29,5, 29,3, 13,9.
Получение 35: (±)-этил-α-аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (диастереомеры 2, соединение 235)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и метиловый эфир N-(4-гидроксибутил)-(±)-аллилглицина.
13С ЯМР (CDCl3) δ 172,6, 162,2, 133,9, 133,4, 122,6, 117,9, 113,7, 65,2, 61,0, 57,8, 55,3, 42,1, 34,0, 29,6, 27,7, 14,2.
Получение 36: (αR)-метил-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 1, соединение 236)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-лейцина.
1Н ЯМР (CDCl3) δ 7,75 (м, 2H), 6,95 (м, 2H), 4,43 (м, 1H), 4,34 (м, 1H), 4,17 (м, 1H), 3,84 (с, 3H), 3,56 (с, 3H), 3,37 (м, 2H), 2,10-1,55 (м, 5H), 1,03 (д, 3H), 0,97 (д, 3H).
Получение 37: (αR)-метил-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 2, соединение 237)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-лейцина.
13С ЯМР (CDCl3) δ 173,7, 162,5, 133,8, 122,2, 113,9, 66,0, 55,4, 55,3, 52,0, 40,4, 38,5, 26,5, 24,5, 22,8, 21,5.
Получение 38: (±)-этил-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (диастереомеры 1, соединение 238)
Общая методика 6.
Исходные вещества: соединение 205 и этил-2-йод-4-метилвалероат.
13С ЯМР (CDCl3) δ 172,9, 162,1, 133,4, 122,5, 113,5, 65,3, 60,5, 57,3, 55,3, 43,8, 39,9, 29,8, 29,5, 24,9, 23,0, 22,0, 13,9.
Получение 39: (±)-этил-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (диастереомеры 2, соединение 239)
Общая методика 6.
Исходные вещества: соединение 205 и этил-2-йод-4-метилвалероат.
13С ЯМР (CDCl3) δ 173,6, 162,2, 133,2, 122,8, 113,7, 65,2, 60,9, 55,9, 55,3, 41,7, 38,4, 29,6, 27,7, 24,6, 22,7, 22,3, 14,2.
Получение 40: (αS)-метил-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 1,соединение 240)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-L-лейцина.
13С ЯМР (CDCl3) δ 173,5, 162,5, 133,8, 121,7, 113,9, 66,7, 55,7, 55,3, 51,6, 41,2, 38,6, 26,9, 24,7, 23,1, 21,7.
Получение 41: (αS)-метил-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 2, соединение 241)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-L-лейцина.
13С ЯМР (CDCl3) δ 173,7, 162,5, 133,9, 122,2, 113,9, 66,0, 55,4, 55,3, 52,0, 40,4, 38,5, 26,5, 24,5, 22,8, 21,5.
Получение 42: (±)-этил-2-(4-метоксифенил)-α-октил-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (диастереомеры 1, соединение 242)
Общая методика 6.
Исходные вещества: соединение 205 и этил-2-йоддеканоат.
1Н ЯМР (CDCl3) δ 7,74 (м, 2H), 6,91 (м, 2H), 4,61 (м, 1H), 4,34 (м, 1H), 4,16 (м, 1H), 3,89 (д.кв, 2H), 3,82 (с, 3H), 3,20 (м, 1H), 3,07 (м, 1H), 2,02-1,10 (м, 18H), 0,98 (т, 3H), 0,88 (ш.т, 3H).
Получение 43: (±)-этил-2-(4-метоксифенил)-α-октил-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (диастереомеры 2, соединение 243)
Общая методика 6.
Исходные вещества: соединение 205 и этил-2-йоддеканоат.
13С ЯМР (CDCl3) δ 173,4, 162,2, 133,3, 122,7, 113,7, 65,2, 60,9, 57,8, 55,3, 41,6, 31,8, 29,6, 29,3, 29,2, 29,1, 27,7, 26,3, 22,6, 14,2, 14,1.
Получение 44: (αS)-этил-2-(4-метоксифенил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 1, соединение 244)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и этиловый эфир N-(3-гидроксипропил)-L-фенилаланина.
1Н ЯМР (CDCl3) δ 7,75 (м, 2H), 7,35-7,16 (м, 5H), 6,93 (м, 2H), 4,58 (м, 1H), 4,29-4,02 (м, 2H), 3,95 (кв, 2H), 3,83 (с, 3H), 3,54-3,26 (м, 3H), 3,14 (дд, 1H), 1,89 (м, 2H), 1,04 (т, 3H).
Получение 45: (αS)-этил-2-(4-метоксифенил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 2, соединение 245)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и этиловый эфир N-(3-гидроксипропил)-L-фенилаланина.
1Н ЯМР (CDCl3) δ 7,23-7,05 (м, 7H), 6,70 (м, 2H), 4,60 (м, 1H), 4,50 (м, 1H), 4,21 (кв, 2H), 4,12 (м, 1H), 3,81 (с, 3H), 3,60 (м, 1H), 3,20 (м, 2H), 2,91 (дд, 1H), 2,20 (м, 1H), 1,83 (м, 1H), 1,28 (т, 3H).
Получение 46: (αR)-метил-2-(4-метоксифенил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 1, соединение 246)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-фенилаланина.
13С ЯМР (CDCl3) δ 172,2, 162,5, 136,8, 133,8, 129,4, 128,4, 126,7, 121,7, 113,9, 66,2, 58,5, 55,3, 51,6, 41,1, 36,3, 26,7.
Получение 47: (αR)-метил-2-(4-метоксифенил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 2, соединение 247)
Исходные вещества: 4-метоксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-фенилаланина.
13С ЯМР (CDCl3) δ 172,8, 162,1, 137,2, 133,5, 129,2, 128,7, 126,8, 121,4, 113,8, 66,5, 59,2, 55,3, 52,2, 41,0, 35,6, 26,2.
Получение 48: (±)-этил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетат (соединение 248)
Общая методика 4.
Исходные вещества: 4-феноксифенилфосфонилдихлорид и этиловый эфир N-(3-гидроксипропил)глицина.
1Н ЯМР (CDCl3) δ 7,85 (м, 2H), 7,38 (м, 2H), 7,18 (м, 1H), 7,04 (м, 4H), 4,50 (м, 1H), 4,23 (м, 1H), 4,14 (кв, 2H), 4,02 (дд, 1H), 3,68 (дд, 1H), 3,41 (м, 1H), 3,28 (м, 1H), 2,12 (м, 1H), 2,03 (м, 1H), 1,23 (т, 3H).
Получение 49: (±)-метил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетат (соединение 249)
Общая методика 4.
Исходные вещества: 4-феноксифенилфосфонилдихлорид и метиловый эфир N-(4-гидроксибутил)глицина.
1Н ЯМР (CDCl3) δ 7,87 (м, 2H), 7,37 (м, 2H), 7,16 (м, 1H), 7,03 (м, 4H), 4,54 (м, 1H), 4,37 (м, 1H), 4,15 (м, 1H), 3,85 (дд, 1H), 3,70 (с, 3H), 3,16 (м, 1H), 2,94 (м, 1H), 1,77 (м, 4H).
Получение 50: (±)-метил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорокан-3-ацетат (соединение 250)
Общая методика 4.
Исходные вещества: 4-феноксифенилфосфонилдихлорид и метиловый эфир N-(5-гидроксипентил)глицина.
13С ЯМР (CDCl3) δ 171,6, 160,6, 155,9, 133,5, 129,9, 124,7, 124,2, 119,9, 117,6, 66,1, 51,8, 46,0, 45,4, 28,6, 25,1, 24,4.
Получение 51: (±)-метил-α-аллил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетат (диастереомеры 1, соединение 251)
Общая методика 4.
Исходные вещества: 4-феноксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-(±)аллилглицина.
13С ЯМР (CDCl3) δ 172,3, 160,9, 155,8, 134,1, 133,9, 130,0, 124,4, 124,3, 120,0, 118,0, 117,7, 66,9, 57,0, 51,8, 41,4, 34,4, 26,7.
Получение 52: (±)-метил-α-аллил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетат (диастереомеры 2, соединение 252)
Общая методика 4.
Исходные вещества: 4-феноксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-(±)аллилглицина.
13С ЯМР (CDCl3) δ 172,6, 160,9, 155,8, 134,0, 134,0, 130,0, 124,6, 124,4, 119,9, 118,0, 117,6, 66,3, 57,3, 52,1, 40,8, 34,3, 26,3.
Получение 53: (±)-этил-α-бутил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетат (диастереомеры 1, соединение 253)
Общая методика 6.
Исходные вещества: соединение 206 и этил-2-йодгексаноат.
13С ЯМР (CDCl3) δ 172,6, 160,5, 156,0, 133,5, 129,9, 125,0, 124,2, 119,8, 117,5, 65,4, 60,5, 59,2, 43,9, 30,8, 29,8, 29,4, 28,7, 22,5, 14,0, 13,9.
Получение 54: (±)-этил-α-бутил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетат (диастереомеры 2, соединение 254)
Общая методика 6.
Исходные вещества: соединение 206 и этил-2-йодгексаноат.
13С ЯМР (CDCl3) δ 173,3, 160,5, 155,9, 133,4, 130,0, 125,2, 124,2, 119,8, 117,7, 65,3, 60,9, 57,8, 41,7, 29,6, 29,0, 28,5, 27,7, 22,3, 14,2, 13,8.
Получение 55: (αR)-метил-α-(2-метилпропил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 1, соединение 255)
Общая методика 4.
Исходные вещества: 4-феноксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-лейцина.
13С ЯМР (CDCl3) δ 173,4, 160,8, 155,8, 133,9, 130,0, 124,3, 124,3, 119,9, 117,7, 66,9, 55,7, 51,7, 41,2, 38,6, 26,9, 24,7, 23,2, 21,7.
Получение 56: (αR)-метил-α-(2-метилпропил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 2, соединение 256)
Общая методика 4.
Исходные вещества: 4-феноксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-лейцина.
13С ЯМР (CDCl3) δ 173,7, 160,9, 155,9, 133,9, 130,0, 124,9, 124,3, 119,8, 117,8, 66,1, 55,4, 52,0, 40,4, 38,4, 26,4, 24,5, 22,9, 21,5.
Получение 57: (±)-этил-α-октил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетат (диастереомеры 1, соединение 257)
Общая методика 6.
Исходные вещества: соединение 206 и этил-2-йоддеканоат.
13С ЯМР (CDCl3) δ 172,6, 160,4, 156,0, 133,5, 129,9, 125,0, 124,2, 119,8, 117,5, 65,4, 60,5, 59,3, 43,9, 31,9, 31,1, 29,8, 29,5, 29,3, 26,5, 22,7, 14,1, 13,9.
Получение 58: (±)-этил-α-октил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетат (диастереомеры 2, соединение 258)
Общая методика 6.
Исходные вещества: соединение 206 и этил-2-йоддеканоат.
MS. Вычислено для С28Н40NO5P501,26; найдено [M+H]+=502, [M+Na]+=524.
Получение 59: (αR)-метил-α-(1-метилэтил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 1, соединение 259)
Общая методика 4.
Исходные вещества: 4-феноксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-валина.
13С ЯМР (CDCl3) δ 172,4, 160,7, 155,8, 133,6, 130,0, 124,9, 124,4, 119,9, 117,7, 66,8, 63,0, 51,1, 41,0, 27,2, 26,7, 19,4, 19,3.
Получение 60: (±)-этил-2-оксо-2-(2-фенилэтил)-1,3,2-оксазафосфоринан-3-ацетат (соединение 260)
Общая методика 6.
Исходные вещества: соединение 207 и этилбромацетат.
1Н ЯМР (CDCl3) δ 7,25 (м, 5H), 4,39 (м, 1H), 4,17 (м, 4H), 3,60 (дд, 1H), 3,44 (м, 1H), 3,05 (м, 1H), 2,17 (м, 3H), 1,90 (м, 1H), 1,61 (м, 1H), 1,36 (м, 1H), 1,26 (т, 3H).
Получение 61: (±)-метил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорокан-3-ацетат (соединение 261)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и метиловый эфир N-(5-гидроксипентил)глицина.
13С ЯМР (CDCl3) δ 171,7, 162,2, 133,3, 122,2, 113,7, 66,0, 55,3, 51,8, 46,2, 45,4, 28,7, 25,2, 24,4.
Получение 62: (±)-метил-2-оксо-2-фенил-1,3,2-оксазафосфорокан-3-ацетат (соединение 262)
Общая методика 4.
Исходные вещества: фенилфосфонилдихлорид и метиловый эфир N-(5-гидроксипентил)глицина.
13С ЯМР (CDCl3) δ 171,6, 131,6, 131,4, 130,8, 128,2, 66,2, 51,8, 46,2, 45,4, 28,7, 25,1, 24,4.
Получение 63: (±)-метил-2-гептил-2-оксо-1,3,2-оксазафосфорокан-3-ацетат (соединение 263)
Общая методика 4.
Исходные вещества: н-гептилфосфонилдихлорид и метиловый эфир N-(5-гидроксипентил)глицина.
13С ЯМР (CDCl3) δ 171,9, 65,9, 51,8, 46,0, 44,8, 31,7, 30,9, 28,9, 28,6, 27,1, 25,2, 24,5, 22,6, 22,5, 14,1.
Получение 64: (αR)-метил-2-(4-бифенилил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 1, соединение 264)
Общая методика 4.
Исходные вещества: 4-бифенилилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-валина.
1Н ЯМР (CDCl3) δ 7,78 (м, 2H), 7,66 (м, 2H), 7,60 (м, 2H), 7,46 (м, 2H), 7,39 (м, 1H), 4,48 (м, 1H), 4,27 (м, 1H), 3,92 (т, 1H), 3,74 (м, 1H), 3,60-3,30 (м, 1H), 3,42 (с, 3H), 2,21 (м, 2H), 1,99 (м, 1H), 1,16 (д, 3H), 0,92 (д, 3H).
Получение 65: (αR)-метил-2-(4-бифенилил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 2, соединение 265)
Общая методика 4.
Исходные вещества: 4-бифенилилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-валина.
1Н ЯМР (CDCl3) δ 7,90 (м, 2H), 7,68 (м, 2H), 7,61 (м, 2H), 7,47 (м, 2H), 7,39 (м, 1H), 4,53 (м, 1H), 4,30 (м, 1H), 3,82-3,66 (м, 1H), 3,78 (с, 3H), 3,60 (дд, 1H), 3,26 (м, 1H), 2,12 (м, 2H), 1,84 (м, 1H), 0,83 (д, 3H), 0,73 (д, 3H).
Получение 66: (αR)-метил-2-(4-бифенилил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 1, соединение 266)
Общая методика 4.
Исходные вещества: 4-бифенилилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-фенилаланина.
1Н ЯМР (CDCl3) δ 7,85 (м, 2H), 7,65 (м, 2H), 7,59 (м, 2H), 7,45 (м, 3H), 7,37-7,16 (м, 5H), 4,72 (м, 1H), 4,30-4,05 (м, 2H), 3,53-3,30 (м, 3H), 3,48 (с, 3H), 3,16 (дд, 1H), 1,91 (м, 2H).
Получение 67: (αR)-метил-2-(4-бифенилил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 2, соединение 267)
Общая методика 4.
Исходные вещества: 4-бифенилилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-фенилаланина.
1Н ЯМР (CDCl3) δ 7,56 (м, 2H), 7,47 (м, 2H), 7,40 (м, 3H), 7,25-7,15 (м, 5H), 7,10 (м, 2H), 4,72 (м, 1H), 4,54 (м, 1H), 4,25-4,07 (м, 1H), 3,78 (с, 3H), 3,60 (м, 1H), 3,24 (м, 2H), 2,94 (дд, 1H), 2,23 (м, 1H), 1,88 (м, 1H).
Получение 68: (±)-этил-2-[4-(4-хлорфенокси)фенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (соединение 268)
Общая методика 4.
Исходные вещества: 4-(4-хлорфенокси)фенилфосфонилдихлорид и метиловый эфир N-(4-гидроксибутил)глицина.
13С ЯМР (CDCl3) δ 171,3, 160,1, 154,6, 133,5, 130,0, 129,3, 125,1, 121,1, 117,8, 65,3, 61,0, 48,4, 47,3, 29,5, 26,5, 14,2.
Получение 69: (±)-этил-2-[4-(4-хлорфенокси)фенил]-2-оксо-1,3,2-оксазафосфорокан-3-ацетат (соединение 269)
Общая методика 4.
Исходные вещества: 4-(4-хлорфенокси)фенилфосфонилдихлорид и метиловый эфир N-(5-гидроксипентил)глицина.
1Н ЯМР (CDCl3) δ 7,94 (м, 2H), 7,32 (м, 2H), 7,05-6,94 (м, 4H), 4,47 (м, 2H), 4,16 (д.кв, 2H), 4,04 (м, 1H), 3,71 (дд, 1H), 3,18 (м, 1H), 3,03 (м, 1H), 2,00-1,56 (м, 5H), 1,44 (м, 1H), 1,24 (т, 3H).
Получение 70: (±)-этил-2-(4'-бром-4-бифенилил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (соединение 270)
Общая методика 4.
Исходные вещества: 4'-бром-4-бифенилилфосфонилдихлорид и этиловый эфир N-(3-гидроксипропил)глицина.
1Н ЯМР (CDCl3) δ 7,95 (м, 2H), 7,72-7,42 (м, 6H), 4,53 (м, 1H), 4,26 (м, 1H), 4,15 (кв, 2H), 4,06 (дд, 1H), 3,74 (дд, 1H), 3,47 (м, 1H), 3,31 (м, 1H), 2,16 (м, 1H), 2,03 (м, 1H), 1,23 (т, 3H).
Получение 71: (±)-этил-2-(4'-бром-4-бифенилил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (соединение 271)
Общая методика 4.
Исходные вещества: 4'-бром-4-бифенилилфосфонилдихлорид и этиловый эфир N-(4-гидроксибутил)глицина.
13С ЯМР (CDCl3) δ 171,3, 143,1, 139,2, 132,0, 131,9, 129,8, 128,8, 126,8, 122,3, 65,4, 61,0, 48,6, 47,4, 29,5, 26,6, 14,2.
Получение 72: (±)-метил-2-(4'-бром-4-бифенилил)-2-оксо-1,3,2-оксазафосфорокан-3-ацетат (соединение 272)
Общая методика 4.
Исходные вещества: 4'-бром-4-бифенилилфосфонилдихлорид и метиловый эфир N-(5-гидроксипентил)глицина.
1Н ЯМР (CDCl3) δ 8,02 (м, 2H), 7,63 (м, 2H), 7,58 (м, 2H), 7,47 (м, 2H), 4,50 (м, 2H), 4,07 (м, 1H), 3,77 (м, 1H), 3,71 (с, 3H), 3,23 (м, 1H), 3,05 (м, 1H), 2,00-1,33 (м, 6H).
Получение 73: (±)-этил-2-оксо-2-[2-(1-нафтил)этил]-1,3,2-оксазафосфоринан-3-ацетат (соединение 273)
Общая методика 4.
Исходные вещества: 2-(1-нафтил)этилфосфонилдихлорид и этиловый эфир N-(3-гидроксипропил)глицина.
13С ЯМР (CDCl3) δ 170,7, 137,6, 133,9, 131,5, 128,9, 127,0, 126,1, 125,7, 125,6, 123,5, 67,0, 61,1, 49,8, 47,2, 28,4, 26,2, 25,9, 14,2.
Получение 74: (±)-этил-2-фенил-2-тиоксо-1,3,2-оксазафосфоринан-3-ацетат (соединение 274)
Общая методика 4.
Исходные вещества: тиофенилфосфонилдихлорид и этиловый эфир N-(3-гидроксипропил)глицина.
13С ЯМР (CDCl3) δ 170,2, 132,7, 132,4, 131,7, 128,6, 66,3, 61,0, 50,8, 47,0, 26,3, 14,2.
Получение 75: (±)-этил-2-фенил-2-тиоксо-1,3,2-оксазафосфорепан-3-ацетат (соединение 275)
Общая методика 4.
Исходные вещества: тиофенилфосфонилдихлорид и этиловый эфир N-(4-гидроксибутил)глицина.
13С ЯМР (CDCl3) δ 171,3, 135,4, 131,3, 130,5, 128,2, 64,7, 61,0, 49,9, 47,9, 29,1, 25,7, 14,2.
Получение 76: (±)-метил-2-фенил-2-тиоксо-1,3,2-оксазафосфорокан-3-ацетат (соединение 276)
Общая методика 4.
Исходные вещества: тиофенилфосфонилдихлорид и метиловый эфир N-(5-гидроксипентил)глицина.
13С ЯМР (CDCl3) δ 171,5, 135,7, 131,2, 130,6, 128,2, 66,0, 51,9, 46,9, 45,4, 28,3, 25,0, 24,2.
Получение 77: (±)-этил-2-[4-(хлорфенокси)фенил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (соединение 277)
Общая методика 4.
Исходные вещества: 4-(4-хлорфенокси)фенилфосфонилдихлорид и этиловый эфир N-(3-гидроксипропил)глицина.
13С ЯМР (CDCl3) δ 170,3, 160,6, 154,4, 134,2, 130,0, 129,5, 124,5, 121,2, 117,8, 66,9, 61,1, 49,3, 47,3, 26,1, 14,2.
Получение 78: (αR)-метил-2-[4-(4-хлорфенокси)фенил]-α-(2-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 1, соединение 278)
Общая методика 4.
Исходные вещества: 4-(4-хлорфенокси)фенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-валина.
13С ЯМР (CDCl3) δ 172,3, 160,3, 154,5, 133,6, 130,0, 129,5, 125,5, 121,1, 117,8, 66,8, 63,1, 51,1, 41,0, 27,2, 26,7, 19,4, 19,3.
Получение 79: (αR)-метил-2-[4-(4-хлорфенокси)фенил]-α-(2-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 2, соединение 279)
Общая методика 4.
Исходные вещества: 4-(4-хлорфенокси)фенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-валина.
13С ЯМР (CDCl3) δ 173,0, 160,6, 154,4, 134,5, 130,0, 129,6, 124,3, 121,2, 117,6, 66,0, 63,4, 51,8, 40,2, 27,6, 26,5, 19,6, 19,4.
Получение 80: (±)-этил-2-(4-бромфенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (соединение 280)
Общая методика 4.
Исходные вещества: 4-бромфенилфосфонилдихлорид и этиловый эфир N-(3-гидроксипропил)глицина.
(CDCl3) δ 7,75 (м, 2H), 7,60 (м, 2H), 4,50 (м, 1H), 4,22 (м, 1H), 4,14 (кв, 2H), 4,04 (дд, 1H), 3,68 (дд, 1H), 3,42 (м, 1H), 3,27 (м, 1H), 2,14 (м, 1H), 2,00 (м, 1H), 1,23 (т, 3H).
Получение 81: (±)-этил-2-(4-бромфенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (соединение 281)
Общая методика 4.
Исходные вещества: 4-бромфенилфосфонилдихлорид и этиловый эфир N-(4-гидроксибутил)глицина.
13С ЯМР (CDCl3) δ 171,2, 132,9, 131,5, 129,7, 126,6, 65,4, 61,1, 48,5, 47,4, 29,4, 26,5, 14,2.
Получение 82: (±)-этил-2-[4-(фенилметокси)фенил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (соединение 282)
Общая методика 4.
Исходные вещества: 4-(фенилметокси)фенилфосфонилдихлорид и этиловый эфир N-(3-гидроксипропил)глицина.
13С ЯМР (CDCl3) δ 170,4, 161,8, 136,3, 134,1, 128,7, 128,2, 127,5, 121,6, 114,9, 70,0, 66,7, 61,0, 49,3, 47,2, 26,1, 14,1.
Получение 83: (±)-этил-2-[4-(фенилметокси)фенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (соединение 283)
Общая методика 4.
Исходные вещества: 4-(фенилметокси)фенилфосфонилдихлорид и этиловый эфир N-(4-гидроксибутил)глицина.
13С ЯМР (CDCl3) δ 171,4, 161,4, 136,5, 133,2, 128,7, 128,1, 127,5, 122,4, 114,7, 70,0, 65,2, 61,0, 48,6, 47,4, 29,5, 26,5, 14,2.
Получение 84: (±)-этил-2-[4-(фенилметокси)фенил]-2-оксо-1,3,2-оксазафосфорокан-3-ацетат (соединение 284)
Общая методика 4.
Исходные вещества: 4-(фенилметокси)фенилфосфонилдихлорид и этиловый эфир N-(5-гидроксипентил)глицина.
1Н ЯМР (CDCl3) δ 7,89 (м, 2H), 7,45-7,28 (м, 5H), 7,02 (м, 2H), 5,10 (с, 2H), 4,45 (м, 2H), 4,15 (д.кв, 2H), 4,02 (м, 1H), 3,71 (дд, 1H), 3,16 (м, 1H), 3,01 (м, 1H), 2,00-1,60 (м, 5H), 1,43 (м, 1H), 1,23 (т, 3H).
Получение 85: (±)-этил-2-оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфоринан-3-ацетат (соединение 285)
Общая методика 4.
Исходные вещества: 4-(трифторметилфенокси)фенилфосфонилдихлорид и этиловый эфир N-(3-гидроксипропил)глицина.
1Н ЯМР (CDCl3) δ 7,91 (м, 2H), 7,62 (м, 2H), 7,14-7,05 (м, 4H), 4,52 (м, 1H), 4,24 (м, 1H), 4,15 (кв, 2H), 4,06 (дд, 1H), 3,70 (дд, 1H), 3,45 (м, 1H), 3,29 (м, 1H), 2,14 (м, 1H), 2,03 (м, 1H), 1,24 (т, 3H).
Получение 86: (±)-этил-2-оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфорепан-3-ацетат (соединение 286)
Общая методика 4.
Исходные вещества: 4-(трифторметилфенокси)фенилфосфонилдихлорид и этиловый эфир N-(4-гидроксибутил)глицина.
13С ЯМР (CDCl3) δ 171,4, 159,3, 159,0, 133,6, 127,3, 126,2, 119,0, 118,9, 65,4, 61,1, 48,4, 47,4, 29,5, 26,5, 14,2.
Получение 87: (αR)-метил-α-(2-метилэтил)-2-оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 1, соединение 287)
Общая методика 4.
Исходные вещества: 4-(трифторметилфенокси)фенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-валина.
13С ЯМР (CDCl3) δ 172,3, 159,2, 159,1, 133,8, 127,4, 126,7, 126,0, 124,1, 119,0, 118,9, 66,9, 63,1, 51,1, 41,0, 27,2, 26,7, 19,4, 19,3.
Получение 88: (αR)-метил-α-(2-метилэтил)-2-оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 2, соединение 288)
Общая методика 4.
Исходные вещества: 4-(трифторметилфенокси)фенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-валина.
13С ЯМР (CDCl3) δ 173,0, 159,5, 159,0, 134,6, 127,4, 126,1, 125,6, 124,1, 119,2, 118,7, 66,1, 63,5, 51,8, 40,2, 27,6, 26,5, 19,7, 19,4.
Получение 89: (±)-этил-2-[4-(4-бромфенокси)фенил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (соединение 289)
Общая методика 4.
Исходные вещества: 4-(4-бромфенокси)фенилфосфонилдихлорид и этиловый эфир N-(3-гидроксипропил)глицина.
13С ЯМР (CDCl3) δ 170,3, 160,5, 155,0, 134,2, 133,0, 124,7, 121,6, 117,9, 117,0, 66,9, 61,1, 49,3, 47,3, 26,1, 14,2.
Получение 90: (±)-этил-2-[4-(4-бромфенокси)фенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (соединение 290)
Общая методика 4.
Исходные вещества: 4-(4-бромфенокси)фенилфосфонилдихлорид и этиловый эфир N-(4-гидроксибутил)глицина.
13С ЯМР (CDCl3) δ 171,4, 160,0, 155,3, 133,5, 132,9, 125,2, 121,4, 117,9, 116,7, 65,3, 61,0, 48,4, 47,3, 29,5, 26,5, 14,2.
Получение 91: (±)-этил-2-(4-нитрофенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (соединение 291)
Общая методика 4.
Исходные вещества: 4-нитрофенилфосфонилдихлорид и этиловый эфир N-(4-гидроксибутил)глицина.
13С ЯМР (CDCl3) δ 171,1, 149,8, 138,0, 132,6, 123,1, 65,9, 61,3, 48,4, 47,4, 29,4, 26,6, 14,2.
Получение 92: (±)-этил-2-[N-(4-хлорбензоил)-4-аминофенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (соединение 292)
Методика: раствор соединения 291 в метаноле гидрировали при помощи Pd на угле (10%) в течение 1 часа при атмосферном давлении. В результате фильтрования и концентрирования получали этил-2-(4-аминофенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетат. Данный сырой анилин растворяли в CH2Cl2 с 3 эквивалентами триэтиламина, раствор охлаждали до 0°С и добавляли 2 эквивалента 4-хлорбензоилхлорида без растворителя. После перемешивания в течение ночи при к.т. смесь концентрировали при пониженном давлении, вновь растворяли в этилацетате и промывали водой и насыщенным раствором соли. После фильтрования и упаривания указанное в заголовке соединение очищали флэш-хроматографией.
13С ЯМР (CDCl3) δ 171,2, 165,3, 141,6, 138,0, 133,1, 132,0, 129,2, 128,7, 125,3, 120,3, 65,4, 61,1, 48,8, 47,4, 29,4, 26,5, 14,2.
Получение 93: (±)-этил-2-(N-бензоил-4-аминофенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетат (соединение 293)
Методика: аналогична получению 92, за исключением того, что вместо 4-хлорбензоилхлорида использовали бензоилхлорид.
13С ЯМР (CDCl3) δ 171,3, 166,1, 141,4, 134,7, 132,3, 131,9, 128,6, 127,4, 125,5, 119,9, 65,3, 61,0, 48,7, 47,4, 29,5, 26,5, 14,2.
Получение 94: (αR)-метил-α-(2-метилэтил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетат (диастереомер 1, соединение 294)
Общая методика 4.
Исходные вещества: 4-феноксифенилфосфонилдихлорид и метиловый эфир N-(3-гидроксипропил)-D-валина.
13С ЯМР (CDCl3) δ 173,0, 161,1, 155,7, 134,4, 130,0, 124,4, 123,6, 120,0, 117,5, 66,0, 63,4, 51,7, 40,2, 27,5, 26,5, 19,6, 19,4.
Получение 95: (±)-этил-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (диастереомеры 1, соединение 295)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и этиловый эфир N-(3-гидроксипропил)-(±)-норлейцина.
13С ЯМР (CDCl3) δ 172,7, 162,5, 133,9, 121,8, 113,9, 66,8, 60,7, 57,6, 55,3, 41,2, 29,4, 28,4, 26,9, 22,4, 14,1, 13,9.
Получение 96: (±)-этил-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетат (диастереомеры 2, соединение 296)
Общая методика 4.
Исходные вещества: 4-метоксифенилфосфонилдихлорид и этиловый эфир N-(3-гидроксипропил)-(±)-норлейцина.
13С ЯМР (CDCl3) δ 173,1, 162,5, 133,8, 122,4, 113,9, 65,9, 60,9, 57,3, 55,3, 40,2, 29,1, 28,4, 26,5, 22,1, 14,2, 13,8.
Получение 97: (±)-этил-2-оксо-2-фенил-1,3,2-оксазафосфоронан-3-ацетат (соединение 297)
Общая методика 4.
Исходные вещества: фенилфосфонилдихлорид и метиловый эфир N-(5-гидроксипентил)глицина.
13С ЯМР (CDCl3) δ 171,1, 131,9, 131,7, 130,4, 128,2, 60,9, 60,6, 45,9, 42,3, 27,7, 24,4, 19,1, 18,4, 14,2.
Получение 100: (αR)-2-(4-метоксифенил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 1, соединение 300)
Общая методика 3.
Исходные вещества: соединение 226.
1Н ЯМР (CD3OD) δ 7,72 (м, 2H), 7,07 (м, 2H), 4,46 (м, 1H), 4,27 (м, 1H), 3,89 (с, 3H), 3,73 (т, 1H), 3,67-3,36 (м, 2H), 2,21 (м, 2H), 1,98 (м, 1H), 1,16 (д, 3H), 1,02 (д, 3H).
Получение 101: (αR)-2-(4-метоксифенил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 2, соединение 301)
Общая методика 3.
Исходные вещества: соединение 227.
1Н ЯМР (CD3OD) δ 7,86 (м, 2H), 6,98 (м, 2H), 4,50 (м, 1H), 4,33 (м, 1H), 3,84 (с, 3H), 3,51 (м, 1H), 3,37-3,10 (м, 2H), 2,13 (м, 3H), 0,81 (д, 3H), 0,54 (д, 3H).
Получение 102: (αR)-2-(4-бифенилил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 1, соединение 302)
Общая методика 3.
Исходные вещества: соединение 264.
1Н ЯМР (CD3OD) δ 8,06 (м, 2H), 7,55 (ш.с, 4H), 7,35 (ш.с, 3H), 4,47 (м, 2H), 3,41 (м, 1H), 3,23 (м, 1H), 2,18 (м, 3H), 0,88 (ш.д, 3H), 0,45 (д, 3H).
Получение 103: (αR)-2-(4-бифенилил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 1, соединение 303)
Общая методика 3.
Исходные вещества: соединение 266.
1Н ЯМР (CD3OD) δ 7,87 (м, 2H), 7,73 (м, 2H), 7,65 (м, 2H), 7,46 (м, 2H), 7,42-7,25 (м, 5H), 7,21 (м, 1H), 4,60 (м, 1H), 4,16 (м, 2H), 3,60-3,28 (м, 3H), 3,14 (дд, 1H), 1,90 (м, 2H).
Получение 104: (αR)-2-(4-бифенилил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 2, соединение 304)
Общая методика 3.
Исходные вещества: соединение 267.
1Н ЯМР (CD3OD) δ 7,54 (м, 2H), 7,49-7,25 (м, 7H), 6,99 (м, 3H), 6,89 (м, 2H), 4,51 (м, 1H), 4,18 (м, 2H), 3,71-3,28 (м, 2H), 3,14 (м, 1H), 2,85 (дд, 1H), 2,14 (м, 2H).
Получение 105: (±)-2-оксо-2-фенил-1,3,2-оксазафосфорепан-3-уксусная кислота (соединение 305)
Общая методика 3.
Исходные вещества: соединение 220.
13С ЯМР (DMSO-d6) δ 172,4, 131,3, 131,2, 130,8, 128,1, 64,7, 47,8, 46,9, 28,9, 25,9.
Получение 106: (±)-2-оксо-2-фенил-1,3,2-оксазафосфорокан-3-уксусная кислота (соединение 306)
Общая методика 3.
Исходное вещество: соединение 262.
13С ЯМР (DMSO-d6) δ 172,2, 131,4, 131,3, 130,9, 128,1, 65,3, 45,8, 45,3, 27,9, 24,6, 24,0.
Получение 107: (±)-α-бутил-2-оксо-2-фенил-1,3,2-оксазафосфорепан-3-уксусная кислота (диастереомеры 1, соединение 307)
Общая методика 3.
Исходные вещества: соединение 221.
13С ЯМР (CD3OD) δ 175,3, 132,9, 132,6, 131,5, 129,3, 67,3, 61,0, 45,9, 31,9, 30,6, 30,5, 30,1, 23,5, 14,3.
Получение 108: (±)-α-бутил-2-оксо-2-фенил-1,3,2-оксазафосфорепан-3-уксусная кислота (диастереомеры 2, соединение 307)
Общая методика 3.
Исходные вещества: соединение 222.
1Н ЯМР (CD3OD) δ 7,84 (м, 2H), 7,62 (м, 1H), 7,54 (м, 2H), 4,79 (м, 1H), 4,33 (м, 1H), 4,25 (м, 1H), 3,23 (м, 1H), 3,06 (м, 1H), 1,96 (м, 3H), 1,85 (м, 1H), 1,72 (м, 1H), 1,55 (м, 1H), 1,23 (м, 2H), 1,00 (м, 2H), 0,77 (т, 3H).
Получение 109: (±)-2-(4-метоксифенил)-2-оксо-2-фенил-1,3,2-оксазафосфоринан-3-уксусная кислота (соединение 309)
Общая методика 3.
Исходное вещество: соединение 223.
13С ЯМР (CD3OD) δ 176,0, 164,8, 135,5, 115,3, 68,5, 56,0, 27,2.
Получение 110: (±)-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-уксусная кислота (соединение 310)
Общая методика 3.
Исходное вещество: соединение 224.
Получение 111: (±)-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомеры 1, соединение 311)
Общая методика 3.
Исходное вещество: соединение 295.
13С ЯМР (DMSO-d6) δ 173,6, 161,6, 133,0, 122,5, 113,9, 67,1, 56,8, 55,2, 41,1, 28,6, 27,9, 26,4, 21,6, 13,8.
Получение 112: (±)-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомеры 2, соединение 312)
Общая методика 3.
Исходное вещество: соединение 296.
13С ЯМР (CDCl3) δ 172,6, 163,7, 135,1, 118,0, 114,1, 66,5, 57,9, 55,5, 40,8, 27,8, 26,9, 26,1, 22,0, 13,8.
Получение 113: (±)-α-бутил-2-(4-метоксифенил)-2-оксо-2-фенил-1,3,2-оксазафосфорепан-3-уксусная кислота (диастереомеры 1, соединение 313)
Общая методика 3.
Исходное вещество: соединение 228.
1Н ЯМР (DMSO-d6) δ 7,63 (м, 2H), 6,98 (м, 21-1), 4,45 (кв, 1H), 4,11 (м, 1H), 4,03 (м, 1H), 3,79 (с, 3H), 3,20-2,90 (м, 2H), 1,90-1,20 (м, 10H), 0,87 (ш.т, 3H).
Получение 114: (±)-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-уксусная кислота (диастереомеры 2, соединение 314)
Общая методика 3.
Исходное вещество: соединение 229.
1Н ЯМР (DMSO-d6) δ 7,65 (м, 2H), 7,01 (м, 2H), 4,55 (кв, 1H), 4,05 (м, 2H), 3,80 (с, 3H), 3,09 (м, 1H), 2,84 (м, 1H), 1,90-1,20 (м, 6H), 1,10 (м, 2H), 0,86 (м, 2H), 0,67 (т, 3H).
Получение 115: (±)-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорокан-3-уксусная кислота (диастереомеры 1, соединение 315)
Общая методика 3.
Исходное вещество: соединение 230.
MS. Вычислено для C18H28NO5P 369,17; найдено [M+H]+=370, [M-H]-=368.
Получение 116: (±)-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорокан-3-уксусная кислота (диастереомеры 2, соединение 316)
Общая методика 3.
Исходное вещество: соединение 231.
MS. Вычислено для C18H28NO5P 369,17; найдено [M+H]+=370, [M-H]-=368.
Получение 117: (±)-α-аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомеры 1, соединение 317)
Общая методика 3.
Исходное вещество: соединение 232.
1Н ЯМР (CD3OD) δ 7,78 (м, 2H), 7,02 (м, 2H), 5,95 (м, 1H), 5,20 (м, 1H), 5,12 (м, 1H), 4,38 (м, 1H), 4,20 (м, 2H), 3,85 (с, 3H), 3,38 (м, 2H), 2,66 (м, 2H), 2,06 (м, 1H), 1,91 (м, 1H).
Получение 118: (±)-α-аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомеры 2, соединение 318)
Общая методика 3.
Исходное вещество: соединение 233.
1Н ЯМР (CD3OD) δ 7,73 (м, 2H), 7,04 (м, 2H), 5,47 (м, 1H), 5,02 (м, 1H), 4,89 (ш.д, 1H), 4,52 (м, 1H), 4,30 (м, 1H), 4,05 (м, 1H), 3,86 (с, 3H), 3,31 (м, 1H), 3,26 (м, 1H), 2,56 (м, 1H), 2,41 (м, 1H), 2,21 (м, 1H), 2,03 (м, 1H).
Получение 119: (αR)-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 1, соединение 319)
Общая методика 3.
Исходное вещество: соединение 236.
1Н ЯМР (CD3OD) δ 7,82 (м, 2H), 7,07 (м, 2H), 4,46 (м, 1H), 4,23 (м, 2H), 3,89 (с, 3H), 3,43 (м, 2H), 2,04 (м, 2H), 1,84 (м, 2H), 1,69 (м, 1H), 1,05 (д, 3H), 1,03 (д, 3H).
Получение 120: (αR)-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 2, соединение 320)
Общая методика 3.
Исходное вещество: соединение 237.
1Н ЯМР (CD3OD) δ 7,79 (м, 2H), 7,09 (м, 2H), 4,58 (м, 1H), 4,36 (м, 1H), 4,01 (м, 1H), 3,90 (с, 3H), 3,57 (м, 1H), 3,31 (м, 1H), 2,27 (м, 1H), 2,14 (м, 1H), 1,62 (м, 2H), 1,42 (м, 1H), 0,82 (д, 3H), 0,59 (д, 3H).
Получение 121: (±)-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфорепан-3-уксусная кислота (диастереомеры 1, соединение 321)
Общая методика 3.
Исходное вещество: соединение 238.
1Н ЯМР (CD3OD) δ 7,72 (м, 2H), 6,98 (м, 2H), 4,58 (м, 1H), 4,30 (м, 1H), 4,18 (м, 1H), 3,83 (с, 3H), 3,21 (м, 1H), 3,10 (м, 1H), 2,03-1,55 (м, 7H), 1,03 (д, 3H), 0,98 (д, 3H).
Получение 122: (±)-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфорепан-3-уксусная кислота (диастереомеры 2, соединение 322)
Общая методика 3.
Исходное вещество: соединение 239.
1Н ЯМР (CD3OD) δ 7,72 (м, 2H), 7,03 (м, 2H), 4,72 (м, 1H), 4,35 (м, 1H), 4,16 (м, 1H), 3,85 (с, 3H), 3,22 (м, 1H), 3,01 (м, 1H), 1,89 (м, 3H), 1,68 (м, 2H), 1,30 (м, 2H), 0,81 (д, 3H), 0,79 (д, 3H).
Получение 123: (αS)-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 1, соединение 323)
Общая методика 3.
Исходное вещество: соединение 240.
13С ЯМР (DMSO-d6) δ 174,0, 161,8, 133,2, 122,5, 114,1, 67,3, 55,2, 55,2, 41,1, 38,1, 26,6, 24,1, 23,2, 21,4.
Получение 124: (αS)-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 2, соединение 324)
Общая методика 3.
Исходное вещество: соединение 241.
13С ЯМР (DMSO-d6) δ 174,1, 163,1, 162,0, 133,4, 122,8, 114,0, 66,4, 55,4, 54,9, 40,3, 37,6, 25,8, 24,0, 22,8, 21,0.
Получение 125: (±)-2-(4-метоксифенил)-α-октил-2-оксо-1,3,2-оксазафосфорепан-3-уксусная кислота (диастереомеры 1, соединение 325)
Общая методика 3.
Исходное вещество: соединение 242.
1Н ЯМР (CD3OD) δ 7,72 (м, 2H), 6,98 (м, 2H), 4,62 (м, 1H), 4,18 (м, 1H), 4,13 (м, 1H), 3,83 (с, 3H), 3,21 (м, 1H), 3,11 (м, 1H), 2,00-1,20 (м, 18H), 0,90 (ш.т, 3H).
Получение 126: (±)-2-(4-метоксифенил)-α-октил-2-оксо-1,3,2-оксазафосфорепан-3-уксусная кислота (диастереомеры 2, соединение 326)
Общая методика 3.
Исходное вещество: соединение 243.
1Н ЯМР (CD3OD) δ 7,73 (м, 2H), 7,02 (м, 2H), 4,71 (м, 1H), 4,25 (м, 1H), 4,17 (м, 1H), 3,85 (с, 3H), 3,17 (м, 1H), 3,01 (м, 1H), 1,90 (м, 3H), 1,77 (м, 1H), 1,66 (м, 1H), 1,52 (м, 1H), 1,37-1,04 (м, 10H), 0,96 (м, 2H), 0,88 (м, 3H).
Получение 127: (αR)-2-(4-метоксифенил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 1, соединение 327)
Общая методика 3.
Исходное вещество: соединение 246.
13С ЯМР (CD3OD) δ 164,8, 139,2, 135,3, 130,9, 129,8, 128,0, 122,7, 115,5, 68,8, 56,3, 43,3, 37,9, 28,1.
Получение 128: (αR)-2-(4-метоксифенил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 2, соединение 328)
Общая методика 3.
Исходное вещество: соединение 247.
13С ЯМР (CD3OD) δ 179,5, 164,4, 140,2, 136,1, 130,4, 129,3, 127,2, 119,6, 114,9, 67,8, 63,0, 55,9, 42,1, 36,2, 27,4.
Получение 129: (±)-2-(4-метоксифенил)-2-оксо-α-пропил-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомеры 1, соединение 329)
Соединение 317 (0,18 ммоль) растворяли в метаноле (4 мл), прибавляли 10% Pd/C (25 мг) и гидрировали смесь в течение 6 ч, фильтровали через целит и концентрировали при пониженном давлении, получая соединение 329.
1Н ЯМР (CD3OD) δ 7,74 (м, 2H), 7,04 (м, 2H), 4,54 (м, 1H), 4,32 (м, 1H), 3,89 (м, 1H), 3,86 (с, 3H), 3,54 (м, 1H), 3,24 (м, 1H), 2,22 (м, 1H), 2,08 (м, 1H), 1,74 (м, 1H), 1,63 (м, 1H), 1,17 (м, 1H), 1,00 (м, 1H), 0,72 (т, 3H).
Получение 130: (±)-2-(4-метоксифенил)-2-оксо-α-пропил-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомеры 2, соединение 330)
Соединение 318 (0,16 ммоль) растворяли в метаноле (5 мл), прибавляли 10% Pd/C (25 мг) и гидрировали смесь в течение 5 ч, фильтровали через целит и концентрировали при пониженном давлении, получая соединение 330.
1Н ЯМР (CD3OD) δ 7,80 (м, 2H), 7,02 (м, 2H), 4,40 (м, 1H), 4,20 (м, 1H), 4,04 (м, 1H), 3,84 (с, 3H), 3,39 (м, 2H), 2,14-1,40 (м, 6H), 0,99 (т, 3H).
Получение 131: (±)-α-аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-уксусная кислота (диастереомеры 1, соединение 331)
Общая методика 3.
Исходное вещество: соединение 234.
1Н ЯМР (CD3OD) δ 7,73 (м, 2H), 6,98 (м, 2H), 5,93 (м, 1H), 5,20 (м, 1H), 5,13 (м, 1H), 4,61 (м, 1H), 4,35 (м, 1H), 4,15 (м, 1H), 3,83 (с, 3H), 3,20 (м, 1H), 3,07 (м, 1H), 2,75 (м, 1H), 2,58 (м, 1H), 1,88 (м, 2H), 1,78 (м, 2H).
Получение 132: (±)-α-аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-уксусная кислота (диастереомеры 2, соединение 332)
Общая методика 3.
Исходное вещество: соединение 235.
1Н ЯМР (CD3OD) δ 7,72 (м, 2H), 7,00 (м, 2H), 5,50 (м, 1H), 4,92 (м, 1H), 4,77 (м, 1H), 4,23 (м, 1H), 4,11 (м, 1H), 3,84 (с, 3H), 3,25 (м, 1H), 2,95 (м, 2H), 2,52 (м, 1H), 2,24 (м, 1H), 2,06-1,72 (м, 3H), 1,62 (м, 1H).
Получение 133: (±)-α-аллил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомеры 1, соединение 333)
Общая методика 3.
Исходное вещество: соединение 250.
1Н ЯМР (CD3OD) δ 7,82 (м, 2H), 7,41 (м, 2H), 7,20 (м, 1H), 7,06 (м, 2H), 7,03 (м, 2H), 5,95 (м, 1H), 5,21 (м, 1H), 5,13 (м, 1H), 4,41 (м, 1H), 4,23 (м, 2H), 3,39 (м, 2H), 2,72 (м, 1H), 2,62 (м, 1H), 2,08 (м, 1H), 1,92 (м, 1H).
Получение 134: (±)-α-аллил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомеры 2, соединение 334)
Общая методика 3.
Исходное вещество: соединение 252.
1Н ЯМР (CD3OD) δ 7,77 (м, 2H), 7,42 (м, 2H), 7,21 (м, 1H), 7,06 (м, 4H), 5,48 (м, 1H), 5,03 (м, 1H), 4,89 (м, 1H), 4,54 (м, 1H), 4,32 (м, 1H), 4,10 (м, 1H), 3,49 (м, 1H), 3,28 (м, 1H), 2,59 (м, 1H), 2,45 (м, 1H), 2,23 (м, 1H), 2,04 (м, 1H).
Получение 135: (±)-α-бутил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-уксусная кислота (диастереомеры 1, соединение 335)
Общая методика 3.
Исходное вещество: соединение 253.
1Н ЯМР (CD3OD) δ 7,77 (м, 2H), 7,41 (м, 2H), 7,20 (м, 1H), 7,04 (м, 4H), 4,74 (м, 1H), 4,26 (м, 1H), 4,17 (м, 1H), 3,40-2,90 (м, 2H), 2,00-0,84 (м, 10H), 0,77 (т, 3H).
Получение 136: (±)-α-бутил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-уксусная кислота (диастереомеры 2, соединение 336)
Общая методика 3.
Исходное вещество: соединение 254.
1Н ЯМР (CD3OD) δ 7,81 (м, 2H), 7,39 (м, 2H), 7,18 (м, 1H), 7,03 (м, 2H), 6,98 (м, 2H), 4,65 (м, 1H), 4,15 (м, 1H), 3,97 (м, 1H), 3,35 (м, 1H), 3,10 (м, 1H), 2,06-1,60 (м, 6H), 1,40 (м, 4H), 0,91 (ш.т, 3H).
Получение 137: (αR)-α-(2-метилпропил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 1, соединение 337)
Общая методика 3.
Исходное вещество: соединение 255.
1Н ЯМР (CD3OD) δ 7,81 (м, 2H), 7,41 (м, 2H), 7,20 (м, 1H), 7,06 (м, 2H), 7,03 (м, 2H), 4,43 (м, 1H), 4,21 (м, 2H), 3,40 (м, 2H), 2,00 (м, 2H), 1,79 (м, 2H), 1,66 (м, 1H), 1,01 (д, 3H), 0,99 (д, 3H).
Получение 138: (αR)-α-(2-метилпропил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 2, соединение 338)
Общая методика 3.
Исходное вещество: соединение 256.
1Н ЯМР (CD3OD) δ 7,79 (м, 2H), 7,41 (м, 2H), 7,21 (м, 1H), 7,10-7,00 (м, 4H), 4,55 (м, 1H), 4,34 (м, 1H), 3,98 (м, 1H), 3,53 (м, 1H), 3,26 (м, 1H), 2,24 (м, 1H), 2,09 (м, 1H), 1,59 (м, 2H), 1,38 (м, 1H), 0,79 (д, 3H), 0,58 (д, 3H).
Получение 139: (±)-α-октил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-уксусная кислота (диастереомеры 1, соединение 339)
Общая методика 3.
Исходное вещество: соединение 257.
1Н ЯМР (CD3OD) δ 7,76 (м, 2H), 7,40 (м, 2H), 7,19 (м, 1H), 7,05 (м, 2H), 7,00 (м, 2H), 4,64 (д.кв, 1H), 4,17 (м, 2H), 3,15 (м, 2H), 2,02-1,25 (м, 18H), 0,90 (ш.т, 3H).
Получение 140: (±)-α-октил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-уксусная кислота (диастереомеры 2, соединение 340)
Общая методика 3.
Исходное вещество: соединение 258.
MS. Вычислено для C26H36NO5P 473,23; найдено [M+H]+ =474, [M-H]-=472.
Получение 141: (αR)-α-(2-метилэтил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 1, соединение 341)
Общая методика 3.
Исходное вещество: соединение 259.
13С ЯМР (CD3OD) δ 175,4, 162,6, 157,1, 134,8, 131,2, 125,7, 125,5, 121,1, 118,7, 69,1, 65,7, 42,8, 28,4, 27,9, 20,1, 20,0.
Получение 142: (αR)-α-(2-метилэтил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 2, соединение 342)
Общая методика 3.
Исходное вещество: соединение 294.
13С ЯМР (CD3OD) δ 178,6, 162,9, 156,9, 136,4, 131,3, 125,8, 124,3, 121,1, 118,2, 68,4, 67,3, 42,2, 27,3, 20,9, 19,6.
Получение 143: (±)-2-(4-(4-хлорфенокси)фенил)-2-оксо-1,3,2-оксазафосфорепан-3-уксусная кислота (соединение 343)
Общая методика 3.
Исходное вещество: соединение 268.
13С ЯМР (DMSO-d6) δ 173,1, 158,9, 154,5, 133,3, 130,0, 128,0, 126,6, 121,1, 117,5, 64,5, 48,8, 46,6, 29,0, 25,7.
Получение 144: (αR)-2-[4-(4-хлофенокси)фенил]-α-(2-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 1, соединение 344)
Общая методика 3.
Исходное вещество: соединение 278.
13С ЯМР (CD3OD) δ 175,4, 162,0, 156,0, 135,0, 131,2, 130,6, 126,2, 122,4, 119,0, 69,1, 65,7, 42,8, 28,3, 27,9, 20,1, 20,0.
Получение 145: (αR)-α-(2-метилэтил)-2-оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 1, соединение 345)
Общая методика 3.
Исходное вещество: соединение 287.
13С ЯМР (CD3OD) δ 174,8, 160,9, 160,8, 135,1, 128,6, 125,0, 120,4, 120,2, 69,2, 65,3, 42,7, 28,3, 27,8, 20,1, 19,9.
Получение 146: (αR)-α-(2-метилэтил)-2-оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфоринан-3-уксусная кислота (диастереомер 2, соединение 346)
Общая методика 3.
Исходное вещество: соединение 288.
MS. Вычислено для C21H23F3NO5P 457,13; найдено [M+H]+=458, [M-H]-=456.
Получение 147: (±)-2-[4-(4-бромфенокси)фенил]-2-оксо-1,3,2-оксазафосфоринан-3-уксусная кислота (соединение 347)
Общая методика 3.
Исходное вещество: соединение 289.
13С ЯМР (CD3OD) δ 173,3, 162,3, 156,5, 135,3, 134,2, 125,6, 122,9, 119,1, 118,1, 69,1, 49,7, 48,5, 27,2.
Получение 148: (±)-2-[4-(4-бромфенокси)фенил]-2-оксо-1,3,2-оксазафосфорепан-3-уксусная кислота (соединение 348)
Общая методика 3.
Исходное вещество: соединение 290.
13С ЯМР (CD3OD) δ 176,9, 161,8, 156,7, 134,9, 134,2, 125,8, 122,8, 118,9, 117,9, 67,3, 50,8, 30,7, 27,9.
Получение 149: (±)-2-(4-нитрофенил)-2-оксо-1,3,2-оксазафосфорепан-3-уксусная кислота (соединение 349)
Общая методика 3.
Исходное вещество: соединение 291.
1Н ЯМР (DMSO-d6) δ 8,27 (м, 2H), 8,18 (м, 2H), 6,7 (ш.с, 1H), 4,43 (кв, 1H), 4,11 (дд, 1H), 3,90 (дд, 1H), 3,60 (дд, 1H), 2,93 (м, 2H), 1,87-1,50 (м, 4H).
Получение 150: (±)-2-[N-(4-хлорбензоил)-4-аминофенил]-2-оксо-1,3,2-оксазафосфорепан-3-уксусная кислота (соединение 350)
Общая методика 3.
Исходное вещество: соединение 292.
1Н ЯМР (DMSO-d6) δ 10,51 (ш.с, 1H), 8,00 (м, 2H), 7,85 (м, 4H), 7,62 (м, 2H), 4,37 (кв, 1H), 4,03 (дд, 1H), 3,87 (дд, 1H), 3,59 (дд, 1H), 2,95 (м, 2H), 1,85-1,45 (м, 4H).
Получение 151: (±)-2-(N-(4-бензоил-4-аминофенил)-2-оксо-1,3,2-оксазафосфорепан-3-уксусная кислота (соединение 351)
Общая методика 3.
Исходное вещество: соединение 293.
13С ЯМР (CD3OD) δ 174,4, 169,0, 143,6, 136,1, 133,4, 133,1, 129,7, 128,7, 126,5, 121,3, 67,2, 30,7, 27,7.
Получение 152: (±)-2-фенил-2-тиоксо-1,3,2-оксазафосфоринан-3-уксусная кислота (соединение 352)
Получение 153: (±)-2-фенил-2-тиоксо-1,3,2-оксазафосфорепан-3-уксусная кислота (соединение 353)
Общая методика 3.
Исходное вещество: соединение 275.
13С ЯМР (DMSO-d6) δ 172,2, 135,4, 131,1, 130,0, 128,1, 64,4, 48,9, 47,5, 28,5, 25,0.
Пример 1: (±)-2-(4-хлорфенокси)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 101)
Общая методика 2.
Исходное вещество: соединение 210.
13С ЯМР (DMSO-d6) δ 165,0, 149,5, 129,5, 128,5, 122,0, 70,2, 48,0, 47,6, 25,3.
Пример 2: (±)-2-(4-хлорфенокси)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 102)
Общая методика 2.
Исходное вещество: соединение 211.
MS. Вычислено для C12H16ClN2O5P 334,05; найдено [M+H]+=335, [M+Na]+=357.
Пример 3: (±)-2-[(4-бромфенил)метил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 103)
Общая методика 2.
Исходное вещество: соединение 212.
1Н ЯМР (DMSO-d6) δ 10,0-8,0 (ш.с, 2H), 7,47 (м, 2H), 7,27 (м, 2H), 4,21 (м, 2H), 3,70-2,90 (м, 6H), 1,92 (м, 1H), 1,49 (м, 1H).
Пример 4: (±)-2-[(4-бифенилил)метил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 104)
Общая методика 2.
Исходное вещество: соединение 213.
1Н ЯМР (DMSO-d6) δ 11,0-8,0 (ш.с, 2H), 7,65 (м, 2H), 7,59 (м, 2H), 7,46 (м, 2H), 7,42-7,30 (м, 3H), 4,24 (м, 2H), 3,65-3,15 (м, 5H), 3,02 (м, 1H), 1,94 (м, 1H), 1,51 (м, 1H).
Пример 5: (±)-2-(4-бифенилил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 105)
Общая методика 2.
Исходное вещество: соединение 214.
1Н ЯМР (DMSO-d6) δ 11,0-9,8 (ш.с, 1H), 9,2-8,7 (ш.с, 1H), 7,87 (м, 1H), 7,80 (м, 3H), 7,72 (м, 2H), 7,51 (м, 2H), 7,42 (м, 1H), 4,36 (м, 1H), 4,13 (м, 1H), 3,58 (м, 2H), 3,40-3,10 (м, 2H), 2,07 (м, 1H), 1,86 (м, 1H).
Пример 6: (±)-2-(4-бифенилил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 106)
Общая методика 2.
Исходное вещество: соединение 215.
13С ЯМР (DMSO-d6) δ 166,8, 142,9, 139,4, 131,7, 130,2, 129,1, 128,1, 126,9, 126,5, 64,8, 46,5, 29,0, 25,9.
Пример 7: (±)-2-гептил-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 107)
Общая методика 2.
Исходное вещество: соединение 216.
1Н ЯМР (DMSO-d6) δ 11,0-9,8 (ш.с, 1H), 9,1-8,6 (ш.с, 1H), 4,16 (м, 2H), 3,55 (дд, 1H), 3,40-3,15 (м, 2H), 2,98 (м, 1H), 2,05-1,60 (м, 4H), 1,55-1,12 (м, 10H), 0,87 (т, 3H).
Пример 8: (±)-2-гептил-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 108)
Общая методика 2.
Исходное вещество: соединение 217.
13С ЯМР (DMSO-d6) δ 166,9, 63,5, 46,6, 46,4, 31,0, 30,1, 28,9, 28,2, 26,1, 25,6, 22,1, 22,0, 13,8.
Пример 9: (±)-2-оксо-2-[4-(фениламино)фенил]-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 109)
Общая методика 2.
Исходное вещество: соединение 218.
1Н ЯМР (DMSO-d6) δ 11,0-9,8 (ш.с, 1H), 9,15-8,50 (м, 2H), 7,59 (м, 2H), 7,30 (м, 2H), 7,16 (м, 2H), 7,09 (м, 2H), 6,95 (м, 1H), 4,29 (м, 1H), 4,08 (м, 1H), 3,70-2,80 (м, 4H), 2,00 (м, 1H), 1,88 (м, 1H).
Пример 10: (±)-2-оксо-2-фенил-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 110)
Общая методика 2.
Исходное вещество: соединение 219.
1Н ЯМР (DMSO-d6) δ 10,6-9,9 (ш.с, 1H), 9,1-8,7 (ш.с, 1H), 7,77 (м, 2H), 7,53 (м, 3H), 4,34 (м, 1H), 4,10 (м, 1H), 3,75-2,50 (м, 4H), 2,04 (м, 1H), 1,82 (м, 1H).
Пример 11: (±)-2-оксо-2-фенил-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 111)
Общая методика 2.
Исходное вещество: соединение 220.
13С ЯМР (DMSO-d6) δ 166,7, 131,5, 131,3, 131,0, 128,2, 64,7, 46,5, 46,4, 29,0, 25,9.
Пример 12: 2-оксо-2-фенил-1,3,2-оксазафосфоронан-3-ацетогидроксамовая кислота (соединение 112)
Общая методика 2.
Исходное вещество: соединение 297.
1Н ЯМР (DMSO-d6) δ 10,53 (ш.с, 1H), 8,91 (ш.с, 1H), 7,97 (м, 2H), 7,59-7,42 (м, 3H), 4,48 (м, 1H), 4,01 (дд, 1H), 3,88 (м, 1H), 3,42 (м, 1H), 2,89 (м, 1H), 2,62 (м, 1H), 1,90-1,60 (м, 2H), 1,58-1,05 (м, 6H).
Пример 13: (±)-α-бутил-2-оксо-2-фенил-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 113)
Общая методика 1.
Исходное вещество: соединение 307.
13С ЯМР (DMSO-d6) δ 168,1, 131,4, 131,1, 130,7, 128,1, 64,7, 55,0, 42,2, 31,2, 29,4, 28,7, 28,0, 21,9, 13,8.
Пример 14: (±)-α-бутил-2-оксо-2-фенил-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 114)
Общая методика 1.
Исходное вещество: соединение 308.
1Н ЯМР (DMSO-d6) δ 10,60 (ш.с, 1H), 8,86 (ш.с, 1H), 7,72 (м, 2H), 7,56 (м, 1H), 7,49 (м, 2H), 4,34 (м, 1H), 4,11 (м, 1H), 3,94 (м, 1H), 2,84 (м, 1H), 1,86-1,49 (м, 5H), 1,26 (м, 1H), 1,09 (м, 2H), 0,85 (м, 2H), 0,67 (т, 3H).
Пример 15: (±)-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 115)
Общая методика 2.
Исходное вещество: соединение 223.
1Н ЯМР (DMSO-d6) δ 11,0-8,0 (м, 2H), 7,71 (м, 2H), 7,04 (м, 2H), 4,30 (м, 1H), 4,06 (м, 1H), 3,82 (с, 3H), 3,46 (м, 2H), 3,21 (м, 2H), 2,01 (м, 1H), 1,85 (м, 1H).
Пример 16: (±)-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 116)
Общая методика 2.
Исходное вещество: соединение 224.
13С ЯМР (DMSO-d6) δ 166,7, 161,5, 132,8, 122,7, 113,6, 64,4, 55,1, 46,4, 46,3, 28,9, 25,8.
Пример 17: (±)-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоронан-3-ацетогидроксамовая кислота (соединение 117)
Общая методика 2.
Исходное вещество: соединение 225.
13С ЯМР (DMSO-d6) δ 166,4, 161,6, 133,5, 122,4, 113,7, 59,6, 55,3, 44,0, 41,5, 27,3, 23,9, 18,5, 17,9.
Пример 18: (αR)-2-(4-метоксифенил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1, соединение 118)
Общая методика 1.
Исходное вещество: соединение 300.
1Н ЯМР (CD3OD) δ 7,60 (м, 2H), 7,06 (м, 2H), 4,36 (м, 1H), 4,11 (м, 1H), 3,85 (с, 3H), 3,71 (м, 1H), 3,42 (м, 2H), 2,30 (м, 1H), 2,11 (м, 1H), 1,86 (м, 1H), 1,12 (д, 3H), 0,96-0,88 (д, 3H).
Пример 19: (αR)-2-(4-метоксифенил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2, соединение 119)
Общая методика 1.
Исходное вещество: соединение 301.
13С ЯМР (DMSO-d6) δ 167,9, 161,8, 133,6, 122,2, 113,7, 66,3, 60,4, 55,2, 25,7, 25,6, 19,3, 19,3.
Пример 20: (±)-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 1, соединение 120)
Общая методика 1.
Исходное вещество: соединение 311.
13С ЯМР (DMSO-d6) δ 168,0, 161,5, 132,8, 122,5, 114,1, 67,2, 55,2, 53,9, 41,2, 29,4, 27,6, 26,7, 21,7, 13,8.
Пример 21: (±)-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 2, соединение 121)
Общая методика 1.
Исходное вещество: соединение 312.
13С ЯМР (CDCl3) δ 168,7, 163,3, 134,6, 119,6, 114,0, 66,4, 55,4, 55,0, 40,5, 27,8, 26,6, 26,3, 22,1, 13,9.
Пример 22: (±)-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1, соединение 122)
Общая методика 1.
Исходное вещество: соединение 313.
13С ЯМР (DMSO-d6) δ 168,2, 161,3, 132,6, 122,8, 113,6, 64,5, 55,1, 55,0, 42,1, 31,2, 29,4, 28,7, 28,0, 21,9, 13,9.
Пример 23: (±)-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2, соединение 123)
Общая методика 1.
Исходное вещество: соединение 314.
13С ЯМР (DMSO-d6) δ 168,1, 161,6, 132,7, 122,7, 113,7, 64,9, 55,2, 54,2, 41,0, 28,8, 28,4, 27,8, 27,5, 21,6, 13,6.
Пример 24: (±)-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота (диастереомеры 1, соединение 124)
Общая методика 1.
Исходное вещество: соединение 315.
1Н ЯМР (DMSO-d6) δ 10,77 (ш.с, 1H), 8,75 (ш.с, 1H), 7,59 (м, 2H), 6,99 (м, 2H), 4,26 (м, 1H), 3,94 (м, 2H), 3,80 (с, 3H), 3,53 (м, 1H), 2,82 (м, 1H), 1,93-1,40 (м, 8H), 1,27 (м, 2H), 1,17 (м, 2H), 0,84 (т, 3H).
Пример 25: (±)-α-бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота (диастереомеры 2, соединение 125)
Общая методика 1.
Исходное вещество: соединение 316.
MS. Вычислено для C18H29N2O5P 384,18; найдено [M+H]+=385, [M-H]-=383.
Пример 26: (±)-α-аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 1, соединение 126)
Общая методика 1.
Исходное вещество: соединение 317.
13С ЯМР (DMSO-d6) δ 167,4, 161,6, 134,4, 132,8, 122,5, 117,4, 114,1, 67,1, 55,2, 53,6, 41,1, 34,2, 26,6.
Пример 27: (±)-α-аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 2, соединение 127)
Общая методика 1.
Исходное вещество: соединение 318.
13С ЯМР (DMSO-d6) δ 167,6, 162,0, 134,5, 133,7, 121,6, 117,3, 113,9, 66,7, 55,2, 54,0, 32,8, 25,7.
Пример 28: (±)-α-аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1, соединение 128)
Общая методика 1.
Исходное вещество: соединение 331.
13С ЯМР (DMSO-d6) δ 167,5, 161,4, 134,6, 132,7, 122,7, 117,5, 113,7, 64,5, 55,1, 54,5, 42,0, 35,6, 29,0, 28,7.
Пример 29: (±)-α-аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2, соединение 129)
Общая методика 1.
Исходное вещество: соединение 332.
1Н ЯМР (DMSO-d6) δ 10,54 (ш.с, 1H), 8,87 (ш.с, 1H), 7,64 (м, 2H), 7,03 (м, 2H), 5,39 (м, 1H), 4,94 (дд, 1H), 4,81 (дд, 1H), 4,33 (м, 1H), 4,05 (м, 2H), 3,81 (с, 3H), 2,81 (м, 1H), 2,39 (м, 1H), 2,07 (м, 1H), 1,76 (м, 2H), 1,57 (м, 2H).
Пример 30: (αR)-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1, соединение 130)
Общая методика 1.
Исходное вещество: соединение 319.
13С ЯМР (DMSO-d6) δ 168,0, 161,6, 132,8, 122,4, 114,1, 67,2, 55,2, 52,1, 41,1, 26,7, 24,0, 22,8, 21,9.
Пример 31: (αR)-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2, соединение 131)
Общая методика 1.
Исходное вещество: соединение 320.
13С ЯМР (DMSO-d6) δ 168,1, 162,0, 133,5, 121,9, 113,9, 66,5, 55,3, 52,0, 40,1, 37,3, 25,8, 23,7, 22,3, 21,8.
Пример 32: (αS)-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1, соединение 132)
Общая методика 1.
Исходное вещество: соединение 323.
13С ЯМР (DMSO-d6) δ 168,1, 161,5, 132,8, 122,5, 114,1, 67,2, 55,2, 52,1, 41,1, 26,8, 24,0, 22,8, 21,9.
Пример 33: (αS)-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2, соединение 133)
Общая методика 1.
Исходное вещество: соединение 324.
13С ЯМР (DMSO-d6) δ 168,1, 162,0, 133,5, 122,0, 113,9, 66,5, 55,3, 52,0, 40,1, 37,3, 25,8, 23,7, 22,3, 21,8.
Пример 34: (±)-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1, соединение 134)
Общая методика 1.
Исходное вещество: соединение 321.
13С ЯМР (DMSO-d6) δ 168,1, 161,3, 132,7, 122,7, 113,6, 64,5, 55,1, 53,2, 41,9, 40,5, 29,3, 28,7, 24,3, 22,5, 22,4.
Пример 35: (±)-2-(4-метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2, соединение 135)
Общая методика 1.
Исходное вещество: соединение 322.
1Н ЯМР (DMSO-d6) δ 10,3 (ш.с, 1H), 8,85 (ш.с, 1H), 7,64 (м, 2H), 7,03 (м, 2H), 4,31 (м, 1H), 4,03 (м, 2H), 3,80 (с, 3H), 2,82 (м, 1H), 1,75 (м, 2H), 1,56 (м, 3Н), 1,30-0,88 (м, 2Н), 0,75 (д, 3Н), 0,69 (д, 3Н).
Пример 36: (±)-2-(4-метоксифенил)-α-пропил-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 1, соединение 136)
Общая методика 1.
Исходное вещество: соединение 329.
1Н ЯМР (DMSO-d6) δ 10,40 (ш.с, 1H), 8,85 (ш.с, 1H), 7,56 (м, 2H), 7,03 (м, 2H), 4,25 (м, 1H), 3,95 (м, 2H), 3,81 (с, 3H), 3,57 (м, 1H), 3,16 (м, 1H), 1,96-1,20 (м, 6H), 0,92 (т, 3H).
Пример 37: (±)-2-(4-метоксифенил)-α-пропил-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 2, соединение 137)
Общая методика 1.
Исходное вещество: соединение 330.
1Н ЯМР (DMSO-d6) δ 10,57 (ш.с, 1H), 8,86 (ш.с, 1H), 7,67 (м, 2H), 7,06 (м, 2H), 4,36-4,10 (м, 2H), 3,82 (с, 3H), 3,62 (м, 1H), 3,48 (м, 1H), 3,10 (м, 1H), 2,01 (м, 1H), 1,90 (м, 1H), 1,58 (м, 1H), 1,44 (м, 1H), 1,03 (м, 1H), 0,88 (м, 1H), 0,65 (т, 3H).
Пример 38: (±)-2-(4-метоксифенил)-α-октил-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1, соединение 138)
Общая методика 1.
Исходное вещество: соединение 325.
13С ЯМР (CDCl3) δ 168,2, 161,3, 132,6, 122,8, 113,7, 64,5, 55,1, 42,3, 31,5, 31,2, 29,4, 28,9, 28,8, 28,5, 25,8, 22,0, 13,9.
Пример 39: (±)-2-(4-метоксифенил)-α-октил-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2, соединение 139)
Общая методика 1.
Исходное вещество: соединение 326.
1Н ЯМР (DMSO-d6) δ 10,55 (ш.с, 1H), 8,84 (ш.с, 1H), 7,64 (м, 2H), 7,02 (м, 2H), 4,31 (м, 1H), 4,07 (м, 1H), 3,91 (кв, 1H), 3,80 (с, 3H), 3,22 (м, 1H), 2,84 (м, 1H), 1,85-0,93 (м, 18H), 0,84 (т, 3H).
Пример 40: (αR)-2-(4-метоксифенил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1, соединение 140)
Общая методика 1.
Исходное вещество: соединение 327.
1Н ЯМР (CD3OD) δ 7,64 (м, 2H), 7,32-7,15 (м, 5H), 7,04 (м, 2H), 4,21 (м, 2H), 4,10 (м, 1H), 3,84 (с, 3H), 3,83 (м, 1H), 3,43 (м, 1H), 3,31 (м, 1H), 3,06 (дд, 1H), 1,87 (м, 2H).
Пример 41: (αS)-2-(4-метоксифенил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1, соединение 141)
Общие методики: 3, затем 1.
Исходное вещество: соединение 244 (промежуточную карбоновую кислоту не охарактеризовывали).
1Н ЯМР (CD3OD) δ 7,54 (м, 2H), 7,23-7,05 (м, 5H), 6,94 (м, 2H), 4,12 (м, 2H), 3,99 (м, 1H), 3,75 (с, 3H), 3,72 (м, 1H), 3,40-3,18 (м, 2H), 2,96 (дд, 1H), 1,79 (м, 2H).
Пример 42: (αS)-2-(4-метоксифенил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2, соединение 142)
Общие методики: 3, затем 1.
Исходное вещество: соединение 245 (промежуточную карбоновую кислоту не охарактеризовывали).
1Н ЯМР (DMSO-d6) δ 10,55 (ш.с, 1H), 8,90 (ш.с, 1H), 7,23-7,16 (м, 3H), 7,10-6,94 (м, 4H), 6,78 (м, 2H), 4,27 (м, 1H), 4,05 (м, 2H), 3,78 (с, 3H), 3,63 (м, 1H), 3,12 (м, 1H), 2,90 (м, 2H), 2,06 (м, 1H), 1,75 (м, 1H).
Пример 43: (±)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 143)
Общая методика 2.
Исходное вещество: соединение 248.
1Н ЯМР (DMSO-d6) δ 10,5-8,5 (м, 2H), 7,78 (м, 2H), 7,45 (м, 2H), 7,23 (м, 1H), 7,11 (м, 2H), 7,05 (м, 2H), 4,32 (м, 1H).
Пример 44: (±)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 144)
Общая методика 2.
Исходное вещество: соединение 249.
1Н ЯМР (DMSO-d6) δ 11,0-10,1 (ш.с, 1H), 9,3-8,5 (ш.с, 1H), 7,82 (м, 2H), 7,44 (м, 2H), 7,22 (м, 1H), 7,10 (м, 2H), 7,03 (м, 2H), 4,35 (м, 1H), 4,05 (м, 1H), 3,82 (м, 1H), 3,54 (м, 1H), 2,91 (м, 2H), 1,88-1,43 (м, 4H).
Пример 45: (±)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота (соединение 145)
Общая методика 2.
Исходное вещество: соединение 250.
1Н ЯМР (DMSO-d6) δ 10,1 (ш.с, 1H), 8,89 (ш.с, 1H), 7,89 (м, 2H), 7,44 (м, 2H), 7,22 (м, 1H), 7,09 (м, 2H), 7,02 (м, 2H), 4,23 (м, 1H), 4,04-3,80 (м, 2H), 3,43 (м, 1H), 2,94 (м, 2H), 1,89-1,20 (м, 6H).
Пример 46: (±)-α-аллил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 1, соединение 146)
Общая методика 1.
Исходное вещество: соединение 333.
13С ЯМР (DMSO-d6) δ 167,6, 160,0, 155,2, 134,4, 134,0, 130,2, 124,7, 124,4, 119,6, 117,4, 117,4, 66,9, 54,0, 40,3, 32,9, 25,7.
Пример 47: (±)-α-аллил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 2, соединение 147)
Общая методика 1.
Исходное вещество: соединение 334.
1Н ЯМР (DMSO-d6) δ 10,3 (ш.с, 1H), 9,2 (ш.с, 1H), 7,63 (м, 2H), 7,45 (м, 2H), 7,23 (м, 1H), 7,11 (м, 2H), 7,04 (м, 2H), 5,76 (м, 1H), 5,17 (м, 1H), 5,09 (м, 1H), 4,26 (м, 1H), 4,10 (м, 1H), 3,98 (м, 1H), 3,61 (м, 1H), 3,17 (м, 1H), 2,50 (м, 2H), 1,89 (м, 1H), 1,70 (м, 1H).
Пример 48: (αR)-α-(2-метилпропил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1, соединение 148)
Общая методика 1.
Исходное вещество: соединение 337.
13С ЯМР (DMSO-d6) δ 168,0, 159,9, 155,3, 133,9, 130,2, 125,1, 124,4, 119,4, 117,6, 66,8, 52,0, 37,4, 25,9, 23,7, 22,3, 21,9.
Пример 49: (αR)-α-(2-метилпропил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2, соединение 149)
Общая методика 1.
Исходное вещество: соединение 338.
13С ЯМР (DMSO-d6) δ 168,0, 159,6, 155,1, 133,1, 130,2, 125,4, 124,4, 119,7, 117,5, 67,4, 52,1, 41,0, 26,7, 24,0, 22,8, 21,9.
Пример 50: (αR)-α-(2-метилэтил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1, соединение 150)
Общая методика 1.
Исходное вещество: соединение 341.
1Н ЯМР (DMSO-d6) δ 10,64-9,51 (с, 1H), 8,82-8,63 (с, 1H), 7,56 (м, 2H), 7,45 (м, 2H), 7,23 (м, 1H), 7,11 (м, 2H), 7,04 (м, 2H), 4,28 (м, 1H), 3,96 (м, 1H), 3,64 (м, 1H), 3,53 (т, 1H), 3,14 (м, 1H), 2,15 (м, 1H), 1,94 (м, 1H), 1,69 (м, 1H), 1,01 (д, 3H), 0,82 (д, 3H).
Пример 51: (αR)-α-(2-метилэтил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2, соединение 151)
Общая методика 1.
Исходное вещество: соединение 342.
1Н ЯМР (DMSO-d6) δ 10,4 (ш.с, 1H), 8,87 (с, 1H), 7,76 (м, 2H), 7,45 (м, 2H), 7,23 (м, 1H), 7,13-7,01 (м, 4H), 4,28 (м, 2H), 3,56 (м, 1H), 3,16 (м, 1H), 3,08 (м, 1H), 2,19-1,74 (м, 3H), 0,72 (д, 3H), 0,50 (д, 3H).
Пример 52: (±)-α-бутил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1, соединение 152)
Общая методика 1.
Исходное вещество: соединение 335.
1Н ЯМР (DMSO-d6) δ 10,66 (ш.с, 1H), 8,72 (ш.с, 1H), 7,67 (дд, 2H), 7,44 (ш.т, 2H), 7,22 (ш.т, 1H), 7,10 (ш.д, 2H), 6,99 (дд, 2H), 4,36 (кв, 1H), 4,16-3,75 (м, 3H), 2,74 (м, 1H), 1,90-1,12 (м, 10H), 0,88 (т, 3H).
Пример 53: (±)-α-бутил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2, соединение 153)
Общая методика 1.
Исходное вещество: соединение 336.
1Н ЯМР (DMSO-d6) δ 10,58 (ш.с, 1H), 8,86 (ш.с, 1H), 7,72 (м, 2H), 7,44 (м, 2H), 7,22 (м, 1H), 7,07 (м, 2H), 7,05 (м, 2H), 4,33 (м, 1H), 4,09 (м, 1H), 3,92 (кв, 1H), 3,31 (м, 1H), 2,84 (м, 1H), 1,88-1,50 (м, 4H), 1,29 (м, 2H), 1,11 (м, 2H), 0,87 (м, 2H), 0,70 (т, 3H).
Пример 54: (±)-α-октил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1, соединение 154)
Общая методика 1.
Исходное вещество: соединение 339.
MS. Вычислено для C26H37N2O5P 488,24; найдено [M+H]+=489, [M-H]-=487.
Пример 55: (±)-α-октил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2, соединение 155)
Общая методика 1.
Исходное вещество: соединение 340.
1Н ЯМР (DMSO-d6) δ 10,65 (ш.с, 1H), 8,71 (ш.с, 1H), 7,67 (м, 2H), 7,44 (м, 2H), 7,22 (м, 1H), 7,10 (м, 2H), 6,99 (дд, 2H),4,36 (кв, 1H), 4,17-3,75 (м, 3H), 2,75 (м, 1H), 1,89-1,10 (м, 18H), 0,87 (т, 3H).
Пример 56: (±)-2-оксо-2-(2-фенилэтил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 156)
Общая методика 2.
Исходное вещество: соединение 260.
1Н ЯМР (DMSO-d6) δ 11,0-9,2 (ш.с, 1H), 9,2-8,5 (ш.с, 1H), 7,28 (м, 4H), 7,19 (м, 1H), 4,21 (м, 2H), 3,63 (дд, 1H), 3,42-3,20 (м, 2H), 3,00 (м, 1H), 2,76 (м, 2H), 2,28-1,88 (м, 3H), 1,72 (м, 1H).
Пример 57: (±)-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота (соединение 157)
Общая методика 2.
Исходное вещество: соединение 261.
13С ЯМР (DMSO-d6) δ 166,5, 161,6, 133,1, 123,0, 113,6, 65,3, 55,3, 44,7, 44,6, 28,1, 24,6, 24,1.
Пример 58: (±)-2-оксо-2-фенил-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота (соединение 158)
Общая методика 2.
Исходное вещество: соединение 262.
13С ЯМР (DMSO-d6) δ 166,3, 131,7, 131,3, 131,1, 128,1, 65,5, 44,6, 44,5, 28,0, 24,5, 24,2.
Пример 59: (±)-2-гептил-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота (соединение 159)
Общая методика 2.
Исходное вещество: соединение 263.
13С ЯМР (DMSO-d6) δ 166,5, 64,8, 44,5, 43,9, 31,0, 30,1, 28,2, 27,9, 26,2, 24,7, 24,1, 22,0, 22,0, 13,8.
Пример 60: (αR)-2-(4-бифенилил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2, соединение 160)
Общая методика 1.
Исходное вещество: соединение 302.
MS. Вычислено для C20H25N2O4P 388,16; найдено [M+H]+=389, [M+Na]+=411.
Пример 61: (±)-2-[4-(4-хлорфенокси)фенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 161)
Общая методика 2.
Исходное вещество: соединение 268.
13С ЯМР (DMSO-d6) δ 166,6, 159,0, 154,4, 133,3, 130,0, 128,0, 126,1, 121,2, 117,5, 64,6, 46,4, 28,9, 25,8.
Пример 62: (±)-2-[4-(4-хлорфенокси)фенил]-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота (соединение 162)
Общая методика 2.
Исходное вещество: соединение 269.
13С ЯМР (DMSO-d6) δ 166,2, 159,0, 154,4, 133,4, 130,0, 128,0, 126,4, 121,1, 117,5, 65,5, 44,3, 27,9, 24,4, 24,0.
Пример 63: (αR)-2-[4-(4-хлорфенокси)фенил]-α-(2-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 163)
Общая методика 1.
Исходное вещество: соединение 344.
1Н ЯМР (DMSO-d6) δ 10,64 (ш.с, 1H), 8,81 (с, 1H), 7,58 (м, 2H), 7,49 (м, 2H), 7,14 (м, 2H), 7,07 (м, 2H), 4,28 (м, 1H), 3,97 (м, 1H), 3,66 (м, 1H), 3,52 (м, 1H), 3,14 (м, 1H), 2,16 (м, 1H), 1,94 (м, 1H), 1,70 (м, 1H), 1,01 (д, 3H), 0,82 (д, 3H).
Пример 64: (±)-2-(4'-бром-4-бифенилил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 164)
Общая методика 2.
Исходное вещество: соединение 270.
1Н ЯМР (DMSO-d6) δ 10,4 (ш.с, 1H), 9,0 (ш.с, 1H), 7,93-7,74 (м, 4H), 7,69 (ш.с, 4H), 4,36 (м, 1H), 4,13 (м, 1H), 3,69-3,13 (м, 4H), 2,06 (м, 1H), 1,86 (м, 1H).
Пример 65: (±)-2-(4'-бром-4-бифенилил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 165)
Общая методика 2.
Исходное вещество: соединение 271.
13С ЯМР (DMSO-d6) δ 166,6, 141,5, 138,4, 131,8, 131,7, 130,6, 128,9, 126,3, 121,6, 64,7, 46,4, 46,3, 28,9, 25,8.
Пример 66: (±)-2-(4'-бром-4-бифенилил)-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота (соединение 166)
Общая методика 2.
Исходное вещество: соединение 272.
MS. Вычислено для C19H22BrN2O4P 452,05; найдено [M-H]-=451.
Пример 67: (±)-2-[2-(1-нафтил)этил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 167)
Общая методика 2.
Исходное вещество: соединение 273.
13С ЯМР (CDCl3) δ 166,9, 136,7, 133,9, 131,3, 129,0, 127,3, 126,3, 125,8, 125,7, 125,6, 123,2, 67,0, 49,6, 47,4, 27,3, 26,0, 25,8.
Пример 68: (±)-2-фенил-2-тиоксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 168)
Общая методика 2.
Исходное вещество: соединение 274.
13С ЯМР (DMSO-d6) δ 165,2, 132,7, 132,2, 131,2, 128,5, 66,3, 49,4, 46,5, 25,5.
Пример 69: (±)-2-фенил-2-тиоксо-1,3,2-оксазафосфорепан-3-ацетамид (соединение 169)
Общая методика 2.
Исходное вещество: соединение 275.
13С ЯМР (DMSO-d6) δ 166,5, 135,6, 130,9, 130,1, 128,0, 64,3, 47,3, 46,9, 28,4, 24,8.
Пример 70: (±)-2-фенил-2-тиоксо-1,3,2-оксазафосфорокан-3-ацетамид (соединение 170)
Общая методика 2.
Исходное вещество: соединение 276.
13С ЯМР (DMSO-d6) δ 166,0, 136,0, 130,9, 130,4, 128,0, 65,5, 44,9, 44,4, 27,5, 24,1, 23,8.
Пример 71: (±)-2-[4-(4-хлорфенокси)фенил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 171)
Общая методика 2.
Исходное вещество: соединение 277.
13С ЯМР (DMSO-d6) δ 165,7, 159,4, 154,2, 133,7, 130,0, 128,2, 125,7, 121,4, 117,7, 67,1, 47,9, 47,1, 25,4.
Пример 72: (±)-2-(4-бромфенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 172)
Общая методика 2.
Исходное вещество: соединение 280.
1Н ЯМР (DMSO-d6) δ 10,6-9,8 (ш.с, 1H), 9,2-8,7 (ш.с, 1H), 7,71 (м, 4H), 4,34 (м, 1H), 4,12 (м, 1H), 3,95-3,30 (м, 2H), 3,25 (м, 2H), 2,05 (м, 1H), 1,83 (м, 1H).
Пример 73: (±)-2-(4-бромфенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 173)
Общая методика 2.
Исходное вещество: соединение 281.
13С ЯМР (DMSO-d6) δ 166,5, 133,0, 131,1, 130,7, 125,2, 64,8, 46,4, 46,3, 28,8, 25,8.
Пример 74: (±)-2-оксо-2-(4-фенилметоксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 174)
Общая методика 2.
Исходное вещество: соединение 282.
1Н ЯМР (DMSO-d6) δ 7,72 (м, 2H), 7,50-7,30 (м, 5H), 7,12 (м, 2H), 5,17 (с, 2H), 4,30 (м, 1H), 4,07 (м, 1H), 3,46 (м, 2H), 3,22 (м, 2H), 2,01 (м, 1H), 1,85 (м, 1H).
Пример 75: (±)-2-оксо-2-(4-фенилметоксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 175)
Общая методика 2.
Исходное вещество: соединение 283.
13С ЯМР (DMSO-d6) δ 166,7, 160,5, 136,6, 132,8, 128,4, 127,8, 127,6, 123,0, 114,4, 69,2, 64,5, 46,3, 28,9, 25,7.
Пример 76: (±)-2-оксо-2-(4-фенилметоксифенил)-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота (соединение 176)
Общая методика 2.
Исходное вещество: соединение 284.
13С ЯМР (DMSO-d6) δ 166,3, 160,5, 136,6, 133,0, 128,4, 127,8, 127,6, 123,2, 114,3, 69,1, 65,2, 44,4, 27,9, 24,5, 24,0.
Пример 77: (±)-2-[2-(4-хлорфенокси)фенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 177)
Соединение 177 было выделено в виде побочного продукта при синтезе соединения 161 (пример 61).
13С ЯМР (DMSO-d6) δ 166,9, 157,8, 155,7, 133,6, 133,3, 129,6, 127,2, 123,4, 122,9, 120,5, 119,2, 64,5, 47,3, 47,2, 28,8, 26,0.
Пример 78: (±)-2-оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 178)
Общая методика 2.
Исходное вещество: соединение 285.
13С ЯМР (DMSO-d6) δ 165,7, 159,0, 158,2, 133,8, 127,5, 126,9, 124,2, 124,1, 119,1, 118,9, 67,2, 47,9, 47,1, 25,4.
Пример 79: (±)-2-оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 179)
Общая методика 2.
Исходное вещество: соединение 286.
13С ЯМР (DMSO-d6) δ 166,6, 159,2, 157,8, 133,4, 127,5, 127,2, 124,1, 124,1, 118,9, 118,8, 64,7, 46,4, 28,9, 25,8.
Пример 80: (αR)-α-(2-метилэтил)-2-оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1, соединение 180)
Общая методика 1.
Исходное вещество: соединение 287.
MS. Вычислено для C21H24F3N2O5P 472,14; найдено [M+H]+=473, [M-H]-=471.
Пример 81: (αR)-α-(2-метилэтил)-2-оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2, соединение 181)
Общая методика 1.
Исходное вещество: соединение 288.
MS. Вычислено для C21H24F3N2O5P 472,14; найдено [M+H]+=473, [M-H]-=471.
Пример 82: (±)-2-[4-(4-бромфенокси)фенил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (соединение 182)
Общая методика 2.
Исходное вещество: соединение 289.
1Н ЯМР (DMSO-d6) δ 10,1 (ш.с, 1H), 8,8 (ш.с, 1H), 7,79 (м, 2H), 7,61 (м, 2H), 7,13-7,05 (м, 4H), 4,33 (м, 1H), 4,11 (м, 1H), 3,49 (м, 2H), 3,25 (м, 2H), 2,04 (м, 1H), 1,85 (м, 1H).
Пример 83: (±)-2-[4-(4-бромфенокси)фенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 183)
Общая методика 2.
Исходное вещество: соединение 290.
13С ЯМР (DMSO-d6) δ 166,6, 158,9, 154,9, 133,3, 132,9, 126,2, 121,5, 117,6, 116,0, 64,6, 46,4, 28,9, 25,8.
Пример 84: (±)-2-(4-нитрофенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 184)
Общая методика 2.
Исходное вещество: соединение 291.
1Н ЯМР (CDCl3) δ 10,5 (ш.с, 1H), 8,9 (ш.с, 1H), 8,24 (м, 2H), 8,04 (м, 2H), 4,60 (м, 1H), 4,22 (дд, 1H), 3,83 (м, 2H), 3,07 (м, 2H), 1,78 (м, 4H).
Пример 85: (±)-2-[N-(4-хлорбензоил)-4-аминофенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 185)
Общая методика 2.
Исходное вещество: соединение 292.
13С ЯМР (DMSO-d6) δ 166,7, 164,6, 141,6, 136,5, 133,3, 131,7, 129,6, 128,4, 126,1, 119,5, 64,6, 46,5, 46,3, 28,9, 25,8.
Пример 86: (±)-2-(N-бензоил-4-аминофенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (соединение 186)
Общая методика 2.
Исходное вещество: соединение 293.
13С ЯМР (DMSO-d6) δ 166,7, 165,8, 141,8, 134,6, 131,7, 131,7, 128,3, 127,7, 125,8, 119,4, 64,5, 46,5, 46,3, 28,9, 25,8.
Пример 87: капсулы, содержащие соединение 161
Соединение 161 растворяли во фракционированном кокосовом масле до конечной концентрации 10 мг/мл. Смешивали при нагревании десять массовых частей желатина, 5 массовых частей глицерина, 0,08 массовых частей сорбата калия и 14 массовых частей дистиллированной воды и формовали в мягкие желатиновые капсулы. Затем каждую из них заполняли 500 мкл раствора соединения 161 в масле.
Пример 88: таблетка, содержащая соединение 161
Активное вещество, лактозу и крахмал смешивают до гомогенного состояния в подходящем смесителе и увлажняют 5%-ным водным раствором метилцеллюлозы 15 cps. Перемешивание продолжают до образования гранул. При необходимости влажные гранулы пропускают через подходящее сито и сушат, пока содержание воды не составит менее 1%, в подходящей сушильной камере, например, в псевдоожиженном слое или сушильной печи. Высушенные гранулы пропускают через 1-миллиметровое сито и смешивают до гомогенного состояния с карбоксиметилцеллюлозой натрия. Добавляют стеарат магния и продолжают перемешивание в течение небольшого промежутка времени.
При помощи подходящего таблетирующего устройства из гранул получают таблетки массой 200 мг.
Пример 89: состав для инъекций, содержащий соединение 161
Активное вещество растворяют в этаноле (10%), затем добавляют воду для инъекций, изотоничную за счет хлорида натрия, для достижения 100%. Данную смесь помещают в ампулы и стерилизуют.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ПИРИДИНОНА И ПИРИДАЗИНОНА | 2012 |
|
RU2632915C2 |
| ПРОИЗВОДНЫЕ АЗЕТИДИНОНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С ГИПОХОЛЕСТЕРИНЕМИЧЕСКОЙ АКТИВНОСТЬЮ И СПОСОБ СНИЖЕНИЯ УРОВНЯ ХОЛЕСТЕРИНА В СЫВОРОТКЕ | 1994 |
|
RU2138480C1 |
| ПРОИЗВОДНЫЕ 2-ПИРИДОНА | 2010 |
|
RU2551847C2 |
| БОРСОДЕРЖАЩИЕ ИНГИБИТОРЫ PDE4 | 2019 |
|
RU2793936C2 |
| ЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ 11БЕТА-ГИДРОКСИСТЕРОИД-ДЕГИДРОГЕНАЗЫ 1 | 2009 |
|
RU2539979C2 |
| БИАРИЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ АГОНИСТОВ GPR120 | 2014 |
|
RU2641003C2 |
| ИНГИБИТОРЫ СЕТР | 2006 |
|
RU2513107C2 |
| НОВЫЕ ТИЕНОПИРИМИДИНОВЫЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2014 |
|
RU2605403C2 |
| 3- ИЛИ 4-ЗАМЕЩЕННЫЕ ПИПЕРИДИНОВЫЕ СОЕДИНЕНИЯ | 2009 |
|
RU2504543C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИЗОСЕРИНА | 2011 |
|
RU2557546C2 |
Настоящее изобретение относится к производным 1,3,2-оксазафосфациклоалкана общей формулы I
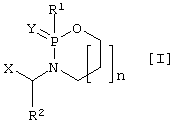
в которой Y представляет О или S; n равно 1, 2, 3 или 4; X представляет гидроксамовую кислоту или карбоновую кислоту; R2 представляет водород, (С1-8)алкил, (С2-6)алкенил или арил(С0-6)алкил, их солям, гидратам или сольватам. Данные соединения являются ингибиторами матриксных металлопротеиназ, принимающих участие в распаде ткани, что предполагает возможность их использования в терапии человека и в ветеринарии. 3 н. и 8 з.п. ф-лы, 4 табл.
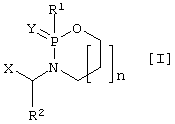
в которой Y представляет О или S;
n равно 1, 2, 3 или 4;
X представляет гидроксамовую кислоту или карбоновую кислоту;
R1 представляет
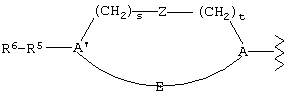
в которой Е, если он присутствует, представляет связь;
s и t независимо равны 0, 1, 2 или 3;
А и А' независимо представляют связь или ненасыщенный циклический углеводородный ди- или трирадикал, необязательно замещенный (C1-6)алкокси, фенилом, галогеном, циано, трифторметилом, нитро или галогеналкилом;
Z представляет связь, О, S, С(О), NR7C(O) или NR7, где R7 представляет водород;
R5 представляет связь, алкановый дирадикал, один или более эфирных дирадикалов (R-O-R') или аминные дирадикалы (R-N-R'), где R и R' независимо представляют алкановый дирадикалы с содержанием углерода от 0 до 1;
R6 представляет водород, линейный, насыщенный или ненасыщенный углеводородный радикал, необязательно замещенный галогеном, циано, нитро, галогеналкилом или алкокси;
R2 представляет водород, (C1-8)алкил, (С2-6)алкенил или арил(С0-6)алкил;
при условии, что когда все из А, А', Z и R5 представляют связи, a s и t оба равны 0 (нулю), то R6 не является водородом;
или его соль, гидрат или сольват.
или его соль, гидрат или сольват.
(±)-2-(4-Хлорфенокси)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-(4-Хлорфенокси)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-2-[(4-Бромфенил)метил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-[(4-Бифенилил)метил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-(4-Бифенилил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-(4-Бифенилил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-2-Гептил-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-Гептил-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-2-Оксо-2-[4-(фениламино)фенил]-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-Оксо-2-фенил-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-Оксо-2-фенил-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-2-Оксо-2-фенил-1,3,2-оксазафосфоронан-3-ацетогидроксамовая кислота,
(±)-α-Бутил-2-оксо-2-фенил-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-α-Бутил-2-оксо-2-фенил-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-2-(4-Метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-(4-Метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-2-(4-Метоксифенил)-2-оксо-1,3,2-оксазафосфоронан-3-ацетогидроксамовая кислота,
(αR)-2-(4-Метоксифенил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1),
(αR)-2-(4-Метоксифенил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2),
(±)-α-Бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 1),
(±)-α-Бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 2),
(±)-α-Бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1),
(±)-α-Бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2),
(±)-α-Бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота (диастереомеры 1),
(±)-α-Бутил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота (диастереомеры 2),
(±)-α-Аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 1),
(±)-α-Аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 2),
(±)-α-Аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1),
(±)-α-Аллил-2-(4-метоксифенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2),
(αR)-2-(4-Метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1, соединение 130),
(αR)-2-(4-Метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2),
(αS)-2-(4-Метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1),
(αS)-2-(4-Метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2),
(±)-2-(4-Метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1),
(±)-2-(4-Метоксифенил)-α-(2-метилпропил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2),
(±)-2-(4-Метоксифенил)-α-пропил-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 1),
(±)-2-(4-Метоксифенил)-α-пропил-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 2),
(±)-2-(4-Метоксифенил)-α-октил-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1),
(±)-2-(4-Метоксифенил)-α-октил-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2),
(αR)-2-(4-Метоксифенил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1),
(αS)-2-(4-Метоксифенил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1),
(αS)-2-(4-Метоксифенил)-2-оксо-α-фенилметил-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2),
(±)-2-Оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-Оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-2-Оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота,
(±)-α-Аллил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 1),
(±)-α-Аллил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомеры 2),
(αR)-α-(2-Метилпропил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1),
(αR)-α-(2-Метилпропил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2),
(αR)-α-(2-Метилэтил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1),
(αR)-α-(2-Метилэтил)-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2),
(±)-α-Бутил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1),
(±)-α-Бутил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2),
(±)-α-Октил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 1),
(±)-α-Октил-2-оксо-2-(4-феноксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота (диастереомеры 2),
(±)-2-Оксо-2-(2-фенилэтил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-(4-Метоксифенил)-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота,
(±)-2-Оксо-2-фенил-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота,
(±)-2-Гептил-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота (соединение 159),
(αR)-2-(4-Бифенилил)-α-(1-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2),
(±)-2-[4-(4-Хлорфенилокси)фенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-2-[4-(4-Хлорфенилокси)фенил]-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота,
(αR)-2-[4-(4-Хлорфенилокси)фенил]-α-(2-метилэтил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-(4'-Бром-4-бифенилил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-(4'-Бром-4-бифенилил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-2-(4'-Бром-4-бифенилил)-2-оксо-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота,
(±)-2-[2-(1-Нафтил)этил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-Фенил-2-тиоксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-Фенил-2-тиоксо-1,3,2-оксазафосфорепан-3-ацетамид,
(±)-2-Фенил-2-тиоксо-1,3,2-оксазафосфорокан-3-ацетамид,
(±)-2-[4-(4-Хлорфенилокси)фенил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-(4-Бромфенил)-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-(4-Бромфенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-2-Оксо-2-(4-фенилметоксифенил)-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-Оксо-2-(4-фенилметоксифенил)-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-2-Оксо-2-(4-фенилметоксифенил)-1,3,2-оксазафосфорокан-3-ацетогидроксамовая кислота,
(±)-2-[2-(4-Хлорфенокси)фенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-2-Оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-Оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(αR)-α-(2-Метилэтил)-2-оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 1),
(αR)-α-(2-Метилэтил)-2-оксо-2-[4-(4-трифторметилфенокси)фенил]-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота (диастереомер 2),
(±)-2-[4-(4-Бромфенокси)фенил]-2-оксо-1,3,2-оксазафосфоринан-3-ацетогидроксамовая кислота,
(±)-2-[4-(4-Бромфенокси)фенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-2-(4-Нитрофенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-2-[N-(4-Хлорбензоил)-4-аминофенил]-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота,
(±)-2-(N-Бензоил-4-аминофенил)-2-оксо-1,3,2-оксазафосфорепан-3-ацетогидроксамовая кислота
и соответствующие карбоновые кислоты.
| RU, 2026299 C1, 10.01.1995 | |||
| СПОСОБ КОМБИНИРОВАННОГО ПОЛИВА | 2014 |
|
RU2567129C1 |
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
Авторы
Даты
2006-02-27—Публикация
2001-07-03—Подача