Область техники
Настоящее изобретение относится к новому способу получения производных пиридина, обладающих превосходной гербицидной активностью, и к исходным соединениям, используемым для способа.
Предшествующий уровень техники
Производные пиридина (d):

[где R1 представляет собой С1-С6-алкоксигруппу, R3 представляет атом галогена, цианогруппу или нитрогруппу и R4 представляет собой атом водорода или атом галогена] обладают превосходной гербицидной активностью. Производные пиридина [d] содержат два гетероциклических кольца, которые представляют собой урациловое кольцо и пиридиновое кольцо, и является весьма желательным выгодный способ их получения.
Задача настоящего изобретения - получить производные пиридина [d], обладающие специфической системой заместителей, и исходные соединения, используемые в этом способе.
Описание изобретения
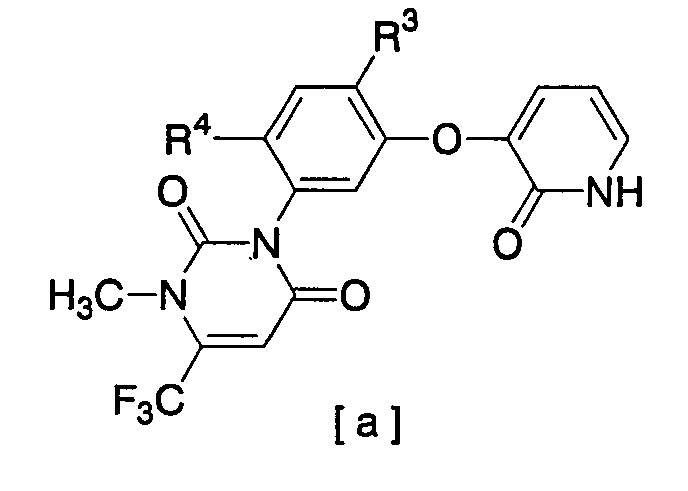
Для создания выгодного способа получения производных пиридина [d] авторы настоящего изобретения проводили интенсивные исследования. В результате они обнаружили, что производное пиридина [d] может быть получено взаимодействием производного пиридона [a]:
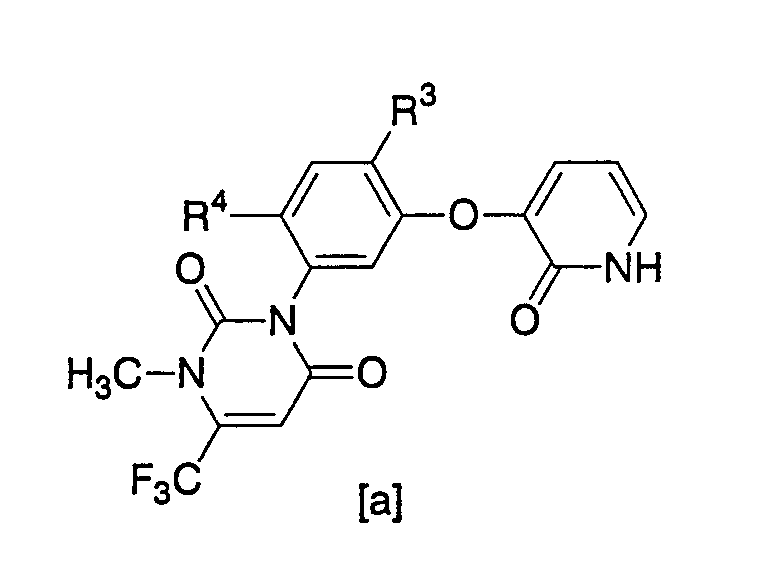
[где R3 и R4 имеют значения, указанные выше] с производным α-диазоэфира [f]
N2CHCOR1 [f]
[где R1 имеет значение, указанное выше] в присутствии кислоты для осуществления региоселективного О-алкилирования, вследствие чего было создано настоящее изобретение. За счет выбора способа настоящего изобретения может быть выгодно получено производное пиридина [d], имеющее специфическую систему заместителей.
Именно, настоящее изобретение относится к способу получения производного пиридина [d] взаимодействием производного пиридона [a] с производным α-диазоэфира [f] в присутствии кислоты (далее указывается как «способ настоящего изобретения) и к производному пиридона [a], которое представляет собой необходимое исходное соединение, используемое в этом способе.
В настоящем изобретении примеры С1-С6-алкоксильной группы, данные для R1, включают метоксигруппу, этоксигруппу, пропоксигруппу и т.д. и примеры атома галогена, данные для R3 и R4, включают атом фтора, атом хлора и атом брома.
Способ настоящего изобретения осуществляется взаимодействием производного пиридона [а] с производным α-диазоэфира [f] в присутствии кислоты, и реакцию обычно проводят в растворителе. Примеры растворителя включают ароматические углеводороды, такие как бензол, толуол, ксилол и т.д.; галогенированные углеводороды, такие как 1,2-дихлорэтан, хлорбензол, дихлорбензол и т.д.; и их смеси.
В настоящем способе кислота означает кислоту, определенную Льюисом, а именно вещество, которое может принимать электронную пару, и включает апротонную кислоту и протонную кислоту (кислота Бренстеда). Примеры апротонной кислоты включают соли родия (II), трифторид бора и тетрахлорид олова и примеры протонной кислоты включают сульфоновые кислоты, такие как трифторметансульфоновая кислота, п-толуолсульфоновая кислота и т.д.; трифторуксусную кислоту и серную кислоту. Термин «соли родия (II)» означает металлическую соль, включающую катион двухвалентного родия и соответствующий анион, и, кроме того, необязательно соответствующий лиганд, и типичные примеры представляют собой димер трифторацетата родия (II) ([(CF3CO2)2Rh]2), димер ацетата родия (II) ([(CH3CO2)2Rh]2) и т.д. В качестве трифторида бора может быть использован сам BF3 или его комплекс, и примеры комплекса включают диэтилэфирный комплекс, диметилсульфидный комплекс, тетрагидрофурановый комплекс и т.д. Принимая во внимание скорость реакции, предпочтительно использовать в качестве кислоты димер трифторацетата родия (II), комплекс трифторид бора/диэтиловый эфир, тетрахлорид олова или трифторметансульфоновую кислоту.
В настоящей реакции теоретически необходим один моль производного α-диазоэфира [f] в расчете на один моль производного пиридона [a], а практически используются от 1 до 2 моль производного α-диазоэфира. В настоящей реакции кислота имеет каталитическую активность и ее используют с учетом скорости реакции в количестве, находящемся в диапазоне от 0,001 до 5 моль, предпочтительно в количестве 0,01 моль или более в расчете на моль производного пиридона [a]. Температура реакционной массы в настоящей реакции с учетом ее скорости обычно составляет от -50 до 120°С, предпочтительно -20°С или более. Время реакции обычно находится в диапазоне от мгновения до 72 часов.
Используемые для настоящей реакции реагенты добавляют в реакционный сосуд, например, в следующем порядке:
1) Способ включает предварительное смешивание производного пиридона [a], кислоты и растворителя и добавление в смесь по каплям производного α-диазоэфира [f].
2) Способ включает предварительное смешивание производного пиридона [a], производного α-диазоэфира [f] и растворителя и добавление в смесь по каплям кислоты.
3) Способ включает предварительное смешивание производного пиридона [a] и растворителя и добавление в смесь по каплям соответственно кислоты и производного α-диазоэфира [f].
Окончание настоящей реакции может быть установлено отбором части реакционной смеси, анализом пробы жидкостной хроматографией, тонкослойной хроматографией и т.д. и измерением оставшегося количества производного пиридона [a] или производного α-диазоэфира [f].
После реакции производное пиридина [d] может быть получено, например, следующими методами дополнительной обработки реакционной смеси:
1) Фильтрация реакционной смеси и концентрирование фильтрата.
2) Хроматографирование реакционной смеси на силикагеле и затем концентрирование.
3) Вливание реакционной смеси в водный раствор бикарбоната натрия, экстракция органическим растворителем, сушка и концентрирование органического слоя.
Полученное производное пиридина [d] может быть очищено таким методом, как хроматография, перекристаллизация и т.д.
В случае взаимодействия производного пиридона [а] со сложноэфирным соединением [x]:
Х1CH2COR1 [х]
[где R1 имеет значение, указанное выше, и Х1 представляет собой атом хлора, атом брома, метансульфонилоксигруппу или п-толуолсульфонилоксигруппу]
в присутствии основания, основным продуктом было производное пиридона [y]:

[где R3, R4 и R1 имеют значения, указанные выше]
Производное α-диазоэфира [f], используемое в настоящем изобретении, как таковое, имеется в продаже или может быть получено известным способом взаимодействием соединения [h]:
Н2NCH2COR1 [h]
[где R1 имеет значение, указанное выше] или его соли с минеральной кислотой (то есть гидрохлоридной соли) с нитритом натрия в кислой среде (Смотри: Organic Syntheses Collective. Volume IV, p.424-426).
Производное α-диазоэфира [f], полученное взаимодействием соединения [h] или его соли с минеральной кислотой с нитритом натрия в кислой среде, может быть использовано в качестве исходного в способе настоящего изобретения без выделения. Т.е. раствор производного α-диазоэфира [f], полученного взаимодействием производного α-диазоэфира [h] с нитритом натрия в кислой среде, экстракцией органическим растворителем, может применяться в способе настоящего изобретения после соответствующей обработки, такой как сушка безводным сульфатом магния. Примеры используемого указанного выше растворителя включают ароматические углеводороды, такие как бензол, толуол, ксилол и т.д.; и галогенированные углеводороды, такие как дихлорметан, 1,2-дихлорэтан, хлорбензол, дихлорбензол, бензотрифторид и т.д.
Производное пиридона [a], используемое в способе настоящего изобретения, может быть получено из известного соединения следующими способами:
Способ 1 получения
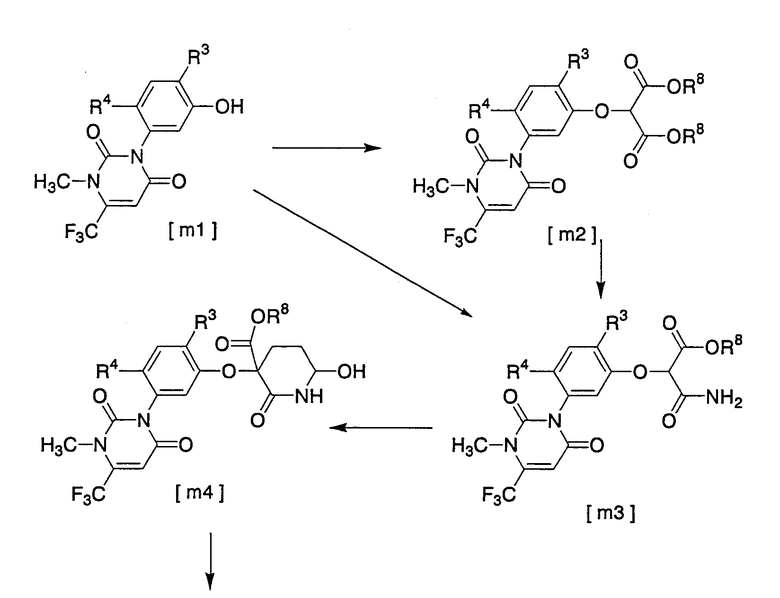

[где R3 и R4 имеют значения, указанные выше, и R8 представляет собой низшую алкильную группу, такую как метильная группа, этильная группа и т.д.]
Соединение [m1] → [соединение m2]
Соединение [m2] получают взаимодействием соединения [m1] с соединением [m7]:
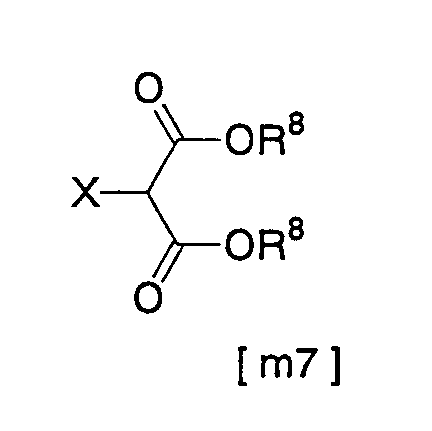
[где R8 имеет значение, указанное выше, и Х представляет собой удаляемую группу, такую как атом хлора, атом брома и т.д.] в присутствии основания.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от комнатной температуры до 80°С, и время реакции обычно находится в диапазоне от мгновения до 12 часов.
В данной реакции теоретически необходимы один моль соединения [m7] и один моль основания в расчете на один моль соединения [m1], но количества могут свободно изменяться в соответствии с условиями реакции.
Примеры используемого для реакции основания включают карбонат калия и примеры растворителя включают нитрилы, такие как ацетонитрил и т.д.; и амиды кислот, такие как N,N-диметилформамид, N-метил-2-пирролидон и т.д.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду или подкисленную воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [m2] → соединение [m3]
Соединение [m3] получается взаимодействием соединения [m2] с аммиаком.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от -20°С до 50°С, и время реакции обычно находится в диапазоне от мгновения до 12 часов.
В данной реакции теоретически необходим один моль аммиака в расчете на один моль соединения [m2], но количество может свободно изменяться в соответствии с условиями реакции.
Примеры используемого для реакции растворителя включают спирты, такие как метанол, этанол и т.д.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [m1] → соединение [m3]
Соединение [m3] получается взаимодействием соединения [m1] с соединением [m8]:

[где R8 и Х имеют значения, указанные выше] в присутствии основания.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от комнатной температуры до 80°С, и время реакции обычно находится в диапазоне от мгновения до 12 часов.
В данной реакции теоретически необходимы один моль соединения [m8] и один моль основания в расчете на один моль соединения [m1], но количества могут свободно изменяться в соответствии с условиями реакции.
Примеры используемого для реакции основания включают карбонат калия и примеры растворителя включают нитрилы, такие как ацетонитрил и т.д.; и амиды кислот, такие как N,N-диметилформамид, N-метил-2-пирролидон и т.д.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду или подкисленную воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [m3] → соединение [m4]
Соединение [m4] получается взаимодействием соединения [m3] с акролеином в присутствии основания.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от -30 до 50°С, предпочтительно от -10 до 20°С. Время реакции обычно находится в диапазоне от мгновения до 12 часов.
В данной реакции теоретически необходимы один моль акролеина и от 0,01 до 2 моль основания в расчете на один моль соединения [m3], но количества могут свободно изменяться в соответствии с условиями реакции.
Примеры используемого для реакции основания включают алкоксиды металлов, такие как трет-бутоксид калия и т.д.; и неорганические основания, такие как карбонат калия и т.д.
Примеры используемого для реакции растворителя включают простые эфиры, такие как тетрагидрофуран и т.д.; и сложные эфиры, такие как этилацетат и т.д.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [m4] → соединение [m5]
Соединение [m5] получается взаимодействием соединения [m4] в присутствии кислоты.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от комнатной температуры до 150°С, и время реакции обычно находится в диапазоне от мгновения до 24 часов.
В данной реакции используется от 0,001 до 0,2 моль кислоты в расчете на один моль соединения [m4], но количество может свободно изменяться в соответствии с условиями реакции.
Примеры используемой для реакции кислоты включают органические кислоты, такие как уксусная кислота, п-толуолсульфоновая кислота и т.д.; и неорганические кислоты, такие как хлористоводородная кислота и т.д. Примеры растворителя включают простые эфиры, такие как тетрагидрофуран и т.д.; и сложные эфиры, такие как этилацетат и т.д.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [m5] → соединение [m6]
Соединение [m6] получается из соединения [m5] в присутствии воды и галогенида щелочного металла, обычно в растворителе.
Температура реакции обычно находится в диапазоне от 80 до 140°С, и время реакции обычно находится в диапазоне от мгновения до 48 часов.
В данной реакции используются от 0,5 до 2 моль воды и от 1 до 5 моль галогенида щелочного металла в расчете на один моль соединения [m5], но количества могут свободно изменяться в соответствии с условиями реакции.
Примеры используемого для реакции галогенида щелочного металла включают хлорид лития, хлорид натрия, иодид лития и иодид натрия и примеры растворителя включают диметилсульфоксид и пиридин.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [m6] → производное пиридона [а]
Производное пиридона [а] получается взаимодействием соединения [m6] с дегидрирующим реагентом.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от 60 до 190°С, и время реакции обычно находится в диапазоне от мгновения до 48 часов.
Используемый для настоящей реакции дегидрирующий реагент означает хиноидные окислительные реагенты, такие как хлоранил и т.д.; и гетерогенный металлический катализатор, такой как палладий на угле и т.д.
В данной реакции используется от 1 до 3 моль хиноидного окислительного реагента, или от 10 до 30 мас.% гетерогенного металлического катализатора в расчете на один моль соединения [m6], но количество может свободно изменяться в зависимости от условий реакции.
Примеры растворителя включают ароматические углеводороды, такие как толуол, ксилол и т.д.; галогенированные ароматические углеводороды, такие как хлорбензол, дихлорбензол, бензотрифторид и т.д.; простые эфиры, такие как диоксан, тетрагидрофуран, диглим, дифениловый эфир и т.д.; и их смеси.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь разбавляют органическим растворителем, затем вливают в водный раствор бикарбоната натрия, экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [m1] известно из патента США № 4859229 и может быть получено известным способом или подобными способами.
Соединение [m7] как таковое имеется в продаже или может быть получено известным способом.
Соединение [m8] может быть получено взаимодействием соединения [m7] с аммиаком при условиях реакции, представленных выше для превращения «Соединение [m2] → соединение [m3]».
Способ 2 получения

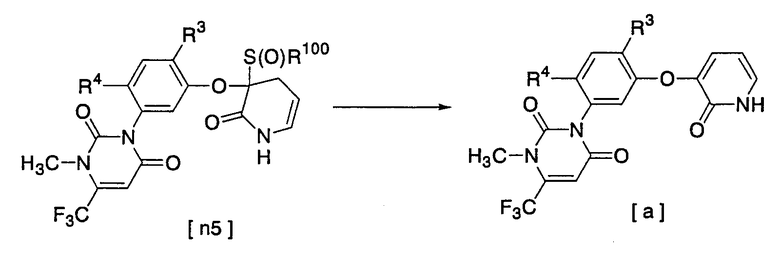
[где R3 и R4 имеют значения, указанные выше; R100 представляет собой низшую алкильную группу, такую как метильная группа, этильная группа и т.д., или фенильную группу; и n равно 1 или 2]
Соединение [m1] → [соединение n1]
Соединение [n1] может быть получено взаимодействием соединения [m1] с хлорацетонитрилом или бромацетонитрилом в присутствии основания.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от -20 до 80°С, и время реакции обычно находится в диапазоне от мгновения до 24 часов.
В данной реакции теоретически необходимы один моль хлорацетонитрила или бромацетонитрила и один моль основания в расчете на один моль соединения [m1], но количества могут свободно изменяться в соответствии с условиями реакции.
Примеры используемого для реакции основания включают гидрид натрия, карбонат калия, бикарбонат натрия, гидроксид натрия и гидроксид калия и примеры растворителя включают нитрилы, такие как ацетонитрил и т.д.; амиды кислот, такие как N,N-диметилформамид, N-метил-2-пирролидон и т.д.; простые эфиры, такие как тетрагидрофуран, 1,4-диоксан, диметиловый эфир этиленгликоля, 2-метоксиэтиловый эфир и т.д.; углеводороды, такие как толуол и т.д.; и сложные эфиры, такие как метилацетат, этилацетат и т.д.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду или подкисленную воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n1] → соединение [n2]
Соединение [n2] может быть получено взаимодействием соединения [n1] с дисульфидным соединением [n6]:
(R100S)2 [n6]
[где R100 имеет значение, указанное выше] в присутствии основания.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от -50 до 10°С, и время реакции обычно находится в диапазоне от мгновения до 12 часов.
В данной реакции теоретически необходимы один моль дисульфидного соединения [n6] в расчете на один моль соединения [n1], но количество может свободно изменяться в соответствии с условиями реакции.
Примеры растворителя включают амиды кислот, такие как ДМФА, N-метилпирролидин-2-он и т.д.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n2] → соединение [n3]
Соединение [n3] может быть получено взаимодействием соединения [n2] с окислителем.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от -20 до 50°С, и время реакции обычно находится в диапазоне от мгновения до 24 часов.
Окислитель представляет собой перкислоты, такие как м-хлорпербензойная кислота и т.д.; и пероксид водорода. Примеры используемого для реакции растворителя включают галогенированные соединения, такие как хлороформ, дихлорметан и т.д.
В данной реакции теоретически необходимы один и два моля окислителя в расчете на один моль соединения [n2], когда n=1 и n=2 соответственно, но количество может свободно изменяться в соответствии с условиями реакции.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n3] → соединение [n4]
Соединение [n4] может быть получено взаимодействием соединения [n3] в присутствии воды и диоксида марганца.
Реакцию обычно осуществляют в растворителе. Температура реакции обычно находится в диапазоне от 50 до 120°С и время реакции обычно находится в диапазоне от мгновения до 24 часов.
Диоксид марганца в данной реакции используется в количестве от каталитического количества до избытка.
Примеры используемого для реакции растворителя включают воду и смеси воды с органическим растворителем (спирты, такие как метанол, этанол, изопропанол и т.д.; кетоны, такие как ацетон, метилэтилкетон, метилизобутилкетон и т.д.; и простые эфиры, такие как тетрагидрофуран, 1,4-диоксан и т.д.).
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n4] получается также взаимодействием соединения [n3] в присутствии воды и тетрабората натрия.
Соединение [n4] → производное пиридона [а]
Производное пиридона [а] может быть получено взаимодействием соединения [n4], где n равно 1, с акролеином в присутствии основания и последующим превращением в присутствии кислоты.
Реакцию обычно осуществляют в растворителе. Температура реакции на первой стадии находится в диапазоне от -20 до 50°С и температура реакции на второй стадии находится в диапазоне от комнатной температуры до 80°С. Время реакции обычно находится в диапазоне от мгновения до 48 часов.
Примеры используемого для реакции основания включают гидрид натрия, трет-бутоксид калия, гидроксид натрия, карбонат калия, фторид калия и т.д. и примеры кислоты включают уксусную кислоту, трифторуксусную кислоту, метансульфоновую кислоту, п-толуолсульфоновую кислоту, трифторид бора и его комплекс (например, комплекс трифторид бора-метанол). Примеры растворителя включают простые эфиры, такие как диэтиловый эфир, метилтрет-бутиловый эфир, диметоксиэтан, тетрагидрофуран, 1,4-диоксан и т.д.; галогенированные соединения, такие как хлороформ, дихлорметан и т.д.; и углеводороды, такие как толуол и т.д.
В данной реакции теоретически необходимы количества основания и кислоты, равные соответственно от каталитического количества до одного эквивалента и от каталитического количества до избытка, и один моль акролеина в расчете на один моль соединения [n4], но количества могут свободно изменяться в соответствии с условиями реакции.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n4] → соединение [n5]
Соединение [n5] может быть получено взаимодействием соединения [n4], где n равно 2, с акролеином в присутствии основания и последующим превращением в присутствии кислоты.
Реакцию обычно осуществляют в растворителе. Температура реакции первой стадии находится в диапазоне от -20 до 50°С и температура реакции второй стадии находится в диапазоне от комнатной температуры до 50°С. Время реакции обычно находится в диапазоне от мгновения до 48 часов.
Примеры используемого для реакции основания включают гидрид натрия, трет-бутоксид калия, гидроксид натрия, карбонат калия, фторид калия и т.д. и примеры кислоты включают уксусную кислоту, трифторуксусную кислоту, метансульфоновую кислоту, п-толуолсульфоновую кислоту, трифторид бора и его комплекс (например, комплекс трифторид бора-метанол). Примеры растворителя включают простые эфиры, такие как диэтиловый эфир, метилтрет-бутиловый эфир, диметоксиэтан, тетрагидрофуран, 1,4-диоксан и т.д.; галогенированные соединения, такие как хлороформ, дихлорметан и т.д.; и углеводороды, такие как толуол и т.д.
В данной реакции теоретически необходимы количества основания и кислоты, равные соответственно от каталитического количества до одного эквивалента и от каталитического количества до избытка, и один моль акролеина в расчете на один моль соединения [n4], но количества могут свободно изменяться в соответствии с условиями реакции.
Соединение [n5] → производное пиридона [а]
Производное пиридона [а] может быть получено взаимодействием соединения [n5] в присутствии кислоты.
Реакцию обычно осуществляют в растворителе. Температура реакции находится в диапазоне от 50 до 130°С, и время реакции обычно находится в диапазоне от мгновения до 48 часов.
Примеры кислоты включают уксусную кислоту, трифторуксусную кислоту, метансульфоновую кислоту, п-толуолсульфоновую кислоту, трифторид бора и его комплекс (например, комплекс трифторид бора-метанол). Примеры растворителя включают соединения серы, такие как диметилсульфоксид и т.д.; производные простых эфиров, такие как диметоксиэтан, тетрагидрофуран, 1,4-диоксан и т.д.; и углеводороды, такие как толуол и т.д.
В данной реакции кислота используется в количестве от каталитического количества до избытка.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Кроме того, соединение [n4] получают также следующим способом:
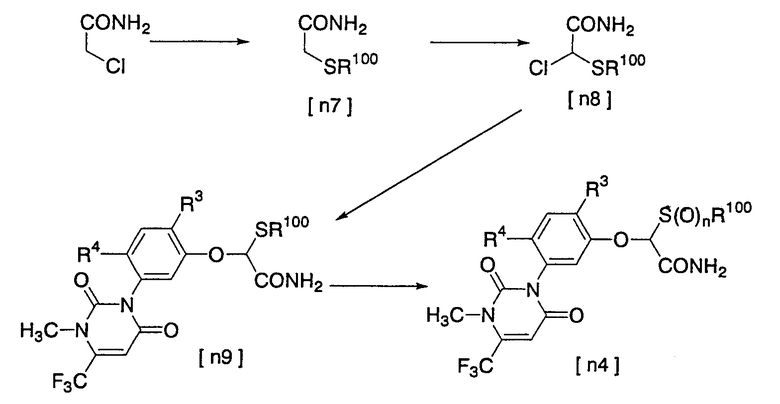
[где R3, R4 и R100 имеют значения, указанные выше]
2-Хлорацетамид → соединение [n7]
Соединение [n7] может быть получено взаимодействием соединения [n10]
NaSR100 [n10]
[где R100 имеет значения, указанные выше] с 2-хлорацетамидом.
Реакцию обычно осуществляют в растворителе. Температура реакции находится в диапазоне от комнатной температуры до 50°С, и время реакции обычно находится в диапазоне от мгновения до 48 часов.
Примеры растворителя включают спирты, такие как метанол, этанол, изопропанол и т.д.; воду и их смеси.
В данной реакции теоретически необходим один моль соединения [n10] в расчете на один моль 2-хлорацетамида, но количество может свободно изменяться в соответствии с условиями реакции.
После реакции саму реакционную смесь концентрируют; или после взаимодействия одного моля 2-хлорацетамида реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n7] → соединение [n8]
Соединение [n8] может быть получено взаимодействием соединения [n7] с хлорирующим реагентом.
Реакцию обычно осуществляют в растворителе. Температура реакции находится в диапазоне от -10 до 30°С, и время реакции обычно находится в диапазоне от мгновения до 48 часов.
Примеры растворителя включают галогенированные соединения, такие как хлороформ, дихлорметан и примеры хлорирующего реагента включают сульфурилхлорид.
В данной реакции теоретически необходим один моль хлорирующего реагента в расчете на один моль соединения [n7], но количество может свободно изменяться в зависимости от условий реакции.
После реакции саму реакционную смесь концентрируют; или после взаимодействия одного моля хлорирующего реагента реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n8] → соединение [n9]
Соединение [n9] может быть получено взаимодействием соединения [n8] с соединением [m1] в присутствии основания и необязательно дополнительно иодидной соли.
Реакцию обычно осуществляют в растворителе. Температура реакции находится в диапазоне от -10 до 80°С, и время реакции обычно находится в диапазоне от мгновения до 48 часов.
Примеры растворителя включают кетоны, такие как ацетон, метилэтилкетон, метилизобутилкетон и т.д.; соединения серы, такие как диметилсульфоксид и т.д.; простые эфиры, такие как диэтиловый эфир, метилтрет-бутиловый эфир, диметоксиэтан, тетрагидрофуран, 1,4-диоксан и т.д.; и углеводороды, такие как толуол. Примеры основания включают гидрид натрия, карбонат калия, бикарбонат натрия, гидроксид натрия и трет-бутоксид калия и примеры иодидной соли включают иодид натрия и иодид калия.
В данной реакции теоретически необходим один моль соединения [m1] в расчете на один моль соединения [n8] и теоретически необходим один моль основания в расчете на один моль соединения [m1], но количества могут свободно изменяться в зависимости от условий реакции.
После реакции саму реакционную смесь концентрируют; или после взаимодействия одного моля соединения [n8] реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Соединение [n9] → соединение [n4]
Соединение [n4] может быть получено взаимодействием соединения [n9] с окислителем.
Реакцию обычно осуществляют в растворителе. Температура реакции находится в диапазоне от -30 до 50°С, и время реакции обычно находится в диапазоне от мгновения до 24 часов.
Окислитель представляет собой перкислоты, такие как м-хлорпербензойная кислота и т.д.; и пероксид водорода. Примеры используемого для реакции растворителя включают галогенированные соединения, такие как хлороформ, дихлорметан и т.д.
В данной реакции теоретически необходимы один и два моля окислителя в расчете на один моль соединения [n9], когда n=1 и n=2 соответственно, но количество может свободно изменяться в зависимости от условий реакции.
После реакции реакционную смесь, в случае необходимости, фильтруют и фильтрат концентрируют; реакционную смесь вливают в воду и осажденные кристаллы отфильтровывают; или реакционную смесь экстрагируют органическим растворителем, органический слой сушат и подвергают обычным операциям дополнительной обработки, таким как концентрирование и т.д., с получением целевого соединения. Затем полученное соединение можно очистить такими методами, как хроматография, перекристаллизация и т.д.
Способ 3 получения
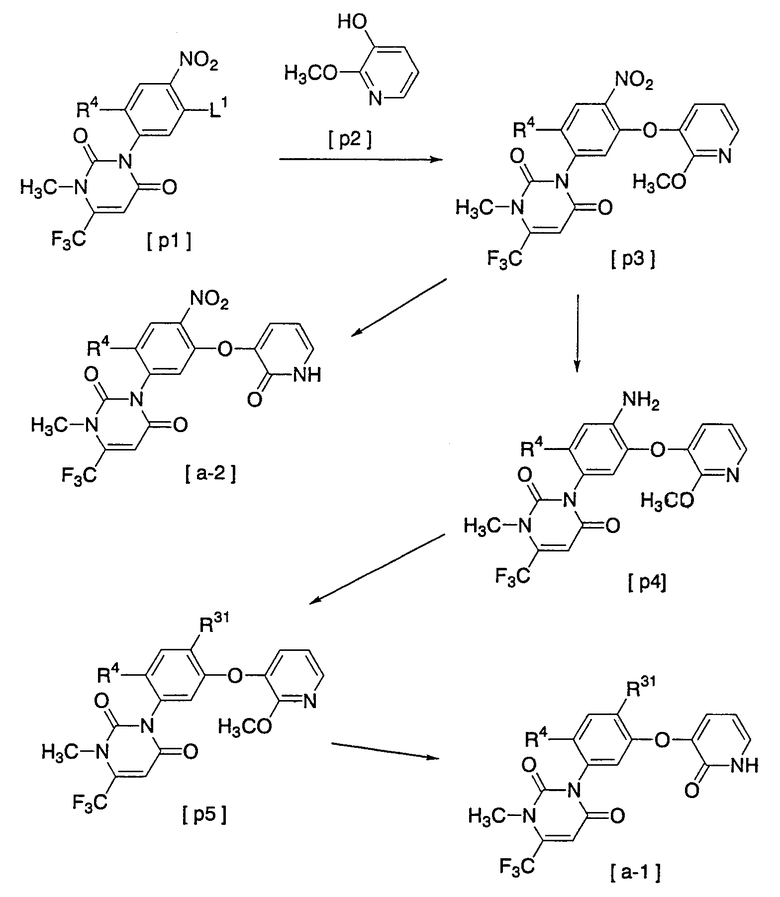
[R4 имеет значение, указанное выше, R31 представляет собой атом галогена или цианогруппу и L1 представляет собой атом фтора или атом хлора]
Соединение [р1] → соединение [р3]
Соединение [р3] может быть получено взаимодействием соединения [р1] и соединения [р2] с основанием, таким как карбонат калия, обычно в растворителе.
Соединение [р3] → соединение [р4]
Соединение [р4] может быть получено взаимодействием соединения [р3] в атмосфере водорода в присутствии катализатора, такого как палладий на угле и т.д., обычно в растворителе или взаимодействием с порошком железа в смешанном растворителе, состоящем из уксусной кислоты и воды.
Соединение [р4] → соединение [р5]
Соединение [р5] может быть получено взаимодействием соединения [р4] с диазотирующим реагентом, таким как нитрит натрия и т.д., и последующего взаимодействия с хлоридом меди, бромидом меди или цианидом меди в растворителе.
Соединение [р5] → соединение [а-1]
Производное пиридона [а], где R3 представляет собой атом галогена или цианогруппу, а именно производное пиридона [а-1], может быть получено взаимодействием соединения [р5] с трибромидом бора, обычно в растворителе.
Соединение [р3] → соединение [а-2]
Производное пиридона [а], где R3 представляет собой нитрогруппу, а именно производное пиридона [а-2], может быть получено взаимодействием соединения [р3] с трибромидом бора, обычно в растворителе.
Соединение [р2] может быть получено следующим способом:
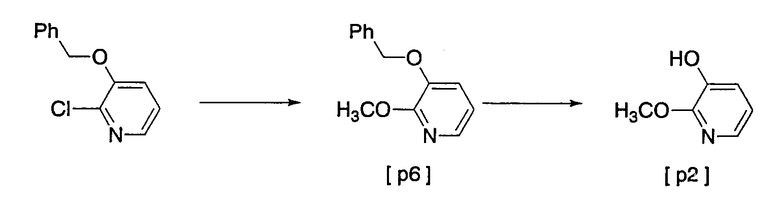
2-Хлор-3-бензилоксипиридин → соединение [р6]
Соединение [р6] может быть получено взаимодействием 2-хлор-3-бензилоксипиридина с метанолом в присутствии основания, обычно в растворителе.
Соединение [р2] → соединение [р6]
Соединение [р6] может быть получено взаимодействием соединения [р2] в атмосфере водорода в присутствии катализатора, такого как палладий на угле и т.д., обычно в растворителе.
Кроме того, соединение [р2] может быть также получено способом, описанным в патенте США № 3701779, или его модификацией.
2-Хлор-3-бензилоксипиридин может быть получен способом, описанным в Heterocycles, 1994, 38(6), 1355-1360.
Способ 4 получения


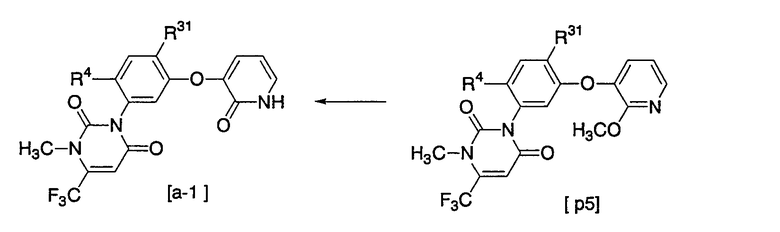
[где R4, R31 и L1 имеют значения, указанные выше]
Соединение [q1] → соединение [q2]
Соединение [q2] может быть получено взаимодействием соединения [q1] с 2-хлор-3-гидроксипиридином в присутствии основания, такого как карбонат калия и т.д., обычно в растворителе.
Соединение [q2] → соединение [q3]
Соединение [q3] может быть получено взаимодействием соединения [q2] в атмосфере водорода в присутствии катализатора, такого как палладий на угле и т.д., обычно в растворителе, или взаимодействием с порошком железа в смешанном растворителе, состоящем из уксусной кислоты и воды.
Соединение [q3] → соединение [q4]
Соединение [q4] может быть получено взаимодействием соединения [q3] с диазотирующим реагентом, таким как нитрит натрия и т.д., и затем с хлоридом меди, бромидом меди или цианидом меди в растворителе.
Соединение [q4] → соединение [q5]
Соединение [q5] может быть получено взаимодействием соединения [q4] с метанолом в присутствии основания, обычно в растворителе.
Соединение [q5] → соединение [q6]
Соединение [q6] может быть получено взаимодействием соединения [q5] с азотной кислотой в серной кислоте.
Соединение [q6] → соединение [q7]
Соединение [q7] может быть получено взаимодействием соединения [q6] в атмосфере водорода в присутствии катализатора, такого как палладий на угле и т.д., обычно в растворителе, или взаимодействием с порошком железа в смешанном растворителе, состоящем из уксусной кислоты и воды.
Соединение [q7] → соединение [q8]
Соединение [q8] может быть получено взаимодействием соединения [q7] с фосгеном, обычно в растворителе.
Соединение [q8] → соединение [q9]
Соединение [q9] может быть получено взаимодействием соединения [q8] с этил 4,4,4-трифтор-3-аминокротонатом в присутствии основания, такого как гидрид натрия и т.д., обычно в растворителе.
Соединение [q9] → соединение [q5]
Соединение [q5] может быть получено взаимодействием соединения [q9] с метилирующим реагентом, таким как диметилсульфат, метилиодид и т.д., в присутствии основания, такого как гидрид натрия и т.д., обычно в растворителе.
Соединение [р5] → соединение [а-1]
Производное пиридона [а-1], которое представляет собой производное пиридона [а], где R3 представляет атом галогена или цианогруппу, может быть получено взаимодействием соединения [р5] с трибромидом бора, обычно в присутствии растворителя.
Производное пиридона [а] является, кроме того, соединением, обладающим гербицидной активностью, и поэтому является применимым в качестве активного ингредиента гербицида.
Производное пиридина [е]:

[где R3 и R4 имеют значения, указанные выше; R6 представляет собой С1-С6-галогеналкоксильную группу, С3-С6-алкенилоксигруппу, С3-С6-галогеналкенилоксигруппу, С3-С6-алкинилоксигруппу, С3-С6-галогеналкинилоксигруппу, С3-С8-циклоалкоксильную группу, С3-С8-галогенциклоалкоксильную группу, С3-С8-циклоалкенилоксигруппу, С3-С8-циклоалкинилоксигруппу, С3-С8-галогенциклоалкенилоксигруппу, С1-С6-алкоксикарбонил, С1-С6-алкоксильную группу, С1-С6-алкилиденаминооксигруппу, С1-С6-алкиламинооксигруппу, (С1-С6-алкил)(С1-С3-алкил)аминооксигруппу, необязательно замещенную феноксигруппу, необязательно замещенную фенил С1-С4-алкоксильную группу, аминогруппу, С1-С6-алкоксиаминогруппу, (С1-С6-алкокси)(С1-С3-алкил)аминогруппу, С1-С6-алкиламиногруппу, (С1-С6-алкил) С1-С6-алкиламиногруппу, необязательно замещенную фениламиногруппу или необязательно замещенную фенил С1-С4-алкиламиногруппу], которое легко получается из производного пиридина [d], представляет собой соединение, обладающее превосходной гербицидной активностью, также как и производное пиридина [d].
Производное пиридина [e] может быть получено: 1) реакцией производного пиридина [d] с соединением [z]
H-R6 [z]
[где R6 имеет значение, указанное выше] или 2) гидролизом производного пиридина [d], превращением в его галогенидкислотное соединение с использованием галогенирующего реагента и последующим взаимодействием продукта с соединением [z].
С точки зрения гербицидной активности в производном пиридина [d] и производном пиридина [e] для группы, обозначенной R3, предпочтительным является атом галогена, в особенности атом хлора, и для группы, обозначенной R4, предпочтительным является атом галогена, в особенности атом фтора.
Производное пиридина [d], производное пиридина [e] и производное пиридона [a] обладают превосходной гербицидной активностью и некоторые из них проявляют высокую избирательность в отношении сельскохозяйственных культур и сорных растений. Производное пиридина [d], производное пиридина [e] и производное пиридона [a] обладают гербицидной активностью против различных перечисленных ниже причиняющих вред сорных растений как при опрыскивании листьев, так и при обработке почвы на нагорном поле.
Сорняки семейства Onagraceae (энотеры): Oenothera erythrosepala и Oenothera laciniata;
Сорняки семейства Ranunculaceae (лютики): Ranunculus muricatus и Ranunculus sardous;
Сорняки семейства Polygonaceae (гречиха): Polygonum convolvulus (горец вьющийся), Polygonum lapathifolium (горец перечный), Polygonum pensylvanicum (горец пенсильванский), Polygonum persicaria (колокольчик), Rumex crispus (щавель курчавый), Rumex obtusifolius и Polygonum cuspidatum (горец японский);
Сорняки семейства Portulacaceae (портулак): Portulaca oleracea (портулак огородный);
Сорняки семейства Caryophyllaceae (гвоздики): Stellaria media (звездчатка средняя) и Cerastium glomeratum (ясколка скученноцветковая);
Сорняки семейства Chenopodiaceae (мари): Chenopodium album (марь белая) и Kochia scoparia (кохия венечная);
Сорняки семейства Amaranthaceae (щирицы): Amaranthus retroflexus (щирица колосистая) и Amaranthus hybridus (щирица гибридная);
Сорняки семейства Crusiferae (крестоцветные): Raphanus raphanistrum (редька дикая), Sinapis arvensis (горчица полевая), Capsella bursa-pastoris (пастушья сумка обыкновенная) и Lepidum virginicum;
Сорняки семейства Leguminosae (бобы): Sesbania exaltata (сесбания экзалтата), Cassia obtusifolia (резуха канадская), Desmodium tortuosum (флоридский клевер), Trifolium repens (клевер ползучий), Vicia sativa (горошек посевной) и Medicago lupulina (люцерна хмелевидная);
Сорняки семейства Malvaceae (представители семейства мальвовых): Abutilon theophrasti (лимнохарис) и Sida spinosa (грудинка колючая);
Сорняки семейства Violaceae (фиалки): Viola arvensis (фиалка полевая) и Viola tricolor (фиалка трехцветная);
Сорняки семейства Rubiaceae (подмаренники): Galium aparine (подмаренники цепкие);
Сорняки семейства Convolvulaceae (ипомеи): Ipomoea hederacea (плющелистная ипомея), Ipomoea purpurea (ипомея пурпурная), Ipomoea hederacea var integriuscula, Ipomoea lacunose и Convolvulus arvensis (вьюнок полевой);
Сорняки семейства Labiatae (мяты): Lamium purpureum (яснотка пурпуровая) и Lamium amplexicaule (яснотка стеблеобъемлющая);
Сорняки семейства Solanaceae (паслены): Datura stramonium (дурман вонючий) и Solanum nigrum (паслен черный);
Сорняки семейства Scrophulariaceae (норичники шишковатые): Veronica persica (вероника персидская), Veronica arvensis и Veronica hederaefolia (вероника плющелистная);
Сорняки семейства Compositae (гибриды): Xanthium pensylvanicum (дурнишник обыкновенный), Helianthus annuus (подсолнечник однолетний), Matricaria chamomilla, Matricaria perforate orinodora (ромашка), Chrysanthemum segetum (хризантема посевная), Matricaria matricarioides (ромашка ромашковидная), Ambrosia artemisiifolia (амброзия обыкновенная), Ambrosia trifida (амброзия трехнадрезанная), Erigeron canadensis, Artemisia princeps (полынь японская), Selidago altissima и Taraxacum officinala;
Сорняки семейства Boraginaceae (бурачники): Myosotis arvensis (незабудка полевая);
Сорняки семейства Asclepiadaceae (частухи): Asclepias syriaca (ваточник сирийский);
Сорняки семейства Euphorbiaceae (молочаи): Euphorbia helioscopia (молочай солнцегляд) и Euphorbia maculate (молочай пятнистый);
Сорняки семейства Geraniaceae (герани): Geranium carolinianum (герань каролинская);
Сорняки семейства Oxalidaceae (кислицы): Oxalis corymbosa (кислица ползучая);
Сорняки семейства Cucurbitaceae (тыквы): Sicyos angulatus;
Сорняки семейства Gramineae (злаковые травы): Echinochloa crus-galli (куриное просо), Setaria viridis (щетинник зеленый), Setaria faberi (многощетинник), Digitaris sanguinalis (росичка кровяная), Eleusine indica (елеузина индийская), Poa annua (мятлик однолетний), Alopecurus myosuroides (лисохвост мышехвостниковидный), Avena fatua (овес пустой), Sorghum halepense (сорго алепское), Agropyron repens (свинорой), Bromus tectorum (костер кровельный), Cynodone dactylon (бермудская трава), Panicum dichotomiflorum (просо вильчатоцветковое), Panicum texanum (просо техасское), Sorghum vulgare (сорго африканское зерновое) и Alopecurus geniculatus (водяной лисохвост);
Сорняки семейства Commelinaceae (традесканции виргинские): Commelina communis (коммелина обыкновенная);
Сорняки семейства Equisetaceae (хвощи): Equisetum arvense (хвощ полевой); и
Сорняки семейства Cyperaceae (осоки): Cyperus iria (сыть вееровидная), Cyperus rotundus (сыть круглая), Cyperus esculentus (осока чешуеплодная).
Кроме того, некоторые из производных пиридина [d] и производных пиридона [a] не являются токсичными для основных сельскохозяйственных культур, включающих кукурузу (Zea mays), пшеницу (Triticum aestivum), ячмень (Hordeum vulgare), рис (Oryza sativa), сорго (Sorghum bicolor), сою культурную (Glycine max), хлопчатник (Gossypium spp.), свеклу сахарную (Beta vulgaris), земляной орех (Arachis hypogaea), подсолнечник (Helianthus annuus), капусту и т.д.; и садовых растений, включающих цветы, овощи и т.д. Кроме того, производное пиридина [d], производное пиридина [е] и производное пиридона [а] эффективно используются для борьбы с различными причиняющими вред сорными растениями при непахотном выращивании сои культурной, кукурузы, пшеницы и т.д. и некоторые из производных пиридина [d], производных пиридина [e] и производных пиридона [a] не проявляют токсичность в отношении сельскохозяйственных культур.
Производное пиридина [d], производное пиридина [е] и производное пиридона [а] обладают также гербицидной активностью против различных перечисленных ниже причиняющих вред сорных растений при обработке затоплением рисового поля.
Сорняки семейства Gramineae (злаковые травы): Echinochloa oryzicola (просо петушье), Scrophulariaceae (норичник шишковатый); Lindernia procumbens (линдерния лежачая); Lythraceae (дербенник): Rotala indica (ротала ветвистая) и Ammannia multiflora;
Семейство Elatinaceae (повойнички): Elatine triandra (повойничек);
Семейство Cyperaceae (осоки): Cyperus difformis (зонтиколистная осока), Scripus juncoides (камыш твердостеблевый), Eleocharis acicularis (игольчатая болотница), Cyperus serotinus и Eleocharis kuroguwai (водяной каштан);
Семейство Pontederiaceae (водяные гиацинты): Monochoria vaginalis;
Семейство Alismataceae (частухи обыкновенные): Sagittaria pygmaea (стрелолист), Sagittaria trifolia и Alisma canaliculatum (частуха водяная);
Семейство Potamogetonaceae (рдесты): Potamogeton distinctus (крупнолистный рдест); и
Семейство Umbelliferae (зонтичные): Oenanthe javanica (сельдерей водный).
Некоторые соединения из производных пиридина [d], производных пиридина [е] и производных пиридона [а] также не проявляют значительную фитотоксичность в отношении пересаженной культуры риса.
Кроме того, с использованием производного пиридина [d], производного пиридина [е] и производного пиридона [а] можно бороться с сорняками, которые прорастают или будут прорастать на некультивированных землях, таких как дамбы (насыпи), береговые откосы рек, дорожные обочины, железнодорожные пути, зеленые полосы парков, земельные участки, места стоянок; аэропорты, промышленные объекты, включающие заводы (фабрики), товарные склады и т.д., неиспользованные земельные наделы и неиспользованные земли в городе; и во фруктовых садах, на лугах (пастбищах), газонах и в лесах. Производное пиридина [d], производное пиридина [е] и производное пиридона [а] обладают также гербицидной активностью против водяных сорных трав, таких как Eichhornia crassipes (водяной гиацинт) и т.д., которые произрастают или будут произрастать в реках, водных путях, каналах, прудах и т.д.
Производное пиридина [d], производное пиридина [е] и производное пиридона [а] имеют такие же свойства, как и гербицидные соединения, описанные в опубликованном международном патенте WO 95/34659. В случае возделываемых культур, где толерантность сообщается культурам за счет введения гена толерантности к гербицидам, представленного в описании указанного патента, производное пиридина [d], производное пиридина [е] и производное пиридона [а] могут быть использованы в больших количествах, чем те количества, которые используются при выращивании обычных культур без толерантности, что обеспечивает возможность более эффективной борьбы с другими неблагоприятными сорными растениями.
Когда производное пиридина [d], производное пиридина [е] или производное пиридона [а] используется в качестве активного ингредиента гербицида, его обычно смешивают с твердыми или жидкими носителями, поверхностно-активными веществами и другими вспомогательными добавками с получением при этом эмульгируемых концентратов, смачивающихся порошков, образующих суспензию концентратов, гранул, концентрированных эмульсий, диспергируемых в воде гранул и т.д.
Указанные препараты могут включать производное пиридина [d], производное пиридина [е] и производное пиридона [а] в качестве активного ингредиента, взятого в количестве от 0,001 до 80 мас.%, предпочтительно от 0,005 до 70 мас.%.
Твердый носитель может включать, например, минеральные тонкоизмельченные порошки, такие как каолиновая глина, аттапульгит, бентонит, кислая глина, пирофиллит, тальк, диатомовая земля, кальцит и т.д.; органические тонкоизмельченные порошки, такие как порошок ореховой скорлупы и т.д.; водорастворимые тонкоизмельченные порошки органических соединений, таких как мочевина и т.д.; тонкоизмельченные порошки неорганических солей, таких как сульфат аммония и т.д.; и тонкоизмельченные порошки синтетического гидратированного оксида кремния. Жидкий носитель может включать, например, ароматические углеводороды, такие как метилнафталин, фенилксилилэтан, алкилбензол (например, ксилол) и т.д.; спирты, такие как изопропанол, этиленгликоль, 2-этоксиэтанол и т.д.; сложные эфиры, такие как диалкилфталат и т.д., кетоны, такие как ацетон, циклогексанон, изофорон и т.д.; минеральные масла, такие как машинное масло и т.д.; растительные масла, такие как соевое масло, хлопковое масло и т.д.; диметилсульфоксид; N,N-диметилформамид; ацетонитрил; N-метилпирролидон; воду; и т.д.
В качестве поверхностно-активного вещества для эмульгирования, диспергирования или повышения смачивающей способности могут быть использованы анионогенные поверхностно-активные вещества, такие как алкилсульфатные соли, алкилсульфонатные соли, алкиларилсульфонатные соли, диалкилсульфосукцинатные соли, фосфатные соли простого полиоксиэтиленалкиларилового эфира и т.д.; и неионогенные поверхностно-активные вещества, такие как простые полиоксиэтиленалкиловые эфиры, простые полиоксиэтиленалкилариловые эфиры, блок-сополимеры полиоксиэтилена и полиоксипропилена, сложные эфиры жирных кислот и сорбитана, сложные эфиры полиоксиэтиленсорбитана и жирных кислот и т.д.
В качестве других вспомогательных добавок могут быть указаны соли лигнинсульфоновой кислоты, соли альгиновой кислоты, поливиниловый спирт, аравийская камедь, КМЦ (карбоксиметилцеллюлоза), кислый ИПФ (кислый изопропилфосфат) и т.д.
Из производного пиридина [d], производного пиридина [е] или производного пиридона [а] получают препарат и затем используют для обработки почвы, опрыскивания листьев или обработки затоплением до или после появления сорняков. Обработка почвы может включать поверхностную обработку почвы и внесение в толщу почвы. Кроме того, опрыскивание листьев может включать нанесение на растения и непосредственное нанесение, когда оно осуществляется только на сорные растения с тем, чтобы исключить попадание на культурные растения.
Кроме того, имеются ситуации, когда при введении в смесь других гербицидов повышенная гербицидная активность подтверждается.
В случае, когда производное пиридина [d], производное пиридина [е] или производное пиридона [а] используется в качестве активного ингредиента гербицида, доза внесения может изменяться в зависимости от погодных условий, вида препаратов, времени внесения, способов внесения, состояния почвы, целевых культур и целевых сорных растений, но обычно она составляет от 0,01 до 20000 г, предпочтительно от 1 до 12000 г на один гектар. Когда вносят эмульгируемые концентраты, смачивающиеся порошки, образующие суспензию концентраты, концентрированные эмульсии, диспергируемые в воде гранулы и т.д., их вносят обычно при разбавлении водой, взятой в количестве от 10 до 1000 литров (если необходимо, вода может включать вспомогательную добавку, такую как вещество, повышающее смачивающую способность), с тем, чтобы указанное количество можно было внести на каждый гектар. Гранулы и некоторые виды текущих препаратов обычно вносят без разбавления. Кроме вышеуказанных поверхностно-активных веществ, вспомогательная добавка, которая может быть использована в данном изобретении, в случае необходимости, может включать сложные эфиры полиоксиэтилена и жирных кислот, соли лигнинсульфоновой кислоты, соли абиетиновой кислоты, соли динафтилметандисульфоновой кислоты, концентрированное масло сельскохозяйственной культуры, растительные масла, такие как соевое масло, кукурузное масло, хлопковое масло, подсолнечное масло и т.д.
Далее настоящее изобретение более подробно объяснено примерами и ссылочными примерами, но указанные примеры ни в коей мере не ограничивают настоящее изобретение.
Пример 1
К смеси 0,5 г 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-1Н-пиридин-2-она

8 мг димера трифторацетата родия (II) и 15 мл дихлорэтана при 80°С в течение 3 часов добавляли по каплям 0,15 г метилдиазоацетата. После добавления по каплям реакционную смесь дополнительно перемешивали в течение одного часа при 80°С и затем концентрировали. Остаток подвергали хроматографии на колонке с силикагелем (элюент:смесь гексан/этилацетат = от 3/1 до 0/1) с получением 0,18 г извлеченного 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-1Н-пиридин-2-она и 0,34 г 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-(метоксикарбонилметокси)пиридина.

Т.пл. 52,2°С.
1H ЯМР (300 МГц, CDCl3, TMS δ (ч/млн)): 3,50 (3H, кв, J=1,0 Гц), 3,70 (3Н, c), 4,90 (1H, д, J=15,8 Гц), 4,97 (1H, д, J=15,8 Гц), 6,29 (1H, c), 6,90-6,95 (2H, м), 7,32 (1H, дд, J=1,9 Гц, 7,7 Гц), 7,37 (1H, д, J=8,7 Гц), 7,92 (1H, дд, J=1,9 Гц, 4,9 Гц).
Пример 2
В смесь 1,0 г 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-1Н-пиридин-2-она, 42 мкл комплекса трифторид бора-диэтиловый эфир и 40 мл 1,2-дихлорэтана в течение 2 часов при комнатной температуре добавляли по каплям 0,4 мл этилдиазоацетата (степень чистоты 90%). После добавления по каплям реакционную смесь дополнительно перемешивали в течение двух часов и затем подвергали хроматографии на колонке с силикагелем (элюент:смесь гексан/этилацетат = 2:1) с получением 1,10 г 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-(этоксикарбонилметокси)пиридина.
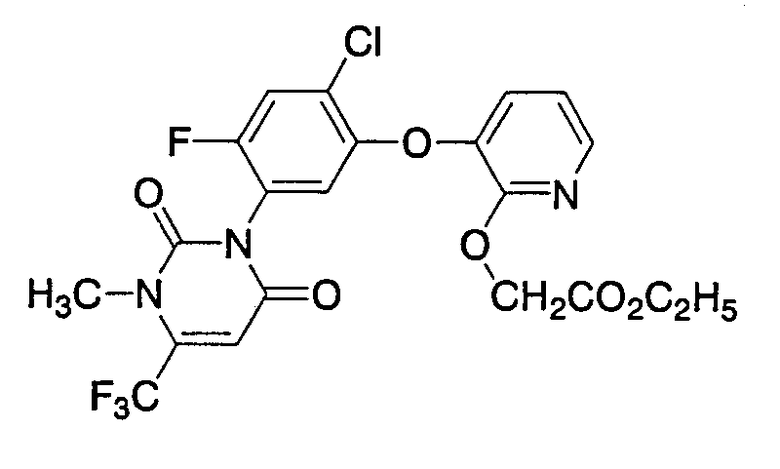
1H ЯМР (300 МГц, CDCl3, TMS δ (ч/млн)): 1,25 (3H, т, J=7,1 Гц), 3,50 (3H, кв, J=1,2 Гц), 4,16 (2H, кв, J=7,1 Гц), 4,88 (1H, д, J=15,9 Гц), 4,96 (1H, д, J=15,9 Гц), 6,29 (1H, c), 6,9-7,0 (2H, м), 7,3-7,4 (2H, м), 7,9-8,0 (1H, м).
N-алкилированное соединение 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-1-(этоксикарбонилметокси)-1Н-пиридин-2-он не обнаруживали.
Условия анализа:
Высокоэффективная жидкостная хроматография
Жидкостный хроматограф LC-10AS (производство фирмы Shimadzu Corp.)
Детектор: детектор УФ-Vis SPD-10A (производство фирмы Shimadzu Corp.)
Аналитическая длина волны: 254 нм
Колонка: SUMIPAX ODS A-212 (производство фирмы Sumika Chemical Analysis Service)
Температура колонки: комнатная температура
Подвижная фаза: ацетонитрил/вода = 1/1
Пример 3
Первая стадия
В смесь 1,01 г гидрохлорида этилглицината, 1,83 г воды и 5,15 г 1,2-дихлорэтана примерно при -5°С добавляли по каплям раствор 0,60 г нитрита натрия в 1,82 г воды. После добавления по каплям реакционную смесь дополнительно перемешивали в течение 1,5 часов при такой же температуре, в нее добавляли по каплям 0,67 г 5%-ной серной кислоты и затем опять перемешивали в течение 10 минут. Затем отделенный органический слой промывали 5%-ным водным раствором бикарбоната натрия и сушили над безводным сульфатом магния с получением 1,2-дихлорэтанового раствора этилдиазоацетата.
Вторая стадия
В смесь 1,8 г 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-1Н-пиридин-2-она, 0,026 г комплекса трифторид бора-диэтиловый эфир и 6 мл 1,2-дихлорэтана при комнатной температуре в течение 30 минут добавляли по каплям 1,2-дихлорэтановый раствор этилдиазоацетата, полученный на первой стадии. После добавления по каплям реакционную смесь дополнительно перемешивали в течение 1,5 часов, в нее добавляли по каплям 2 мл 15%-ной серной кислоты и затем опять перемешивали в течение 30 минут. К реакционной смеси добавляли 20 мл водного насыщенного раствора бикарбоната натрия и отделенный органический слой сушили над безводным сульфатом магния и концентрировали. Остаток подвергали хроматографии на колонке с силикагелем (элюент:смесь гексан/этилацетат = 2/1) с получением 1,94 г 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-(этоксикарбонилметокси)пиридина.
Пример 4
В смесь 1,0 г 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-1Н-пиридин-2-она, 121 мг тетрахлорида олова и 40 мл 1,2-дихлорэтана при комнатной температуре в течение 2 часов добавляли по каплям 0,4 мл этилдиазоацетата (степень чистоты 90%). После добавления по каплям реакционную смесь дополнительно перемешивали в течение 2 часов и подвергали хроматографии на колонке с силикагелем (элюент:смесь гексан/этилацетат = 2/1) с получением 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-(этоксикарбонилметокси)пиридина.
Пример 5
В смесь 1,0 г 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-1Н-пиридин-2-она, 70 мг трифторметансульфоновой кислоты и 40 мл 1,2-дихлорэтана при комнатной температуре в течение 2 часов добавляли по каплям 0,4 мл этилдиазоацетата (степень чистоты 90%). После добавления по каплям реакционную смесь дополнительно перемешивали в течение 2 часов и подвергали хроматографии на колонке с силикагелем (элюент:смесь гексан/этилацетат = 2/1) с получением 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-(этоксикарбонилметокси)пиридина.
Далее описаны ссылочные промеры для получения исходных соединений и т.д.
Ссылочный пример 1
Первая стадия
К смеси 20,0 г 2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенола, 10,8 г диметилхлормалоната и 120 мл N,N-диметилформамида добавляли 9,79 г карбоната калия и перемешивали при 70°С в течение 1,5 часов. После охлаждения реакционной смеси до комнатной температуры ее вливали в смесь хлористоводородной кислоты и льда и экстрагировали этилацетатом. Органический слой последовательно промывали 10%-ным водным раствором карбоната калия и насыщенным солевым раствором, сушили над безводным сульфатом магния и концентрировали. Остаток промывали метанолом и диизопропиловым эфиром с получением 21,6 г диметил [2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]малоната.
Т.пл. 141,1°С.
1H ЯМР (300 МГц, CDCl3, TMS δ (ч/млн)): 3,55 (д, 3H, J=1,1 Гц), 3,86 (c, 6H), 5,15 (c, 1H), 6,35 (c, 1H), 6,99 (д, 1H, J=6,5 Гц), 7,3-7,4 (м, 1H).
Вторая стадия
В смесь 21,6 г диметил [2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]малоната, 80 мл хлороформа и 80 мл метанола при 0°С добавляли по каплям 26,3 мл 7 н. раствора аммиак/метанол. После добавления по каплям реакционную смесь перемешивали в течение 20 минут и затем при комнатной температуре в течение 7 часов. Реакционную смесь фильтровали и концентрировали с получением 6,91 г метил 2-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-карбоксамидацетата.
Т.пл. 196,4°С (разл.)
1H ЯМР (250 МГц, CDCl3, TMS δ (ч/млн)): 3,56 (c, 3H), 3,84 (c, 3H), 5,06 (c, 1H), 5,76 (в.c, 1H), 6,36 (c, 1H), 6,8-7,0 (м, 2H), 7,37 (д, 1H, J=8,7 Гц).
Третья стадия
К смеси 363 мг метил 2-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-карбоксиамидацетата, 6,0 мл тетрагидрофурана и 50 мг акролеина при 0°С добавляли 9 мг трет-бутоксида калия и перемешивали в течение 30 минут. Затем после добавления к реакционной смеси 17 мг моногидрата п-толуолсульфоновой кислоты смесь кипятили с обратным холодильником в течение одного часа при перемешивании. Реакционную смесь охлаждали до комнатной температуры, затем в нее вливали воду и смесь экстрагировали этилацетатом. Органический слой сушили над безводным сульфатом магния и концентрировали. Остаток подвергали хроматографии на колонке с силикагелем с получением 202 мг 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-3-метоксикарбонил]-3,4-дигидро-1Н-пиридин-2-она.
Т.пл. 82,4°С.
Четвертая стадия
Смесь 202 мг 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-3-метоксикарбонил-3,4-дигидро-1Н-пиридин-2-она, 52 мг хлорида лития, 2 мл диметилсульфоксида и 10 мкл воды перемешивали при 120°С в течение одного часа. Реакционную смесь охлаждали до комнатной температуры, затем в нее вливали воду и смесь экстрагировали этилацетатом. Органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом магния и концентрировали. Остаток подвергали хроматографии на колонке с силикагелем с получением 70 мг 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-3,4-дигидро-1Н-пиридин-2-она.
Т.пл. 91,0°С.
1H ЯМР (300 МГц, CDCl3, TMS δ (ч/млн)): 2,7-2,8 (м, 2Н), 3,53 (с, 3Н), 4,6-4,8 (м, 1Н), 5,0-5,2 (м, 1H), 6,0-6,1 (м, 1H), 6,33 (c, 1H), 7,1-7,2 (м, 1H), 7,28 (д, 1H, J=9,0 Гц), 7,7-8,1 (м, 1H).
Пятая стадия
Смесь 144 мг 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-3,4-дигидро-1Н-пиридин-2-она, 0,66 мл тетрагидрофурана и 163 мг о-хлоранила кипятили с обратным холодильником в течение одного часа при перемешивании. Реакционную смесь охлаждали до комнатной температуры, затем в нее вливали воду и смесь экстрагировали этилацетатом. Органический слой сушили над безводным сульфатом магния и концентрировали. Остаток подвергали хроматографии на колонке с силикагелем с получением 72 мг 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-1Н-пиридин-2-она.
1H ЯМР (300 МГц, CDCl3, TMS δ (ч/млн)): 3,52 (c, 3Н), 6,22 (дд, 1H, J=7,0, 7,0 Гц), 6,32 (c, 1H), 6,95 (д, 1H, J=6,6 Гц), 7,00 (дд, 1H, J=7,0, 1,6 Гц), 7,2-7,3, (м, 1H), 7,39 (д, 1H, J=8,9 Гц).
Ссылочный пример 2
Первая стадия
К смеси 1,3 г гидрида натрия и 100 мл диметоксиэтана при комнатной температуре добавляли 10 г 2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенола и перемешивали в течение 30 минут. Затем в нее добавляли 2,2 г иодида натрия и 6,7 г неочищенного 2-хлор-2-(метилтио)ацетамида, перемешивали при комнатной температуре в течение 3 часов и в реакционную смесь вливали воду. Реакционную смесь экстрагировали этилацетатом. Органический слой промывали водным раствором бикарбоната натрия, сушили над безводным сульфатом магния и концентрировали. Остаток подвергали хроматографии на колонке с силикагелем (элюент:этилацетат) с получением 10,2 г 2-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-(метилтио)ацетамида.
1H ЯМР (300 МГц, CDCl3, TMS δ (ч/млн)): 2,18 (3H, c), 3,56 (3H, кв, J=1,3 Гц), 5,54 (1H, д, J=3,4 Гц), 5,94 (1H, шир), 6,37 (1H, д, 3=2,9 Гц), 6,80 (1H, шир), 7,06-7,11 (1H, м), 7,36 (1H, д, J=9,0 Гц).
Вторая стадия
К смеси 2-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-(метилтио)ацетамида и 50 мл хлороформа при комнатной температуре в течение 3 дней добавляли 3,7 г м-хлорпербензойной кислоты. К реакционной смеси добавляли водный раствор бикарбоната натрия и водный раствор тиосульфата натрия. Реакционную смесь экстрагировали этилацетатом. Органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом магния и концентрировали. Остаток подвергали хроматографии на колонке с силикагелем (элюент:этилацетат) с получением 3,3 г 2-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-(метилсульфонил)ацетамида.
1H ЯМР (300 МГц, CDCl3, TMS δ (ч/млн)): 3,11 (3H, c), 3,46 (1,5H, c), 3,49 (1,5H, c), 5,44 (1H, c), 6,26 (0,5H, c), 6,30 (0,5H, c), 6,55 (1H, шир), 7,03 (1H, шир), 7,27-7,34 (2H, м).
Третья стадия
К смеси 1,3 г 2-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-(метилсульфонил)ацетамида, 0,21 г акролеина и 20 мл ТГФ при комнатной температуре добавляли 0,03 г трет-бутоксида калия и перемешивали в течение 3,5 часов. Затем добавляли 0,1 г п-толуолсульфоновой кислоты и реакционную смесь кипятили с обратным холодильником в течение 4 часов при перемешивании. Реакционную жидкость концентрировали при пониженном давлении и остаток подвергали хроматографии на колонке с силикагелем (элюент:смесь гексан/этилацетат = 1/1) с получением 0,55 г 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-3-(метилсульфонил)-3,4-дигидро-1Н-пиридин-2-она.
1H ЯМР (300 МГц, CDCl3, TMS δ (ч/млн)): 2,75-2,88 (1H, м), 3,19-3,31 (1H, м), 3,30 (1H, c), 3,54 (3H, c), 4,97-5,05 (1H, м), 6,00-6,05 (1H, м), 7,27-7,36 (2H, м), 8,04 (1H, д, J=4,1 Гц).
Четвертая стадия
Смесь одного эквивалента 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-3-(метилсульфонил)-3,4-дигидро-1Н-пиридин-2-она, 0,1 эквивалента п-толуолсульфоновой кислоты и толуола кипятили с обратным холодильником при перемешивании. После реакции реакционную жидкость концентрировали и остаток подвергали хроматографии на колонке с силикагелем с получением 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-1Н-пиридин-2-она.
Ссылочный пример 3
Первая стадия
К 8,33 г диметилхлормалоната при 0°С добавляли по каплям 7 н. раствор аммиак/метанол и затем перемешивали в течение 10 минут. После этого реакционную смесь перемешивали при комнатной температуре в течение 2 часов, фильтровали и концентрировали. Остаток растворяли в смешанном растворителе, состоящем из хлороформа и метанола. Раствор фильтровали и затем концентрировали. Остаток подвергали хроматографии на колонке с силикагелем с получением 4,4 г метил 2-хлор-2-карбоксамидацетата.
Т.пл. 79,5°С.
1H ЯМР (300 МГц, CDCl3, TMS δ (ч/млн)): 3,86 (c, 3H), 4,79 (c, 1H), 5,8-6,0 (шир.c, 1H), 6,5-6,7 (шир.c, 1H).
Вторая стадия
К смеси 0,50 г 2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенола, 0,22 г метил-2-хлор-2-карбоксамидацетата и 0,75 мл N,N-диметилформамида добавляли 0,24 г карбоната калия и перемешивали при 50-60°С в течение 0,5 часа. К смеси добавляли 0,75 мл N,N-диметилформамида и затем перемешивали при 50-60°С в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры и вливали на лед. Осажденные кристаллы отфильтровывали и последовательно промывали водой и гексаном с получением 0,42 г метил 2-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-(карбоксамид)ацетата.
Ссылочный пример 4
Первая стадия
К смеси 10 г 3-(2,5-дифтор-4-нитрофенил)-1-метил-6-трифторметил-1Н-пиримидин-2,4-диона, 5,0 г 3-гидрокси-2-метоксипиридина и 100 мл N,N-диметилформамида добавляли 7,8 г карбоната калия и кипятили с обратным холодильником в течение 6 часов при перемешивании. Затем реакционную смесь вливали в воду и экстрагировали этилацетатом. Органический слой последовательно промывали водным раствором бикарбоната натрия и насыщенным солевым раствором, сушили над сульфатом магния и концентрировали с получением 12,8 г 3-[4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-2-нитро-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-метоксипиримидина.
1H ЯМР (300 МГц, CDCl3, TMS δ (ч/млн)): 3,52 (3H, кв, J=1,2 Гц), 3,93 (3H, c), 6,32 (1H, c), 6,76 (1H, д, J=5,8 Гц), 6,93 (1H, дд, J=5,0 Гц, 7,8 Гц), 7,40 (1H, дд, J=1,4 Гц, 7,8 Гц), 7,90 (1H, д, J=8,6 Гц), 8,04 (1H, дд, J=1,4 Гц, 5,0 Гц).
Вторая стадия
В смесь 6,3 г порошка железа, 50 мл уксусной кислоты и 50 мл воды при 80°С добавляли по каплям 60 мл этилацетатного раствора 3-[4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-2-нитро-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-метоксипиримидина. После добавления по каплям реакционную смесь перемешивали в течение 15 минут при этой же температуре и охлаждали до комнатной температуры. Реакционную смесь вливали в воду и экстрагировали этилацетатом. Органический слой последовательно промывали водой, водным раствором бикарбоната натрия и насыщенным солевым раствором и концентрировали с получением 12,1 г 3-[2-амино-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-метоксипиридина.
1H ЯМР (300 МГц, CDCl3, TMS δ (ч/млн): 3,51 (3H, кв, J=1,0 Гц), 4,00 (3H, c), 4,20 (1H, шир), 6,30 (1H, c), 6,62 (1H, д, J=10,6 Гц), 6,63 (1H, д, J=7,1 Гц), 6,82 (1H, дд, J=5,0 Гц, 7,8 Гц), 7,18 (1H, дд, J=1,4 Гц, 7,8 Гц), 7,90 (1H, дд, J=1,4 Гц, 5,0 Гц).
Третья стадия
В смесь 12 г 3-[2-амино-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-метоксипиридина, 2,8 г хлорида меди (I), 5,7 г хлорида меди (II) и 100 мл ацетонитрила добавляли по каплям 4,6 г изоамилнитрита. После добавления по каплям реакционную смесь перемешивали в течение 2 часов и оставляли на 2 дня. Затем в нее добавляли водный раствор аммиака и смесь экстрагировали этилацетатом. Органический слой последовательно промывали водой и насыщенным солевым раствором, сушили над безводным сульфатом магния и концентрировали. Остаток подвергали хроматографии на колонке с силикагелем (элюент:смесь гексан/этилацетат = 2/1) с получением 8,6 г 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-метоксипиридина.
Т.пл. 179,5°С.
Четвертая стадия
К смеси 0,5 г 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-2-метоксипиридина и 10 мл хлороформа добавляли 0,5 г трибромида бора и перемешивали при комнатной температуре в течение 3 часов. Затем реакционную смесь концентрировали. Остаток вливали в воду и экстрагировали этилацетатом. Органический слой сушили над безводным сульфатом магния и концентрировали. Остаток подвергали хроматографии на колонке с силикагелем (элюент:этилацетат) с получением 0,31 г 3-[2-хлор-4-фтор-5-(3-метил-2,6-диоксо-4-трифторметил-1,2,3,6-тетрагидропиримидин-1-ил)фенокси]-1Н-пиридин-2-она.
Т.пл. 180,8°С.
Ниже перечислены некоторые из производных пиридина [d] и производных пиридина [e] с номерами их соединений.
Данные соединения имеют следующую формулу:

Затем ниже перечислены некоторые из производных пиридона [a] с номерами их соединений.
Данные соединения имеют следующую формулу:
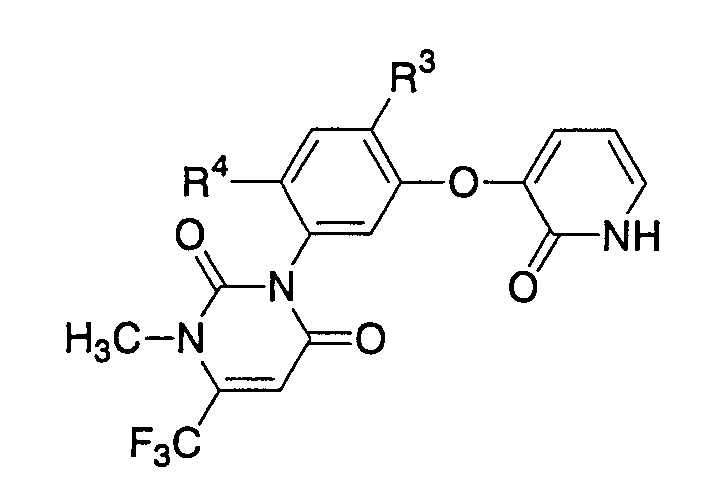
Далее следуют примеры препаратов, где в качестве гербицидных активных ингредиентов используются производное пиридина [d] и производное пиридона [a], в данных примерах часть(и) представляет(ют) часть(и) по массе.
Ссылочный пример 1 препарата
Пятьдесят частей каждого из соединений 1-84, 3 части лигнинсульфоната кальция, 2 части лаурилсульфата натрия и 45 частей синтетического гидратированного оксида кремния тщательно измельчали и смешивали с получением смачиваемого порошка каждого соединения.
Ссылочный пример 2 препарата
Десять частей каждого из соединений 1-84, 14 частей простого полиоксиэтиленстирилфенилового эфира, 6 частей додецилбензолсульфоната кальция, 35 частей ксилола и 35 частей циклогексанона тщательно смешивали с получением эмульгируемого концентрата каждого соединения.
Ссылочный пример 3 препарата
Две части каждого из соединений 1-84, 2 части синтетического гидратированного оксида кремния, 2 части лигнинсульфоната кальция, 30 частей бентонита и 64 части каолиновой глины тщательно измельчали и смешивали и смесь тщательно перемешивали с водой, затем гранулировали и сушили с получением гранул каждого соединения.
Ссылочный пример 4 препарата
Двадцать пять частей каждого из соединений 1-84, 50 частей 10%-ного водного раствора поливинилового спирта и 25 частей воды смешивали и измельчали до достижения среднего размера частиц 5 мкм или менее с получением суспендируемого концентрата каждого соединения.
Ссылочный пример 5 препарата
Пять частей каждого из соединений 1-84 добавляли к 40 частям 10%-ного водного раствора поливинилового спирта и смесь эмульгировали диспергированием с использованием гомогенизатора до достижения среднего размера частиц 10 мкм или менее, затем добавляли 55 частей воды, при этом получали концентрированную эмульсию каждого соединения.
Далее показано, что производное пиридина [d] и производное пиридона [a] применимы в качестве гербицидных активных ингредиентов.
Ссылочный пример 1 испытаний
Цилиндрические пластиковые горшочки, каждый из которых имеет диаметр 10 см и глубину 10 см, наполняли почвой и затем засевали плющелистной ипомеей и лимнохарисом. Подопытные растения выращивали в теплице в течение 10 дней. Затем из каждого из соединений 1, 2, 3, 6, 8, 12, 15, 16, 19, 21, 40, 59 и 76 получали эмульгируемый концентрат в соответствии со ссылочным примером 2 препарата и разбавляли водой, содержащей вещество, повышающее смачивающую способность. Полученный разбавленный препарат однородно разбрызгивали на листву подопытных растений с использованием опрыскивателя при норме расхода 1000 литров на гектар. После разбрызгивания подопытные растения выращивали в теплице в течение 12 дней и определяли гербицидную активность. В результате было найдено, что каждое из соединений 1, 2, 3, 6, 8, 12, 15, 16, 19, 21, 40, 59 и 76 полностью подавляло рост плющелистной ипомеи и лимнохариса при норме расхода 125 г/га.
Ссылочный пример 2 испытаний
Цилиндрические пластиковые горшочки, каждый из которых имеет диаметр 10 см и глубину 10 см, наполняли почвой и затем засевали плющелистной ипомеей и лимнохарисом. Из каждого из соединений 1, 2, 3, 6, 8, 12, 15, 16, 19, 21, 40, 59 и 76 получали эмульгируемый концентрат в соответствии со ссылочным примером 2 препарата и разбавляли водой. Полученный разбавленный препарат однородно разбрызгивали на поверхность почвы с использованием опрыскивателя при норме расхода 1000 литров на гектар. После разбрызгивания подопытные растения выращивали в теплице в течение 19 дней и определяли гербицидную активность. В результате было найдено, что каждое из соединений 1, 2, 3, 6, 8, 12, 15, 16, 19, 21, 40, 59 и 76 полностью подавляло рост плющелистной ипомеи и лимнохариса при норме расхода 500 г/га.
Промышленная применимость
В соответствии со способом настоящего изобретения может быть выгодно получено новое производное пиридина [d], обладающее превосходной гербицидной активностью.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ УРАЦИЛА, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ, СПОСОБ БОРЬБЫ С СОРНЯКАМИ И ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ (ВАРИАНТЫ) | 2001 |
|
RU2264395C2 |
| ПРОИЗВОДНЫЕ УРАЦИЛА, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ ПОДАВЛЕНИЯ РОСТА СОРНЯКОВ | 2000 |
|
RU2259359C2 |
| ПРОИЗВОДНЫЕ ДИГИДРОБЕНЗОФУРАНА, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ УНИЧТОЖЕНИЯ СОРНЯКОВ | 1994 |
|
RU2125993C1 |
| ПРОИЗВОДНЫЕ УРАЦИЛА, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С СОРНЯКАМИ | 1990 |
|
RU2029472C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕНОКСИЗАМЕЩЕННЫХ 2-ПИРИДОНОВЫХ СОЕДИНЕНИЙ | 2003 |
|
RU2300526C2 |
| ДИАРИЛОВЫЕ ЭФИРЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩИЕ ИХ ГЕРБИЦИДНЫЕ КОМПОЗИЦИИ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СПОСОБ БОРЬБЫ С СОРНЯКАМИ И СПОСОБ ДЕСИКАЦИИ РАСТЕНИЙ | 1998 |
|
RU2180336C2 |
| НОВОЕ СОЕДИНЕНИЕ БЕНЗИМИДАЗОЛОНА И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2018 |
|
RU2803938C2 |
| КОНДЕНСИРОВАННЫЕ ТРИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ ИМИДАЗОЛА В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ TNF | 2014 |
|
RU2700004C1 |
| КОНДЕНСИРОВАННЫЕ ТРИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ ИМИДАЗОЛА В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ TNF | 2014 |
|
RU2679914C9 |
| КОНДЕНСИРОВАННЫЕ ПРОИЗВОДНЫЕ ИМИДАЗОЛА И ПИРАЗОЛА В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ TNF | 2014 |
|
RU2687093C1 |
Изобретение относится к новому способу получения производного пиридина формулы [d]

где R1, R3 и R4 являются такими, как они определены ниже, взаимодействием нового производного пиридона [а]
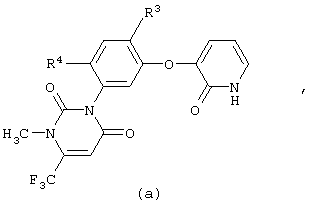
где R3 представляет собой атом галогена, цианогруппу или нитрогруппу и R4 представляет собой атом водорода или атом галогена, с производным α-диазоэфира [f]
N2CHCOR1, [f]
где R1 представляет собой C1-С6-алкоксигруппу, в присутствии кислоты. Описываемый способ является удобным и выгодным способом получения производных пиридина формулы [d], обладающих специфической системой заместителей и проявляющих гербицидную активность. 2 н. и 6 з.п. ф-лы, 2 табл.
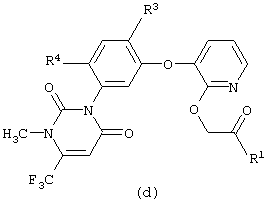
где R1, R3 и R4 являются такими, как они определены ниже,
взаимодействием производного пиридона [а]
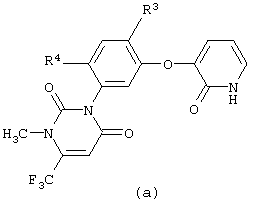
где R3 представляет собой атом галогена, цианогруппу или нитрогруппу;
R4 представляет собой атом водорода или атом галогена,
с производным α-диазоэфира [f]
N2CHCOR1, [f]
где R1 представляет собой C1-С6-алкоксигруппу,
в присутствии кислоты.
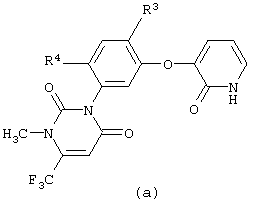
где R3 представляет собой атом галогена, цианогруппу или нитрогруппу;
R4 представляет собой атом водорода или атом галогена.
Приоритет по пунктам:
| ПРОИЗВОДНЫЕ 3-(3-АРИЛОКСИФЕНИЛ)-1-(ЗАМЕЩЕННЫЙ МЕТИЛ)-S-ТРИАЗИН-2,4,6-ТРИОНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНОЕ СОЕДИНЕНИЕ, СПОСОБ ПОДАВЛЕНИЯ НЕЖЕЛАТЕЛЬНЫХ ВИДОВ РАСТЕНИЙ И ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ | 1996 |
|
RU2159769C2 |
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| ПРИВОДНОЙ МЕХАНИЗМ ШТОРНОГО ОБТЮРАТОРА КИНОАППАРАТА | 0 |
|
SU255047A1 |
Авторы
Даты
2006-03-20—Публикация
2002-07-31—Подача