Изобретение относится к медицине и касается способов защиты организма при облучении, конкретно к композиции с радиопротекторными свойствами и к способу ее получения, и может найти применение в радиобиологическом эксперименте, в клинической и сельскохозяйственной практике на территориях с радиоактивным загрязнением.
Для решения поставленной задачи ранее использовали традиционные средства с различным действием: энтеросорбенты, иммуностимуляторы, антибактериальные и противогрибковые препараты, радиопротекторы. К последним относятся как специфические соединения, например, содержащие серу (Куна П. Химическая радиозащита. М., 1989), фосфор (RU 204969), так и неспецифические, в частности витамины Е и С.
При этом неспецифические радиопротекторы отличаются тем, что в дополнение к радиопротекторному (выраженному значительно слабее, чем у специфических средств) действию обладают иммуномодулирующей, ранозаживляющей, противовирусной или иной дополнительной активностью, которая способствует выживанию организмов, подвергшихся лучевому поражению, не только в первые дни после облучения, но и в более поздние сроки, когда проявляются осложнения и нарушения не только вследствие «радиационного синдрома», но и со стороны различных органов.
К неспецифическим радиопротекторам также относятся биофлавоноиды, кверцитин и дигидрокверцитин (ДКВ), которые используют в составе комплексных препаратов и биологических добавок, обладающих помимо радиопротекторного, также общеукрепляющим действием (RU 2065278; RU 2187319; RU 2043030).
Сухие молочные продукты и молочные консервы согласно RU 2043030 обладают радиопротекторным свойствам благодаря добавлению в них 0,005-2% ДКВ и 0,005-1% аскорбиновой кислоты. Однако данная композиция является продуктом питания, т.е. при высокой пищевой ценности обладает слабым радиозащитным эффектом, а кроме того, неприемлема для лиц с аллергией на молочные продукты или с иным рационом питания.
Целью настоящего изобретения является создание препарата с более высоким радиопротекторным эффектом. Такой эффект обеспечивает композиция под торговым названием «софилар», содержащая 97-99% арабиногалактана (АГ) и 1-3% ДКВ. Софилар обладает выраженным радиопротекторным действием. Препарат может быть выполнен в стандартной лекарственной форме, пригодной для приема внутрь.
Традиционно АГ использовался как нетоксичный наполнитель или полимер-носитель при создании лекарственных средств (US5912008; US6372194; US6399086), а также как средство для диагностики некоторых бактерий, обладающее слабым антибактериальным эффектом (ЕР 13 8784). Выявлена некоторая иммунологическая активность АГ (Phytochemistry 1988, 27(8), 2511-2517).
ДКВ (3,5,7,3',4'-пентагидроксифлаванон), как биофлавоноид оказывает разнонаправленное действие и имеет более широкое применение в составе с другими флавоноидами при комплексной терапии широкого круга заболеваний (RU2090205; WO 93/23096; DE 4432947; WO 96/10341; US 5424331; ЕР 719554 и др.). В частности, известно его радиозащитное действие (Ильюченко Т.Ю. и др. «Фармакология и токсикология», 1975, №5, с.607-612).
Неожиданно было выявлено, что сочетание ДКВ с АГ в заявленном соотношении обладает радиопротекторным действием более сильным, чем действие ДКВ при самостоятельном применении. Кроме того, АГ как традиционный наполнитель может служить необходимым компонентом при создании лекарственного препарата без введения иных дополнительных эксципиентов: композиция в заявленном соотношении ингредиентов является стабильной, пластичной и позволяет таблетировать готовую лекарственную форму, в которой количество ДКВ определяется весом готовой таблетки.
В результате проведенных исследований было выявлено, что эффективность действия ДКВ как радиопротектора повышалась в отсутствии других биофлавоноидов и оказывала более направленное действие.
Пример 1.
Радиопротекторные свойства ДКВ разной степени чистоты и в разных композициях
Эксперимент проводился на 6 группах мышей линии СВА средней массой 20 г, по 10 особей в каждой группе, подвергнутых внешнему гамма облучению 3,0 Гр (мощность дозы - 41,13 рад/мин) на установке «Гамма-Cell»; время облучения 7 мин, расстояние от источника 12,5 см). ДКВ разной степени очистки вводили внутрижелудочно из расчета 1 мг на мышь в виде взвеси в 3%-ном растворе крахмала или в виде смеси с АГ за 20 мин до облучения; контрольная группа получала крахмальную взвесь.
Готовили следующие препараты для введения группам животных: ДКВ с чистотой 93% (дополнительно включал дигидрокемпферол и нарингенин) в крахмальной взвеси; ДКВ с чистотой 98% в крахмальной взвеси; смесь ДКВ (0,05%) и АГ (99,5%); смесь ДКВ (1-2%) и АГ (99-98%); смесь ДКВ (3%) и АГ (97%).
Эффективность лечения проверяли по содержанию лейкоцитов в периферической крови через 9 дней (счет проводили при помощи счетной камеры Тома-Горяева) и по количеству клеток в мозге бедренной кости - через 14 дней, соответственно, после облучения. Результаты эксперимента приведены в таблицах.
Как видно из таблицы 1, по обоим анализируемым показателям более чистый препарат, содержащий 98% ДКВ, оказывал более сильное и выраженное действие, чем менее чистый, с содержанием ДКВ 93%. Так, показатели контрольной группы клеточности костного мозга отличались от группы с 98% ДКВ в крахмале в 2.1 раза против отличия в 1,7 раз для группы с 93% ДКВ в крахмале.
Отличие от контроля усилилось в результате введения вместо крахмала композиции с АГ (таблица 2). Содержание лейкоцитов в крови было достоверно выше после введения софилара, чем после введения ДКВ в крахмале, что показывает преимущества заявленной композиции. Показатели клеточности костного мозга для софилара также были выше, хотя эти различия были статистически недостоверными. Вместе с тем, сниженное до 0,05% содержание ДКВ в смеси с АГ, хотя и оказывало радиопротекторное действие, но его результаты статистически недостоверно отличались от контрольной группы животных.
Таким образом, представленные результаты показали, что содержание ДКВ от 1 до 3 об.% в смеси с АГ оказывает наиболее выраженное радиопротекторное действие. Не исключено, что такой дополнительный эффект может быть обусловлен не только взаимным усилением иммуномодулирующего действия компонентов, но также пролонгацией радиопротекторного эффекта ДКВ за счет особенностей высокомолекулярной структуры полисахарида.
Следует также отметить повышение биодоступности ДКВ в предложенной композиции, а также тот факт, что в приведенных результатах не отражено возможное усиление антибактериального, противогрибкового, противовирусного действия, также вносящее свой вклад в защиту поврежденных при облучении кожных покровов. Не выявлено токсического или какого-либо нежелательного побочного действия композиции при ее внутрижелудочном введении крысам в дозе 200 мг/кг.
Увеличение содержания ДКВ в композиции до 5% не приводило к дополнительному усилению радиозащитного эффекта, а потому не является целесообразным.
Данный препарат также можно использовать и по традиционному для ДВК назначению: в качестве источника витамина Р, антиоксиданта, гепатопротектора, иммуномодулятора, противоопухолевого препарата и как пробиотическое волокно.
Другим аспектом настоящего изобретения является способ получения указанной композиции «софилар»
Известны способы получения композиций АГ с примесями биофлавоноидов. Так, RU 2040268 описывает получение АГ из опилок древесины лиственницы путем экстракции водой при обычной (комнатной) температуре, фильтрования, упаривания водного экстракта, очищения от фенольных примесей добавлением ацетона, декантацию надосадочной жидкости, промывания полученного осадка АГ ацетоном и высушивания. Полученный продукт содержал 2,4% примесей в виде смеси ДКВ с дигидрокемпферолом.
Согласно RU 2143437 смесь, содержащую до 98-99% АГ с примесями в виде 0,01% смеси ДВК с другими биофлавоноидами, можно получать из отходов производства ДКВ путем обработки остывшего после извлечения ДКВ водного экстракта растворами коагулянта и флокулянта, осаждения этиловьм спиртом, промывания осадка этиловым спиртом и высушивания.
Вместо осаждения известно использование для выделения АГ из раствора полиамидного сорбента, как описано в RU 2002756 (способ не нашел распространения ввиду сложности и высокой стоимости работы с сорбентами в промышленных масштабах); или ионообменной колонки согласно ЕР 138784 (способ приводит к большим потерям АГ, а усложненная технология делает его неоправданно дорогим).
Предложенный в настоящем изобретении способ касается, как и RU 2143437, использования отходов производства ДКВ, отработанных опилок лиственницы. Однако целью способа является получение не АГ повышенной чистоты, а препарата с определенным содержанием ДКВ, обладающего радиопротекторным действием. В связи с поставленной целью способ отличает использование в качестве экстрагента вместо ацетона или ацетонитрила только этанола для того, чтобы остатки растворителя в готовом продукте не приводили к нежелательным побочным эффектам или проявлениям токсичности.
Кроме того, предложенный способ обеспечивает отсутствие в софиларе нарингенина и кверцетина, которые в α-форме ядовиты. Отсутствуют в нем и другие биофлавоноиды, снижающие, как показано выше, его эффективность по заявленному назначению.
Способ заключается в следующем: проводили выделение ДВК из древесины лиственницы экстракцией этиловым спиртом при комнатной температуре в периодической системе; полученный экстракт упаривали; поддерживая температуру 60°С на протяжении получаса из экстракта осаждали смолу; помещали маточный раствор в холодильную камеру для кристаллизации; выпавшие в осадок ДКВ и другие биофлавоноиды отделяли фильтрованием под вакуумом; экстрагировали отработанные опилки водой при температуре 80°С (строго) в периодической системе; полученный экстракт в зависимости от того, какое содержание ДКВ хотели в нем получить либо сушили, либо дополнительно экстрагировали этиловым спиртом, а осажденный продукт фильтровали и сушили. Для иллюстрации способа приводятся следующие примеры.
Пример 2.
Способ получения композиции с содержанием ДКВ 2-3 об.%
Опилки древесины лиственницы обрабатывали для выделения ДКВ и других био-флавоноидов как описано выше; далее 130 кг отработанных опилок заливали 350 л воды при температуре 80°С (строго) и экстрагировали 2 часа в периодической системе; получали 300 л экстракта, который сушили на распылительной сушке. Выход готового продукта (97-98 об.% арабиногалактана и 2-3 об.% дигидрокверцетина) составлял 16 кг.
Пример 3.
Способ получения композиции с содержанием ДКВ 1-2 об.%
Опилки древесины лиственницы обрабатывали для выделения ДКВ и других био-флавоноидов как описано выше; далее 130 кг отработанных опилок заливали 350 л воды при температуре 80°С (строго) и экстрагировали 2 часа в периодической системе; получали 300 л экстракта, который упаривали до 32 л; добавляли 20 л этилового спирта, экстрагировали в течение 30 мин; осажденную субстанцию фильтровали, сушили под вакуумом. Выход готового продукта (98-99 об.% арабиногалактана и 1-2 об.% дигидрокверцетина) составлял 16 кг.
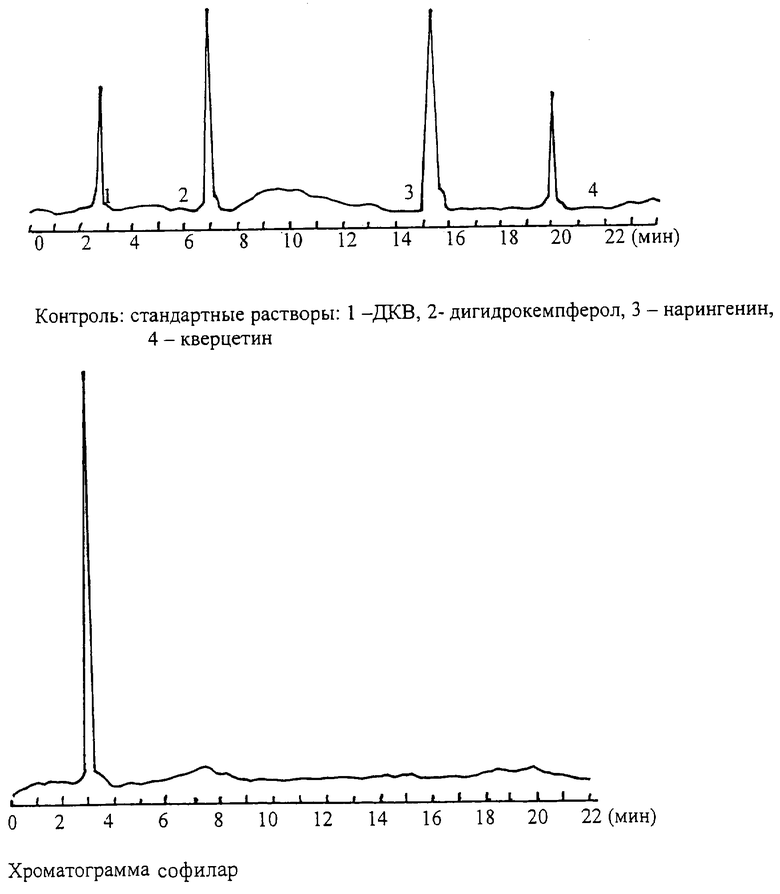
Чистоту выделения ДКВ в продукте, полученном заявленным способом, контролировали традиционным методом с использованием ВЭЖХ (Воскобойникова И.В. и др. Фармация, 1992, №6 с.74-75). Анализ проводили на хроматографе SP-7850 с УФ-детектором при длине волны 290 нм с использованием колонки Lichrosorb 150×4,6 мм; в качестве подвижной фазы использовали смесь ацетонитрил - 2%-ная уксусная кислота, 30:70, чувствительность метода - 0,1 мкг/мл.
На приведенной хроматограмме (см. чертеж) видно, что время выхода пика ДКВ составляло 3 мин; отсутствие других пиков подтверждает факт отсутствия в софиларе других флавоноидов: дигидрокемпферола (время выхода пика должно было составлять 7 мин), нарингенина (время выхода пика должно было составлять 15,3 мин) и кверцитина (время выхода пика должно было составлять 20 мин).
Пример 4. Таблетки
Продукт, полученный в примере №3, тонко измельчают и затем на роторной таблетирующей машине прессуют таблетки по 0,2 г.
Пример 5. Таблетки, мг:
К продукту, полученному в примере №3, добавляют микрокристаллическую целлюлозу, кросповидон, стеарат магния, лактозу в указанном соотношении и 1 мг диоксида кремния, смешивают в диффузионном смесителе, просеивают через мельницу с ситами. К образовавшейся смеси добавляют оставшуюся часть диоксида кремния, и готовят окончательную смесь в диффузионном смесителе, затем прессуют в таблетки на стандартном оборудовании.
Пример 6. Капсулы, мг:
Продукт примера №2 тонко измельчают и смешивают с также измельченными предварительно смешанными в диффузионном смесителе стеаратом магния и лактозой. Смесь просеивают через мельницу с ситами. Ингредиенты смешивают около 10 мин и помещают в сухие желатиновые капсулы.
** означает Р< 0,05 по отношению к соответствующему показателю дигидрокверцетина 98%-й чистоты в крахмале
Изобретение относится к области фармацевтики и касается композиции с радиопротекторным действием и способу ее получения. Изобретение заключается в том, что используют отходы производства биофлавоноидов из древесины лиственницы для получения с радиопротекторным действием и содержит 1-3 об.% 5 дигидрокверцетина и 99-97 об.% арабиногалактана. Изобретение касается способа получения. Изобретение обеспечивает более сильным радиопротекторное действие чем действие дигидрокверцетина при самостоятельном применении, а композиция не требует введения иных дополнительных эксципиентов и в заявленном соотношении ингредиентов является стабильной, пластичной, позволяет таблетировать готовую лекарственную форму с повышенной биодоступностью. 2 н. и 3 з.п. ф-лы, 1 ил., 2 табл.
| СПОСОБ ПОЛУЧЕНИЯ АРАБИНОГАЛАКТАНА | 1994 |
|
RU2040268C1 |
| ИЛЬЮЧЕНОК Т.Ю | |||
| и др | |||
| Фармакология и токсикология | |||
| - М., 1975, №5, с.607-612 | |||
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОЧИСТОГО АРАБИНОГАЛАКТАНА | 1998 |
|
RU2143437C1 |
| СПОСОБ ПЕРЕРАБОТКИ ДРЕВЕСИНЫ ЛИСТВЕННИЦЫ И СПОСОБ ВЫДЕЛЕНИЯ НАТИВНЫХ БИОФЛАВОНОИДОВ, ПОЛУЧЕННЫХ В ПРОЦЕССЕ ПЕРЕРАБОТКИ | 2000 |
|
RU2165416C1 |
Авторы
Даты
2006-05-27—Публикация
2003-07-09—Подача