Изобретение относится к медицине и химико-фармацевтической промышленности и касается создания нового средства для комплексной терапии заболеваний.
Современное представление о протекании практически любой нозологической формы заболевания в организме человека с учетом его исходного состояния, наличия сопутствующей патологии, диктует необходимость проведения комплексной терапии.
В то же время увеличение числа назначаемых препаратов в свою очередь может приводить к нежелательным последствиям в плане побочных или токсических осложнений. В этой связи весьма актуальной задачей является создание препаратов широкого спектра действия. Биофлавоноиды (Р-витамины), например кверцетин и рутин, давно используются при лечении ишемической болезни сердца, атеросклероза, капилляротоксикозов, легочных заболеваний, что обусловлено прежде всего их влиянием на ключевые звенья развития ряда патологических процессов, связанных с ускорением свободнорадикального окисления липидов мембран и нарушением проницаемости стенки капилляров.
Перспективным в этом направлении является дигидрокверцетин (3,3',4', 5,7-пентагидроксифлаванон), получаемый из древесины лиственницы.
Известно, что дигидрокверцетин обладает широким спектром фармакологических свойств капилляропротекторным и антиоксидантным действием, сочетающимся с гастро- и гепатопротекторным, гиполипидемическим и диуретическим действием.
Дигидрокверцетин является ближайшим аналогом заявляемого средства широкого спектра действия [1]
Известен ряд способов получения дигидрокверцетина, например, из измельченной древесины лиственницы путем обработки водой, экстрагирования органическим растворителем (вода-ацетон, 1:4) непосредственно после обработки сырья водой, упаривания экстракта и кристаллизации из горячей воды. Различие в растворимости флавоноидных соединений в воде приводит к тому, что в процессе кристаллизации из горячей воды получается продукт, обогащенный на 95-97% дигидрокверцетином [2]
Наиболее близким к предлагаемому способу получения препарата на основе дигидрокверцетина является способ, основанный на экстракции измельченной древесины лиственницы водой при нагревании (98-100oС), охлаждении, фильтровании и упаривании полученного водного экстракта, смешивании его с полиамидным сорбентом, высушивании и экстрагировании целевого продукта этилацетатом с последующей кристаллизацией из горячей воды. Получаемый продукт содержит 97,2% дигидрокверцетина и 2,8% дигидрокемпферола [3]
В то же время работы по изучению биофлавоноидных соединений показали, что стремление повысить степень чистоты дигидрокверцетина и его выход недостаточно оправдано.
Сопровождающие дигидрокверцетин два других биофлавоноидных соединения, дигидрокемпферол и нарингенин, являются его биогенетическими предшественниками и также обладают биологической активностью.
Например, нарингенин проявляет эффективное Р-витаминное и спазмолитическое действие (Физиологически активные вещества. Киев: Наукова Думка, 1966, с.3-9).
Дигидрокемпферол и нарингенин, в свою очередь наряду с дигидрокверцетином обладают также антирадикальной эффективностью, что является предпосылкой для их использования в составе лекарственного препарата (Антирадикальная эффективность некоторых природных фенольных соединений. Журнал общей химии, 1972, т.ХLII, вып. 6, с.1414-1420).
Новый отечественный препарат, относящийся к группе витамина Р и названный Диквертином (ВФС 42-2397-94 от 29.07.96), представляет собой биофлавоноидный продукт, получаемый из измельченной древесины лиственницы и состоящий из трех флавононовых соединений дигидрокверцетина (3,3',4',5,7-пентагидроксифлаванона), дигидрокемпферола (3,4',5,7-тетрагидроксифлаванона) и нарингенина (3,4',7-тригидроксифлаванона). При этом содержание дигидрокверцетина составляет не менее 90% а содержание дигидрокемпферола и нарингенина в сумме не более 10% а именно дигидрокверцетин 90-92% дигидрокемпферол и нарингенин 8-10% причем нарингенина не более 2%
Препарат Диквертин представляет собой мелкокристаллический или аморфный порошок от светло-желтого до желтого цвета, без запаха, слегка горьковатого вкуса, растворимый в 96%-ном спирте, очень мало растворимый в воде, практически не растворимый в хлороформе.
На хроматограмме ВЭЖХ (фиг.1) содержатся пик дигидрокверцетина, величина соотношения времени выхода которого с временем выхода пика на хроматограмме ГСО дигидрокверцетина (фиг.2) равна 1,00±0,15, а также пик дигидрокемпферола и пик нарингенина с величинами соотношения времен удерживания соответственно равными 1,40±0,15 и 1,94±0,15.
Клиническое изучение Диквертина, представляющего собой композицию трех биофлавоноидов, подтвердило, что препарат обладает антиоксидантными свойствами, капилляропротекторной и противоотечной активностью. Диквертин активирует процессы регенерации слизистой желудка, оказывает гепатопротекторное (антитоксическое) действие, а также нерезко выраженное спазмолитическое и иммуностимулирующее действие, проявляет противовоспалительный и антигистаминный эффект.
Такой широкий спектр действия обусловлен как известными свойствами дигидрокверцетина, так и наличием в препарате двух других биофлавоноидов, проявляющих, по-видимому, синергетическую активность.
Диквертин может быть с успехом использован для лечения легочных и сердечных заболеваний как средство, обладающее выраженной антиоксидантной и капилляропротекторной активностью в сочетании со спазмолитическим и иммуностимулирующим действием.
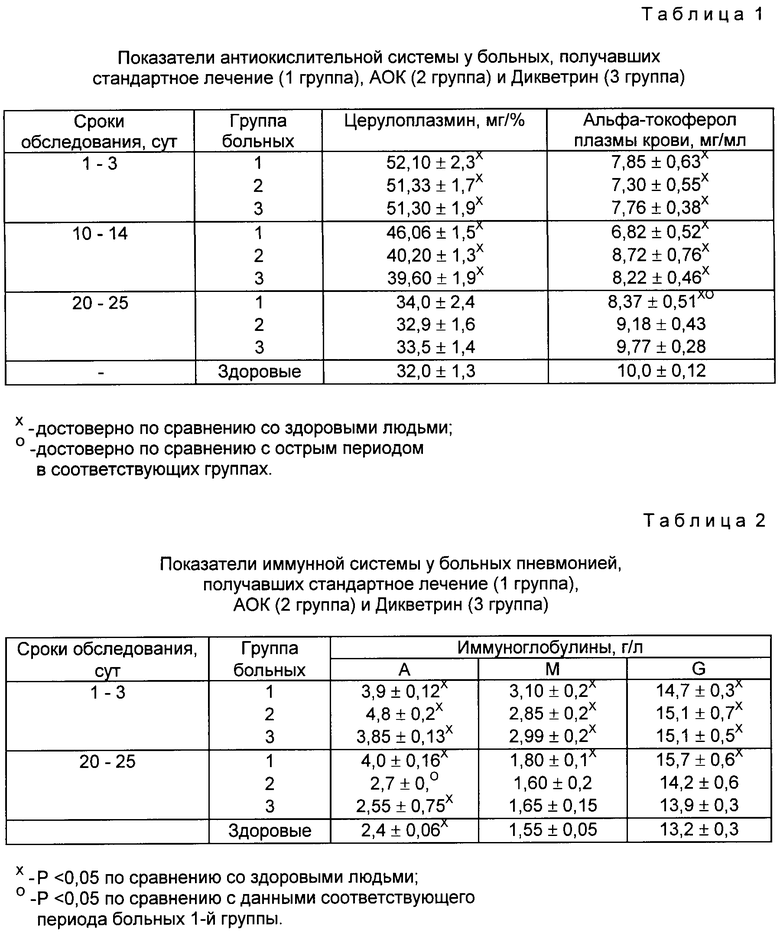
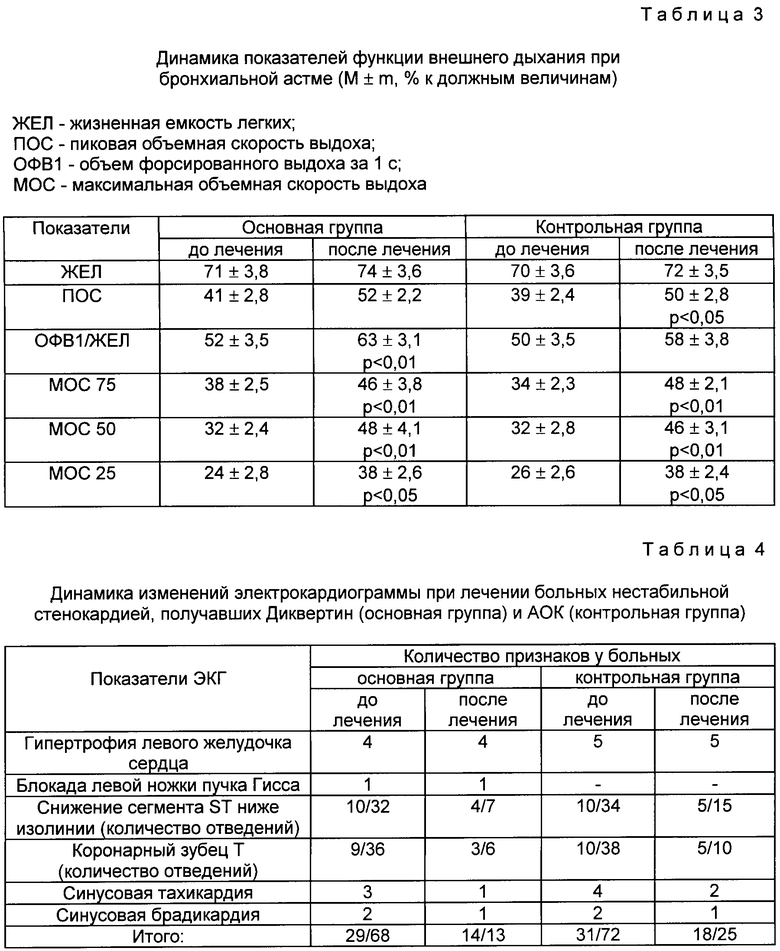
В табл. 1-4 представлены сведения, подтверждающие эффективность препарата. В табл. 1, 2 и 4 сведения приведены в сравнении с антиокислительным комплексом (АОК), включающим альфа-токоферол в комбинации с тиосульфатом натрия.
Способ получения композиции биофлавоноидов указанного состава заключается в следующем. Опилки древесины лиственницы сибирской или даурской заливают кипящей водой, перемешивают, добавляют ацетон, концентрированную хлороводородную кислоту до рН 2, выдерживают при 40oС, отфильтровывают. Опилки промывают ацетоном, ацетоновый слив объединяют с экстрактом и упаривают. Смолообразную массу перемешивают с нагретым до 50 С 96%-ным этиловым спиртом или его водным раствором, фильтруют, кристаллизуют и сушат.
Предлагаемый способ получения диквертина обладает следующими достоинствами. Замена водного экстрагента на подкисленный водно-ацетоновый повышает выход конечного продукта. Использование водно-ацетоновой экстракции позволяет понизить температуру экстракции с 98-100 до 40oС, что практически исключает окисление. Исключение стадии очистки полиамидным сорбентом позволяет упростить процесс.
Пример 1. К 100 г опилок древесины лиственницы (влажность 20%) приливают 75 мл кипящей воды, перемешивают в течение 5 мин, приливают 390 мл ацетона, добавляют по каплям концентрированную хлороводородную кислоту до рН 2 и выдерживают в течение 20 мин при 40oС. Водно-ацетоновый экстракт отфильтровывают, опилки промывают 20 мл ацетона, ацетоновый слив объединяют с экстрактом и упаривают на роторном испарителе. К полученной смолообразной массе приливают 10 мл нагретого до 50oС 96%-ного этилового спирта, перемешивают и фильтруют. В результате кристаллизации получают 2,31 г диквертина, содержание в котором дигидрокверцетина составляет 2,12 г, дигидрокемпферола 0,16 г, нарингенина 0,03 г, то есть соответственно 91,70; 7,0 и 1,35% от диквертина. Выход диквертина равен 96,7% от суммы содержащихся в древесине трех вышеназванных биофлавоноидов и 2,89% от массы абс.сухой древесины (а.с.д.).
Пример 2. Из 100 г опилок древесины лиственницы (влажность 20%), обработанных кипящей водой и проэкстрагированных в условиях примера 1, получают смолообразную массу, приливают к ней 10 мл 50 об.-го водного раствора этилового спирта, перемешивают и фильтруют. В результате кристаллизации получают 2,32 г диквертина, содержание в котором дигидрокверцетина составляет 2,11 г, дигидрокемпферола 0,17, нарингенина 0,04 г, то есть соответственно 90,80, 7,35 и 1,85% от диквертина. Выход диквертина равен 97,1% от суммы содержащихся в древесине трех вышеназванных биофлавоноидов и 2,9% от массы а.с.д.
Как видно из примера 1, замена водной экстракции водноацетоновой в кислой среде и использование кристаллизации из этилового спирта взамен очистки на полиамидном сорбенте позволяет упростить процесс и достичь некоторого увеличения выхода конечного продукта.
На основании примера 2 видно, что замена на стадии кристаллизации этилового спирта 96% на его 50%-ный водный раствор не снижает выхода диквертина.
Получаемый в условиях прототипа продукт содержит 97,2% дигидрокверцетина и 2,8% дигидрокемпферола при отсутствии нарингенина, чем он существенно отличается от диквертина.
Количественный анализ содержания флавоноидов в конечном продукте проводился методом высокоэффективной жидкостной хроматографии. Колонка 250 х 4,6 мм, сорбент Lichrosorb 10 RP-2, подвижная фаза ацетонитрил 2% уксусная кислота (3:7), аналитическая длина волны 290 нм. Относительная ошибка единичного определения при уровне значимости 95% не превышала 3%
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫДЕЛЕНИЯ ДИГИДРОКВЕРЦЕТИНА | 1997 |
|
RU2114631C1 |
| СПОСОБ ПОЛУЧЕНИЯ АРАБИНОГАЛАКТАНА | 1994 |
|
RU2040268C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИГИДРОКВЕРЦЕТИНА | 1996 |
|
RU2091076C1 |
| СПОСОБ КОМПЛЕКСНОЙ ТЕРАПИИ ЗАБОЛЕВАНИЙ | 1996 |
|
RU2090205C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИГИДРОКВЕРЦЕТИНА | 1994 |
|
RU2038094C1 |
| СПОСОБ ПРОИЗВОДСТВА МАССЫ ДЛЯ САХАРИСТЫХ КОНДИТЕРСКИХ ИЗДЕЛИЙ НА ЖИРОВОЙ ОСНОВЕ | 1996 |
|
RU2097977C1 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ ДРЕВЕСИНЫ ЛИСТВЕННИЦЫ | 2003 |
|
RU2261881C1 |
| СОСТАВ БИОФЛАВОНОИДНОГО КОМПЛЕКСА СИБЕЛ ДЛЯ ПИЩЕВЫХ И ПАРФЮМЕРНЫХ ИЗДЕЛИЙ И СПОСОБ ПОЛУЧЕНИЯ БИОФЛАВОНОИДНОГО КОМПЛЕКСА СИБЕЛ ДЛЯ ПИЩЕВЫХ И ПАРФЮМЕРНЫХ ИЗДЕЛИЙ | 2001 |
|
RU2186097C1 |
| СОСТАВ БИОФЛАВОНОИДНОГО КОМПЛЕКСА СИБЛАРЕКС ДЛЯ БИОЛОГИЧЕСКИ АКТИВНЫХ ДОБАВОК, МЕДИЦИНСКИХ И ХИМИКО-ФАРМАЦЕВТИЧЕСКИХ ИЗДЕЛИЙ И СПОСОБ ПОЛУЧЕНИЯ БИОФЛАВОНОИДНОГО КОМПЛЕКСА СИБЛАРЕКС ДЛЯ БИОЛОГИЧЕСКИ АКТИВНЫХ ДОБАВОК, МЕДИЦИНСКИХ И ХИМИКО-ФАРМАЦЕВТИЧЕСКИХ ИЗДЕЛИЙ | 2001 |
|
RU2183966C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА "БИОСКАН-С" И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1999 |
|
RU2154967C1 |

Изобретение относится к химико-фармацевтической промышленности и медицине, касается нового биофлавоноидного препарата и способа его получения. Сущность изобретения: диквертин представляет собой сумму биофлавоноидов при следующем соотношении компонентов, %: дигидрокверцетин 90-92, дигидрокемпферол и нарингенин 8-10; причем нарингенина не более 2%. Диквертин имеет широкий спектр действия, регулирует метаболические процессы, может применяться в комплексной терапии заболеваний. Диквертин получают путем экстракции опилок древесины лиственницы водно-ацетоновым экстрагентом в кислой среде непосредственно после обработки сырья кипящей водой, целевой продукт кристаллизуют из спирта или водно-спиртового раствора. 2 с.п.ф-лы, 4 табл. 2 ил.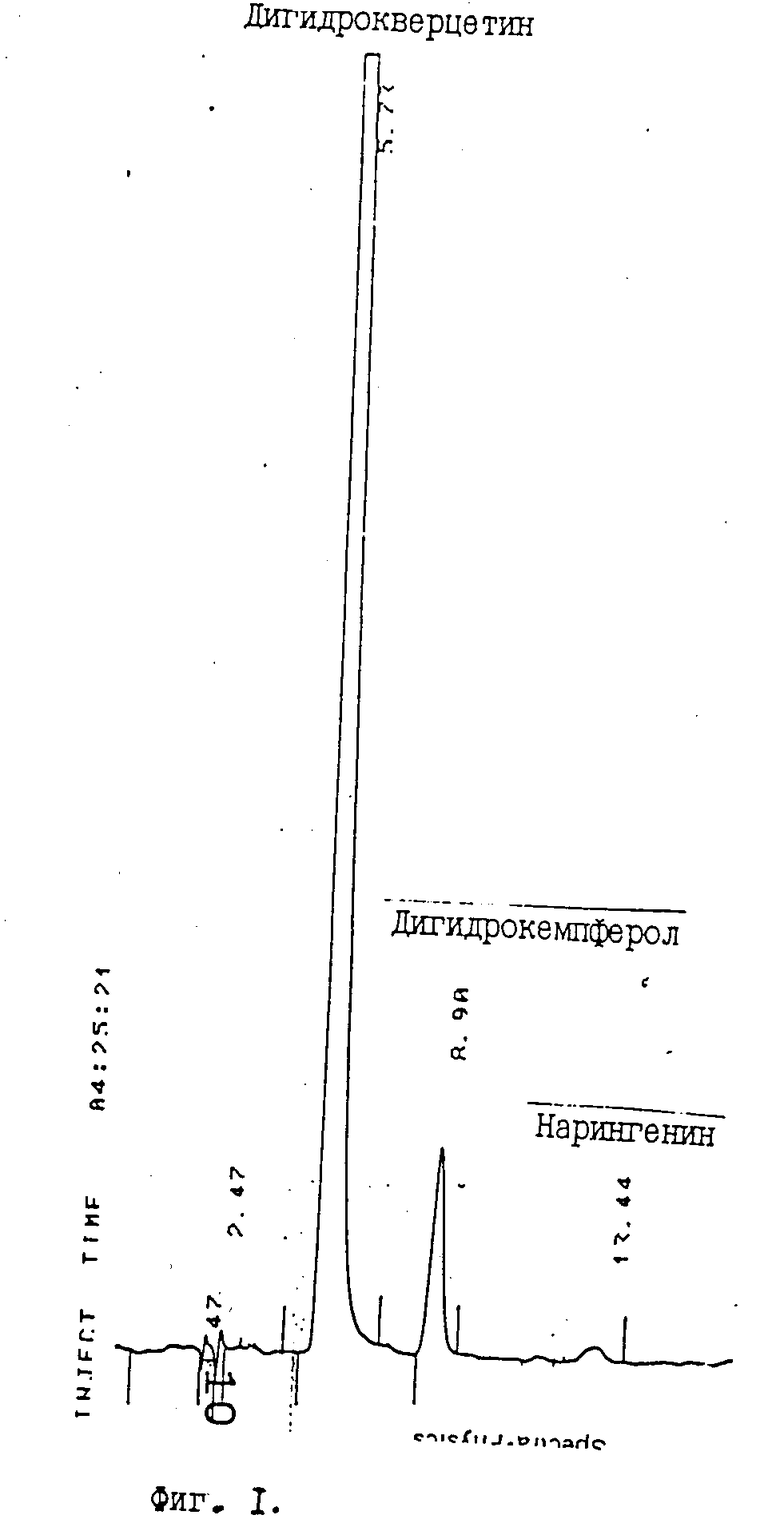
2. Способ получения средства для комплексной терапии заболеваний, заключающийся в экстракции опилок древесины лиственницы, фильтровании, упаривании экстракта, кристаллизации целевого продукта, его фильтровании и сушке, отличающийся тем, что экстракцию проводят водно-ацетоновым экстрагентом в кислой среде непосредственно после обработки сырья кипящей водой и кристаллизуют целевой продукт из спирта или водно-спиртового раствора.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| АНТИОКСИДАНТНОЕ, КАПИЛЛЯРОПРОТЕКТОРНОЕ, ПРОТИВОВОСПАЛИТЕЛЬНОЕ И АНТИГИСТАМИННОЕ СРЕДСТВО | 1992 |
|
RU2014841C1 |
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИГИДРОКВЕРЦЕТИНА | 1994 |
|
RU2038094C1 |
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Патент РФ N 2000797, кл | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1997-08-27—Публикация
1996-12-02—Подача