Изобретение относится к аналитической химии и может быть использовано в химической, микробиологической, пищевой промышленности, а также на предприятиях агропромышленного комплекса.
Известен способ определения лизина в водных растворах с применением анионита АВ-17-8 с активными группами [N(CH3)3]+. В этом способе определение лизина проводят при рН 11,5 (при этом значении рН лизин существует в виде аниона в растворе) [В.Д.Копылова, А.Н.Амелин, Ю.С.Перегудов и др. Взаимодействие полиэлектролитов с аминокислотами // Сорбционные и хроматографические процессы. - 2005. - Т.5, Вып.2. - С.260-264].
Наиболее близким по технической сущности и достигаемому эффекту является способ определения глицина в водных растворах методом капиллярного электрофореза [В.Ф.Селеменев, А.В.Калач, Н.Ю.Страшилина. Исследование аминокислотного состава плодов Cornus mas и Mespilus germanica методом капиллярного электрофореза // Сорбционные и хроматографические процессы. - 2004. - Т.4, Вып.3. - С.353-358]. В данном способе для определения аминокислот (в том числе и глицина) используют метод капиллярного электрофореза. Предварительно на пробу, содержащую аминокислоты, действуют раствором Na2CO3 и фенилизоцианата (ФТК) для дериватизации. Затем полученную смесь выпаривают при температуре 30-35°С, а сухой остаток растворяют в 500 мм3 дистиллированной воды. Полученные таким образом ФТК-производные аминокислот помещают в пробирку типа «Eppen-dorf», центрифугируют (n=6000 об/мин) и помещают во входной карусели автосемплера прибора «Капель-105». В качестве электролита применяют фосфатный буферный раствор (рН 9,13), ввод пробы осуществляют при давлении Р=30 мбар, длина волны λ=254 нм, температура анализа 30°С. В этих условиях продолжительность анализа составляет 15-20 мин. Таким способом возможно определение следующих аминокислот: глицин, серин, триптофан, пролин, валин, метионин, лейцин, изолейцин, гистидин, фенилаланин, тирозин, лизин, аргинин.
Недостатком прототипа является сложное аппаратурное оформление анализа, недостаточная экспрессность и значительный расход реагентов для определения глицина в водных растворах.
Технической задачей изобретения является упрощение аппаратурного оформления анализа, уменьшение расхода реактивов, а также повышение экспрессности определения глицина в водных растворах.
Поставленная задача достигается тем, что в способе определения глицина в водных растворах, включающем ввод анализируемой пробы в ячейку детектирования и регистрацию аналитического сигнала, согласно изобретению в качестве ячейки детектирования используют пьезорезонансный сенсор, регистрацию аналитического сигнала осуществляют при элюировании анализируемой пробы, содержащей глицин в диапазоне концентраций 1·10-5-1·10-1 моль/дм3, при температуре 20±2°С и скорости элюента 30 см3/мин, в качестве элюента применяют смесь этилового спирта с водой в соотношении 1:1, измеряют резонансную частоту сенсора и вычисляют относительный сдвиг частоты по разнице частот колебаний сенсора в элюенте и после анализа, концентрацию глицина оценивают на основании градуировочного графика зависимости относительного сдвига частоты от концентрации глицина.
Технический результат заключается в упрощении аппаратурного оформления анализа, уменьшении расхода реактивов для анализа и повышении экспрессности определений.
Способ осуществляется следующим образом.
1. Подготовка пьезосенсора к работе
При выполнении эксперимента использовали кварцевые резонаторы АТ-среза с серебряными электродами диаметром 5 мм и толщиной 0,3 мм с номинальной резонансной частотой колебаний 8-10 МГц.
Снижение рабочей частоты колебаний пьезорезонансных сенсоров рассчитывали по уравнению Зауэрбрея [Sauerbrey G.G. Messung von plattenschwingungen sehr kleiner amplitude dutch lichtstrom-modulation // Z. Phys. - 1964. - Bd.178. - S.457-471]:
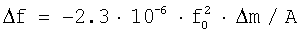 ,
,
где Δm - масса модификатора, г; f0 - резонансная частота пьезосенсора, МГц; Δf - изменение частоты резонатора, Гц; А - площадь поверхности модификатора, см2.
Условия элюирования: температура анализа 20±2°С; скорость элюента 30 см3/мин; время между последовательным инжектированием пробы t=90 с.
2. Градуировка пьезорезонансного сенсора. Предварительно рассчитанную массу навески глицина (необходимую для приготовления стандартного раствора глицина с молярной концентрацией 1,0·10-1 моль/дм3) взвешивают на аналитических весах, количественно переносят в мерную колбу вместимостью 100 см3, растворяют в дистиллированной воде и доводят до метки. Таким образом, получают стандартный раствор глицина с концентрацией 1,0·10-1 моль/дм3. Из этого стандартного раствора методом последовательного разбавления готовят серию растворов глицина с концентрациями 5,0·10-2; 1,0·10-2; 5,0·10-3; 1,0·10-3; 1,0·10-4; 1,0·10-5 моль/дм3.
В 6 химических стаканов пипеткой отбирают по 10,00 см3 стандартных растворов глицина. Затем поочередно (по 2 см3) каждый раствор шприцем инжектируют и элюируют. В качестве элюента применяют смесь этилового спирта с водой в соотношении 1:1. Перед началом измерений следует измерить сигнал пьезорезонансного сенсора в элюенте Δf2.
Для фиксирования откликов сенсора после введения каждой пробы измеряют резонансную частоту сенсора и вычисляют относительный сдвиг частоты Δfa по уравнению:
Δfa=Δf1-Δf2,
где Δf1 и Δf2 - частоты колебаний сенсора до и после анализа, Гц.
Измерения выполняют, переходя от разбавленных растворов к более концентрированным. По полученным результатам строят градуировочный график, откладывая по оси ординат Δfa, Гц, по оси абсцисс - соответствующие значения концентраций глицина.
Порядок проведения определений. После установления стабильного нулевого сигнала пьезорезонансного сенсора в канал с элюентом шприцем вводят анализируемый раствор объем пробы 1,0-2,0 см3.
Получают зависимость Δfa=f(t), которая описывает зависимость аналитического сигнала пьезорезонансного сенсора от времени.
Относительное содержание (массовую долю) аминокислоты в пробе находят по градуировочному графику.
Примеры осуществления способа
Пример 1. После помещения пьезорезонансного сенсора в ячейку детектирования и установления стабильного нулевого сигнала в канал с элюентом шприцем вводят анализируемый раствор (объем пробы 0,5 см3), содержащий глицин в концентрации 5,0·10-6 моль/дм3. Получают зависимость Δfa=f(t), которая описывает зависимость аналитического сигнала пьезорезонансного сенсора от времени. Способ неосуществим, так как сигнал сенсора находится на уровне шумов и проведение анализа невозможно. Результаты определений приведены в табл.1.
Пример 2. Подготовку сенсора проводили по аналогии с примером 1. Концентрация глицина в пробе 1,0·10-5 моль/дм3; объем пробы 1,0 см3. Способ осуществим. Результаты определения приведены в табл.1.
Пример 3. Подготовку сенсора проводили по аналогии с примером 1. Концентрация глицина в пробе 1,0·10-5 моль/дм3; объем пробы 2,0 см3. Способ осуществим. Результаты определения приведены в табл.1.
Пример 4. Подготовку сенсора проводили по аналогии с примером 1. Концентрация глицина в пробе 5,0·10-5 моль/дм3; объем пробы 2,0 см3. Способ осуществим. Результаты определения приведены в табл.1.
Пример 5. Подготовку сенсора проводили по аналогии с примером 1. Концентрация глицина в пробе 1,0·10-3 моль/дм3; объем пробы 2,0 см3. Способ осуществим. Результаты определения приведены в табл.1.
Пример 6. Подготовку сенсора проводили по аналогии с примером 1. Концентрация глицина в пробе 1,0·10-2 моль/дм3; объем пробы 2,0 см3. Способ осуществим. Результаты определения приведены в табл.1.
Пример 7. Подготовку сенсора проводили по аналогии с примером 1. Концентрация глицина в пробе 5,0·10-2 моль/дм3; объем пробы 2,0 см3. Способ осуществим. Результаты определения приведены в табл.1.
Пример 8. Подготовку сенсора проводили по аналогии с примером 1. Концентрация глицина в пробе 5,0·10-2 моль/дм3; объем пробы 3,0 см3. Способ неосуществим, так как наблюдается срыв генераций колебаний сенсора. Результаты определения приведены в табл.1.
Пример 9. Подготовку сенсора проводили по аналогии с примером 1. Концентрация глицина в пробе 1,0·10-2 моль/дм3; объем пробы 1,0 см3. Способ осуществим. Результаты определения приведены в табл.1.
Результаты сравнения характеристик предлагаемого способа с прототипом представлены в табл.2.
Из приведенных примеров видно, что при концентрациях менее 1,0·10-5 (пример 1) и более 5,0·10-2 моль/дм3 (пример 9) определение глицина в водных растворах невозможно. В первом случае по причине малой чувствительности сенсора, во втором - вследствие нестабильности показаний и срыва колебаний сенсора. Увеличение объема вводимой пробы свыше 2,0 см3 приводит также к срыву колебаний сенсора (пример 8).
Таким образом, предлагаемый способ определения глицина в водных растворах по сравнению с прототипом позволяет:
1) упростить аппаратурное оформление определений;
2) уменьшить расход реактивов при проведении анализа;
2) повысить экспрессность анализа.
Примеры осуществления способа
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕКСАНА В ВОЗДУХЕ | 2002 |
|
RU2216016C1 |
| СПОСОБ ОЦЕНКИ КАЧЕСТВА АЗОТСОДЕРЖАЩИХ МИНЕРАЛЬНЫХ УДОБРЕНИЙ С ИСПОЛЬЗОВАНИЕМ ПЬЕЗОСЕНСОРОВ | 2013 |
|
RU2543687C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФЕНОЛА В ВОЗДУХЕ | 2010 |
|
RU2441231C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НИТРОМЕТАНА В ВОЗДУХЕ | 2002 |
|
RU2236672C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АЦЕТОНИТРИЛА В ВОЗДУХЕ РАБОЧЕЙ ЗОНЫ | 2003 |
|
RU2237238C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПАРОВ МЕТИЛАЦЕТАТА В ПРИСУТСТВИИ БЕНЗИЛАЦЕТАТА В ВОЗДУХЕ РАБОЧЕЙ ЗОНЫ | 2009 |
|
RU2396555C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НОНАНА В ВОЗДУХЕ | 2003 |
|
RU2240554C1 |
| ЭКСПРЕССНЫЙ СПОСОБ ОЦЕНКИ БЕЗОПАСНОСТИ ИЗДЕЛИЙ ИЗ ФЕНОЛФОРМАЛЬДЕГИДНЫХ ПЛАСТМАСС | 2014 |
|
RU2555775C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНИЛИНА В ВОДНЫХ СРЕДАХ | 2007 |
|
RU2346274C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СУММАРНОГО СОДЕРЖАНИЯ НИТРОАЛКАНОВ C -C В ВОЗДУХЕ РАБОЧЕЙ ЗОНЫ | 2002 |
|
RU2211447C1 |
Изобретение относится к аналитической химии и может быть использовано в химической, микробиологической, пищевой промышленности, а также на предприятиях агропромышленного комплекса. В способе определения глицина в водных растворах, включающем ввод анализируемой пробы в ячейку детектирования и регистрацию аналитического сигнала, в качестве ячейки детектирования используют пьезорезонансный сенсор, регистрацию аналитического сигнала осуществляют при элюировании анализируемой пробы, содержащей глицин в диапазоне концентраций 1·10-5-1·10-1 моль/дм3, при температуре 20±2°С и скорости элюента 30 см3/мин, в качестве элюента применяют смесь этилового спирта с водой в соотношении 1:1, измеряют резонансную частоту сенсора и вычисляют относительный сдвиг частоты по разнице частот колебаний сенсора в элюенте и после анализа, концентрацию глицина оценивают на основании градуировочного графика зависимости относительного сдвига частоты от концентрации глицина. Технический результат заключается в упрощении аппаратурного оформления анализа, уменьшении расхода реактивов для анализа и повышении экспрессности определений. 2 табл.
Способ определения глицина в водных растворах, включающем ввод анализируемой пробы в ячейку детектирования и регистрацию аналитического сигнала, отличающийся тем, что в качестве ячейки детектирования используют пьезорезонансный сенсор, регистрацию аналитического сигнала осуществляют при элюировании анализируемой пробы, содержащей глицин в диапазоне концентраций 1·10-5-1·10-1 моль/дм3, при температуре 20±2°С и скорости элюента 30 см3/мин, в качестве элюента применяют смесь этилового спирта с водой в соотношении 1:1, измеряют резонансную частоту сенсора и вычисляют относительный сдвиг частоты по разнице частот колебаний сенсора в элюенте и после анализа, концентрацию глицина оценивают на основании градуировочного графика зависимости относительного сдвига частоты от концентрации глицина.
| СЕЛЕМЕНЕВ В.Ф., КАЛАЧ А.В., СТРАШИЛИНА Н.Ю | |||
| Сорбционные и хроматографические процессы | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Способ количественного определения @ -аминокислот | 1986 |
|
SU1361477A1 |
| СПОСОБ СПЕКТРОФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ АМИНОКИСЛОТ | 1991 |
|
RU2012869C1 |
| Способ определения трифенилхлорметана и его замещенных | 1983 |
|
SU1129519A1 |
| ПОЛЮДЕК-ФАБИНИ Р., БЕЙРИХ Т | |||
| Органический анализ | |||
| - Л.: Химия, 1981, с.168-177. | |||
Авторы
Даты
2006-08-20—Публикация
2005-07-11—Подача