Изобретение относится к области химии и биохимии, в частности к способу получения новых веществ модифицированных гликозаминогликанов, которые могут быть использованы в медицине, фармакологии.
Кислые гликозаминогликаны (ГАГ) из соединительных тканей животных и человека являются гетерополисахаридами линейного строения с различной молекулярной массой, степенью сульфатирования и содержат D-глюкуроновую или L-идуроновую кислоты. Наиболее представительными из класса ГАГ являются гиалуроновая кислота (несульфатированный ГАГ), хондроитинсульфаты и гепарин (наиболее сульфатированный ГАГ).
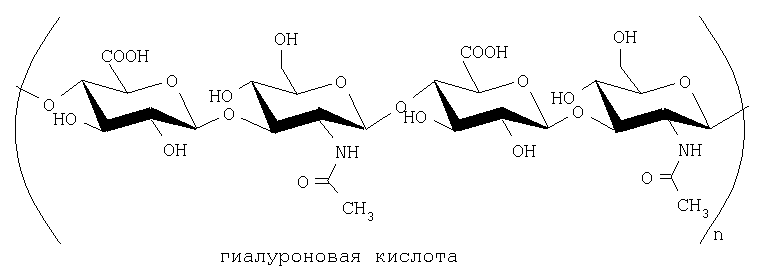
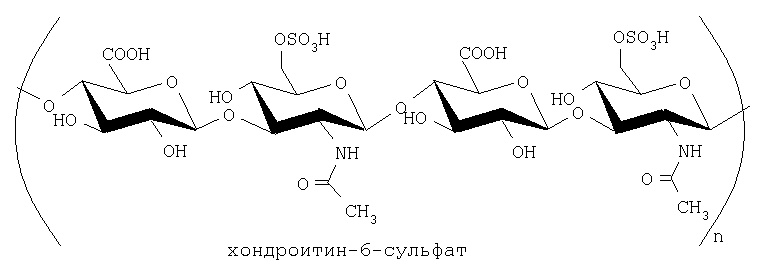
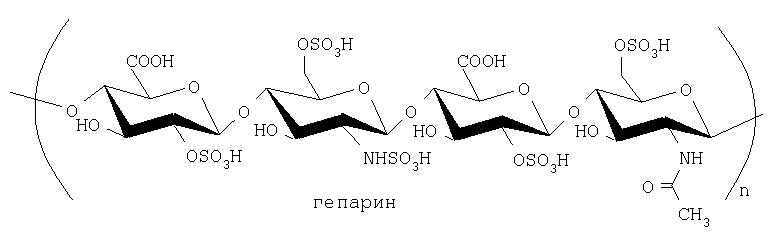
На основе ГАГ выпускаются следующие фармакопейные препараты.
Высокомолекулярная гиалуроновая кислота (M=106 Да) входит в состав вискоэластичных гелей «Provisk» (Швеция) и «Healon» Канада), применяющихся в офтальмохирургии при операциях экстракции катаракты, является действующим веществом в пленках «Seprafilm» для предупреждения спаечной болезни брюшины. Низкомолекулярной гиалуроновой кислотой пропитывают салфетки «Гиаплюс», предназначенных для лечения ожоговой болезни. Лекарственное средство «Куриозин» (в виде раствора и геля) для лечения трофических язв и угрей представляет собой цинковую соль гиалуроновой кислоты, а препарат «Цистистат» предназначается для восстановления поврежденной слизистой оболочки мочевого пузыря при интерстициальном цистите. Гиалуроновая кислота является составным компонентом косметических кремов и тоников для стимуляции роста волос. Запатентовано также применение гиалуроновой кислоты в лечении герпеса, псориаза, а также для изготовления суппозиториев различного назначения.
Хондроитинсульфаты из хрящей крупного рогатого скота входят в состав мази «Хондроксид» (для местного лечения остеоартритов), являются действующим веществом лекарственных препаратов «Хонсурид» (для ускорения репаративных процессов) и «Румалон» (для лечения суставов).
Гепарин известен в качестве антикоагулянтного и антитромботического средства и применяется внутривенно при операциях на сосудах. Кроме антикоагулянтных и антитромботических, у гепарина выявлены антибактериальные, антивирусные, противовоспалительные [Бычков С.М. Новые данные о гепарине. // Вопросы медицинской химии. 1981. №6. С.726-735] и противоопухолевые свойства [Lapierre F., Holme К., Lam L. Chemical modification of heparin that diminish anticoagulant but preserve its heparanase-inhibitory, angiostatic, anti-tumor and anti-metastatic properties. // Glycobiology. 1996. V.6(3). P.355-366]. Обнаружено также ингибирующее действие гепарина на рост и репликацию вируса иммунодефицита человека [Rider C.C. The potential for heparin and its derivatives in the therapy and prevention of HIV-1 infection. // Glycoconj. J. 1997. V.14(5). P.639-642]. Гепариновую мазь, в состав которой, кроме гепарина, входит анестезин (местноанестезирующее средство), применяют наружно при поверхностных тромбофлебитах и язвах конечностей, тромбозе геморроидальных вен, при этом уменьшаются воспалительные процессы [Машковский М.Д. Лекарственные средства. - Харьков: Торсинг, 1997. - Т.1, 2. - 590 С.].
Ковалентное связывание низкомолекулярных биологически активных соединений с полимерной матрицей способствует снижению токсичности лекарственных средств, увеличению длительности их действия, достигается более эффективная «доставка» лекарств к органам-мишеням. Например, в комбинации с гиалуроновой кислотой некоторые лекарственные субстанции образуют в эпидермисе как бы депо этих лекарств и высвобождаются из композиции медленнее, чем в отсутствие гиалуроновой кислоты [Vercruysse К.Р., Prestwich G.D. // Therapeutic Drug Carrier Systems. 1998. V.15(5). P.513-555].
Известно получение конъюгата гиалуроновой кислоты (ГК-СООН) с ибупрофеном, или бруфеном (d,1-2-(4-изобутилфенил)-пропионовой кислотой), лекарственным препаратом, обладающим противовоспалительной, анальгезирующей и жаропонижающей активностью. Синтез конъюгатов осуществляют в три стадии:
(1) при помощи 1-этил-3-[3-(диметиламино)пропил]карбодиимида (EDC) сначала получают конъюгаты (IIa-в) гиалуроновой кислоты с дигидразидами янтарной (Ia), адипиновой (Iб) и субаровой кислот (Iв) [конверсия карбоксильных групп составляет 30%(IIa), 56 (IIб) и 46 (IIв)];
(2) из ибупрофена и N-гидроксисукцинимида (NHS) в присутствии дициклогексилкарбодиимида (DCC) синтезируют N-гидроксисукцинимидный эфир ибупрофена (NHS-эфир ибупрофена);
(3) производные гиалуроновой кислоты (IIa-в) в смеси 0.1 н. NaHCO3 (pH 8.5) и ДМФА (1:2) реагируют с NHS-эфиром ибупрофена с образованием конъюгатов (IIIa-в). Таким образом удается ввести 24% мол. ибупрофена (по отношению к карбоксильным группам гиалуроновой кислоты).

Авторами предлагается одностадийный способ получения модифицированных ГАГ* (* Гиалуроновую кислоту и смесь хондроитинсульфатов получали из пупочных канатиков новорожденных, гепарин - из фармакопейного препарата для внутривенного введения.), обладающих анальгезирующими свойствами, путем взаимодействия ГАГ с 1-фенил-2,3-диметил-4-аминопиразоном-5(4-аминоантипирином) в водной среде при рН 4.7-4.8 в присутствии конденсирующего реагента - водорастворимого 1-этил-3-[3-(диметиламино)пропил]карбодиимида (EDC). Реакция протекает при комнатной температуре в течение 60 минут с высокой конверсией карбоксильных групп ГАГ (83-100%). Очистка продуктов от низкомолекулярных реагентов достигается двух- или трехкратным осаждением конъюгатов этиловым спиртом из водного раствора.
Спектры 1Н-ЯМР регистрировали для растворов в D2O на спектрометре Bruker АМХ-300 (рабочая частота для 1Н-ЯМР-300.13 МГц), в качестве внутреннего стандарта использовали натриевую соль 3-(триметилсилил)-1-пропансульфоновой кислоты. Контроль рН растворов проводили с помощью рН-метра «рН-340».
Водорастворимые конъюгаты ГАГ с 4-аминоантипирином получают следующим образом (схема 2, примеры 1-3).
Пример 1. К смеси 0.15 ммоль гиалуроновой кислоты (из пупочных канатиков) и 91.4 мг (0.45 ммоль) 4-аминоантипирина в 15 мл Н2О добавляют 0.1 н. NaOH (или, если требуется, 0.1 н. HCl) до рН 4.7-4.8, затем при интенсивном перемешивании и температуре 20-22°С вносят 86.4 мг (0.45 ммоль) карбодиимида, поддерживая рН 4.7-4.8 титрованием 0.1 н. HCl. Через 1 ч к охлажденной до 0°С реакционной смеси последовательно добавляют 0.1 н. NaOH (до рН 7), 2-3 мл насыщенного раствора NaCl и 60-65 мл охлажденного этанола. Выпавший осадок отделяют центрифугированием, растворяют в 10 мл 6% NaCl, добавляют 30-40 мл этанола. Вновь выпавший осадок центрифугируют, промывают этанолом (10×3 мл), затем эфиром (10×3 мл) и сушат при температуре ≤60°С и пониженном давлении. Получают ˜60 мг конъюгата гиалуроновой кислоты с 4-аминоантипирином, растворимого в воде. Конверсия карбоксильных групп составляет 83% мол. (определено из соотношения интенсивностей сигналов фенильных протонов (δ 7.5 и 7.7 м.д.) и сигнала метальных протонов NHCOMe-группы (δ 2.1 м.д.) в N-ацетилглюкозаминопиранозильных звеньях гиалуроновой кислоты).
Пример 2. Реакцию хондроитин-4-сульфата и хондроитин-6-сульфата (смесь) с 4-аминоантипирином проводят аналогично примеру 1. Получают ˜80 мг водорастворимого продукта в виде порошка белого цвета. Конверсия карбоксильных групп составляет 87% мол. (определено из соотношения интенсивностей сигналов фенильных протонов (δ 7.5 и 7.7 м.д.) и сигнала метальных протонов NHCOMe-группы (δ 2.1 м.д.) в звеньях N-ацетил-D-глюкозамина хондроитинсульфатов).
Пример 3. Реакцию гепарина с 4-аминоантипирином проводят аналогично примеру 1. Получают ˜90 мг конъюгата гепарина, растворимого в воде порошка белого цвета. Конверсия карбоксильных групп составляет 100% мольн. (определено из соотношения интенсивностей сигналов фенильных протонов (δ 7.5 и 7.7 м.д.) и сигналов двух аномерных протонов гепарина в области 5.3-5.5 м.д.).
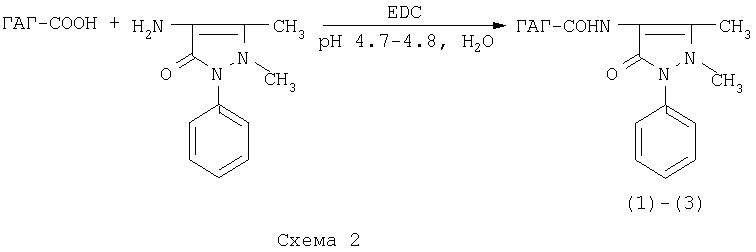
Конъюгаты ГАГ с 4-аминоантипирином являются структурными аналогами антипирина, анальгина, амидопирина, бутадиона и обладают анальгезирующими свойствами.
Анальгезирующее действие конъюгатов изучали на модели «уксусных корчей», вызванных внутрибрюшинным введением крысам 1 мл ˜1% раствора уксусной кислоты [Тринус Ф.П., Клебанов Б.М., Мохорт Н.А. Методы скрининга и фармакологического изучения противовоспалительных, анальгезирующих и жаропонижающих веществ (методические указания). Киев, 1974. - 27 С.]. Конъюгаты гиалуроновой кислоты (1) и хондроитинсульфатов (2) с 4-аминоантипирином вводили в дозе 50 мг/кг, конъюгат гепарина (3) - в дозе 40 мг/кг. В качестве препарата сравнения использовали анальгин. Профилактическое введение конъюгата (1) уменьшало частоту болевых проявлений в 1.9 раза по сравнению с нелеченной группой животных, конъюгата (2) - в 2.7 раза, конъюгата (3) - в 1.6 раза. Препарат сравнения анальгин снижал частоту болевых проявлений в 2.1-2.5 раза. Анальгезирующие свойства конъюгата хондроитинсульфатов с 4-аминоантипирином в дозе 50 мг/кг сопоставимы с анальгином.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНЪЮГАТ ГИАЛУРОНОВОЙ КИСЛОТЫ С НОВОКАИНОМ С АМФОТЕРНЫМИ СВОЙСТВАМИ | 2011 |
|
RU2473351C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННОГО ДЕРМАТАНСУЛЬФАТА | 2005 |
|
RU2318830C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЪЮГАТОВ АЛЬГИНОВОЙ КИСЛОТЫ | 2005 |
|
RU2283848C1 |
| ПРОИЗВОДНЫЕ ГИАЛУРОНОВОЙ КИСЛОТЫ С ПОНИЖЕННОЙ БИОДЕГРАДИРУЕМОСТЬЮ | 2007 |
|
RU2350625C2 |
| ПРОТИВОВОСПАЛИТЕЛЬНОЕ СРЕДСТВО С АНТИКОАГУЛЯНТНОЙ, ПРОТИВООПУХОЛЕВОЙ И АНТИМЕТАСТАТИЧЕСКОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2412712C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЪЮГАТОВ ГЕПАРИНА | 2005 |
|
RU2298406C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННЫХ АРАБИНОГАЛАКТАНОВ | 2007 |
|
RU2359975C2 |
| АНТИКОАГУЛЯНТНОЕ СРЕДСТВО С ПРОТИВОВОСПАЛИТЕЛЬНОЙ И ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2408379C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОБЛАДАЮЩИХ ПОНИЖЕННОЙ РАСТВОРИМОСТЬЮ В ВОДЕ ПЛЕНОЧНЫХ МАТЕРИАЛОВ НА ОСНОВЕ МОДИФИЦИРОВАННЫХ АМИНОСАЛИЦИЛОВЫМИ КИСЛОТАМИ КАРБОКСИЛСОДЕРЖАЩИХ ПОЛИСАХАРИДОВ | 2007 |
|
RU2343932C1 |
| СПОСОБ СИНТЕЗА КОНЪЮГАТОВ ГЛИКОЗАМИНОГЛИКАНОВ (GAG) С БИОЛОГИЧЕСКИ АКТИВНЫМИ МОЛЕКУЛАМИ, ПОЛИМЕРНЫЕ КОНЪЮГАТЫ И ИХ СООТВЕТСТВУЮЩИЕ ПРИМЕНЕНИЯ | 2010 |
|
RU2530649C2 |
Способ получения модифицированных гликозаминогликанов, обладающих анальгезирующими свойствами, отличающийся тем, что гликозаминогликаны подвергают взаимодействию с 1-фенил-2,3-диметил-4-аминопиразолоном-5(4-аминоантипирином) в водной среде при рН 4.7-4.8 в присутствии конденсирующего агента - водорастворимого 1-этил-3-[3-(диметиламино)пропил]карбодиимида при комнатной температуре с последующей очисткой от низкомолекулярных реагентов. Способ является одностадийным, что упрощает технологию получения модифицированных гликозаминогликанов.
Способ получения модифицированных гликозаминогликанов, обладающих анальгезирующими свойствами, отличающийся тем, что гликозаминогликаны подвергают взаимодействию с 1-фенил-2,3-диметил-4-аминопиразолоном-5(4-аминоантипирином) в водной среде при рН 4.7-4.8 в присутствии конденсирующего агента - водорастворимого 1-этил-3-[3-(диметиламино)пропил]карбодиимида при комнатной температуре с последующей очисткой от низкомолекулярных реагентов.
| JP 57102903 А, 26.06.1982 | |||
| ЕР 0483485 А2, 06.05.1992 | |||
| ГИДРОДИНАМИЧЕСКИЙ БЕЗРЕАКТИВНЫЙ ИНСТРУМЕНТ ДЛЯ ОЧИСТКИ ПОВЕРХНОСТИ | 2003 |
|
RU2232694C1 |
Авторы
Даты
2006-09-10—Публикация
2005-02-28—Подача